6 ZEPPA G. BELVISO S.
|
|
|
- Corinna Bernardi
- 5 anni fa
- Visualizzazioni
Transcript
1 Appunti di Tecniche avanzate per il controllo degli alimenti Parte 6 ZEPPA G. BELVISO S. Università degli Studi di Torino
2
3 Spettrometria di massa Zeppa G. Università degli Studi di Torino Tra i rivelatori per GC e LC lo SPETTROMETRO DI MASSA merita una trattazione più approfondita visto il suo enorme potenziale. Serve a misurare la massa delle molecole. Fornisce la massa molecolare e anche la formula molecolare (C 6 H 12 O 6 ) La molecola deve essere ionizzata, così da misurare il rapporto massa/carica (m/z) dello ione risultante.
4 Alcune definizioni Massa Atomica: la media ponderale delle masse esatte degli isotopi presenti in natura di quel particolare elemento. Unità di misura: Da (u: unità di massa atomica unificate) = 1/12 della massa del 12 C Massa Esatta: è la massa relativistica dell isotopo: non coincide con la somma delle masse esatte dei protoni e dei neutroni e dipende dall energia di legame. (O=15,994915; C=12,00000; H= 1,008665). Massa Nominale: coincide con il numero di protoni e neutroni che contiene l isotopo più pesante. Es. 12 C ha massa nominale = 12. Lo spettrometro di massa è quindi in grado di distinguere i singoli isotopi (m/z) di ciascun elemento (H= 1; C=12,13; N=14,15; O=16,18).
5
6 Per calcolare la massa esatta di una molecola esistono anche delle tabelle che riportano valori di massa esatta per le varie composizioni Per calcolare la massa esatta di una molecola di cui è nota la composizione elementare è anche possibile utilizzare semplici calcolatori di massa esatta disponibili on line
7 - Per misurare sperimentalmente la massa esatta bisogna avere a disposizione uno spettrometro di massa ad alta risoluzione (HRMS) che fornisce la massa esatta della molecola e da questa, consultando delle tabelle, si può ricavare la formula bruta - Strumenti a bassa risoluzione forniscono solo la massa nominale degli ioni e quindi possono differenziare ioni che hanno massa nominale diversa cioè che differiscono di almeno una o più unità di massa
8
9
10 Potere risolvente Zeppa G. Università degli Studi di Torino Il potere risolvente dello strumento determina la capacità di separare tra di loro ioni di uguale massa nominale ma diversa massa esatta. Potere Risolvente = M1/(M2 - M1) dove M1 è il valore di massa inferiore, M2 è la massa superiore tra due picchi adiacenti. Per separare tra di loro gli ioni CO ( ) ed N 2 ( ) è quindi necessaria una risoluzione di /( )=2500 All aumentare della massa molecolare è necessaria una risoluzione maggiore. Ad esempio per separare tra di loro gli ioni C 11 H 10 N ( ) e C 12 H 12 ( ) è necessaria una risoluzione di Gli spettrometri di massa ad alta risoluzione arrivano fino a
11
12 SCHEMA A BLOCCHI DI UNO SPETTROMETRO DI MASSA Sorgente Analizzatore Detector La sorgente serve a volatilizzaree ionizzare il campione L'analizzatore serve a misurare il rapporto m/zdegli ioni prodotti Il detector serve a rivelare gli ioni che arrivano dall'analizzatore
13 SCHEMA A BLOCCHI DI UNO SPETTROMETRO DI MASSA
14 SPETTROMETRIA DI MASSA IN GC Gli analiti devono passare da una zona a p atm a una zona ad alto vuoto ( torr). Si usa un interfaccia che serve per portare gli ioni dall uscita dalla colonna allo spettrometro di massa. Può essere: a) a connessione diretta b) con split aperto c) a jet È una zona di pre-vuoto ed è riscaldata ( C).
15 Sorgente a ionizzazione elettronica (EI) Le molecole gassose (es. da GC) vengono bombardate da un fascio di elettroni ad alta energia (70 ev) da cui si formano gli ioni. Si ha la formazione dello ione molecolare (uguale alla massa della molecola) e ioni frammento, formatisi per rottura dei legami nello ione molecolare generando frammenti diversi.
16 - Nella camera di ionizzazione le molecole del campione da analizzare, in fase gassosa, interagiscono con un fascio di elettroni ad energia di 70 ev generato da un filamento incandescente (Renio o Tugsteno) ed accelerate attraverso un potenziale regolabile dall'operatore verso una zona di focalizzazione del fascio e quindi all analizzatore. - E la modalità più classica, tuttora molto utilizzata - E una ionizzazione «hard» con possibili frammentazioni estese che riducono od eliminano lo ione molecolare - Il campione deve essere in forma di vapore - Adatta per composti piccoli (<800 Da), volatili e termicamente stabili - Interfaccia con GC
17 IONIZZAZIONE ELETTRONICA (EI) M + e - M +. + e - + e - 70 ev IONE ~55 ev 0.1 ev MOLECOLARE Abbondanza relativa m/z Estesa frammentazione informazioni strutturali
18 Spettro del 2-butanone (EI) Picco Base CH 3 O C CH 2 CH 3-29 Ione Molecolare m/z 43 m/z Perdita di frammenti logici (m/z 43 e m/z 57)
19 Le molecole si frammentano in modo caratteristico dando frammenti comuni all interno della classe chimica di appartenenza
20 Alcani Si verifica la scissione di un legame C-C in uno ione a numero dispari di elettroni con formazione di un catione ed un radicale neutro Zeppa G. Università degli Studi di Torino
21 Lo spettro di massa degli idrocarburi saturi è caratterizzato da gruppi di ioni distanti tra di loro 14 unità di massa. Gli ioni a massa dispari sono di regola i più abbondanti (più intensi) e la loro osservazione è indicativa della presenza di catene alifatiche. Questi ioni diminuiscono di intensità quanto più l idrocarburo è a lunga catena.
22 Sorgente a ionizzazione chimica (CI) Zeppa G. Università degli Studi di Torino
23 E una ionizzazione «soft» che genera uno ione molecolare MH+ con un basso eccesso di energia (< a 5 ev) e quindi le reazioni di frammentazioni sono poco importanti Lo ione molecolare è sempre presente e quindi si hanno informazioni sul PM ma la frammentazione è scarsa e quindi si hanno scarse informazioni sulla struttura Il campione deve essere in stato di vapore Adatto per composti piccoli (<800 Da), volatili e termicamente stabili Avviene se introduciamo nella camera di ionizzazione un gas reagente (metano, propano o MeOH, ACN trasferiti in fase vapore) in concentrazioni relativamente elevate (~1 mbar). R RH + reazione primaria RH + + M MH + + R reazione secondaria (protonazione)
24 Confronto tra uno spettro ottenuto con ionizzazione elettronica (EI) ed uno spettro ottenuto con ionizzazione chimica (CI)
25 ANALIZZATORI Gli ANALIZZATORI hanno il compito di separare gli ioni formati nella sorgente in base al rapporto massa/carica (m/z). Gli analizzatori più usati in GC-MS sono il quadrupolo e la trappola ionica. Il triplo quadrupolo e la trappola ionica possono anche fare esperimenti di massa/massa(ms/ms): si parla di spettrometria MS/MS o tandem-ms.
26 ANALIZZATORE A QUADRUPOLO Zeppa G. Università degli Studi di Torino
27 Il filtro di massa a quadrupolo, il più usato, consiste di 4 o 8 barre metalliche disposte parallelamente alle quali viene applicata una corrente continua (DC) e una radiofrequenza (RF) (le barre diametralmente opposte sono collegate elettricamente tra di loro). Variando la forza dei campi, si realizza la deviazione iperbolica selettiva degli ioni in funzione del rapporto m/z. Facilmente collegabili a sistemi introduzione. Misura masse fino a 4000 m/z. Risolve picchi separati di 0.3 m/z (strumento a bassa risoluzione). Opera a risoluzione costante (ioni a m/z 100 e 101 hanno lo stesso grado di separazione di ioni a m/z 500 e 501).
28 Il quadrupolo può acquisire gli spettri in due modalità differenti: SIM (single ion monitoring): si monitorano solo specifici m/z (analisi target). Aumento della sensibilità, perché posso aumentare il tempo di acquisizione. SCAN MODE: si acquisiscono gli spettri in un determinato range di masse. La sensibilità è funzione del range di masse osservato, della velocità di scansione e della risoluzione (o riduco il range ma perdo delle informazioni, o aumento il tempo di scansione che però non origina un buon spettro di massa).
29 TRIPLO QUADRUPOLO
30 ANALIZZATORE A TRAPPOLA IONICA Zeppa G. Università degli Studi di Torino Opera con un principio simile a quello del quadrupolo tuttavia non funziona da filtro. Anziché permettere agli ioni di attraversare il campo quadrupolare, la IT trattiene tutti gli ioni al suo interno LA IT è costituita da 3 elettrodi in acciaio inossidabile le cui superfici interne sono di forma iperbolica. Gli elettrodi sono disposti in una geometria a «sandwich» con un elettrodo ad anello nel centro (ring electrode) e due elettrodi laterali (end-cup) uno di entrata ed uno di uscita degli ioni podti sopra e sotto il ring electrode Misura masse fino a 6000 m/z Risolve picchi separati di 0.1 m/z Potere risolvente di Da 10 a 100 volte più sensibile rispetto al quadrupolo
31 Gli ioni provenienti dalla sorgente sono raccolti nella trappola e mantenuti in orbite attraverso la combinazione di voltaggi di corrente continua e di radiofrequenze. All interno della IT è presente elio ad una pressione di 10-3 Torr che collide con gli ioni determinando una diminuzione della loro energia cinetica che si riflette in una riduzione dell ampiezza delle loro oscillazioni (raffreddamento o «cooling»). In questo modo l elio contribuisce a focalizzare gli ioni verso il centro della IT aumentando sensibilità e risoluzione. Si vede lo spettro di tutti gli ioni presenti nella trappola ad un dato momento. La trappola ripete in modo continuo il seguente ciclo: Riempimento della trappola con ioni Scansione degli ioni in funzione del rapporto m/z. Non fa quindi un analisi in continuo ma una serie di analisi in breve tempo. Ideale per analisi di MS/MS.
Componenti di uno spettrometro di massa
 Componenti di uno spettrometro di massa Camera di ionizzazione La biomolecola da analizzare viene ionizzata (i) mediante irraggiamento laser della biomolecola stessa dispersa in una matrice cristallina
Componenti di uno spettrometro di massa Camera di ionizzazione La biomolecola da analizzare viene ionizzata (i) mediante irraggiamento laser della biomolecola stessa dispersa in una matrice cristallina
La risoluzione di un buon spettrometro di massa è 1 amu (atomic mass number) su10 4 amu.
 PRINCIPI DELLA SPETTROMETRIA DI MASSA A differenza delle altre tecniche analitiche (IR, UV-vis, NMR) in cui il campione rimane intatto dopo l analisi, la spettrometria di massa, che forma ed utilizza ioni
PRINCIPI DELLA SPETTROMETRIA DI MASSA A differenza delle altre tecniche analitiche (IR, UV-vis, NMR) in cui il campione rimane intatto dopo l analisi, la spettrometria di massa, che forma ed utilizza ioni
Spettrometria di massa tandem
 Spettrometria di massa tandem Sorgenti come electrospray e MALDI hanno il vantaggio di provocare poche o nessuna frammentazione, e quindi: garantiscono la misura del peso molecolare possono essere usate
Spettrometria di massa tandem Sorgenti come electrospray e MALDI hanno il vantaggio di provocare poche o nessuna frammentazione, e quindi: garantiscono la misura del peso molecolare possono essere usate
METODI FISICI IN CHIMICA ORGANICA
 METODI FISICI IN CHIMICA ORGANICA Prima parte Composizione elementare e formula bruta - analisi elementare - grado di insaturazione - spettrometria di massa 1 Metodi Fisici in Chimica Organica-La formula
METODI FISICI IN CHIMICA ORGANICA Prima parte Composizione elementare e formula bruta - analisi elementare - grado di insaturazione - spettrometria di massa 1 Metodi Fisici in Chimica Organica-La formula
METODI FISICI IN CHIMICA ORGANICA
 METODI FISICI IN CHIMICA ORGANICA Prima parte Composizione elementare e formula bruta - analisi elementare - grado di insaturazione - spettrometria di massa (parte I) 1 Metodi Fisici in Chimica Organica-La
METODI FISICI IN CHIMICA ORGANICA Prima parte Composizione elementare e formula bruta - analisi elementare - grado di insaturazione - spettrometria di massa (parte I) 1 Metodi Fisici in Chimica Organica-La
Visita agli spettrometri di massa Dott. Fabio Hollan
 Visita agli spettrometri di massa Dott. Fabio Hollan Strumento a ionizzazione ESI: Electrospray Ionization (formazione di particelle liquide cariche dalle quali gli ioni vengono emessi per desorbimento
Visita agli spettrometri di massa Dott. Fabio Hollan Strumento a ionizzazione ESI: Electrospray Ionization (formazione di particelle liquide cariche dalle quali gli ioni vengono emessi per desorbimento
Spettrometria di massa
 La spettrometria di massa è una tecnica analitica di delucidazione strutturale basata sulla ionizzazione di una molecola e sulla sua successiva frammentazione in ioni di diverso rapporto massa/carica (M/z)
La spettrometria di massa è una tecnica analitica di delucidazione strutturale basata sulla ionizzazione di una molecola e sulla sua successiva frammentazione in ioni di diverso rapporto massa/carica (M/z)
Principali tipi di ioni
 Principali tipi di ioni Ione molecolare Ioni di frammentazione Ioni di riarrangiamento Ioni a carica multipla Ioni metastabili Ioni negativi Ioni di interazione ione-molecola 1 Lo ione molecolare Lo ione
Principali tipi di ioni Ione molecolare Ioni di frammentazione Ioni di riarrangiamento Ioni a carica multipla Ioni metastabili Ioni negativi Ioni di interazione ione-molecola 1 Lo ione molecolare Lo ione
Spettrometria di massa (principi fondamentali)
 Spettrometria di massa (principi fondamentali) Rilevamento con spettrometria di massa (MS) Una tecnica più raffinata del PID è la spettrometria di massa che prevede l analisi in massa di ioni formati (con
Spettrometria di massa (principi fondamentali) Rilevamento con spettrometria di massa (MS) Una tecnica più raffinata del PID è la spettrometria di massa che prevede l analisi in massa di ioni formati (con
Scuola Nazionale sulle Tecnologie del Vuoto Trento, 9 14 Dicembre 2002
 Scuola Nazionale sulle Tecnologie del Vuoto Trento, 9 14 Dicembre 2002 Davide Bassi INFM e Dipartimento di Fisica Università di Trento 1 Sommario Misura delle pressioni parziali Il campionamento di miscele
Scuola Nazionale sulle Tecnologie del Vuoto Trento, 9 14 Dicembre 2002 Davide Bassi INFM e Dipartimento di Fisica Università di Trento 1 Sommario Misura delle pressioni parziali Il campionamento di miscele
Relazione spettro struttura della molecola organica. Ciascuna sostanza una volta ionizzata, si FRAMMENTA secondo
 Relazione spettro struttura della molecola organica Ciascuna sostanza una volta ionizzata, si FRAMMENTA secondo regole di frammentazione ben precise,, che dipendono dalla struttura della molecola stessa
Relazione spettro struttura della molecola organica Ciascuna sostanza una volta ionizzata, si FRAMMENTA secondo regole di frammentazione ben precise,, che dipendono dalla struttura della molecola stessa
5.1 SPETTROMETRIA DI MASSA
 5.1 SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica analitica che fornisce informazioni utili sulla struttura chimica dei composti esaminati, permettendone l identificazione e la determinazione
5.1 SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica analitica che fornisce informazioni utili sulla struttura chimica dei composti esaminati, permettendone l identificazione e la determinazione
Diagramma a blocchi: tipi di analizzatori
 Diagramma a blocchi: tipi di analizzatori Sistema di vuoto Introduzione Sorgente di ioni Analizzatore Detector Data System Diagramma a blocchi: tipi di analizzatori Sistema di vuoto Introduzione Sorgente
Diagramma a blocchi: tipi di analizzatori Sistema di vuoto Introduzione Sorgente di ioni Analizzatore Detector Data System Diagramma a blocchi: tipi di analizzatori Sistema di vuoto Introduzione Sorgente
Analizzatore a tempo di volo (TOF)
 La sorgente MALDI è una sorgente ad impulsi: non genera un flusso continuo di ioni, ma una grande quantità di ioni in pochissimo tempo. Questa sorgente necessita di un particolare analizzatore, l analizzatore
La sorgente MALDI è una sorgente ad impulsi: non genera un flusso continuo di ioni, ma una grande quantità di ioni in pochissimo tempo. Questa sorgente necessita di un particolare analizzatore, l analizzatore
ISOTOPI. STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso.
 ISOTOPI STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso. Il nucleo atomico è costituito da PROTONI,, che hanno una carica elettrica positiva, e da NEUTRONI,,
ISOTOPI STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso. Il nucleo atomico è costituito da PROTONI,, che hanno una carica elettrica positiva, e da NEUTRONI,,
Spettroscopia di Massa
 Spettroscopia di Massa Joseph John Thomson 1906 Nobel Prize for Physics "in recognition of the great merits of his theoretical and experimental investigations on the conduction of electricity by gases"
Spettroscopia di Massa Joseph John Thomson 1906 Nobel Prize for Physics "in recognition of the great merits of his theoretical and experimental investigations on the conduction of electricity by gases"
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
ESERCIZI SPETTROMETRIA DI MASSA
 ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
Peso Atomico. Tre problemi da risolvere!! (2) Quale unità di misura conviene adottare?
 Peso Atomico Tre problemi da risolvere!! (1) Difetto di massa (2) Quale unità di misura conviene adottare? (3) Come tener conto della miscela isotopica naturale per ciascun elemento? Il difetto di massa
Peso Atomico Tre problemi da risolvere!! (1) Difetto di massa (2) Quale unità di misura conviene adottare? (3) Come tener conto della miscela isotopica naturale per ciascun elemento? Il difetto di massa
SPETTROMETRIA DI MASSA: PERCHE?
 SPETTROMETRIA DI MASSA: PERCHE? Una tecnica analitica potente usata per: 1. Identificare composti incogniti 2. Quantificare composti noti anche se presenti in tracce 3. Chiarire la struttura e determinare
SPETTROMETRIA DI MASSA: PERCHE? Una tecnica analitica potente usata per: 1. Identificare composti incogniti 2. Quantificare composti noti anche se presenti in tracce 3. Chiarire la struttura e determinare
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA II PARTE Spettroscopia IR Spettroscopia NMR Spettrometria di massa SPETTROSCOPIA INFRAROSSA Le radiazioni infrarosse non hanno sufficiente energia da eccitare gli
S P E T T R O S C O P I A SPETTROSCOPIA II PARTE Spettroscopia IR Spettroscopia NMR Spettrometria di massa SPETTROSCOPIA INFRAROSSA Le radiazioni infrarosse non hanno sufficiente energia da eccitare gli
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Spettrometria di massa
 Spettrometria di massa La spettrometria di massa e una tecnica che consente di misurare il peso di atomi o molecole. La determinazione della massa, o del peso molecolare e sempre utile per individuare
Spettrometria di massa La spettrometria di massa e una tecnica che consente di misurare il peso di atomi o molecole. La determinazione della massa, o del peso molecolare e sempre utile per individuare
SPETTROMETRIA DI MASSA. Prof. Antonio Lavecchia
 SPETTROMETRIA DI MASSA Prof. Antonio Lavecchia Spettrometria di Massa E una tecnica analitica che permette di determinare: la formula molecolare la massa delle sostanze, misurando il rapporto massa/carica
SPETTROMETRIA DI MASSA Prof. Antonio Lavecchia Spettrometria di Massa E una tecnica analitica che permette di determinare: la formula molecolare la massa delle sostanze, misurando il rapporto massa/carica
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. Massa atomica MOLE. a.a.
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Esempi di tecniche analitiche che sono dirette applicazioni di elettromagnetismo
 Esempi di tecniche analitiche che sono dirette applicazioni di elettromagnetismo spettrometria di massa elettroforesi Spettrometria di massa Tecnica per indagine che si basa sulla ionizzazione di una molecola
Esempi di tecniche analitiche che sono dirette applicazioni di elettromagnetismo spettrometria di massa elettroforesi Spettrometria di massa Tecnica per indagine che si basa sulla ionizzazione di una molecola
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali
 Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2012/13 Test di autovalutazione 2 ottobre 2012 Cognome: Nome: Matematica e logica 1.
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2012/13 Test di autovalutazione 2 ottobre 2012 Cognome: Nome: Matematica e logica 1.
Sorgenti di ioni negativi
 Sorgenti di ioni negativi Fabio Scarpa INFN Laboratori Nazionali di Legnaro Fabio Scarpa 1 Argomenti Trattati Cenni di richiamo sugli ioni Affinità elettronica Metodi e procedure di ionizzazione Sputtering
Sorgenti di ioni negativi Fabio Scarpa INFN Laboratori Nazionali di Legnaro Fabio Scarpa 1 Argomenti Trattati Cenni di richiamo sugli ioni Affinità elettronica Metodi e procedure di ionizzazione Sputtering
ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n
 Alcani ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n H 2n+1, m/z 43, 57, 71, 85, 99 ), con intensità massima per i cationi a
Alcani ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n H 2n+1, m/z 43, 57, 71, 85, 99 ), con intensità massima per i cationi a
Introduzione alla Chimica. Paolo Mazza
 Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
L Atomo Nucleare. Rutherford protoni James Chadwick neutroni 1932
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Laboratorio di Chimica Generale ed Inorganica. Lezione 3. Atomi ed elementi Unità di massa atomica Mole
 Laboratorio di Chimica Generale ed Inorganica Lezione 3 Atomi ed elementi Unità di massa atomica Mole Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale
Laboratorio di Chimica Generale ed Inorganica Lezione 3 Atomi ed elementi Unità di massa atomica Mole Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale
(98,9x12) + (1,1x13) = 12,01 100
 5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
Ionizzazione electrospray (ESI)
 Ionizzazione electrospray (ESI) Campione in fase liquida Analizzatore e - - Il potenziale applicato alla fine dell ago e e sufficientemente alto da nebulizzare la soluzione in una miriade di goccioline
Ionizzazione electrospray (ESI) Campione in fase liquida Analizzatore e - - Il potenziale applicato alla fine dell ago e e sufficientemente alto da nebulizzare la soluzione in una miriade di goccioline
Cos è uno spettrometro di massa
 Cos è uno spettrometro di massa Lo spettrometro di massa è uno strumento che produce ioni e li separa in fase gassosa in base al loro rapporto massa/carica (m/z). Un analisi in spettrometria di massa può
Cos è uno spettrometro di massa Lo spettrometro di massa è uno strumento che produce ioni e li separa in fase gassosa in base al loro rapporto massa/carica (m/z). Un analisi in spettrometria di massa può
Lo spettrometro di massa: geometria e tipologia di analizzatori. Cosa è uno spettrometro di massa, come funziona e cosa c è dentro.
 Lo spettrometro di massa: geometria e tipologia di analizzatori Cosa è uno spettrometro di massa, come funziona e cosa c è dentro. Lo spettrometro di massa: geometria e tipologia di analizzatori Un breve
Lo spettrometro di massa: geometria e tipologia di analizzatori Cosa è uno spettrometro di massa, come funziona e cosa c è dentro. Lo spettrometro di massa: geometria e tipologia di analizzatori Un breve
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
Capitolo 5 La quantità chimica: la mole
 Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
Capitolo 5 La quantità chimica: la mole 1. La massa di atomi e molecole: un po di storia 2. Le reazioni tra i gas e il principio di Avogadro 3. Quanto pesano un atomo o una molecola? 4. La massa atomica
GC GC/MS. Chiaravalle, 11-12 FEBBRAIO 2010
 GC GC/MS Chiaravalle, 11-12 FEBBRAIO 2010 GAS-CROMATOGRAFO GAS di TRASPORTO (carrier): Gas inerte (azoto,elio..): trasporta componenti della miscela lungo la colonna cromatografica INIETTORE: - Assicura
GC GC/MS Chiaravalle, 11-12 FEBBRAIO 2010 GAS-CROMATOGRAFO GAS di TRASPORTO (carrier): Gas inerte (azoto,elio..): trasporta componenti della miscela lungo la colonna cromatografica INIETTORE: - Assicura
LEGGI PONDERALI DELLA CHIMICA
 LEGGI PONDERALI DELLA CHIMICA LEGGE DI LAVOISIER (1743-1794) In ogni reazione la massa totale dei reagenti è uguale alla massa totale dei prodotti. Massa Totale R = Massa Totale P Esempio rame + zolfo
LEGGI PONDERALI DELLA CHIMICA LEGGE DI LAVOISIER (1743-1794) In ogni reazione la massa totale dei reagenti è uguale alla massa totale dei prodotti. Massa Totale R = Massa Totale P Esempio rame + zolfo
Facoltà di Scienze M.F.N.
 Facoltà di Scienze M.F.N. Laboratorio di Chimica rganica II Anno Accademico. Relazione Gruppo: Modello Modello: a cura di V. Lucchini, M. Selva 1 Generale. + Tutti i composti impiegati nelle sintesi descritte
Facoltà di Scienze M.F.N. Laboratorio di Chimica rganica II Anno Accademico. Relazione Gruppo: Modello Modello: a cura di V. Lucchini, M. Selva 1 Generale. + Tutti i composti impiegati nelle sintesi descritte
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI
 DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea magistrale in Chimica organica e bioorganica Anno accademico 2017/2018-1 anno CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI CHIM/06-6 CFU
DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea magistrale in Chimica organica e bioorganica Anno accademico 2017/2018-1 anno CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI CHIM/06-6 CFU
Applicazione della tecnica ESI-MS/MS all identificazione e quantificazione di molecole complesse Carla Zannoni
 Applicazione della tecnica ESI-MS/MS all identificazione e quantificazione di molecole complesse Carla Zannoni Eni SpA Spettrometria di massa con campione in fase liquida: principi di funzionamento ed
Applicazione della tecnica ESI-MS/MS all identificazione e quantificazione di molecole complesse Carla Zannoni Eni SpA Spettrometria di massa con campione in fase liquida: principi di funzionamento ed
ESERCIZI W X Y Z. Numero di massa Neutroni nel nucleo Soluzione
 ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione.
 Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
SPETTROMETRIA DI MASSA
 SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica analitica potente usata per identificare prodotti incogniti, per determinazioni quantitative di composti noti e per r chiarire le proprietà
SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica analitica potente usata per identificare prodotti incogniti, per determinazioni quantitative di composti noti e per r chiarire le proprietà
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Analisi di composti volatili con la Gas Cromatografia accoppiata alla spettrometria di Massa (GC-MS)
 Analisi di composti volatili con la Gas Cromatografia accoppiata alla spettrometria di Massa (GC-MS) La spettrometria di massa è una tecnica analitica potente usata per identificare prodotti incogniti,
Analisi di composti volatili con la Gas Cromatografia accoppiata alla spettrometria di Massa (GC-MS) La spettrometria di massa è una tecnica analitica potente usata per identificare prodotti incogniti,
2 ZEPPA G. BELVISO S.
 Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
GASCROMATOGRAFIA INTRODUZIONE
 GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI. C. Daniel
 MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI C. Daniel La spettrometria di massaèampiamente usata per l analisi delle biomolecole (proteine, polisaccaridi) ma èsempre stata
MODULO: TECNICHE DI ANALISI Matrix Assisted Laser Desorption Ionisation MALDI C. Daniel La spettrometria di massaèampiamente usata per l analisi delle biomolecole (proteine, polisaccaridi) ma èsempre stata
CAMERE a DERIVA e MWPC
 CAMERE a DERIVA e MWPC Daniela Calvo INFN-Sezione di Torino Lezioni sui rivelatori per il personale tecnico-amministrativo Torino-26 aprile 2004 1 RIVELATORI A GAS GENERALITA LE PARTICELLE CARICHE ATTRAVERSANDO
CAMERE a DERIVA e MWPC Daniela Calvo INFN-Sezione di Torino Lezioni sui rivelatori per il personale tecnico-amministrativo Torino-26 aprile 2004 1 RIVELATORI A GAS GENERALITA LE PARTICELLE CARICHE ATTRAVERSANDO
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
Misure di pressione. Misura diretta. Misura indiretta. Lab di rivelatori LS. Misure di pressione (Ciullo G.) Lab di rivelatori LS
 Misure di pressione Misura diretta» Fenomeni di trasporto Misura indiretta» Ionizzazione Misura diretta Manometri capacitivi Baratron Piezo Membranovac Diaframma capacitivo: Misuratori tra i più ال precisi
Misure di pressione Misura diretta» Fenomeni di trasporto Misura indiretta» Ionizzazione Misura diretta Manometri capacitivi Baratron Piezo Membranovac Diaframma capacitivo: Misuratori tra i più ال precisi
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
Aspetti di base di Spettrometria di Massa
 Aspetti di base di Spettrometria di Massa Cenni storici Utilizzo della SM Componenti dello SM: 1-Sistemi di introduzione del campione 2-Tecniche di ionizzazione: EI CI 3-Analizzatori di massa: magnetici
Aspetti di base di Spettrometria di Massa Cenni storici Utilizzo della SM Componenti dello SM: 1-Sistemi di introduzione del campione 2-Tecniche di ionizzazione: EI CI 3-Analizzatori di massa: magnetici
Spettrometria di massa a tempo di volo (Time of Flight Mass Spectrometry TOF-MS) per l analisi in linea di inquinanti. B. Apicella, N.
 Spettrometria di massa a tempo di volo (Time of Flight Mass Spectrometry TOF-MS) per l analisi in linea di inquinanti B. Apicella, N. Spinelli Perchè Sviluppare studiare nuove la combustione? tecniche
Spettrometria di massa a tempo di volo (Time of Flight Mass Spectrometry TOF-MS) per l analisi in linea di inquinanti B. Apicella, N. Spinelli Perchè Sviluppare studiare nuove la combustione? tecniche
Risonanza Magnetica Nucleare NMR
 Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
Sommario della lezione 2. Materia e definizioni. Struttura dell atomo
 Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
CORSO DI SPETTROMETRIA DI MASSA 2015
 Società Chimica Italiana Divisione di Spettrometria di Massa Università degli Studi di Siena Dipartimento di Biotecnologie, Chimica e Farmacia CORSO DI SPETTROMETRIA DI MASSA 2015 Certosa di Pontignano
Società Chimica Italiana Divisione di Spettrometria di Massa Università degli Studi di Siena Dipartimento di Biotecnologie, Chimica e Farmacia CORSO DI SPETTROMETRIA DI MASSA 2015 Certosa di Pontignano
Massa degli atomi e delle molecole
 Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9
 Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
Pinzani, Panero, Bagni Sperimentare la chimica Soluzioni degli esercizi Capitolo 9 Esercizio PAG 198 ES 1 PAG 198 ES 2 PAG 198 ES 3 PAG 198 ES 4 PAG 198 ES 5 PAG 198 ES 6 PAG 198 ES 7 PAG 198 ES 8 PAG
Prova in itinere di Chimica Generale 8 Gennaio 2014
 Prova in itinere di Chimica Generale 8 Gennaio 2014 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 A Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Prova in itinere di Chimica Generale 8 Gennaio 2014 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 A Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Gas-cromatografia. onna.
 Gas-cromatografia La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
Gas-cromatografia La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
CHIMICA ANALITICA. Gas Chromatography
 CHIMICA ANALITICA GC Gas Chromatography Dott. Carlo Carlo I.G. Tuberoso I.G. Tuberoso Appunti Appunti didattici didattici uso laboratorio Chimica Analitica ver. 00 ver. 00-09 La gas cromatografia si basa
CHIMICA ANALITICA GC Gas Chromatography Dott. Carlo Carlo I.G. Tuberoso I.G. Tuberoso Appunti Appunti didattici didattici uso laboratorio Chimica Analitica ver. 00 ver. 00-09 La gas cromatografia si basa
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Reazioni di decomposizione
 Reazioni di decomposizione Uno ione ad elett.. dispari Ione a elett.. pari + radicale Uno ione ad elett.. dispari Ione a elett.. dispari + molecola neutra Uno ione ad elett.. pari Ione a elett.. pari +
Reazioni di decomposizione Uno ione ad elett.. dispari Ione a elett.. pari + radicale Uno ione ad elett.. dispari Ione a elett.. dispari + molecola neutra Uno ione ad elett.. pari Ione a elett.. pari +
Conduttanza Q Δ. m s P > P 1 P 2 Q > Vuoto e Spettrometria di Massa
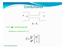 Conduttanza P P 2 Q > Se ΔP P 0 ; si ha flusso di gas (Q): P > P 2 Si definisce conduttanza ( C ): Q C= Δ P 3 m s Altre equazioni maestre Per dimensionare un sistema da vuoto, individuata la grandezza
Conduttanza P P 2 Q > Se ΔP P 0 ; si ha flusso di gas (Q): P > P 2 Si definisce conduttanza ( C ): Q C= Δ P 3 m s Altre equazioni maestre Per dimensionare un sistema da vuoto, individuata la grandezza
PERCORSI ABILITANTI SPECIALI CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA
 PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
QUESTIONARIO TECNICO
 DIREZIONE GENERALE Via Caduti del Lavoro, 40 60131 ANCONA Tel. 071/2132720 - Fax 071/2132740 e-mail: arpam.direzionegenerale@ambiente.marche.it http://arpa.marche.it QUESTIONARIO TECNICO ALLEGATO D GASCROMATOGRAFO
DIREZIONE GENERALE Via Caduti del Lavoro, 40 60131 ANCONA Tel. 071/2132720 - Fax 071/2132740 e-mail: arpam.direzionegenerale@ambiente.marche.it http://arpa.marche.it QUESTIONARIO TECNICO ALLEGATO D GASCROMATOGRAFO
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Atomi, Molecole e Ioni Lezione 2
 2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
A_Test di valutazione di CHIMICA:
 COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
ESERCITAZIONI di Metodi Fisici in Chimica Organica
 ESERCITAZIONI di Metodi Fisici in Chimica Organica PRIMA DI ANALIZZARE GLI SPETTRI DI QUALUNQUE COMPOSTO INCOGNITO BISOGNA SEMPRE DETERMINARE LA SUA FORMULA BRUTA MINIMA E DA QUESTA RICAVARE IL GRADO DI
ESERCITAZIONI di Metodi Fisici in Chimica Organica PRIMA DI ANALIZZARE GLI SPETTRI DI QUALUNQUE COMPOSTO INCOGNITO BISOGNA SEMPRE DETERMINARE LA SUA FORMULA BRUTA MINIMA E DA QUESTA RICAVARE IL GRADO DI
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali
 Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2013/14 Test di autovalutazione 2 ottobre 2013 Cognome: Nome: Matematica e logica 1.
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2013/14 Test di autovalutazione 2 ottobre 2013 Cognome: Nome: Matematica e logica 1.
CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
 CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 8 LA SPETTROMETRIA DI MASSA INTRODUZIONE La Spettrometria di Massa consiste nel pesare singole molecole tramite
CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 8 LA SPETTROMETRIA DI MASSA INTRODUZIONE La Spettrometria di Massa consiste nel pesare singole molecole tramite
gruppo ELEMENTI periodo
 gruppo ELEMENTI periodo METALLI NON-METALLI Metalli: duttili, malleabili, conducono corrente elettrica e calore, sono lucenti. Se un elemento non possiede nessuna delle proprietà sopra elencate è
gruppo ELEMENTI periodo METALLI NON-METALLI Metalli: duttili, malleabili, conducono corrente elettrica e calore, sono lucenti. Se un elemento non possiede nessuna delle proprietà sopra elencate è
Misure di Spettrometria di massa Figura 1 Schema a blocchi del sistema utilizzato per la spettrom
 Misure di Spettrometria di massa Per le misure di spettometria di massa è stato usato un sistema schematizzato in figura 1, di seguito si riportano gli spettri secondo la sequenza temporale in cui sono
Misure di Spettrometria di massa Per le misure di spettometria di massa è stato usato un sistema schematizzato in figura 1, di seguito si riportano gli spettri secondo la sequenza temporale in cui sono
Chimica. La scienza che studia le trasformazioni della materia. Acqua (ghiaccio) Acqua (Liquido) Trasformazione Fisica
 Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Corso di Master Universitario di I livello in VERIFICHE DI QUALITA IN RADIODIAGNOSTICA, MEDICINA NUCLEARE E RADIOTERAPIA
 Corso di Master Universitario di I livello in VERIFICHE DI QUALITA IN RADIODIAGNOSTICA, MEDICINA NUCLEARE E RADIOTERAPIA Esame relativo al corso Tecnologie e tecniche di imaging radiodiagnostica Nome:
Corso di Master Universitario di I livello in VERIFICHE DI QUALITA IN RADIODIAGNOSTICA, MEDICINA NUCLEARE E RADIOTERAPIA Esame relativo al corso Tecnologie e tecniche di imaging radiodiagnostica Nome:
Emissione α. La sua carica elettrica è pari a +2e La sua massa a riposo è circa 7x10-27 kg.
 Reazioni nucleari Un nucleo instabile può raggiungere una nuova condizione di stabilità attraverso una serie di decadimenti con emissione di particelle α, β, γ o di frammenti nucleari (fissione). Emissione
Reazioni nucleari Un nucleo instabile può raggiungere una nuova condizione di stabilità attraverso una serie di decadimenti con emissione di particelle α, β, γ o di frammenti nucleari (fissione). Emissione
SCHEMA DI UN GASCROMATOGRAFO
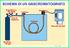 SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
SPETTROMETRIA DI MASSA
 SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica che permette di misurare la massa di una molecola (e in alcuni casi di suoi frammenti). In uno spettrometro di massa, la molecola deve essere
SPETTROMETRIA DI MASSA La spettrometria di massa è una tecnica che permette di misurare la massa di una molecola (e in alcuni casi di suoi frammenti). In uno spettrometro di massa, la molecola deve essere
O OIENI A.S. ITAI SANREMO SEDEE DATAA 31/10/2018
 Istituto Istruzione Superiore Cristoforo Colombo Liceo Scientifico delle Scienze applicate Liceo Scientifico Sportivo Istitutoo Tecnologico indirizzo Costruzioni Ambiente e Territorio Istituto Tecnico
Istituto Istruzione Superiore Cristoforo Colombo Liceo Scientifico delle Scienze applicate Liceo Scientifico Sportivo Istitutoo Tecnologico indirizzo Costruzioni Ambiente e Territorio Istituto Tecnico
INTRODUZIONE ALLA SPETTROMETRIA
 INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
LEGAMI INTERMOLECOLARI LEGAMI INTERMOLECOLARI
 I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
Corso di Chimica Analitica della Sicurezza Corso di Laurea Magistrale In Chimica Industriale - ARES
 Prof. Alessandro Bacaloni Corso di Chimica Analitica Corso di Laurea Magistrale In Chimica Industriale - ARES Tecniche analitiche per la misura dell inquinamento chimico Principali tecniche analitiche
Prof. Alessandro Bacaloni Corso di Chimica Analitica Corso di Laurea Magistrale In Chimica Industriale - ARES Tecniche analitiche per la misura dell inquinamento chimico Principali tecniche analitiche
