Corso zero CHIMICA Ingegneria Meccanica Ingegneria Elettrica A.A. 2009/2010
|
|
|
- Antonino Bonifacio Castaldo
- 7 anni fa
- Visualizzazioni
Transcript
1 Corso zero CHIMICA Ingegneria Meccanica Ingegneria Elettrica A.A. 2009/2010 Prof.ssa Giovanna Di Pasquale 1 2 1
2 Il mondo della chimica abbraccia tutto ciò che intorno a noi ha natura materiale 3 4 2
3 Il freddo fa diminuire nelle foglie la clorofilla, verde, rendendo visibili i colori di altri pigmenti 5 6 3
4 Alluminio (Al) 7 Il corindone, ossido di alluminio Al 2 O 3. può essere rosso (var. rubino), blu (var. zaffiro), arancio (var. padparadshah), bianco, giallo, bruno, grigio; sono possibili sfumature di viola, verde e rosa. Il colore dipende dal tipo di impurezza presente (es. nel rubino il colore rosso è dovuto a tracce di ioni Cr 3+ ) 8 4
5 9 Questa fotografia è stata scattata durante un sodium party 10 5
6 11 Il manico è in polietilene Le setole dello spazzolino da denti sono una delle prime cose realizzate in nylon. 12 6
7 Questi blue jeans e queste t-shirts sono fatti di cotone, una forma della cellulosa
8 Grandezze fisiche e unità di misura L interpretazione di qualsiasi fenomeno fisico e chimico e la sua traduzione quantitativa in leggi, espresse in termini matematici, richiede la misura accurata delle grandezze fisiche in esso coinvolte Estensive Il valore dipende dall estensione del campione sottoposto alla misura (es. volume, massa ecc.) Intensive Il valore non dipende dalle dimensioni del campione (es. pressione, temperatura, densità, concentrazione) 15 Sistema Internazionale delle Unità di Misura (SI) Si basa sulle sette unità di misura delle grandezze fondamentali Grandezze fondamentali? si possono misurare direttamente in base all unità prescelta Grandezze derivate? si ricavano da quelle fondamentali mediante semplici operazioni matematiche 16 8
9 Grandezze fondamentali Metro (m) Chilogrammo (kg) pari a ,73 volte la lunghezza d onda della luce rossoarancione emessa dal kripton-86 alla temperatura del punto triplo dell azoto pari alla massa del prototipo di platino-iridio depositato nell Ufficio Internazionale dei Pesi e Misure di Sèvres Secondo (s) pari alla durata di oscillazioni della radiazione emessa dal cesio-133 in una ben definita transizione di stato energetico 17 Ampere (A) Kelvin (K) Candela (cd) Mole (mol) pari all intensità della corrente elettrica, che fluendo tra due sottili conduttori rettilinei, posti parallelamente nel vuoto alla distanza di 1 metro e indefinitamente lunghi, genera tra essi una forza di N per metro conduttore pari all intervallo di temperatura corrispondente a 1/273,16 volte la temperatura del punto triplo dell acqua pari all intensità luminosa emessa da un corpo nero alla temperatura di fusione del platino (2045 K) in direzione perpendicolare al foro di uscita dell area di 1/ pari alla quantità di materia che contiene un numero di entità elementari (che devono essere sempre specificate) uguale al numero di atomi contenuti in 0,012 Kg di carbonio
10 19 Grandezze derivate Nome Simbolo Unità di misura frequenza (numero di cicli per secondo) Hertz Hz s -1 forza (massa x accelerazione) newton N m kg s -2 pressione (forza/superficie) pascal Pa m -1 kg s -2 energia, lavoro (forza per spostamento) joule J m 2 kg s -2 potenza (lavoro/tempo) watt W m 2 kg s -3 quantità di elettricità, carica elettrica (secondi x ampere) coulomb C s A potenziale elettrico, differenza di potenziale, forza elettromotrice (potenza/ampere) volt V m 2 kg s -3 A
11 Prefissi di divisione e moltiplicazione fattore nome simbolo 10-1 Deci d 10-2 Centi c 10-3 Milli m 10-6 Micro m 10-9 Nano n Pico p Femto f atto a fattore nome simbolo 10 Deca da 10 2 Etto h 10 3 Chilo k 10 6 Mega M 10 9 Giga G Tera T Peta P exa E
12 Corrispondenza tra vecchie unità ancora in uso ed unità SI Nome Caloria Elettronvolt Litroatmosfera Chilowattora Erg Dina Atmosfera Torr Litro Centimetro cubo Angstrom Unità di massa atomica Simbolo cal ev Litroatm kwh erg dina atm torr L cc Å u Definizione SI 1cal=4,1868 J 1eV=1, J 1 litroatmosfera=101,27j 1kWh=3, J 1 erg= 10-7 J 1 dina=10-5 N 1 atm= Pa 1torr=1mmHg=133,32Pa 1 L=10-3 m 3 1 cc=10-6 m 3 1 Å= m 1 u=1, kg
13 Quando si devono introdurre le misure delle grandezze fisiche nelle espressioni matematiche che le correlano, ed eseguire i relativi calcoli numerici, occorre osservare tassativamente le seguenti regole: Tutti i valori delle grandezze devono essere espressi nelle unità di misura dello stesso sistema; Si possono sommare o sottrarre tra loro solo le grandezze della stessa specie, espresse nell identica unità di misura (o nell identico multiplo o sottomultiplo); 25 Le operazioni di moltiplicazione, di divisione e di elevamento a potenza devono essere effettuate sia sui valori numerici delle grandezze, sia sulle unità di misura delle grandezze; L uguaglianza tra i due membri di un equazione deve essere soddisfatta sia per il valore numerico, sia per l unità di misura 26 13
14 Metodo scientifico 27 La chimica studia la materia Composizione e struttura Proprietà fisiche Proprietà chimiche 28 14
15 Composizione e struttura H2O 29 La chimica studia la materia Composizione e struttura Proprietà fisiche Proprietà chimiche 30 15
16 Stati di aggregazione della materia 31 Proprietà fisiche? proprietà che una sostanza presenta di per sé, senza trasformarsi o interagire con un altra sostanza? Una sostanza subisce una trasformazione fisica quando modifica la sua forma fisica, ma non la sua composizione 32 16
17 Proprietà fisiche - Punto di congelamento o fusione temperatura alla quale le fasi solide e liquide di una sostanza coesistono all equilibrio (P= 1 atm, H 2 O: 0 C; alcool etilico: -117 C; glicole etilenico: -15,6 C) - Temperatura di ebollizione Temperatura alla quale il valore della pressione di vapore del liquido diventa eguale a quello della pressione esterna (P= 1 atm, H 2 O:100 C; alcool etilico: 78,5 C; glicole etilenico: 198 C) - Conducibilità elettrica Capacità di una sostanza nel trasportare la corrente elettrica per movimento di particelle cariche come elettroni o ioni (il rame e molti altri metalli sono buoni conduttori) 33 - Viscosit à resistenza interna di un fluido che scorre (come unità di misura si usa il poise). (L H 2 O, a 25 C, ha una viscosità di 8, poise mentre la glicerina, liquido viscoso, alla stessa temperatura ha una viscosità di 9,4 poise) - Solubilità massima quantità di sostanza pura (detto soluto) che si può sciogliere in una data quantità di un mezzo dissolvente (detto solvente) ad una data temperatura, dando origine ad una soluzione (100 g di H 2 O sciolgono 35,7 di NaCl a 0 e 39,1 g a 100 C) 34 17
18 Densità massa per unità di volume
19 37 La chimica studia la materia Composizione e struttura Proprietà fisiche Proprietà chimiche 38 19
20 Proprietà chimiche? proprietà che una sostanza presenta quando si trasforma in un altra sostanza? Una sostanza subisce una trasformazione chimica quando modifica la sua composizione Es. Acqua Corrente elettrica? idrogeno gassoso + ossigeno Corrente elettrica 2H 2 O? 2 H 2 + O 2 39 H 2 O (s) T T? H 2 O (l)? H 2 O (g) Trasformazione fisica Trasformazione chimica Corrente elettrica 2H 2 O? 2 H 2 + O
21 HgO? Hg + ½ O 2 T 41 Cu + 4 HNO 3? Cu(NO 3 ) + 2 NO H 2 O 42 21
22 UNA SOSTANZA E IDENTIFICATA DAL PROPRIO INSIEME DI PROPRIETA FISICHE E CHIMICHE 43 Proprietà caratteristiche del rame (Cu) Proprietà fisiche Colore bruno rossastro Lucentezza metallica Duttile e Malleabile Buon conduttore del calore e dell elettricità Può essere miscelato con lo zinco per formare l ottone Densità: 8,95g/cm 3 Temperatura di fusione = 1083 C Temperatura di ebollizione = 2570 C Proprietà chimiche Forma lentamente un carbonato blu-verde in aria umida Reagisce con l acido nitrico e con l acido solforico Forma lentamente una soluzione di colore blu intenso in ammoniaca acquosa 44 22
23 STORIA DELLA CHIMICA ARISTOTELE ( a.c.) Teoria dei quattro principi ultimi (aria, acqua, terra, fuoco). Dalla loro combinazione traevano origine la materia e le sue trasformazioni 45 DEMOCRITO ( a.c.) Introdusse la teoria atomistica ALCHIMIA (II-V secolo d.c.) Consisteva nella ricerca della sostanza capace di trasformare qualsiasi metallo in oro XIX secolo Finalmente iniziò la ricerca quantitativa e sistematica dell informazione 46 23
24 Che cosa hanno in comune le seguenti cose? L aria La sabbia La coca cola Un panino Un libro Un computer Una macchina Un elefante L Oceano Pacifico Il pianeta Saturno 47 Ogni cosa è fatta di atomi 48 24
25 Teoria atomica di Dalton del 1803: 1. Ogni elemento è composto da particelle estremamente piccole chiamate atomi. 2. Tutti gli atomi di un dato elemento sono identici; gli atomi di elementi diversi sono diversi e hanno proprietà differenti (inclusa una massa differente) 3. Nel corso delle reazioni chimiche gli atomi di un elemento non si trasformano in atomi di un elemento diverso; nel corso delle reazioni chimiche gli atomi non vengono né creati né distrutti. 4. I composti si formano quando atomi di più di un elemento si combinano; un dato composto ha sempre lo stesso numero relativo di atomi di diverse specie. 49 Gli atomi sono i mattoni che stanno alla base della materia; essi sono le unità più piccole di un elemento che conservano le proprietà chimiche di quel dato elemento: Un elemento è costituito da un solo tipo di atomo Nei composti gli atomi di due o più elementi si combinano in rapporti definiti La molecola è la più piccola particella di sostanza che ha proprietà chimiche uguali a quelle della sostanza. Può essere costituita da atomi uguali o diversi 50 25
26
27
28 Numero atomico e numero di massa Numero atomico: numero dei protoni del nucleo Numero di massa: somma del numero dei protoni e del numero dei neutroni - Ogni atomo risulta univocamente individuato quando sono noti il numero atomico e il numero di massa - Gli atomi sono particelle elettricamente neutre 55 ATOMI E SIMBOLI Isotopi: atomi dello stesso elemento con differente numero di massa Elemento Isotopi Percentuale Idrogeno 1 H % 2 H 0.015% 3 H (tracce) Carbonio 12 C 98.90% 13 C 1.10% 14 C* (tracce) *E' nota l'importanza della sua valutazione in reperti archeologici, in quanto correlabile con l'età del manufatto 56 28
29 57 ATOMI E SIMBOLI Na 58 29
30 59 Differenza tra miscele e composti MISCELA - I componenti si possono separare applicando tecniche fisiche - La composizione è variabile - Le proprietà sono correlate con quelle dei componenti COMPOSTO - I componenti non sono separabili mediante tecniche fisiche - La composizione è costante - Le proprietà sono diverse da quelle dei componenti 60 30
31 Separazione fisica di una miscela eterogenea di dicromato di potassio e polvere di ferro
32
33 65 Proprietà del sodio, del cloro e del cloruro di sodio Sodio (Na) T fusione T ebollizione Colore 97,8 C 881,4 C argenteo Densità 0,97 g/cm 3 Comportamento in acqua reattivo Cloruro di sodio (NaCl) T fusione 801 C T ebollizione 1413 C Cloro (Cl 2 ) T fusione -101 C T ebollizione -34 C Colore giallo-verde Densità 0,0032g/cm 3 Comportamento in acqua lievemente reattivo Colore bianco Densità 2,16 g/cm 3 Comportamento in acqua solubile 66 33
34 Miscela Omogenea? La composizione risulta identica in ogni punto (es. soluzione) Eterogenea? E possibile riconoscere i componenti ad occhio nudo o con il microscopio (es. rocce. latte)
35 69 35
Grandezze fisiche fondamentali
 Grandezze fisiche fondamentali La grandezza fisica rappresenta la proprietà di un corpo. Le grandezze fisiche fondamentali sono 7. La differenza rispetto a quelle derivate è che quelle derivate presentano
Grandezze fisiche fondamentali La grandezza fisica rappresenta la proprietà di un corpo. Le grandezze fisiche fondamentali sono 7. La differenza rispetto a quelle derivate è che quelle derivate presentano
Corso di Chimica Generale e Inorganica
 Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
LA MISURA DELLE GRANDEZZE FISICHE. Prof Giovanni Ianne
 LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
Alcune informazioni utili
 Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Parte Prima. La Materia e le sue Trasformazioni. 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico?
 Parte Prima La Materia e le sue Trasformazioni 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico? L'acqua pura: a. ha una definita temperatura di ebollizione
Parte Prima La Materia e le sue Trasformazioni 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico? L'acqua pura: a. ha una definita temperatura di ebollizione
Le unità fondamentali SI
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Esperienze di Fisica
 Esperienze di Fisica Dr. Alen Khanbekyan Tel.: 057734665 E-mail: khanbekyan@unisi.it Relazioni. Per ogni prova pratica deve essere preparata una relazione scritta strutturata nel modo seguente:. Introduzione
Esperienze di Fisica Dr. Alen Khanbekyan Tel.: 057734665 E-mail: khanbekyan@unisi.it Relazioni. Per ogni prova pratica deve essere preparata una relazione scritta strutturata nel modo seguente:. Introduzione
Il metodo scientifico
 Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
LE GRANDEZZE FISICHE E LE UNITA DI MISURA
 LE GRANDEZZE FISICHE E LE UNITA DI MISURA LA FISICA STUDIA E DESCRIVE I FENOMENI NATURALI ATTRAVERSO LE GRANDEZZE FISICHE, CHE SONO PROPRIETA MISURABILI DI UN SISTEMA, CON LO SCOPO DI TROVARE LEGGI CHE
LE GRANDEZZE FISICHE E LE UNITA DI MISURA LA FISICA STUDIA E DESCRIVE I FENOMENI NATURALI ATTRAVERSO LE GRANDEZZE FISICHE, CHE SONO PROPRIETA MISURABILI DI UN SISTEMA, CON LO SCOPO DI TROVARE LEGGI CHE
SISTEMA INTERNAZIONALE DELLE UNITÀ DI MISURA
 SI SISTEMA INTERNAZIONALE DELLE UNITÀ DI MISURA SETTE UNITÀ FONDAMENTALI LUNGHEZZA metro m Il metro è la lunghezza uguale a 1.650.763,73 lunghezze d'onda, nel vuoto, della radiazione corrispondente alla
SI SISTEMA INTERNAZIONALE DELLE UNITÀ DI MISURA SETTE UNITÀ FONDAMENTALI LUNGHEZZA metro m Il metro è la lunghezza uguale a 1.650.763,73 lunghezze d'onda, nel vuoto, della radiazione corrispondente alla
Le Grandezze e il Sistema Internazionale di misura
 Le Grandezze e il Sistema Internazionale di misura Si dice GRANDEZZA tutto ciò ce si può misurare. Esempio L altezza di una torre, il volume di una stanza, la superficie di un muro, l ampiezza di un angolo,
Le Grandezze e il Sistema Internazionale di misura Si dice GRANDEZZA tutto ciò ce si può misurare. Esempio L altezza di una torre, il volume di una stanza, la superficie di un muro, l ampiezza di un angolo,
Materia. Tutto ciò che occupa spazio e ha massa
 ISBN: 9788879476539 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore.
ISBN: 9788879476539 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore.
Introduzione alla Chimica. Paolo Mazza
 Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Sommario della lezione 2. Materia e definizioni. Struttura dell atomo
 Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Calcoli applicati alla chimica analitica. Unità di misura del Sistema Internazionale
 Calcoli applicati alla chimica analitica Unità di misura del Sistema Internazionale Soluzioni e loro concentrazioni Stechiometria chimica 1 Unità di misura SI Il Sistema Internazionale delle Unità (SI)
Calcoli applicati alla chimica analitica Unità di misura del Sistema Internazionale Soluzioni e loro concentrazioni Stechiometria chimica 1 Unità di misura SI Il Sistema Internazionale delle Unità (SI)
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Materia. Tutto ciò che occupa spazio e ha massa
 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore. Hanno un volume
Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore. Hanno un volume
I.T.C.G. Hodierna. Corso per Geometri. Materia: Fisica. Prof. Giuseppe Frangiamore
 I.T.C.G. Hodierna Corso per Geometri Materia: Fisica Prof. Giuseppe Frangiamore CAPITOLO I Che cosa studia la fisica La fisica studia tutti i fenomeni naturali ricercando le leggi che li governano. Grazie
I.T.C.G. Hodierna Corso per Geometri Materia: Fisica Prof. Giuseppe Frangiamore CAPITOLO I Che cosa studia la fisica La fisica studia tutti i fenomeni naturali ricercando le leggi che li governano. Grazie
grandezze fisiche leggi fisiche
 INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
Sistemi di unità di Misura
 Sistemi di unità di Misura Costruzione di un sistema di unità di misura: 1) Scegliere un particolare gruppo ( 4) di grandezze fisiche (lunghezza, tempo, massa, velocità, accelerazione, energia, potenza,
Sistemi di unità di Misura Costruzione di un sistema di unità di misura: 1) Scegliere un particolare gruppo ( 4) di grandezze fisiche (lunghezza, tempo, massa, velocità, accelerazione, energia, potenza,
Unità di misura e formule utili. Lezione 6
 Unità di misura e formule utili Lezione 6 Unità di misura Il Sistema Internazionale di unità di misura (SI) nasce dall'esigenza di utilizzare comuni unità di misura per la quantificazione e la misura delle
Unità di misura e formule utili Lezione 6 Unità di misura Il Sistema Internazionale di unità di misura (SI) nasce dall'esigenza di utilizzare comuni unità di misura per la quantificazione e la misura delle
Chimica Generale ed Inorganica
 Dipartimento di Ecologia e Biologia Chimica Generale ed Inorganica Prof.ssa Giorgia Botta Contatti Tel: 0761-357314 Dipartimento DEB Facoltà di Agraria, lab 08 e-mail: botta.giorgia@gmail.com Proprietà,
Dipartimento di Ecologia e Biologia Chimica Generale ed Inorganica Prof.ssa Giorgia Botta Contatti Tel: 0761-357314 Dipartimento DEB Facoltà di Agraria, lab 08 e-mail: botta.giorgia@gmail.com Proprietà,
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
GRANDEZZE FONDAMENTALI E DERIVATE
 GRANDEZZE FONDAMENTALI E DERIVATE GRANDEZZA FISICA = sostanza o corpo che può essere misurata Il Sistema Internazionale (SI) delle unità di misura classifica le grandezze fisiche in: GRANDEZZE FONDAMENTALI
GRANDEZZE FONDAMENTALI E DERIVATE GRANDEZZA FISICA = sostanza o corpo che può essere misurata Il Sistema Internazionale (SI) delle unità di misura classifica le grandezze fisiche in: GRANDEZZE FONDAMENTALI
Le unità di misura. Le sette grandezze fondamentali e le relative unità di misura sono riportate nella tabella seguente.
 Le unità di misura Il sistema di unità di misura attualmente in uso è stato stabilito nell'ambito della 11 a Conferenza Generale dei Pesi e delle Misure nel 1960, nella quale è stato costituito il Sistema
Le unità di misura Il sistema di unità di misura attualmente in uso è stato stabilito nell'ambito della 11 a Conferenza Generale dei Pesi e delle Misure nel 1960, nella quale è stato costituito il Sistema
un sistema di unita di misura delle grandezze fisiche e l insieme delle unita di misura di tutte le grandezze fisiche?
 Sistemi di unita di misura un sistema di unita di misura delle grandezze fisiche e l insieme delle unita di misura di tutte le grandezze fisiche? Grandezze FONDAMENTALI : Grandezze DERIVATE : - necessitano
Sistemi di unita di misura un sistema di unita di misura delle grandezze fisiche e l insieme delle unita di misura di tutte le grandezze fisiche? Grandezze FONDAMENTALI : Grandezze DERIVATE : - necessitano
Circuiti Elettrici Lineari Concetti Fondamentali
 Facoltà di Ingegneria Università degli studi di Pavia Corso di Laurea Triennale in Ingegneria Elettronica e Informatica Circuiti Elettrici Lineari Concetti Fondamentali Circuiti Elettrici Lineari a.a.
Facoltà di Ingegneria Università degli studi di Pavia Corso di Laurea Triennale in Ingegneria Elettronica e Informatica Circuiti Elettrici Lineari Concetti Fondamentali Circuiti Elettrici Lineari a.a.
METODO SPERIMENTALE. Per la comprensione di un fenomeno è importante individuare i fattori essenziali e distinguerli da quelli secondari.
 INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
Le 7 grandezze fondamentali e le relative unità di misura sono riportate nella tabella sottostante:
 Le unità di misura L attuale sistema di unità di misura è stato stabilito dall 11 Conferenza Generale dei Pesi e delle Misure nel 1960 che ha costituito il Sistema Internazionale delle Unità di misura
Le unità di misura L attuale sistema di unità di misura è stato stabilito dall 11 Conferenza Generale dei Pesi e delle Misure nel 1960 che ha costituito il Sistema Internazionale delle Unità di misura
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica -
 Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
del 23 novembre 1994 (Stato 1 gennaio 2013)
 Ordinanza sulle unità 941.202 del 23 novembre 1994 (Stato 1 gennaio 2013) Il Consiglio federale svizzero, visti gli articoli 2 capoverso 2 e 3 capoverso 2 della legge federale del 17 giugno 2011 1 sulla
Ordinanza sulle unità 941.202 del 23 novembre 1994 (Stato 1 gennaio 2013) Il Consiglio federale svizzero, visti gli articoli 2 capoverso 2 e 3 capoverso 2 della legge federale del 17 giugno 2011 1 sulla
fenomeni na- turali grandezze fisiche principi leggi metodo scientifico modello
 La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
Corso di Laurea in Chimica. Laboratorio di Chimica Generale
 Corso di Laurea in Chimica Laboratorio di Chimica Generale Prof. Claudia Caltagirone Anno Accademico 2018/2019 Prof. Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it
Corso di Laurea in Chimica Laboratorio di Chimica Generale Prof. Claudia Caltagirone Anno Accademico 2018/2019 Prof. Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it
Elementi di Fisica Tecnica Ambientale
 Elementi di Fisica Tecnica Ambientale Prof. Piercarlo Romagnoni Dorsoduro 2206 30123 Venezia 1 Una premessa Simbologia = differenza Esempio: t = t 2 t 1 d = differenziale/ infinitesimo dv = volume infinitesimo
Elementi di Fisica Tecnica Ambientale Prof. Piercarlo Romagnoni Dorsoduro 2206 30123 Venezia 1 Una premessa Simbologia = differenza Esempio: t = t 2 t 1 d = differenziale/ infinitesimo dv = volume infinitesimo
IMPIANTIDI CLIMATIZZAZIONE
 IMPIANTIDI CLIMATIZZAZIONE FACOLTÀ DI ARCHITETTURA FISICA TECNICA E IMPIANTI A.A. 2012/2013 MASSIMILIANO PANCANI Ingegnere Energetico e Nucleare m.pancani@gmail.com ogni tanto Dopo il corso saprete tutto
IMPIANTIDI CLIMATIZZAZIONE FACOLTÀ DI ARCHITETTURA FISICA TECNICA E IMPIANTI A.A. 2012/2013 MASSIMILIANO PANCANI Ingegnere Energetico e Nucleare m.pancani@gmail.com ogni tanto Dopo il corso saprete tutto
Corso di Fisica. Ada Solano / Giovanni Pollarolo. Dipartimento di Fisica Università degli Studi di Torino
 Corso di Fisica Ada Solano / Giovanni Pollarolo Dipartimento di Fisica Università degli Studi di Torino Informazioni generali sul corso DOCENTI Ada Solano email: ada.solano@unito.it tel. 011 670 7310 Giovanni
Corso di Fisica Ada Solano / Giovanni Pollarolo Dipartimento di Fisica Università degli Studi di Torino Informazioni generali sul corso DOCENTI Ada Solano email: ada.solano@unito.it tel. 011 670 7310 Giovanni
UNITA DI MISURA Università La Sapienza di Roma
 UNITA DI MISURA Livio de Santoli, Francesco Mancini Università La Sapienza di Roma livio.desantoli@uniroma1.it francesco.mancini@uniroma1.it www.eeplus.it www.ingenergia.it Le proprietà della materia che
UNITA DI MISURA Livio de Santoli, Francesco Mancini Università La Sapienza di Roma livio.desantoli@uniroma1.it francesco.mancini@uniroma1.it www.eeplus.it www.ingenergia.it Le proprietà della materia che
GRANDEZZE FISICHE E MISURA
 GRANDEZZE FISICHE E MISURA 1 Una grandezza è la proprietà di un fenomeno, corpo o sostanza, che può essere espressa quantitativamente mediante un numero e un riferimento Quindi il colore delle matite non
GRANDEZZE FISICHE E MISURA 1 Una grandezza è la proprietà di un fenomeno, corpo o sostanza, che può essere espressa quantitativamente mediante un numero e un riferimento Quindi il colore delle matite non
Il Sistema Internazionale di Unità di Misura (SI)
 Il Sistema Internazionale di Unità di Misura (SI) REGOLE DI SCRITTURA I nomi delle unità di misura debbono essere scritti normalmente con tutte le lettere, compresa la prima, minuscole, a meno che non
Il Sistema Internazionale di Unità di Misura (SI) REGOLE DI SCRITTURA I nomi delle unità di misura debbono essere scritti normalmente con tutte le lettere, compresa la prima, minuscole, a meno che non
Misure e Unità di Misura
 2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
APPUNTI delle lezioni prof. Celino PARTE 1
 APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
Corso di Laurea in Fisica
 Anno accademico 2016/2017 Corso di Laurea in Fisica Laboratorio 1 Docente: Prof. Annalisa D Angelo Esercitatori: Cristina Morone, Alessandro Rizzo, Lucilla Lanza, Valeria Di Felice, Massimo Bassan people.roma2.infn.it/~annalisa/lab1
Anno accademico 2016/2017 Corso di Laurea in Fisica Laboratorio 1 Docente: Prof. Annalisa D Angelo Esercitatori: Cristina Morone, Alessandro Rizzo, Lucilla Lanza, Valeria Di Felice, Massimo Bassan people.roma2.infn.it/~annalisa/lab1
Argomenti per il Recupero di Fisica
 Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze Fondamentali e Derivate
Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze Fondamentali e Derivate
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE
 CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
Corso di chimica generale
 Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Impianti di. Climatizzazione. ing. Massimiliano Pancani
 Impianti di Climatizzazione Indice delle dispense Capitolo 1 I fondamentali Unità di misura Temperatura Umidità Pressione Energia Potenza Capitolo 2 Sistemi energetici Sistemi energetici Impianti tecnici
Impianti di Climatizzazione Indice delle dispense Capitolo 1 I fondamentali Unità di misura Temperatura Umidità Pressione Energia Potenza Capitolo 2 Sistemi energetici Sistemi energetici Impianti tecnici
Lezione di oggi. Sistema internazionale di unità di misura
 Lezione di oggi Sistema internazionale di unità di misura Processo di misura Risultato di una misurazione = STIMA + INCERTEZZA + U.M. Miglior stima della grandezza che deve essere quantificata Ampiezza
Lezione di oggi Sistema internazionale di unità di misura Processo di misura Risultato di una misurazione = STIMA + INCERTEZZA + U.M. Miglior stima della grandezza che deve essere quantificata Ampiezza
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Unità di misura. Grandezze fisiche. Unità di Misura. Strumenti di misura. Grandezza fisica: qualsiasi proprietà della materia che può essere misurata
 Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Unità di misura Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Unità di misura Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
L Atomo Nucleare. Rutherford protoni James Chadwick neutroni 1932
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
INTRODUZIONE GRANDEZZE FISICHE GRANDEZZE FISICHE
 INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
Corso di Chimica Dott.ssa Fioravanti
 Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di Fisica Tecnica EA - a.a. 2005/06 27 febbraio 2006
 1 Unità di misura La misura è una tecnica mediante la quale a una grandezza fisica (ad esempio le proprietà come definite nel testo) si associa un numero, risultato di una procedura che prevede un confronto
1 Unità di misura La misura è una tecnica mediante la quale a una grandezza fisica (ad esempio le proprietà come definite nel testo) si associa un numero, risultato di una procedura che prevede un confronto
Elettronica Grandezze elettriche e unità di misura
 Elettronica Grandezze elettriche e unità di misura Valentino Liberali Dipartimento di Fisica Università degli Studi di Milano valentino.liberali@unimi.it Elettronica Grandezze elettriche e unità di misura
Elettronica Grandezze elettriche e unità di misura Valentino Liberali Dipartimento di Fisica Università degli Studi di Milano valentino.liberali@unimi.it Elettronica Grandezze elettriche e unità di misura
Unita di misura SI Sistema Internazionale
 Unita di misura SI Sistema Internazionale 18.11.95 Pisa/Gmp Tab 1. Unita base Quantita Unita Sm b Definizione Lunghezza metro m Lunghezza pari a 1.650.763,73 volte la lunghezza d onda nel vuoto della luce
Unita di misura SI Sistema Internazionale 18.11.95 Pisa/Gmp Tab 1. Unita base Quantita Unita Sm b Definizione Lunghezza metro m Lunghezza pari a 1.650.763,73 volte la lunghezza d onda nel vuoto della luce
Chimica Generale ed Inorganica
 CCS-Biologia CCS- Scienze Geologiche A.A. 2016-2017 Chimica Generale ed Inorganica Prof. Francesco Isaia Prof. Vito Lippolis Dipartimento di Scienze Chimiche e Geologiche Cittadella Universitaria Email:
CCS-Biologia CCS- Scienze Geologiche A.A. 2016-2017 Chimica Generale ed Inorganica Prof. Francesco Isaia Prof. Vito Lippolis Dipartimento di Scienze Chimiche e Geologiche Cittadella Universitaria Email:
Chimica. Scienza che studia: proprietà, composizione e struttura della materia, e le trasformazioni che in essa avvengono
 Chimica Scienza che studia: proprietà, composizione e struttura della materia, e le trasformazioni che in essa avvengono La Chimica è una scienza sperimentale: Si basa su misure ottenute da esperimenti
Chimica Scienza che studia: proprietà, composizione e struttura della materia, e le trasformazioni che in essa avvengono La Chimica è una scienza sperimentale: Si basa su misure ottenute da esperimenti
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012
 CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 U01 U.01 Fondamenti U.01 Fondamenti 1/29 SISTEMI TERMODINAMICI E LORO PROPRIETA U.01 Fondamenti 2/29 1 CONCETTI FONDAMENTALI DELLA TERMODINAMICA
CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 U01 U.01 Fondamenti U.01 Fondamenti 1/29 SISTEMI TERMODINAMICI E LORO PROPRIETA U.01 Fondamenti 2/29 1 CONCETTI FONDAMENTALI DELLA TERMODINAMICA
CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO STATE TRATTE DAL LIBRO FONDAMENTI DI FISICA DI D. HALLIDAY,
CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO STATE TRATTE DAL LIBRO FONDAMENTI DI FISICA DI D. HALLIDAY,
Se si mescolano 24,50 g. di NaCl in polvere e 100,00 g. di acqua:
 A. Si mescolano 15,30 g. di zucchero con 5,65 g. di NaCl dopo averli pesati. Determinare: A. Le percentuali dei due componenti B. Gli errori assoluti e relativi compiuti sulle due pesate C. L errore assoluto
A. Si mescolano 15,30 g. di zucchero con 5,65 g. di NaCl dopo averli pesati. Determinare: A. Le percentuali dei due componenti B. Gli errori assoluti e relativi compiuti sulle due pesate C. L errore assoluto
Fisicaa Applicata, Area Tecnica, M. Ruspa. GRANDEZZE FISICHE e MISURA DI GRANDEZZE FISICHE
 GRANDEZZE FISICHE e MISURA DI GRANDEZZE FISICHE 1 LA FISICA COME SCIENZA SPERIMENTALE OSSERVAZIONI SPERIMENTALI Studio di un fenomeno MISURA DI GRANDEZZE FISICHE IPOTESI VERIFICA LEGGI FISICHE Relazioni
GRANDEZZE FISICHE e MISURA DI GRANDEZZE FISICHE 1 LA FISICA COME SCIENZA SPERIMENTALE OSSERVAZIONI SPERIMENTALI Studio di un fenomeno MISURA DI GRANDEZZE FISICHE IPOTESI VERIFICA LEGGI FISICHE Relazioni
ESERCIZI UNITA A SOMMARIO
 Es.A/0 ESERCIZI UNITA A SOMMARIO A. UNITA DI MISURA A.I. A.II. A.III. A.IV. A.V. Dimensioni fisiche Misure e unità di misura Sistema Internazionale (SI) ed unità di misura fondamentali Unità di misura
Es.A/0 ESERCIZI UNITA A SOMMARIO A. UNITA DI MISURA A.I. A.II. A.III. A.IV. A.V. Dimensioni fisiche Misure e unità di misura Sistema Internazionale (SI) ed unità di misura fondamentali Unità di misura
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
IL SISTEMA INTERNAZIONALE DI MISURA
 IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
fenomeni na- turali grandezze fisiche principi leggi metodo scientifico modello
 La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
Gli Stati della Materia
 John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Capitolo 1 Materia e Misure 1 Benvenuti nel Mondo della Chimica 2 Versione italiana a cura di Giaime Marongiu e Guido Ennas
John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Capitolo 1 Materia e Misure 1 Benvenuti nel Mondo della Chimica 2 Versione italiana a cura di Giaime Marongiu e Guido Ennas
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. Massa atomica MOLE. a.a.
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Tutte le altre grandezze fisiche derivano da queste e sono dette grandezze DERIVATE (es. la superficie e il volume).
 Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE. UdM 1
 UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE UdM 1 Lo studio dei fenomeni naturali si basa sulle osservazioni sperimentali e richiede la misura di certe grandezze fisiche. Ai fini della misurazione
UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE UdM 1 Lo studio dei fenomeni naturali si basa sulle osservazioni sperimentali e richiede la misura di certe grandezze fisiche. Ai fini della misurazione
Sistemi di unità di misura
 Maffei Antonella matricola 146381 - Lezione del 18/10/2002 ore 10:30-12:30 Sistemi di unità di misura L unità di misura è un astrazione della matematica che ci permette di fare delle osservazioni e dei
Maffei Antonella matricola 146381 - Lezione del 18/10/2002 ore 10:30-12:30 Sistemi di unità di misura L unità di misura è un astrazione della matematica che ci permette di fare delle osservazioni e dei
CHIMICA GENERALE ED INORGANICA
 Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
SI e costanti fondamentali
 SI e costanti fondamentali La revisione del Sistema Internazionale di unità di misura 16-20 ottobre 2017: il CIPM (Comitato Internazionale Pesi e Misure decide di sottoporre alla prossima CGPM una Risoluzione
SI e costanti fondamentali La revisione del Sistema Internazionale di unità di misura 16-20 ottobre 2017: il CIPM (Comitato Internazionale Pesi e Misure decide di sottoporre alla prossima CGPM una Risoluzione
Fenomeno fisico. Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici
 Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
STRUTTURA DELLA MATERIA. Prof.ssa PATRIZIA GALLUCCI
 STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Grandezze fisiche Una grandezza fisica è una proprieta di un corpo o di un sistema che puo essere misurata sperimentalmente.
 Grandezze fisiche Una grandezza fisica è una proprieta di un corpo o di un sistema che puo essere misurata sperimentalmente. Sensazione di caldo/freddo? Temperatura? Si espirme come: Numero + unità di
Grandezze fisiche Una grandezza fisica è una proprieta di un corpo o di un sistema che puo essere misurata sperimentalmente. Sensazione di caldo/freddo? Temperatura? Si espirme come: Numero + unità di
Chimica Generale ed Inorganica. Lezione 1
 Chimica Generale ed Inorganica Lezione 1 Implicazioni della Chimica nella Vita Quotidiana Salute e Medicina Sistemi di disinfettazione Anestesia Vaccini e antibiotici Terapia genica Energia ed Ambiente
Chimica Generale ed Inorganica Lezione 1 Implicazioni della Chimica nella Vita Quotidiana Salute e Medicina Sistemi di disinfettazione Anestesia Vaccini e antibiotici Terapia genica Energia ed Ambiente
Chimica. 1) Il simbolo del Carbonio è: A) C B) Ca. C) Ce D) Cu. 2) Secondo il principio della conservazione della materia:
 Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO
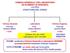 CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica CH 3
 Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
ATOMO. Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas)
 http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
L2 - Completa la seguente frase: "L'auto sta al telaio come il corpo sta..."
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
LA STRUTTURA DELLA MATERIA
 LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
Unità di misura. Grandezze fisiche. Unità di Misura. Grandezza fisica: qualsiasi proprietà della materia che può essere misurata
 Unità di misura Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Unità di misura Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Fisica I semestre. Lunedi 11 h - 12 h mercoledi 9 h - 11 h venerdi 9 h - 11 h Eserc.
 Fisica I semestre Pierazzini m. Giuseppe E_mail: pierazzini@unipi.it Tf 050.2214220 Fax 050.2214205 Dipartimento di Fisica E. Fermi stanza B,II,206 Lezioni ed esercitazioni Lunedi 11 h - 12 h mercoledi
Fisica I semestre Pierazzini m. Giuseppe E_mail: pierazzini@unipi.it Tf 050.2214220 Fax 050.2214205 Dipartimento di Fisica E. Fermi stanza B,II,206 Lezioni ed esercitazioni Lunedi 11 h - 12 h mercoledi
Materiali e Tecnologie elettriche Appendice A1
 Università di Napoli Federico II Facoltà di Ingegneria Corso di Laurea in Ingegneria Elettrica prof. G. Lupò Materiali e Tecnologie elettriche Appendice A1 LE UNITÀ DI MISURA DEL SISTEMA INTERNAZIONALE
Università di Napoli Federico II Facoltà di Ingegneria Corso di Laurea in Ingegneria Elettrica prof. G. Lupò Materiali e Tecnologie elettriche Appendice A1 LE UNITÀ DI MISURA DEL SISTEMA INTERNAZIONALE
Grandezze fisiche e loro misura
 Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e che implicano grandezze misurabili. - Sono
Grandezze fisiche e loro misura Cos è la fisica? e di che cosa si occupa? - Scienza sperimentale che studia i fenomeni naturali suscettibili di sperimentazione e che implicano grandezze misurabili. - Sono
