CLARITROMICINA ZENTIVA 500 MG COMPRESSE RIVESTITE CON FILM. Variazioni degli stampati relativamente agli aspetti della sicurezza
|
|
|
- Leonora Salvadori
- 7 anni fa
- Visualizzazioni
Transcript
1 FARMACOVIGILANZA CLARITROMICINA ZENTIVA 500 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/P/64297 (codice pratica C1B/2013/3542) del 17 giugno 2014 dell Agenzia Italiana del Farmaco, pubblicata in G.U. Foglio delle inserzioni n. 93 del 7 agosto Di seguito sono evidenziate le variazioni introdotte nella versione attuale dell RCP e messe a confronto con la versione precedente. Paragrafo Claritromicina Zentiva RCP versione precedente (novembre 2013) Claritromicina Zentiva RCP versione attuale (agosto 2014) 4.2 Posologia e modo di somministrazione... Posologia... Sono stati condotti studi clinici usando claritromicina sospensione pediatrica in bambini da 6 mesi a 12 anni di età. Quindi bambini sotto i 12 anni di età devono usare claritromicina sospensione pediatrica (granulato per sospensione orale). Dosaggio nell insufficienza epatica e renale... Tuttavia, in pazienti con clearance della creatinina inferiore ai 30 ml/minuto con o senza insufficienza epatica, il dosaggio deve essere dimezzato oppure raddoppiato l intervallo di dosaggio della claritromicina. Dosaggio nella compromissione epatica e renale... Tuttavia, in pazienti con compromissione renale e clearance della creatinina inferiore ai 30 ml/min il dosaggio di claritromicina deve essere ridotto della metà, ad esempio 250 mg una volta al giorno, o 250 mg due volte al giorno in molte infezioni gravi. Il trattamento non deve continuare oltre 14 giorni in questi pazienti. Poiché le compresse non possono essere divise la dose non può essere ridotta oltre i 500 mg giornalieri, Claritromicina Zentiva 500 mg non deve essere usata in questa popolazione di pazienti (vedere paragrafo 4.3). 4.3 Controindicazioni Poiché la dose non può essere ridotta oltre i 500 mg giornalieri, Claritromicina Zentiva 500 mg è controindicato in pazienti con clearance della creatinina meno di 30 ml/min. Claritromicina è controindicata in gravidanza (vedere paragrafo 4.6). spostato nel paragrafo 4.4 Somministrazione concomitante con cisapride, pimozide, astemizolo e La concomitante somministrazione di claritromicina e uno qualsiasi dei seguenti 1
2 terfenadina. Livelli elevati di cisapride, pimozide e terfenadina possono portare a... tachicardia ventricolare, fibrillazione ventricolare e torsioni di punta. Effetti simili sono stati osservati con la somministrazione concomitante di astemizolo e di altri macrolidi ( vedere paragrafo 4.5). medicinali è controindicato: astemizolo, cisapride, pimozide, terfenadina poiché questi possono portare a... tachicardia ventricolare, fibrillazione atriale e torsione di punta (vedere paragrafo 4.5). La somministrazione concomitante con ticagrelor o ranolazina è controindicata. Claritromicina e i derivati dell ergot non devono essere somministrati contemporaneamente (vedere paragrafo 4.5). La somministrazione concomitante di claritromicina e ergotamina o diidroergotamina è controindicata, poichè questo può portare a tossicità da ergotamina (vedere paragrafo 4.5). Claritromicina non deve essere data a pazienti con un anamnesi di prolungamento del QT o aritmia ventricolare, inclusa la torsione di punta (vedere paragrafo 4.4 e 4.5). Claritromicina non deve essere data in concomitanza di inibitori di HMG-CoA reduttasi (statine) che sono ampiamente metabolizzate dal CYP3A4 (lovastatina o simvastatina) a causa dell aumentato rischio di miopatia inclusa rabdomiolisi (vedere paragrafo 4.5) Claritromicina è controindicata in pazienti con insufficienza epatica grave. Claritromicina non deve essere usata in pazienti che soffrono di insufficienza epatica grave in combinazione con compromissione renale. Come con altri potenti inibitori del CYP3A4, claritromicina non deve essere usata in pazienti che assumono colchicina. 4.4 Avvertenze speciali e precauzioni d impiego dal paragrafo 4.3 Il medico non deve prescrivere claritromicina a donne in gravidanza senza aver valutato benefici contro rischi, soprattutto durante i primi tre mesi di gravidanza (vedere paragrafo 4.6). Si richiede attenzione in pazienti con insufficienza renale grave (vedere paragrafo 4.2). 2
3 La claritromicina viene escreta principalmente attraverso il fegato e i reni. E necessario porre attenzione durante la somministrazione di questo antibiotico in pazienti con insufficienza epatica o renale. La claritromicina viene escreta principalmente attraverso il fegato. Quindi è necessario porre attenzione durante la somministrazione di antibiotici in pazienti con compromissione epatica. Si deve fare attenzione quando si sta somministrando claritromicina a pazienti con moderata o grave compromissione renale. Sono stati riportati casi di insufficienza epatica fatale (vedere paragrafo 4.8). Alcuni pazienti possono aver avuto malattie epatiche pre-esistenti o possono aver preso altri medicinali epatotossici. I pazienti devono essere avvisati di interrompere il trattamento e contattare il medico se si sviluppano segni e sintomi di malattie epatiche, così come anoressia, ittero, urine scure, prurito o addome trattabile. Con l uso di antibiotici ad ampio spettro sono state osservati casi di coliti pseudomembranose. E importante pertanto effettuare tale diagnosi in pazienti che sviluppano diarrea grave durante o dopo il trattamento con claritromicina. Con l uso di quasi tutti gli antibatterici, inclusi i macrolidi, sono stati segnalati casi di colite pseudomembranosa, con un intervallo di gravità compreso tra il moderato e il rischioso per la vita. Sono stati segnalati casi di diarrea da Clostridium difficile (CDAD) con l uso della maggior parte degli antibatterici, compresa la claritromicina, che può variare dalla diarrea moderata alla colite fatale. Il trattamento con agenti antibatterici altera la normale flora batterica intestinale, che può condurre ad una proliferazione eccessiva del C. difficile. In tutti i pazienti che, in seguito all assunzione di antibiotici, lamentino episodi di diarrea, si deve valutare l eventuale presenza di CDAD (diarrea da Clostridium difficile). Questi pazienti devono essere sottoposti ad un attenta anamnesi poiché è stato segnalato che il CDAD si può presentare nel corso dei due mesi che seguono l assunzione di agenti antibatterici. Quindi la sospensione del trattamento deve avvenire senza tener conto dell indicazione terapeutica. Deve essere effettuato un test microbico e iniziato un trattamento adeguato. Va evitata la somministrazione di agenti antiperistaltici. Sono stati riportati casi post-marketing di tossicità da colchicina con l uso concomitante di colchicina e claritromicina, specialmente in pazienti anziani, alcuni dei quali si sono verificati in pazienti con 3
4 insufficienza renale. Sono stati riportati decessi in alcuni di questi pazienti (vedere paragrafo. 4.5). La somministrazione di colchicina in concomitanza alla claritromicinaè controindicata (vedere paragrafo 4.3). Si raccomanda attenzione nella somministrazione concomitante di claritromicina e triazolobenzodiazepine, come triazolam e midazolam (vedere paragrafo. 4.5). Si raccomanda attenzione nella somministrazione concomitante di claritromicina e altri farmaci ototossici, in particolare amminoglicosidi. E quindi consigliabile un monitoraggio periodico della funzionalità vestibolare e uditiva durante e dopo il trattamento. A causa del rischio di un prolungamento dell intervallo QT, la claritromicina deve essere usata con cautela nei pazienti con malattie coronariche, storia di aritmia ventricolare, grave insufficienza cardiaca, ipokalemia e/o ipomagnesemia non compensata, bradicardia (<50 bpm), o... La claritromicina non deve essere usata in pazienti con prolungamento del QT congenito o acquisito (vedere paragrafo 4.3 & 4.5). A causa del rischio di un prolungamento dell intervallo QT, la claritromicina deve essere utilizzata con cautela nei pazienti con malattia coronarica, grave insufficienza cardiaca, ipomagnesiemia, bradicardia (<50 bpm), o... Claritromicina Zentiva non deve essere utilizzato in pazienti con congenito o acquisito prolungamento dell intervallo QT documentato e con aritmia ventricolare regressa (vedere paragrafo 4.3). - Faringiti/ tonsilliti: La claritromicina non è il farmaco di scelta per la cura di faringiti e tonsilliti causate da Streptococcus pyogenes. Per queste e per la profilassi della febbre reumatica acuta la penicillina è il farmaco di scelta. - Infezioni del tessuto molle Il principale responsabile delle infezioni del tessuto molle, Staphylococcus aureus, è frequentemente resistente alla claritromicina. Perciò, il test di sensibilità è considerato un presupposto per il trattamento delle infezioni del tessuto molle con claritromicina. Infezioni della cute e dei tessuti molli di intensità da media a moderata: Queste infezioni sono molto spesso provocate da Staphylococcus aureus e Streptococcus pyogenes, i quali possono entrambi essere resistenti ai macrolidi. Quindi è necessario effettuare un test di sensibilità. Nei casi in cui non possano essere utilizzati antibiotici betalattamici (ad es. allergie), è preferibile utilizzare altri antibiotici, come clindamicina. Attualmente i macrolidi giocano un ruolo fondamentale nelle infezioni della pelle e dei tessuti molli, come quelle causate da Corynebacterium minutissimum, acne vulgaris, erisipela e in quelle situazioni in cui non può essere instaurata una terapia a base di penicillina. Nel caso in cui si verificassero gravi reazioni di ipersensibilità acuta, come 4
5 anafilassi, Sindrome di Stevens-Johnson e necrolisi epidermica tossica, la terapia con claritromicina deve essere immediatamente interrotta e deve essere immediatamente adottato un trattamento idoneo. La claritromicina inibisce il metabolismo di alcuni inibitori dell HMG-CoA reduttasi, ciò porta ad un aumento delle concentrazioni plasmatiche di queste sostanze. (vedere paragrafo 4.5). Inibitori della HMG-CoA riduttasi (statine): E controindicato l uso concomitante di claritromicina e lovastatina o simvastatina (vedere paragrafo 4.3). Si deve prestare attenzione quando viene prescritta claritromicina con altre statine. Rabdomiolisi è stata riportata in pazienti che assumevano contemporaneamente claritromicina e statine. I pazienti devono essere monitorati per segni e sintomi di miopatia. In situazioni in cui l uso concomitanmte di claritromicina e statine non può essere evitato, si raccomada di prescrivere il dosaggio più basso registrato della statina. Si può considerare l uso di altre statine il cui metabolismo non dipende dal CYP3A (ad esempio fluvastatina) (vedere paragrafo 4.5). Come per gli altri macrolidi, la claritromicina può causare inasprimento o peggioramento della miastenia grave e deve essere perciò usata con cautela nei pazienti con miastenia grave. La claritromicina è un inibitore del CYP3A e l uso concomitante di altri prodotti medicinali che subiscono metabolismo esteso da parte di questo enzima deve essere limitato a situazioni dove è chiaramente indicato (vedere paragrafo 4.5). eliminati Sinusiti batteriche acute La claritromicina non è la sostanza di prima scelta per il trattamento delle sinusiti Ipoglicemizzanti orali/insulina: L uso concomitante di claritromicina e agenti ipoglicemizzanti orali (come sulfoniluree) e/o insulina può condurre ad una severa ipoglicemia. E raccomandato un attento monitoraggio del glucosio (vedere paragrafo 4.5). Anticoagulanti orali: C è il rischio di gravi emorragie ed un aumento significativo del rapporto internazionale normalizzato (INR) e del 5
6 tempo di protrombina quando la claritromicina è co-somministrata con warfarin (vedere paragrafo 4.5). L INR e il tempo di protrombina devono essere frequentemente monitorati in quei pazienti che vengono trattati contemporaneamente con claritromicina ed agenti anticoagulanti. H. pylori può sviluppare resistenza alla claritromicina. L uso prolungato o ripetuto della claritromicina può portare ad una crescita eccessiva di batteri o funghi non sensibili. Se si verifica una super-infezione, la claritromicina deve essere sospesa ed iniziata una terapia appropriata. L utilizzo di una qualsiasi terapia antibiotica, come con claritromicina, per trattare le infezioni da H.pylori può provocare l insorgenza di batteri resistenti ai farmaci. Come con altri antibiotici l uso prolungato di claritromicina può provocare l insorgenza di sovrainfezioni da batteri resistenti o da miceti che richiedono l interruzione del trattamento e l adozione di idonee terapie. I pazienti ipersensibili alla lincomicina o alla clindamicina possono essere ipersensibili anche alla claritromicina. Pertanto, porre attenzione in caso di prescrizione della claritromicina a tali pazienti. E necessario porre attenzione alla possibilità di una resistenza crociata tra claritromicina ed altri macrolidi, lincomicina e clindamicina. 4.5 Interazioni con altri medicinali ed altre forme di interazione La claritromicina è un inibitore del metabolismo di cisapride e terfenadina, con conseguente aumento dei livelli plasmatici di terfenadina da 2 a 3 volte. Ciò è stato associato al prolungamento dell'intervallo QT e alle aritmie cardiache, incluse tachicardia ventricolare, fibrillazione ventricolare e torsioni di punta. Sono stati riportati sintomi simili in pazienti trattati con pimozide in associazione con la claritromicina. La somministrazione concomitante di claritromicina e terfenadina, cisapride o pimozide è controindicata (vedere paragrafo 4.3). L uso dei seguenti medicinali è assolutamente controindicato a causa dei potenziali gravi effetti dovuti alla loro interazione farmacologica. Cisapride, pimozide, astemizolo e terfenadina Elevati livelli di cisapride sono stati riscontrati in pazienti che assumevano contemporaneamente cisapride e claritromicina. L assunzione concomitante ha dato luogo a intervallo QT prolungato, aritmie cardiache inclusa tachicardia ventricolare, fibrillazione ventricolare e torsione di punta. Effetti simili sono stati osservati in pazienti che assumevano contemporaneamente claritromicina e pimozide (vedere paragrafo. 4.3). In letteratura è riportato che i macrolidi alterano il metabolismo della terfenadina aumentandone i livelli che occasionalmente sono stati associati ad aritmie cardiache, quali intervallo QT prolungato, tachicardia ventricolare, fibrillazione ventricolare e torsione di punta (vedere paragrafo. 4.3). In uno studio su 14 volontari sani, la 6
7 concomittante somministrazione di claritromicina e terfenadina ha portato ad un incremento di due-tre volte del livello sierico del metabolita acido della terfenadina e ad un prolungamento dell intervallo QT che non ha portato a nessun effetto clinico rilevabile. Effetti simili sono stati associati con la somministrazione concomitante di astemizolo ed altri macrolidi. Vasocostrittori dell'ergot (per esempio diidroergotamina, ergotamina) La claritromicina non deve essere co-somministrata con i derivati dell ergot (vedere paragrafo 4.3). Sono stati riportati casi di ergotismo dovuti ad aumento dei livelli plasmatici degli alcaloidi dell ergot. Inibitori dell' HMG-CoA riduttasi La claritromicina inibisce il metabolismo di alcuni inibitori della HMG-CoA riduttasi, ciò porta ad un aumento delle concentrazioni plasmatiche di questi medicinali. La co somministrazione di claritromicina e simvastatina è stata raramente associata a rabdomiolisi. La claritromicina può causare interazioni simili con l'atorvastatina e minore interazione con cerivastatina. Quando è indicata la co somministrazione di claritromicina con simvastatina, atorvastatina, o cerivastatina, i pazienti devono essere attentamente monitorati per valutare eventuali segni e sintomi di miopatie. L effetto di altri medicinali sulla claritromicina: Induttori del CYP3A4: Gli induttori del CYP3A4 (come rifampicina, rifabutina,...) possono indurre il metabolismo della claritromicina.... Ergotamina/diidroergotamina Alcune segnalazioni post-marketing indicano che la co-somministrazione di claritromicina ed ergotamina o diidroergotamina è stata associata a tossicità acuta da ergot caratterizzata da vasospasmo ed ischemia delle estremità e di altri tessuti, incluso il sistema nervoso centrale. E controindicata la concomitante somministrazione di claritromicina e questi medicinali (vedere paragrafo. 4.3). Inibitori della HMG-CoA riduttasi (statine): E controindicato l uso concomitante di claritromicina e lovastatina o simvastatina (vedere paragrafo 4.3) poichè le statine sono estesamente metabolizzate dal CYP3A4 e il trattamento concomitante con claritromicina aumenta la loro concentrazione plasmatica e il rischio di miopatia, inclusa rabdomiolisi. Segnalazioni di rabdomiolisi sono state riportate in pazienti che assumevano contemporaneamente claritromicina e queste statine. Se il trattamento con claritromicina non può essere evitato, la terapia con simvastatina deve essere sospesa nel corso del trattamento. Deve essere usata cautela nel prescrivere claritromicina con le statine. In situazioni in cui non è possibile evitare l'uso concomitante di claritromicina con le statine, si consiglia di prescrivere il dosaggio più basso registrato della statina. Si può considerare l uso di una statina che non dipende dal metabolismo del CYP3A (ad esempio fluvastatina). I pazienti devono essere monitorati per segni e sintomi di miopatia. L effetto di altri prodotti medicinali su claritromicina I farmaci che inducono il CYP3A (ad es. rifampicina,...) possono indurre il metabolismo della claritromicina.... 7
8 In alcune circostanze, può essere necessario aumentare la dose di claritromicina e monitorarne la sicurezza e l efficacia. La claritromicina è metabolizzata dall enzima CYP3A4. Perciò, potenti inibitori di questo enzima possono inibire il metabolismo della claritromicina, portando ad un aumento delle concentrazioni plasmatiche di claritromicina. In alternativa, gli induttori del CYP3A4 possono ridurre i livelli plasmatici di claritromicina. eliminati Sono state osservate la riduzione del 39% dell AUC della claritromicina ed un aumento del 34% dell AUC del metabolita attivo 14-idrossi quando la claritromicina viene usata in concomitanza con l induttore CYP3A4 efavirenz. Rifabutina: La somministrazione concomitante di rifabutina e claritromicina risulta rispettivamente in aumento e in diminuzione, nei livelli plasmatici. Può intervenire un aumento del rischio di uveiti associato all uso di rifabutina. La concomitante somministrazione di rifabutina e claritromicina ha determinato un aumento dei livelli sierici della rifabutina, una diminuzione dei livelli sierici della claritromicina, associati ad un maggiore rischio di uveite. E stato accertato o si sospetta che i seguenti farmaci influenzino le concentrazioni di claritromicina circolante; potrebbe essere necessario procedere ad un aggiustamento del dosaggio di claritromicina o potrebbe essere presa in considerazione l eventualità di un ricorso a terapie alternative. Efavirenz, nevirapina, rifampicina, rifabutina e rifapentina I farmaci che risultano essere forti induttori del metabolismo del citocromo P450 come l efavirenz, la nevirapina, la rifampicina, la rifabutina e la rifapentina possono accelerare il metabolismo della claritromicina e di conseguenza abbassare i livelli plasmatici della claritromicina, aumentando al contempo i livelli plasmatici del 14-OH-claritromicina, un metabolita che risulta anche attivo dal punto di vista microbiologico. Poiché le attività microbiologiche della claritromicina e del 14-OH-claritromicina sono differenti per batteri diversi, l effetto terapeutico previsto potrebbe essere annullato nel corso della somministrazione concomitante di claritromicina e di induttori enzimatici. Etravirina Etravirina diminuisce i liveli di esposizione alla claritromicina; tuttavia le concentrazioni del metabolita attivo, 14- OH-claritromicinma, sonoaumentate. Poichè 14-OH-claritromicina ha ridotto l attività contro il micobacterium avium 8
9 complex (MAC), l attività complessiva contro questo patogeno può essere alterata; quindi deve essere considerata una alternativa alla claritromicina per il trattamento della MAC. Inibitori del CYP3A4: Ritonavir (200 mg tre volte al giorno) inibisce il metabolismo della claritromicina (500 mg due volte al giorno), con un aumento della Cmax, Cmin e AUC del 31%, 182% e 77%, rispettivamente. La formazione del metabolita attivo 14 idrossi è quasi completamente inibita. Una riduzione della dose di claritromicina non è probabilmente richiesta in pazienti con funzionalità renale normale, ma la dose giornaliera di claritromicina non deve superare 1 g (500 mg due volte al giorno). Comunque, la dose di claritromicina deve essere ridotta nei pazienti con insufficienza renale. Per i pazienti con una clearance della creatinina da 30 a 60 ml/min, la dose di claritromicina deve essere ridotta del 50%, e per quelli con clearance della creatinina < 30 ml/min la dose deve essere ridotta del 75%. Fluconazolo La somministrazione concomitante di 200 mg di fluconazolo al giorno e di una dose pari a 500 mg di claritromicina due volte al giorno a 21 volontari sani ha determinato aumenti della concentrazione minima basale media di claritromicina (Cmin) e dell area sotto la curva (AUC) pari al 33% ed al 18%, rispettivamente. Le concentrazioni allo stato stazionario del metabolita attivo, la 14-OH-claritromicina, non sono state influenzate in maniera significativa dalla somministrazione concomitante di fluconazolo. Non è necessario procedere ad alcun aggiustamento della dose di claritromicina. Ritonavir Uno studio di farmacocinetica ha dimostrato che la contemporanea somministrazione di 200 mg di ritonavir ogni 8 ore e 500 mg di claritromicina ogni 12 ore conduce ad una marcata inibizione del metabolismo della claritromicina. Con la concomitante somministrazione di ritonavir è stato osservato un aumento della Cmax della claritromicina pari al 31%, un aumento della Cmin del 182% ed un aumento della AUC del 77%. E stata notata una completa inibizione della formazione del 14-OH-claritromicina. In considerazione della larga finestra terapeutica della claritromicina, in pazienti con funzione renale normale, non sono necessarie riduzioni del dosaggio. Comunque, in pazienti con compromissione renale deve essere considerato il seguente aggiustamento posologico: per pazienti con clearance della creatinina (CLCR) compresa tra 30 e 60 ml/minuto, il dosaggio deve essere ridotto del 50%; in pazienti con CLCR <30 ml/minuto la dose deve essere ridotta del 75%. Non somministrare contemporaneamente più di 1 g/giorno di claritromicina con ritonavir. Simili aggiustamenti posologici devono essere considerati per quei pazienti con funzionalità renale ridotta ai quali viene somministrato ritonavir come potenziatore farmacocinetico di altri inibitori della HIV proteasi, inclusi atazanavir e saquinavir 9
10 (vedere paragrafo seguente, Interazioni farmacologiche bi-direzionali). L effetto della claritromicina su altri prodotti medicinali: La claritromicina è un inibitore dell'enzima metabolizzante CYP3A4 e della P-glicoproteina di trasporto. La claritromicina non deve essere usata durante il trattamento con altri medicinali che sono substrato del CYP3A4, a meno che i loro livelli plasmatici, gli effetti terapeutici o gli effetti indesiderati possano essere attentamente monitorati (vedere paragrafo 4.3). Medicinali che sono substrato di CYP3A4 e che vengono somministrati in concomitanza con la claritromicina possono richiedere una riduzione della dose. In alternativa, il trattamento con queste sostanze può essere sospeso durante la terapia con la claritromicina. Co somministrazione con medicinali che possono prolungare l intervallo QT: Torsioni di punta sono state riportate in pazienti che hanno ricevuto claritromicina in concomitanza con chinidina o disopiramide. Inoltre, queste combinazioni devono essere evitate, oppure i livelli plasmatici di chinidina o disopiramide attentamente monitorati per permettere Effetti della claritromicina su altri medicinali Interazioni basate sul CYP3A La somministrazione concomitante di claritromicina la quale, come è noto, inibisce il CYP3A, e di un farmaco metabolizzato principalmente dal CYP3A, potrebbe essere associata ad aumenti delle concentrazioni del farmaco che potrebbero potenziare o prolungare gli effetti terapeutici e gli effetti avversi del farmaco somministrato in concomitanza. La claritromicina deve essere utilizzata con cautela nei pazienti sottoposti a terapia con altri farmaci che sono ritenuti substrati dell enzima CYP3A, soprattutto se il substrato del CYP3A presenta un ristretto margine di sicurezza (ad esempio la carbamazepina) e/o se il substrato viene metabolizzato in maniera estesa da questo enzima. Si devono prendere in considerazione aggiustamenti del dosaggio e, quando risulti possibile, si devono attentamente monitorare le concentrazioni sieriche dei farmaci metabolizzati principalmente dal CYP3A nei pazienti sottoposti a terapia concomitante con claritromicina. I farmaci o classi di farmaci noti o ritenuti essere metabolizzati dallo stesso isozima CYP3A sono: alprazolam, astemizolo, carbamazepina, cilostazolo, cisapride, ciclosporina, disopiramide, alcaloidi della segale cornuta, lovastatina, metilprednisolone, midazolam, omeprazolo, anticoagulanti orali (es. warfarin, vedere paragrafo 4.4), pimozide, chinidina, rifabutina, sildenafil, simvastatina, tacrolimus, terfenadina, triazolam e vinblastina. Altri farmaci che interagiscono con un meccanismo simile attraverso altri isozimi nell ambito del sistema del citocromo P450 sono fenitoina, teofillina e valproato. Antiaritmici Sono stati riportati casi post-marketing di torsione di punta a seguito dell impiego concomitante di claritromicina e chinidina o disopiramide. Nel corso della somministrazione di questi farmaci in concomitanza a claritromicina è necessario effettuare un monitoraggio del tracciato elettrocardiografico per rilevare l eventuale 10
11 l aggiustamento della dose. Porre attenzione in caso di somministrazione della claritromicina a pazienti trattati con altri prodotti che possano prolungare l'intervallo QT (vedere paragrafo 4.4). Sebbene le concentrazioni plasmatiche di claritromicina e omeprazolo possono aumentare in caso di somministrazione contemporanea, non è necessario un aggiustamento del dosaggio. L aumento della concentrazione plasmatica di claritromicina può anche verificarsi in caso di co-somministrazione con antiacidi o ranitidina. Non è necessario alcun aggiustamento di dosaggio. presenza di un prolungamento dell intervallo QT. Monitorare le concentrazioni sieriche di chinidina e disopiramide durante l impiego in terapia di claritromicina. Sono stati riportati casi post-marketing di ipoglicemia con la concomitante somministrazione di di claritromicina e disopiramide. Quindi devono essere monitorati i livelli di glucosio durante la somministrazione concomitante di clariromicina e disopiramide. Agenti ipoglicemizzanti orali/insulina Con certi medicinali ipoglicemizzanti come nateglinide e repaglinide, l inibizione dell enzima CYP3A dalla claritromicina potrebbe essere coinvolta e potrebbe causare ipoglicemia quando usati in concomitanza. E raccomadato un attento monitoraggio del glucosio. Omeprazolo Soggetti adulti sani hanno ricevuto claritromicina (500 milligrammi ogni 8 ore) in associazione all omeprazolo (40 milligrammi al giorno). Le concentrazioni plasmatiche basali di omeprazolo sono risultate aumentate (la Cmax, l AUC 0-24, ed il T½ sono aumentati rispettivamente del 30%, dell 89% e del 34%) a causa della somministrazione concomitante di claritromicina. Il valore del ph gastrico medio nel corso di 24 ore è risultato pari a 5.2, quando l omeprazolo è stato somministrato in monoterapia, ed è risultato pari a 5.7, quando l omeprazolo è stato somministrato in concomitanza alla claritromicina. Aumenti plasmatici della claritromicina possono anche verificarsi quando è cosomministrata con antiacidi o ranitidina. Non sono necessari aggiustamenti del dosaggio. eliminati Al dosaggio raccomandato non ci sono interazioni cliniche significative tra la claritromicina ed il lansoprazolo. Sildenafil, tadalafil e vardenafil Ognuno di questi inibitori della fosfodiesterasi viene metabolizzato, almeno 11
12 parzialmente, dal CYP3A ed il CYP3A potrebbe essere inibito dalla concomitante somministrazione di claritromicina. È molto probabile che la somministrazione concomitante di claritromicina e sildenafil, tadalafil o vardenafil determini un aumento dell esposizione all inibitore della fosfodiesterasi. Deve pertanto essere presa in considerazione una riduzione del dosaggio di sildenafil, tadalafil e vardenafil quando tali farmaci vengono somministrati in concomitanza alla claritromicina. Carbamazepina: La claritromicina può potenziare gli effetti della carbamazepina a causa di una riduzione nella velocità di escrezione. Teofillina: La somministrazione di claritromicina a pazienti trattati con teofillina è stata associata ad un aumento della concentrazione sierica di teofillina e ad una potenziale tossicità della teofillina. Teofillina, carbamazepina Risultati di studi clinici hanno dimostrato che i livelli plasmatici di carbamazepina e teofillina possono subire un modesto ma statisticamente significativo (p 0.05) aumento quando questi siano somministrati contemporaneamente alla claritromicina. Potrebbe essere necessaria una riduzione del dosaggio. Benzodiazepine La somministrazione concomitante con claritromicina (250 mg due volte al giorno) porta all aumento di 2.7 volte dell'auc di midazolam dopo somministrazione endovenosa e di 7 volte dopo somministrazione per via orale Tolterodina La via metabolica principale della tolterodina passa attraverso l isoforma 2D6 del citocromo P450 (CYP2D6). Tuttavia, in un sottoinsieme di popolazione sprovvisto di CYP2D6, la via metabolica identificata è rappresentata dal CYP3A. In questo sottoinsieme di popolazione, l inibizione del CYP3A determina concentrazioni sieriche di tolterodina significativamente più elevate. In presenza degli inibitori del CYP3A, come la claritromicina, potrebbe essere necessaria una riduzione del dosaggio di tolterodina nella popolazione di pazienti metabolizzatori lenti CYP2D6 Triazolobenzodiazepine (ad esempio, alprazolam, midazolam, triazolam) Quando il midazolam è stato somministrato in concomitanza alla claritromicina in compresse (500 mg due volte al giorno), l AUC del midazolam è risultata aumentata di 2,7 volte in seguito alla somministrazione di midazolam per via endovenosa e di 7 volte in seguito alla somministrazione di questo farmaco per via orale Nel caso di benzodiazepine la cui eliminazione non dipenda dal CYP3A (temazepam, nitrazepam, lorazepam), è improbabile che si verifichi un interazione importante dal punto di vista clinico con la claritromicina. 12
13 Nel corso dell esperienza post-marketing, in seguito all uso concomitante di claritromicina e triazolam, sono state segnalate interazioni farmacologiche ed effetti a carico del sistema nervoso centrale (SNC) (ad esempio sonnolenza e confusione). Si consiglia di monitorare il paziente per un aumento degli effetti farmacologici a carico del Sistema Nervoso Centrale. Digossina La concentrazione di digossina nel plasma può aumentare quando co-somministrata con claritromicina. Il monitoraggio dei livelli plasmatici di digossina deve essere considerato quando il co-trattamento con la claritromicina è iniziato o terminato. Altre interazioni farmacologiche Aminoglicosidi Si consiglia cautela per quanto riguarda la somministrazione concomitante di claritromicina con altri farmaci ototossici, in particolare con aminoglicosidi. Vedere paragrafo 4.4. Colchicina La colchicina è un substrato sia del CYP3A che dell efflux transporter, P-glicoproteina (Pgp). E noto che la claritromicina ed altri macrolidi inibiscono il CYP3A e la Pgp. Quando la claritromicina e la colchicina sono somministrate contemporaneamente, l inibizione del CYP3A e/o della Pgp da parte della claritromicina può portare ad aumentata esposizione alla colchicina. Monitorare i pazienti per l insorgenza di sintomi clinici di tossicità da colchicina (vedere paragrafo. 4.4). Digossina Si ritiene che la digossina sia un substrato dell efflux tranporter, P-glicoproteina (Pgp). E noto che la claritromicina è in grado di inibire la Pgp. Quando la digossina e la claritromicina vengono somministrate in concomitanza, l inibizione della Pgp da parte della claritromicina potrebbe determinare un aumento dell esposizione alla digossina. Sono anche stati segnalati aumenti delle concentrazioni plasmatiche di digossina nel corso della vigilanza post-marketing nei pazienti sottoposti a terapia concomitante a base di digossina e claritromicina. Alcuni pazienti hanno evidenziato segni clinici analoghi a quelli che si presentano in caso di tossicità da digossina, tra cui l insorgenza di aritmie potenzialmente fatali. Le concentrazioni plasmatiche di digossina devono essere monitorate attentamente mentre i pazienti sono sottoposti a terapia concomitante con digossina e claritromicina. 13
14 Warfarin: La claritromicina può potenziare gli effetti del warfarin. Il tempo di protombina deve essere monitorato frequentemente e le dosi di warfarin aggiustate se necessario. Zidovudina... Questo può essere generalmente evitato mantenendo un appropriato intervallo tra le somministrazioni di claritromicina e zidovudina di 1-2 ore. Nei bambini, non sono state riportate tali reazioni. eliminato Zidovudina... Poichè la claritromicina sembra interferire con l assorbimento della zidovudina somministrata contemporaneamente per via orale, è opportuno sfalsare le due somministrazioni per permettere un intervallo di almeno 4 ore. Tale interazione non compare nei pazienti pediatrici quando la claritromicina sia assunta nella forma granulare contemporaneamente a zidovudina o didanosina. Questa interazione è improbabile quando la claritromicina è somministrata per via intravenosa. Fenitoina e valproato: Vi sono stati report spontanei o pubblicati di interazioni degli inibitori del CYP3A, inclusa la claritromicina, con farmaci non considerati essere metabolizzati dal CYP3A (ad es. fenitoina e valproato). Determinazioni dei livelli sierici sono raccomandate per questi farmaci quando somministrati concomitantemente alla claritromicina. Sono sati riportati livelli sierici aumentati. Interazioni Farmacologiche Bidirezionali Atazanavir La claritromicina e l atazanavir sono entrambi substrati ed inibitori del CYP3A ed esistono prove di interazione farmacologica bidirezionale tra questi farmaci. La somministrazione concomitante di claritromicina (500 mg due volte al giorno) e di atazanavir (400 mg una volta al giorno) ha determinato un aumento di ben 2 volte dell esposizione alla claritromicina ed una diminuzione del 70% dell esposizione al 14-OH-claritromicina con un aumento del 28% dell AUC di atazanavir. In virtù della larga finestra terapeutica della claritromicina, non è necessario procedere ad alcuna riduzione del dosaggio nei pazienti che presentano funzionalità renale normale. Nel caso di pazienti che presentino un insufficienza renale di grado moderato (nei quali la clearance della creatinina va da 30 a 60 ml/min), il dosaggio di claritromicina deve essere ridotto del 50%. Nel caso di pazienti in cui la clearance della creatinina risulti minore di 30 ml/min, il dosaggio di claritromicina 14
15 deve essere ridotto del 75%, utilizzando un idonea formulazione di claritromicina. Si sconsiglia la somministrazione di dosi di claritromicina superiori a 1000 mg al giorno in concomitanza alla somministrazione degli inibitori della proteasi. Antagonisti dei canali del calcio Si deve prestare attenzione con la somministrazione concomitante di claritromicina e antagonisti dei canali del calcio metabolizzati dal CYP3A4 (ad esempio verapamil, amlodipina, diltiazem) a causa del rischio di ipotensione. Le concentrazioni plasmatiche di claritromicina così come gli antagonisti dei canali del calcio possono aumentare l interazione. Ipotensione, bradiaritmia e acidosi lattica sono state osservate in pazienti che assumevano claritromicina e verapamil in concomitanza. Itraconazolo La claritromicina e l itraconazolo sono entrambi substrati ed inibitori del CYP3A e ciò determina un interazione farmacologica bidirezionale fra questi farmaci. La claritromicina può determinare un aumento dei livelli plasmatici di itraconazolo mentre l itraconazolo potrebbe aumentare i livelli plasmatici della claritromicina. I pazienti che assumono claritromicina ed itraconazolo in concomitanza devono essere attentamente monitorati per rilevare l eventuale presenza di segni e sintomi del potenziamento e del prolungamento degli effetti farmacologici di questi farmaci. Saquinavir La claritromicina e il saquinavir sono entrambi substrati ed inibitori del CYP3A e ciò determina un interazione farmacologica bidirezionale fra questi farmaci. La somministrazione concomitante di claritromicina (500 mg due volte al giorno) e di saquinavir (capsule molli di gelatina, 1200 mg tre volte al giorno) a 12 volontari sani ha determinato valori basali di AUC e Cmax che sono risultati superiori del 177% e del 187% rispetto a quelli rilevati in caso di somministrazione di saquinavir in monoterapia. I valori relativi all AUC ed alla Cmax della claritromicina sono risultati approssimativamente superiori del 40% rispetto a quelli rilevati in caso di somministrazione di claritromicina in monoterapia. Non è necessario procedere ad alcun aggiustamento del dosaggio 15
16 quando i due farmaci vengono somministrati in concomitanza per un periodo di tempo limitato alle dosi/formulazioni studiate. Le osservazioni emerse dagli studi di interazione farmacologica eseguiti utilizzando la formulazione in capsule molli di gelatina potrebbero non essere rappresentative degli effetti rilevati ricorrendo alla formulazione di saquinavir in capsule rigide di gelatina. Le osservazioni emerse dagli studi di interazione farmacologica svolti somministrando saquinavir in monoterapia potrebbero non essere rappresentative degli effetti rilevati con la terapia combinata saquinavir/ritonavir. Nel momento in cui saquinavir venisse somministrato in concomitanza al ritonavir, si deve procedere ad un attenta valutazione degli effetti potenziali che il ritonavir potrebbe avere sulla claritromicina. 4.6 Fertilità, gravidanza e allattamento Gravidanza I dati sull'uso della claritromicina nel primo trimestre in più di 200 gravidanze non hanno dimostrato una chiara evidenza di effetti teratogeni o avversi sulla salute dei neonati. I dati su di un numero limitato di donne in gravidanza che hanno ricevuto la claritromicina nel primo trimestre suggeriscono la possibilità di un aumentato rischio di aborto. Non sono fino ad ora disponibili altri dati epidemiologici rilevanti. I dati provenienti dagli studi sugli animali hanno dimostrato la presenza di tossicità riproduttiva (vedere paragrafo 5.3). Il rischio potenziale nell'uomo non è noto. CLARITROMICINA ZENTIVA non deve inoltre essere usata durante la gravidanza a meno che non strettamente necessario. Gravidanza Non è stata valutata la sicurezza della claritromicina per l utilizzo nelle donne in stato di gravidanza. Sulla base dei risultati ottenuti da studi su topi, ratti, conigli e scimmie non può essere esclusa la possibilità di effetti avversi sullo sviluppo embio-fetale. Di conseguenza non è raccomandato l uso in gravidanza senza un attenta valutazione del rischio/beneficio. Allattamento Allattamento Non è stata dimostrata la sicurezza della claritromicina durante l allattamento di bambini.... Si deve considerare anche la possibilità di sensibilizzazione. La claritromicina deve inoltre essere usata solo se i benefici per la madre sono superiori ai potenziali rischi per il feto. 16
17 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari CLARITROMICINA ZENTIVA non ha effetto sulla capacità di guidare o sull uso di macchinari. Non sono disponibili dati dell effetto della claritromicina sulla capacità di guidare o sull uso di macchinari. Il rischio di capogiri, vertigini, confusione e disorientamento, che può verificarsi in seguito alla somministrazione, deve essere tenuto in considerazione prima che il paziente guidi o utilizzi macchinari. 4.8 Effetti collaterali Gli effetti indesiderati più frequentemente riportati in soggetti adulti che ricevono la claritromicina includono diarrea (3%), nausea (3%), gusto alterato (3%), dispepsia (2%), dolore addominale/disagio (2%) e emicranie (2%). a Riassunto del profilo di sicurezza Le più frequenti e comuni reazioni avverse correlate alla terapia a base di claritromicina sia per i pazienti adulti che per i pazienti pediatrici sono dolore addominale, diarrea, nausea, vomito ed alterazione del gusto. Questi eventi avversi sono di solito di media intensità e sono coerenti con il profilo di sicurezza noto per gli antibiotici macrolidici (vedere paragrafo b del paragrafo. 4.8). Non c è una differenza significativa nell incidenza di tali reazioni avverse gastrointestinali, durante gli studi clinici, tra pazienti con o senza infezioni da micobatteri pre-esistenti. b. Tabella riassuntiva delle reazioni avverse La seguente tabella riassume le reazioni avverse segnalate durante gli studi clinici e l esperienza post-marketing relative alla claritromicina compresse a rilascio immediato, granulato per sospensione orale, polvere per soluzione iniettabile e compresse a rilascio prolungato e modificato. Infezioni ed infestazioni Comune: Eccessiva crescita di organismi resistenti, Candidosi orale Infezioni ed infestazioni Non comune: Celluliti¹, candidiasi, gastroenteriti², infezioni 3, infezioni della vagina Non nota: Colite pseudomembranosa, erisipela Patologie del sistema emolinfopoietico... Patologie del sistema emolinfopoietico Non comune:..., neutropenia 4, trombocitemia³, eosinofilia 4 Non nota: Agranulocitosi,... Disordini del sistema immunitario Non comuni: Reazioni allergiche (la gravità di queste variano dall orticaria, alla lieve eruzione cutanea fino Disturbi del sistema immunitario 5 Non comune: Reazione anafilattoide¹, ipersensibilità Non nota: Reazione anafilattica, 17
18 all anafilassi) angioedema Disturbi del metabolismo e della nutrizione Non comune: Anoressia, appetito ridotto Disturbi psichiatrici Molto rari: Psicosi,..., Incubi Disturbi psichiatrici Non comune:..., nervosismo 3, strillare 3 Non nota: Disturbo psicotico,..., depressione,..., sogni anormali Patologie del sistema nervoso Comuni: Alterazione dell olfatto Patologie del sistema nervoso Comune: Disgeusia,..., alterazione del gusto Non comune: Perdita di coscienza¹, discinesia¹,..., sonnolenza 6, tremore Non nota:..., ageusia, parosmia, anosmia,... Patologie dell orecchio e del labirinto Molto rari: Perdita reversibile dell udito Patologie dell orecchio e del labirinto Non comune:..., udito compromesso,... Non nota: Sordità Patologie cardiache... Patologie cardiache Non comune: Arresto cardiaco¹, fibrillazione atriale¹,..., extrasistoli¹, palpitazioni Patologie vascolari Comune: Vasodilatazione¹ Non nota: Emorragia 8 Patologie respiratorie, toraciche e mediastiniche Non comune: Asma¹, epistassi 2, embolia polmonare¹ Patologie gastrointestinali Comuni:..., Scolorimento reversibile dei denti, Scolorimento reversibile della lingua Molto rari: Alterazione del gusto (come sapore metallico o amaro),..., Pancreatiti, Colite pseudomembranosa Patologie gastrointestinali Non comune: Esofagite¹, malattia da reflusso gastroesofageo 2, gastrite, proctalgia 2..., distensione dell addome 4, costipazione, bocca secca, eruttazione, flatulenza Non nota: Pancreatite acuta, alterazione del colore della lingua, alterazione del colore dei denti Patologie epatobiliari Non comuni: Disfunzione epatica,..., Itterizia Patologie epatobiliari Comune: Test di funzione epatica anormale Non comune:..., alanina aminotransferasi 18
19 Molto rari: Insufficienza epatica a decorso fatale è stata riportata particolarmente nei pazienti con malattia epatica pre-esistente o nei pazienti che ricevono altri medicinali epatotossici aumentata, aspartato aminotransferasi aumentata, Gamma-glutamil transferasi aumentata 4 Non nota: Insufficienza epatica 10, ittero epatocellulare Patologie della cute e del tessuto sottocutaneo... Patologie della cute e del tessuto sottocutaneo Comune: Eruzione cutanea, iperidrosi Non comune: Dermatite bollosa¹,..., orticaria, esantema maculopapulare 3 Non nota:..., eruzione da farmaci con eosinofilia e sintomi sistemici (DRESS), acne Patologie del sistema muscoloscheletrico e del tessuto connettivo Non comuni: Atralgia,... Patologie del sistema muscoloscheletrico e del tessuto connettivo Non comune: Spasmi muscolari 3, rigidità muscolo scheletrica¹,... Non nota: Rabdomiolisi 2,11, miopatia Patologie sistemiche e condizioni relative alla sede di somministrazione... Patologie sistemiche e condizioni relative alla sede di somministrazione Molto comune: Flebite in sede di iniezione¹ Comune: Dolore in sede di iniezione¹, infiammazione in sede di iniezione¹ Non comune: Malessere 4, piressia 3,..., dolore toracico 4, brividi 4, affaticamento 4 Esami diagnostici Molto rari: Alterazioni nei test di funzionalità epatica (elevati livelli di transaminasi). E stata riportata ipoglicemia in particolare dopo la somministrazione concomitante con medicinali antidiabetici ed insulina Esami diagnostici Non comune: Rapporto albumine/globuline anormale¹, fosfatasi alcalina ematica aumentata 4, latticodeidrogenasi ematica aumentata 4 Non nota: Aumento del rapporto internazionale normalizzato 8,..., colore dell urina anormale ¹Reazione avversa riportata solo per la formulazione polvere per soluzione per iniezione 2 Reazione avversa riportata solo per la formulazione a rilascio prolungato 3 Reazione avversa riportata solo per la formulazione granulato per sospensione orale 4 Reazione avversa riportata solo per la formulazione compresse a rilascio immediato 5,7,9,10 Vedere paragrafo a) 6,8,11 Vedere paragrafo c) 19
20 c. Descrizione di reazioni avverse selezionate Flebiti in sede di iniezione, dolore in sede di iniezione, dolore provocato dalla puntura dell ago e infiammazione in sede di iniezione sono specifiche per la formulazione endovenosa. In alcuni casi di rabdomiolisi riportati la claritromicina era stata somministrata in concomitanza a statine, fibrati, colchicina o allopurinolo (vedere paragrafo. 4.3 e 4.4). Sono stati riportati casi post-marketing di interazione farmacologica ed effetti sul Sistema Nervoso Centrale (SNC) (ad es. Sonnolenza e confusione) con l uso concomitante di claritromicina e triazolam. Si suggerisce di monitorare il paziente nel caso di aumenti degli effetti farmacologici a livello del SNC (vedere paragrafo. 4.5). Sono stati riportati casi di presenza di compresse a rilascio prolungato di claritromicina nelle feci, in molti di questi casi si sono verificati in pazienti con disturbi gastrointestinali funzionali o anatomici (inclusi ileostomia o colonstomia) con tempo di transito gastrointestinale ridotto. In diversi casi si erano verificati residui di compressa nelladiarrea. Si raccomanda ai pazienti che hanno residui di compresse nelle feci e non notano nessun miglioramento nelle loro condizioni, di considerare il passaggio a una diìversa formulazione della claritromicina (ad esempio sospensione) o un altro antibiotico. Popoplazione speciale: Reazioni avverse in pazienti immunocompromessi (vedere paragrafo e) d. Popolazioni pediatriche Sono stati condotti studi clinici somministrando la sospensione pediatrica a base di claritromicina in bambini dai 6 mesi ai 12 anni di età. Di conseguenza i bambini al di sotto dei 12 anni di età devono assumere la sospensione pediatrica. Non sono disponibili dati a sufficienza per raccomandare uno schema posologico per l utilizzo di claritromicina IV in pazienti di età inferiore a 18 anni. Ci si aspetta che frequenza, tipo e gravità delle reazioni avverse siano le stesse degli adulti. 20
21 Pazienti immunocompromessi... In pazienti adulti, gli effetti indesiderati più frequentemente riportati dai pazienti trattati con dosi giornaliere di 1000 mg di claritromicina sono stati: nausea,... Usando questo criterio, circa il 2-3% dei pazienti che ricevono 1000 mg di claritromicina al giorno ha avuto un anormale innalzamento dei livelli di SGOT e SGPT ed un anormale abbassamento di leucociti e piastrine. Una percentuale inferiore di pazienti ha anche avuto un elevata concentrazione di urea nel sangue. e. Altre popolazioni speciali Pazienti immunocompromessi... Nei pazienti adulti, la reazione avversa più frequentemente riportata da pazienti trattati con dosi giornaliere totali pari a 1000 mg e 2000 mg di claritromicina sono state: nausea,... L incidenza era comparabile per quei pazienti trattati con 1000 mg e 2000 mg, ma erano generalmente 3-4 volte più frequenti in quei pazienti che ricevevano una dose giornaliera totale di claritromicina pari a 4000 mg. Sulla base di questi criteri, circa il 2% o il 3% dei pazienti che avevano assunto 1000 mg o 2000 mg di claritromicina al giorno mostravano valori estremamente elevati di SGOT e SGPT, e livelli estremamente bassi di globuli bianchi e conta piastrinica. Una più bassa percentuale di pazienti inclusa in questi due gruppi di dosaggio ha mostrato anche elevati valori di azotemia. Un incidenza lievemente più elevata di valori anormali è stata notata in pazienti trattati con 4000 mg di claritromicina al giorno per tutti i parametri esclusa la formula leucocitaria. 21
FRISIUM 10 MG CAPSULE RIGIDE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA FRISIUM 10 MG CAPSULE RIGIDE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/1598/2013 del 27 settembre
FARMACOVIGILANZA FRISIUM 10 MG CAPSULE RIGIDE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/1598/2013 del 27 settembre
KLACID 250 mg compresse rivestite Claritromicina
 KLACID 250 mg compresse rivestite Claritromicina CATEGORIA FARMACOTERAPEUTICA Antibatterico generale per uso sistemico - Macrolidi. INDICAZIONI TERAPEUTICHE Trattamento di infezioni causate da patogeni
KLACID 250 mg compresse rivestite Claritromicina CATEGORIA FARMACOTERAPEUTICA Antibatterico generale per uso sistemico - Macrolidi. INDICAZIONI TERAPEUTICHE Trattamento di infezioni causate da patogeni
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Claritromicina Ranbaxy 125 mg/5ml sospensione orale Claritromicina Ranbaxy 250 mg/5ml sospensione orale 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Claritromicina Ranbaxy 125 mg/5ml sospensione orale Claritromicina Ranbaxy 250 mg/5ml sospensione orale 2. COMPOSIZIONE QUALITATIVA
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia
 Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO CLARITROMICINA DOC Generici 250 mg compresse rivestite con film. CLARITROMICINA DOC Generici 500 mg compresse rivestite con
1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO CLARITROMICINA DOC Generici 250 mg compresse rivestite con film. CLARITROMICINA DOC Generici 500 mg compresse rivestite con
LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA LORMETAZEPAM ZENTIVA 2,5 MG/ML GOCCE ORALI, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA VENLAFAXINA ZENTIVA 37,5 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO VENLAFAXINA ZENTIVA 75 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO VENLAFAXINA ZENTIVA 150 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO
FARMACOVIGILANZA VENLAFAXINA ZENTIVA 37,5 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO VENLAFAXINA ZENTIVA 75 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO VENLAFAXINA ZENTIVA 150 MG CAPSULE RIGIDE A RILASCIO PROLUNGATO
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Maggio 2013 Nuove importanti restrizioni all uso di Protelos/Osseor (ranelato di
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Maggio 2013 Nuove importanti restrizioni all uso di Protelos/Osseor (ranelato di
RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW. Dott. Domenico Pecora Brescia
 RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW Dott. Domenico Pecora Brescia Scelta del NAO Scheda tecnica Piani terapeutici AIFA Linee guida Position paper Rimborsabilità NAO
RENDERE PIÙ SEMPLICE LA SCELTA DELLA TERAPIA ANTICOAGULANTE: NAO KNOW HOW Dott. Domenico Pecora Brescia Scelta del NAO Scheda tecnica Piani terapeutici AIFA Linee guida Position paper Rimborsabilità NAO
AZITROMICINA ZENTIVA 500 MG COMPRESSE RIVESTITE CON FILM. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA AZITROMICINA ZENTIVA 500 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA AZITROMICINA ZENTIVA 500 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ESAPENT 1000 mg Capsule molli ESAPENT 500 mg Capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ESAPENT 1000 mg capsule
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ESAPENT 1000 mg Capsule molli ESAPENT 500 mg Capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ESAPENT 1000 mg capsule
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ebastina Teva 10 mg compresse orodispersibili Ebastina Teva 20 mg compresse orodispersibili 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ebastina Teva 10 mg compresse orodispersibili Ebastina Teva 20 mg compresse orodispersibili 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE CLARITROMICINA EG 250 mg compresse rivestite con film CLARITROMICINA EG 500 mg compresse rivestite con film Medicinale equivalente Legga attentamente
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE CLARITROMICINA EG 250 mg compresse rivestite con film CLARITROMICINA EG 500 mg compresse rivestite con film Medicinale equivalente Legga attentamente
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG
 IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG Marchio: Johnson e Johnson Codice Min.: 023673066 Link: clicca qui per acquistare IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG CATEGORIA FARMACOTERAPEUTICA: Antipropulsivi.
IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG Marchio: Johnson e Johnson Codice Min.: 023673066 Link: clicca qui per acquistare IMODIUM 2 MG 8 CAPSULE RIGIDE DA 2 MG CATEGORIA FARMACOTERAPEUTICA: Antipropulsivi.
Foglio illustrativo: informazioni per l'utilizzatore. Zitromax Avium 600 mg compresse rivestite con film. Azitromicina
 Foglio illustrativo: informazioni per l'utilizzatore Zitromax Avium 600 mg compresse rivestite con film Azitromicina Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Foglio illustrativo: informazioni per l'utilizzatore Zitromax Avium 600 mg compresse rivestite con film Azitromicina Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA' MEDICINALE OLBETAM 250 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula contiene: acipimox 250 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITA' MEDICINALE OLBETAM 250 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula contiene: acipimox 250 mg
DORZOLAMIDE E TIMOLOLO ZENTIVA 20 MG/ML + 5 MG/ML COLLIRIO, SOLUZIONE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA DORZOLAMIDE E TIMOLOLO ZENTIVA 20 MG/ML + 5 MG/ML COLLIRIO, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla
FARMACOVIGILANZA DORZOLAMIDE E TIMOLOLO ZENTIVA 20 MG/ML + 5 MG/ML COLLIRIO, SOLUZIONE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI
 ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
CEFODIE Cefonicid. Categoria farmacoterapeutica Antibiotico iniettabile.
 Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
Foglio illustrativo: informazioni per il paziente. COLCHICINA LIRCA 1 mg compresse Colchicina
 Foglio illustrativo: informazioni per il paziente COLCHICINA LIRCA 1 mg compresse Colchicina Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente COLCHICINA LIRCA 1 mg compresse Colchicina Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
FOGLIO ILLUSTRATIVO. MYCOBUTIN 150 mg capsule rigide rifabutina
 FOGLIO ILLUSTRATIVO MYCOBUTIN 150 mg capsule rigide rifabutina CATEGORIA FARMACOTERAPEUTICA Antibiotico: Antimicobatterico. INDICAZIONI TERAPEUTICHE MYCOBUTIN è indicato per il trattamento di infezioni
FOGLIO ILLUSTRATIVO MYCOBUTIN 150 mg capsule rigide rifabutina CATEGORIA FARMACOTERAPEUTICA Antibiotico: Antimicobatterico. INDICAZIONI TERAPEUTICHE MYCOBUTIN è indicato per il trattamento di infezioni
Foglio illustrativo. In caso di reazioni da ipersensibilità il trattamento deve essere interrotto immediatamente e non ripreso.
 Foglio illustrativo IMMUCYTAL Compresse IMMUCYTAL Granulato per soluzione orale Categoria Farmacoterapeutica Vaccini batterici. Indicazioni terapeutiche Profilassi delle infezioni batteriche ricorrenti
Foglio illustrativo IMMUCYTAL Compresse IMMUCYTAL Granulato per soluzione orale Categoria Farmacoterapeutica Vaccini batterici. Indicazioni terapeutiche Profilassi delle infezioni batteriche ricorrenti
RIVISTA: lnt Journal of lmpotence Research (2006) 18, MJ. Dresser, D. Desai, S. Gidwani, AD. Seftel, NB. Modi O B I E T T I V I
 I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
Facoltà di Scienze Motorie Università degli Studi di Verona. Corso di Farmacologia Lezione 8: Interazioni Farmacologiche
 Facoltà di Scienze Motorie Università degli Studi di Verona Corso di Farmacologia Lezione 8: Interazioni Farmacologiche EFFETTO DI UNA INTERAZIONE Interazioni tra farmaci n Sommazione n Addizione Farmaco
Facoltà di Scienze Motorie Università degli Studi di Verona Corso di Farmacologia Lezione 8: Interazioni Farmacologiche EFFETTO DI UNA INTERAZIONE Interazioni tra farmaci n Sommazione n Addizione Farmaco
Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali
 Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
INTERAZIONI FARMACOLOGICHE
 INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
Foglio illustrativo: informazioni per l'utilizzatore. CLARITROMICINA EUROGENERICI 500 mg compresse rivestite con film a rilascio prolungato
 Foglio illustrativo: informazioni per l'utilizzatore CLARITROMICINA EUROGENERICI 500 mg compresse rivestite con film a rilascio prolungato Medicinale equivalente Legga attentamente questo foglio prima
Foglio illustrativo: informazioni per l'utilizzatore CLARITROMICINA EUROGENERICI 500 mg compresse rivestite con film a rilascio prolungato Medicinale equivalente Legga attentamente questo foglio prima
Terapia del dolore in oncologia
 Terapia del dolore in oncologia Classi farmacologiche e interazioni con farmaci di uso comune Dr. Gianluigi Lunardi UC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar Interazioni tra farmaci
Terapia del dolore in oncologia Classi farmacologiche e interazioni con farmaci di uso comune Dr. Gianluigi Lunardi UC Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar Interazioni tra farmaci
Foglio illustrativo: informazioni per il paziente. CEFTAZIDIMA EG 1 g/ 3 ml polvere e solvente per soluzione iniettabile per uso intramuscolare
 Foglio illustrativo: informazioni per il paziente CEFTAZIDIMA EG 1 g/ 3 ml polvere e solvente per soluzione iniettabile per uso intramuscolare Medicinale equivalente Legga attentamente questo foglio prima
Foglio illustrativo: informazioni per il paziente CEFTAZIDIMA EG 1 g/ 3 ml polvere e solvente per soluzione iniettabile per uso intramuscolare Medicinale equivalente Legga attentamente questo foglio prima
FOGLIO ILLUSTRATIVO. MYCOBUTIN 150 mg capsule rigide rifabutina
 FOGLIO ILLUSTRATIVO MYCOBUTIN 150 mg capsule rigide rifabutina CATEGORIA FARMACOTERAPEUTICA Antibiotico: Antimicobatterico. INDICAZIONI TERAPEUTICHE MYCOBUTIN è indicato per il trattamento di infezioni
FOGLIO ILLUSTRATIVO MYCOBUTIN 150 mg capsule rigide rifabutina CATEGORIA FARMACOTERAPEUTICA Antibiotico: Antimicobatterico. INDICAZIONI TERAPEUTICHE MYCOBUTIN è indicato per il trattamento di infezioni
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VERMOX 500mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene: Principio attivo: Mebendazolo 500
Farmaci utilizzati nelle malattie infettive
 Farmaci utilizzati nelle malattie infettive Concetti generali β-lattamine Ott 2002 Concetti generali Antibiosi, antibiotici Effetto batteriostatico / battericida Spettro d azione Resistenza Rapporto sito
Farmaci utilizzati nelle malattie infettive Concetti generali β-lattamine Ott 2002 Concetti generali Antibiosi, antibiotici Effetto batteriostatico / battericida Spettro d azione Resistenza Rapporto sito
Foglio illustrativo: informazioni per il paziente. CEFIXIMA EUROGENERICI 400 mg compresse dispersibili. Medicinale equivalente
 Foglio illustrativo: informazioni per il paziente CEFIXIMA EUROGENERICI 400 mg compresse dispersibili Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente CEFIXIMA EUROGENERICI 400 mg compresse dispersibili Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Antibatterici attivi sulla sintesi degli acidi nucleici
 Antibiotici Antibatterici attivi sulla sintesi degli acidi nucleici Chinoloni Cumarine Inibitori della diidrofolato reduttasi Sulfonamidi Rifamicine Inibitori della sintesi proteica Tetracicline Macrolidi
Antibiotici Antibatterici attivi sulla sintesi degli acidi nucleici Chinoloni Cumarine Inibitori della diidrofolato reduttasi Sulfonamidi Rifamicine Inibitori della sintesi proteica Tetracicline Macrolidi
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE CLARITROMICINA EG 250 mg compresse rivestite con film CLARITROMICINA EG 500 mg compresse rivestite con film Medicinale equivalente Legga attentamente
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE CLARITROMICINA EG 250 mg compresse rivestite con film CLARITROMICINA EG 500 mg compresse rivestite con film Medicinale equivalente Legga attentamente
Facoltà di Scienze Motorie Università degli Studi di Verona. Lezione 8: Interazioni Farmacologiche
 Facoltà di Scienze Motorie Università degli Studi di Verona Corso di Farmacologia Lezione 8: Interazioni Farmacologiche EFFETTO DI UNA INTERAZIONE Nella pratica clinica l uso di più farmaci è spesso utile
Facoltà di Scienze Motorie Università degli Studi di Verona Corso di Farmacologia Lezione 8: Interazioni Farmacologiche EFFETTO DI UNA INTERAZIONE Nella pratica clinica l uso di più farmaci è spesso utile
Additions appear in italics and underlined deletions in italics and strikethrough
 ALLEGATO III 1 AMENDMENTS TO BE INCLUDED IN THE RELEVANT SECTIONS OF THE SUMMARY OF PRODUCT CHARACTERISTICS OF NIMESULIDE CONTAINING MEDICINAL PRODUCTS (SYSTEMIC FORMULATIONS) Additions appear in italics
ALLEGATO III 1 AMENDMENTS TO BE INCLUDED IN THE RELEVANT SECTIONS OF THE SUMMARY OF PRODUCT CHARACTERISTICS OF NIMESULIDE CONTAINING MEDICINAL PRODUCTS (SYSTEMIC FORMULATIONS) Additions appear in italics
FOGLIO ILLUSTRATIVO confezione 50 compresse. Sodio bicarbonato Sella 500 mg compresse. CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato
 FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
FOGLIO ILLUSTRATIVO confezione 50 compresse Sodio bicarbonato Sella 500 mg compresse CATEGORIA FARMACOTERAPEUTICA Antiacidi con sodio bicarbonato INDICAZIONI TERAPEUTICHE Trattamento a breve termine dell
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose
 GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
GLUCOBAY 50 mg compresse GLUCOBAY 100 mg compresse acarbose Categoria farmacoterapeutica Farmaco usato nel diabete; ipoglicemizzanti orali. Indicazioni terapeutiche Diabete mellito non-insulino-dipendente
Foglio illustrativo: informazioni per il paziente. DISSENTEN 2 mg compresse loperamide
 Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Foglio illustrativo: informazioni per il paziente DISSENTEN 2 mg compresse loperamide Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei.
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Foglio illustrativo: informazioni per l'utilizzatore. Zitromax 500 mg polvere per soluzione per infusione. Azitromicina
 Foglio illustrativo: informazioni per l'utilizzatore Zitromax 500 mg polvere per soluzione per infusione Azitromicina Legga attentamente questo foglio prima che venga somministrato questo medicinale perché
Foglio illustrativo: informazioni per l'utilizzatore Zitromax 500 mg polvere per soluzione per infusione Azitromicina Legga attentamente questo foglio prima che venga somministrato questo medicinale perché
Foglio illustrativo. LOPERAMIDE ANGENERICO 2mg capsule rigide. Loperamide. Medicinale Equivalente
 Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
Foglio illustrativo LOPERAMIDE ANGENERICO 2mg capsule rigide Loperamide Medicinale Equivalente CATEGORIA FARMACOTERAPEUTICA Antipropulsivi INDICAZIONI TERAPEUTICHE Trattamento sintomatico della diarrea
CATEGORIA FARMACOTERAPEUTICA Preparato antivertigine. TITOLARE AIC Italfarmaco S.p.A. - Viale Fulvio Testi, Milano
 FLUGERAL 5 mg capsule rigide 20 capsule FLUGERAL 5 mg capsule rigide 30 capsule FLUGERAL 5 mg capsule rigide 50 capsule FLUGERAL 10 mg capsule rigide 20 capsule FLUGERAL 10 mg capsule rigide 30 capsule
FLUGERAL 5 mg capsule rigide 20 capsule FLUGERAL 5 mg capsule rigide 30 capsule FLUGERAL 5 mg capsule rigide 50 capsule FLUGERAL 10 mg capsule rigide 20 capsule FLUGERAL 10 mg capsule rigide 30 capsule
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente COLECALCIFEROLO EG 25.000 U.I./2,5 ml soluzione orale Colecalciferolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Foglio illustrativo: informazioni per il paziente COLECALCIFEROLO EG 25.000 U.I./2,5 ml soluzione orale Colecalciferolo Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Riassunto delle Caratteristiche del Prodotto
 Riassunto delle Caratteristiche del Prodotto 1. DENOMINAZIONE DEL MEDICINALE Omega 3 Mylan Generics Capsule molli da 1000 mg. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000
Riassunto delle Caratteristiche del Prodotto 1. DENOMINAZIONE DEL MEDICINALE Omega 3 Mylan Generics Capsule molli da 1000 mg. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000
Foglio illustrativo: informazioni per l utilizzatore. CEFOTAXIMA EG 1 g polvere e solvente per soluzione iniettabile per uso intramuscolare
 Foglio illustrativo: informazioni per l utilizzatore CEFOTAXIMA EG 1 g polvere e solvente per soluzione iniettabile per uso intramuscolare Medicinale equivalente Legga attentamente questo foglio prima
Foglio illustrativo: informazioni per l utilizzatore CEFOTAXIMA EG 1 g polvere e solvente per soluzione iniettabile per uso intramuscolare Medicinale equivalente Legga attentamente questo foglio prima
Approfondimenti scientifici
 Approfondimenti scientifici 2 J. Studi comparativi di farmacocinetica e sicurezza di capsule orali e compresse orodispersibili di lansoprazolo in soggetti sani W. FRESTON Aliment Pharmacol Ther 2003; 17:
Approfondimenti scientifici 2 J. Studi comparativi di farmacocinetica e sicurezza di capsule orali e compresse orodispersibili di lansoprazolo in soggetti sani W. FRESTON Aliment Pharmacol Ther 2003; 17:
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Norvir 80 mg/ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml di soluzione orale contiene
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Norvir 80 mg/ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml di soluzione orale contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
FOGLIO ILLUSTRATIVO. azitromicina
 1 1 FOGLIO ILLUSTRATIVO AZITROMICINA PFIZER 100 mg polvere per sospensione orale AZITROMICINA PFIZER 150 mg polvere per sospensione orale AZITROMICINA PFIZER 200 mg polvere per sospensione orale AZITROMICINA
1 1 FOGLIO ILLUSTRATIVO AZITROMICINA PFIZER 100 mg polvere per sospensione orale AZITROMICINA PFIZER 150 mg polvere per sospensione orale AZITROMICINA PFIZER 200 mg polvere per sospensione orale AZITROMICINA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE BICALUTAMIDE DOC Generici 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una compressa contiene
ALLEGATO III SEZIONI RILEVANTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIETTO ILLUSTRATIVO
 ALLEGATO III SEZIONI RILEVANTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIETTO ILLUSTRATIVO Nota: le modifiche di questo riassunto delle caratteristiche del prodotto e del foglio illustrativo
ALLEGATO III SEZIONI RILEVANTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIETTO ILLUSTRATIVO Nota: le modifiche di questo riassunto delle caratteristiche del prodotto e del foglio illustrativo
3. INDICAZIONE DEL(I) PRINCIPIO(I) ATTIVO(I) E DEGLI ALTRI INGREDIENTI
 FOGLIETTO ILLUSTRATIVO PER: Onsior 5 mg compresse per cani Onsior 10 mg compresse per cani Onsior 20 mg compresse per cani Onsior 40 mg compresse per cani 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO PER: Onsior 5 mg compresse per cani Onsior 10 mg compresse per cani Onsior 20 mg compresse per cani Onsior 40 mg compresse per cani 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE
SCHEMI TERAPEUTICI IN ONCOLOGIA: PRESCRIZIONE, ALLESTIMENTO E SOMMINISTRAZIONE DEI FARMACI AL PAZIENTE Carcinoma del rene e casi clinici
 III CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna 22 e 23 febbraio 2012 SCHEMI TERAPEUTICI IN ONCOLOGIA: PRESCRIZIONE,
III CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna 22 e 23 febbraio 2012 SCHEMI TERAPEUTICI IN ONCOLOGIA: PRESCRIZIONE,
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri)
 AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ECOMESOL 1% crema vaginale ECOMESOL 50 mg ovuli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ECOMESOL 1% crema vaginale: 100 g
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ECOMESOL 1% crema vaginale ECOMESOL 50 mg ovuli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA ECOMESOL 1% crema vaginale: 100 g
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
Allegato III. Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo
 Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Azitromicina ratiopharm Italia 200mg/5 ml polvere per sospensione orale.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Azitromicina ratiopharm Italia 200mg/5 ml polvere per sospensione orale. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 5 ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Azitromicina ratiopharm Italia 200mg/5 ml polvere per sospensione orale. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 5 ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Eccipienti con effetti noti: lattosio monoidrato 119,61 mg/compressa
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VASCOMAN 10 mg compresse VASCOMAN 20 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA VASCOMAN 10 mg compresse Ogni compressa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VASCOMAN 10 mg compresse VASCOMAN 20 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA VASCOMAN 10 mg compresse Ogni compressa
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO
 ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 25 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 25 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
Trattamento farmacologico dell ulcera gastro-duodenale L. 29
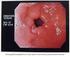 Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
Trattamento farmacologico dell ulcera gastroduodenale L. 29 Fisiologia della secrezione acida dello stomaco vago PI 2 K + + M 3 2 + Cellula Antrale D peptidi Cellula Antrale elicobacter pylori vago Antiacidi
4. INFORMAZIONI CLINICHE
 ALLEGATO 1: MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO (RCP) Il Riassunto delle Caratteristiche del Prodotto di abacavir solfato (ZIAGEN) è stato modificato sulla base delle osservazioni
ALLEGATO 1: MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO (RCP) Il Riassunto delle Caratteristiche del Prodotto di abacavir solfato (ZIAGEN) è stato modificato sulla base delle osservazioni
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Kaletra (80 mg + 20 mg) / ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 1 ml di Kaletra soluzione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Kaletra (80 mg + 20 mg) / ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 1 ml di Kaletra soluzione
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO
 ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
CHE COSA E FLUIBRON TOSSE SECCA 30 mg/5 ml sciroppo è un farmaco sedativo della tosse.
 PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
FOGLIO ILLUSTRATIVO 1 / 5
 FOGLIO ILLUSTRATIVO 1 / 5 Foglio illustrativo: informazioni per il paziente Borocaina gola 1,5 mg pastiglie gusto arancia Borocaina gola 1,5 mg pastigliegusto ciliegia Borocaina gola 1,5 mg p pastigliegusto
FOGLIO ILLUSTRATIVO 1 / 5 Foglio illustrativo: informazioni per il paziente Borocaina gola 1,5 mg pastiglie gusto arancia Borocaina gola 1,5 mg pastigliegusto ciliegia Borocaina gola 1,5 mg p pastigliegusto
Foglio illustrativo: informazioni per il paziente. DALACIN C 150 mg capsule rigide. Clindamicina
 Foglio illustrativo: informazioni per il paziente DALACIN C 150 mg capsule rigide Clindamicina Legga attentamente questo foglio prima di prendere/dare al suo bambino questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per il paziente DALACIN C 150 mg capsule rigide Clindamicina Legga attentamente questo foglio prima di prendere/dare al suo bambino questo medicinale perché contiene importanti
AZIENDA PER I SERVIZI SANITARI N 1 TRIESTINA CENTRO CARDIOVASCOLARE. Direttore: dott. Andrea Di Lenarda
 AZIENDA PER I SERVIZI SANITARI N 1 TRIESTINA CENTRO CARDIOVASCOLARE Direttore: dott. Andrea Di Lenarda Responsabile infermieristico: Donatella Radini OPUSCOLO INFORMATIVO PAZIENTI Nuovi farmaci anticoagulanti
AZIENDA PER I SERVIZI SANITARI N 1 TRIESTINA CENTRO CARDIOVASCOLARE Direttore: dott. Andrea Di Lenarda Responsabile infermieristico: Donatella Radini OPUSCOLO INFORMATIVO PAZIENTI Nuovi farmaci anticoagulanti
Acido ascorbico Medicinale equivalente
 Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
Foglio illustrativo: informazioni per l utilizzatore Acido ascorbico Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per
Per l elenco completo degli eccipienti, vedere paragrafo 6.1.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Cetirizina Germed 10 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 10 mg
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Cetirizina Germed 10 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene 10 mg
RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIBRADIN 10 mg capsule a rilascio modificato LIBRADIN 20 mg capsule a rilascio modificato 2. COMPOSIZIONEQUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DELPRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIBRADIN 10 mg capsule a rilascio modificato LIBRADIN 20 mg capsule a rilascio modificato 2. COMPOSIZIONEQUALITATIVA E QUANTITATIVA
RUOLO INFERMIERISTICO NELLA GESTIONE DELLA TERAPIA ANTICOAGULANTE ORALE (TAO) Lusi Pappalardo -- Convegno REP
 RUOLO INFERMIERISTICO NELLA GESTIONE DELLA TERAPIA ANTICOAGULANTE ORALE (TAO) 1 WARFARIN: SOSTANZA CHE RIDUCE LA CAPACITÀ DEL SANGUE DI COAGULARE. E DISPONIBILE IN COMPRESSE DIVISIBILI, CHE POSSONO QUINDI
RUOLO INFERMIERISTICO NELLA GESTIONE DELLA TERAPIA ANTICOAGULANTE ORALE (TAO) 1 WARFARIN: SOSTANZA CHE RIDUCE LA CAPACITÀ DEL SANGUE DI COAGULARE. E DISPONIBILE IN COMPRESSE DIVISIBILI, CHE POSSONO QUINDI
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vimpat 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa rivestita
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vimpat 50 mg compresse rivestite con film 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna compressa rivestita
Allegato I. Conclusioni scientifiche e motivazioni per la variazione dei termini dell'/delle autorizzazione/i all immissione in commercio
 Allegato I Conclusioni scientifiche e motivazioni per la variazione dei termini dell'/delle autorizzazione/i all immissione in commercio 1 Conclusioni scientifiche Sulla base del Rapporto di valutazione
Allegato I Conclusioni scientifiche e motivazioni per la variazione dei termini dell'/delle autorizzazione/i all immissione in commercio 1 Conclusioni scientifiche Sulla base del Rapporto di valutazione
Foglio illustrativo: informazioni per l'utilizzatore
 Foglio illustrativo: informazioni per l'utilizzatore Azitromicina Pfizer 500 mg compresse rivestite con film Azitromicina Pfizer 200 mg/5 ml polvere per sospensione orale Azitromicina Legga attentamente
Foglio illustrativo: informazioni per l'utilizzatore Azitromicina Pfizer 500 mg compresse rivestite con film Azitromicina Pfizer 200 mg/5 ml polvere per sospensione orale Azitromicina Legga attentamente
Interazioni Comuni. Interazioni Specifiche
 Interazioni Comuni Antagonisti ormonali: possibile aumento del rischio di miopatia con danazolo; Antiaritmici: aumento del rischio di miopatia con amiodarone; Ciclosporina: aumento del rischio di miopatia
Interazioni Comuni Antagonisti ormonali: possibile aumento del rischio di miopatia con danazolo; Antiaritmici: aumento del rischio di miopatia con amiodarone; Ciclosporina: aumento del rischio di miopatia
Foglio illustrativo: informazioni per l'utilizzatore. Zitromax 500 mg compresse rivestite con film Zitromax 200 mg/5 ml polvere per sospensione orale
 Foglio illustrativo: informazioni per l'utilizzatore Zitromax 500 mg compresse rivestite con film Zitromax 200 mg/5 ml polvere per sospensione orale Azitromicina Legga attentamente questo foglio prima
Foglio illustrativo: informazioni per l'utilizzatore Zitromax 500 mg compresse rivestite con film Zitromax 200 mg/5 ml polvere per sospensione orale Azitromicina Legga attentamente questo foglio prima
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Kaletra 80 mg / ml + 20 mg/ ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 1 ml di Kaletra
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Kaletra 80 mg / ml + 20 mg/ ml soluzione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni 1 ml di Kaletra
Foglio illustrativo: informazioni per il paziente FOSFOMICINA EG ADULTI 3 G GRANULATO PER SOLUZIONE ORALE. Medicinale equivalente
 Foglio illustrativo: informazioni per il paziente FOSFOMICINA EG ADULTI 3 G GRANULATO PER SOLUZIONE ORALE Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente FOSFOMICINA EG ADULTI 3 G GRANULATO PER SOLUZIONE ORALE Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Aptivus 250 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 250 mg di tipranavir.
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Aptivus 250 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 250 mg di tipranavir.
IRC: ANTIBIOTICI,MA SOPRATTUTTO CON PRUDENZA? Dott. Maurizio Gherzi S.C. Nefrologia e Dialisi Ospedale di Ceva
 IRC: QUALI ANTIBIOTICI O TUTTI GLI ANTIBIOTICI,MA SOPRATTUTTO CON PRUDENZA? I Dott. Maurizio Gherzi S.C. Nefrologia e Dialisi Ospedale di Ceva PERCHE SI SVILUPPA NEFROTOSSICITA? (1) Il flusso di sangue
IRC: QUALI ANTIBIOTICI O TUTTI GLI ANTIBIOTICI,MA SOPRATTUTTO CON PRUDENZA? I Dott. Maurizio Gherzi S.C. Nefrologia e Dialisi Ospedale di Ceva PERCHE SI SVILUPPA NEFROTOSSICITA? (1) Il flusso di sangue
Foglio illustrativo: informazioni per il paziente. Neo-Cibalgina compresse
 Foglio illustrativo: informazioni per il paziente Neo-Cibalgina compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei. Prenda questo
Foglio illustrativo: informazioni per il paziente Neo-Cibalgina compresse Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni per lei. Prenda questo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE LIOTONDOL 2,5% gel 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di gel contengono: Principio attivo: ketoprofene 2,5 g.
