Impariamo a fare il sapone artigianale!
|
|
|
- Giacomo Alberti
- 7 anni fa
- Visualizzazioni
Transcript
1 Workshop Impariamo a fare il sapone artigianale! In collaborazione di: IAAS ASA Sassari e EuReKÅ Sassari Con: Roberta Cucciari
2 Programma 15:15 - Presentazione dell'occorrente per fare il sapone, con storie e racconti di come si faceva una volta, e breve spiegazione delle reazione chimiche coinvolte nel processo di saponificazione 15:30 - Saponificazione: processo di saponificazione e aggiunta ingredienti 16:00 -Preparazione di una saponificazione che faranno i partecipanti al corso 17:00 - Pausa di sedimentazione nuove conoscenze 17:20 - Taglio del sapone 18:00 - Confezione delle saponette 18:30 - Tavola rotonda, domande, racconti, storie, aneddoti autosufficienza domestica e sostenibilità ecologica. Conversione degli stili di vita alla salute ed alla sobrietà. 19:00 - Distribuzione sapone, saluti e ringraziamenti.
3 un po di storia Si ritiene che sia del tutto casuale la scoperta del sapone, ma è anche possibile che sia avvenuta per via empirica. Probabilmente per prime si ottennero liscivie alcaline dalla cenere di legno, che poi vennero mescolate al sego, scarti animali, oli vegetali.
4 A quando risale il primo sapone? Secondo Plinio il Vecchio secondo il quale i Galli, gli Egiziani e i Fenici producevano sapone da sego di capra e cenere. Galeno, il medico di Marco Aurelio (II secolo d.c.), fu apparentemente il primo a riconoscere le qualità pulenti del sapone, ma la sua propaganda non fu molto efficace. Mentre gli uomini cominciarono a usarlo, le donne erano scettiche, e continuarono ad usare solo acqua. Tuttavia il sapone era un articolo di lusso, utilizzato per regali di alto pregio, e quindi di rarissimo uso. Nel XVIII secolo la manifattura del sapone divenne maggiormente diffusa. La limitazione era nella soda caustica che non era facilmente disponibile, mentre il grasso animale lo era. Quindi dalle ceneri di legno si otteneva carbonato di potassio che non è molto efficace né rapido nell'azione; si cominciò a rafforzare la soluzione con calce ottenendo idrossido di potassio e carbonato di calcio; il procedimento semi industriale rendeva necessario l'utilizzo di enormi quantità di legna.
5 Le foreste furono salvate dal processo Leblanc per la produzione di carbonato di sodio. Il primo detergente sintetico fu un olio di ricino solfato usato nell'industria tessile dal La prima formulazione sintetica risale al 1907 (Henkel) Il primo detergente anionico sintetico fu prodotto negli anni '30 dalla Shell solfonando olefine derivanti dal petrolio e si chiamava Teepol. Dopo la guerra la disponibilità di idrocarburi a basso costo rese attraente l'idea di un detergente di sintesi.. Questo tensioattivo fu la base per i detergenti degli anni '50 e '60. Il problema di questi tensioattivi era che non essendo biodegradabili cominciarono a dare problemi ambientali. In seguito i gruppi aromatici furono sostituiti (totalmente o parzialmente) con gruppi alifatici lineari, meno dannosi per l'ambiente naturale.
6 ..Ma cosa è il sapone? Il sapone è generalmente un sale di sodio o di potassio di un acido carbossilico alifatico a lunga catena, derivato da un idrolisi alcalina di esteri come i trigliceridi. Il sapone appartiene a una particolare classe di composti organici, chiamati tensioattivi.
7 Cosa è un tensioattivo? I tensioattivi so no sostanze che hanno la proprietà di abbassare
8 Perché il sapone pulisce? Tipica struttura 3D di una micella testa idrofilica o polare Azione detergente del sapone coda idrofobica o apolare Idrofilica: ha affinità con l acqua. Idrofobica: ha repulsione con l acqua.
9 Quali sono i reagenti? Trigliceridi e esteri: di origine vegetale o animale Alcali: idrossido di sodio, o di potassio
10 Cosa sono gli alcali? Un alcalo è una base forte. Una base forte in soluzione acquosa è completamente dissociata, e cioè dà luogo ad una ionizzazione totale. Le principali basi forti sono: idrossido di sodio NaOH idrossido di potassio KOH idrossido di calcio Ca(OH)2 idrossido di bario Ba(OH)2 idrossido di magnesio Mg(OH)2.
11 Cosa è un trigliceride? Modello molecolare 3D CH2- OH CH2-OCOR CH-OH + 3 RCOOH CH-OCOR formula di un generico trigliceride CH2-OH CH2-OCOR I trigliceridi sono i materiali di riserva e si trovano immagazzinati nelle cellule adipose. Possono essere saturi o insaturi possono avere lo stesso acido e quindi essere semplici oppure formati da acidi diversi ed essere chiamati misti. La maggioranza degli acidi naturali sono misti. Insolubili in acqua essi si dispongono con le teste polari dalla parte del liquido polare, viceversa con la parte idrofoba si rivolgono sempre verso la parte apolare. Si formano degli aggregati molecolari rotondeggianti dette micelle, hanno dimensioni microscopiche. Glicerolo Acido Carbossilico a catena lunga
12 Come si fa il sapone? O H 3 C C O carbossilato (sapone) Reazione di saponificazione 2 O O 3 1 H 3 C C OH H 3 C C O H O CH 3 4 O CH 3 K+ o Na+ O CH3 Il nucleofilo (ambiente basico) estere uscito funge ora da base strappando il protone CH3OH K+ o Na+ alcol È un meccanismo di sostituzione nucleofila bimolecolare
13 ..nel dettaglio L idrolisi basica di un estere lo trasforma nel sale dell acido carbossilico corrispondente. Il nucleofilo, in questo caso, è lo ione idrossido (OH-); il gruppo uscente è lo ione alcossido (RO-). Quest ultimo, in realtà, non è di per sé un buon gruppo uscente per una reazione SN2: tuttavia l energia di legame del carbonile è alta per cui è molto forte la tendenza ad eliminare lo ione alcossido e a riformare il carbonile. La reazione va a completamento (freccia unica e doppia, nell ultimo passaggio) perché lo ione alcossido (o lo ione idrossido) è una base molto più forte del carbossilato e quindi strappa il protone all acido carbossilico via via che questo si forma.
14 Grazie per l attenzione.
LIPIDI. I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi.
 LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
LIPIDI. Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI. Steroidi Acidi grassi Trigliceridi Fosfolipidi Prostaglandine Vitamine liposolubili
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Con il termine generico di lipidi si definisce una classe. eterogenea dal punto di vista chimico di composti
 on il termine generico di lipidi si definisce una classe eterogenea dal punto di vista chimico di composti presenti nei tessuti animali e vegetali, accomunati dalla somiglianza di proprietà fisiche, come
on il termine generico di lipidi si definisce una classe eterogenea dal punto di vista chimico di composti presenti nei tessuti animali e vegetali, accomunati dalla somiglianza di proprietà fisiche, come
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Lipidi. Grassi e Oli Cere Fosfolipidi Eicosanoidi (Prostaglandine, Trombossani, Leucotrieni) Terpeni Steroidi Vitamine solubili nei lipidi
 Lipidi I lipidi sono un gruppo di composti organici, a struttura anche molto diversa, che hanno come comune caratteristica la solubilità in solventi organici (es. etere, cloroformio, acetone e benzene)
Lipidi I lipidi sono un gruppo di composti organici, a struttura anche molto diversa, che hanno come comune caratteristica la solubilità in solventi organici (es. etere, cloroformio, acetone e benzene)
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Le definizioni di acido e di base Un percorso storico
 Le definizioni di acido e di base Un percorso storico Corpaci Ivana Teoria degli acidi e delle basi w Cos è un acido?! Una sostanza corrosiva, chimicamente molto attiva, che colora di rosso la cartina
Le definizioni di acido e di base Un percorso storico Corpaci Ivana Teoria degli acidi e delle basi w Cos è un acido?! Una sostanza corrosiva, chimicamente molto attiva, che colora di rosso la cartina
Caratteristiche generali
 Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
Aspetti generali dei lipidi
 7.3 I lipidi Aspetti generali dei lipidi I lipidi, anche detti grassi, sono composti organici ternari, ovvero formati da tre elementi chimici C, H, O (possono contenere anche P, N). Caratteristiche: -
7.3 I lipidi Aspetti generali dei lipidi I lipidi, anche detti grassi, sono composti organici ternari, ovvero formati da tre elementi chimici C, H, O (possono contenere anche P, N). Caratteristiche: -
CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00
![CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00 CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00](/thumbs/68/59131328.jpg) CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
Composti Carbossilici. Reattività
 omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
omposti arbossilici eattività omposti carbossilici N ' ' Ammide N' 2 Estere ' ' Anidride () 2 X Alogenuro acilico X I composti carbossilici hanno la caratteristica comune di possedere un gruppo carbonilico
H + Pertanto, [H + ] è espressa in termini di. ph = -log [H + ]
![H + Pertanto, [H + ] è espressa in termini di. ph = -log [H + ] H + Pertanto, [H + ] è espressa in termini di. ph = -log [H + ]](/thumbs/98/135766427.jpg) ph La concentrazione molare di H + in una soluzione acquosa è di solito molto bassa. Pertanto, [H + ] è espressa in termini di ph = -log [H + ] 31 ph di soluzioni di acidi forti Abbiamo detto che gli acidi
ph La concentrazione molare di H + in una soluzione acquosa è di solito molto bassa. Pertanto, [H + ] è espressa in termini di ph = -log [H + ] 31 ph di soluzioni di acidi forti Abbiamo detto che gli acidi
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Lipidi. Piccole molecole organiche di scarsa solubilità in acqua. Grassi, oli, cere, alcuni ormoni, alcune vitamine
 Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi. Piccole molecole organiche di scarsa solubilità in acqua. Grassi, oli, cere, alcuni ormoni, alcune vitamine
 Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lezione 6. Acidi e Basi Equilibri Acido Base ph delle Soluzioni Saline
 2018 Lezione 6. Acidi e Basi Equilibri Acido Base ph delle Soluzioni Saline 1 Definizioni di Acido e Base Arrhenius - Brønsted - Lewis Acido di Arrhenius è una sostanza che libera in acqua ioni H + (H
2018 Lezione 6. Acidi e Basi Equilibri Acido Base ph delle Soluzioni Saline 1 Definizioni di Acido e Base Arrhenius - Brønsted - Lewis Acido di Arrhenius è una sostanza che libera in acqua ioni H + (H
Arrhenius. HCl H + + Cl - NaOH Na + + OH -
 Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
LIPIDI FUNZIONI. Agenti emulsionanti (acido colico) Riserva energetica a livello cellulare (trigliceridi) Vitamine (vit.
 LIPIDI Classe eterogenea di composti organici naturali che hanno come caratteristiche comuni: la presenza di una porzione idrofobica nella molecola; la conseguente insolubilità in acqua; l uso di solventi
LIPIDI Classe eterogenea di composti organici naturali che hanno come caratteristiche comuni: la presenza di una porzione idrofobica nella molecola; la conseguente insolubilità in acqua; l uso di solventi
Caratteristiche generali
 Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
Acido maleico anidride maleica acido ftalico andidride ftalica
 Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Appunti di Stechiometria per Chimica
 Appunti di Stechiometria per Chimica Equilibri in soluzione acquosa Teoria degli acidi/basi secondo Brönsted-Lowry Acido una qualunque sostanza che è capace di donare uno ione idrogeno ad un altra sostanza
Appunti di Stechiometria per Chimica Equilibri in soluzione acquosa Teoria degli acidi/basi secondo Brönsted-Lowry Acido una qualunque sostanza che è capace di donare uno ione idrogeno ad un altra sostanza
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione
![ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione](/thumbs/57/40353116.jpg) ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
Soluti in acqua. Elettroliti. Non elettroliti
 Soluti in acqua Elettroliti Forti Dissociazione Elettrolitica COMPLETA Soluto Deboli Dissociazione Elettrolitica NON COMPLETA Non elettroliti Dissociazione Elettrolitica NaCl (s) + acqua Na + (aq) + Cl
Soluti in acqua Elettroliti Forti Dissociazione Elettrolitica COMPLETA Soluto Deboli Dissociazione Elettrolitica NON COMPLETA Non elettroliti Dissociazione Elettrolitica NaCl (s) + acqua Na + (aq) + Cl
Introduzione alla biochimica AO 11/14
 Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
Introduzione alla biochimica AO 11/14 Il Gruppo Carbonilico 1. E uno dei gruppi funzionali più importanti 2. Sp2, legame polarizzato 1. Ossigeno elettronegativo: effetto induttivo 2. Effetto di risonanza
I lipidi hanno un ampia varietà. idrofobica
 I lipidi hanno un ampia varietà strutturale: Grasso animale, Colesterolo hanno in comune la natura idrofobica trigliceridi steroidi Acidi grassi Acido stearico, Acido linolenico Doppi legami Z (cis) Gli
I lipidi hanno un ampia varietà strutturale: Grasso animale, Colesterolo hanno in comune la natura idrofobica trigliceridi steroidi Acidi grassi Acido stearico, Acido linolenico Doppi legami Z (cis) Gli
Acidi e Basi. Capitolo 15
 Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Attività laboratoriale di «Trasformazione dei prodotti»
 Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE
 SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
HCl è un acido NaOH è una base. HCl H + + Clˉ NaOH Na + + OHˉ. Una reazione acido-base di Arrhenius forma acqua e un sale. HCl + NaOH H 2 O + NaCl
 Secondo Arrhenius un acido è una sostanza che dissociandosi in acqua libera protoni (H + ). Una base è una sostanza che dissociandosi in acqua libera ioni ossidrile (OHˉ). H 2 O HCl H + + Clˉ H 2 O NaOH
Secondo Arrhenius un acido è una sostanza che dissociandosi in acqua libera protoni (H + ). Una base è una sostanza che dissociandosi in acqua libera ioni ossidrile (OHˉ). H 2 O HCl H + + Clˉ H 2 O NaOH
Applicazioni biotecnologiche degli enzimi: le lipasi
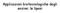 Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile
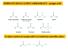 DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
Idrolisi salina. acido e base reagendo insieme formano un sale e acqua AH BOH AB H2O
 Idrolisi salina acido e base reagendo insieme formano un sale e acqua AH BOH AB HO metallo + non metallo sale K + F KF (fluoruro di potassio) ossido + anidride sale MgO + SO 3 MgSO 4 (solfato di magnesio)
Idrolisi salina acido e base reagendo insieme formano un sale e acqua AH BOH AB HO metallo + non metallo sale K + F KF (fluoruro di potassio) ossido + anidride sale MgO + SO 3 MgSO 4 (solfato di magnesio)
Applicazioni biotecnologiche degli enzimi: le lipasi
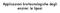 Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Lipidi. 1.Trigliceridi 2.Fosfogliceridi 3.Sfingolipidi 4.Prostaglandine 5.Terpeni 6.Steroidi
 Lipidi Lipidi Sono sostanze solubili in composti organici non polari, e possono essere suddivise in 6 distinte tipologie sulla base della loro struttura e funzione: 1.Trigliceridi 2.Fosfogliceridi 3.Sfingolipidi
Lipidi Lipidi Sono sostanze solubili in composti organici non polari, e possono essere suddivise in 6 distinte tipologie sulla base della loro struttura e funzione: 1.Trigliceridi 2.Fosfogliceridi 3.Sfingolipidi
Ionizzazione spontanea dell acqua: autoprotolisi o autoionizzazione dell acqua. [ H ] 2
![Ionizzazione spontanea dell acqua: autoprotolisi o autoionizzazione dell acqua. [ H ] 2 Ionizzazione spontanea dell acqua: autoprotolisi o autoionizzazione dell acqua. [ H ] 2](/thumbs/57/40353351.jpg) Equilibri ionici in soluzione acquosa L acqua, anche se purissima, rivela una conducibilità elettrica piccola ma misurabile che indica la presenza di ioni. Una ridotta frazione di molecole di acqua è dissociata
Equilibri ionici in soluzione acquosa L acqua, anche se purissima, rivela una conducibilità elettrica piccola ma misurabile che indica la presenza di ioni. Una ridotta frazione di molecole di acqua è dissociata
Le Reazioni Chimiche
 Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
2. La chimica della vita Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA
 Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Capitolo 8 Acidi Carbossilici e Derivati
 Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Equilibri in soluzione acquosa unità 1, modulo G del libro
 Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
LA MOLE. Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12
 LA MOLE Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12 NA = 6,022 x 10 23 particelle /mol numero di Avogadro 1 mole
LA MOLE Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12 NA = 6,022 x 10 23 particelle /mol numero di Avogadro 1 mole
14/05/2013. Lipidi. Piccole molecole organiche di scarsa solubilità in acqua. Grassi, oli, cere, alcuni ormoni, alcune vitamine
 Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi. Piccole molecole organiche di scarsa solubilità in acqua. Grassi, oli, cere, alcuni ormoni, alcune vitamine
 Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
Lipidi Piccole molecole organiche di scarsa solubilità in acqua Grasso animale, Colesterolo Grassi, oli, cere, alcuni ormoni, alcune vitamine Divisi in due gruppi: con legami esterei idrolizzabili e non
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
CHIMICA ORGANICA. 2 a D. Novembre Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14. Ponte Felcino Perugia.
 CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
NOMENCLATURA CHIMICA
 NOMENCLATURA CHIMICA Cationi monoatomici Ione + nome dell elemento Sel elementonepuòformarepiùdiuno: - suffisso oso per lo stato con carica minore - suffisso ico per quello con carica maggiore oppure si
NOMENCLATURA CHIMICA Cationi monoatomici Ione + nome dell elemento Sel elementonepuòformarepiùdiuno: - suffisso oso per lo stato con carica minore - suffisso ico per quello con carica maggiore oppure si
MODULO 2 UNITÀ 2.3 I LIPIDI
 MODULO 2 UNITÀ 2.3 I LIPIDI Pag. 116 Aspetti generali I lipidi, anche detti grassi, sono composti ternari C, H, O (possono contenere anche P, N) Caratteristiche: sono untuosi al tatto sono insolubili in
MODULO 2 UNITÀ 2.3 I LIPIDI Pag. 116 Aspetti generali I lipidi, anche detti grassi, sono composti ternari C, H, O (possono contenere anche P, N) Caratteristiche: sono untuosi al tatto sono insolubili in
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
Equilibri ionici in soluzione acquosa. Acidi, basi, scala del ph
 Equilibri ionici in soluzione acquosa Acidi, basi, scala del ph 1 Data una generica reazione bisogna cercare di capire perché una reazione procede spontaneamente in una direzione piuttosto che in quella
Equilibri ionici in soluzione acquosa Acidi, basi, scala del ph 1 Data una generica reazione bisogna cercare di capire perché una reazione procede spontaneamente in una direzione piuttosto che in quella
PIANO DI STUDIO DELLA DISCIPLINA
 ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 https://isisfacchinetti.gov.it CHIMICA ORGANICA PIANO DELLE
ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 https://isisfacchinetti.gov.it CHIMICA ORGANICA PIANO DELLE
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia LIPIDI
 Precorsi Test AMMISSINE Medicina e hirurgia - Professioni Sanitarie Università degli Studi di Perugia LIPIDI a.a. 2016/2017 LIPIDI lipide significa grasso A temperatura ambiente alcuni sono solidi (grassi),
Precorsi Test AMMISSINE Medicina e hirurgia - Professioni Sanitarie Università degli Studi di Perugia LIPIDI a.a. 2016/2017 LIPIDI lipide significa grasso A temperatura ambiente alcuni sono solidi (grassi),
PON C4 "LE SCIENZE IN GARA!"
 PON C4 "LE SCIENZE IN GARA!" Approfondimenti di Chimica e Biologia: ph, poh, soluzioni tampone, acidi monoprotici e poliprotici, acido acetico, acetati, ammine, ammidi. prof. Ciro Formica Calcolo della
PON C4 "LE SCIENZE IN GARA!" Approfondimenti di Chimica e Biologia: ph, poh, soluzioni tampone, acidi monoprotici e poliprotici, acido acetico, acetati, ammine, ammidi. prof. Ciro Formica Calcolo della
Equilibri ionici in soluzione acquosa. Acidi, basi, scala del ph
 Equilibri ionici in soluzione acquosa Acidi, basi, scala del ph 1 L equilibrio chimico LA LEGGE DELL EQUILIBRIO CHIMICO (legge dell azione di massa) Ad equilibrio raggiunto il rapporto tra il prodotto
Equilibri ionici in soluzione acquosa Acidi, basi, scala del ph 1 L equilibrio chimico LA LEGGE DELL EQUILIBRIO CHIMICO (legge dell azione di massa) Ad equilibrio raggiunto il rapporto tra il prodotto
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Struttura dei lipidi. acidi grassi trigliceridi cere
 Struttura dei lipidi acidi grassi trigliceridi cere LIPIDI a differenza di carboidrati, proteine, acidi nucleici hanno strutture chimiche differenti fra loro sono composti apolari o anfipatici, scarsamente
Struttura dei lipidi acidi grassi trigliceridi cere LIPIDI a differenza di carboidrati, proteine, acidi nucleici hanno strutture chimiche differenti fra loro sono composti apolari o anfipatici, scarsamente
Cos è la Fisiologia Scienza che studia la vita e le funzioni organiche dei vegetali, degli animali e dell uomo
 Cos è la Fisiologia Scienza che studia la vita e le funzioni organiche dei vegetali, degli animali e dell uomo Cosa studia? Studia l omeostasi, ovvero tutti i processi con i quali è mantenuto costante
Cos è la Fisiologia Scienza che studia la vita e le funzioni organiche dei vegetali, degli animali e dell uomo Cosa studia? Studia l omeostasi, ovvero tutti i processi con i quali è mantenuto costante
Derivati degli acidi carbossilici
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Derivati degli acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze
04/10/17 I LEGAMI DEL CARBONIO. Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole
 04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
Equilibri ionici in soluzione. Acidi, basi, scala del ph
 Equilibri ionici in soluzione Acidi, basi, scala del ph 1 L equilibrio chimico LA LEGGE DELL EQUILIBRIO CHIMICO (legge dell azione di massa) Ad equilibrio raggiunto il rapporto tra il prodotto delle concentrazioni
Equilibri ionici in soluzione Acidi, basi, scala del ph 1 L equilibrio chimico LA LEGGE DELL EQUILIBRIO CHIMICO (legge dell azione di massa) Ad equilibrio raggiunto il rapporto tra il prodotto delle concentrazioni
Lipidi Semplici: Gliceridi (Mono, Di e Trigliceridi; esteri del GLICEROLO con Ac. Grassi a lunga catena). CERE
 I lipidi sono un gruppo eterogeneo di sostanze. Essi sono caratterizzati dalla insolubilità in acqua (o scarsa solubilità) e dalla affinità per i solventi apolari e per gli altri lipidi (natura fortemente
I lipidi sono un gruppo eterogeneo di sostanze. Essi sono caratterizzati dalla insolubilità in acqua (o scarsa solubilità) e dalla affinità per i solventi apolari e per gli altri lipidi (natura fortemente
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
ACIDI E BASI ORGANICI: pka e ph
 Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Gli Acidi e le Basi. Nell acqua distillata la [H 3 O + ] = [OH - ] quindi
![Gli Acidi e le Basi. Nell acqua distillata la [H 3 O + ] = [OH - ] quindi Gli Acidi e le Basi. Nell acqua distillata la [H 3 O + ] = [OH - ] quindi](/thumbs/70/63736139.jpg) Gli Acidi e le Basi Nell acqua distillata la [H 3 O ] = [OH - ] quindi [H 3 O ] 1 = [OH ] Esistono soluti elettroliti che modificano questo rapporto; -Gli elettroliti, che aggiunti all acqua, rendono il
Gli Acidi e le Basi Nell acqua distillata la [H 3 O ] = [OH - ] quindi [H 3 O ] 1 = [OH ] Esistono soluti elettroliti che modificano questo rapporto; -Gli elettroliti, che aggiunti all acqua, rendono il
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
RELAZIONE CHIMICA TITOLO: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA
 RELAZIONE CHIMICA TITOLO: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA OBIETTIVO: OSSERVARE LE REAZIONI CHE AVVENGONO TRA ALCUNI IONI IN SOLUZIONE ACQUOSA E DESCRIVERE L ASPETTO DEL PRECIPITATO CHE SI FORMA
RELAZIONE CHIMICA TITOLO: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA OBIETTIVO: OSSERVARE LE REAZIONI CHE AVVENGONO TRA ALCUNI IONI IN SOLUZIONE ACQUOSA E DESCRIVERE L ASPETTO DEL PRECIPITATO CHE SI FORMA
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa
 Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Le Reazioni Chimiche
 I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
Diapositive n. 3, 4 Ma quali sono le proprietà degli acidi e delle basi?
 it Acidi e basi. Diapositiva n. 2 La parola acido viene dal latino acidum che significa aspro, pungente. La parola alcali (le parole alcali e basi sono sinonimi) viene dall arabo al-qalì che sta ad indicare
it Acidi e basi. Diapositiva n. 2 La parola acido viene dal latino acidum che significa aspro, pungente. La parola alcali (le parole alcali e basi sono sinonimi) viene dall arabo al-qalì che sta ad indicare
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Gilbert Keith Chesterton
 Un'avventura è soltanto un fastidio considerato nel modo giusto. Un fastidio è soltanto un'avventura considerata nel modo sbagliato. Gilbert Keith Chesterton LA MOLE Si definisce MOLE una quantita di sostanza
Un'avventura è soltanto un fastidio considerato nel modo giusto. Un fastidio è soltanto un'avventura considerata nel modo sbagliato. Gilbert Keith Chesterton LA MOLE Si definisce MOLE una quantita di sostanza
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione. Composti: specie chimiche definite formate da due o più elementi
 Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
MEMBRANE. struttura: fosfolipidi e proteine
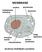 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
Produzione di metilesteri
 BIODIESEL Tra i biocombustibili in sostituzione del diesel si possono usare anche olii vegetali, in percentuale controllata con gasolio, questi presentano un elevata viscosità e numerose controindicazioni
BIODIESEL Tra i biocombustibili in sostituzione del diesel si possono usare anche olii vegetali, in percentuale controllata con gasolio, questi presentano un elevata viscosità e numerose controindicazioni
