METABOLISMO DEGLI AMMINOACIDI
|
|
|
- Mariangela Vittoria Messina
- 9 anni fa
- Просмотров:
Транскрипт
1 PRINCIPI NUTRITIVI
2 METABOLISMO DEGLI AMMINOACIDI Nel corso della digestione le proteine vengono degradate in amminoacidi. Contrariamente ai carboidrati, gli amminoacidi non vengono immagazzinati, ma vengono ossidati per produrre ATP oppure utilizzati per la sintesi di nuove proteine. Gli amminoacidi in eccesso introdotti con la dieta vengono convertiti in trigliceridi di riserva. Nel digiuno sono fondamentali per la gluconeogenesi.
3 METABOLISMO DEGLI AMMINOACIDI Sintesi proteica pool di amminoacidi assorbimento 1. digestione proteine della dieta (fonte primaria) a. turnover proteine ( riciclaggio o ricambio ) sintesi endogena precursori metabolici (α-chetoacidi) 2. degradazione proteine cellulari endocellulare b. proteine danneggiate, difettose, etc fonte di azoto (come NH 4+ ) composti azotati (nucleotidi e altri a.a.) carburante metabolico (non possono essere accumulati o escreti) deamminazione necessaria scheletri carboniosi intermedi metabolici
4 AMMINOACIDI ESSENZIALI AMINOACIDI ESSENZIALI AMINOACIDI NON ESSENZIALI Valina Leucina Glicina Alanina β-ossidazione piruvato Isoleucina Serina Treonina Metionina Cisteina Tirosina ossalacetato corpi chetonici Fenilalanina Acido Aspartico Lisina Asparagina Triptofano Acido glutammico Istidina * Glutammina Arginina * Prolina * Essenziali solo nel corso dello sviluppo
5 TURNOVER DELLE PROTEINE estremamente variabile da proteina a proteina tempo di emivita Può essere influenzato da: i) danneggiamenti e/o alterazioni ii) difetti di sintesi rapido turnover detossificazione proteine regolatorie degradazione proteine Segnale biologico: ubiquitinazione etichettatura segnale di morte Ub (8.5 kda)
6 DIGESTIONE ED ASSORBIMENTO DELLE PROTEINE Proteolisi Enzimi gastrici e pancreatici un lavoro pericoloso Enzimi enterici (peptidasi) zimogeni (pro-enzimi) pancreatici stomaco pepsinogeno pepsina tripsina attivatore comune
7 PEPSINOGENO E PEPSINA Per molte ragioni gli enzimi digestivi sono degli ottimi candidati per la ricerca scientifica. Possono essere isolati facilmente e sono presenti in grande quantità nei succhi digestivi. Sono anche straordinariamente stabili perché sono adatti a lavorare nelle particolari condizioni presenti nel sistema digestivo.
8 PEPSINOGENO E PEPSINA
9 DIGESTIONE DELLE PROTEINE ALIMENTARI
10 DIGESTIONE DELLE PROTEINE ALIMENTARI
11 UPTAKE DEGLI AMMINOACIDI
12 IDROLASI GASTRICHE E PANCREATICHE endopeptidasi
13 DIGESTIONE DELLE PROTEINE
14 ENZIMI DIGESTIVI PROTEOLITICI metallo-proteasi (enteriche) esopeptidasi amminoacidi Idrolasi endopeptidasi oligopeptidi proteasi carbossiliche e serin-proteasi (gastriche e pancreatiche) Proteine peptidi amminoacidi uptake endopeptidasi esopeptidasi trasportatori
15 ENDOPEPTIDASI DIGESTIVE Enzima Origine ph ottimale Attivatore Pepsina stomaco 1,5 2,5 HCl - Pepsina Tripsina pancreas esocrino 7,5 8,5 Enteropeptidasi Tripsina Chimotripsina Elastasi pancreas esocrino pancreas esocrino 7,5 8,5 Tripsina 7,5 8,5 Tripsina
16 ESOPEPTIDASI DIGESTIVE Enzima Origine ph ottimale Attivatore Carbossipeptidasi A pancreas esocrino ph del succo intestinale Tripsina Carbossipeptidasi B pancreas esocrino ph del succo intestinale Tripsina Amminopeptidasi mucosa intestinale ph del succo intestinale sempre attive Dipeptidasi e Tripeptidasi mucosa intestinale ph del succo intestinale sempre attive Peptidasi intracellulari epitelio intestinale ph citosolico sempre attive
17 PROTEASI DIGESTIVE Enzima Proenzima Attivatore Reazione catalizzata Proteasi carbossiliche Pepsina A Pepsinogeno A ph acido, pepsina R R CO-NHCHCO-NHCHCO R = Tyr, Phe, Leu Serin-proteasi Tripsina Chimotripsina Elastasi Tripsinogeno Chimotripsinogeno Proelastasi Enteropeptidasi, Tripsina Tripsina Tripsina R R CO-NHCHCO-NHCHCO R = Arg, Lys R R CO-NHCHCO-NHCHCO R = Tyr, Trp, Phe, Met, Leu R R CO-NHCHCO-NHCHCO R = Ala, Gly, Ser Zn-peptidasi Carbossipeptidasi A Procarbossipeptidasi A Tripsina R CO-NHCHCO 2 R = Val, Leu, Ile, Ala Carbossipeptidasi B Procarbossipeptidasi B Tripsina R Amminopeptidasi CO-NHCHCO 2 R = Arg, Lys
18 BIOCHIMICA DELLA NUTRIZIONE L assorbimento degli amminoacidi è rapido nel duodeno e nel digiuno e lento nell ileo e richiede l intervento di un trasportatore. Sembra esistere un unico trasportatore per gli amminoacidi neutri (ala, ser), uno per quelli basici (arg, lys), uno per gli acidi (glu, asp) ed uno per glicina, prolina e idrossiprolina.
19 REGOLAZIONE DEL METABOLISMO PROTEICO Regolazione ormonale del metabolismo degli amminoacidi se introdotti in eccesso, stimola l utilizzo metabolico degli aa per sintetizzare lipidi e produrre energia INSULINA stimola la sintesi proteica GLUCAGONE stimola la degradazione delle proteine stimola la gluconeogenesi
20 AZOTO essenziale per la vita amminoacidi proteine Nucleotidi acidi nucleici In natura - N2 atmosferico (N.B. N N triplo legame, molta energia per metabolizzarlo) - ione nitrato NO3 presente nel suolo Nei sistemi biologici sono presenti le forme ridotte - ione ammonio NH4+ libero - gruppo amminico (-NH3+) e gruppo ammidico (-NH- C=O ) presenti in composti organici
21 GLI ANIMALI DIPENDONO DA BATTERI E PIANTE PER L AZOTO I.Soltanto alcuni batteri anaerobi, simbionti nelle radici delle leguminose, sono in grado di fissare (ridurre) l N2 atmosferico con produzione di NH4+, che è quindi ossidato da altri batteri a nitrato NO3. II. Le piante sono in grado di utilizzare NO3 con produzione di NH4+, che è quindi incorporato nei composti organici azotati (punto d ingresso glutammato e glutammina) III. Gli animali assumono composti organici azotati (amminoacidi)
22 Tutte le macromolecole biologiche sono derivati (composti) del carbonio
23
24 Gli atomi di carbonio uniti con legame covalente possono formare catene lineari, ramificate o anche strutture cicliche A questi scheletri carboniosi si possono unire gruppi di altri atomi chiamati gruppi funzionali Le reazioni delle molecole si basano sulle reazioni dei rispettivi gruppi funzionali
25
26
27 Stereochimica In biochimica, oltre ai gruppi funzionali è anche importante la distribuzione spaziale degli atomi di una molecola nello spazio cioè la sua stereochimica
28 a)rappresentazione in prospettiva b) Modello a palle e bastoncino c) Modello spaziale
29 Isomeri configurazionali sono una conseguenza della presenza nella molecola o di un doppio legame o di un centro chilarico Isomeri configurazionali non si possono interconvertire l uno nell altro senza che si abbia una temporanea rottura di uno o più legami
30
31 Una molecola con un solo centro chiralico darà origine a due steroisomeri con caratteristiche fisiche e sopprattutto biologiche molto diverse a) enantiomeri b) diasteroisomeri
32
33
34 Conformazioni della molecola di etano
35 Reazioni biochimiche Nelle cellule avvengono migliaia di reazioni biochimiche tutte riconducibili a 4-5 tipi diversi di reazioni a) Estrazione dell energia dalle sostanze nutritive b) Trasformazioni di sostanze semplici come il glucosio in amminoacidi, nucleotidi, lipidi, etc ) Polimerizzazione di subunità monomeriche in macromolecole
36 1 Reazioni di ossido-riduzione 2 Scissione e formazione di legami carbonio-carbonio (reazioni di sostituzione nucleofila) 3 Reazione di ridistribuzione degli elettroni che porta ad isomerizzazione 4 Reazioni di trasferimento di gruppi per attivare intermedi metabolici 5. Reazioni di condensazione
37
38 AMMINOACIDI
39 Asparagina: primo amminoacido identificato1806 Treonina: l ultimo amminoacido identificato 1938 Asparagina: asparagi Glutammato: glutine Tirosina: dal formaggio (greco tyros)
40
41 GLI AMMINOACIDI PRESENTANO ALMENO UN ATOMO DI CARBONIO CHIRALICO, PRODUCONO DUE STEREOISOMERI: Stereoisomero L Stereoisomero D
42 Sistema di nomenclatura D-L, convenzione proposta da Fisher nel 1891
43
44 Lo stato di ionizzazione di un amminoacido varia in funzione del ph
45 Uno zwitterone (ione ibrido) può agire sia come acido sia come base. Le sostanze con questa doppia natura sono dette anfoteriche
46
47 Gruppo tioetere Secondo C chirale
48
49 Gruppi ammidici Gruppo tiolico
50 Gruppo idrocarburico aromatico
51 Gli amminoacidi aromatici sono in grado di assorbire la luce ultravioletta ad una lunghezza d onda pari a 280 nm Proprietà utilizzata dai ricercatori per individuare e quantizzare le proteine Legge di Lambert-Beer Log Io/I = εcl Log Io/I è definito assorbanza c=moli per litro l= 1cm cammino ottico
52 Gruppo amminico primario Gruppo guanidinico Gruppo imidazolico
53 CLASSIFICAZIONE NUTRIZIONALE AMMINOACIDI ESSENZIALI : devono necessariamente essere introdotti preformati con la dieta valina* leucina* isoleucina* metionina* fenilalanina* triptofano* istidina lisina treonina * possono essere ottenuti per transaminazione dai rispettivi α-chetoacidi gli altri tre vanno introdotti come tali AMMINOACIDI NON ESSENZIALI semi-indispensabili risparmiano i precursori essenziali tirosina (sintetizzata da fenilalanina) cisteina (sintetizzata da metionina)
54 condizionatamente essenziali glicina, serina, prolina, glutammina, arginina possono non essere sufficienti in alcuni stati particolari quali infezioni, traumi, bambini prematuri,.. non essenziali alanina, aspartato, asparagina, glutammato Le reazioni di transaminazione, reversibili, permettono di ridistribuire il gruppo NH3 fra gli amminoacidi Vanno comunque integrati con la dieta e l apporto deve essere bilanciato in quanto: - Il pool di amminoacidi non è totalmente riutilizzabile - NH3 principalmente prodotto di rifiuto, anche se vi è un riutilizzo limitato a riformare amminoacidi
55 perdita obbligatoria di azoto con le urine secrezioni intestinali, turnover enterociti, desquamazione pelle,... NH3 deriva dal catabolismo degli amminoacidi, dellebasi puriniche (tramite deaminasi) e delle basi pirimidiniche
56 Metabolismo della catena carboniosa degli amminoacidi Lo scheletro carbonioso fornisce energia attraverso l interazione con la via glicolitica ed il ciclo di Krebs In condizioni fisiologiche esiste una relazione tra il livello dei carboidrati nella dieta ed il metabolismo degli amminoacidi Aumenta quando l'apporto di energia è sufficiente ma viene fornito da proteine a scapito dei carboidrati e dei lipidi La sua efficienza (molecole di ATP prodotte) è inferiore rispetto alla degradazione degli altri due substrati (carboidrati e lipidi): - non tutto lo scheletro carbonioso degli amminoacidi è soggetto ad ossidazione - la formazione di urea (il prodotto finale del catabolismo azotato) richiede il consumo di 3 molecole di ATP
57 Formazione di acidi non volatili dal catabolismo di a.a. solforati: metionina, cisteina>so42- fosfoproteine > fosfati Fosfolipidi acidi grassi e glucosio acetoacetato, β-idrossibutirrato, lattato acidi nucleici basi puriniche>urati nutrienti con anioni inorganici (superiori alla quantita di cationi inorganici) Richiede l escrezione di un catione NH4+ (fornito dalla glutammina) per permettere all organismo di conservare cationi quali Na+, K+, Ca2+, dieta ricca in proteine genera acidi non volatili
PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a)
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Digestione e assorbimento delle proteine
 Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Ossidazione degli amminoacidi e produzione dell urea
 Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Catabolismo di proteine
 Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Catabolismo di proteine
 Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Il metabolismo dell azoto
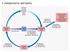 Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
Il metabolismo dell azoto La fissazione dell azoto Radici di una leguminosa e il simbionte Rhizobium leguminosarum. Microrganismi azotofissatori : ad es. batteri appartenenti ai generi Clostridium e Azotobacter.
Metabolismo. Metabolismo. Il complesso di tutte le reazioni organiche di trasformazioni tra energia e materia viene definito come metabolismo.
 Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi
 Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
CATABOLISMO AMMINOACIDI
 CATABOLISMO AMMINOACIDI 1 Catabolismo aminoacidi Digestione di proteone dalla dieta Turnover delle proteine Digiuno prolungato 2 Digestione delle proteine dalla dieta L organismo ricava la maggior parte
CATABOLISMO AMMINOACIDI 1 Catabolismo aminoacidi Digestione di proteone dalla dieta Turnover delle proteine Digiuno prolungato 2 Digestione delle proteine dalla dieta L organismo ricava la maggior parte
Nella Biosfera viene mantenuto un un equilibrio tra l azoto totale inorganico e quello organico
 Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
L integrazione proteica nelle diverse fisiopatologie
 Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Digestione delle proteine: 6 fasi
 orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Corso di Formazione in Dietologia e Nutrizione
 Corso di Formazione in Dietologia e Nutrizione La dieta equilibrata: Alimentazione dell adulto 2 P Marina Mariani Che cosa sono i macronutrienti Proteine Lipidi Glucidi Cosa sono i macronutrienti Per vivere
Corso di Formazione in Dietologia e Nutrizione La dieta equilibrata: Alimentazione dell adulto 2 P Marina Mariani Che cosa sono i macronutrienti Proteine Lipidi Glucidi Cosa sono i macronutrienti Per vivere
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
Amminoacidi: l eliminazione dell azoto
 Amminoacidi: l eliminazione dell azoto P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Gli aa. Non sono conservati nell organismo, quelli che eccedono
Amminoacidi: l eliminazione dell azoto P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Gli aa. Non sono conservati nell organismo, quelli che eccedono
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
Degradazione delle proteine della dieta. Catabolismo degli aminoacidi
 Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, Padova. Tel.
 Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: [email protected] Funzioni delle
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: [email protected] Funzioni delle
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
La scienza nell alimentazione
 La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
La scienza nell alimentazione Intorno al 1800 la chimica prese parte all alimentazione dando al cibo un sapore migliore ma allo stesso tempo più dannoso per il corpo umano. La materia di studio della Scienza
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE
 BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Fegato e metabolismo lipidico
 Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
Fegato e metabolismo lipidico LIPIDI : Acidi grassi liberi o esterificati ad Acil gliceroli ( mono, di, tri) Fosfolipidi e colesterolo FONTI : Grassi della dieta Depositati sotto forma di goccioline (tessuto
PRINCIPI NUTRITIVI O NUTRIENTI
 Corso per istruttori di Body Building PRINCIPI NUTRITIVI O NUTRIENTI Dott. Gianfranco Serino DIETISTA ISTRUTTORE DI BODY BUILDING PRINCIPI NUTRITIVI O NUTRIENTI Gli alimenti con il processo della digestione
Corso per istruttori di Body Building PRINCIPI NUTRITIVI O NUTRIENTI Dott. Gianfranco Serino DIETISTA ISTRUTTORE DI BODY BUILDING PRINCIPI NUTRITIVI O NUTRIENTI Gli alimenti con il processo della digestione
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
Applicazioni biotecnologiche degli enzimi: le proteasi
 Applicazioni biotecnologiche degli enzimi: le proteasi Campi di applicazione delle proteasi Le proteasi catalizzano l idrolisi di legami peptidici Esopeptidasi ed endopeptidasi Specificità di riconoscimento
Applicazioni biotecnologiche degli enzimi: le proteasi Campi di applicazione delle proteasi Le proteasi catalizzano l idrolisi di legami peptidici Esopeptidasi ed endopeptidasi Specificità di riconoscimento
Digestione, assorbimento e metabolismo
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Digestione, assorbimento e metabolismo H 2 O + CO 2 + Q ATP Q ADP+P i W Biomol. + O 2 Sintesi Biomol. O 2 Energia Organismo ATP
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Digestione, assorbimento e metabolismo H 2 O + CO 2 + Q ATP Q ADP+P i W Biomol. + O 2 Sintesi Biomol. O 2 Energia Organismo ATP
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
Son Formula supplementazione aminoacidica sicura
 Son Formula supplementazione aminoacidica sicura Dott. Giovanni Posabella Medico Chirurgo Specialista in Medicina dello Sport Docente Università degli Studi dell Aquila Esperto in omeopatia, omotossicologia
Son Formula supplementazione aminoacidica sicura Dott. Giovanni Posabella Medico Chirurgo Specialista in Medicina dello Sport Docente Università degli Studi dell Aquila Esperto in omeopatia, omotossicologia
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Amilasi salivare e pancreatica (Cl - ) Amilosio degradato in maltotriosio e maltosio (destrine)
 Assorbimento dei glucidi Dieta: polisaccaridi (amido, glicogeno), Disaccaridi (lattosio, saccarosio) Demolizione ad opera di endoglicosidasi presenti nel cavo orale e nel lume intestinale mediante idrolisi
Assorbimento dei glucidi Dieta: polisaccaridi (amido, glicogeno), Disaccaridi (lattosio, saccarosio) Demolizione ad opera di endoglicosidasi presenti nel cavo orale e nel lume intestinale mediante idrolisi
Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore)
 Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore) La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato
Attenzione: Lunedì 15 la lezione sarà dalle 14 alle 16 (al posto di L. Migliore) La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
(o dotto di Santorini)
 Pancreas Il pancreas è una ghiandola a funzione mista. (o dotto di Santorini) Papilla di Vater Sfintere di Oddi Dotto di Wirshung (regola rilascio e impedisce reflusso) Il pancreas esocrino secerne tutti
Pancreas Il pancreas è una ghiandola a funzione mista. (o dotto di Santorini) Papilla di Vater Sfintere di Oddi Dotto di Wirshung (regola rilascio e impedisce reflusso) Il pancreas esocrino secerne tutti
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
LEZIONE 2 COMPOSTI DEL CARBONIO: MACROMOLECOLE:
 LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
PROTEINE. DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico.
 LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Unità fondamentale di tutti gli organismi viventi.
 La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
La quantità di glu presente nei liquidi extracellulari è di circa 20g, 80kcal.
 I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Metabolismo dei composti azotati: aminoacidi e nucleotidi
 Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
 METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
Cap.21 CATABOLISMO DEI LIPIDI
 Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
mediante proteasi industriali
 Valorizzazione delle farine disoleate mediante proteasi industriali Alessandra Stefan Unità operativa: CSGI (Consorzio per lo Sviluppo dei Sistemi a Grande Interfase, Firenze) Dipartimento di Farmacia
Valorizzazione delle farine disoleate mediante proteasi industriali Alessandra Stefan Unità operativa: CSGI (Consorzio per lo Sviluppo dei Sistemi a Grande Interfase, Firenze) Dipartimento di Farmacia
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Proteine Gli amminoacidi:principali caratteristiche chimico-fisiche.potere tampone. I 20 amminoacidi delle proteine:classificazione.
 Proteine Gli amminoacidi:principali caratteristiche chimico-fisiche.potere tampone. I 20 amminoacidi delle proteine:classificazione.amminoacidi essenziali. Proprietà del legame peptidico.proteine fibrose
Proteine Gli amminoacidi:principali caratteristiche chimico-fisiche.potere tampone. I 20 amminoacidi delle proteine:classificazione.amminoacidi essenziali. Proprietà del legame peptidico.proteine fibrose
PROTEINA GREGGIA (P.G.)
 PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
