Università degli Studi di Napoli Federico II
|
|
|
- Luca Leonardi
- 7 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi di Napoli Federico II Facoltà di Farmacia Corso di Laurea in Chimica e Tecnologie Farmaceutiche Tesi sperimentale in Chimica Fisica "Caratterizzazione strutturale mediante diffrazione dei raggi X e dicroismo circolare del mutante des-(16-20)-rnasi A" Relatore: Ch.ma Prof.ssa Filomena Sica Candidata: Nancy Acampa Matricola: 512/2343 ANNO ACCADEMICO 2009/2010
2 Capitolo 1 INTRODUZIONE Negli ultimi anni, in campo scientifico grande attenzione è stata rivolta all aggregazione delle proteine. Questo processo è il risultato di differenti meccanismi tra loro interconnessi, come ad esempio cambiamenti conformazionali e strutturali delle singole molecole proteiche, processi di nucleazione, interazioni proteina-proteina e conseguente formazione di legami intermolecolari (Vitagliano et al.,1999). L aggregazione proteica è un fenomeno rilevante sia per l acquisizione di nuove funzioni, sia per la produzione di depositi di natura patologica. Infatti, alcune condizioni neurodegenerative, sono associate alla deposizione, in particolari aree celebrali o del sistema nervoso periferico, di aggregati fibrillari polimerici di specifiche proteine o peptidi. Queste patologie comprendono condizioni diffuse soprattutto nella popolazione anziana, come il morbo di Alzheimer e il morbo di Parkinson e patologie non frequenti o addirittura rare, come varie encefalopatie spongiformi trasmissibili, come ad esempio l Encefalopatia spongiforme bovina (BSE) e la Sindrome di Creutzfeldt-Jakob (CJD) oppure vari tipi di atassia, sclerosi laterale amiotrofica, etc. La presenza di aggregati proteici è stata anche riscontrata, nelle cosiddette malattie da espansione glutamminica (ad indicare che la proteina in questione si aggrega quando il numero di residui di glutammina, costituenti sequenze ininterrotte nell ambito di essa, superi le 40 unità circa), quali, la malattia di Huntington e quella di Kennedy (Perutz, 1999). Gli aggregati proteici vengono definiti fibrille amiloidi quando si formano in vivo fuori la cellula e inclusioni intracellulari quando si formano in vivo nella cellula. Gli studi condotti nell ultimo decennio, hanno permesso di 4
3 stabilire la struttura a livello molecolare delle fibrille amiloidi, i cambiamenti strutturali cui vanno incontro le proteine e i peptidi che le costituiscono e i fattori che determinano tali cambiamenti. Ciò ha permesso di gettare le basi per possibili approcci terapeutici delle patologie connesse alla formazione di fibrille (M. Stefani 2004). Alla base del fenomeno di aggregazione, spesso, c è un evoluzione delle proteine, da una forma monomerica ad una oligomerica, che può presentare diversi vantaggi rispetto al relativo monomero, quali: la possibilità di un controllo allosterico dell attività enzimatica, una maggiore concentrazione locale dei siti catalitici, superfici di legame più estese, l evoluzione di nuovi siti attivi all interfaccia tra le subunità, l acquisizione di nuove proprietà biologiche (Liu e Eisenberg, 2002). 1.1 Il 3D-domain swapping Uno dei meccanismi proposti per spiegare la formazione di strutture oligomeriche a partire da forme monomeriche preesistenti, è il 3D-domain swapping (Bennet et al.,1995). Con tale termine si intende un fenomeno che prevede lo scambio reciproco di uno o più elementi strutturali ( domini ) tra subunità monomeriche identiche con conseguente formazione di un dimero o un oligomero di più alto ordine. Il dominio scambiato va ad occupare la stessa posizione e stabilisce con il resto della catena peptidica, le stesse interazioni che aveva nella forma monomerica. Il meccanismo di scambio di domini strutturali prevede la rottura delle interazioni tra i domini di una proteina monomerica strutturalmente complessa, con formazione di un monomero aperto. In questa conformazione la proteina riforma le interazioni con un dominio identico appartenente ad un altra unità monomerica con conseguente formazione di un dimero o, in generale, di un oligomero scambiante. Nella banca data di strutture di proteine, Protein Data Bank (PDB), sono state depositate oltre 110 strutture di proteine caratterizzate dal fenomeno del domain swapping e da un analisi di queste è emerso, 5
4 che non è possibile stabilire delle analogie di funzioni, dimensioni o sequenze, e ciò impedisce, nota una proteina e la sua sequenza, di stabilire a priori se questa scambierà un dominio o meno. In molti casi i domini coinvolti nello scambio sono localizzati nella regione N-terminale o C-terminale della proteina e in alcuni casi interessano entrambe le zone. Una caratteristica comune a molti oligomeri definiti scambianti, mostrata da analisi statistiche condotte sulle superfici di interazioni di dimeri scambianti (Schulunegger, et al.,1997; Sinha, et al.,2001), è la ridotta superficie di interazione, legata alla specifica struttura quaternaria. Ciò determina la possibilità di ampi moti intersubunità inusuali, se confrontati a quelli di dimeri convenzionali, che permettono l accesso a molteplici strutture quaternarie e quindi favoriscono la crescita dell aggregato (Merlino, et al.,2005). Per tali ragioni questo meccanismo, consentendo un certo grado di adattabilità della superficie oligomerica, può giocare un ruolo rilevante nei meccanismi di riconoscimento molecolare, che si verificano durante i fenomeni di aggregazione di proteine, compresi quelli di tipo patologico. In tutte le proteine che presentano scambio di domini strutturali, possono essere individuate tre regioni caratteristiche: l interfaccia chiusa ( interfaccia-c), che è costituita dalle regioni di contatto tra il dominio scambiato e il resto della catena polipeptidica ed è identica nella proteina monomerica e in quella oligomerica; l interfaccia aperta (interfaccia-o), che è rappresentata dalla regione di interazione che si viene a creare tra le subunità proteiche in seguito al fenomeno di scambio; essa è quindi presente nell oligomero scambiante ma non nel monomero; il peptide cerniera (hinge peptide), che è il segmento di catena peptidica che connette il dominio scambiato al corpo principale della proteina e che adotta conformazioni diverse nella proteina monomerica e oligomerica (Mazzarella, et al., 1993). Figura 1.1: 6
5 Figura 1.1: Illustrazione schematica della formazione di un dimero mediante 3D-domain swapping. L interfaccia chiusa determina nella massima parte la stabilità dell aggregato, mentre l interfaccia aperta e il peptide cerniera, sono importanti nel determinare la specifica struttura quaternaria dell oligomero. Studi energetici condotti sulla tossina della difterite (DT) una proteina monomerica secreta dal Corynebacterium difteriae che, in seguito a un trattamento di congelamento e scongelamento in tampone fosfato a ph neutro, forma un dimero scambiante (Bennet, et al., 1994-A) e indagini su altri sistemi scambianti (Chen, et al., 2005) hanno consentito di stimare la variazione di energia libera standard che si verifica durante il processo di scambio (Bennet, et al., 1994-B). Una caratteristica generale del fenomeno è che la forma monomerica e quella oligomerica scambiante della proteina, mostrano una piccola differenza di energia libera e sono separate da un alta barriera energetica. L energia paragonabile deriva dal fatto che, il dominio scambiato, ha un intorno proteico essenzialmente identico nel monomero in conformazione chiusa e nell oligomero scambiante e stabilisce identici legami non covalenti con i restanti domini della proteina in entrambe le forme, cosicchè l oligomero è stabilizzato dalle stesse interazioni che tengono insieme i diversi domini della proteina monomerica. La piccola differenza di energia libera tra il monomero e 7
6 la corrispondente forma dimerica è un indice della stabilità relativa della forma scambiante ed è influenzata da tre fattori: 1) la maggiore entropia dei monomeri rispetto all oligomero; 2) le nuove interazioni che il peptide cerniera sperimenta nel passare dalla forma monomerica a quella scambiante; 3) la formazione di un ulteriore interfaccia nell oligomero scambiante che non è presente nel monomero (l interfaccia aperta). L alta barriera che separa il monomero dall oligomero scambiante, può essere considerata l energia di attivazione del processo di oligomerizzazione tramite domain swapping ed è dovuta alla necessità di passare durante il fenomeno di scambio, attraverso uno stato di transizione, che è il monomero aperto. L energia di attivazione dello scambio, può essere ridotta da numerosi eventi molecolari e ambientali. In generale, transienti condizioni parzialmente denaturanti, destabilizzano il monomero in conformazione chiusa e, quindi, favoriscono lo scambio di domini tra subunità. Mutazioni, variazioni di ph o di temperatura, aumento della concentrazione proteica, interazioni con recettori o ligandi sono fattori in grado di influenzare la velocità di interconversione tra i diversi stati aggregati. In vivo queste condizioni si possono verificare come conseguenza di stati patologici o in seguito al passaggio di una proteina in tessuti o in compartimenti cellulari specializzati. Lo scambio potrebbe avvenire anche durante un processo di strutturazione (folding) di una proteina, se si accumulano intermedi che hanno domini strutturati ma non associati, ossia se l associazione dei domini strutturati è lenta rispetto al folding degli stessi. Il domino scambiato può consistere in un singolo elemento di struttura secondaria (un α-elica o un β-strand o un β- sheet) oppure di un intero domino globulare costituito da centinaia di residui (Schlunegger, et al., 1997). Ciò chiarisce perchè non si può prevedere se una proteina può dare o meno luogo al fenomeno dell interscambio dei domini, sulla sola base della sequenza amminoacidica che 8
7 la costituisce (Liu e Eisenberg, 2002). L unico requisito necessario è che la proteina contenga un segmento di catena polipeptidica che possa fungere da peptide cerniera: esso deve avere la lunghezza opportuna e la flessibilità intrinseca per poter adottare differenti conformazioni nella forma chiusa del monomero e in quella scambiante. Un esame dei peptidi cerniera di un gran numero di strutture proteiche scambianti, ha evidenziato che essi mostrano una varietà di lunghezze, di sequenze e di strutture secondarie, anche se è abbastanza frequente la presenza di residui di prolina e/o glicina rispetto ad altri residui (Schlunegger, et al., 1997). Entrambi sono residui con caratteristiche peculiari: la glicina è l amminoacido con la maggiore libertà conformazionale, la sua presenza potrebbe conferire al peptide cerniera la flessibilità necessaria per fargli adottare conformazioni alternative nel monomero e nell oligomero scambiante; la prolina invece, avendo la catena laterale legata covalentemente all azoto del gruppo peptidico, presenta un numero limitato di conformazioni accessibili e riduce lo spazio conformazionale dell amminoacido che lo precede. Tali vincoli tendono generalmente ad introdurre una maggiore tensione nella forma monomerica rispetto a quella dimerica, favorendo l oligomerizzazione. L effetto di mutazioni, delezioni o allungamenti sullo scambio di domini strutturali varia al variare del sistema proteico esaminato. 1.2 Le ribonucleasi come sistema modello Un sistema modello ideale per lo studio dello scambio dei domini strutturali, è rappresentato dalla famiglia delle ribonucleasi di tipo pancreatico (Raines, 1998) sia per la contemporanea presenza del prototipo monomerico, la ribonucleasi bovina pancreatica (RNasi A), e della controparte dimerica naturale, la ribonucleasi seminale bovina (BS-RNasi) (Mazzarella, et al., 1993), sia per la tendenza di molti suoi membri a generare oligomeri scambianti in condizioni 9
8 blandamente denaturanti. Le ribonucleasi di tipo pancreatico sono endoribonucleasi specifiche per substrati che presentano una base pirimidinica in posizione 3 del legame fosfodiestereo che viene idrolizzato (Raines, 1998). La reazione di degradazione dell acido ribonucleico (RNA) procede con un meccanismo a due stadi. Il primo stadio della reazione è una trans fosforilazione con formazione di un monofosfato ciclico 2-3, che rappresenta il substrato della successiva reazione di idrolisi in cui viene rilasciato il nucleotide 3 -monofosfato. Il substrato è, generalmente, RNA a singola elica (Usher, et al., 1972), ma alcuni membri della famiglia (ribonucleasi bovina seminale, ribonucleasi pancreatica umana) sono in grado di esercitare la loro azione catalitica anche su doppie eliche di RNA e su catene di acido ribonucleico in ibridi DNA-RNA (Libonati and Floridi 1969; D Alessio, et al., 1972; D Alessio, et al., 1974). Il meccanismo catalitico della degradazione dell RNA prevede il coinvolgimento di due residui di istidina (His12 e His119) e di un residuo di lisina (Lys41), che costituiscono la triade catalitica del sito attivo, localizzato tra i due lobi della tipica struttura a forma di V di questa classe di enzimi. Il prototipo monomerico della famiglia delle ribonucleasi di tipo pancreatico è la ribonucleasi pancreatica bovina (RNasi A), un enzima a lungo utilizzato come sistema modello per lo studio di aspetti funzionali e strutturali delle proteine (Blackburn, et al., 1982; Raines 1998). L RNasi A è una piccola proteina compatta di 124 residui amminoacidici, per cui non è nota alcuna funzione oltre quella di degradare l RNA (Raines, 1998). La stabilità della proteina è assicurata da quattro ponti disolfurici intracatena (Kartha, et al., 1967), mentre per il corretto ripiegamento della macromolecola sono fondamentali quattro residui di prolina, due dei quali, Pro93 e Pro114, hanno i corrispondenti legami peptidici in conformazione cis. La RNasi A è stata la prima proteina che ha mostrato, in condizioni blandamente denaturanti, la tendenza a generare diverse forme oligomeriche tramite il fenomeno dello scambio di elementi strutturali (Crestfield, et al.,1965). Nel 1962 si scoprì che l enzima, per liofilizzazione da soluzioni di acido acetico al 40%, formava, con una resa del 30% circa, due dimeri, stabilizzati dallo 10
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Modello per la struttura (presunta) di un RNA viroide: le lineette interne indicano i legami tra le basi complementari
 Viroidi Agenti infettivi costituiti da una sola molecola di RNA circolare a singolo filamento (+ o -), ripiegato a formare regioni a doppia elica, prive di capside, sensibili a RNasi Aree a doppia elica
Viroidi Agenti infettivi costituiti da una sola molecola di RNA circolare a singolo filamento (+ o -), ripiegato a formare regioni a doppia elica, prive di capside, sensibili a RNasi Aree a doppia elica
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
STRUTTURAZIONE DELLE PROTEINE
 STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le Biomolecole II parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA
 LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA LE PROTEINE CON STRUTTURA NON NATIVA VENGONO DEGRADATE ATTRAVERSO LA VIA UBIQUITINA- PROTEASOMA IL CONTROLLO DI QUALITA GARANTISCE
LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA LE PROTEINE CON STRUTTURA NON NATIVA VENGONO DEGRADATE ATTRAVERSO LA VIA UBIQUITINA- PROTEASOMA IL CONTROLLO DI QUALITA GARANTISCE
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Macromolecole Biologiche. La struttura secondaria (III)
 La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
RUOLI BIOLOGICI DELLE PROTEINE. Biochimica
 RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008. Eloise Mastrangelo
 Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Ruolo dello ione Cu II nell aggregazione dell Ubiquitina: implicazioni per le malattie neurodegenerative. Vincenza CALO
 GIORNATA PUGLIESE su FARMACO e PRODOTTI per la SALUTE II EDIZIONE Il farmaco per le diagnosi precoci e malattie rare Ruolo dello ione Cu II nell aggregazione dell Ubiquitina: implicazioni per le malattie
GIORNATA PUGLIESE su FARMACO e PRODOTTI per la SALUTE II EDIZIONE Il farmaco per le diagnosi precoci e malattie rare Ruolo dello ione Cu II nell aggregazione dell Ubiquitina: implicazioni per le malattie
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI
 Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
La struttura delle proteine e e descritta da quattro livelli di organizzazione
 La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Formazione delle strutture amiloidi_1
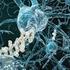 Formazione delle strutture amiloidi_1 Gli aggregati possono essere amorfi AMILOIDOGENESI Formazione delle strutture amiloidi_2 Gli aggregati possono essere strutturati monomero dimero monomero oligomero
Formazione delle strutture amiloidi_1 Gli aggregati possono essere amorfi AMILOIDOGENESI Formazione delle strutture amiloidi_2 Gli aggregati possono essere strutturati monomero dimero monomero oligomero
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 5
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Capitolo 1. Le proteine. 1.1 La struttura delle proteine
 Capitolo 1 Le proteine 1.1 La struttura delle proteine Le proteine sono le macromolecole più versatili dei sistemi viventi e hanno un ruolo fondamentale in tutti i processi biologici. Le proteine possono
Capitolo 1 Le proteine 1.1 La struttura delle proteine Le proteine sono le macromolecole più versatili dei sistemi viventi e hanno un ruolo fondamentale in tutti i processi biologici. Le proteine possono
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei.
 DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Il legame peptidico è polare
 Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
Scaricato da Il legame peptidico è polare SONO FAVORITE QUELLE CONFIGURAZIONI CHE CONSENTONO IL MAGGIOR NUMERO DI INTERAZIONI TRA LE PARTI DELLA CATENA POLIPEPTIDICA. A CAUSA DELLA POLARITA' DEL LEGAME
LEZIONE DEL 27/03/2017
 LEZIONE DEL 27/03/2017 Struttura primaria sequenze amminoacidiche --> ponti disolfuro; Strutture secondarie (stabilizzate dai legami idrogeno intercatena): dipendono dal legame peptidico; Strutture terziarie
LEZIONE DEL 27/03/2017 Struttura primaria sequenze amminoacidiche --> ponti disolfuro; Strutture secondarie (stabilizzate dai legami idrogeno intercatena): dipendono dal legame peptidico; Strutture terziarie
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA
 LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA LE PROTEINE CON STRUTTURA NON NATIVA VENGONO DEGRADATE ATTRAVERSO LA VIA UBIQUITINA- PROTEASOMA IL CONTROLLO DI QUALITA GARANTISCE
LE PROTEINE SINTETIZZATE VENGONO SOTTOPOSTE AD UN CONTROLLO DI QUALITA LE PROTEINE CON STRUTTURA NON NATIVA VENGONO DEGRADATE ATTRAVERSO LA VIA UBIQUITINA- PROTEASOMA IL CONTROLLO DI QUALITA GARANTISCE
Fondamentali in ogni organismo, hanno molteplici ruoli:
 Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
MUSCOLO. Muscolo striato scheletrico. FGE aa
 MUSCOLO Muscolo striato scheletrico FGE aa.2015-16 Tipi di muscoli Muscolo scheletrico Muscolo liscio Muscolo cardiaco Tipi di muscoli Muscolo scheletrico Muscolo liscio Muscolo cardiaco Tipi di muscoli
MUSCOLO Muscolo striato scheletrico FGE aa.2015-16 Tipi di muscoli Muscolo scheletrico Muscolo liscio Muscolo cardiaco Tipi di muscoli Muscolo scheletrico Muscolo liscio Muscolo cardiaco Tipi di muscoli
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Complesso Maggiore di Istocompatibilita (MHC)
 Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
Acidi Nucleici: DNA = acido deossiribonucleico
 Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
UNIVERSITÀ DI PISA. Facoltà di Farmacia. Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche
 UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
