Capitolo 1. Le proteine. 1.1 La struttura delle proteine
|
|
|
- Gina Franchi
- 6 anni fa
- Visualizzazioni
Transcript
1 Capitolo 1 Le proteine 1.1 La struttura delle proteine Le proteine sono le macromolecole più versatili dei sistemi viventi e hanno un ruolo fondamentale in tutti i processi biologici. Le proteine possono agire da catalizzatori, trasportare o conservare altre molecole come l ossigeno, fornire un supporto meccanico o una protezione immunitaria, generare un movimento, trasmettere impulsi nervosi e controllare la crescita e il differenziamento. Le proteine sono polimeri lineari costituiti da unità monomeriche dette amminoacidi, legati tra di loro attraverso un legame covalente, che prende il nome di legame peptidico, per questo le proteine sono note come polipeptidi. Figura 1.1: Struttura generica di un amminoacido 2
2 1.1 La struttura delle proteine Un α-amminoacido (Fig.1.1) è costituito da un atomo di carbonio centrale, detto carbonio α (C α ) a cui sono legati un gruppo amminico, un gruppo carbossilico, un atomo di idrogeno e un gruppo R, spesso indicato con il nome di catena laterale, specifico per ognuno di essi. Gli α-amminoacidi sono molecole chirali. Le due forme, che sono immagini speculari l una dell altra, sono dette isomero L e isomero D. Le proteine sintetizzate dagli organismi viventi sono costituite quasi esclusivamente dagli isomeri L. Gli amminoacidi in soluzione a ph neutro sono ioni dipolari o zwitterioni. Nella forma dipolare il gruppo amminico di un amminoacido è protonato -NH + 3 e il gruppo carbossilico è dissociato -COO. amminoacido varia con il ph. Lo stato di ionizzazione di un Nelle proteine sono presenti 20 tipi di catene laterali che variano per dimensioni, carica, capacità di formare legami idrogeno e reattività chimica. Tutte le proteine in tutte le specie - batteri, archeobatteri ed eucarioti - vengono costruite a partire dagli stessi 20 amminoacidi [1]. Le catene laterali degli amminoacidi hanno differenti tendenze a partecipare alle interazioni l una con l altra e con l acqua. Queste differenze influenzano profondamente i loro contributi alla stabilità e alle funzioni delle proteine. Gli amminoacidi idrofobici (fondo rosa in Fig.1.2) tendono ad evitare il contatto con l acqua, e sono coinvolti solo in legami di Van der Waals. Vedremo in seguito come questo effetto sia fondamentale in un processo che porta il nome di folding. Gli amminoacidi idrofilici (fondo azzurro in Fig.1.2) sono capaci di legarsi tra loro, allo scheletro peptidico, alle molecole polari organiche e all acqua, attraverso la formazione di legami idrogeno. Questa tendenza domina le interazioni alle quali partecipano. Alcuni di questi possono cambiare il loro stato di carica a seconda del ph o del microambiente da cui sono circondati. 3
3 Le proteine Figura 1.2: Struttura e caratteristiche chimiche delle catene laterali degli amminoacidi 4
4 1.1 La struttura delle proteine Gli amminoacidi anfipatici (fondo viola in Fig.1.2) possono essere sia idrofobici sia idrofilici a seconda delle condizioni del microambiente in cui si trovano. Questa loro caratteristica è ideale per la formazione delle interfacce [2]. Nella Fig.1.2 manca l amminoacido con la struttura più semplice, la glicina (Gly, G), la cui catena laterale è formata esclusivamente da un atomo di idrogeno. Nella Fig.1.2 sono indicati in grigio chiaro gli atomi di idrogeno, in grigio scuro gli atomi di carbonio, in rosso gli atomi di ossigeno, in giallo gli atomi di zolfo, e infine in azzurro gli atomi di azoto. Le proteine sono formate dall unione del gruppo carbossilico di un amminoacido con il gruppo amminico dell amminoacido successivo attraverso un legame covalente, che prende il nome di legame peptidico [3]. Nella Fig.1.3 è Figura 1.3: Formazione del legame peptidico e idrolisi mostrata la formazione di un dipeptide a partire da due amminoacidi con rilascio di una molecola d acqua. L equilibrio di questa reazione è spostato verso l idrolisi piuttosto che verso la sintesi, perciò la biosintesi dei legami peptidici richiede l immissione di energia libera. Tuttavia i legami peptidici sono cinetica- 5
5 Le proteine mente stabili: in assenza di eventi di catalisi l emivita di un legame peptidico in soluzione acquosa è di circa 1000 anni. Il legame peptidico ha caratteristiche di parziale doppio legame, che impediscono la rotazione intorno ad esso. L impossibilità di ruotare del legame ne determina la planarità e restringe le conformazioni possibili dello scheletro covalente. Al contrario i legami tra l atomo di C α e il carbonio carbonilico (C ), e tra il C α e l atomo di azoto del gruppo amminico sono legami semplici. Di conseguenza due unità peptidiche rigide adiacenti possono avere un certo grado di libertà di rotazione intorno a questi legami. La libertà di rotazione su ciascun lato dell unità peptidica permette alle proteine di ripiegarsi in modi diversi. Le rotazioni di questi legami sono definite da angoli diedrici o torsionali. Nella Fig.1.4 sono mostrati questi angoli e i piani che li definiscono [4]. L angolo di rotazione intorno al legame tra l azoto e l atomo C α è detto φ, mentre quello tra il C α e l atomo C è detto ψ. Non tutte le combinazioni di φ e ψ sono possibili. Ramachandran [5] osservò Figura 1.4: Catena polipeptidica estesa in cui sono mostrate le tipiche lunghezze di legame, gli angoli di legame e i diedri 6
6 1.1 La struttura delle proteine che molte combinazioni sono proibite a causa di impedimenti sterici tra gli atomi. I valori permessi possono essere visualizzati attraverso un grafico bidimensionale detto appunto grafico di Ramachandran. Nella Fig.1.5 è mostrato un grafico di Ramachandran in cui con il colore rosso indichiamo quelle combinazioni degli angoli torsionali che sono permesse, nelle quali cioè non ci sono impedimenti sterici, con il rosa le regioni permesse solo se alcuni impedimenti sterici sono rilassati. Come si vede dal grafico, circa tre quarti delle possibili combinazioni tra gli angoli torsionali vengono escluse da impedimenti sterici. Figura 1.5: Plot di Ramachandran Nella struttura di una proteina si distinguono quattro livelli di organizzazione. La struttura primaria della proteina è rappresentata dalla sequenza dei suoi amminoacidi, che a sua volta determina i vari modi in cui essa può ripiegarsi nelle strutture di livello superiore. La struttura secondaria rappresenta la struttura tridimensionale locale di una proteina, in cui possono essere presenti tratti di catena polipeptidica che formano α-eliche e foglietti β (β-sheet). L α-elica è una struttura a forma di bastoncino, la cui parte interna è formata dalla catena principale polipeptidica strettamente avvolta; le catene laterali si estendono verso l esterno con un andamento a spirale. L α-elica è stabilizzata da legami idrogeno tra gruppi N-H e C=O della catena 7
7 Le proteine principale. Il gruppo C=O di ciascun amminoacido è unito da un legame idrogeno al gruppo N-H dell amminoacido che si trova quattro residui più avanti nella sequenza lineare (Fig.1.6). Ciascun residuo è spostato rispetto al precedente di Figura 1.6: Alfa elica Figura 1.7: Foglietti β 1.5Å lungo l asse dell elica e forma con esso un angolo di 100 il che significa che vi sono 3.6 residui amminoacidici per ogni giro di elica. Il passo dell α-elica, 8
8 1.1 La struttura delle proteine che corrisponde al prodotto dello spostamento (1.5Å) per il numero di residui per giro (3.6Å), è di 5.4Å. Le α-eliche sono una struttura compatta [6], con valori approssimativi degli angoli φ e ψ di -60 e -50 rispettivamente (vedi Fig.1.5). Il foglietto β ha una struttura diversa da quella a bastoncello dell α-elica. Una catena polipeptidica a foglietto β è quasi completamente estesa invece di essere strettamente avvolta e coinvolge legami idrogeno tra gruppi N-H e C=O appartenenti a residui anche molto distanti tra loro nella sequenza lineare. Nei foglietti β, due o più strati che possono essere molto distanti nella struttura primaria sono tenuti fianco a fianco da legami idrogeno. Gli strati (Fig.1.7) possono scorrere lungo la stessa direzione, allora parleremo di foglietto β parallelo, oppure in direzioni opposte, foglietto beta antiparallelo [7]. La distanza tra due residui consecutivi è 3.3Å e gli angoli φ e ψ sono approssimativamente -130 e 125 (vedi Fig.1.5). L organizzazione tridimensionale completa di una catena poliptedica prende il nome di struttura terziaria. Vedremo nel 1.2 quali sono le interazioni che permettono ad una proteina di assumere una determinata struttura terziaria. Per buona parte delle proteine, la struttura terziaria rappresenta l ultimo livello di organizzazione strutturale. E il caso delle proteine cosiddette monomeriche, costituite cioè da un unica unità funzionale, biologicamente attiva. Molte altre proteine (ad esempio, un gran numero di enzimi), nella loro forma attiva sono invece costituite dall associazione di due o più unità di struttura terziaria (dette monomeri o subunità), uguali (proteine omo-oligomeriche) o diverse (proteine etero-oligomeriche). Si parla in tal caso di struttura quaternaria, per riferirsi all organizzazione multimerica della proteina. Nella struttura quaternaria, le subunità sono tenute insieme da interazioni generalmente non covalenti. Raramente, più catene peptidiche sono unite da legami covalenti, come accade ad esempio nelle immunoglobuline, in cui le catene leggere e pesanti sono tenute insieme da ponti disolfuro [8]. 9
9 Le proteine 1.2 Folding vs Misfolding Il folding è il processo attraverso il quale le proteine acquisiscono la loro struttura tridimensionale. Il folding può aver luogo sia contemporaneamente alla sintesi proteica sia dopo che questa è stata completata. Soltanto una volta terminato il folding, le proteine sono in grado di svolgere la loro funzione fisiologica [9]. La prima teoria del folding proteico è stata proposta negli anni 20 del XX secolo dallo scienziato cinese Hsien Wu [10]. In Europa e negli Stati Uniti le prime importanti ricerche sono state quelle negli anni sessanta di Christian B. Anfinsen, il quale formulò un dogma della biologia molecolare che porta il suo nome. Il dogma afferma che, almeno per le piccole proteine globulari, la struttura nativa è determinata unicamente dalla sequenza di amminoacidi che costituiscono la proteina [11]. Come la proteina raggiunga questa struttura rientra nel campo di studio del folding proteico, che si basa su un dogma correlato chiamato paradosso di Levinthal [12]. Il paradosso di Levinthal afferma che il numero di conformazioni possibili per una data proteina è astronomicamente grande. Effettivamente, questo rende la predizione computazionale della struttura proteica tramite la valutazione di tutte le possibili configurazioni irrealizzabile persino per proteine relativamente piccole. Inoltre, alcune proteine necessitano dell assistenza di altre proteine chiamate chaperonine per realizzare un folding corretto. E stato suggerito che ciò contraddirebbe il dogma di Anfinsen. In realtà le chaperonine non sembrano avere effetto sullo stato finale della proteina, ma bensì avere il ruolo di prevenire l eventuale aggregazione delle molecole proteiche prima che la proteina abbia raggiunto la struttura di folding corretta [10]. La funzione fisiologica di una proteina, sia essa un enzima, un trasportatore, un recettore o una proteina strutturale, è condizionata dalla sua struttura terziaria. Questo è il motivo per cui il folding ha una notevole importanza ed è oggetto di 10
10 1.2 Folding vs Misfolding ricerca. La capacità delle proteine di ripiegarsi in strutture ben definite à gov- Figura 1.8: Ripiegamento proteico ernata dalle leggi della termodinamica. Consideriamo un sistema costituito da una soluzione acquosa di molecole proteiche tutte identiche (Fig.1.8) ma ripiegate in modo diverso. La conformazione nativa unica corrisponde ad un minimo dell energia libera. Durante il processo di sintesi proteica il sistema, costituito dalla proteina nascente più l ambiente circostante, è disordinato e l entropia dell insieme delle molecole è relativamente alta. In determinate condizioni il ripiegamento delle proteine può avvenire spontaneamente. Quindi l entropia del solo sistema proteico deve diminuire a scapito di un aumento dell entropia del resto dell Universo. Al processo spontaneo di folding contribuisce anche la presenza delle forze idrofobiche. In una soluzione acquosa le molecole di soluto possono interagire con le molecole d acqua attraverso la formazione di legami ionici e legami idrogeno. Nel caso di soluti non ionizzabili, che non possono dare origine a questo tipo di legami, le molecole d acqua formano loro intorno una gabbia. Lo stato delle molecole d acqua che formano la gabbia è più ordinato (a minore entropia) di quello delle molecole libere in soluzione. Quando due molecole non polari si avvicinano, alcune molecole d acqua vengono rilasciate e ritornano libere nel mezzo (Fig.1.9). Il termine entropico favorisce così l aggregazione di molecole idrofobiche. 11
11 Le proteine Figura 1.9: Effetto idrofobico Le catene laterali di alcuni amminoacidi che costituiscono le proteine sono costituite da gruppi non polari che tendono ad escludere l acqua costituendo esse stesse il mezzo idrofobico in cui risiedere. Al contrario gli amminoacidi con catene laterali polari possono tranquillamente formare legami idrogeno con l acqua. Queste proprietà fanno sì che, generalmente, la parte proteica a contatto con l acqua sia formata da amminoacidi idrofilici, mentre gli amminoacidi idrofobici rivolgono le loro catene laterali all interno. Nel processo di ripiegamento delle proteine si formano legami idrogeno. La variazione di energia libera, data da G = H T S, è una misura della spontaneita della reazione. Quando si ha una variazione di energia libera negativa dovuta alla combinazione delle variazioni di entropia associata agli effetti idrofobici e di entalpia associata alla formazione di legami, il processo di ripiegamento proteico può avvenire spontaneamente [1]. L ipotesi di Anfinsen è legata all assunzione che lo stato nativo di una proteina rappresenta un minimo assoluto dell energia libera. Il minimo può essere raggiunto percorrendo strade diverse e passando attraverso stati intermedi metastabili. Questo schema è rappresentato in Fig.1.10 dove la struttura nativa di una proteina è localizzata in un minimo assoluto dell energia libera. Può accadere però che, nel corso del processo di folding, lo stato della proteina corrisponda ad un minimo locale, vicino sia energeticamente che strutturalmente a quello assoluto separati attraverso una barriera di potenziale. Questo è quello che accade 12
12 1.2 Folding vs Misfolding Figura 1.10: Andamento dell energia libera ad alcune proteine che, probabilmente a causa di fattori esterni, modificano la propria struttura tridimensionale in maniera tale da essere in un minimo locale dell energia libera che si trova nelle vicinanze del minimo globale, ma con una struttura tridimensionale (misfolded) non più in grado si svolgere la propria funzione. Naturalmente la struttura primaria della proteina non si modifica durante questa trasformazione [13]. Il non corretto folding proteico è all origine di una grande varieta di patologie raggruppate sotto il nome di Protein Conformational Diseases (PCD) [14]. Questo gruppo di patologie include il morbo di Alzheimer (AD), l encefalopatia spongiforme trasmissibile, il morbo di Huntington, il morbo di Parkinson, il diabete di tipo 2, l amiloidosi da dialisi, la sclerosi amiotrofica laterale, e più di 15 altre, meno note, patologie. Notiamo che non c è omologia tra la sequenza primaria delle proteine coinvolte nelle diverse PCD. Nella maggioranza dei casi nella proteina misfolded la struttura secondaria è prevalentemente β [15] (Fig.1.11). Con questa struttura possono formarsi legami idrogeno tra amminoacidi appartenenti alla stessa molecola proteica o a molecole diverse favorendo, in quest ultimo caso, i processi di oligomerizzazione e di aggregazione. In molte PCD sono infatti presenti aggregati che depositandosi nei 13
13 Le proteine Figura 1.11: Cambiamenti conformazionali di una proteina tessuti di diversi organi li danneggiano. La presenza di depositi amiloidi è spesso usata per la diagnosi di queste malattie, che sono pertanto note anche come amiloidosi [16]. Non è chiaro tuttavia se i depositi proteici siano la causa delle PCD o se ne siano soltanto un epifenomeno. Dal punto di vista microscopico, il processo dettagliato attraverso il quale proteine solubili subiscono un parziale svolgimento (unfolding) e un riavvolgimento scorretto (misfolding) costituisce la principale e irrisolta questione. Sono state avanzate tre differenti ipotesi per descrivere le relazioni tra stati conformazionali e aggregazione. Nella ipotesi cosiddetta della polimerizzazione (Fig.1.12A), l aggregazione induce cambiamenti nella conformazione proteica; nell ipotesi conformazionale (Fig.1.12B) il misfolding proteico è considerato indipendente dall aggregazione, e questa non rappresenta necessariamente il punto d arrivo del cambiamento conformazionale; il terzo modello, detto di conformazione/oligomerizzazione (Fig.1.12C), rappresenta una visione intermedia, nella quale piccoli cambiamenti conformazionali innescano l oligomerizzazione che è essenziale per la stabilizzazione del misfolding proteico. Una questione centrale nella ipotesi con- 14
14 1.3 Ruolo biologico dei metalli Figura 1.12: Ipotesi di aggregazione formazionale è l identificazione dei fattori che inducono il misfolding. Alcune variazioni delle condizioni ambientali, fra le quali il ph, la presenza di ioni metallici [17], l influenza di certe proteine e l interazione con membrane cellulari, o semplicemente un aumento della concentrazione della proteina stessa, sono state individuate come fattori determinanti per questo processo. La comprensione dei meccanismi molecolari che sono alla base dei processi di aggregazione è un passo indispensabile per una terapia efficace delle patologie che ne derivano. 1.3 Ruolo biologico dei metalli Gli ioni metallici svolgono funzioni fondamentali all interno degli organismi viventi. La maggior parte di essi viene utilizzata come cofattore da parte delle 15
15 Le proteine proteine, che li inglobano all interno della loro struttura. I tre metalli sui quali vogliamo concentrare la nostra attenzione sono il Fe, il Cu e lo Zn. I principali amminoacidi che li coordinano, tramite un legame di tipo dativo, sono: l istidina, la metionina, la cisteina, la selenocisteina 1, e talvolta anche la tirosina, l acido aspartico e l acido glutammico. Gli ioni metallici appartenenti al cosidetto gruppo d partecipano ai processi catalitici essenzialmente in tre modi: orientano il substrato nel sito catalitico; stabilizzano elettrostaticamente e/o proteggono le cariche negative; partecipano a reazioni redox. Quest ultimo processo è particolarmente pericoloso per l organismo, infatti se la reazione avviene senza controlli esterni possono generarsi delle molecole altamente reagenti, che prendono il nome di radicali liberi, in grado di alterare lo stato d ossidazione delle cellule. Per questo motivo gli ioni metallici non vengono mai lasciati liberi di circolare nell organismo, ma sono sempre legati a proteine di trasporto che hanno il compito di trasportarli e depositarli nel luogo in cui devono partecipare ai processi in cui sono coinvolti. Lo ione Fe è il metallo di transizione più abbondante negli esseri umani, la quantità media in un uomo adulto del peso di 70kg è di circa 4g. Viene digerito a livello del duodeno, dove subisce varie reazioni di ossidazione e riduzione per poter essere assorbito e poi immagazzinato dall organismo. Nel nostro organismo lo ione Fe si trova principalmente in due stati redox Fe 2+ e Fe 3+. Generalmente tetracoordinato, lo si può trovare anche con numeri 1 La selenocisteina (Sec) è il 21 amminoacido conosciuto e il suo nome è associato al fatto che contiene un atomo di Se. Esso non è un derivato della cisteina, ma deriva dalla serina. È codificato dal codone UGA, normalmente un codone di stop, che tuttavia in presenza di un particolare segmento di mrna viene interpretato come elemento costitutivo. 16
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
Macromolecole Biologiche Interazioni non covalenti
 Interazioni non covalenti D H A δ - δ + δ - Le interazioni non covalenti Interazioni fra atomi che non sono legati da legami covalenti. Le interazioni non covalenti sono molto meno intense rispetto alle
Interazioni non covalenti D H A δ - δ + δ - Le interazioni non covalenti Interazioni fra atomi che non sono legati da legami covalenti. Le interazioni non covalenti sono molto meno intense rispetto alle
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
Le interazioni deboli:
 Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
1. Le biomolecole: Struttura e funzione delle proteine
 1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica. legami tra molecole più stabili
 I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
I legami fra molecole nei liquidi non sono forti ed esse possono fluire Riducendo l agitazione termica legami tra molecole più stabili formazione una massa rigida Una disposizione ordinata delle molecole
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
FUNZIONI DELLE PROTEINE
 FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
L'energia media V di interazione fra uno ione avente carica q e un dipolo permanente ad una distanza r Ä
 Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
MEMBRANE. struttura: fosfolipidi e proteine
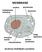 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 6
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
BIOMOLECOLE STRUTTURA E FUNZIONE
 BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
La quantità chimica LA MOLE
 La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
SCUOLA PRIMARIA DI MAGGIATE Classe terza
 SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
SCUOLA PRIMARIA DI MAGGIATE Classe terza Anno scolastico 2012-2013 TERRE ACQUE Osservando il nostro pianeta possiamo notare che la maggior parte della superficie è occupata dalle acque. Infatti esse occupano
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Legame Chimico. Legame Chimico
 Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Mutazioni genetiche 2
 Mutazioni genetiche 2 Cosa sono le mutazioni? Le proteine sono in grado di svolgere la loro funzione solo se la loro sequenza amminoacidica è quella corretta. In caso contrario si possono generare delle
Mutazioni genetiche 2 Cosa sono le mutazioni? Le proteine sono in grado di svolgere la loro funzione solo se la loro sequenza amminoacidica è quella corretta. In caso contrario si possono generare delle
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
I MEDIATORI CHIMICI DELLA FLOGOSI
 I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
UNITA DIDATTICA P A1.01
 Titolo: Grandezze fisiche fondamentali e derivate, unità di misura. Conversioni di unità di misura e notazione scientifica. Codice: A1-P-Tec-Gra Campo di indagine della chimica. Il Sistema Internazionale
Titolo: Grandezze fisiche fondamentali e derivate, unità di misura. Conversioni di unità di misura e notazione scientifica. Codice: A1-P-Tec-Gra Campo di indagine della chimica. Il Sistema Internazionale
I lipidi. Semplici Complessi
 Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
PROGRAMMA DISCIPLINARE SVOLTO a. s / N.B. il programma è pubblico ad uso degli studenti e delle famiglie.
 Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Chimica. La Chimica è la scienza che cerca di comprendere il comportamento della materia studiando il comportamento di atomi e molecole
 Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO. Fig. 4
 CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO Fig. 4 1 E PERCE BANDE E NON RIGE? E 3 Nell pratica : E 2 E 1 E 0 4000 600 cm -1 4000 600 cm -1 Tra 2 livelli vibrazionali puliti Sottolivelli rotazionali 2
CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO Fig. 4 1 E PERCE BANDE E NON RIGE? E 3 Nell pratica : E 2 E 1 E 0 4000 600 cm -1 4000 600 cm -1 Tra 2 livelli vibrazionali puliti Sottolivelli rotazionali 2
Introduzione alle macchine a stati (non definitivo)
 Introduzione alle macchine a stati (non definitivo) - Introduzione Il modo migliore per affrontare un problema di automazione industriale (anche non particolarmente complesso) consiste nel dividerlo in
Introduzione alle macchine a stati (non definitivo) - Introduzione Il modo migliore per affrontare un problema di automazione industriale (anche non particolarmente complesso) consiste nel dividerlo in
PROGRAMMA EFFETTIVAMENTE SVOLTO DAL DOCENTE
 Ministero dell istruzione, dell università e della ricerca Istituto d Istruzione Superiore Severi-Correnti IIS Severi-Correnti 02-318112/1 via Alcuino 4-20149 Milano 02-33100578 codice fiscale 97504620150
Ministero dell istruzione, dell università e della ricerca Istituto d Istruzione Superiore Severi-Correnti IIS Severi-Correnti 02-318112/1 via Alcuino 4-20149 Milano 02-33100578 codice fiscale 97504620150
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni
 5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
Roberta Pierattelli. Metalli in Biologia. Qualche richiamo di chimica generale e inorganica
 Roberta Pierattelli Metalli in Biologia Qualche richiamo di chimica generale e inorganica Le proprietà periodiche n =1 n =2 n =3 n =4 n =5 n =6 n =7 Il numero del gruppo corrisponde alla somma degli elettroni
Roberta Pierattelli Metalli in Biologia Qualche richiamo di chimica generale e inorganica Le proprietà periodiche n =1 n =2 n =3 n =4 n =5 n =6 n =7 Il numero del gruppo corrisponde alla somma degli elettroni
La corrente alternata
 La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Il DNA conserva l informazione genetica
 Il DNA conserva l informazione genetica Gli esperimenti di Frederick Griffith (1928) Gli esperimenti di Oswald Avery (1944) + Estratti dal ceppo IIIS ucciso al calore di Polisaccaridi Lipidi Proteine Acidi
Il DNA conserva l informazione genetica Gli esperimenti di Frederick Griffith (1928) Gli esperimenti di Oswald Avery (1944) + Estratti dal ceppo IIIS ucciso al calore di Polisaccaridi Lipidi Proteine Acidi
Membri dell universo microbico
 Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
Chimica. Lezione 2 Il legame chimico Parte I
 Chimica Lezione 2 Il legame chimico Parte I GLI ATOMI TENDONO A LEGARSI SPONTANEAMENTE FRA DI LORO, PER FORMARE DELLE MOLECOLE, OGNI QUALVOLTA QUESTO PROCESSO PERMETTE LORO DI RAGGIUNGERE UNA CONDIZIONE
Chimica Lezione 2 Il legame chimico Parte I GLI ATOMI TENDONO A LEGARSI SPONTANEAMENTE FRA DI LORO, PER FORMARE DELLE MOLECOLE, OGNI QUALVOLTA QUESTO PROCESSO PERMETTE LORO DI RAGGIUNGERE UNA CONDIZIONE
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
DISEGNO PROSPETTICO CAPITOLO 1 METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE PROIEZIONI ORTOGRAFICHE PROIEZIONI ASSONOMETRICHE
 CAPITOLO DISEGNO PROSPETTICO METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE La norma UNI EN ISO 0209-2 raccoglie i principali metodi di rappresentazione raccomandati per il disegno
CAPITOLO DISEGNO PROSPETTICO METODI DI RAPPRESENTAZIONE PER IL DISEGNO TECNICO: QUADRO GENERALE La norma UNI EN ISO 0209-2 raccoglie i principali metodi di rappresentazione raccomandati per il disegno
Relazione sequenza-struttura e funzione
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione sequenza-struttura e funzione Marco Nardini Dipartimento
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione sequenza-struttura e funzione Marco Nardini Dipartimento
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
Tecnologie di Recupero e Riciclo dei Materiali Alberto Simboli I MATERIALI NELLA PRODUZIONE
 Tecnologie di Recupero e Riciclo dei Materiali Alberto Simboli 3. I MATERIALI NELLA PRODUZIONE 3.1. INTRODUZIONE Origine dei materiali I materiali, dal punto di vista della loro origine si possono suddividere
Tecnologie di Recupero e Riciclo dei Materiali Alberto Simboli 3. I MATERIALI NELLA PRODUZIONE 3.1. INTRODUZIONE Origine dei materiali I materiali, dal punto di vista della loro origine si possono suddividere
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
BILANCIAMENTO REAZIONE DI OSSIDO-RIDUZIONE
 http://aliceappunti.altervista.org BILANCIAMENTO REAZIONE DI OSSIDO-RIDUZIONE TESTO: Il permanganato di potassio viene aggiunto ad una soluzione acida contenente perossido di idrogeno (acqua ossigenata).
http://aliceappunti.altervista.org BILANCIAMENTO REAZIONE DI OSSIDO-RIDUZIONE TESTO: Il permanganato di potassio viene aggiunto ad una soluzione acida contenente perossido di idrogeno (acqua ossigenata).
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Chimica. 1) Il simbolo del Carbonio è: A) C B) Ca. C) Ce D) Cu. 2) Secondo il principio della conservazione della materia:
 Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri).
 Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Corso di BIOINFORMATICA Applicazioni BIO-Mediche
 Corso di BIOINFORMATICA Applicazioni BIO-Mediche - Introduzione al Molecular Docking (algoritmi di ricerca e Moderni software) Pietro BUFFA Responsabile Unità Operativa di Bioinformatica Dipartimento di
Corso di BIOINFORMATICA Applicazioni BIO-Mediche - Introduzione al Molecular Docking (algoritmi di ricerca e Moderni software) Pietro BUFFA Responsabile Unità Operativa di Bioinformatica Dipartimento di
LA CHIMICA DEI GLUCIDI
 1.1 La classificazione chimica dei glucidi LA CHIMICA DEI GLUCIDI GLUCIDI (sono comunemente chiamati zuccheri) Si dividono in: SEMPLICI Sono chiamati MONOSACCARIDI Sono formati da una sola molecola di
1.1 La classificazione chimica dei glucidi LA CHIMICA DEI GLUCIDI GLUCIDI (sono comunemente chiamati zuccheri) Si dividono in: SEMPLICI Sono chiamati MONOSACCARIDI Sono formati da una sola molecola di
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
LA FORZA...SIA CON TE!
 LA FORZA...SIA CON TE! CHE COS'E' LA FORZA? E' UNA GRANDEZZA FISICA VETTORIALE. L'UNITA' DI MISURA NEL S.I. E' IL "NEWTON" ( N ), DAL CELEBRE SCIENZIATO INGLESE ISAAC NEWTON, CHE NE HA STUDIATO LE LEGGI,
LA FORZA...SIA CON TE! CHE COS'E' LA FORZA? E' UNA GRANDEZZA FISICA VETTORIALE. L'UNITA' DI MISURA NEL S.I. E' IL "NEWTON" ( N ), DAL CELEBRE SCIENZIATO INGLESE ISAAC NEWTON, CHE NE HA STUDIATO LE LEGGI,
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
7 Cenni di ottica per la fotografia
 7 Cenni di ottica per la fotografia 7.1 Schematizzazione di un obiettivo fotografico Gli obiettivi fotografici sono generalmente composti da un numero elevato di lenti. Tuttavia per semplicità possiamo
7 Cenni di ottica per la fotografia 7.1 Schematizzazione di un obiettivo fotografico Gli obiettivi fotografici sono generalmente composti da un numero elevato di lenti. Tuttavia per semplicità possiamo
Peptidi, proteine ed e nzim i i 1
 Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA. Parte 3. Lo spazio. Prof. Gianfranco Ciaschetti
 Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA Parte 3 Lo spazio Prof. Gianfranco Ciaschetti Solitamente, per spazio intendiamo un volume in tre dimensioni di estensione illimitata. In grafica,
Progettazione Multimediale REGOLE DI COMPOSIZIONE GRAFICA Parte 3 Lo spazio Prof. Gianfranco Ciaschetti Solitamente, per spazio intendiamo un volume in tre dimensioni di estensione illimitata. In grafica,
Stato di ossidazione formale del metallo
 Stato di ossidazione formale del metallo i metalli di transizione possono dare composti in cui il metallo si trova in stato di ossidazione formale variabile, da +8, [RuO 4 ], a 4, [Cr(CO) 4 ] 4- la carica
Stato di ossidazione formale del metallo i metalli di transizione possono dare composti in cui il metallo si trova in stato di ossidazione formale variabile, da +8, [RuO 4 ], a 4, [Cr(CO) 4 ] 4- la carica
I leucociti o globuli bianchi sono cellule coinvolte nella risposta immunitaria. Grazie al loro intervento il corpo umano si difende dagli attacchi
 GLOBULI BIANCHI I leucociti sono cellule del sangue provviste di nucleo e si trovano nel circolo sanguigno, nel sistema linfatico e nei tessuti. La loro caratteristica assenza di pigmentazione gli conferisce
GLOBULI BIANCHI I leucociti sono cellule del sangue provviste di nucleo e si trovano nel circolo sanguigno, nel sistema linfatico e nei tessuti. La loro caratteristica assenza di pigmentazione gli conferisce
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Indice. Dalla sequenza alla struttura. 1.0 Visione d insieme: funzione e architettura delle proteine 2. 1.1 Gli amminoacidi 4
 Indice Prefazione XIII Protein Data Bank: una nota degli autori XIV Nota all edizione italiana XV Ringraziamenti XVI CAPITOLO 1 Dalla sequenza alla struttura 1.0 Visione d insieme: funzione e architettura
Indice Prefazione XIII Protein Data Bank: una nota degli autori XIV Nota all edizione italiana XV Ringraziamenti XVI CAPITOLO 1 Dalla sequenza alla struttura 1.0 Visione d insieme: funzione e architettura
I LIPIDI (GRASSI) Cosa sono
 I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
Rapporti tra malnutrizione e salute
 La nutrizione Rapporti tra malnutrizione e salute La nutrizione è uno dei più importanti determinanti della salute. Esiste una stretta correlazione tra alimentazione non corretta e insorgenza di numerose
La nutrizione Rapporti tra malnutrizione e salute La nutrizione è uno dei più importanti determinanti della salute. Esiste una stretta correlazione tra alimentazione non corretta e insorgenza di numerose
Chimica SM 032. Informazioni sul corso
 Chimica SM 032 Informazioni sul corso Chimica (6 CFU) Docente : Jan Kašpar e-mail: kaspar@units.it tel. 040 5583960 Ed. C11 V piano - stanza 504 home page corso: www.dsch.units.it e seguire link phone
Chimica SM 032 Informazioni sul corso Chimica (6 CFU) Docente : Jan Kašpar e-mail: kaspar@units.it tel. 040 5583960 Ed. C11 V piano - stanza 504 home page corso: www.dsch.units.it e seguire link phone
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica. Lezione del 7 Marzo 2016
 C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
