Fisica per Medicina. Lezione 25 - Ottica e Fisica Moderna. Dr. Cristiano Fontana
|
|
|
- Renato Nigro
- 6 anni fa
- Visualizzazioni
Transcript
1 Fisica per Medicina Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana Dipartimento di Fisica ed Astronomia Galileo Galilei Università degli Studi di Padova 12 dicembre 2017 Indice Onde Ottica Fisica moderna Struttura atomica Struttura nucleare 2/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
2 Lavoro e potenziale elettrostatico Abbiamo visto che il lavoro compiuto per muovere una carica in due punti di un campo elettrostatico è W = U = q V (1) Il lavoro si misura in Joule, ma quando si ha a che fare con cariche elementari (i.e. singoli elettroni) il Joule diventa poco pratico da utilizzare. Se calcoliamo il lavoro fatto su un elettrone con una differenza di potenziale di 1 V otteniamo W = e V = C 1 V = J (2) Quindi quando si accelerano cariche elementari si utilizza, per motivi di praticità, l elettronvolt che corrisponde all energia che si ottiene accelerando la carica elementare di 1 V: 1 ev = e V = C 1 V = J (3) 3/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Lenti I Distanza focale f > 0 Il principio della rifrazione è sfruttato anche nelle lenti, perché la loro forma arrotondata è in grado di deviare i fasci luminosi in modo da concentrarli. Formula delle lenti sottili Per delle lenti sottili vale la formula 1 f = 1 p + 1 q (4) ove p è la distanza di un oggetto, q è la distanza di messa a fuoco e f è la lunghezza focale della lente f < 0 4/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
3 Lenti II Distanza focale f > 0 Le lenti possono essere di diversi tipi, ma il loro comportamento dipende dalla lunghezza focale: Lenti convergenti: hanno lunghezza focale positiva, f > 0. Lenti divergenti: hanno lunghezza focale negativa, f < 0. f < 0 5/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Lenti III Lente di lunghezza focale f p f f q I raggi che sono creati da una sorgente posta in p sono concentrati in q, secondo la legge delle lenti sottili 1 f = 1 p + 1 q (5) 6/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
4 Lenti IV Orizzontale: p = q = f Lente di lunghezza focale f f f Passante per f: p = f q= Passante per il centro: nessuna deviazione Per determinare l immagine di un oggetto si intersecano diversi raggi che provengono dall oggetto stesso. 7/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Lenti V Distanza focale f > 0 È definito anche il potere diottrico di una lente come l inverso della focale D = 1 f (6) Si misura in diottrie [D] = 1 [f ] = m 1 (7) f < 0 Per un sistema di lenti, il potere risultante è la somma D = D 1 + D 2 (8) 8/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
5 Lenti VI Lente di lunghezza focale f q h θ f f θ p h' Osservando che h p lente è h = tan θ = q, vediamo che l ingrandimento M della M = h h = q p (9) 9/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Occhio Cornea Pupilla Cristallino Nervo ottico Iride Corpo ciliare Coroide Retina L occhio è molto simile ad una macchina fotografica: Cornea e cristallino: lente; corpo ciliare: messa a fuoco; pupilla ed iride: diaframma; retina: sensore di luce; coroide: strato opaco scuro per evitare riflessioni. Figura: Schema dell occhio umano [wiki]. 10/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
6 Potere dell occhio I L occhio contiene due lenti, la cornea ed il cristallino D occhio = D } cornea {{} fissa + D cristallino }{{} variabile 22 m m 1 }{{} infinito 33 m 1 }{{} vicino (10) (11) 45 m 1 55 m 1 (12) 11/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Potere dell occhio II Se p = allora f = q; quindi col potere diottrico per la messa a fuoco all infinito possiamo calcolare la dimensione interna dell occhio: d = 1 D infinito = 1 = m = 2.22 cm (13) 1 45 m e quindi calcolare la posizione di messa a fuoco più vicina p, col potere diottrico per la messa a fuoco da vicino 1 p + 1 d = D vicino (14) p = d D vicino d 1 = 0.1 m = 10 cm (15) 12/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
7 Difetti dell occhio I Occhio normale Occhio miope Occhio ipermetrope Nell occhio normale il punto di messa a fuoco è la retina, nell occhio miope il punto di messa a fuoco è anteriore alla retina, nell occhio ipermetrope o nell occhio presbite è posteriore alla retina. 13/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Difetti dell occhio II Correzioni Occhio miope D lente < 0 Occhio ipermetrope D lente > 0 Nel caso della miopia le lenti devono essere divergenti per allontanare i punti troppo vicini. Nel caso dell ipermetropia o della presbiopia le lenti devono essere convergenti. 14/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
8 La struttura dell atomo 1 fm Å = 100,000 fm L atomo è costituito da un nucleo di carica positiva ed un insieme di elettroni (carica negativa). Rispetto alla dimensione complessiva dell atomo il nucleo è molto più piccolo. Gli elettroni si distribuiscono in una nube attorno al nucleo, in delle strutture chiamati orbitali. 15/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Esperimento di Rutherford I Schema dell esperimento Nei primi anni del 900 si pensava che l atomo fosse costituito da una carica positiva distribuita in cui sono immersi gli elettroni. Con l esperimento di Rutherford si scoprì che la carica è tutta concentrata in un nucleo di dimensioni molto più piccole dell atomo. 16/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
9 Esperimento di Rutherford II Risultato per il modello di Thomson Modello di Thomson Nei primi anni del 900 si pensava che l atomo fosse costituito da una carica positiva distribuita in cui sono immersi gli elettroni. Con l esperimento di Rutherford si scoprì che la carica è tutta concentrata in un nucleo di dimensioni molto più piccole dell atomo. 17/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Esperimento di Rutherford III Risultato per il modello di Rutherford Modello di Rutherford Nei primi anni del 900 si pensava che l atomo fosse costituito da una carica positiva distribuita in cui sono immersi gli elettroni. Con l esperimento di Rutherford si scoprì che la carica è tutta concentrata in un nucleo di dimensioni molto più piccole dell atomo. 18/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
10 Esperimento di Rutherford IV Modelli a confronto Modello di Thomson Modello di Rutherford Nei primi anni del 900 si pensava che l atomo fosse costituito da una carica positiva distribuita in cui sono immersi gli elettroni. Con l esperimento di Rutherford si scoprì che la carica è tutta concentrata in un nucleo di dimensioni molto più piccole dell atomo. 19/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Livelli atomici Sperimentalmente si vede che gli atomi possono avere delle energie quantizzate. Ovvero il sistema dell atomo può liberare o assorbire solo particolari valori di energia. In prima approssimazione, i livelli energetici possibili sono descritti da E n = E RZ 2 n 2 (16) ove Z è la carica del nucleo, n è un numero naturale diverso da zero e E R è detta energia di Rydberg ed è pari a E R = e4 m e 8ɛ 2 = 13.6 ev. (17) 0h2 20/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
11 Emissione ed assorbimento Essendo l energia quantizzata le transizioni possibili hanno solo energie possibilidescritte dalla formula: In prima approssimazione, i livelli energetici possibili sono descritti da [ 1 E = E R Z 2 n1 2 1 ] n2 2 (18) E.g. La serie di Lyman è la serie di transizioni possibili con n 1 = 1, per l idrogeno: [ E Lyman n 2 =2 = E R 1 1 ] hc n2 2 = 10.2 ev λ = = 121 nm (19) E Lyman 2 che è nell ultravioletto. La serie di Balmer ha n 1 = 2 ed ha quattro linee nel visibile, la serie di Paschen ha n 1 = 3 e si trova nell infrarosso. 21/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 La struttura del nucleo Il nucleo è costituito da protoni e neutroni, che sono tenuti insieme dalla forza nucleare forte. Il numero di protoni è anche chiamato Z, il numero di neutroni N e la loro somma A è il numero di massa Z + N = A Numero di Numero di Numero di protoni neutroni massa 22/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
12 Massa del nucleo Protoni e neutroni hanno una massa circa uguale tra di loro m p = kg = 938 MeV/c 2 (20) m n = kg = 940 MeV/c 2 (21) La massa degli elettroni è molto più piccola m e = kg = MeV/c 2 (22) Essendo molto grande il rapporto tra massa dei protoni ed elettroni la massa dell atomo è circa uguale alla massa del nucleo m p m e = 938 MeV/c (23) MeV/c Le masse sono tipicamente espresse con l unità elettronvolt, che è un energia, per mezzo della legge di equivalenza tra massa ed energia E = mc 2 (24) 23/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Isotopi Gli isotopi sono dei nuclei con lo stesso numero di protoni (e quindi stesso Z ) ma diverso numero di neutroni. 1. Chimicamente si comportano tutti allo stesso modo (a parte rari casi). 2. Dal punto di vista nucleare però sono molto diversi tra di loro. E.g. gli isotopi del potassio 39 K: è stabile, ha un abbondaza del 93%; 40 K: è una sorgente radioattiva naturale perché è instabile, ha un abbondanza del 0.012%; 41 K: è stabile, ha un abbondaza del 7%. 24/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
13 Tavola dei nuclei I... 5 Be 5 Be 5 Be 5 Be 9 Be 10 Be 11 Be 12 Be 13 Be 14 Be Z=3 4 Li 5 Li 6 Li 7 Li 8 Li 9 Li 10 Li 11 Li Z=2 Z=1 Z=0 3 He 4 He 5 He 6 He 7 He 8 He 9 He 1 H 2 H 3 H 4 H 5 H 6 H 1 n 10 He N=0 N=1 N=2 N=3 N=4 N=5... Figura: Ingrandimento della tavola dei nuclei [IAEA NDS] In analogia alla tavola periodica degli elementi si definisce una tavola dei nuclei, che sono disposti secondo i numeri Z ed N. In questa rappresentazione i nuclei stabili sono disegnati in nero, gli altri colori rappresentano la vita media. 25/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Tavola dei nuclei II N=Z Z N Vite medie Figura: Tavola dei nuclei [IAEA NDS] I nuclei stabili si raggruppano lungo la cosiddetta valle di stabilità; più ci si allontana e minore diventa la vita media. I nuclei stabili sono al di sotto della retta Z = N ovvero hanno il numero N superiore a Z, perché i neutroni compensano la forza repulsiva elettrostatica tra i protoni. 26/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
14 Forza nucleare forte I protoni sono carichi positivamente e quindi tendono a respingersi. Tenendo in considerazione la dimensione tipica del raggio di un nucleo le forze repulsive sono molto intense r m (25) F C = 1 4πε 0 e 2 r N. (26) La repulsione è compensata da una forza attrattiva detta forza forte. Per stabilizzare un nucleo quindi si possono aggiungere neutroni che non sono carichi ma si attraggono per la forza forte. 27/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Decadimenti I Cosa vuol dire che un nucleo è instabile? Vuol dire che decade in un altro nucleo, tramutandosi nel nuovo materiale. Il tecnezio usato in medicina nucleare Il 99 Mo decade in 99m Tc con una vita media τ = 66 h. A sua volta decade con una vita media τ = 6 h in 99g Tc emettendo un raggio γ con energia E = 140 kev. Il gamma prodotto è utilizzato in diverse tecniche di medicina nucleare. Radon-222 L uranio naturale 238 U decade alpha con una vita media τ = yr, dopo una serie di decadimenti raggiunge il 226 Ra. Questo decade alpha con una vita media τ = 1600 yr in 222 Rn. Il radon è un gas nobile che decade alpha ed è quindi pericoloso se inalato. 28/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
15 Decadimenti II Possibili decadimenti 1. Fissione: Il nucleo si spacca in molti altri nuclei più leggeri, tipico per i nuclei molto pesanti (e.g. Uranio). 2. Decadimento alpha: Il nucleo emette una particella alpha, che è un nucleo di 4 He (N = 2, Z = 2): Z Z 2, N N 2 & A A 4 (27) 3. Decadimento beta-: Un neutrone si trasforma in un protone emettendo un elettrone (n p + e + ν e ): Z Z + 1, N N 1 & A = A (28) 4. Decadimento beta+: Un protone si trasforma in un neutrone emettendo un positrone (p n + e + + ν e ): Z Z 1, N N + 1 & A = A (29) 5. Decadimento gamma: Un nucleo eccitato (come può essere anche un atomo eccitato) torna allo stato fondamentale emettendo un fotone molto energetico chiamato raggio gamma (raggio γ). I valori di N e Z non cambiano. 29/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Decadimenti III Decadimenti e tabella dei nuclidi Z+1 Z Z-1 Z-2 α β - β + I processi di decadimento possono essere visualizzati sulla tavola dei nuclei, in funzione della variazione dei numeri N e Z. E.g. Il decadimento alpha cambia il valore di N e Z di due e quindi ci si sposta in diagonale di due posizioni. N-2 N-1 N N+1 30/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
16 Decadimento alpha Il decadimento alpha è tipico per gli elementi più pesanti. È dovuto all interazione forte e quindi ha tempi di vita medi tipicamente piccoli. E.g. Il gas nobile radon-222 decade alpha in polonio Rn 218 Po + α (30) 31/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Decadimenti beta I due decadimenti beta sono dovuti all interazione debole e quindi hanno tipicamente tempi di vita medi lunghi. Si osservi come non cambia il numero di massa degli elementi, perché si tratta di una trasmutazione di un protone in un neutrone o viceversa. E.g. Il carbonio-14 decade in azoto-14 per decadimento beta- 14 C 14 N + e + ν e (31) E.g. Il fluoro-18 decade in ossigeno-18 per decadimento beta+ 18 F 18 O + e + + ν e (32) Il positrone emesso dal 18 F è usato in medicina nucleare per la Positron Emission Tomography (PET). 32/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
17 Decadimento gamma Il decadimento gamma è un decadimento che si ha quando un nucleo eccitato si diseccita emettendo un fotone molto energetico (chiamato anche raggio gamma). E.g. Il tecnezio-99m decade in tecnezio-99g emettendo un gamma da 140 kev. Il 99m Tc è uno stato eccitato del tecnezio, mentre il 99g Tc è lo stato fondamentale del nucleo. 99m Tc 99g Tc + e + ν e (33) Il gamma emesso dal 99m Tc è usato in medicina nucleare per le scintigrafie e la Single Photon Emission Tomography (SPET). 33/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Energia di legame del nucleo Average binding energy per nucleon (MeV) 9 8 O 16 C 12 He Li 7 Li 6 H 3 He 3 H 2 H 1 Fe 56 Number of nucleons in nucleus U 235 U L energia di legame del nucleo dipende dal numero di protoni e neutroni. Tipicamente si rappresenta come positiva, ma il realtà dovrebbe essere negativa perché i nuclei sono degli stati legati. Più è alta l energia di legame e più è difficile spaccare il nucleo nei singoli costituenti. 34/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
18 Fusione ed energia di legame Average binding energy per nucleon (MeV) 9 8 O 16 C 12 He Li 7 Li 6 + H 3 He 3 H 2 H 1 Fe 56 ΔE>0 H 3 + ΔE<0 Number of nucleons in nucleus U 235 U Figura: Grafico dell energia di legame per alcuni isotopi comuni [wiki]. Nella fusione si fondono nuclei leggeri per avere nuclei più pesanti, ma non sempre il processo rilascia energia. Fondendo nuclei troppo pesanti è necessario fornire energia al sistema perché l energia di legame del nucleo somma diventa più bassa di quella dei nuclei iniziali. 35/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Fissione ed energia di legame 9 Average binding energy per nucleon (MeV) 8 O 16 C 12 He Li 7 Li 6 H 3 He 3 H 2 H 1 Fe 56 ΔE<0 H 3 ΔE> Number of nucleons in nucleus U 238 U 235 Nella fissione un nucleo si spacca per generare nuclei più leggeri. Quando i nuclei più pesanti si scindono possono liberare energia, mentre per i nuclei più leggeri è necessario fornire energia. Figura: Grafico dell energia di legame per alcuni isotopi comuni [wiki]. 36/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
19 Legge dei decadimenti I Un nucleo instabile ha una probabilità costante nel tempo di decadere. Se la probabilità di vedere un decadimento in un istante di tempo è λ allora la probabilità di vederlo per un insieme di N nuclei è Nλ. Ma un decadimento comporta la variazione del numero di nuclei e quindi la variazione nell istante di tempo è proporzionale al numero di nuclei: dn dt = λn (34) ove abbiamo messo un meno perché si tratta di una riduzione del numero di nuclei. Questa è un equazione differenziale che ha come risultato N(t) = N 0 e λt (35) che rappresenta il numero di nuclei sopravvissuti all istante t. 37/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Legge dei decadimenti II In genere si definisce la vita media τ come τ = 1 λ (36) e quindi la (35) diventa N(t) = N 0 e t τ (37) La vita media rappresenta il tempo che impiega il campione di nuclei instabili a ridursi al 37% del numero iniziale. 38/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
20 Tempo di dimezzamento I Calcoliamo il tempo che impiega il campione a ridursi al 50% dei nuclei iniziali log t N = N 0e τ (38) t 1 12 τ (39) [ = e ] = t 1 2 τ (40) log 2 = t 1 2 τ (41) = τ log 2 (42) t 1 2 t 1 2 è comunemente chiamato tempo di dimezzamento. 39/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017 Tempo di dimezzamento II Invertiamo la relazione τ = t 1 2 log 2 (43) e vediamo cosa succede se mettiamo nella legge dei decadimenti il tempo di dimezzamento N(t) = N 0 e t τ (44) = N 0 e log 2 t t 12 (45) = N 0 2 t t 12 (46) ove abbiamo applicato le proprietà dell esponenziale. Questa è la legge dei decadimenti espressa in termini del tempo di dimezzamento. 40/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
21 Attività di una sorgente Si definisce attività di una sorgente il numero di decadimenti al secondo, ovvero A = dn dt = λn (47) L attività si misura in Becquerel: 1 Bq = 1 1/s (48) Comunemente si usano anche i Curie: 1 Ci = Bq. (49) 41/41 FISICA PER MEDICINA Lezione 25 - Ottica e Fisica Moderna Dr. Cristiano Fontana 12 dicembre 2017
LA STRUTTURA DELL ATOMO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL ATOMO IL NUCLEO In fisica
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL ATOMO IL NUCLEO In fisica
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
TECNICHE RADIOCHIMICHE
 TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
La chimica nucleare. A cura della prof. ssa. Barone Antonina
 La chimica nucleare A cura della prof. ssa Barone Antonina La radioattività Nella seconda metà dell 800, Henry Becquerel, Pierre e Marie Curie, scoprirono che alcuni elementi( uranio, torio, radio) emettevano
La chimica nucleare A cura della prof. ssa Barone Antonina La radioattività Nella seconda metà dell 800, Henry Becquerel, Pierre e Marie Curie, scoprirono che alcuni elementi( uranio, torio, radio) emettevano
P. Sapia Università della Calabria. a.a. 2009/10
 FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
Il Nucleo. Dimensioni del nucleo dell'ordine di 10. m Il raggio nucleare R = R 0 -15
 Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
ELEMENTI di CHIMICA NUCLEARE. La FISSIONE NUCLEARE
 ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
ARGOMENTO: Cenni di Fisica del Nucleo
 UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
Elio GIROLETTI - Università degli Studi di Pavia - Dip. Fisica nucleare e teorica marzo 2005
 UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro webgiro elio giroletti radioattività (cenni) ELEMENTI
UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro webgiro elio giroletti radioattività (cenni) ELEMENTI
Emissione α. La sua carica elettrica è pari a +2e La sua massa a riposo è circa 7x10-27 kg.
 Reazioni nucleari Un nucleo instabile può raggiungere una nuova condizione di stabilità attraverso una serie di decadimenti con emissione di particelle α, β, γ o di frammenti nucleari (fissione). Emissione
Reazioni nucleari Un nucleo instabile può raggiungere una nuova condizione di stabilità attraverso una serie di decadimenti con emissione di particelle α, β, γ o di frammenti nucleari (fissione). Emissione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
Chimica Nucleare. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Un po' di fisica nucleare: La radioattività
 Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
Cenni di fisica moderna
 Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
Le radiazioni e la loro misura
 Le radiazioni e la loro misura Le radiazioni e le radiazioni ionizzanti Nuclei, radioattività, reazioni nucleari Einstein, la legge E = mc 2 e l'energia nucleare Uso degli strumenti di misura Che cosa
Le radiazioni e la loro misura Le radiazioni e le radiazioni ionizzanti Nuclei, radioattività, reazioni nucleari Einstein, la legge E = mc 2 e l'energia nucleare Uso degli strumenti di misura Che cosa
La Radioattività. da:ispra istituto superiore per la ricerca e protezione ambientale
 La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
1.1 Struttura dell atomo
 CAPITOLO I Richiami di fisica generale e descrizione delle radiazioni ionizzanti. Struttura dell atomo L atomo è la più piccola porzione di un elemento chimico, che conserva le proprietà dell elemento
CAPITOLO I Richiami di fisica generale e descrizione delle radiazioni ionizzanti. Struttura dell atomo L atomo è la più piccola porzione di un elemento chimico, che conserva le proprietà dell elemento
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z. H deuterio (6000 volte abbondante)
 Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
FNPA1 Prova parziale del 16/04/2012
 FNPA1 Prova parziale del 16/04/01 Problema 1 L energia di legame dei nuclei 4 He e 7 3 Li è rispettivamente 8.3 e 39.3 MeV. a) Verificare se la reazione p + 7 3 Li 4 3 He + 4 3 He è esotermica o endotermica.
FNPA1 Prova parziale del 16/04/01 Problema 1 L energia di legame dei nuclei 4 He e 7 3 Li è rispettivamente 8.3 e 39.3 MeV. a) Verificare se la reazione p + 7 3 Li 4 3 He + 4 3 He è esotermica o endotermica.
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Esercizi su Chimica Nucleare e Nucleogenesi
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
Introduzione alla Fisica Nucleare. Josè Javier Valiente Dobon Rosanna Depalo Alberto Boso
 STAGE ai LNL EDIZIONE 2016 Introduzione alla Fisica Nucleare Josè Javier Valiente Dobon Rosanna Depalo Alberto Boso 21 Giugno 2016 STAGE ai LNL EDIZIONE 2016 Lezione 1 Storia dell' atomo I costituenti
STAGE ai LNL EDIZIONE 2016 Introduzione alla Fisica Nucleare Josè Javier Valiente Dobon Rosanna Depalo Alberto Boso 21 Giugno 2016 STAGE ai LNL EDIZIONE 2016 Lezione 1 Storia dell' atomo I costituenti
Spettro elettromagnetico
 Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
La radioattività può avere un origine sia artificiale che naturale.
 http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti.
 1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
p e c = ev Å
 Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Lezione 24 Radiazioni Ionizzanti
 Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
Le leggi del decadimento radioattivo. Figura 1.7 la rappresentazione dei nuclei stabili nel piano Z-N
 Le leggi del decadimento radioattivo Figura 1.7 la rappresentazione dei nuclei stabili nel piano Z-N Stabiltà e instabilità nucleare Se analizziamo attentamente la carta dei nuclidi, vediamo che in essa
Le leggi del decadimento radioattivo Figura 1.7 la rappresentazione dei nuclei stabili nel piano Z-N Stabiltà e instabilità nucleare Se analizziamo attentamente la carta dei nuclidi, vediamo che in essa
Definizioni riguardo alle lenti sferiche Una lente è un mezzo trasparente limitato da due superfici di cui almeno una curva.
 1 Le lenti Definizioni riguardo alle lenti sferiche Una lente è un mezzo trasparente limitato da due superfici di cui almeno una curva. Si chiama asse ottico della lente la retta che congiunge i centri
1 Le lenti Definizioni riguardo alle lenti sferiche Una lente è un mezzo trasparente limitato da due superfici di cui almeno una curva. Si chiama asse ottico della lente la retta che congiunge i centri
Cenni di Fisica Nucleare
 Cenni di Fisica Nucleare Densita' costante r~ r (numero di nucleoni) 1/3 Dimensione finita dei nuclei Cenni di Fisica Nucleare Nomenclatura: N. massa= N. protoni+n. Neutroni = Z+N Simbolo chimico: Ca,
Cenni di Fisica Nucleare Densita' costante r~ r (numero di nucleoni) 1/3 Dimensione finita dei nuclei Cenni di Fisica Nucleare Nomenclatura: N. massa= N. protoni+n. Neutroni = Z+N Simbolo chimico: Ca,
I decadimenti radioattivi
 Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 3 I decadimenti radioattivi Radioattività naturale Osservazione di Bequerel della presenza di trasmutazioni di atomi. Osservazione
Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 3 I decadimenti radioattivi Radioattività naturale Osservazione di Bequerel della presenza di trasmutazioni di atomi. Osservazione
LE LENTI E L OCCHIO UMANO Prof. Erasmo Modica erasmo@galois.it
 LE LENTI E L OCCHIO UMANO Prof. Erasmo Modica erasmo@galois.it LE LENTI E LE LORO PROPRIETÀ Una lente è uno strumento costituito da un mezzo trasparente delimitato da due superfici curve, oppure da una
LE LENTI E L OCCHIO UMANO Prof. Erasmo Modica erasmo@galois.it LE LENTI E LE LORO PROPRIETÀ Una lente è uno strumento costituito da un mezzo trasparente delimitato da due superfici curve, oppure da una
La fisica del XX secolo ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione
 ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
SPECT (Gamma Camera)
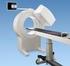 SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
OTTICA DELLA VISIONE. Disegno schematico dell occhio umano
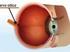 OTTICA DELLA VISIONE Disegno schematico dell occhio umano OTTICA DELLA VISIONE Parametri fisici Raggio di curvatura (cm) Cornea 0.8 Anteriore del cristallino Posteriore del cristallino.0 0.6 Indice di
OTTICA DELLA VISIONE Disegno schematico dell occhio umano OTTICA DELLA VISIONE Parametri fisici Raggio di curvatura (cm) Cornea 0.8 Anteriore del cristallino Posteriore del cristallino.0 0.6 Indice di
Fisica del VITA MEDIA o <<TEMPO SCALA>> di una stella. RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA
 Bollitore tibetano Fisica del 1900 VITA MEDIA o di una stella RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA M i c h e l s o n In Fisica oramai, è soltanto questione di mettere
Bollitore tibetano Fisica del 1900 VITA MEDIA o di una stella RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA M i c h e l s o n In Fisica oramai, è soltanto questione di mettere
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
FAM. T 1) α ν. (e α ν T 1) 2. (con l ipotesi ν > 0) si ottiene
 Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
Serie 42: Soluzioni FAM C. Ferrari Esercizio 1 Corpo nero 1. Abbiamo: Sole λ max = 500nm - spettro visibile (giallo); Sirio B λ max = 290nm - ultravioletto; corpo umano λ max = 9300nm - infrarosso. 2.
Le particelle dell atomo
 La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Cenni di Fisica del Nucleo
 Capitolo 8 Cenni di Fisica del Nucleo 8.1 Proprietà generali dei nuclei In questo capitolo affrontiamo lo studio dei nuclei. Un nucleo è un insieme di neutroni e protoni legati insieme ( incollati ) dalla
Capitolo 8 Cenni di Fisica del Nucleo 8.1 Proprietà generali dei nuclei In questo capitolo affrontiamo lo studio dei nuclei. Un nucleo è un insieme di neutroni e protoni legati insieme ( incollati ) dalla
Caratterizzazione del nuclide. Elio GIROLETTI - Università degli Studi di Pavia - Dip. Fisica nucleare e teorica. ottobre 2008
 UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro elio giroletti radioattività e radiazioni RISCHI FISICI
UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro elio giroletti radioattività e radiazioni RISCHI FISICI
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI
 ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
Atomo: modello microscopico
 Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Capitolo 6 : Decadimenti, Risonanze, Modello di Yukawa, Interazioni tra Particelle
 Capitolo 6 : Decadimenti, Risonanze, Modello di Yukawa, Interazioni tra Particelle Corso di Fisica Nucleare e Subnucleare I Professor Carlo Dionisi A.A. 2004-2005 1 Legge di decadimento Decadimento di
Capitolo 6 : Decadimenti, Risonanze, Modello di Yukawa, Interazioni tra Particelle Corso di Fisica Nucleare e Subnucleare I Professor Carlo Dionisi A.A. 2004-2005 1 Legge di decadimento Decadimento di
dal 15 al 26/06/2015 Gerti Xhixha LEZIONE DI MARTEDI 16 GIUGNO 2015
 dal 15 al 26/06/2015 Gerti Xhixha xhixha@fe.infn.it LEZIONE DI MARTEDI 16 GIUGNO 2015 1 Introduzione alla fisica nucleare Breve storia dell atomo I costituenti dei nuclei atomici Leggi di conservazione
dal 15 al 26/06/2015 Gerti Xhixha xhixha@fe.infn.it LEZIONE DI MARTEDI 16 GIUGNO 2015 1 Introduzione alla fisica nucleare Breve storia dell atomo I costituenti dei nuclei atomici Leggi di conservazione
Il nucleo degli atomi
 Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
Il nucleo atomico 1. Energia di legame nucleare 2. La radioattività naturale 3. Banda di stabilità degli isotopi degli elementi naturali 4. Decadimenti radioattivi 5. Reazioni nucleari Il nucleo degli
dal 18 al 22/06/2012 Gerti Xhixha
 dal 18 al 22/06/2012 Gerti Xhixha (xhixha@fe.infn.it) 1 Introduzione alla fisica nucleare Breve storia dell atomo I costituenti dei nuclei atomici Leggi di conservazione Scale di lunghezza, massa e tempo
dal 18 al 22/06/2012 Gerti Xhixha (xhixha@fe.infn.it) 1 Introduzione alla fisica nucleare Breve storia dell atomo I costituenti dei nuclei atomici Leggi di conservazione Scale di lunghezza, massa e tempo
Caratterizzazione del nuclide. Elio GIROLETTI - Università degli Studi di Pavia - Dip. Fisica nucleare e teorica febbraio 2009
 UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro elio giroletti Elio GIROLETTI dip. Fisica nucleare e
UNIVERSITÀ DEGLI STUDI DI PVI dip. Fisica nucleare e teorica via assi 6, 271 Pavia, Italy tel. 38298.795 - girolett@unipv.it - www.unipv.it/webgiro elio giroletti Elio GIROLETTI dip. Fisica nucleare e
MISURA DELLA MASSA DELL ELETTRONE
 MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
VISIONE_01 OTTICA GEOMETRICA. FGE aa
 VISIONE_01 OTTICA GEOMETRICA FGE aa.2015-16 OBIETTIVI Principi di refrazione delle lenti, indice di refrazione Lenti biconcave e lenti biconvesse, fuoco principale e distanza focale Potere refrattivo di
VISIONE_01 OTTICA GEOMETRICA FGE aa.2015-16 OBIETTIVI Principi di refrazione delle lenti, indice di refrazione Lenti biconcave e lenti biconvesse, fuoco principale e distanza focale Potere refrattivo di
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
Materia e forze alla scala subatomica: il nucleo atomico, le particelle elementari
 Materia e forze alla scala subatomica: il nucleo atomico, le particelle elementari Andrea Bizzeti Università di Modena e Reggio Emilia Dipartimento di Scienze Fisiche, Informatiche e Matematiche Modena,
Materia e forze alla scala subatomica: il nucleo atomico, le particelle elementari Andrea Bizzeti Università di Modena e Reggio Emilia Dipartimento di Scienze Fisiche, Informatiche e Matematiche Modena,
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z. H deuterio (6000 volte abbondante)
 Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
DECADIMENTI. Fissione spontanea di atomi instabili con emissione di neutroni
 DECADIMENTI Fissione spontanea di atomi instabili con emissione di neutroni DECADIMENTO ALPHA Tipico di elementi pesanti che diventano più stabili dopo il decadimento. DECADIMENTO BETA Prodotto da interazione
DECADIMENTI Fissione spontanea di atomi instabili con emissione di neutroni DECADIMENTO ALPHA Tipico di elementi pesanti che diventano più stabili dopo il decadimento. DECADIMENTO BETA Prodotto da interazione
La radiazione elettromagnetica. aumento della frequenza n della radiazione aumento dell energia E della radiazione
 La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
La radiazione elettromagnetica aumento della frequenza n della radiazione aumento dell energia E della radiazione La radiazione elettromagnetica Un onda elettromagnetica è caratterizzata dalla lunghezza
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER:
 ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
ELEMENTI DI DI OTTICA E FISICA NUCLEARE INSEGNAMENTO COMPLEMENTARE (9 CFU) PER: CORSO DI LAUREA TRIENNALE IN SCIENZE E TECNOLOGIE PER LO STUDIO E LA CONSERVAZIONE DEI BENI CULTURALI E DEI SUPPORTI DELLA
Il nucleo dell'atomo
 Il nucleo dell'atomo L'atomo si può considerare suddiviso in due regioni: Il nucleo, carico positivamente: è formato di protoni e neutroni La nuvola elettronica, carica negativamente: lo spazio intorno
Il nucleo dell'atomo L'atomo si può considerare suddiviso in due regioni: Il nucleo, carico positivamente: è formato di protoni e neutroni La nuvola elettronica, carica negativamente: lo spazio intorno
A 2 Z A 2 Z. PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 1842 m e
 PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 184 m e Z = numero atomico = numero dei protoni (elettroni) proprietà chimiche A = numero di massa = numero dei protoni + neutroni massa
PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 184 m e Z = numero atomico = numero dei protoni (elettroni) proprietà chimiche A = numero di massa = numero dei protoni + neutroni massa
1 p. 1 q 1 R. altrimenti se il mezzo circostante ha un indice di rifrazione n 0. , al posto di n si deve usare
 2 Lenti Le lenti sono costituite da un mezzo rifrangente, di indice di rifrazione n, omogeneo, delimitato da superfici sferiche nel caso in cui il mezzo circostante é l aria: l equazione delle lenti é
2 Lenti Le lenti sono costituite da un mezzo rifrangente, di indice di rifrazione n, omogeneo, delimitato da superfici sferiche nel caso in cui il mezzo circostante é l aria: l equazione delle lenti é
CAPITOLO 20 LA CHIMICA NUCLEARE
 CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
Interazione radiazione materia Dott.ssa Alessandra Bernardini
 Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza. Lezione 10. Fusione nucleare
 Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 10 Fusione nucleare Fusione nucleare (Das-Ferbel, cap. 5.3) Abbiamo già accennato alla fusione nucleare che costituisce la sorgente
Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 10 Fusione nucleare Fusione nucleare (Das-Ferbel, cap. 5.3) Abbiamo già accennato alla fusione nucleare che costituisce la sorgente
Paolo Montagna, Paolo Vitulo
 - radioattività naturale - legge del decadimento radioattivo - equilibrio secolare Stage per le scuole superiori Dipartimento di Fisica 10 giugno 2013 Paolo Montagna, Paolo Vitulo Dipartimento di Fisica
- radioattività naturale - legge del decadimento radioattivo - equilibrio secolare Stage per le scuole superiori Dipartimento di Fisica 10 giugno 2013 Paolo Montagna, Paolo Vitulo Dipartimento di Fisica
Ottica geometrica. Propagazione per raggi luminosi (pennello di luce molto sottile)
 Ottica geometrica Propagazione per raggi luminosi (pennello di luce molto sottile) All interno di un mezzo omogeneo la propagazione e rettilinea: i raggi luminosi sono pertanto rappresentati da tratti
Ottica geometrica Propagazione per raggi luminosi (pennello di luce molto sottile) All interno di un mezzo omogeneo la propagazione e rettilinea: i raggi luminosi sono pertanto rappresentati da tratti
Atomi a più elettroni
 Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
Atomi a più elettroni L atomo di elio è il più semplice sistema di atomo a più elettroni. Due sistemi di livelli tra i quali non si osservano transizioni Sistema di singoletto->paraelio Righe singole,
M. Marengo LA RADIOATTIVITA. Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna
 M. Marengo LA RADIOATTIVITA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna Rev Febbraio 2010 mario.marengo@unibo.it La radioattività + Bequerel osservò che alcuni materiali
M. Marengo LA RADIOATTIVITA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna Rev Febbraio 2010 mario.marengo@unibo.it La radioattività + Bequerel osservò che alcuni materiali
April 11, 2011. Fisica Nucleare. Monica Sambo. Sommario. Introduzione. Radioattivitá. Fisica del nucleo. Bibliografia. Esempio. Raggi emessi Esempio
 April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
April 11, 2011 1 2 3 4 Indicando con Z il numero dei protoni (numero atomico dell atomo) e con N il numero dei neutroni si definisce A il numero di massa del : A = Z + N (1) Nei nuclei leggeri si ha la
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
La fisica nucleare. Capitolo. Concetti da rivedere 24.1 LA STRUTTURA NUCLEARE
 24txtI:GIAMBATTISTA 14-12-2007 12:06 Pagina 943 Capitolo 24 La fisica nucleare Forze fondamentali (Paragrafo 2.9) Funzioni esponenziali (Appendice A.3, Paragrafo 17.10) Concetti da rivedere 24.1 LA STRUTTURA
24txtI:GIAMBATTISTA 14-12-2007 12:06 Pagina 943 Capitolo 24 La fisica nucleare Forze fondamentali (Paragrafo 2.9) Funzioni esponenziali (Appendice A.3, Paragrafo 17.10) Concetti da rivedere 24.1 LA STRUTTURA
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. Massa atomica MOLE. a.a.
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Problemi con l'atomo. Significato delle righe spettrali. Modello dell'atomo
 Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Problemi con l'atomo Significato delle righe spettrali Modello dell'atomo Righe spettrali della luce emissione e assorbimento Posizione delle righe spettrali Dipende dall'elemento considerato Per l'idrogeno
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
ISOTOPI. Gli atomi sono costituiti da protoni, elettroni e neutroni.
 ISOTOPI Gli atomi sono costituiti da protoni, elettroni e neutroni. I protoni hanno carica positiva e sono localizzati all interno del nucleo dell atomo, in una regione di spazio di dimensioni dell ordine
ISOTOPI Gli atomi sono costituiti da protoni, elettroni e neutroni. I protoni hanno carica positiva e sono localizzati all interno del nucleo dell atomo, in una regione di spazio di dimensioni dell ordine
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
1 S/f. M = A t = A + CT = 1 S f
 Ot Una lente sottile con focale f 50 mm è utilizzata per proiettare su di uno schermo l immagine di un oggetto posto a 5 m. SI determini la posizione T dello schermo e l ingrandimento che si ottiene La
Ot Una lente sottile con focale f 50 mm è utilizzata per proiettare su di uno schermo l immagine di un oggetto posto a 5 m. SI determini la posizione T dello schermo e l ingrandimento che si ottiene La
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
La misura della radioattivita γ lezione 1. Cristiana Peroni Corsi di LS in Scienze Biomolecolari Universita di Torino Anno accademico
 La misura della radioattivita γ lezione 1 Cristiana Peroni Corsi di LS in Scienze Biomolecolari Universita di Torino Anno accademico 2007-2008 1 Generalita sul corso 2 Misure di radioattivita con un rivelatore
La misura della radioattivita γ lezione 1 Cristiana Peroni Corsi di LS in Scienze Biomolecolari Universita di Torino Anno accademico 2007-2008 1 Generalita sul corso 2 Misure di radioattivita con un rivelatore
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
LA STRUTTURA DELL ATOMO
 Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Cos è. la Chimica? G. Micera Chimica Generale e Inorganica
 Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Produzione dei raggi X
 I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
I RAGGI X Produzione dei raggi X Tubo a raggi X Emissione per frenamento Emissione per transizione Spettro di emissione pag.1 Lunghezza d onda, frequenza, energia (fm) λ (m) 10 14 RAGGI GAMMA ν 10 12 (Å)
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Esercizi. 1. Fotoni, elettroni. 2. Struttura della materia. 3. Nuclei, radioattività. 4. Produzione e consumo di energia E-X - 0
 Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Il nucleare non è il diavolo. Il problema:
 2005 Anno Mondiale della Fisica Il nucleare non è il diavolo Progetto di monitoraggio della radioattività ambientale nelle scuole Sezione di Torino dell INFN e Dipartimenti di Fisica dell Università di
2005 Anno Mondiale della Fisica Il nucleare non è il diavolo Progetto di monitoraggio della radioattività ambientale nelle scuole Sezione di Torino dell INFN e Dipartimenti di Fisica dell Università di
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
GEOCRONOLOGIA. Il prima problema affrontato fu quello dell età della Terra legato inevitabilmente all età dell Universo.
 GEOCRONOLOGIA L esigenza di conoscere i tempi di occorrenza di fenomeni naturali (l età della Terra, formazione di rocce, nascita e morte di alcune specie animali, ecc) ha portato a cercare METODI affidabili
GEOCRONOLOGIA L esigenza di conoscere i tempi di occorrenza di fenomeni naturali (l età della Terra, formazione di rocce, nascita e morte di alcune specie animali, ecc) ha portato a cercare METODI affidabili
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
ATOMI E MOLECOLE. Psicobiologia Lezione nr. 1. Prof. Lasaponara
 ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
