ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
|
|
|
- Lelio Pasquali
- 5 anni fa
- Visualizzazioni
Transcript
1 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1
2 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta. Vedere paragrafo 4.8 per informazioni sulle modalità di segnalazione delle reazioni avverse. 1. DENOMINAZIONE DEL MEDICINALE Amyvid 800 MBq/ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml di soluzione iniettabile contiene 800 MBq di florbetapir ( 18 F) alla data e ora di calibrazione (ToC, Time of Calibration). L attività per flaconcino varia da 800 MBq a MBq alla data e ora di calibrazione. Il fluoro ( 18 F) decade in ossigeno stabile ( 18 O) con un emivita di circa 110 minuti emettendo una radiazione di positroni di 634 kev, seguita da radiazione da annichilazione fotonica di 511 kev. Eccipienti con effetti noti: Questo medicinale contiene 79 mg/ml di etanolo e fino a 37 mg di sodio. Per l elenco completo degli eccipienti, vedere paragrafo FORMA FARMACEUTICA Soluzione iniettabile. Soluzione limpida incolore. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Medicinale solo per uso diagnostico. Amyvid è un radiofarmaco indicato per rilevare con la tomografia ad emissione di positroni (PET) le immagini della densità delle placche neuritiche di β -amiloide nel cervello di pazienti adulti con decadimento cognitivo che vengono valutati per la malattia di Alzheimer (AD) e altre cause di decadimento cognitivo. Amyvid deve essere usato congiuntamente alla valutazione clinica. Una scansione negativa indica la presenza di poche placche o l assenza di placche, il che non è coerente con una diagnosi di AD. Per i limiti nell interpretazione di una scansione positiva vedere i paragrafi 4.4 e Posologia e modo di somministrazione Una scansione PET con florbetapir deve essere richiesta da medici con esperienza nella gestione clinica delle patologie neurodegenerative. Le immagini ottenute con Amyvid devono essere interpretate solo da valutatori che hanno effettuato un training su come interpretare le immagini della PET con florbetapir ( 18 F). Nei casi in cui con la scansione PET è difficile localizzare la sostanza grigia e il margine della sostanza bianca/grigia, si raccomanda un esame recente con tomografia computerizzata (TC) o con risonanza magnetica (RM), co-registrato con l esame PET, per ottenere un immagine combinata PET-TC o PET-RM (vedere il paragrafo 4.4 Interpretazione delle immagini). 2
3 Posologia L attività raccomandata per un adulto che pesa 70 kg è 370 MBq di florbetapir ( 18 F). Il volume dell iniezione non deve essere inferiore a 1 ml e non superare 10 ml. Popolazioni speciali Persone anziane Non è raccomandato un aggiustamento della dose in base all età. Insufficienza renale ed epatica E necessaria una valutazione attenta dell attività da somministrare perché in questi pazienti è possibile che l esposizione alle radiazioni risulti maggiore. Vedere il paragrafo 4.4. Non sono stati eseguiti studi estesi per determinare il range o l aggiustamento della dose con questo medicinale nelle popolazioni normali e speciali. Le farmacocinetiche di florbetapir ( 18 F) in pazienti con insufficienza renale o epatica non sono state caratterizzate. Popolazione pediatrica Non c è un uso rilevante di Amyvid nella popolazione pediatrica. Modo di somministrazione Per uso endovenoso. Per uso multidose. L attività di florbetapir ( 18 F) deve essere misurata con un calibratore di dose immediatamente prima dell iniezione. La dose è somministrata per iniezione endovenosa in bolo, seguita da un lavaggio con una soluzione iniettabile di cloruro di sodio 9 mg/ml (0,9%) per assicurare la somministrazione completa della dose. L iniezione di Amyvid attraverso un catetere endovenoso corto (approssimativamente di 4 cm o meno) minimizza il potenziale assorbimento del principio attivo da parte del catetere. L'iniezione di florbetapir ( 18 F) deve essere endovenosa per evitare l irradiazione dovuta a travaso locale, così come la rilevazione di immagini artefatte. Acquisizione delle immagini Un immagine PET di 10 minuti deve essere acquisita circa minuti dopo l iniezione endovenosa di Amyvid. I pazienti devono stare supini con la testa posizionata in modo tale da centrare il cervello, incluso il cervelletto, nel campo visivo dello scanner della PET. Per ridurre il movimento della testa possono essere impiegati un nastro o altri poggiatesta flessibili. La ricostruzione deve includere la correzione per l attenuazione per avere pixel transassiali delle dimensioni comprese tra 2,0 e 3,0 mm. 4.3 Controindicazioni Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo Avvertenze speciali e precauzioni di impiego Per ogni paziente l esposizione a radiazioni deve essere giustificata sulla base dei possibili benefici. Giustificazione di un rapporto beneficio/rischio individuale L attività somministrata deve, in ogni caso, essere la più bassa possibile per ottenere le informazioni diagnostiche richieste. 3
4 Insufficienza renale e insufficienza epatica Per questi pazienti è necessaria un attenta valutazione del rapporto beneficio/rischio poiché è possibile che l esposizione alle radiazioni risulti aumentata. Florbetapir ( 18 F) è escreto principalmente attraverso il sistema epatobiliare e per i pazienti con insufficienza epatica esiste la possibilità di un aumentata esposizione alle radiazioni. Vedere anche il paragrafo 4.2. Popolazione pediatrica Per informazioni sull uso nella popolazione pediatrica, vedere i paragrafi 4.2 o 5.1. Interpretazione delle immagini con Amyvid Le immagini con Amyvid devono essere interpretate solo da valutatori che hanno effettuato il training su come interpretare le immagini della PET con florbetapir ( 18 F). Una scansione negativa indica una densità scarsa o assente di placche neuritiche corticali di ß-amiloide. Una scansione positiva indica una densità da moderata a frequente. Sono stati osservati errori di interpretazione dell immagine nella valutazione della densità delle placche neuritiche cerebrali di β-amiloide, inclusi dei falsi negativi. La valutazione delle immagini deve essere eseguita principalmente nell orientamento transassiale e, quando necessario, anche sui piani sagittale e coronale. Si raccomanda che la valutazione delle immagini includa tutte le sezioni transassiali del cervello usando una scala in bianco e nero con l intensità massima della scala impostata alla massima intensità di pixel su tutto il cervello. L interpretazione dell immagine come negativa o positiva viene effettuata confrontando visivamente l attività della sostanza grigia corticale con l attività della sostanza bianca corticale adiacente (vedere la Figura 1). Scansioni negative hanno più attività nella sostanza bianca che nella sostanza grigia, creando un evidente contrasto grigia-bianca. Scansioni positive avranno: a) Due o più aree del cervello (ciascuna più larga di una singola circonvoluzione corticale) in cui il contrasto grigia-bianca è ridotto o assente. Questo è il modo in cui appare più comunemente una scansione positiva. b) Una o più aree in cui l attività della sostanza grigia è intensa e supera in modo evidente l attività della sostanza bianca adiacente. 4
5 Figura 1: Immagini PET con Amyvid che mostrano esempi di scansioni negative (le due righe in alto) e di scansioni positive (le due righe in basso). Le figure da sinistra a destra mostrano le immagini PET relative alla sezione sagittale, coronale e trasversale. L ultima figura a destra mostra l immagine ingrandita dell area del cervello evidenziata nel rettangolo. Le due frecce in alto indicano il normale contrasto grigia-bianca preservato con un attività corticale inferiore a quella della sostanza bianca adiacente. Le due frecce in basso indicano aree con un ridotto contrasto grigia-bianca e un aumentata attività corticale che è paragonabile all attività della sostanza bianca adiacente. Limitazioni di utilizzo Una scansione positiva non è sufficiente da sola a stabilire una diagnosi di AD o di un altro disturbo cognitivo poiché nei pazienti anziani asintomatici e in alcune demenze neurodegenerative (AD, demenza da corpi di Lewy, demenza da malattia di Parkinson) possono essere presenti depositi di placche neuritiche nella sostanza grigia. Per le limitazioni di utilizzo nei pazienti con deterioramento cognitivo lieve (MCI), vedere il paragrafo 5.1. L efficacia di Amyvid nel prevedere lo sviluppo di AD o monitorare la risposta alla terapia non è stata stabilita (vedere il paragrafo 5.1). Alcune scansioni possono essere di difficile interpretazione a causa del rumore di fondo dell immagine, della marcata atrofia con assottigliamento corticale o dell immagine sfocata che possono portare ad errori di interpretazione. Nei casi in cui è difficile individuare con le scansioni PET la sede della sostanza grigia e il margine della sostanza bianca/grigia, ed è disponibile un immagine recente di TC o di RM registrata 5
6 contemporaneamente all esame PET, chi effettua l interpretazione deve esaminare l immagine combinata della PET-TC o della PET-RM per chiarire la correlazione tra il reperto della PET e l anatomia della sostanza grigia. In alcuni casi è stata identificata un aumentata captazione in strutture extracerebrali quali le ghiandole salivali, la cute, i muscoli e le ossa (vedere il paragrafo 5.2). L esame delle immagini sagittali e le immagini della TC o della RM registrate contemporaneamente possono aiutare a distinguere l osso occipitale dalla sostanza grigia occipitale. Dopo l esame Nelle prime 24 ore successive all iniezione, il contatto ravvicinato con bambini e donne in gravidanza deve essere limitato. Avvertenze specifiche Il contenuto di sodio è superiore a 1 mmol (fino a 37 mg per dose). Questo deve essere tenuto in considerazione nei pazienti con una dieta a basso contenuto di sodio. Questo medicinale contiene 10 vol % di etanolo (alcol), cioè fino a 790 mg per dose, equivalenti a 20 ml di birra o 8 ml di vino per dose. Questa quantità può essere dannosa per chi soffre di alcolismo e ciò deve essere tenuto in considerazione nelle donne in gravidanza e che stanno allattando e nei gruppi ad alto rischio come i pazienti con malattia epatica o epilessia. 4.5 Interazioni con altri medicinali ed altre forme di interazione Non sono stati effettuati studi di interazione in vivo. Studi di legame in vitro non hanno mostrato interferenze del legame di florbetapir ( 18 F) alle placche di ß- amiloide in presenza degli altri medicinali comunemente assunti dai pazienti con AD. 4.6 Fertilità, gravidanza e allattamento Donne potenzialmente fertili Quando è prevista la somministrazione di radiofarmaci ad una donna potenzialmente fertile, è importante determinare se è o non è in stato di gravidanza. Ove non sia provato il contrario, qualsiasi donna che abbia saltato un ciclo mestruale deve essere considerata in stato di gravidanza. In caso di dubbi riguardo ad una possibile gravidanza (se la donna ha saltato un ciclo mestruale, se il ciclo mestruale è molto irregolare, etc.), devono essere proposte alla paziente tecniche alternative che non utilizzino radiazioni ionizzanti (qualora ve ne siano). Gravidanza Le metodiche che utilizzano radionuclidi impiegate su donne in stato di gravidanza generano radiazioni che coinvolgono il feto. Pertanto, durante la gravidanza devono essere eseguiti soltanto gli esami ritenuti essenziali, quando il probabile beneficio supera di gran lunga il rischio per la madre e per il feto. Non sono stati condotti studi nelle donne in stato di gravidanza. Non sono stati eseguiti studi negli animali per valutare gli effetti di florbetapir ( 18 F) sulla riproduzione (vedere il paragrafo 5.3). Allattamento Non è noto se florbetapir ( 18 F) sia escreto nel latte umano durante l allattamento. Prima della somministrazione di radiofarmaci a una madre che sta allattando al seno si deve valutare la possibilità di ritardare la somministrazione del radionuclide fino a quando la madre abbia terminato l allattamento al seno e considerare se sia stato scelto il radiofarmaco più appropriato tenendo presente l eliminazione di attività nel latte materno. Se la somministrazione è ritenuta necessaria, l allattamento deve essere interrotto per 24 ore e il latte prodotto deve essere eliminato. Nelle prime 24 ore successive all iniezione, il contatto ravvicinato con bambini deve essere limitato. 6
7 Fertilità Non sono stati effettuati studi sulla fertilità. 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Non pertinente. 4.8 Effetti indesiderati Riassunto del profilo di sicurezza Le reazioni avverse sono state raccolte negli studi clinici che hanno coinvolto 555 soggetti con 665 somministrazioni di Amyvid soluzione iniettabile. Non sono state riportate reazioni avverse gravi correlate alla somministrazione di Amyvid. Elenco delle reazioni avverse La frequenza è definita come molto comune ( 1/10), comune ( 1/100, <1/10), non comune ( 1/1.000, <1/100), raro ( 1/10.000, <1/1.000), molto raro (<1/10.000), non nota (la frequenza non può essere definita sulla base dei dati disponibili). Nella realtà le reazioni avverse potrebbero verificarsi con una frequenza anche inferiore a quella riportata di seguito, ma la dimensione del database da cui sono stati ottenuti i dati non ha permesso di assegnare le categorie di frequenza inferiore alla categoria non comune ( 1/1.000, <1/100). Patologie del sistema nervoso Comuni: cefalea Non comuni: disgeusia Patologie vascolari Non comuni: vampate di calore Patologie gastrointestinali Non comuni: nausea Patologie della cute e del tessuto sottocutaneo Non comuni: prurito, orticaria Patologie sistemiche e condizioni relative alla sede di somministrazione Non comuni: rash a livello del sito di infusione, reazione in corrispondenza del sito di iniezione (tra cui emorragia, irritazione e dolore). L'esposizione alle radiazioni ionizzanti è correlata all'induzione di cancro e al potenziale sviluppo di difetti ereditari. Poiché, quando viene somministrata l'attività raccomandata di 370 MBq di florbetapir ( 18 F), la dose efficace è 7 msv, queste reazioni avverse sono attese con una bassa probabilità. Segnalazione delle reazioni avverse sospette La segnalazione delle reazioni avverse sospette che si verificano dopo l autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione riportato nell Allegato V. 7
8 4.9 Sovradosaggio Data la piccola quantità di florbetapir ( 18 F) in ogni dose, il sovradosaggio non dovrebbe provocare effetti farmacologici. Nel caso di somministrazione di un sovradosaggio di radiazioni, la dose assorbita dal paziente deve essere ridotta se possibile aumentando l eliminazione del radionuclide dal corpo con una frequente minzione e defecazione. Potrebbe essere utile calcolare la dose efficace che è stata impiegata. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: radiofarmaceutici diagnostici, sistema nervoso centrale, Codice ATC: V09AX05. Meccanismo d azione Florbetapir ( 18 F) si lega alle placche neuritiche di ß-amiloide. Gli studi di legame che usano i tradizionali metodi di colorazione neuropatologica su cervelli con AD post-mortem hanno dimostrato una correlazione statisticamente significativa (p < ) tra il legame di florbetapir ( 18 F) in vitro e il deposito di aggregati ß- amiloidi. In vivo, la correlazione tra la captazione di florbetapir ( 18 F) nella sostanza grigia corticale e la quantità totale di ß-amiloide è stata valutata in pazienti in fin di vita usando l anticorpo anti-amiloide 4G8 che evidenzia la ß-amiloide trovata sia nelle placche neuritiche che diffuse. Il legame in vivo di florbetapir ( 18 F) ad altre strutture ß-amiloidi o ad altre strutture o recettori cerebrali rimane sconosciuto. Effetti farmacodinamici Alle basse concentrazioni chimiche presenti in Amyvid, florbetapir ( 18 F) non ha una attività farmacologica rilevabile. Negli studi clinici completati, la captazione di florbetapir ( 18 F) in 6 aree corticali predefinite del cervello (precuneo, frontale, cingolato anteriore, cingolato posteriore, parietale e temporale) è stata misurata quantitativamente usando come indice il valore di captazione standardizzato (SUV, Standardised Uptake Value). I rapporti medi dei SUV corticali (SUVR, relativi al cervelletto) sono più alti nei pazienti con AD rispetto a quelli dei soggetti volontari sani. I valori medi dei SUVR corticali rispetto a quelli cerebellari nei pazienti con AD mostrano sostanziali aumenti continui dal tempo zero nei 30 minuti dopo la somministrazione e successivamente, con solo delle piccole variazioni, fino a 90 minuti dopo la somministrazione. Non sono state notate differenze nei risultati in termini di SUVR nei soggetti che assumevano i comuni trattamenti per l AD rispetto a quelli che non li assumevano. Efficacia clinica E stato eseguito uno studio pivotal su 59 pazienti in fin di vita con l obiettivo di stabilire la performance diagnostica di Amyvid nel rilevare la densità delle placche neuritiche corticali (densità assente o scarsa vs densità moderata o frequente). I risultati della PET sono stati confrontati con la più alta densità di placche neuritiche misurata sulle sezioni della corteccia frontale, temporale o parietale di pazienti sottoposti ad autopsia nei 24 mesi successivi alla scansione PET. Non è stato possibile misurare in modo affidabile lo stato cognitivo dei soggetti. In tutti i 59 soggetti, la valutazione della PET in cieco da parte di 5 medici nucleari ha dato come risultato nella maggior parte dei casi una sensibilità di lettura del 92% (95% IC: 78-98%) e una specificità del 100% (95% IC: %). In uno studio su 47 volontari sani giovani (di età inferiore a 40 anni), che si presumeva essere privi di depositi ß-amiloidi, tutte le scansioni PET con Amyvid sono state negative. La sensibilità e la specificità di Amyvid nel rilevare la densità delle placche neuritiche corticali sono state ulteriormente valutate in due altri studi in cui differenti gruppi di valutatori hanno interpretato le immagini di alcuni soggetti poi sottoposti ad esame autoptico nello studio pivotal. I risultati di questi studi sono stati analoghi ai risultati ottenuti nello studio pivotal. La consistenza tra i valutatori, usando valori della kappa di Fleiss, variava da 0.75 a
9 In uno studio longitudinale, 142 soggetti (con diagnosi clinica di MCI, AD o cognitivamente normali) sono stati sottoposti alle scansioni PET con florbetapir ( 18 F) all inizio dello studio e poi sono stati seguiti per 3 anni per valutare la relazione tra le immagini ottenute con Amyvid e le variazioni dello stato diagnostico. I valori di performance diagnostica della PET con florbetapir ( 18 F) sono riportati nella tabella di seguito: Accordo con la diagnosi di MCI all inizio dello studio Accordo con la diagnosi di di AD clinicamente manifesta all inizio dello studio N=51 N=31 Sensibilità 19/51 = 37,3% (95% IC: 24,1-51,9%) 21/31 = 67,7% (95% IC: 51,3-84,2%) Specificità Utilizzando casi non-mci (cognitivamente normali & con AD clinicamente manifesta) 69/100 = 69,0% (95% IC: 59,9-78,1%) Utilizzando casi non-ad (cognitivamente normali & con MCI) 91/120 = 75,8% (95% IC: 68,2-83,5%) Quoziente di probabilità positivo 1.20 (95% IC: ) 2.80 (95% CI: ) Dei pazienti che all inizio dello studio avevano avuto una diagnosi clinica di MCI, 9 (19%) sono passati ad AD clinicamente manifesta dopo 36 mesi. Dei 17 pazienti con MCI che hanno avuto una scansione PET positiva, 6 (35%) hanno avuto una diagnosi di probabile AD clinicamente manifesta dopo 36 mesi rispetto a 3 (10%) dei 30 pazienti che hanno avuto una scansione negativa. La sensibilità della scansione con Amyvid nel rilevare la percentuale di passaggio da MCI ad AD nei 9 pazienti è stata del 66,7% (95% IC: 35-88%), la specificità nei 38 pazienti che non hanno avuto questa evoluzione è stata del 71,0% (95% IC: 55-83%) e il quoziente di probabilità positivo è stato di 2.31 (95% IC: %). Il disegno di questo studio non permette di stimare il rischio di evoluzione da MCI ad AD clinicamente manifesta. Popolazione pediatrica L Agenzia europea dei medicinali ha previsto l esonero dall obbligo di presentare i risultati degli studi con Amyvid in tutti i sottogruppi della popolazione pediatrica poiché non è indicato per l uso nella popolazione pediatrica. 5.2 Proprietà farmacocinetiche Distribuzione Florbetapir ( 18 F) si distribuisce nell organismo entro alcuni minuti dall iniezione e poi è rapidamente metabolizzato. Captazione a livello degli organi La massima captazione di florbetapir ( 18 F) a livello encefalico si verifica entro alcuni minuti dall iniezione, seguita da una rapida clearance a livello encefalico nei primi 30 minuti successivi all iniezione. Gli organi di maggiore esposizione sono gli organi di eliminazione, principalmente la colecisti, il fegato e l intestino. I soggetti di controllo sani mostrano livelli di accumulo relativamente bassi di florbetapir ( 18 F) a livello della corteccia e del cervelletto. Analisi regionali mostrano livelli leggermente più alti di accumulo nel caudato, nel putamen e nell ippocampo. Il livello più alto di captazione si verifica nelle regioni composte principalmente da sostanza bianca (ponte e centro semiovale). Nei soggetti con AD, le regioni corticali e il putamen mostrano una captazione significativamente maggiore rispetto ai soggetti di controllo. Nei soggetti con AD, come nei soggetti di controllo, c è un ridotto accumulo nel cervelletto e nell ippocampo e un elevato accumulo nel ponte e nel centro semiovale. 9
10 Le basi biofisiche dell accumulo di florbetapir ( 18 F) nella sostanza bianca del cervello umano vivente non possono essere ancora del tutto spiegate. Si ipotizza che una clearance inferiore del radiofarmaco possa contribuire all accumulo nella sostanza bianca poiché il flusso ematico cerebrale regionale nella sostanza bianca è meno della metà di quello nella corteccia. In alcuni casi è stata identificata un aumentata captazione in strutture extracerebrali quali il cuoio capelluto, le ghiandole salivali, i muscoli e le ossa del cranio. La ragione di questa captazione non è nota, ma potrebbe essere dovuta all accumulo di florbetapir ( 18 F) o di qualche suo metabolita radioattivo o alla radioattività presente nel sangue. Eliminazione L eliminazione avviene principalmente per clearance epatica ed escrezione nella colecisti e nell intestino. Un certo accumulo/escrezione è osservato anche nella vescica. Nelle urine la radioattività è presente sottoforma di metaboliti polari di florbetapir ( 18 F). Emivita Florbetapir ( 18 F) scompare molto rapidamente dal circolo sanguigno dopo l iniezione endovenosa. Meno del 5% della radioattività 18 F iniettata rimane nel sangue 20 minuti dopo la somministrazione e meno del 2% è presente 45 minuti dopo la somministrazione. Il fluoro 18 F residuo in circolo durante la finestra di minuti di rilevamento delle immagini è principalmente nelle forme polari del 18 F. L emivita radioattiva del 18 F è 110 minuti. Insufficienza renale/epatica Le farmacocinetiche in pazienti con insufficienza renale o epatica non sono state caratterizzate. 5.3 Dati preclinici di sicurezza Tossicologia animale e sicurezza farmacologica I dati non clinici rivelano che non c è un rischio specifico per l uomo sulla base degli studi convenzionali di sicurezza farmacologica e di tossicità a dose singola e ripetuta, nei quali è stato usato florbetapir [la forma non radioattiva di florbetapir ( 18 F)]. Uno studio con una dose acuta è stato eseguito nei ratti ed è stato determinato che il NOAEL (No Observed Adverse Effect Level - la dose senza effetto avverso osservabile) è almeno 100 volte la massima dose per l uomo. La tossicità potenziale di iniezioni endovenose di florbetapir ripetute per 28 giorni è stata valutata nei ratti e nei cani beagle ed il NOAEL è stato almeno 25 volte la massima dose per l uomo. In un test di reversione della mutazione (test di Ames) su batteri in vitro, sono stati osservati aumenti del numero delle colonie revertite in 2 dei 5 ceppi esposti a florbetapir. In uno studio in vitro di aberrazione cromosomica con culture di cellule linfocitarie periferiche umane, florbetapir non ha causato un aumento della percentuale di cellule con aberrazione cromosomica dopo 3 ore di esposizione, con o senza attivazione; tuttavia, un esposizione per 22 ore ha prodotto un aumento delle aberrazioni cromosomiche in tutte le concentrazioni testate. La tossicità genomica potenziale in vivo di florbetapir è stata valutata in uno studio sui micronuclei dei ratti. Con questo metodo, florbetapir non ha determinato un aumento del numero degli eritrociti policromatici micronucleati al più alto livello di dose ottenibile, 372 µg/kg/die somministrato due volte al giorno per 3 giorni consecutivi. Questa dose è circa 500 volte la dose umana massima e non ha mostrato evidenze di mutazioni geniche. Non sono stati effettuati studi su animali per valutare la cancerogenicità potenziale a lungo termine, la fertilità o gli effetti di florbetapir ( 18 F) sulla riproduzione. Non sono stati effettuati studi di tossicologia animale e sicurezza farmacologica con florbetapir ( 18 F). 10
11 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Etanolo assoluto Sodio ascorbato Sodio cloruro Acqua per preparazioni iniettabili 6.2 Incompatibilità In assenza di studi di compatibilità, questo medicinale non deve essere miscelato con altri medicinali. 6.3 Periodo di validità 7.5 ore dall ora di calibrazione 6.4 Precauzioni particolari per la conservazione Questo medicinale non richiede alcuna temperatura particolare di conservazione. Per le precauzioni di conservazione dopo la prima apertura, vedere il paragrafo 6.3. La conservazione dei radiofarmaci deve avvenire in conformità con le normative nazionali in materia di prodotti radioattivi. 6.5 Natura e contenuto del contenitore Amyvid è fornito in flaconcini trasparenti di vetro di Tipo I borosilicato da 10 ml o 15 ml con tappi di elastomero clorobutilico rivestito con FluroTec e ghiere di alluminio. Un flaconcino multidose della capacità di 10 ml contiene da 1 a 10 ml di soluzione, corrispondenti a MBq alla data e ora di calibrazione. Un flaconcino multidose della capacità di 15 ml contiene da 1 a 15 ml di soluzione, corrispondenti a MBq alla data e ora di calibrazione. A seguito delle differenze del processo di produzione, è possibile che i flaconcini di alcuni lotti di prodotto siano distribuiti con tappi di gomma forati. Ogni flaconcino è racchiuso in un contenitore schermato di spessore adeguato per minimizzare l esposizione alle radiazioni esterne. Confezione: 1 flaconcino. 6.6 Precauzioni particolari per lo smaltimento e la manipolazione Avvertenza generale: I radiofarmaci devono essere ricevuti, usati e somministrati solo da personale autorizzato all interno di apposite strutture cliniche. Il loro ricevimento, conservazione, uso, trasferimento e smaltimento sono soggetti alle norme e/o alle opportune autorizzazioni rilasciate dalle autorità competenti. I prodotti radiofarmaceutici devono essere preparati secondo modalità che soddisfino i requisiti sia in materia di sicurezza radiologica sia di qualità farmaceutica. Devono essere adottate precauzioni di asepsi appropriate. Se l integrità del flaconcino è compromessa, questo non deve essere usato. 11
12 Le procedure di somministrazione devono essere eseguite in modo da rendere minimo il rischio di contaminazione del prodotto medicinale e di irradiazione degli operatori. E obbligatoria un adeguata protezione. La somministrazione di radiofarmaci comporta rischi per altre persone (incluso il personale sanitario in stato di gravidanza) dovuti alla radiazione esterna o alla contaminazione per versamento di urine, vomito, etc. Pertanto devono essere adottate le dovute precauzioni di protezione dalle radiazioni in conformità con la normativa locale vigente. Il medicinale non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità alla normativa locale vigente. 7. TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO Eli Lilly Nederland B.V., Grootslag 1-5, NL-3991 RA Houten, Paesi Bassi 8. NUMERO(I) DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO EU/1/12/805/001 EU/1/12/805/ DATA DELLA PRIMA AUTORIZZAZIONE/RINNOVO DELL AUTORIZZAZIONE 14 gennaio DATA DI REVISIONE DEL TESTO 11. DOSIMETRIA Le dosi calcolate di radiazioni assorbite, da organi e tessuti, da un paziente adulto di corporatura media (70 kg) dopo la somministrazione di 370 MBq di florbetapir ( 18 F) usando i metodi standard per il calcolo della dosimetria (ICRP Volume 30) sono elencate nella tabella di seguito. Non sono state fatte assunzioni sullo svuotamento della vescica. 12
13 Dose assorbita per attività somministrata (µgy/mbq) Organo/tessuto Media Ghiandole surrenali 13,6 Cervello 10,0 Mammelle 6,2 Parete della colecisti 143,0 Parete dell intestino crasso inferiore 27,8 Intestino tenue 65,5 Parete dello stomaco 11,7 Parete dell intestino crasso superiore 74,4 Parete del cuore 12,7 Reni 13,0 Fegato 64,4 Polmoni 8,5 Muscoli 8,6 Ovaie 17,6 Pancreas 14,4 Midollo osseo 14,3 Cellule osteogeniche 27,6 Cute 5,9 Milza 8,9 Testicoli 6,8 Timo 7,3 Tiroide 6,8 Parete della vescica 27,1 Utero 15,6 Corpo in toto 11,6 a Dose Efficace [µsv/mbq] 18,6 a Coefficiente di qualità (Q) assunto pari a 1 per la conversione dalla dose assorbita alla dose efficace di 18 F. La dose efficace che risulta dalla somministrazione di una dose di 370 MBq per un adulto che pesa 70 kg è circa 7 msv. Se contemporaneamente viene eseguita una scansione TC come parte della procedura della PET, l esposizione alla radiazione ionizzante aumenterà in misura dipendente dalle impostazioni utilizzate per l acquisizione della TC. Per un attività somministrata di 370 MBq, la dose di radiazioni standard erogata all organo target (cervello) è 3,7 mgy. Per un attività somministrata di 370 MBq, le dosi di radiazioni standard erogate agli organi critici, colecisti, parete dell intestino crasso superiore, parete dell intestino crasso inferiore, intestino tenue e fegato sono state rispettivamente 53 mgy, 27,5 mgy, 10,3 mgy, 24,2 mgy e 23,8 mgy. 12. ISTRUZIONI PER LA PREPARAZIONE DI RADIOFARMACI Metodo di preparazione La confezione deve essere controllata prima dell uso e l attività misurata usando un calibratore di dose. I prelievi devono essere eseguiti in condizioni asettiche. I flaconcini non devono essere aperti prima di aver disinfettato il tappo, la soluzione deve essere prelevata attraverso il tappo utilizzando una siringa monodose dotata di un adeguata schermatura di protezione e un ago sterile monouso oppure utilizzando un sistema automatico di somministrazione autorizzato. Devono essere usate solamente siringhe di propilene/hdpe. Se l integrità del flaconcino è compromessa, il prodotto non deve essere usato. Amyvid può essere diluito in condizioni asettiche con una soluzione iniettabile di cloruro di sodio 9 mg/ml (0,9%) fino a una diluizione massima di 1:5. Il prodotto diluito deve essere usato entro 4 ore dalla diluizione. 13
14 Controllo qualità La soluzione deve essere controllata visivamente prima della somministrazione. Devono essere usate solo soluzioni limpide, senza particelle visibili. Informazioni più dettagliate su questo medicinale sono disponibili sul sito web della Agenzia europea dei medicinali: 14
15 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta. Vedere paragrafo 4.8 per informazioni sulle modalità di segnalazione delle reazioni avverse. 1. DENOMINAZIONE DEL MEDICINALE Amyvid 1900 MBq/ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml di soluzione iniettabile contiene 1900 MBq di florbetapir ( 18 F) alla data e ora di calibrazione (ToC, Time of Calibration). L attività per flaconcino varia da 1900 MBq a MBq alla data e ora di calibrazione. Il fluoro ( 18 F) decade in ossigeno stabile ( 18 O) con un emivita di circa 110 minuti emettendo una radiazione di positroni di 634 kev, seguita da radiazione da annichilazione fotonica di 511 kev. Eccipienti con effetti noti: Questo medicinale contiene 79 mg/ml di etanolo e fino a 37 mg di sodio. Per l elenco completo degli eccipienti, vedere paragrafo FORMA FARMACEUTICA Soluzione iniettabile. Soluzione limpida incolore. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Medicinale solo per uso diagnostico. Amyvid è un radiofarmaco indicato per rilevare con la tomografia ad emissione di positroni (PET) le immagini della densità delle placche neuritiche di β-amiloide nel cervello di pazienti adulti con decadimento cognitivo che vengono valutati per la malattia di Alzheimer (AD) e altre cause di decadimento cognitivo. Amyvid deve essere usato congiuntamente alla valutazione clinica. Una scansione negativa indica la presenza di poche placche o l assenza di placche, il che non è coerente con una diagnosi di AD. Per i limiti nell interpretazione di una scansione positiva vedere i paragrafi 4.4 e Posologia e modo di somministrazione Una scansione PET con florbetapir deve essere richiesta da medici con esperienza nella gestione clinica delle patologie neurodegenerative. Le immagini ottenute con Amyvid devono essere interpretate solo da valutatori che hanno effettuato un training su come interpretare le immagini della PET con florbetapir ( 18 F). Nei casi in cui con la scansione PET è difficile localizzare la sostanza grigia e il margine della sostanza bianca/grigia, si raccomanda un esame recente con tomografia computerizzata (TC) o con risonanza magnetica (RM), co-registrato con l esame PET, per ottenere un immagine combinata PET-TC o PET-RM (vedere il paragrafo 4.4 Interpretazione delle immagini). 15
16 Posologia L attività raccomandata per un adulto che pesa 70 kg è 370 MBq di florbetapir ( 18 F). Il volume dell iniezione non deve essere inferiore a 1 ml e non superare 10 ml. Popolazioni speciali Persone anziane Non è raccomandato un aggiustamento della dose in base all età. Insufficienza renale ed epatica E necessaria una valutazione attenta dell attività da somministrare perché in questi pazienti è possibile che l esposizione alle radiazioni risulti maggiore. Vedere il paragrafo 4.4. Non sono stati eseguiti studi estesi per determinare il range o l aggiustamento della dose con questo medicinale nelle popolazioni normali e speciali. Le farmacocinetiche di florbetapir ( 18 F) in pazienti con insufficienza renale o epatica non sono state caratterizzate. Popolazione pediatrica Non c è un uso rilevante di Amyvid nella popolazione pediatrica. Modo di somministrazione Per uso endovenoso. Per uso multidose. L attività di florbetapir ( 18 F) deve essere misurata con un calibratore di dose immediatamente prima dell iniezione. La dose è somministrata per iniezione endovenosa in bolo, seguita da un lavaggio con una soluzione iniettabile di cloruro di sodio 9 mg/ml (0,9%) per assicurare la somministrazione completa della dose. L iniezione di Amyvid attraverso un catetere endovenoso corto (approssimativamente di 4 cm o meno) minimizza il potenziale assorbimento del principio attivo da parte del catetere. L'iniezione di florbetapir ( 18 F) deve essere endovenosa per evitare l irradiazione dovuta a travaso locale, così come la rilevazione di immagini artefatte. Acquisizione delle immagini Un immagine PET di 10 minuti deve essere acquisita circa minuti dopo l iniezione endovenosa di Amyvid. I pazienti devono stare supini con la testa posizionata in modo tale da centrare il cervello, incluso il cervelletto, nel campo visivo dello scanner della PET. Per ridurre il movimento della testa possono essere impiegati un nastro o altri poggiatesta flessibili. La ricostruzione deve includere la correzione per l attenuazione per avere pixel transassiali delle dimensioni comprese tra 2,0 e 3,0 mm. 4.3 Controindicazioni Ipersensibilità al principio attivo o ad uno qualsiasi degli eccipienti elencati al paragrafo Avvertenze speciali e precauzioni di impiego Per ogni paziente l esposizione a radiazioni deve essere giustificata sulla base dei possibili benefici. Giustificazione di un rapporto beneficio/rischio individuale L attività somministrata deve, in ogni caso, essere la più bassa possibile per ottenere le informazioni diagnostiche richieste. 16
17 Insufficienza renale e insufficienza epatica Per questi pazienti è necessaria un attenta valutazione del rapporto beneficio/rischio poiché è possibile che l esposizione alle radiazioni risulti aumentata. Florbetapir ( 18 F) è escreto principalmente attraverso il sistema epatobiliare e per i pazienti con insufficienza epatica esiste la possibilità di un aumentata esposizione alle radiazioni. Vedere anche il paragrafo 4.2. Popolazione pediatrica Per informazioni sull uso nella popolazione pediatrica, vedere i paragrafi 4.2 o 5.1. Interpretazione delle immagini con Amyvid Le immagini con Amyvid devono essere interpretate solo da valutatori che hanno effettuato il training su come interpretare le immagini della PET con florbetapir ( 18 F). Una scansione negativa indica una densità scarsa o assente di placche neuritiche corticali di ß-amiloide. Una scansione positiva indica una densità da moderata a frequente. Sono stati osservati errori di interpretazione dell immagine nella valutazione della densità delle placche neuritiche cerebrali di β -amiloide, inclusi dei falsi negativi. La valutazione delle immagini deve essere eseguita principalmente nell orientamento transassiale e, quando necessario, anche sui piani sagittale e coronale. Si raccomanda che la valutazione delle immagini includa tutte le sezioni transassiali del cervello usando una scala in bianco e nero con l intensità massima della scala impostata alla massima intensità di pixel su tutto il cervello. L interpretazione dell immagine come negativa o positiva viene effettuata confrontando visivamente l attività della sostanza grigia corticale con l attività della sostanza bianca corticale adiacente (vedere la Figura 1). Scansioni negative hanno più attività nella sostanza bianca che nella sostanza grigia, creando un evidente contrasto grigia-bianca. Scansioni positive avranno: a) Due o più aree del cervello (ciascuna più larga di una singola circonvoluzione corticale) in cui il contrasto grigia-bianca è ridotto o assente. Questo è il modo in cui appare più comunemente una scansione positiva. b) Una o più aree in cui l attività della sostanza grigia è intensa e supera in modo evidente l attività della sostanza bianca adiacente. 17
18 Figura 1: Immagini PET con Amyvid che mostrano esempi di scansioni negative (le due righe in alto) e di scansioni positive (le due righe in basso). Le figure da sinistra a destra mostrano le immagini PET relative alla sezione sagittale, coronale e trasversale. L ultima figura a destra mostra l immagine ingrandita dell area del cervello evidenziata nel rettangolo. Le due frecce in alto indicano il normale contrasto grigia-bianca preservato con un attività corticale inferiore a quella della sostanza bianca adiacente. Le due frecce in basso indicano aree con un ridotto contrasto grigia-bianca e un aumentata attività corticale che è paragonabile all attività della sostanza bianca adiacente. Limitazioni di utilizzo Una scansione positiva non è sufficiente da sola a stabilire una diagnosi di AD o di un altro disturbo cognitivo poiché nei pazienti anziani asintomatici e in alcune demenze neurodegenerative (AD, demenza da corpi di Lewy, demenza da malattia di Parkinson) possono essere presenti depositi di placche neuritiche nella sostanza grigia. Per le limitazioni di utilizzo nei pazienti con deterioramento cognitivo lieve (MCI), vedere il paragrafo 5.1. L efficacia di Amyvid nel prevedere lo sviluppo di AD o monitorare la risposta alla terapia non è stata stabilita (vedere il paragrafo 5.1). Alcune scansioni possono essere di difficile interpretazione a causa del rumore di fondo dell immagine, della marcata atrofia con assottigliamento corticale o dell immagine sfocata che possono portare ad errori di interpretazione. Nei casi in cui è difficile individuare con le scansioni PET la sede della sostanza grigia e il margine della sostanza bianca/grigia, ed è disponibile un immagine recente di TC o di RM registrata 18
19 contemporaneamente all esame PET, chi effettua l interpretazione deve esaminare l immagine combinata della PET-TC o della PET-RM per chiarire la correlazione tra il reperto della PET e l anatomia della sostanza grigia. In alcuni casi è stata identificata un aumentata captazione in strutture extracerebrali quali le ghiandole salivali, la cute, i muscoli e le ossa (vedere il paragrafo 5.2). L esame delle immagini sagittali e le immagini della TC o della RM registrate contemporaneamente possono aiutare a distinguere l osso occipitale dalla sostanza grigia occipitale. Dopo l esame Nelle prime 24 ore successive all iniezione, il contatto ravvicinato con bambini e donne in gravidanza deve essere limitato. Avvertenze specifiche Il contenuto di sodio è superiore a 1 mmol (fino a 37 mg per dose). Questo deve essere tenuto in considerazione nei pazienti con una dieta a basso contenuto di sodio. Questo medicinale contiene 10 vol % di etanolo (alcol), cioè fino a 790 mg per dose, equivalenti a 20 ml di birra o 8 ml di vino per dose. Questa quantità può essere dannosa per chi soffre di alcolismo e ciò deve essere tenuto in considerazione nelle donne in gravidanza e che stanno allattando e nei gruppi ad alto rischio come i pazienti con malattia epatica o epilessia. 4.5 Interazioni con altri medicinali ed altre forme di interazione Non sono stati effettuati studi di interazione in vivo. Studi di legame in vitro non hanno mostrato interferenze del legame di florbetapir ( 18 F) alle placche di ß- amiloide in presenza degli altri medicinali comunemente assunti dai pazienti con AD. 4.6 Fertilità, gravidanza e allattamento Donne potenzialmente fertili Quando è prevista la somministrazione di radiofarmaci ad una donna potenzialmente fertile, è importante determinare se è o non è in stato di gravidanza. Ove non sia provato il contrario, qualsiasi donna che abbia saltato un ciclo mestruale deve essere considerata in stato di gravidanza. In caso di dubbi riguardo ad una possibile gravidanza (se la donna ha saltato un ciclo mestruale, se il ciclo mestruale è molto irregolare, etc.), devono essere proposte alla paziente tecniche alternative che non utilizzino radiazioni ionizzanti (qualora ve ne siano). Gravidanza Le metodiche che utilizzano radionuclidi impiegate su donne in stato di gravidanza generano radiazioni che coinvolgono il feto. Pertanto, durante la gravidanza devono essere eseguiti soltanto gli esami ritenuti essenziali, quando il probabile beneficio supera di gran lunga il rischio per la madre e per il feto. Non sono stati condotti studi nelle donne in stato di gravidanza. Non sono stati eseguiti studi negli animali per valutare gli effetti di florbetapir ( 18 F) sulla riproduzione (vedere il paragrafo 5.3). Non è noto se florbetapir ( Allattamento 18 F) sia escreto nel latte umano durante l allattamento. Prima della somministrazione di radiofarmaci a una madre che sta allattando al seno si deve valutare la possibilità di ritardare la somministrazione del radionuclide fino a quando la madre abbia terminato l allattamento al seno e considerare se sia stato scelto il radiofarmaco più appropriato tenendo presente l eliminazione di attività nel latte materno. Se la somministrazione è ritenuta necessaria, l allattamento deve essere interrotto per 24 ore e il latte prodotto deve essere eliminato. 19
20 Nelle prime 24 ore successive all iniezione, il contatto ravvicinato con bambini deve essere limitato. Fertilità Non sono stati effettuati studi sulla fertilità. 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Non pertinente. 4.8 Effetti indesiderati Riassunto del profilo di sicurezza Le reazioni avverse sono state raccolte negli studi clinici che hanno coinvolto 555 soggetti con 665 somministrazioni di Amyvid soluzione iniettabile. Non sono state riportate reazioni avverse gravi correlate alla somministrazione di Amyvid. Elenco delle reazioni avverse La frequenza è definita come molto comune ( 1/10), comune ( 1/100, <1/10), non comune ( 1/1.000, <1/100), raro ( 1/10.000, <1/1.000), molto raro (<1/10.000), non nota (la frequenza non può essere definita sulla base dei dati disponibili). Nella realtà le reazioni avverse potrebbero verificarsi con una frequenza anche inferiore a quella riportata di seguito, ma la dimensione del database da cui sono stati ottenuti i dati non ha permesso di assegnare le categorie di frequenza inferiore alla categoria non comune ( 1/1.000, <1/100). Patologie del sistema nervoso Comuni: cefalea Non comuni: disgeusia Patologie vascolari Non comuni: vampate di calore Patologie gastrointestinali Non comuni: nausea Patologie della cute e del tessuto sottocutaneo Non comuni: prurito, orticaria Patologie sistemiche e condizioni relative alla sede di somministrazione Non comuni: rash a livello del sito di infusione, reazione in corrispondenza del sito di iniezione (tra cui emorragia, irritazione e dolore). L'esposizione alle radiazioni ionizzanti è correlata all'induzione di cancro e al potenziale sviluppo di difetti ereditari. Poiché, quando viene somministrata l'attività raccomandata di 370 MBq di florbetapir ( 18 F), la dose efficace è 7 msv, queste reazioni avverse sono attese con una bassa probabilità. Segnalazione delle reazioni avverse sospette La segnalazione delle reazioni avverse sospette che si verificano dopo l autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione riportato nell Allegato V. 20
21 4.9 Sovradosaggio Data la piccola quantità di florbetapir ( 18 F) in ogni dose, il sovradosaggio non dovrebbe provocare effetti farmacologici. Nel caso di somministrazione di un sovradosaggio di radiazioni, la dose assorbita dal paziente deve essere ridotta se possibile aumentando l eliminazione del radionuclide dal corpo con una frequente minzione e defecazione. Potrebbe essere utile calcolare la dose efficace che è stata impiegata. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: radiofarmaceutici diagnostici, sistema nervoso centrale, Codice ATC: V09AX05. Meccanismo d azione Florbetapir ( 18 F) si lega alle placche neuritiche di ß-amiloide. Gli studi di legame che usano i tradizionali metodi di colorazione neuropatologica su cervelli con AD post-mortem hanno dimostrato una correlazione statisticamente significativa (p < ) tra il legame di florbetapir ( 18 F) in vitro e il deposito di aggregati ß- amiloidi. In vivo, la correlazione tra la captazione di florbetapir ( 18 F) nella sostanza grigia corticale e la quantità totale di ß-amiloide è stata valutata in pazienti in fin di vita usando l anticorpo anti-amiloide 4G8 che evidenzia la ß-amiloide trovata sia nelle placche neuritiche che diffuse. Il legame in vivo di florbetapir ( 18 F) ad altre strutture ß-amiloidi o ad altre strutture o recettori cerebrali rimane sconosciuto. Effetti farmacodinamici Alle basse concentrazioni chimiche presenti in Amyvid, florbetapir ( 18 F) non ha una attività farmacologica rilevabile. Negli studi clinici completati, la captazione di florbetapir ( 18 F) in 6 aree corticali predefinite del cervello (precuneo, frontale, cingolato anteriore, cingolato posteriore, parietale e temporale) è stata misurata quantitativamente usando come indice il valore di captazione standardizzato (SUV, Standardised Uptake Value). I rapporti medi dei SUV corticali (SUVR, relativi al cervelletto) sono più alti nei pazienti con AD rispetto a quelli dei soggetti volontari sani. I valori medi dei SUVR corticali rispetto a quelli cerebellari nei pazienti con AD mostrano sostanziali aumenti continui dal tempo zero nei 30 minuti dopo la somministrazione e successivamente, con solo delle piccole variazioni, fino a 90 minuti dopo la somministrazione. Non sono state notate differenze nei risultati in termini di SUVR nei soggetti che assumevano i comuni trattamenti per l AD rispetto a quelli che non li assumevano. Efficacia clinica E stato eseguito uno studio pivotal su 59 pazienti in fin di vita con l obiettivo di stabilire la performance diagnostica di Amyvid nel rilevare la densità delle placche neuritiche corticali (densità assente o scarsa vs densità moderata o frequente). I risultati della PET sono stati confrontati con la più alta densità di placche neuritiche misurata sulle sezioni della corteccia frontale, temporale o parietale di pazienti sottoposti ad autopsia nei 24 mesi successivi alla scansione PET. Non è stato possibile misurare in modo affidabile lo stato cognitivo dei soggetti. In tutti i 59 soggetti, la valutazione della PET in cieco da parte di 5 medici nucleari ha dato come risultato nella maggior parte dei casi una sensibilità di lettura del 92% (95% IC: 78-98%) e una specificità del 100% (95% IC: %). In uno studio su 47 volontari sani giovani (di età inferiore a 40 anni), che si presumeva essere privi di depositi ß-amiloidi, tutte le scansioni PET con Amyvid sono state negative. La sensibilità e la specificità di Amyvid nel rilevare la densità delle placche neuritiche corticali sono state ulteriormente valutate in due altri studi in cui differenti gruppi di valutatori hanno interpretato le immagini di alcuni soggetti poi sottoposti ad esame autoptico nello studio pivotal. I risultati di questi studi sono stati analoghi ai risultati ottenuti nello studio pivotal. La consistenza tra i valutatori, usando valori della kappa di Fleiss, variava da 0.75 a
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
Foglio illustrativo: informazioni per il paziente. Lyseen 4 mg compresse Lyseen 2 mg/ml soluzione iniettabile pridinolo mesilato
 Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
ESTRATTI, SUNTI E COMUNICATI
 ESTRATTI, SUNTI E COMUNICATI AGENZIA ITALIANA DEL FARMACO ModiÞ cazione dell autorizzazione all immisione in commercio, secondo procedura di mutuo riconoscimento, del medicinale «Multihance» Estratto determinazione
ESTRATTI, SUNTI E COMUNICATI AGENZIA ITALIANA DEL FARMACO ModiÞ cazione dell autorizzazione all immisione in commercio, secondo procedura di mutuo riconoscimento, del medicinale «Multihance» Estratto determinazione
Foglio illustrativo: informazioni per il paziente. ISORAM 4%, soluzione per infusione. Soluzione di aminoacidi
 Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
Foglio illustrativo: informazioni per l utilizzatore. Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato
 Foglio illustrativo: informazioni per l utilizzatore Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan.
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan. Legga attentamente questo foglio prima di usare questo medicinale. - Conservi questo
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan. Legga attentamente questo foglio prima di usare questo medicinale. - Conservi questo
Figura 1 Distrofia simpatico riflessa:
 I conografia Figura 1 istrofia simpatico riflessa: alterazioni radiografiche.,. Quest uomo di 65 anni ha presentato dolore e tumefazione alla mano dopo un lieve trauma. Nella prima radiografia () si rileva
I conografia Figura 1 istrofia simpatico riflessa: alterazioni radiografiche.,. Quest uomo di 65 anni ha presentato dolore e tumefazione alla mano dopo un lieve trauma. Nella prima radiografia () si rileva
IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare
 1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
FARMACOCINETICA 1. Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA
 FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
Foglio illustrativo: informazioni per il paziente. MAALOX 400 mg + 400 mg compresse masticabili. Magnesio idrossido + Alluminio ossido, idrato
 Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
2. P RIMA DI U TILIZZARE ASQUAM
 Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
CEFODIE Cefonicid. Categoria farmacoterapeutica Antibiotico iniettabile.
 Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
IDI FARMACEUTICI srl - Via dei Castelli Romani 83/85-00040 POMEZIA (Roma).
 ALOXIDIL 2% soluzione cutanea (Minoxidil) COMPOSIZIONE QUALI - QUANTITATIVA. L'ALOXIDIL è una soluzione contenente minoxidil, alla concentrazione del 2% (pari a 20 mg/ml) ed eccipienti costituiti da glicole
ALOXIDIL 2% soluzione cutanea (Minoxidil) COMPOSIZIONE QUALI - QUANTITATIVA. L'ALOXIDIL è una soluzione contenente minoxidil, alla concentrazione del 2% (pari a 20 mg/ml) ed eccipienti costituiti da glicole
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 (Foglio illustrativo) PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi
(Foglio illustrativo) PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi
Foglio illustrativo: informazioni per l utilizzatore. VFEND 50 mg compresse rivestite con film VFEND 200 mg compresse rivestite con film Voriconazolo
 Foglio illustrativo: informazioni per l utilizzatore VFEND 50 mg compresse rivestite con film VFEND 200 mg compresse rivestite con film Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per l utilizzatore VFEND 50 mg compresse rivestite con film VFEND 200 mg compresse rivestite con film Legga attentamente questo foglio prima di prendere questo medicinale
FENILCHETONURIA. Adattarsi ad una nuova realtà
 FENILCHETONURIA Adattarsi ad una nuova realtà 9 Che cosa è la fenilchetonuria? Per capire la fenilchetonuria bisogna partire dal concetto che tutti gli alimenti, in quantità variabile, contengono una sostanza
FENILCHETONURIA Adattarsi ad una nuova realtà 9 Che cosa è la fenilchetonuria? Per capire la fenilchetonuria bisogna partire dal concetto che tutti gli alimenti, in quantità variabile, contengono una sostanza
MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto
 MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto 01.0 DENOMINAZIONE DEL MEDICINALE MYCOSTATIN 100.000 UI/ML 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di sospensione orale contiene:
MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto 01.0 DENOMINAZIONE DEL MEDICINALE MYCOSTATIN 100.000 UI/ML 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di sospensione orale contiene:
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica
 Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 RINAZINA 100 mg/100 ml SPRAY NASALE, SOLUZIONE nafazolina Foglio illustrativo PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE
RINAZINA 100 mg/100 ml SPRAY NASALE, SOLUZIONE nafazolina Foglio illustrativo PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE
Ecografia. Rischio clinico nel processo di donazione, prelievo e trapianto di organi e tessuti. Perugia 8 ottobre 2013
 Perugia 8 ottobre 2013 Rischio clinico nel processo di donazione, prelievo e trapianto di organi e tessuti Ecografia Dr. Giancarlo Biscarini (1) Dr. Giulio Gambaracci (2) (1) Radiologia 1 Ospedale S.M.della
Perugia 8 ottobre 2013 Rischio clinico nel processo di donazione, prelievo e trapianto di organi e tessuti Ecografia Dr. Giancarlo Biscarini (1) Dr. Giulio Gambaracci (2) (1) Radiologia 1 Ospedale S.M.della
Foglio illustrativo: informazioni per il paziente. DIAZEPAM ALTER 5 mg/ml gocce orali, soluzione Diazepam. Medicinale Equivalente
 Foglio illustrativo: informazioni per il paziente DIAZEPAM ALTER 5 mg/ml gocce orali, soluzione Diazepam Medicinale Equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per il paziente DIAZEPAM ALTER 5 mg/ml gocce orali, soluzione Diazepam Medicinale Equivalente Legga attentamente questo foglio prima di prendere questo medicinale perché
Foglio illustrativo: informazioni per l utilizzatore. BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato
 Foglio illustrativo: informazioni per l utilizzatore BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato Medicinale equivalente Legga attentamente questo foglio prima di usare questo
Foglio illustrativo: informazioni per l utilizzatore BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato Medicinale equivalente Legga attentamente questo foglio prima di usare questo
Foglio illustrativo: Informazioni per l utilizzatore. Finasteride Ranbaxy 5 mg compresse rivestite con film. Medicinale equivalente
 Foglio illustrativo: Informazioni per l utilizzatore Finasteride Ranbaxy 5 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio illustrativo prima di usare questo medicinale
Foglio illustrativo: Informazioni per l utilizzatore Finasteride Ranbaxy 5 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio illustrativo prima di usare questo medicinale
Nota Informativa Importante. Guida alla Terapia per i Paziente. Guida alla Contraccezione. Modulo d'informazione e Consenso Informato
 AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
Bellavite sperimentazione Gelsemium. Scuola Omeopatia Classica Dulcamara - Faculty of Homeopathy of the United Kingdom
 Bellavite sperimentazione Gelsemium E stato pubblicato su Psychopharmacology 2010; [DOI 10.1007/s00213-010-1855-2], ad opera di Magnani P et al (Dipartimento di Patologia e Dipartimento di Medicina e Sanità
Bellavite sperimentazione Gelsemium E stato pubblicato su Psychopharmacology 2010; [DOI 10.1007/s00213-010-1855-2], ad opera di Magnani P et al (Dipartimento di Patologia e Dipartimento di Medicina e Sanità
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fluorodopa ( 18 F) CIS BIO 90 MBq/mL soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml contiene 90 MBq di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fluorodopa ( 18 F) CIS BIO 90 MBq/mL soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml contiene 90 MBq di
Imaging in vivo delle placche di ß-amiloide come marker preclinico di demenza. Lorenza Federici Università degli Studi di Brescia
 Imaging in vivo delle placche di ß-amiloide come marker preclinico di demenza Lorenza Federici Università degli Studi di Brescia Fondazione Guido Ber Il sottoscritto Lorenza Federici DICHIARA che, nell
Imaging in vivo delle placche di ß-amiloide come marker preclinico di demenza Lorenza Federici Università degli Studi di Brescia Fondazione Guido Ber Il sottoscritto Lorenza Federici DICHIARA che, nell
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinaleperché
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinaleperché
Concetti chiave. Se entro 2 settimane il dolore persiste invariato, senza progressivo miglioramento dei sintomi, è indicata una ulteriore valutazione
 Concetti chiave Il Mal di Schiena è una patologia frequente Lombalgia = irradiazione fino al ginocchio Lombosciatalgia = irradiazione sotto il ginocchio Si definisce Cronica dopo 4 settimane Demedicalizzare
Concetti chiave Il Mal di Schiena è una patologia frequente Lombalgia = irradiazione fino al ginocchio Lombosciatalgia = irradiazione sotto il ginocchio Si definisce Cronica dopo 4 settimane Demedicalizzare
La cefalea. Padova 14 febbraio 2014. Paola Mattiazzo
 La cefalea Padova 14 febbraio 2014 Paola Mattiazzo LA CEFALEA NELL AMBULATORIO DEL PEDIATRA DI BASE ANAMNESI APPROFONDITA E MIRATA ANAMNESI FAMILIARE FAMILIARITA PER CEFALEA FAMILIARITA PER ALTRE PATOLOGIE
La cefalea Padova 14 febbraio 2014 Paola Mattiazzo LA CEFALEA NELL AMBULATORIO DEL PEDIATRA DI BASE ANAMNESI APPROFONDITA E MIRATA ANAMNESI FAMILIARE FAMILIARITA PER CEFALEA FAMILIARITA PER ALTRE PATOLOGIE
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
Allegato 3/A Giudizi individuali sulla discussione dei titoli
 Allegato 3/A Giudizi individuali sulla discussione dei titoli CANDIDATO: BADOLATO RAFFAELE Il Candidato nel discutere le sue pubblicazioni ha esposto con precisione e chiarezza espositiva, con pertinenza
Allegato 3/A Giudizi individuali sulla discussione dei titoli CANDIDATO: BADOLATO RAFFAELE Il Candidato nel discutere le sue pubblicazioni ha esposto con precisione e chiarezza espositiva, con pertinenza
Circolare L-08-01 Valori diagnostici di riferimento (VDR) per esami medico-nucleari
 Pagina 1 / 11 Circolare L-08-01 Valori diagnostici di riferimento () per esami medico-nucleari 1. Finalità Si stabiliscono i valori diagnostici di riferimento () allo scopo di mettere a disposizione dei
Pagina 1 / 11 Circolare L-08-01 Valori diagnostici di riferimento () per esami medico-nucleari 1. Finalità Si stabiliscono i valori diagnostici di riferimento () allo scopo di mettere a disposizione dei
DOVE SIAMO: VID MEDICINSKI CENTER: Ul. Vinka Vodopivca 21, Kromberk, 5000 Nova Gorica ECOGRAFIA & MEDICINA INTERNA. Prenotazione
 MEDICINSKI CENTER ŠINIGOJ NOVA GORICA Centro medico Šinigoj Nova Gorica Sede: Kostanjeviška c.1, 5000 Nova Gorica DOVE SIAMO: VID MEDICINSKI CENTER: Ul. Vinka Vodopivca 21, Kromberk, 5000 Nova Gorica ECOGRAFIA
MEDICINSKI CENTER ŠINIGOJ NOVA GORICA Centro medico Šinigoj Nova Gorica Sede: Kostanjeviška c.1, 5000 Nova Gorica DOVE SIAMO: VID MEDICINSKI CENTER: Ul. Vinka Vodopivca 21, Kromberk, 5000 Nova Gorica ECOGRAFIA
MIASTENIA GRAVIS. l 80% Approssimativamente
 MIASTENIA GRAVIS La miastenia gravis è un disordine di origine immunologico che frequentemente esordisce determinando deficit della muscolatura legata all apparato apparato visivo (muscolatura oculare
MIASTENIA GRAVIS La miastenia gravis è un disordine di origine immunologico che frequentemente esordisce determinando deficit della muscolatura legata all apparato apparato visivo (muscolatura oculare
EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri
 26 febbraio 2016 EMA/137488/2016 EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri Più frequenti scansioni di Risonanza Magnetica
26 febbraio 2016 EMA/137488/2016 EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri Più frequenti scansioni di Risonanza Magnetica
Valutazione efficacia della terapia con campi magneto-elettrici ultradeboli ODONTOIATRIA. Risultati definitivi Marzo 2014
 Valutazione efficacia della terapia con campi magneto-elettrici ultradeboli ODONTOIATRIA Risultati definitivi Marzo 2014 1. Analisi descrittive sul campione Il campione è composto da 20 partecipanti, con
Valutazione efficacia della terapia con campi magneto-elettrici ultradeboli ODONTOIATRIA Risultati definitivi Marzo 2014 1. Analisi descrittive sul campione Il campione è composto da 20 partecipanti, con
Foglio illustrativo: informazioni per l utilizzatore. FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica
 Foglio illustrativo: informazioni per l utilizzatore FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica Legga attentamente questo foglio prima di usare questo medicinale
Foglio illustrativo: informazioni per l utilizzatore FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica Legga attentamente questo foglio prima di usare questo medicinale
Elettroencefalogramma
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Elettroencefalogramma 2/5/2006 Casa è? L elettroencefalogramma (EEG) corrisponde a variazioni dell attività elettrica cerebrale registrate
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Elettroencefalogramma 2/5/2006 Casa è? L elettroencefalogramma (EEG) corrisponde a variazioni dell attività elettrica cerebrale registrate
FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. CAREFINAST 1 mg compresse rivestite con film Finasteride
 FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE CAREFINAST 1 mg compresse rivestite con film Finasteride Legga attentamente questo foglio prima di usare questo medicinale poiché contiene informazioni
FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE CAREFINAST 1 mg compresse rivestite con film Finasteride Legga attentamente questo foglio prima di usare questo medicinale poiché contiene informazioni
UN CASO DI METASTASI DIGITALI DI CARCINOMA POLMONARE IN UN GATTO
 UN CASO DI METASTASI DIGITALI DI CARCINOMA POLMONARE IN UN GATTO Oncologia cutanea SIDEV - Cremona 17/10/2004 Elisa Antoniazzi, Voghera (PV) Walter Bertazzolo, Lodi Segnalamento ed anamnesi Cino, gatto,
UN CASO DI METASTASI DIGITALI DI CARCINOMA POLMONARE IN UN GATTO Oncologia cutanea SIDEV - Cremona 17/10/2004 Elisa Antoniazzi, Voghera (PV) Walter Bertazzolo, Lodi Segnalamento ed anamnesi Cino, gatto,
PROGRAMMA DELL INSEGNAMENTO MEDICINA DELLO SVILUPPO E RIABILITAZIONE(6 CFU)
 Corso di Laurea in PROGRAMMA DELL INSEGNAMENTO MEDICINA DELLO SVILUPPO E RIABILITAZIONE(6 CFU) AREA DI APPRENDIMENTO Al termine del corso, lo studente avrà acquisito conoscenze e capacità di comprensione
Corso di Laurea in PROGRAMMA DELL INSEGNAMENTO MEDICINA DELLO SVILUPPO E RIABILITAZIONE(6 CFU) AREA DI APPRENDIMENTO Al termine del corso, lo studente avrà acquisito conoscenze e capacità di comprensione
ASSISTENZA INFERMIERISTICA AL PAZIENTE CONTROPULSATO
 ASSISTENZA INFERMIERISTICA AL PAZIENTE CONTROPULSATO CPS infermiera AIROLDI BARBARA CPS infermiera MONICA ZANI CARDIOCHIRURGIA TERAPIA INTENSIVA AOU NOVARA NURSING DEL PZ CONTROPULSATO ASSISTENZA INFERMIERISTICA
ASSISTENZA INFERMIERISTICA AL PAZIENTE CONTROPULSATO CPS infermiera AIROLDI BARBARA CPS infermiera MONICA ZANI CARDIOCHIRURGIA TERAPIA INTENSIVA AOU NOVARA NURSING DEL PZ CONTROPULSATO ASSISTENZA INFERMIERISTICA
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005
 VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005 2005 VANTAGGI DELLA VIA ORALE! Le forme farmaceutiche orali sono facili e convenienti da usare
VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005 2005 VANTAGGI DELLA VIA ORALE! Le forme farmaceutiche orali sono facili e convenienti da usare
MALATTIE CISTICHE DEI RENI
 MALATTIE CISTICHE DEI RENI GENETICHE Autosomica dominante Reni policistici dell adulto Sclerosi tuberosa Malattia di von Hippel-Lindau Autosomica recessiva Reni policistici del bambino Nefroftisi giovanile
MALATTIE CISTICHE DEI RENI GENETICHE Autosomica dominante Reni policistici dell adulto Sclerosi tuberosa Malattia di von Hippel-Lindau Autosomica recessiva Reni policistici del bambino Nefroftisi giovanile
LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors)
 LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors) PERCHE QUESTA TERAPIA? Il corpo umano è fatto in modo di autodifendersi dai danni che possono colpirlo, e soprattutto
LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors) PERCHE QUESTA TERAPIA? Il corpo umano è fatto in modo di autodifendersi dai danni che possono colpirlo, e soprattutto
Indice. Parte prima Area legislativo-istituzionale. Parte seconda Area igienico-sanitaria e tecnico-operativa. L autrice XIII.
 L autrice Presentazione XIII XV Parte prima Area legislativo-istituzionale Capitolo 1 La nascita dell operatore socio-sanitario con formazione complementare in assistenza sanitaria 3 L operatore socio-sanitario
L autrice Presentazione XIII XV Parte prima Area legislativo-istituzionale Capitolo 1 La nascita dell operatore socio-sanitario con formazione complementare in assistenza sanitaria 3 L operatore socio-sanitario
Ecografia del surrene
 Ecografia del surrene Metodica di studio Anatomia ecografia Quadri patologici Congresso SIEMG Up-Date Vibo Valentia 01-03 maggio 2014 Visibilità ecografia Sonde convex multifrequenza 2-5 Mhz Surrene destro
Ecografia del surrene Metodica di studio Anatomia ecografia Quadri patologici Congresso SIEMG Up-Date Vibo Valentia 01-03 maggio 2014 Visibilità ecografia Sonde convex multifrequenza 2-5 Mhz Surrene destro
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE
 DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
DIPARTIMENTO ONCOLOGICO UNITA OPERATIVA SEMPLICE DI ONCOLOGIA RICHIESTA/CONSENSO INFORMATO PER INSERIMENTO DI PICC E MIDLINE Istruzioni per la compilazione Per la corretta esecuzione della manovra e per
 Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
Studio AMAROS SOMMARIO
 Studio AMAROS SOMMARIO Studio di fase III il cui principale obiettivo è dimostrare nelle pazienti con metastasi ai linfonodi ascellari, diagnosticate tramite biopsia con linfonodo sentinella, equivalente
Studio AMAROS SOMMARIO Studio di fase III il cui principale obiettivo è dimostrare nelle pazienti con metastasi ai linfonodi ascellari, diagnosticate tramite biopsia con linfonodo sentinella, equivalente
PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL
 PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: NOVEMBRE 2001 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 ELEMENTI IDENTIFICATIVI
PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: NOVEMBRE 2001 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 ELEMENTI IDENTIFICATIVI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC)
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC) 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: Rabipur 2,5 UI/ml, polvere e solvente per soluzioni iniettabili Vaccino rabico per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC) 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: Rabipur 2,5 UI/ml, polvere e solvente per soluzioni iniettabili Vaccino rabico per
Valutazione e pianificazione multidimensionale: meglio strumenti semplici o complessi?
 Valutazione e pianificazione multidimensionale: meglio strumenti semplici o complessi? Venerdì 9 Febbraio 206 L approccio alla persona con problemi di salute dipende sempre da tre dimensioni Dimensione
Valutazione e pianificazione multidimensionale: meglio strumenti semplici o complessi? Venerdì 9 Febbraio 206 L approccio alla persona con problemi di salute dipende sempre da tre dimensioni Dimensione
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore Docetaxel Dong-A 20 mg/1 ml Concentrato per soluzione per infusione Docetaxel Dong-A 80 mg/4 ml Concentrato per soluzione per infusione Medicinale Equivalente
Foglio illustrativo: informazioni per l utilizzatore Docetaxel Dong-A 20 mg/1 ml Concentrato per soluzione per infusione Docetaxel Dong-A 80 mg/4 ml Concentrato per soluzione per infusione Medicinale Equivalente
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO GLUSCAN 600MBq/mL Soluzione iniettabile, Fluorodesossiglucosio( 18 F).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO GLUSCAN 600MBq/mL Soluzione iniettabile, Fluorodesossiglucosio( 18 F). 1 DENOMINAZIONE DEL MEDICINALE GLUSCAN 600 MBq/ml soluzione iniettabile 2 COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO GLUSCAN 600MBq/mL Soluzione iniettabile, Fluorodesossiglucosio( 18 F). 1 DENOMINAZIONE DEL MEDICINALE GLUSCAN 600 MBq/ml soluzione iniettabile 2 COMPOSIZIONE
NEO BOROCILLINA GOLA DOLORE
 FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
Le malattie rare Efficacia, appropriatezza e sostenibilità
 Le malattie rare Efficacia, appropriatezza e sostenibilità Chiara Poggiani, Giovanna Scroccaro Coordinamento Regionale Unico sul Farmaco Regione del Veneto WORKSHOP - Farmaci Orfani e Malattie Rare Biblioteca
Le malattie rare Efficacia, appropriatezza e sostenibilità Chiara Poggiani, Giovanna Scroccaro Coordinamento Regionale Unico sul Farmaco Regione del Veneto WORKSHOP - Farmaci Orfani e Malattie Rare Biblioteca
RACCOMANDAZIONI PROCEDURALI. per l imaging oncologico con F-FDG PET/TC
 Associazione Italiana di Medicina Nucleare ed Imaging Molecolare RACCOMANDAZIONI PROCEDURALI per l imaging oncologico con 18 F-FDG PET/TC A cura del Gruppo di Studio PET Estensori: Alessandro Giordano,
Associazione Italiana di Medicina Nucleare ed Imaging Molecolare RACCOMANDAZIONI PROCEDURALI per l imaging oncologico con 18 F-FDG PET/TC A cura del Gruppo di Studio PET Estensori: Alessandro Giordano,
Andrea Stimamiglio IL PROBLEMA DEL DEFICIT COGNITIVO NEL MEZZO DELLE COMORBIDITA INTERNISTICHE
 Andrea Stimamiglio IL PROBLEMA DEL DEFICIT COGNITIVO NEL MEZZO DELLE COMORBIDITA INTERNISTICHE Comorbidità Con il termine di comorbidità si intende la presenza contemporanea nella stessa persona di più
Andrea Stimamiglio IL PROBLEMA DEL DEFICIT COGNITIVO NEL MEZZO DELLE COMORBIDITA INTERNISTICHE Comorbidità Con il termine di comorbidità si intende la presenza contemporanea nella stessa persona di più
Foglio illustrativo: informazioni per il paziente. Cormeto 250 mg capsule Metirapone
 FOGLIO ILLUSTRATIVO Foglio illustrativo: informazioni per il paziente Cormeto 250 mg capsule Metirapone Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
FOGLIO ILLUSTRATIVO Foglio illustrativo: informazioni per il paziente Cormeto 250 mg capsule Metirapone Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
Studio delle placche di amiloide mediante traccianti Florurati
 Studio delle placche di amiloide mediante traccianti Florurati Premessa: Sono disponibili in Europa, e lo saranno nei prossimi mesi anche in Italia, diversi radiofarmaci fluorurati che hanno dimostrato
Studio delle placche di amiloide mediante traccianti Florurati Premessa: Sono disponibili in Europa, e lo saranno nei prossimi mesi anche in Italia, diversi radiofarmaci fluorurati che hanno dimostrato
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Cuprymina 925 MBq/mL precursore radiofarmaceutico, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Cuprymina 925 MBq/mL precursore radiofarmaceutico, soluzione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di
Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare
 Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare Gli unici test a domicilio per la pianificazione familiare Test di ovulazione Test precoce di gravidanza Test di gravidanza
Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare Gli unici test a domicilio per la pianificazione familiare Test di ovulazione Test precoce di gravidanza Test di gravidanza
RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ruconest 2100 U polvere per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ruconest 2100 U polvere per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
+39.02.8917987 +39.02.89179837 +39.335.8134772
 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETA 1.1. Elementi identificativi del preparato Nome del preparato 1.2. Elementi identificativi della Società Società produttrice: Rappresentante esclusivo
1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETA 1.1. Elementi identificativi del preparato Nome del preparato 1.2. Elementi identificativi della Società Società produttrice: Rappresentante esclusivo
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO THYMOVAR; 15 g strisce per alveare per api mellifere. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una striscia per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO THYMOVAR; 15 g strisce per alveare per api mellifere. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una striscia per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fluodeossiglucosio ( 18 F )-IBA 185 MBq/ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml contiene 185
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fluodeossiglucosio ( 18 F )-IBA 185 MBq/ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml contiene 185
TEST GENETICI PAZIENTI e FAMIGLIARI
 TUMORE OVARICO: NELLA GENETICA IL FUTURO DELLA PREVENZIONE E DELLA CURA TEST GENETICI PAZIENTI e FAMIGLIARI Siranoush Manoukian Unità di Genetica Medica Fondazione IRCCS Istituto Nazionale dei Tumori Milano,
TUMORE OVARICO: NELLA GENETICA IL FUTURO DELLA PREVENZIONE E DELLA CURA TEST GENETICI PAZIENTI e FAMIGLIARI Siranoush Manoukian Unità di Genetica Medica Fondazione IRCCS Istituto Nazionale dei Tumori Milano,
Divisione riduzionale: meiosi
 Anomalie genetiche Divisione riduzionale: meiosi Nelle ovaie, con la meiosi si generano 4 nuclei da ogni ovogonio ma uno solo diventerà cellula-uovo mentre gli altri tre degenerano. Nei testicoli ogni
Anomalie genetiche Divisione riduzionale: meiosi Nelle ovaie, con la meiosi si generano 4 nuclei da ogni ovogonio ma uno solo diventerà cellula-uovo mentre gli altri tre degenerano. Nei testicoli ogni
Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3
 giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Il besilesomab è un anticorpo monoclonale anti-granulociti (BW 250/183) prodotto nelle cellule murine.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Scintimun 1 mg kit per preparazione radiofarmaceutica 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun flaconcino di Scintimun
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Scintimun 1 mg kit per preparazione radiofarmaceutica 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun flaconcino di Scintimun
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Alla data di riferimento, ciascun flacone contiene da 2 a 4 GBq di Samario.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Quadramet 1,3 GBq/ml soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun ml di soluzione contiene 1,3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Quadramet 1,3 GBq/ml soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascun ml di soluzione contiene 1,3
Il Sistema Nervoso. Immagini Invito alla Natura - Paravia SCIENZE NATURALI SCUOLA SECONDARIA DI 1 GRADO DOCENTE - ALICE DE SIMONE
 Il Sistema Nervoso Immagini Invito alla Natura - Paravia SCIENZE NATURALI SCUOLA SECONDARIA DI 1 GRADO DOCENTE - ALICE DE SIMONE NEURONI 10 MILIARDI? 100 Miliardi? Terra Luna 380.000 Km NEURONI I messaggi
Il Sistema Nervoso Immagini Invito alla Natura - Paravia SCIENZE NATURALI SCUOLA SECONDARIA DI 1 GRADO DOCENTE - ALICE DE SIMONE NEURONI 10 MILIARDI? 100 Miliardi? Terra Luna 380.000 Km NEURONI I messaggi
N:B. I puntali applicatori/miscelatori sono monouso.
 1. CARATTERISTICHE GENERALI Il gel sbiancante BY X tra 38% è utilizzato per sbiancare denti con discromie. Il gel viene applicato direttamente sui denti. Secondo la direttiva Medical Devices 93/42/CEE
1. CARATTERISTICHE GENERALI Il gel sbiancante BY X tra 38% è utilizzato per sbiancare denti con discromie. Il gel viene applicato direttamente sui denti. Secondo la direttiva Medical Devices 93/42/CEE
INCONTINENZA URINARIA
 Università degli Studi di Padova Facoltà di Medicina e Chirurgia Corso di Laurea in Infermieristica Infermieristica Clinica in Aree Specialistiche Docente Dott. Fabris Pietro INCONTINENZA URINARIA Perdita
Università degli Studi di Padova Facoltà di Medicina e Chirurgia Corso di Laurea in Infermieristica Infermieristica Clinica in Aree Specialistiche Docente Dott. Fabris Pietro INCONTINENZA URINARIA Perdita
UNIVERSITA DEGLI STUDI DI CASSINO
 UNIVERSITA DEGLI STUDI DI CASSINO FACOLTA DI INGEGNERIA Corso di laurea in ingegneria meccanica Modulo didattico Sicurezza degli impianti industriali Seminario Il documento di valutazione dei rischi (Ing.
UNIVERSITA DEGLI STUDI DI CASSINO FACOLTA DI INGEGNERIA Corso di laurea in ingegneria meccanica Modulo didattico Sicurezza degli impianti industriali Seminario Il documento di valutazione dei rischi (Ing.
GUIDA ALLA PRENOTAZIONE DEGLI ESAMI RADIOLOGICI ECOGRAFIA ED ECOCOLOR-DOPPLER
 Provincia religiosa di San Pietro dell Ordine Ospedaliero di San Giovanni di Dio FATEBENEFRATELLI Ospedale Buccheri La Ferla Via Messina Marine 197, 90123 Palermo U.O.C. di Radiodiagnostica: Direttore
Provincia religiosa di San Pietro dell Ordine Ospedaliero di San Giovanni di Dio FATEBENEFRATELLI Ospedale Buccheri La Ferla Via Messina Marine 197, 90123 Palermo U.O.C. di Radiodiagnostica: Direttore
Valutazione clinico-diagnostica delle lesioni ossee
 Valutazione clinico-diagnostica delle lesioni ossee Incontro AIRO LAM 22/10/2012 Dott. Maurizio Carcaterra U.O. RADIOTERAPIA Ospedale Belcolle Viterbo 1 introduzione Le ossa sono la sede più comune di
Valutazione clinico-diagnostica delle lesioni ossee Incontro AIRO LAM 22/10/2012 Dott. Maurizio Carcaterra U.O. RADIOTERAPIA Ospedale Belcolle Viterbo 1 introduzione Le ossa sono la sede più comune di
I pazienti con diabete di tipo 1 sono in gran parte giovani, ma sono una piccola minoranza rispetto al totale. La maggior parte dei diabetici,
 DIABETE Per quali pazienti diabetici è indicato il trapianto di rene? I pazienti diabetici più comunemente inseriti in lista di trapianto renale sono quelli in cui il diabete è dovuto a un'insufficiente
DIABETE Per quali pazienti diabetici è indicato il trapianto di rene? I pazienti diabetici più comunemente inseriti in lista di trapianto renale sono quelli in cui il diabete è dovuto a un'insufficiente
Lezione del 24 Ottobre 2014
 MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
Foglio illustrativo: informazioni per il paziente e l utilizzatore
 Foglio illustrativo: informazioni per il paziente e l utilizzatore CUROSURF 80 mg/ml SOSPENSIONE PER INSTILLAZIONE ENDOTRACHEOBRONCHIALE frazione fosfolipidica da polmone suino Legga attentamente questo
Foglio illustrativo: informazioni per il paziente e l utilizzatore CUROSURF 80 mg/ml SOSPENSIONE PER INSTILLAZIONE ENDOTRACHEOBRONCHIALE frazione fosfolipidica da polmone suino Legga attentamente questo
Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole e fontanelle cittadine.
 Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
Primi Sintomi della Meningite
 Cosa è la Meningite? La meningite è un gonfiore delle membrane del cervello e del midollo spinale. Può essere a causa di virale, fungina o infezione batterica. La causa più comune di meningite è un'infezione
Cosa è la Meningite? La meningite è un gonfiore delle membrane del cervello e del midollo spinale. Può essere a causa di virale, fungina o infezione batterica. La causa più comune di meningite è un'infezione
Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE
 Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE PNEUMOVAX, soluzione iniettabile in flaconcino Vaccino pneumococcico polisaccaridico 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE PNEUMOVAX, soluzione iniettabile in flaconcino Vaccino pneumococcico polisaccaridico 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale
 Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale Gozzo Endemico - Prevalenza superiore al 5% in una popolazione di bambini - di età compresa tra i 6 e i 12 anni Gozzo Sporadico
Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale Gozzo Endemico - Prevalenza superiore al 5% in una popolazione di bambini - di età compresa tra i 6 e i 12 anni Gozzo Sporadico
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Policlinico di Monza Istituto ad Alta Specializzazione NEVI E CAPELLI. La tecnologia VIDIX VTRACK a servizio del dermatologo
 Policlinico di Monza Istituto ad Alta Specializzazione NEVI E CAPELLI La tecnologia VIDIX VTRACK a servizio del dermatologo INTRODUZIONE Da diversi anni si registra l'aumento dei casi di melanoma, un tumore
Policlinico di Monza Istituto ad Alta Specializzazione NEVI E CAPELLI La tecnologia VIDIX VTRACK a servizio del dermatologo INTRODUZIONE Da diversi anni si registra l'aumento dei casi di melanoma, un tumore
Epatite infettiva del cane (Malattia di Rubarth, Rubarth 1947)
 Epatite infettiva del cane (Malattia di Rubarth, Rubarth 1947) Causata dall adenovirus canino tipo (CAdV1) antigenicamente correlato all adenovirus canino tipo 2 (CAdV2) responsabile di infezioni respiratorie
Epatite infettiva del cane (Malattia di Rubarth, Rubarth 1947) Causata dall adenovirus canino tipo (CAdV1) antigenicamente correlato all adenovirus canino tipo 2 (CAdV2) responsabile di infezioni respiratorie
Encefalo. Protocollo d esame RM
 Encefalo Protocollo d esame RM Queste diapositive fanno parte di un corso completo e sono a cura dello staff di rm-online.it E vietata la riproduzione anche parziale Cenni Anatomici Cenni Anatomici Cenni
Encefalo Protocollo d esame RM Queste diapositive fanno parte di un corso completo e sono a cura dello staff di rm-online.it E vietata la riproduzione anche parziale Cenni Anatomici Cenni Anatomici Cenni
velum wls DATASHEET Rilevatore di Movimento Doppia Tecnologia a Tenda per esterno con antimascheramento Wireless 868 Mhz Bi-Direzionale KSI5402010.
 velum wls Rilevatore di Movimento Doppia Tecnologia a Tenda per esterno con antimascheramento Wireless 868 Mhz Bi-Direzionale KSI540200.303 CARATTERISTICHE PRINCIPALI I I rilevatori di movimento velum
velum wls Rilevatore di Movimento Doppia Tecnologia a Tenda per esterno con antimascheramento Wireless 868 Mhz Bi-Direzionale KSI540200.303 CARATTERISTICHE PRINCIPALI I I rilevatori di movimento velum
Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi
 Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi Legga attentamente questo foglio prima di prendere questo medicinale perchè
Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi Legga attentamente questo foglio prima di prendere questo medicinale perchè
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO STRONGHOLD 15 mg soluzione per spot-on STRONGHOLD 30 mg soluzione per spot-on STRONGHOLD 45 mg soluzione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO STRONGHOLD 15 mg soluzione per spot-on STRONGHOLD 30 mg soluzione per spot-on STRONGHOLD 45 mg soluzione
M. Marengo. GENERATORI DI 99 Mo/ 99m Tc : CARATTERISTICHE E CONTROLLO DI QUALITÀ.
 M. Marengo GENERATORI DI 99 Mo/ 99m Tc : CARATTERISTICHE E CONTROLLO DI QUALITÀ. Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna. mario.marengo@unibo.it Equazione di Bateman
M. Marengo GENERATORI DI 99 Mo/ 99m Tc : CARATTERISTICHE E CONTROLLO DI QUALITÀ. Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna. mario.marengo@unibo.it Equazione di Bateman
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Yttriga precursore radiofarmaceutico, soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Yttriga precursore radiofarmaceutico, soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml di
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE LYRICA 25 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 25 mg di pregabalin.
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE LYRICA 25 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 25 mg di pregabalin.
Percorso di gestione primo - secondo livello per. LUTS/Ipertrofia Prostatica Benigna
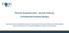 Percorso di gestione primo - secondo livello per LUTS/Ipertrofia Prostatica Benigna Tratto dalle conclusioni del Dipartimento Urologia, IV Congresso della Corte di giustizia Popolare per il Diritto alla
Percorso di gestione primo - secondo livello per LUTS/Ipertrofia Prostatica Benigna Tratto dalle conclusioni del Dipartimento Urologia, IV Congresso della Corte di giustizia Popolare per il Diritto alla
Torino, 19 ottobre 2011
 WORKSHOP Risultati del Programma Regionale di Screening Colorettale Aggiornamenti Protocollo Regionale Sono indicati: Test emocoagulativi? Profilassi antibiotica? Arrigo Arrigoni S.C.GASTROENTEROLOGIA
WORKSHOP Risultati del Programma Regionale di Screening Colorettale Aggiornamenti Protocollo Regionale Sono indicati: Test emocoagulativi? Profilassi antibiotica? Arrigo Arrigoni S.C.GASTROENTEROLOGIA
