Soluzioni degli esercizi del testo
|
|
|
- Leonardo Vitale
- 5 anni fa
- Visualizzazioni
Transcript
1 Klein, Il racconto della chimica Soluzioni degli esercizi del testo Lavorare con le mappe Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. Conoscenze e abilità 1. A 2. B 3. B 4. D 5. A 6. B 7. D 8. B 9. A 10. C 11. nucleo, probabilità 12. maggiore, quanto, differenza 13. livello, principale, interi 14. distanza, volume, energia 15. sottolivelli, secondario, interi da 0, n distanza, energia, forma
2 0, un, sferica 1, 3, bilobata 2, 5, plurilobata 3, 7, plurilobata 17. orientazione, energia, distanza, energia, volume 18. sottolivelli, energetici, crescente, esclusione, due, opposto, paralleli 19. elio, sei, pieni 20. più, precede, due, più, precede, meno, segue 21. V 22. F 23. F 24. V 25. V 26. V 27. V 28. F 29. V 30. V 31. V 32. V 33. a. 4s: n = 4; l =0 b. 2p: n = 2; l =1 c. 4f: n = 4; l =3 34. orbitali: 4; sottolivelli: orbitali: 16; sottolivelli: p, 1d, 2d 37. 4p, 4d, 4f (livello n = 4) 5s, 5f (livello n = 5) 38. 1s e 3s energia, volume = livello (n = 3), p = sottolivello (l = 1) 1 = numero di elettroni che occupano orbitali 3p = livello (n = 3), s = sottolivello (l = 0) 1 = numero di elettroni che occupano orbitali 3s 43. a. Si: 1s 2 2s 2 2p 6 3s 2 3p 2 o [Ne] 3s 2 3p 2 b. Cl: 1s 2 2s 2 2p 6 3s 2 3p 5 o [Ne] 3s 2 3p 5 c. Ca: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 o [Ar] 4s 2 d. Fe: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 o [Ar] 4s 2 3d 6 e. As: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 3 o [Ar] 4s 2 3d 10 4p 3 f. Ce: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 1 5d 1 o [Xe] 6s 2 4f 1 5d 1 Klein, Il racconto della chimica Zanichelli
3 g. U: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 3 6d 1 o [Rn] 7s 2 5f 3 6d a. Ba (Z = 56) manca il 6 in 6s 2 b. K (Z = 19) c. Br (Z = 35) d. N (Z = 7) e. Ar (Z = 18) f. Cd (Z = 48) 45. a. Ca 2+ : 1s 2 2s 2 2p 6 3s 2 3p 6 o [Ar] b. Na + : 1s 2 2s 2 2p 6 o [Ne] c. Cu + : 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 o [Ar] 3d 10 d. Cl : 1s 2 2s 2 2p 6 3s 2 3p 6 o [Ar] e. Br : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 o [Kr] f. S 2 : 1s 2 2s 2 2p 6 3s 2 3p 6 o [Ar] 46. a. Si, Z = 14: 1s 2 2s 2 2p 6 3s 2 3p 2 o [Ne] 3s 2 3p 2 b. Br, Z = 35: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 o [Kr] c. Fe 3+, Z = 26: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3 o [Ar] 4s 2 3d 3 d. Zn 2+, Z = 30: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 o [Ar] 3d 10 e. F, Z = 9: 1s 2 2s 2 2p 6 o [Ne] f. O 2, Z = 8: 1s 2 2s 2 2p 6 o [Ne] g. Ba 2+, Z = 26: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 o [Xe] 47. a. F b. E c. E d. F e. F f. E 48. a. Cs, Z = 55 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 1 o [Xe] 6s 1 b. Te, Z = 52 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 4 o [Kr] 5s 2 4d 10 5p 4 c. Al, Z = 13 1s 2 2s 2 2p 6 3s 2 3p 1 o [Ne] 3s 2 3p 1 d. C, Z = 6 1s 2 2s 2 2p 2 o [He] 2s 2 2p 2 e. Co, Z = 27 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7 o [Ar] 4s 2 3d 7 f. I, Z = 53 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 5 o [Kr] 5s 2 4d 10 5p 5 g. O, Z = 8 1s 2 2s 2 2p 4 o [He] 2s 2 2p 4 h. Li, Z = 3 1s 2 2s 1 o [He] 2s Fluoro e bromo appartengono al gruppo VIIA. In entrambi il sottolivello a più alta energia occupato è di tipo p con 5 elettroni. F: 1s 2 2s 2 2p 5 o [He]2s 2 2p 5 Br: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5 o [Ar]4s 2 3d 10 4p 5 Quindi in entrambi aggiungendo un elettrone si raggiunge la configurazione elettronica del gas nobile che li segue: F : 1s 2 2s 2 2p 6 o [Ne] Br : 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 o [Kr] 50. Klein, Il racconto della chimica Zanichelli
4 Il fluoro appartiene al secondo periodo e gli orbitali occupati a più alta energia appartengono al livello n = 2. Tutti gli orbitali occupati sono di tipo s o p. Il bromo appartiene al quarto periodo e gli orbitali occupati a più alta energia appartengono al livello n = 4. Gli orbitali occupati sono di tipo s, p, d. In particolare, il bromo ha un sottolivello 3d completamente riempito (3d 10 ) che scherma il nucleo, cioè gli elettroni 4p risentono di una forza attrattiva minore rispetto ai 2p del fluoro. Infatti il fluoro è molto elettronegativo (tende facilmente ad acquistare un elettroni in più) mentre il bromo lo è molto meno. 51. Il sodio e il potassio appartengono al primo gruppo. In entrambi il sottolivello a più alta energia occupato è di tipo s con un elettrone. Na: 1s 2 2s 2 2p 6 3s 1 o [Ne] 3s 1 K: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 o [Ar] 4s 1 Entrambi gli atomi perdendo un elettrone raggiungono la configurazione elettronica del gas nobile che li precede. Na + : 1s 2 2s 2 2p 6 o [Ne] K + : 1s 2 2s 2 2p 6 3s 2 3p 6 o [Ar] 52. Il sodio appartiene al terzo periodo e gli orbitali occupati a più alta energia appartengono al livello n = 3. Il potassio appartiene al quarto periodo e gli orbitali occupati a più alta energia appartengono al livello n = 4. Questi elettroni sono relativamente meno legati al nucleo, quindi il potassio ha dimensioni maggiori ed elettronegatività leggermente più bassa rispetto al sodio. 53. K 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 o [Ar] 4s 1 Fe 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 o [Ar] 4s 2 3d 6 Br 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5 o [Ar] 4s 2 3d 10 4p 5 Tutti e tre appartengono al 4 periodo e gli orbitali occupati a con numero quantico principale piu hanno n=4 (in tutti la configurazione interna è quella di Ar). 54. S 2 1s 2 2s 2 2p 6 3s 2 3p 6 Cl 1s 2 2s 2 2p 6 3s 2 3p 6 Ar 1s 2 2s 2 2p 6 3s 2 3p 6 Oppure Ar 1s 2 2s 2 2p 6 3s 2 3p 6 K + 1s 2 2s 2 2p 6 3s 2 3p 6 Ca 2+ 1s 2 2s 2 2p 6 3s 2 3p a. I, Cs +, Ba 2+ b. S 2, Cl, K +, Ca 2+ c. Li +, Be 2+ d. Se 2, Br, Rb +, Sr 2+ e. Ag, In +, Sn 2+, Sb a. All the elements of the 5 th period: Rb, Sr, Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd, In, Sn, Sb, Te, I, Xe. b. All the elements of the 3 rd period: Na, Mg, Al, Si, P, S, Cl, Ar. c. All the elements of the 7 th period, included the actinides: Fr, Ra, Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn, Nh, Fl, Mc, Lv, Ts, Og. d. All the elements of the 2 nd period: Li, Be, B, C, N, O, F, Ne. e. All the elements of the 4 th period: K, Ca, Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Ga, Ge, As, Se, Br, Kr. Klein, Il racconto della chimica Zanichelli
5 57. a. All the elements of the I group: H, Li, Na, K, Rb, Cs, Fr. b. All the noble gases, except He: Ne, Ar, Kr, Xe, Rn, Og. c. All the elements of the VIA group: O, S, Se, Te, Po, Lv. 58. a. O: 1s 2 2s 2 2p 4 b. Ti: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 c. Se: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 4 d. Si: 1s 2 2s 2 2p 6 3s 2 3p 2 e. Xe: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 Klein, Il racconto della chimica Zanichelli
6 Il laboratorio delle competenze 59. Nella teoria di Dalton: La materia è formata da atomi, particelle non ulteriormente divisibili che non si creano né si distruggono. Ciascun elemento è formato da atomi tutti di identica massa (è infatti la massa dell atomo a definire di quale elemento si tratta). Gli atomi partecipano interi alle reazioni chimiche. Ciò significa che in ciascun composto, dove atomi di elementi diversi sono combinati insieme, il rapporto tra il numero di atomi di ciascun elemento è sempre lo stesso ed è espresso da numeri interi; anche il rapporto tra le masse di ciascun elemento è costante. Nel modello quantistico: Gli atomi non sono indivisibili, ma sono formati da particelle più piccole. Inoltre atomi di un elemento possono trasformarsi in atomi di un altro elemento attraverso reazioni nucleari. Non è vero che ciascun elemento è formato da atomi tutti di identica massa, perché ciò che caratterizza l elemento è il numero di protoni contenuti in ciascuno dei suoi atomi. La massa dell atomo è determinata anche dal numero di neutroni. Atomi con stesso numero di protoni (Z) ma diverso numero di neutroni (A Z) sono isotopi dello stesso elemento. Si può comunque definire una massa media degli atomi di un dato elemento. Rimane vero che la massa di un atomo resta invariata durante una reazione chimica, perché ciò che si modifica è la distribuzione degli elettroni (che hanno massa trascurabile rispetto ai nuclei). Si può quindi continuare a considerare che in ciascun composto, dove atomi di elementi diversi sono combinati insieme, il rapporto tra il numero di atomi di ciascun elemento è sempre lo stesso ed è espresso da numeri interi. Il rapporto tra le masse è costante se ci si riferisce alla massa media degli atomi di ogni elemento (scritta sulla tavola periodica). 60. Nel modello di Thomson: Gli atomi sono composti da una massa compatta avente carica elettrica positiva e da elettroni, dotati di una carica negativa tale da bilanciare la carica positiva del nucleo. Gli elettroni sono molto più mobili della massa positiva e possono staccarsi dall atomo sotto effetto di un forte campo elettrico. Gli elettroni hanno tutti la stessa massa e la stessa carica, per qualunque atomo di qualunque elemento. Nel modello quantistico: Gli atomi sono composti da un nucleo carico positivamente, e come nel modello di Thomson da elettroni carichi negativamente che compensano la carica positiva. Come nel modello di Thomson, gli elettroni sono molto più mobili del nucleo. Hanno infatti massa migliaia di volte più piccola del nucleo, e possono staccarsi dal campo elettrico del nucleo per effetto di un forte campo elettrico o di luce UV oppure durante una reazione chimica. Come nel modello di Thomson, gli elettroni hanno tutti stessa massa e stessa carica, per qualunque atomo di qualunque elemento. 61. In Bohr model: Atom s mass is concentrated in the nucleus and the electrons are very distant from it. The diameter of the nucleus is times smaller than the diameter of the whole atom. Electrons rotate very fast around the nucleus on circular orbit. Klein, Il racconto della chimica Zanichelli
7 The diameter of electron s orbits can have only certain values. There is a specific energy amount of the electron for each of these values: as bigger is the diameter, as higher is the energy. When the electron is in its ground state, it doesn t receive neither emit energy, so it remains on its orbit for an indefinite period. If the electron receives a certain quantity of energy (in the form of heat or light), it can jump on a bigger orbit (excited state). Then it returns to the ground state emanating energy. In quantum model: Like in Bohr model, atom s mass is concentrated in the nucleus and the electrons are very distant from it. The diameter of the nucleus is times smaller than the diameter of the whole atom. Like in Bohr model, electrons rotate very fast around the nucleus, but it doesn t rotate on circular orbits. Electrons move in orbitals that can be described through maps of probability to find the electron. The energy and the volume of the orbitals are quantized, rather they can assume only defined values like in Bohr model. In quantum model, also the shape of the orbitals depends on a quantum number. Like in Bohr model each electron remains on its orbital (ground state) for an indefinite period, if it doesn t receive neither emit energy. If the electron receives a certain quantity of energy (in the form of heat or light), it can jump on a bigger orbit (excited state). Then it returns to the ground state emanating energy. 62. Il modello quantistico riesce a spiegare l interazione tra luce e materia, in particolare gli spettri di assorbimento e di emissione delle sostanze: i materiali assorbono la luce alle frequenze che corrispondono ai salti di energia tra livelli energetici permessi (uno o più elettroni passano dallo stato stazionario a stati eccitati); materiali i cui atomi sono stati portati a stati eccitati (attraverso assorbimento di luce o di una sufficiente quantità di calore) emettono luce alle frequenze che corrispondono ai salti di energia tra livelli energetici permessi (uno o più elettroni tornano allo stato fondamentale). Il modello di Rutherford non spiegava questo fenomeno perché non prevedeva quali sono le energie degli elettroni e le loro distanze dal nucleo, né che fossero quantizzate cioè che potessero assumere solo certi valori permessi. 63. Bohr model can t explain the emission spectrum of atoms with more than one electron (that is the atoms of all the elements, except H). In quantum model electron occupy quantized orbitals following certain rules (Aufbau principle, Pauli principle, Hund s rule). This model can explain the emission spectrum of all the elements and all the compounds. Quantum model can also explain the chemical behavior of the elements, and the similarity and the trend of a lot of properties along the groups and the period in the periodic table. 64. Open-ended answer. 65. Risposta aperta. L elio è il secondo l elemento in ordine di abbondanza in tutto l Universo osservabile, dove la sua percentuale in massa è 24%, contro 73,9 % per H e 1% per tutti gli altri elementi. L argon è il gas nobile più abbondante nell atmosfera e nella crosta terrestre. Nell atmosfera è due volte più abbondante di H 2 O e 23 volte più abbondante di CO NaCl Na (I gruppo) ha configurazione elettronica 1s 2 2s 2 2p 6 3s 1 che si può scrivere anche [Ne] 3s 1, quindi tende a perdere un elettrone per raggiungere la configurazione elettronica, particolarmente stabile, del gas nobile che lo precede (Ne). Forma quindi facilmente ioni Klein, Il racconto della chimica Zanichelli
8 Na +. Cl (gruppo VIIA) ha configurazione elettronica 1s 2 2s 2 2p 6 3s 2 3p 5 ovvero [Ne] 3s 2 3p 5 quindi tende ad acquistare un elettrone per raggiungere la configurazione elettronica, particolarmente stabile, del gas nobile che lo segue (Ar). Forma quindi facilmente ioni Cl. Gli ioni Na + (con configurazione elettronica di Ne) e Cl (con configurazione elettronica di Ar) formano tra loro un legame ionico in proporzione 1:1, bilanciando così le loro cariche. MgCl 2 Mg (II gruppo) ha configurazione elettronica 1s 2 2s 2 2p 6 3s 2 ovvero [Ne] 3s 2, quindi tende a perdere due elettroni per raggiungere la configurazione elettronica, particolarmente stabile, del gas nobile che lo precede (Ne). Forma quindi facilmente ioni Mg 2+. Cl (gruppo VIIA) ha configurazione elettronica 1s 2 2s 2 2p 6 3s 2 3p 5 ovvero [Ne] 3s 2 3p 5 quindi tende ad acquistare un elettrone per raggiungere la configurazione elettronica, particolarmente stabile, del gas nobile che lo segue (Ar). Forma quindi facilmente ioni Cl. Gli ioni Mg 2+ (con configurazione elettronica di Ne) e Cl - (con configurazione elettronica di Ar) formano tra loro un legame ionico in proporzione 1:2, bilanciando così le loro cariche. Klein, Il racconto della chimica Zanichelli
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s...
 1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 5. Il degli elementi SEGUI LA MAPPA B C N O F e Ne Na K Mg Ca Sc Ti V Cr Mn Fe Co
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 5. Il degli elementi SEGUI LA MAPPA B C N O F e Ne Na K Mg Ca Sc Ti V Cr Mn Fe Co
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Esperto prof. C. Formica
 Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Massa atomica. Unità di massa atomica: 1/12 della massa del 12 C
 Massa atomica Unità di massa atomica: 1/12 della massa del 12 C Il peso atomico, o più correttamente la massa atomica dei vari elementi si riporta sotto forma di una media ponderata tra i vari isotopi
Massa atomica Unità di massa atomica: 1/12 della massa del 12 C Il peso atomico, o più correttamente la massa atomica dei vari elementi si riporta sotto forma di una media ponderata tra i vari isotopi
Elettronica II Legame covalente e bande di energia nei solidi p. 2
 Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Come si dispongono gli elettroni negli atomi
 Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Il sistema periodico degli elementi
 Il sistema periodico degli elementi Gli elementi mostrano una variazione progressiva delle proprietà chimiche; dopo un definito numero di elementi, le medesime proprietà si ripetono con deboli variazioni
Il sistema periodico degli elementi Gli elementi mostrano una variazione progressiva delle proprietà chimiche; dopo un definito numero di elementi, le medesime proprietà si ripetono con deboli variazioni
tavola periodica Tale disposizione tabulare degli elementi è nota come Da tale disposizione venne elaborata la legge periodica che affermava che:
 Nel 1869 i chimici Dimitri Ivanovich Mendeleev e Julius Lothar Meyer, indipendentemente, trovarono che, ordinando gli elementi in ordine di peso atomico e disponendoli in file orizzontali una sopra l'altra,
Nel 1869 i chimici Dimitri Ivanovich Mendeleev e Julius Lothar Meyer, indipendentemente, trovarono che, ordinando gli elementi in ordine di peso atomico e disponendoli in file orizzontali una sopra l'altra,
Sommario delle lezione 3. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Distribuzione degli elettroni negli orbitali atomici Aufbau
 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
PERIODI VIIB IXB VIB VIIIB
 1 2 3 4 IA IIA PERIODI incasellati in ordine di numero atomico Z crescente in file ORIZZONTALI andando a capo quando inizia il riempimento di un nuovo livello energetico IB IIB IIIB IVB VB VIB VIIIB VIIB
1 2 3 4 IA IIA PERIODI incasellati in ordine di numero atomico Z crescente in file ORIZZONTALI andando a capo quando inizia il riempimento di un nuovo livello energetico IB IIB IIIB IVB VB VIB VIIIB VIIB
L ATOMO: CONFIGURAZIONE ELETTRONICA
 L ATOMO: CONFIGURAZIONE ELETTRONICA 2 L ATOMO DA DEMOCRITO A RUTHERFORD Democrito nel IV secolo a. C. Dalton Thomson nel 1803 nel 1900 nel 1911 Rutherford Bohr nel 1913 La distribuzione degli elettroni
L ATOMO: CONFIGURAZIONE ELETTRONICA 2 L ATOMO DA DEMOCRITO A RUTHERFORD Democrito nel IV secolo a. C. Dalton Thomson nel 1803 nel 1900 nel 1911 Rutherford Bohr nel 1913 La distribuzione degli elettroni
Sommario delle lezione 3. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Verifiche di primo livello: conoscenze
 SUL LIBRO DA PAG 233 A PAG 236 Verifiche di primo livello: conoscenze La moderna teoria atomica e la tavola periodica NEL SITO: 20 esercizi interattivi 1. Quanti e quali sono i numeri quantici? 4: n -
SUL LIBRO DA PAG 233 A PAG 236 Verifiche di primo livello: conoscenze La moderna teoria atomica e la tavola periodica NEL SITO: 20 esercizi interattivi 1. Quanti e quali sono i numeri quantici? 4: n -
Soluzioni degli esercizi del testo
 Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. Conoscenze e abilità 1. C 2. B 3.
Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. Conoscenze e abilità 1. C 2. B 3.
La struttura dell atomo
 La struttura dell atomo raggi catodici (elettroni) raggi canale (ioni positivi) Modello di Thomson Atomo come una piccola sfera omogenea carica di elettricità positiva, nella quale sono dispersi gli elettroni,
La struttura dell atomo raggi catodici (elettroni) raggi canale (ioni positivi) Modello di Thomson Atomo come una piccola sfera omogenea carica di elettricità positiva, nella quale sono dispersi gli elettroni,
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Corso di CHIMICA LEZIONE 3
 Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Elettronica I Introduzione ai semiconduttori
 Elettronica I Introduzione ai semiconduttori Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/ liberali
Elettronica I Introduzione ai semiconduttori Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/ liberali
Capitolo 11 I legami chimici
 Capitolo 11 I legami chimici ai capito? pag. 55 a4, b3, c1, d Mg deve perdere elettroni per assumere la configurazione di Ne e ogni atomo di cloro può acquistare solo 1 elettrone. Ba + Ba + + ; Ba pag.
Capitolo 11 I legami chimici ai capito? pag. 55 a4, b3, c1, d Mg deve perdere elettroni per assumere la configurazione di Ne e ogni atomo di cloro può acquistare solo 1 elettrone. Ba + Ba + + ; Ba pag.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica Esperimento di Thomson elettrone Si ottenne il rapporto carica/massa. Con l esperimento di Millikan venne determinato il valore della carica. Esperimento di Rutherford
Struttura elettronica e tavola periodica Esperimento di Thomson elettrone Si ottenne il rapporto carica/massa. Con l esperimento di Millikan venne determinato il valore della carica. Esperimento di Rutherford
Il legame chimico. Lezioni 17-20
 Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.
 Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org, ncbi.gov Gruppo
Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org, ncbi.gov Gruppo
Unbowed, Unbent, Unbroken
 Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Ad esempio se la distanza di legame in una molecola di Br 2 (Br-Br) è uguale a 2,286 Å allora si assume che il raggio atomico del Br sia 1,14 Å
 RAGGIO ATOMICO Molte delle proprietà degli elementi sono correlati alla struttura elettronica che, a sua volta, determina la loro collocazione nella tavola periodica Un atomo non ha un confine ben delineato
RAGGIO ATOMICO Molte delle proprietà degli elementi sono correlati alla struttura elettronica che, a sua volta, determina la loro collocazione nella tavola periodica Un atomo non ha un confine ben delineato
A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME
 A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
A DIPARTIMENTO DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA Primo parziale 29 Aprile 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
La rappresentazione degli orbitali Orbitali s ( l = 0 )
 Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
Capitolo 2: Gli Atomi e la Teoria Atomica
 Capitolo 2: Gli Atomi e la Teoria Atomica Prime Scoperte Lavoisier 1774 Proust 1799 Dalton 1803-1808 La Legge di Conservazione della Massa Legge della Composizione Costante Teoria Atomica La Teoria Atomica
Capitolo 2: Gli Atomi e la Teoria Atomica Prime Scoperte Lavoisier 1774 Proust 1799 Dalton 1803-1808 La Legge di Conservazione della Massa Legge della Composizione Costante Teoria Atomica La Teoria Atomica
Tavola periodica. Periodo = riga. Gruppo = colonna:
 Periodo = riga Tavola periodica gli eleenti appartenenti ad uno stesso periodo hanno nuero atoico (e quindi nuero di elettroni) crescente da sinistra verso destra, fino a riepiento di uno strato caratterizzato
Periodo = riga Tavola periodica gli eleenti appartenenti ad uno stesso periodo hanno nuero atoico (e quindi nuero di elettroni) crescente da sinistra verso destra, fino a riepiento di uno strato caratterizzato
Configurazioni elettroniche e tavola periodica
 Configurazioni elettroniche e tavola periodica Ritorniamo ora al riempimento successivo dei sottostrati fra gli elementi finora considerati, l'elio He ed il neon Ne hanno gli strati n=1 e n=2 completi
Configurazioni elettroniche e tavola periodica Ritorniamo ora al riempimento successivo dei sottostrati fra gli elementi finora considerati, l'elio He ed il neon Ne hanno gli strati n=1 e n=2 completi
orbitali d Kr Rb At Ra
 Tavola Periodica Lo schema complessivo della tavola periodica fu scoperto dal chimico russo Mendeleev nel 1869. Ordinò gli elementi in gruppi e periodi secondo i valori crescenti del loro peso atomico
Tavola Periodica Lo schema complessivo della tavola periodica fu scoperto dal chimico russo Mendeleev nel 1869. Ordinò gli elementi in gruppi e periodi secondo i valori crescenti del loro peso atomico
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2
 ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
Orbitali atomici. (1s ) < (2s < 2p) < ( 3s < 3p) < ( 4s < 3d < 4p) < ( 5s < 4d < 5p) < ( 6s <4f < 5d < 6p)
 Orbitali atomici Schema di successione dei livelli energetici degli orbitali la cui progressiva saturazione determina la configurazione elettronica degli elementi nel loro stato fondamentale (non in scala).
Orbitali atomici Schema di successione dei livelli energetici degli orbitali la cui progressiva saturazione determina la configurazione elettronica degli elementi nel loro stato fondamentale (non in scala).
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
COME CALCOLARE I NUMERI DI OSSIDAZIONE
 COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
CHIMICA: studio della struttura e delle trasformazioni della materia
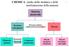 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Sommario della lezione 7. Misure di concentrazione. Nomenclatura
 Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
26/10/2012. Onde elettromagnetiche. b) proprietà periodiche C) configurazione elettronica. f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν
 Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
CARICA EFFICACE Z eff = Z - S
 RAPPRESENTAZIONE SCHEMATICA ENERGIA RELATIVA ORBITALI E 3s 2s 1s 3p 2p 3d 3s 2s 1s 3p 2p 3d 3s 2s 3p 2p 3d IDROGENO (Z = 1) LITIO (Z = 3) 1s POTASSIO (Z = 19) Per Z = 1 (atomo di idrogeno: monoelettronico)
RAPPRESENTAZIONE SCHEMATICA ENERGIA RELATIVA ORBITALI E 3s 2s 1s 3p 2p 3d 3s 2s 1s 3p 2p 3d 3s 2s 3p 2p 3d IDROGENO (Z = 1) LITIO (Z = 3) 1s POTASSIO (Z = 19) Per Z = 1 (atomo di idrogeno: monoelettronico)
Comunicazioni Docente - Studenti
 Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 24 Giugno 2015
 A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 24 Giugno 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 24 Giugno 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
SEZIONE II PRATICHE CON MACCHINE RADIOGENE
 ALLEGATO I DETERMINAZIONE DELLE CONDIZIONI DI APPLICAZIONE DELLE DISPOSIZIONI DEL PRESENTE DECRETO PER LE MATERIE RADIOATTIVE E PER LE MACCHINE RADIOGENE. 0. Criteri di non rilevanza radiologica delle
ALLEGATO I DETERMINAZIONE DELLE CONDIZIONI DI APPLICAZIONE DELLE DISPOSIZIONI DEL PRESENTE DECRETO PER LE MATERIE RADIOATTIVE E PER LE MACCHINE RADIOGENE. 0. Criteri di non rilevanza radiologica delle
Come sono disposti gli elettroni intorno al nucleo in un atomo?
 Come sono disposti gli elettroni intorno al nucleo in un atomo? La natura ondulatoria della radiazione elettromagnetica e della luce La luce è una radiazione elettromagnetica che si muove nello spazio
Come sono disposti gli elettroni intorno al nucleo in un atomo? La natura ondulatoria della radiazione elettromagnetica e della luce La luce è una radiazione elettromagnetica che si muove nello spazio
A DIPARTIMENTO DI FARMACIA CORSO DI CHIMICA GENERALE ED INORGANICA Compito scritto 22 Settembre 2015
 A DIPARTIMENTO DI FARMACIA CORSO DI CHIMICA GENERALE ED INORGANICA Compito scritto 22 Settembre 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle risposte esatte
A DIPARTIMENTO DI FARMACIA CORSO DI CHIMICA GENERALE ED INORGANICA Compito scritto 22 Settembre 2015 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle risposte esatte
ATOMICO RAGGIO IONICO ENERGIA DI IONIZZAZZIONE AFFINITA ELETTRONICA
 TAVOLA PERIODICA La tavola periodica può servire a prevedere un ampio campo di proprietà alcune delle quali decisive ai fini della comprensione della chimica Varie sono le proprietà che in modo periodico
TAVOLA PERIODICA La tavola periodica può servire a prevedere un ampio campo di proprietà alcune delle quali decisive ai fini della comprensione della chimica Varie sono le proprietà che in modo periodico
Sommario delle lezioni 2 e 3. Materia e definizioni. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezioni 2 e 3 Materia e definizioni Struttura dell atomo Configurazione elettronica La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e
Sommario delle lezioni 2 e 3 Materia e definizioni Struttura dell atomo Configurazione elettronica La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e
U.M.A. e le masse ATOMICHE
 U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
Principio dell Aufbau (riempimento)
 LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica Teoria atomica della materia Teoria atomica di Dalton 1.Ciascun elemento è composto da particelle estremamente piccole chiamate atomi. 2.Tutti gli atomi di un dato
Struttura elettronica e tavola periodica Teoria atomica della materia Teoria atomica di Dalton 1.Ciascun elemento è composto da particelle estremamente piccole chiamate atomi. 2.Tutti gli atomi di un dato
Atomi, Molecole e Ioni Lezione 2
 2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
Nuove connessioni aritmetiche tra i numeri magici degli elementi chimici più stabili, i livelli energetici nei gas nobili ed i numeri di Fibonacci
 Nuove connessioni aritmetiche tra i numeri magici degli elementi chimici più stabili, i livelli energetici nei gas nobili ed i numeri di Fibonacci Francesco Di Noto, Michele Nardelli Abstract In this paper
Nuove connessioni aritmetiche tra i numeri magici degli elementi chimici più stabili, i livelli energetici nei gas nobili ed i numeri di Fibonacci Francesco Di Noto, Michele Nardelli Abstract In this paper
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Quesiti e problemi (sul libro da pag. 214)
 Quesiti e problemi (sul libro da pag. 214) 1 La classificazione degli elementi 1 Wolfgang Dobereiner fu il primo scienziato a tentare una classificazione degli elementi. In che cosa consisteva? Quali vantaggi
Quesiti e problemi (sul libro da pag. 214) 1 La classificazione degli elementi 1 Wolfgang Dobereiner fu il primo scienziato a tentare una classificazione degli elementi. In che cosa consisteva? Quali vantaggi
Lezione 2. Atomi, Molecole e Ioni
 2018 Lezione 2. Atomi, Molecole e Ioni Teoria Atomica di Dalton (1808) 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici.
2018 Lezione 2. Atomi, Molecole e Ioni Teoria Atomica di Dalton (1808) 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici.
LA STRUTTURA DELL ATOMO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
ALLEGATO I SEZIONE I PRATICHE CON MATERIE RADIOATTIVE
 ALLEGATO I DETERMINAZIONE DELLE CONDIZIONI DI APPLICAZIONE DELLE DISPOSIZIONI DEL PRESENTE DECRETO PER LE MATERIE RADIOATTIVE E PER LE MACCHINE RADIOGENE. 0. Criteri di non rilevanza radiologica delle
ALLEGATO I DETERMINAZIONE DELLE CONDIZIONI DI APPLICAZIONE DELLE DISPOSIZIONI DEL PRESENTE DECRETO PER LE MATERIE RADIOATTIVE E PER LE MACCHINE RADIOGENE. 0. Criteri di non rilevanza radiologica delle
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Soluzioni degli esercizi del testo
 Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. 5. L elettronegatività è la capacità
Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. 5. L elettronegatività è la capacità
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
L atomo di Bohr. Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913)
 L atomo di Bohr Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913) L atomo di Bohr L atomo di idrogeno presenta un solo elettrone 1. L elettrone
L atomo di Bohr Per spiegare il mistero delle righe spettrali, Bohr propose un Modello Atomico dell Atomo di Idrogeno (1913) L atomo di Bohr L atomo di idrogeno presenta un solo elettrone 1. L elettrone
I gas nobili esistono (solo) allo stato di gas monoatomico
 I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
A Z. L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone. +1e e.
 L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
L'atomo Entità subatomiche Carica elettrica Massa (u.m.a) Protone Neutrone elettrone +1e 0-1e e = Carica elettrica elementare 1.60 10-19 u.m.a.= Unità di Massa Atomica 1.6605 10-4 Il Nuclide A Z Nu Coulomb
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014
 A FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
A FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
GENERALITA SUI LEGAMI CHIMICI
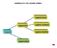 GENERALITA SUI LEGAMI IMII Legame ionico Legami forti Legame covalente Legami Legame metallico Legami deboli 1 Regola dell ottetto (Lewis,, 1916) Lewis: rappresentazione elettroni di valenza con punti
GENERALITA SUI LEGAMI IMII Legame ionico Legami forti Legame covalente Legami Legame metallico Legami deboli 1 Regola dell ottetto (Lewis,, 1916) Lewis: rappresentazione elettroni di valenza con punti
COMPORTAMENTO DUALISTICO della MATERIA
 COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
mvr = n h e 2 r = m v 2 e m r v = La configurazione elettronica r = e 2 m v 2 (1) Quantizzazione del momento angolare (2) 4 πε.
 La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
ISOTOPI. STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso.
 ISOTOPI STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso. Il nucleo atomico è costituito da PROTONI,, che hanno una carica elettrica positiva, e da NEUTRONI,,
ISOTOPI STRUTTURA DELL ATOMO Gli atomi sono costituiti da un nucleo e da. che si muovono intorno ad esso. Il nucleo atomico è costituito da PROTONI,, che hanno una carica elettrica positiva, e da NEUTRONI,,
DISSOLUZIONE DEL CLORURO DI SODIO
 DISSOLUZIONE DEL CLORURO DI SODIO Nel processo di dissoluzione del NaCl le molecole di acqua dipolari attraggono gli ioni del sale, indebolendo l attrazione elettrostatica tra Na + e Cl -. Inizialmente
DISSOLUZIONE DEL CLORURO DI SODIO Nel processo di dissoluzione del NaCl le molecole di acqua dipolari attraggono gli ioni del sale, indebolendo l attrazione elettrostatica tra Na + e Cl -. Inizialmente
GLI ELEMENTI CHIMICI
 I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
M M n+ + n e - X + n e - X n-
 IL LEGAME IONICO 1 Il legame ionico Descrizione generale La formazione di NaCl La valenza ionica L energia reticolare: definizione e esempio di calcolo Proprietà dei solidi ionici Il legame ionico si realizza
IL LEGAME IONICO 1 Il legame ionico Descrizione generale La formazione di NaCl La valenza ionica L energia reticolare: definizione e esempio di calcolo Proprietà dei solidi ionici Il legame ionico si realizza
ψ = Il carbonio (Z=6) - 2 elettroni equivalenti nello stato 2p - la funzione d onda globale deve essere antisimmetrica tripletto di spin, S=1
 s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
LEZIONE 2. Configurazioni elettroniche e tavola periodica
 LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
Elettronica I Introduzione ai semiconduttori. Programma Parte 6
 Elettronica I Introduzione ai semiconduttori Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: valentino.liberali@unimi.it http://www.dti.unimi.it/
Elettronica I Introduzione ai semiconduttori Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: valentino.liberali@unimi.it http://www.dti.unimi.it/
DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015
 A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015 COGNOME NOME MATRICOLA Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
A DIPARTIMENTO DI FARMACIA C.d.S. in Farmacia CHIMICA GENERALE ED INORGANICA Secondo Parziale - 19 Giugno 2015 COGNOME NOME MATRICOLA Segnare con una crocetta la risposta (una sola) che si ritiene esatta.
Gli argomenti trattati
 LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
ARGOMENTO: Cenni di Fisica del Nucleo
 UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
UNIVERSITA DEGLI STUDI DI GENOVA C.L. TECNICHE DIAGNOSTICHE RADIOLOGICHE CORSO INTEGRATO: MISURE ELETTRICHE ED ELETTRONICHE MATERIA: FISICA APPLICATA 2 (2 anno 1 sem) ARGOMENTO: Cenni di Fisica del Nucleo
Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton)
 Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Atomi 16 Si arrivò a dimostrare l esistenza di una forma elementare della materia (atomo) solo nel 1803 (John Dalton) 17 Teoria atomica di Dalton Si basa sui seguenti postulati: 1. La materia è formata
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
STRUTTURA DELL ATOMO
 STRUTTURA DELL ATOMO TEORIA ATOMICA ANTICA ATOMI = particelle unitarie indivisibili Democrito (400 a.c.) TEORIA ATOMICA MODERNA J. Dalton (1808) - atomi = particelle definite e indivisibili - atomi di
STRUTTURA DELL ATOMO TEORIA ATOMICA ANTICA ATOMI = particelle unitarie indivisibili Democrito (400 a.c.) TEORIA ATOMICA MODERNA J. Dalton (1808) - atomi = particelle definite e indivisibili - atomi di
