CAPITOLO 2 ATOMI POLIELETTRONICI E TAVOLA PERIODICA
|
|
|
- Agnolo Damiano
- 7 anni fa
- Visualizzazioni
Transcript
1 CAPITOLO ATOMI POLIELETTRONICI E TAVOLA PERIODICA. (a) non è corretto poichè il numero quantico magnetico m l può avere solo valori interi. (c) non è corretto poichè il massimo valore per il numero quantico secondario l è n. (e) non è corretto poichè il numero quantico di spin m s può avere solo valori ½ e -½..3 L orbitale s con il metodo SCF di Hartree del Berillio è meno diffuso (più piccolo) di quello del litio poichè il berillio ha numero atomico quattro e quindi quattro protoni nel nucleo mentre il litio ha solo tre protoni nel nucleo. L aumentato numero di protoni nel nucleo aumenta l attrazione elettrostatica coulombiana fra elettroni e nucleo. Il metodo SCF tiene in considerazione la repulsione elettrone-elettrone, che rende gli orbitali mediamente più estesi. Siccome la carica del nucleo è la stessa per i due orbitali e la sola differenza è la repulsione interelettronica, gli orbitali s SCF del litio dovrebbero essere un po più estesi di quelli idrogenoidi. (si veda la Figura.).5 Siccome il numero atomico è dispari, è impossibile che tutti gli elettroni siano accoppiati. L elemento è paramagnetico.7 Le configurazioni elettroniche degli elementi sono: (a) N: s s p 3 tre elettroni di tipo p. (b) Si: s s p 6 3s 3p sei elettroni di tipo s. (c) S: s s p 6 3s 3p 4 non ci sono elettroni di tipo d..9 Le configurazioni elettroniche per lo stato fondamentale del Se è: [Ar]4s 3d 0 4p 4.. B: s s p As: [Ar]4s 3d 0 4p 3 V: [Ar]4s 3d 3 I: [Kr]5s 4d 0 5p 5 Ni: [Ar]4s 3d 8 Au: [Xe]6s 4f 4 5d 0 Qual è il significato di [Ar]? di [Kr]? di [Xe]?.3 Ci sono elettroni: Orbitale n l m l m s s s 0 0 s s 0 0 p + p p 0 + p 0 p + Brian B. Laird, Chimica Generale Copyright 00 The McGraw-Hill Companies S.r.l., Publishing Group Italia
2 CAPITOLO : ATOMI POLIELETTRONICI E TAVOLA PERIODICA p 3s s L elemento è il magnesio..5 A causa della regola di Hund ci sono più elementi paramagnetici che diamagnetici. Ci sono tanti elementi a numero atomico pari quanti dispari. Tutti gli elementi a numero dispari di elettroni sono paramagnetici poichè hanno almeno un elettrone disaccoppiato. Alcuni elementi a numero pari di elettroni sono paramagnetici a causa della regola di Hund..7 (a) s s p 5 (alogeno) (b) s s p 6 3s 3p 6 4s (metallo alcalino terroso) (c) s s p 6 3s 3p 6 4s 3d 6 (metallo di transizione) (d) s s p 6 3s 3p 6 4s 3d 0 4p 3 (Gruppo 5A).9 Si tratta di un metallo di transizione. Si ricordi che negli ioni dei metalli di transizione gli orbitali (n )d sono più stabili dell orbitale ns. Quindi quando si forma un catione da un metallo di transizione, gli elettroni vengono rimossi sempre prima dall orbitale ns e poi se necessario dagli orbitali (n )d. Siccome il catione ha carica +3, sono stati tolti 3 elettroni d. Siccome il sotto livello 4s è meno stabile del 3d, due elettroni sono stati tolti dal 4s e uno dal 3d. La configurazione elettronica dell atomo neutro è [Ar]4s 3d 6. Questa è la configurazione elettronica del ferro.. Sc 3+ [Ar] Cu + [Ar]3d 0 Ti 4+ [Ar] Ag + [Kr]4d 0 V 5+ [Ar] Au + [Xe]4f 4 5d 0 Cr 3+ [Ar]3d 3 Au 3+ [Xe] 4f 4 5d 8 Mn + [Ar]3d 5 Pt + [Xe] 4f 4 5d 8.3 Isoelettronici significa che le specie hanno lo stesso numero di elettroni e la stessa configurazione elettronica. Be + e He ( e ) F e N 3 (0 e ) Fe + e Co 3+ (4 e ) S e Ar (8 e ).5 (a) Ti: [Ar] 4s 3d V + : [Ar] 4s 3d 3 (b) Quando si forma un catione dai metalli di transizione gli elettroni vengono emessi prima dall orbitale ns e poi dagli orbitali (n )d..7 La definizione adottata dall International Union of Pure and Applied Chemists (IUPAC) è che Gli elementi di transizione (metalli di transizione) hanno livelli d semipieni o danno origine a cationi che hanno livelli d semipieni. Zn, Cd, e Hg non soddisfano a questa definizione. Zn, Cd, e Hg formano cationi per perdita degli elettroni esterni s..9 As: metalloide Xe: non metallo Fe: metallo Li: metallo B: metalloide Cl: non metallo Ba: metallo P: non metallo I: non metallo Si: non metallo.3 Se ha bassa resistenza elettrica e conduce bene il calore è un metallo..33 L energia di ionizzazione è l energia richiesta per allontanare un elettrone da un elemento o uno ione in fase gas. Maggiore è l attrazione elettrostatica tra elettrone e nucleo, maggiore è l energia di ionizzazione.
3 CAPITOLO : ATOMI POLIELETTRONICI E TAVOLA PERIODICA Minore è il raggio, maggiore è l attrazione elettrostatica fra elettroni e nucleo e maggiore è l energia di ionizzazione.35 Be: [He] s B: [He] s p L andamento generale dell aumento dell elettronegatività da sinistra a destra nella tavola periodica è dovuto all aumento della carica nucleare. L energia di ionizzazione del boro è minore di quella del berillio poiché gli elettroni più esterni del boro si trovano in orbitali p che hanno maggiore energia (meno stabili) dell orbitale s del berillio che contiene i suoi elettroni più esterni...37 Si ricordi che solitamente le dimensioni atomiche variano nel modo seguente: () Da sinistra a destra lungo un periodo il raggio atomico diminuisce a causa dell aumento della carica nucleare effettiva. () Dall alto in basso lungo un gruppo, il raggio atomico aumenta poiché le dimensioni orbitaliche aumentano all aumentare del numero quantico principale. Gli atomi che si stanno considerando appartengono tutti allo stesso periodo. L atomo più a sinistra del periodo ha il maggiore raggio atomico, e l atomo più a destra ha il più piccolo. In ordine di dimensione atomica decrescente si ha: Na > Mg > Al > P > Cl Verifica: Si veda la Figura.6 del testo..39 Lo ione Cu + è più grande Cu + perché ha un elettrone in più..4 Si considera il punto di ebollizione dell argon approssimativamente uguale alla media dei punti di ebollizione di neon e kripton, in base alla posizione nella tavola periodica nel Gruppo 8A C + ( 5.9 C) b.p. = = 99.4 C In effetti il punto di ebollizione dell argon è 85.7 C..43 L andamento generale per l energia di prima ionizzazione è che aumenta da sinistra a destra lungo un periodo e diminuisce dall alto in basso lungo un gruppo. K ha la minore energia di ionizzazione. Ca, a destra del K, ha maggiore energia di ionizzazione. Muovendosi da sinistra a destra nella tavola periodica, le energie di dissociazione aumentano muovendosi verso il P. Nel gruppo degli alogeni il F ha maggiore energia di dissociazione rispetto a P. Infine Ne è a destra di F nel secondo periodo quindi ha maggiore energia di ionizzazione. L ordine corretto è: K < Ca < P < F < Ne Si veda la Tabella. del testo..45 Gli elementi del gruppo 3A (come Al) hanno un solo elettrone nell orbitale p, che è ben schermato dalla carica nucleare dagli elettroni più interni. E richiesta minore energia per allontanare un elettrone in un orbitale p che per rimuovere un elettrone accoppiato nell orbitale s come nel caso del Mg..47 Rimuovere elettroni esterni richiede minore energia se sono schermati da elettroni interni. L elettrone nell orbitale 3s è più facile da allontanare. La configurazione elettronica a gas nobile come s s p 6, è molto stabile, quindi è molto difficile allontanare un elettrone. Si veda la Tabella...49 Il numero atomico del mercurio è Δ E = (.8 0 J)(80 ) = J ΔE = J ion ions mol kj 000 J = kj mol
4 CAPITOLO : ATOMI POLIELETTRONICI E TAVOLA PERIODICA 3.5 L affinità elettronica aumenta da sinistra a destra lungo un periodo ad eccezione dei gas nobili. Il Cl ha la maggior affinità elettronica..53 I metalli alcalini hanno configurazione elettronica di valenza ns per cui possono accettare un altro elettrone nell orbitale. Invece i metalli alcalino terrosi hanno configurazione elettronica ns per cui un ulteriore elettrone dovrebbe entrare nell orbitale p a più alta energia..55 Gli elementi del Gruppo B sono molto meno reattivi di quelli del Gruppo A. Hanno maggiori energie di ionizzazione a causa dello schermaggio degli elettroni d..57 Applicando il principio di esclusione di Pauli e la regola di Hund: (a) F s s p 5 (b) P [Ne] 3s 3p 3 (c) Co [Ar] 4s 3d 7.59 (a) S + e S (b) Ti + Ti 3+ + e (c) Mg + + e Mg + (d) O O + e.6 In accordo con l Handbook of Chemistry and Physics (edizione ), il potassio ha punto di fusione di 63.6 C, il bromo è un liquido rosso marrone con punto di fusione di 7. C, e il bromuro di potassio (KBr) è un solido incolore con punto di fusione di 730 C. M è il potassio (K) e X è il bromo (Br)..63 (a) (i) Entrambi reagiscono con acqua per dare idrogeno; (ii) i loro ossidi sono basici; (iii) i loro alogenuri sono ionici. (b) (i) Entrambi sono forti agenti ossidanti; (ii) entrambi reagiscono con idrogeno per formare HX (dove X è Cl o Br); (iii) entrambi formano alogenuri (Cl o Br ) quando combinati con metalli (Na, K, Ca, Ba)..65 Lo zolfo ha configurazione elettronica dello stato fondamentale [Ne]3s 3p 4. Ha tendenza ad accettare un elettrone per diventare S. Anche se aggiungere un altro elettrone permette di formare S, che è isoelettronico con Ar, l aumento della repulsione interelettronica rende questo processo non favorevole..67 La percentuale di volume occupato da K + in confronto con quello di K è: 4 volume of K + π(33 pm)3 ion volume of K atom 00% = 3 00% = 3.3% 4 π(6 pm)3 3 Quindi c è una diminuzione di volume (00 3.3)% = 76.7% quando K + si forma da K..69 H e He sono specie isoelettroniche con due elettroni. Siccome H ha un solo protone, mentre He ne ha due, il nucleo di H attrae i due elettroni meno fortemente rispetto a He. Quindi, H è più grande..7 La reazione che rappresenta l affinità elettronica del cloro è: Cl(g) + e Cl (g) ΔH = +349 kj mol -
5 4 CAPITOLO : ATOMI POLIELETTRONICI E TAVOLA PERIODICA L energia di una mole di fotoni nei processi seguenti deve essere di +349 kj. Cl (g) + hν Cl(g) + e ΔH = -349 kj mol - Si converte l energia di un fotone per calcolare la lunghezza d onda del fotone. 349 kj mol photons mol photons photons 000 J = Jphoton kj Da cui: λ = hc E = ( J s)( ms ) = m = 343 nm J La radiazione cade nella regione dell ultravioletto nello spettro..73 L aggiunta di un elettrone a un atomo neutro è un processo sfavorevole solitamente a causa della repulsione elettrone-elettrone. L aggiunta di un secondo e terzo elettrone non avviene spontaneamente e quindi è difficile misurarne l affinità elettronica..75 Caratteristiche fisiche: Solido; apparenza come lo iodio; punto di fusione maggiore di 4 C..77 Z = 9 Configurazione elettronica: [Rn]7s 5f 4 6d 0 7p 6 8s.79 Tra la seconda e la terza ionizzazione c è un salto energetico importante, che suggerisce una variazione del numero quantico n. Il terzo elettrone allontanato proviene dallo strato più interno, del core gas nobile, che è difficile da strappare. Per cui l elemento appartiene al Gruppo A..8 (a) SiH 4, GeH 4, SnH 4, PbH 4 (b) Il carattere metallico aumenta spostandosi dall alto in basso nella tavola periodica. Per cui, RbH dovrebbe avere carattere più ionico di NaH. (c) Siccome Ra si trova nel Gruppo A, la reazione con acqua dovrebbe essere analoga a quella degli altri elementi del gruppo. Ra(s) + H O(l) Ra(OH) (aq) + H (g) (d) Berillio (relazione diagonale).83 Si riarrangia l equazione per risolvere per l energia di ionizzazione (E I ). E I = hν mu L energia cinetica dell elettrone emesso è data. Si sostituisce h, c, e λ nella reazione precedente. E I = ( J s)( ms ) m Si esprime in kj mol J photon photons mol ( J) = J kj 000 J = 48 kj mol.85 Na Na + + e I = kj mol - Questa equazione è l opposto dell affinità elettronica per Na +. Quindi l affinità elettronica di Na + è kj mol -. Si noti che è positiva, per cui è energia liberata quando un elettrone viene aggiunto a un atomo o a uno ione..87 Fe + [Ar]3d 6 Fe 3+ [Ar]3d 5 Mn + [Ar]3d 5 Mn 3+ [Ar]3d 4 Uno strato semi pieno ha una extrastabilità. Per cui l ossidazione del manganese è meno facile.
6 CAPITOLO : ATOMI POLIELETTRONICI E TAVOLA PERIODICA 5.89 Si riarrangia l equazione per risolvere per Z eff. Li: Z = n I 3 kj mol eff 50 kj mol Z eff = () =.6 3 kj mol kj mol Na: Z eff = (3) =.84 3 kj mol K: 48.7 kj mol Z eff = (4) =.6 3 kj mol Lungo un gruppo, Z eff aumenta. Li: Z eff n Na: Z eff n Z eff =.6 =.84 3 = = 0.63 K: =.6 = n 4 Il rapporto Z eff /n è circa costante per cui l effetto di schermo è all incirca lo stesso..9 Per un atomo di boro nello spazio tutte le direzioni sono equivalenti. L orbitale p può essere orientato secondo qualsiasi direzione. L elettrone disaccoppiato del boro ha uguale probabilità di essere in uno dei tre orbitali p. Per questo l atomo di boro ha forma sferica.
La tavola periodica. 1- Introduzione
 La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici.
 I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
La rappresentazione degli orbitali Orbitali s ( l = 0 )
 Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
Forma e proprietà dell orbitale 1s
 Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
26/10/2012. Onde elettromagnetiche. b) proprietà periodiche C) configurazione elettronica. f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν
 Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
LEZIONE 2. Configurazioni elettroniche e tavola periodica
 LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s...
 1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Orbitali atomici. (1s ) < (2s < 2p) < ( 3s < 3p) < ( 4s < 3d < 4p) < ( 5s < 4d < 5p) < ( 6s <4f < 5d < 6p)
 Orbitali atomici Schema di successione dei livelli energetici degli orbitali la cui progressiva saturazione determina la configurazione elettronica degli elementi nel loro stato fondamentale (non in scala).
Orbitali atomici Schema di successione dei livelli energetici degli orbitali la cui progressiva saturazione determina la configurazione elettronica degli elementi nel loro stato fondamentale (non in scala).
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Configurazioni elettroniche e periodicità
 Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
Corso di CHIMICA LEZIONE 3
 Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
CARICA EFFICACE Z eff = Z - S
 RAPPRESENTAZIONE SCHEMATICA ENERGIA RELATIVA ORBITALI E 3s 2s 1s 3p 2p 3d 3s 2s 1s 3p 2p 3d 3s 2s 3p 2p 3d IDROGENO (Z = 1) LITIO (Z = 3) 1s POTASSIO (Z = 19) Per Z = 1 (atomo di idrogeno: monoelettronico)
RAPPRESENTAZIONE SCHEMATICA ENERGIA RELATIVA ORBITALI E 3s 2s 1s 3p 2p 3d 3s 2s 1s 3p 2p 3d 3s 2s 3p 2p 3d IDROGENO (Z = 1) LITIO (Z = 3) 1s POTASSIO (Z = 19) Per Z = 1 (atomo di idrogeno: monoelettronico)
La tavola periodica. Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici
 La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici Si possono classificare gli elementi secondo la loro configurazione elettronica: Gas nobili. Elementi
La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici Si possono classificare gli elementi secondo la loro configurazione elettronica: Gas nobili. Elementi
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
PROPRIETÀ PERIODICHE DEGLI ELEMENTI
 PROPRIETÀ PERIODICHE DEGLI ELEMENTI 1) Energia di ionizzazione E ion Energia necessaria per sottrarre ad un atomo, allo stato di gas monoatomico, un elettrone A (g) d A + (g) + e - E ion processo endotermico
PROPRIETÀ PERIODICHE DEGLI ELEMENTI 1) Energia di ionizzazione E ion Energia necessaria per sottrarre ad un atomo, allo stato di gas monoatomico, un elettrone A (g) d A + (g) + e - E ion processo endotermico
Capitolo 10: La Tavola Periodica e Alcune Proprietà Atomiche
 Capitolo 10: La Tavola Periodica e Alcune Proprietà Atomiche Classificazione degli Elementi: La Legge Periodica e la Tavola Periodica Mendeleev notò che gli elementi possono essere suddivisi per gruppi
Capitolo 10: La Tavola Periodica e Alcune Proprietà Atomiche Classificazione degli Elementi: La Legge Periodica e la Tavola Periodica Mendeleev notò che gli elementi possono essere suddivisi per gruppi
I numeri quantici. Numero quantico principale, n: numero intero Caratterizza l energia dell elettrone
 I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
Tavola Periodica degli Elementi
 Tavola Periodica degli Elementi È possibile classificare gli elementi? Hp: In base alla massa atomica. Ogni 8 elementi le proprietà si ripetono. Incongruenze A Ar >A K Il Problema Le proprietà Chimiche
Tavola Periodica degli Elementi È possibile classificare gli elementi? Hp: In base alla massa atomica. Ogni 8 elementi le proprietà si ripetono. Incongruenze A Ar >A K Il Problema Le proprietà Chimiche
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
TAVOLA PERIODICA (Mendeleev, 1869)
 TAVOLA PERIODICA (Mendeleev, 1869) Osservazione e correlazione di proprietà chimiche (reattività, colore, solubilità, acidità, etc.) Li, Na, K, Rb Mg, Ca, Sr, Ba F, Cl, Br, I Ordinamento secondo Peso Atomico
TAVOLA PERIODICA (Mendeleev, 1869) Osservazione e correlazione di proprietà chimiche (reattività, colore, solubilità, acidità, etc.) Li, Na, K, Rb Mg, Ca, Sr, Ba F, Cl, Br, I Ordinamento secondo Peso Atomico
Il sistema periodico degli elementi
 Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
ESERCIZI W X Y Z. Numero di massa Neutroni nel nucleo Soluzione
 ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
TAVOLA PERIODICA DEGLI ELEMENTI
 La Tavola periodica TAVOLA PERIODICA DEGLI ELEMENTI Nel 869 i chimici Mendeleev (russo) e Meyer (tedesco) indipendentemente trovarono che ordinando gli elementi in ordine di peso atomico e disponendoli
La Tavola periodica TAVOLA PERIODICA DEGLI ELEMENTI Nel 869 i chimici Mendeleev (russo) e Meyer (tedesco) indipendentemente trovarono che ordinando gli elementi in ordine di peso atomico e disponendoli
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
Principio dell Aufbau (riempimento)
 LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
Configurazione elettronica e Tavola periodica. Lezioni 13-16
 Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazioni elettroniche e tavola periodica
 Configurazioni elettroniche e tavola periodica Ritorniamo ora al riempimento successivo dei sottostrati fra gli elementi finora considerati, l'elio He ed il neon Ne hanno gli strati n=1 e n=2 completi
Configurazioni elettroniche e tavola periodica Ritorniamo ora al riempimento successivo dei sottostrati fra gli elementi finora considerati, l'elio He ed il neon Ne hanno gli strati n=1 e n=2 completi
Come si dispongono gli elettroni negli atomi
 Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
Come si dispongono gli elettroni negli atomi L equazione di Schroedinger per l atomo di idrogeno elettrone ψ= Eψ nucleo ψ ( r, ϑ, ϕ) = R ( r ) Y ( ϑ, ϕ) n,l l,m l numeri quantici n =,,, l = 0,,,, n m l
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
M M n+ + n e - X + n e - X n-
 IL LEGAME IONICO 1 Il legame ionico Descrizione generale La formazione di NaCl La valenza ionica L energia reticolare: definizione e esempio di calcolo Proprietà dei solidi ionici Il legame ionico si realizza
IL LEGAME IONICO 1 Il legame ionico Descrizione generale La formazione di NaCl La valenza ionica L energia reticolare: definizione e esempio di calcolo Proprietà dei solidi ionici Il legame ionico si realizza
Comunicazioni Docente - Studenti
 Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
Comunicazioni Docente - Studenti 1. Lista di distribuzione: francesco.musiani.chimgenbiotech 2. Scrivere (moderatamente) a: francesco.musiani@unibo.it 3. Avvisi sul sito del docente: https://www.unibo.it/sitoweb/francesco.musiani
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2
 ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
LA TAVOLA PERIODICA. Ingegneria delle costruzioni
 LA TAVOLA PERIODICA Chimica Applicata Dr. Lucia Tonucci Ingegneria delle costruzioni Evidenza sperimentale: alcune proprietà degli elementi chimici hanno andamento periodico Elencando gli elementi secondo
LA TAVOLA PERIODICA Chimica Applicata Dr. Lucia Tonucci Ingegneria delle costruzioni Evidenza sperimentale: alcune proprietà degli elementi chimici hanno andamento periodico Elencando gli elementi secondo
I blocchi s, p, d ed f della Tavola Periodica
 I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietä degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietä degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
Per conoscere la disposizione degli elettroni attorno al nucleo si possono allontanare uno alla volta.
 Per conoscere la disposizione degli elettroni attorno al nucleo si possono allontanare uno alla volta. INFATTI: Se forniamo Energia all atomo i suoi elettroni possono compiere un salto energetico verso
Per conoscere la disposizione degli elettroni attorno al nucleo si possono allontanare uno alla volta. INFATTI: Se forniamo Energia all atomo i suoi elettroni possono compiere un salto energetico verso
Numeri quantici. Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo.
 Numeri quantici Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo. n= 1, 2, 3,. Numero quantico del momento angolare : Determina la forma
Numeri quantici Numero quantico principale n: determina l'energia dell'elettrone e può assumere qualsiasi valore intero positivo. n= 1, 2, 3,. Numero quantico del momento angolare : Determina la forma
Teoria Quantistica e Struttura Elettronica degli Atomi
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Teoria Quantistica e Struttura Elettronica degli Atomi Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Teoria Quantistica e Struttura Elettronica degli Atomi Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
test Di CHiMiCa PER l accesso alle FaColtà UNiVERSitaRiE
 1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile per l elemento M che dà facilmente lo ione M
1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile per l elemento M che dà facilmente lo ione M
TRACCIA: T11)DESCRIVERE LA TAVOLA PERIODICA
 TRACCIA: T11)DESCRIVERE LA TAVOLA PERIODICA La tavola periodica La tavola periodica degli elementi è lo schema con il quale vengono ordinati gli elementi chimici in base al loro numero atomico crescente
TRACCIA: T11)DESCRIVERE LA TAVOLA PERIODICA La tavola periodica La tavola periodica degli elementi è lo schema con il quale vengono ordinati gli elementi chimici in base al loro numero atomico crescente
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
Il legame chimico. Lezioni 17-20
 Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
tavola periodica Tale disposizione tabulare degli elementi è nota come Da tale disposizione venne elaborata la legge periodica che affermava che:
 Nel 1869 i chimici Dimitri Ivanovich Mendeleev e Julius Lothar Meyer, indipendentemente, trovarono che, ordinando gli elementi in ordine di peso atomico e disponendoli in file orizzontali una sopra l'altra,
Nel 1869 i chimici Dimitri Ivanovich Mendeleev e Julius Lothar Meyer, indipendentemente, trovarono che, ordinando gli elementi in ordine di peso atomico e disponendoli in file orizzontali una sopra l'altra,
Tavola periodica. Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi.
 Tavola periodica Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi. Tavola periodica Serve a classificare in modo sistematico le proprietà
Tavola periodica Concetto fondamentale della chimica: strumento per classificare, riconoscere, prevedere le proprietà degli elementi. Tavola periodica Serve a classificare in modo sistematico le proprietà
Orbitali nei primi tre livelli
 Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Tavola periodica. Periodo = riga. Gruppo = colonna:
 Periodo = riga Tavola periodica gli eleenti appartenenti ad uno stesso periodo hanno nuero atoico (e quindi nuero di elettroni) crescente da sinistra verso destra, fino a riepiento di uno strato caratterizzato
Periodo = riga Tavola periodica gli eleenti appartenenti ad uno stesso periodo hanno nuero atoico (e quindi nuero di elettroni) crescente da sinistra verso destra, fino a riepiento di uno strato caratterizzato
Metalli alcalinoterrosi calcogeni. Metalli di transizione
 La configurazione elettronica dei primi 20 elementi E ora possibile costruire la configurazione elettronica di tutti gli elementi della tavola periodica: distribuire cioè gli elettroni di un certo atomo
La configurazione elettronica dei primi 20 elementi E ora possibile costruire la configurazione elettronica di tutti gli elementi della tavola periodica: distribuire cioè gli elettroni di un certo atomo
Semimetalli. Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato.
 Semimetalli Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato. Elementi chimici, quali antimonio, arsenico, bismuto, che presentano proprietà in parte metalliche
Semimetalli Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato. Elementi chimici, quali antimonio, arsenico, bismuto, che presentano proprietà in parte metalliche
Tavola Periodica degli Elementi: Gruppi e Periodi
 La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
orbitali d Kr Rb At Ra
 Tavola Periodica Lo schema complessivo della tavola periodica fu scoperto dal chimico russo Mendeleev nel 1869. Ordinò gli elementi in gruppi e periodi secondo i valori crescenti del loro peso atomico
Tavola Periodica Lo schema complessivo della tavola periodica fu scoperto dal chimico russo Mendeleev nel 1869. Ordinò gli elementi in gruppi e periodi secondo i valori crescenti del loro peso atomico
Soluzioni degli esercizi del testo
 Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. Conoscenze e abilità 1. C 2. B 3.
Klein, Il racconto della chimica e della Terra Soluzioni degli esercizi del testo Lavorare con le mappe 1. 2. Risposta aperta. 3. Risposta aperta. 4. Risposta aperta. Conoscenze e abilità 1. C 2. B 3.
alle FaColtà UNiVERSitaRiE
 tst i HiMia PR l asso all Faoltà UNiVRSitaRi 1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile
tst i HiMia PR l asso all Faoltà UNiVRSitaRi 1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
TAVOLA PERIODICA. 118 elementi, di cui 92 presenti in natura
 TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Gli orbitali atomici. Il modo più semplice di visualizzare un atomo. TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e -
 Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
Tavola periodica degli Elementi
 Tavola periodica degli Elementi Capitolo 9 Il sistema periodico 1. La classificazione degli elementi 2. Il sistema periodico di Mendeleev 3. La moderna tavola periodica 4. I simboli di Lewis 5. Le proprietà
Tavola periodica degli Elementi Capitolo 9 Il sistema periodico 1. La classificazione degli elementi 2. Il sistema periodico di Mendeleev 3. La moderna tavola periodica 4. I simboli di Lewis 5. Le proprietà
Legami Chimici. Insegnamento di Chimica Generale CCS CHI e MAT
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Legami Chimici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 e 2
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Legami Chimici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/ Esercizio 1 e 2
Distribuzione degli elettroni negli orbitali atomici Aufbau
 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
CAPITOLO 0 IL LESSICO DELLA CHIMICA
 CAPITOLO 0 IL LESSICO DELLA CHIMICA 0.1 (a) Chimica. (b) Chimica. (c) Fisica. (d) Fisica. (e) Chimica. 0.3 La terra è una miscela eterogenea di minerali e materia organica. L aria è una miscela omogenea
CAPITOLO 0 IL LESSICO DELLA CHIMICA 0.1 (a) Chimica. (b) Chimica. (c) Fisica. (d) Fisica. (e) Chimica. 0.3 La terra è una miscela eterogenea di minerali e materia organica. L aria è una miscela omogenea
RIASSUNTI DI CHIMICA
 Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
COMPORTAMENTO DUALISTICO della MATERIA
 COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
Esperto prof. C. Formica
 Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
La Tavola Periodica (Mendeleev, 1869)
 La Tavola Periodica (Mendeleev, 1869) Mendeleev osservò che le proprietà (quali reattività, solubilità, acidità ) degli elementi allora noti variavano in modo periodico al variare della loro massa atomica
La Tavola Periodica (Mendeleev, 1869) Mendeleev osservò che le proprietà (quali reattività, solubilità, acidità ) degli elementi allora noti variavano in modo periodico al variare della loro massa atomica
CHIMICA: studio della struttura e delle trasformazioni della materia
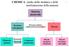 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Negli ultimi anni dell Ottocento gli scienziati capiscono che gli atomi sono formati da: neutroni protoni elettroni
 L ATOMO Negli ultimi anni dell Ottocento gli scienziati capiscono che gli atomi sono formati da: neutroni protoni elettroni Neutroni e protoni si trovano nel nucleo Gli elettroni ruotano intorno al nucleo
L ATOMO Negli ultimi anni dell Ottocento gli scienziati capiscono che gli atomi sono formati da: neutroni protoni elettroni Neutroni e protoni si trovano nel nucleo Gli elettroni ruotano intorno al nucleo
ψ = Il carbonio (Z=6) - 2 elettroni equivalenti nello stato 2p - la funzione d onda globale deve essere antisimmetrica tripletto di spin, S=1
 s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
combinazione di atomi tenuti insieme da forze più o meno un insieme caratteristico di proprietà
 IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
ORBITALE ATOMICO. Forma
 L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
COME CALCOLARE I NUMERI DI OSSIDAZIONE
 COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
COME CALCOLARE I NUMERI DI OSSIDAZIONE 1. Il numero di ossidazione (N.O.) degli atomi nelle sostanze elementari è zero 2. I seguenti elementi hanno sempre, nei loro composti, il N.O. indicato: Elemento
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Sommario delle lezione 3. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
GLI ELEMENTI CHIMICI
 I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014
 A FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
A FACOLTÀ DI FARMACIA C.d.L. in Farmacia CORSO DI CHIMICA GENERALE ED INORGANICA COMPITO SCRITTO - 12 Novembre 2014 COGNOME NOME Segnare con una crocetta la risposta (una sola) che si ritiene esatta. Alle
Elettronica II Legame covalente e bande di energia nei solidi p. 2
 Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Sommario delle lezione 3. Struttura dell atomo. Configurazione elettronica
 Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
Sommario delle lezione 3 Struttura dell atomo Configurazione elettronica Spettri di emissione e assorbimento degli atomi Ogni elemento ha uno spettro caratteristico che può essere usato per identificarlo
La struttura degli atomi
 1 La struttura degli atomi pg. 298 27-28 31-37 43 47 51-53 55-57 61-62 67(a/h) 68(a/i) La struttura degli atomi e gli andamenti periodici pg.332 1-7 11-15 17-18 27-30 37 40-42 51 Solvay conference, 1927
1 La struttura degli atomi pg. 298 27-28 31-37 43 47 51-53 55-57 61-62 67(a/h) 68(a/i) La struttura degli atomi e gli andamenti periodici pg.332 1-7 11-15 17-18 27-30 37 40-42 51 Solvay conference, 1927
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
