Regorafenib. Raccomandazioni evidence-based. Tumori stromali gastrointestinali (GIST) Terza Linea di terapia
|
|
|
- Mauro Vanni
- 7 anni fa
- Visualizzazioni
Transcript
1 Raccomandazioni evidence-based Regorafenib Tumori stromali gastrointestinali (GIST) Terza Linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 52 Direzione Generale, cura della persona, salute e welfare Pag.
2 Gruppo Regionale Panel GReFO, membri Longo Giuseppe - Coordinatore Gruppo GREFO - Onco-ematologia, Az. Osp. Univ. Policlinico, Modena Ardizzoni Andrea - Oncologia, Az. Osp.- Univ. Di Bologna - Policlinico S. Orsola-Malpighi Artioli Fabrizio - Oncologia, Ausl Modena Banzi Maria Chiara - Oncologia, Az. Osp. ASMN, IRCS-Reggio Emilia - Servizio Assistenza Territoriale -Area Farmaco e Dispositivi Medici. Regione Emilia-Romagna Borghi Athos - Medicina Interna, Az. Osp. Univ. Policlinico, Modena Brandes Alba - Oncologia, AUSL di Bologna Cascinu Stefano - Oncologia, Az. Osp. Univ. Policlinico, Modena Cavanna Luigi - Oncologia, Ospedale di Piacenza De Palma Rossana - Internista, Servizio Assistenza Ospedaliera, Regione Emilia-Romagna componente CRF Donati Caterina Farmacista, IRST Meldola (FC) Frassoldati Antonio - Oncologia clinica, Az. Osp. Univ. di Ferrara Frezza Giovanni - Radioterapia, Ospedale Bellaria, Bologna Ibrahim Toni- Oncologia, IRST Meldola (FC) Leoni Maurizio - Oncologia, Ospedale di Ravenna - Ausl Ravenna Maestri Antonio - Oncologia, Ausl Imola Maltoni Marco - Oncologo Palliativista, Ausl della Romagna Marata Anna Maria Farmacologo clinico, coordinatore della CRF, Servizio Assistenza Territoriale -Area Farmaco e Dispositivi Medici. RER Mazzi Giorgio - Direzione Sanitaria, Az. Osp. ASMN, IRCS-Reggio Emilia Pinto Carmine - Oncologia, Az. Osp. ASMN, IRCS - Reggio Emilia Santangelo Claudia - Rappresentante dei pazienti Tamberi Stefano - Oncologia, Ausl della Romagna Trapanese Maria - farmacista, Servizio Assistenza Territoriale -Area Farmaco e Dispositivi Medici. RER Tassinari Davide - Oncologia, Ospedale Infermi - Ausl Rimini Valenti Danila - Oncologia e Cure Palliative, Ausl Bologna Viani Nilla - Dipartimento Farmaceutico, Ausl Modena Zamagni Claudio - Oncologia, Az. Osp. Univ. Policlinico S Orsola-Malpighi, Bologna Zoli Marco - Medicina Interna, Az. Osp. Univ. Policlinico S Orsola-Malpighi, Bologna Aversa Franco - Ematologia, Az. Osp.- Univ. Di Parma Campagna Anselmo - Direzione Sanitaria, Az. Osp. Univ. Policlinico S Orsola-Malpighi, Bologna Cavo Michele - Ematologia, Az. Osp.- Univ. Di Bologna - Policlinico S. Orsola-Malpighi Cuneo Antonio - Ematologia, Arcispedale S. Anna Az. Osp.- Univ. di Ferrara Luppi Mario - Ematologia, Az. Osp.- Univ. di Modena, Policlinico. Merli Francesco - Ematologia, Arcispedale S. Maria Nuova Az. Osp./IRCS Reggio Emilia Potenza Leonardo - Ematologia, Az. Osp.- Univ. di Modena, Policlinico. Rapalli Cristina - Rappresentate dei pazienti Tosi Patrizia - Ematologia, Ospedale Az. USL di Rimini Vallisa Daniele - Ematologia, Ospedale Civile di Piacenza - Az. USL Piacenza Segreteria Scientifica GReFO (c/o - Area Farmaco e Dispositivi Medici, RER) Banzi Maria Chiara - Oncologia, Az. Osp. ASMN/IRCS-Reggio Emilia; Servizio Assistenza Territoriale-Area Farmaco e Dispositivi Medici. RER Formoso Giulio - Farmacista-metodologo, Servizio Assistenza Territoriale-Area Farmaco e Dispositivi Medici. RER Magnano Lucia - Farmacista, Servizio Assistenza Territoriale-Area Farmaco e Dispositivi Medici. RER Potenza Leonardo - Ematologia, Az. Osp.- Univ. di Modena, Policlinico. Regione Emilia-Romagna 2016 Tutti i diritti riservati. La riproduzione, in parte o totale, o la traduzione di questo documento sono consentite a condizione che venga citata la fonte e che la distribuzione non avvenga a fini di lucro o congiuntamente a prodotti commerciali. Il presente documento è stato commissionato dalla Direzione Generale Sanità e Politiche Sociali della Regione Emilia Romagna coerentemente con le strategie definite dalla Commissione Terapeutica Regionale e realizzato da un gruppo di lavoro multidisciplinare col supporto metodologico del Servizio Assistenza Territoriale-Area Farmaco e Dispositivi Medici. Regione Emilia-Romagna. Il presente documento va citato come: Gruppo regionale farmaci oncologici (GReFO). Regorafenib - Tumori stromali gastrointestinali (GIST). Direzione Generale alla Sanità e alle Politiche Sociali, Pag. 2
3 Indice Premessa pag. 4 Quesito Clinico pag. 5 Sintesi delle Raccomandazioni pag. 6 Valutazioni generali del gruppo di lavoro pag. 7 Bibliografia pag. 10 Appendice 1. Metodologia pag. 11 Pag. 3
4 Premessa Il presente documento fornisce raccomandazioni evidence based sui nuovi farmaci oncologici o sulle nuove indicazioni di farmaci già disponibili, al fine di individuarne gli usi appropriati per la pratica clinica e definirne il posto in terapia. A questo proposito la Direzione Generale Cura della Persona, Salute e Welfare della Regione Emilia Romagna ha deliberato, nell ambito delle attività della Commissione Regionale del Farmaco (CRF), (Determinazione n 402 del 15/01/2016), un gruppo di lavoro multidisciplinare costituito da oncologi, ematologi, palliativisti, internisti, farmacisti, medici di organizzazione, metodologi e rappresentanti dei pazienti (GReFO, Gruppo Regionale sui Farmaci Onco-ematologici) con l obiettivo di: - condividere con tutti i centri oncologici regionali la migliore strategia terapeutica che individui per ogni tipologia di neoplasia e per ogni linea terapeutica il trattamento con il miglior rapporto rischio/beneficio ed il rapporto costo/opportunità più favorevole. - operare scelte omogenee a livello dei vari centri oncologici regionali anche al fine di evitare disagi per i pazienti. Il gruppo GReFO elabora raccomandazioni con un approccio per quesiti e risposte. Per la formulazione delle raccomandazioni, viene applicato il metodo GRADE, un metodo sistematico e trasparente per il grading delle raccomandazioni, che coinvolge attivamente il gruppo di lavoro anche attraverso l utilizzo di una serie di voti preliminari fino alla votazione della raccomandazione stessa. Ciò consente di formulare direzione e forza di ogni raccomandazione considerando: - la qualità delle prove di efficacia ed il significato clinico dei risultati, - il rapporto fra i benefici e i rischi del/i trattamento/i, - le preferenze dei pazienti, - l uso delle risorse. Per la descrizione della metodologia GRADE vedi appendice. Le raccomandazioni prodotte riguardano singolarmente tutti i farmaci disponibili per ogni linea terapeutica; ciò al fine di individuare una strategia di cura globale e formulare, per ogni farmaco coinvolto nella singola linea di trattamento, forza e verso della raccomandazione, anche in considerazione delle alternative terapeutiche disponibili (vedi descrizione grafica della strategia terapeutica). La strategia terapeutica e le conseguenti raccomandazioni vengono aggiornate ogniqualvolta un nuovo farmaco viene autorizzato per quella linea e per quella indicazione. Alla definizione della strategia terapeutica viene associata, per ogni svincolo decisionale, una stima (valida per la Regione Emilia Romagna e per un anno) del numero di pazienti coinvolti fino ad arrivare a definire il numero di pazienti attesi per ogni singolo trattamento (vedi descrizione grafica della strategia terapeutica). I numeri via via stimati sono ricavati da una serie di fonti: i registri tumori (dati regionali del registro AIRTUM, i registri locali), dati epidemiologici nazionali e internazionali pubblicati, casistiche locali. Tali fonti forniscono solitamente dati di incidenza, quando possibile il dato di incidenza viene integrato con quello di prevalenza. La stima numerica è stata scelta come alternativa alla percentuale di uso atteso fino ad oggi utilizzata, allo scopo di favorire il monitoraggio regionale dell applicazione delle raccomandazioni prodotte attraverso analisi periodiche dei reali consumi nei singoli contesti locali. A tale scopo è in fase avanzata di realizzazione un database oncologico regionale che convogliando i flussi prescrittivi dei singoli centri oncologici fornirà informazioni di tipo clinico legate alla singola prescrizione. I dati provenienti dal monitoraggio verranno periodicamente discussi all interno del gruppo GReFO ed inviati a tutti i Centri oncologici, alle Direzioni Sanitarie e ai Servizi/Dipartimenti farmaceutici della Regione. Pag. 4
5 Contesto Nel presente documento, si riportano le raccomandazioni del Panel su regorafenib per il trattamento dei tumori stromali gastrointestinali (GIST). Quesito clinico Nei pazienti affetti da tumori stromali gastrointestinali (gastrointestinal stromal tumors, GIST) non resecabili o metastatici, dopo progressione di malattia o intolleranti al trattamento precedente con imatinib e sunitinib, è raccomandabile l utilizzo di regorafenib? Il Panel ha successivamente espresso, rispetto al quesito clinico generale, due raccomandazioni distinte sulla base del Performance Status. Indicazioni registrate EMA/AIFA Stivarga è indicato per il trattamento dei pazienti adulti affetti da tumori stromali gastrointestinali (gastrointestinal stromal tumors, GIST) non resecabili o metastatici, dopo progressione di malattia o intolleranti al trattamento precedente con imatinib e sunitinib Fascia di rimborsabilità A-RNRL / PT-PHT Stivarga è indicato per il trattamento dei pazienti adulti affetti da carcinoma metastatico del colon-retto precedentemente trattati oppure non candidabili al trattamento con le terapie disponibili. Queste comprendono chemioterapia a base di fluoropirimidina, una terapia anti-vegf ed una terapia anti-egfr Pag. 5
6 Sintesi delle raccomandazioni Quesito clinico Nei pazienti affetti da tumori stromali gastrointestinali (gastrointestinal stromal tumors, GIST) non resecabili o metastatici, dopo progressione di malattia o intolleranti al trattamento precedente con imatinib e sunitinib, è raccomandabile l utilizzo di regorafenib? Raccomandazioni Negativa Debole Nei pazienti affetti da tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, con PS: 0-1, regorafenib NON dovrebbe essere utilizzato. Raccomandazione formulata sulla base di: evidenze considerate di qualità: BASSA rapporto benefici/rischi: incerto (Votazioni vedi nel testo del documento) Negativa Forte Nei pazienti affetti da tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, con PS > 2, regorafenib NON deve essere utilizzato. Raccomandazione formulata sulla base di: evidenze non disponibili rapporto benefici/rischi: non valutabile Il Panel ha deciso all unanimità di formulare una raccomandazione negativa forte in considerazione della mancanza di evidenze nel setting di pazienti considerato. Uso atteso del farmaco nella regione Emilia-Romagna: Sulla base della raccomandazioni formulate, nei pazienti con tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, il numero atteso dei pazienti da trattare e le loro caratteristiche sono i seguenti: - regorafenib nei pazienti con PS: 0-1: circa trattamenti/anno. - regorafenib nei pazienti con PS> 2, non ci si aspetta che ci siano pazienti che potrebbero beneficiare del trattamento, se non in casi eccezionali opportunamente documentati. Pag. 6
7 Valutazioni generali del gruppo di lavoro Quesito Clinico Nei pazienti affetti da tumori stromali gastrointestinali (gastrointestinal stromal tumors, GIST) non resecabili o metastatici, dopo progressione di malattia o intolleranti al trattamento precedente con imatinib e sunitinib, è raccomandabile l utilizzo di regorafenib? Valutazione della qualità metodologica delle evidenze disponibili: regorafenib nei GIST, 3 linea di terapia Di seguito si riporta la sintesi dello studio registrativo, di fase III, di regorafenib nei GIST, in terza linea di terapia Demetri et al (GRID) The Lancet 2013 Studio di fase III in doppio cieco, controllato con placebo, riguardante pazienti, PS 0-1, di età media anni, affetti da tumore stromale gastrointestinale non operabile o metastatico, in progressione o intolleranti a imatinib e sunitinib (terza linea vera). I pazienti venivano randomizzati 2:1 a ricevere regorafenib 160 mg/die (per 3 settimane ogni 4) + BSC o placebo + BSC. Alla progressione l 85% dei pazienti nel braccio placebo, in aperto, ha potuto accedere al trattamento attivo con regorafenib. L endpoint primario era la sopravvivenza libera da progressione (PFS), rivalutata centralmente da radiologi indipendenti, mantenuti in cieco, e secondari la sopravvivenza (OS), il tempo alla progressione (TTP), il tasso di risposta (ORR), il controllo di malattia (DCR) e la tossicità. La PFS è risultata statisticamente superiore nel braccio con regorafenib, 4.8 vs 0.9 mesi (HR 0.27;95%CI, ;P<0.0001). La PFS a 3 e a 6 mesi è stata rispettivamente del 60% e 38% per regorafenib e dell 11% e 0% per il placebo. La valutazione della PFS mediana fatta dagli investigatori è stata rispettivamente di 7.4 vs 1.9 mesi (HR 0.22, 95%CI , P<0.0001). La sopravvivenza globale non ha mostrato differenze stasticamente significative tra i due gruppi (29 [22%] vs 17 [26%] eventi; HR 0.77, 95%CI ; p=0.199). Non ci sono state risposte complete in entrambi i gruppi; la risposta complessiva (ORR) è stata del 4.5% con regorafenib e del 1.5% con il placebo. Nel <.4% si è ottenuta stabilità di malattia con il farmaco attivo a fronte del 33.3% con il placebo. Pressoché tutti i pazienti trattati con regorafenib (98%) hanno avuto un evento avverso rispetto al 68% di quelli trattati con il placebo. La tossicità cutanea (hand-foot sindrome) è stata l evento avverso più comune. Le tossicità di grado 3 e 4 più frequenti sono state l ipertensione (23%), l hand-foot sindrome (20%) e la diarrea (5%). Tossicità di grado 5 si è verificata nel 5% dei pazienti di entrambi i gruppi e nel 2% vi è stata correlazione con il farmaco. E stata valutata la qualità di vita con il questionario EQ-5D e non si è rilevata nessuna differenza statisticamente significativa tra i due trattamenti. Referenza (tipo studio) Intervento Controllo 1 Esito principale Esiti secondari Qualità evidenze Demetri et al The Lancet 2013 RCT, fase III, in doppio cieco; 199 pazienti random izzati 2:1 Regorafenib (160 mg/die per 3 sett/4 sett) + BSC Placebo + BSC PFS - OS - TTP - ORR - DCR BASSA (-1 Risk of bias -1 incoerenza) Tabella 2: studi disponibili di fase III su ramucirumab non in associazione a paclitaxel Pag. 7
8 Valutazione della qualità metodologica degli studi secondo i criteri GRADE Risk of bias: lo studio considera come esito principale la PFS; la stima della OS è inclusa come esito secondario, inoltre è inficiata dal crossover; Tra gli obiettivi secondari è dichiarato il tempo alla progressione di cui non vi sono riferimenti all interno della pubblicazione (rischio di selective reporting bias; downgrade -1) Coerenza tra studi: Unico studio disponibile (downgrade - 1) Trasferibilità nella pratica clinica: non applicabile Stime imprecise: non applicabile Rischio di mancata pubblicazione: improbabile Conclusione sulla qualità delle evidenze: Sulla base delle considerazioni soprariportate, la qualità delle evidenze è stata giudicata dal Panel BASSA (Downgrade complessivo di 2 punti) Valutazione dei benefici e dei rischi e votazioni del Panel Si riportano di seguito le votazioni del panel (26 votanti presenti) sul bilancio tra i benefici e i rischi e sulla raccomandazione d uso di regorafenib in terza linea di terapia dei tumori stromali gastrointestinali non resecabili o metastatici. Bilancio Benefici rischi incerto Il bilancio benefici/rischi è stato considerato da 15 membri del panel incerto ; 7 hanno espresso un giudizio sfavorevole e 4 favorevole Forza della raccomandazione La forza della raccomandazione è stata definita come NEGATIVA DEBO- LE. In particolare 17 membri si sono espressi con un giudizio di negativa debole, 4 di negativa forte e 3 di positiva debole e 2 di positiva forte Raccomandazione Negativa Debole Nei pazienti affetti da tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, regorafenib NON dovrebbe essere utilizzato (se non in pazienti particolari, ben informati e motivati) Raccomandazione formulata sulla base di: evidenze considerate di qualità: BASSA rapporto benefici/rischi: incerto Uso atteso del farmaco in regione Emilia-Romagna: Sulla base della raccomandazione formulata, il numero atteso di pazienti, in un anno, che potranno beneficiare del regorafenib è di circa Si tratta di pazienti con tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib e con un buon Performance Status, PS:0-1. Pag. 8
9 Quesito Clinico Nei pazienti affetti da tumori stromali gastrointestinali (gastrointestinal stromal tumors, GIST) non resecabili o metastatici, dopo progressione di malattia o intolleranti al trattamento precedente con imatinib e sunitinib, è raccomandabile l utilizzo di regorafenib? Il Panel in assenza di studi clinici che valutano l efficacia e la sicurezza del regorafenib nei pazienti con performance Status > 2 ha formulato la seguente raccomandazione Raccomandazione Negativa Forte Nei pazienti affetti da tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, con PS > 2, regorafenib NON deve essere utilizzato. Raccomandazione formulata sulla base di: evidenze non disponibili rapporto benefici/rischi: non valutabile Il Panel ha deciso all unanimità di formulare una raccomandazione negativa forte in considerazione della mancanza di evidenze nel setting di pazienti considerato Uso atteso del farmaco nella regione Emilia-Romagna: Sulla base della raccomandazioni formulate, nei pazienti con tumore stromale gastrointestinale (GIST), non resecabile o metastatico, in progressione o intolleranti a imatinib e sunitinib, il numero atteso dei pazienti da trattare e le loro caratteristiche sono i seguenti: - regorafenib nei pazienti con PS> 2: non ci si aspetta che ci siano pazienti che potrebbero beneficiare del trattamento, se non in casi eccezionali opportunamente documentati. Pag. 9
10 Bibliografia Scheda AIRTUM. I tumori in Italia Rapporto 2006 AIOM. Linee guida. SARCOMI DEI TESSUTI MOLLI E GIST. Edizione 2015 NCCN guidelines.soft Tissue Sarcoma. Versione EMA. Stivarga Assessment report su regorafenib. EMEA/H/C/002573/II/0001. Giugno 2014 Wu et Al. Clinical efficacy of secondgeneration tyrosine kinase inhibitors in imatinib-resistant gastrointestinal stromal tumors: a meta-analysis of recent clinical trials. Drug Design, Development and Therapy 2014: phase 3 trial (GRID). The Lancet (26): Demetri GD et al. Efficacy and safety of sunitinib in patients with advancedgastrointestinal stromal tumour after failure of imatinib: a randomised controlled trial. Lancet 2006; 368: Demetri GD et al Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med. 2002; (347): Demetri GD et al. Efficacy and safety of regorafenib for advanced gastrointestinal stromal tumours after failure of imatinib and sunitinib: an international, multicentre, prospective, randomised, placebocontrolled Common Terminology Criteria for Adverse Events v4.0 (CTCAE) Grades Grade refers to the severity of the AE. The CTCAE displays Grades 1 through 5 with unique clinical descriptions of severity for each AE based on this general guideline: Grade 1 Mild; asymptomatic or mild symptoms; clinical or diagnostic observations only; intervention not indicated. Grade 2 Moderate; minimal, local or noninvasive intervention indicated; limiting age-appropriate instrumental ADL*. Grade 3 Severe or medically significant but not immediately life-threatening; hospitalization indicated; disabling; limiting self care ADL**. Grade 4 Life-threatening consequences; urgent intervention indicated. Grade 5 Death related to AE. Activities of Daily Living (ADL) *Instrumental ADL refer to preparing meals, shopping for groceries or clothes, using the telephone, managing money, etc. **Self care ADL refer to bathing, dressing and undressing, feeding self, using the toilet, taking medications, and not bedridden. Legenda Qualità delle evidenze: alta moderata bassa Molto bassa Valutazione benefici/rischi: favorevole incerto sfavorevole PS: Eastern Cooperative Oncology Group (ECOG) performance status (PS). [0=Fully active, able to carry on all pre-disease performance without restriction; 5=Dead]. As published in Am. J. Clin. Oncol.: Oken, M.M., Creech, R.H., Tormey, D.C., Horton, J., Davis, T.E., McFadden, E.T., Carbone, P.P.: Toxicity And Response Criteria Of The Eastern Cooperative Oncology Group. Am J Clin Oncol 5: , Disponibile on-line: PFS: Progression free survival OS: Overall Survival RR: Response Rate Pag. 10
11 Appendice 1. Metodologia Il metodo GRADE prevede, in merito alla valutazione della qualità delle prove di efficacia e sicurezza, di procedere per gradi valutando nell ordine: 1. l importanza degli esiti di efficacia e sicurezza; 2. la qualità metodologica delle prove; 3. il bilancio fra i benefici ed i rischi ricavati dalle prove di efficacia; 4. formulazione della raccomandazione Il gruppo di lavoro ha deciso che passaggi 1, 3 e 4 prevedano una votazione. Partendo dalla qualità teoricamente bassa di uno studio osservazionale è, al contrario, possibile un upgrading di tale qualità fino a divenire molto alta in presenza dei seguenti fattori: associazione intervento-outcome (dimensione dell effetto) gradiente dose-risposta effetto visibile nonostante possibili fattori di confondimento e bias Se la qualità è diversa fra i singoli outcome essenziali, il metodo suggerisce di utilizzare come qualità delle evidenze quella relativa all outcome critico che ha ricevuto il giudizio più basso. Importanza degli esiti di efficacia e sicurezza Il metodo prevede che prima di iniziare la ricerca bibliografica venga definita dal panel l importanza dei possibili esiti di efficacia per ogni singola patologia neoplastica e di sicurezza per ogni singolo farmaco. Tale importanza viene definita votando una griglia quantitativa, che prevede un punteggio da 1 a 9, che consente di classificare gli esiti in: - non importante (punteggio da 1 a 3) - Importante (punteggio da 4 a 6) - critico o essenziale (punteggio da 7 a 9) Solo gli esiti risultati importanti o critici/essenziali vengono poi ricercati negli studi clinici ed i relativi risultati vengono considerati per la definizione della raccomandazione. Qualità metodologica delle prove La qualità delle prove di efficacia è definita, per singolo esito in quattro categorie: alta, moderata, bassa, molto bassa. Partendo dalla qualità teoricamente alta di uno studio randomizzato controllato, vengono sistematicamente considerati una serie di fattori che possono ridurre tale alta qualità: validità interna dello studio (risk of bias) coerenza tra studi (inconsistency) trasferibilità nella pratica clinica (directness) stime imprecise (imprecision e sparse data) possibilità di pubblicazione selettiva dei dati (publication/reporting bias) In base al numero di fattori presenti e all importanza dei limiti metodologici la qualità può subire un downgrading fino a diventare molto bassa. Bilancio fra i benefici ed i rischi Il metodo prevede che, una volta esaminate le prove di efficacia e sicurezza, venga votato il rapporto tra i rischi ed i benefici. Tale rapporto potrà essere definito come: favorevole, incerto o sfavorevole. La definizione del beneficio/rischio rappresenta la sintesi della valutazione delle prove e del loro significato clinico fatta dal singolo membro del gruppo tenendo conto anche delle preferenze espresse dai pazienti e dell uso appropriato delle risorse. Il panel ha deciso di rendere esplicito il risultato della votazione inserendolo nel documento. Formulazione della raccomandazione Ultimo passaggio è quello della formulazione della raccomandazione che potrà essere di entità forte o debole e di verso positivo o negativo. Per la votazione della raccomandazione ogni membro del gruppo di lavoro dovrà considerare tutti gli elementi derivati dai punti precedenti Bibliografia di riferimento: Serie di articoli pubblicati sul JCE 2011 e 2013: G. Guyatt et al. Journal of Clinical Epidemiology. 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; H. Balshem et al. Journal of Clinical Epidemiology 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; 1277e1282 G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; G.H. Guyatt et al. Journal of Clinical Epidemiology 2011; M. Brunetti et al. Journal of Clinical Epidemiology 2013; G. Guyatt et al. Journal of Clinical Epidemiology 2013; G.H. Guyatt et al. Journal of Clinical Epidemiology 2013; G.H. Guyatt et al. Journal of Clinical Epidemiology 2013; J. Andrews et al. Journal of Clinical Epidemiology 2013; J.C. Andrews et al. Journal of Clinical Epidemiology 2013; Pag. 11
12 Pag. 12
Vandetanib. nel carcinoma midollare avanzato della tiroide (I linea di terapia) Raccomandazioni evidence-based
 Raccomandazioni evidence-based Vandetanib nel carcinoma midollare avanzato della tiroide (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 27 Dicembre
Raccomandazioni evidence-based Vandetanib nel carcinoma midollare avanzato della tiroide (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 27 Dicembre
Bevacizumab. Raccomandazioni evidence-based. Tumori ginecologici platino sensibile I recidiva. A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Tumori ginecologici platino sensibile I recidiva A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 37 Ottobre 2014 Direzione Generale alla Sanità
Raccomandazioni evidence-based Tumori ginecologici platino sensibile I recidiva A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 37 Ottobre 2014 Direzione Generale alla Sanità
Mieloma multiplo recidivato e refrattario. (dopo almeno due precedenti trattamenti) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Pomalidomide Mieloma multiplo recidivato e refrattario (dopo almeno due precedenti trattamenti) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso
Raccomandazioni evidence-based Pomalidomide Mieloma multiplo recidivato e refrattario (dopo almeno due precedenti trattamenti) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso
Farmaci per il tumore neuroendocrino del pancreas (pnet), metastatico o non operabile, in progressione di malattia
 Raccomandazioni evidence-based Farmaci per il tumore neuroendocrino del pancreas (pnet), metastatico o non operabile, in progressione di malattia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Raccomandazioni evidence-based Farmaci per il tumore neuroendocrino del pancreas (pnet), metastatico o non operabile, in progressione di malattia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Carcinoma gastrico In progressione dopo chemioterapia con platino e fluoropirimidine (seconda linea)
 Raccomandazioni evidence-based Ramucirumab Carcinoma gastrico In progressione dopo chemioterapia con platino e fluoropirimidine (seconda linea) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
Raccomandazioni evidence-based Ramucirumab Carcinoma gastrico In progressione dopo chemioterapia con platino e fluoropirimidine (seconda linea) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Nab-paclitaxel nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 40 Febbraio
Raccomandazioni evidence-based Nab-paclitaxel nel carcinoma del pancreas esocrino metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 40 Febbraio
APPROPRIATEZZA TERAPEUTICA
 APPROPRIATEZZA TERAPEUTICA Ferrara 6 ottobre 2016 I farmaci ad alto costo in Oncologia Donatella Donati Oncologia Clinica Azienda Ospedaliera Universitaria -Ferrara I tumori in Italia Roma 27 settembre
APPROPRIATEZZA TERAPEUTICA Ferrara 6 ottobre 2016 I farmaci ad alto costo in Oncologia Donatella Donati Oncologia Clinica Azienda Ospedaliera Universitaria -Ferrara I tumori in Italia Roma 27 settembre
Carcinoma colon-rettale metastatico RAS wild type. A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico RAS wild type A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Aggiornamento dicembre 2014
Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico RAS wild type A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Aggiornamento dicembre 2014
Denosumab. nei tumori solidi con metastasi ossee. Raccomandazioni evidence-based. A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Denosumab nei tumori solidi con metastasi ossee A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 28 Gennaio 2014 Direzione Generale alla Sanità
Raccomandazioni evidence-based Denosumab nei tumori solidi con metastasi ossee A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 28 Gennaio 2014 Direzione Generale alla Sanità
A cura del Gruppo Regionale Farmaci Oncologici (GReFO) (pubblicato a maggio 2014) Aggiornata alla pubblicazione della negoziazione AIFA (luglio 2014)
 Raccomandazioni evidence-based Pertuzumab Nel carcinoma mammario avanzato HER2/neu positivo (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 26 Settembre
Raccomandazioni evidence-based Pertuzumab Nel carcinoma mammario avanzato HER2/neu positivo (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 26 Settembre
in progressione, refrattario allo iodio radioattivo
 Raccomandazioni evidence-based Farmaci per il Tumore differenziato della Tiroide A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 58 febbraio 2017 Direzione Generale, cura
Raccomandazioni evidence-based Farmaci per il Tumore differenziato della Tiroide A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 58 febbraio 2017 Direzione Generale, cura
Brentuximab vedotin. Linfoma di Hodgkin (CD30+) recidivante o refrattario. Raccomandazioni evidence-based
 Raccomandazioni evidence-based Brentuximab vedotin Linfoma di Hodgkin (CD30+) recidivante o refrattario A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 47 luglio 2015 Direzione
Raccomandazioni evidence-based Brentuximab vedotin Linfoma di Hodgkin (CD30+) recidivante o refrattario A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 47 luglio 2015 Direzione
Raccomandazioni evidence-based Regorafenib nel carcinoma del colon retto avanzato pretrattato A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Regorafenib nel carcinoma del colon retto avanzato pretrattato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.30 () Aggiornato alla pubblicazione
Raccomandazioni evidence-based Regorafenib nel carcinoma del colon retto avanzato pretrattato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.30 () Aggiornato alla pubblicazione
nel carcinoma della prostata castrazione resistente con metastasi ossee sintomatiche e senza metastasi viscerali note
 Raccomandazioni evidence-based Radium-223 dicloruro nel carcinoma della prostata castrazione resistente con metastasi ossee sintomatiche e senza metastasi viscerali note A cura del Gruppo Regionale Farmaci
Raccomandazioni evidence-based Radium-223 dicloruro nel carcinoma della prostata castrazione resistente con metastasi ossee sintomatiche e senza metastasi viscerali note A cura del Gruppo Regionale Farmaci
Panitumumab. Raccomandazioni evidence-based. Carcinoma colon-rettale metastatico (I linea di terapia)
 Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Ottobre 2014 Direzione
Raccomandazioni evidence-based Panitumumab Carcinoma colon-rettale metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 36 Ottobre 2014 Direzione
Linfoma follicolare refrattario (LF) Idelalisib Ibritumumab tiuxetano
 Raccomandazioni evidence-based Linfoma follicolare refrattario (LF) Idelalisib Ibritumumab tiuxetano A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 57 Maggio 2016 Direzione
Raccomandazioni evidence-based Linfoma follicolare refrattario (LF) Idelalisib Ibritumumab tiuxetano A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 57 Maggio 2016 Direzione
Aflibercept. Raccomandazioni evidence-based. Nel carcinoma del colon retto avanzato (II linea di terapia)
 Raccomandazioni evidence-based Aflibercept Nel carcinoma del colon retto avanzato (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.29 (Pubblicato a )
Raccomandazioni evidence-based Aflibercept Nel carcinoma del colon retto avanzato (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.29 (Pubblicato a )
Tumore del polmone Non Small Cell Lung Cancer, non squamoso (mantenimento dopo I linea)
 Tumore del polmone Non Small Cell Lung Cancer, non squamoso () Raccomandazioni evidence-based A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 38 Aggiornamento Direzione
Tumore del polmone Non Small Cell Lung Cancer, non squamoso () Raccomandazioni evidence-based A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 38 Aggiornamento Direzione
Farmaci per il carcinoma della prostata metastatico castrazione resistente
 Raccomandazioni evidence-based Farmaci per il carcinoma della prostata metastatico castrazione resistente Abiraterone-Enzalutamide Docetaxel Radium223 dicloruro- Cabazitaxel A cura del Gruppo Regionale
Raccomandazioni evidence-based Farmaci per il carcinoma della prostata metastatico castrazione resistente Abiraterone-Enzalutamide Docetaxel Radium223 dicloruro- Cabazitaxel A cura del Gruppo Regionale
Nel tumore polmonare non a piccole cellule (NSCLC) metastatico o non operabile (I linea di terapia)
 Raccomandazioni evidence-based Afatinib Nel tumore polmonare non a piccole cellule (NSCLC) metastatico o non operabile (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
Raccomandazioni evidence-based Afatinib Nel tumore polmonare non a piccole cellule (NSCLC) metastatico o non operabile (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
Farmaci innovativi nel carcinoma colo-rettale
 Incontri Triveneti Padova, 03 dicembre 2015 Farmaci innovativi nel carcinoma colo-rettale Sara Lonardi SS Neoplasie colo-rettali, UOC Oncologia Medica 1 Istituto Oncologico Veneto IRCCS, Padova Anti-angiogenic
Incontri Triveneti Padova, 03 dicembre 2015 Farmaci innovativi nel carcinoma colo-rettale Sara Lonardi SS Neoplasie colo-rettali, UOC Oncologia Medica 1 Istituto Oncologico Veneto IRCCS, Padova Anti-angiogenic
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Le raccomandazioni in campo oncologico: dall analisi per farmaco a quella per indicazione. Anna Maria Marata
 Le raccomandazioni in campo oncologico: dall analisi per farmaco a quella per indicazione ovvero come è evoluto il metodo di lavoro all interno di un gruppo Anna Maria Marata Roma: ISS 14 luglio 2016 Servizio
Le raccomandazioni in campo oncologico: dall analisi per farmaco a quella per indicazione ovvero come è evoluto il metodo di lavoro all interno di un gruppo Anna Maria Marata Roma: ISS 14 luglio 2016 Servizio
splenomegalia in pazienti adulti con mielofibrosi A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Ruxolitinib splenomegalia in pazienti adulti con mielofibrosi A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 39 Direzione Generale alla Sanità
Raccomandazioni evidence-based Ruxolitinib splenomegalia in pazienti adulti con mielofibrosi A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 39 Direzione Generale alla Sanità
Trastuzumab emtansine (TDM-1)
 Raccomandazioni evidence-based Trastuzumab emtansine (TDM-1) nel carcinoma della mammella avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.33 (Pubblicato a ) Aggiornato
Raccomandazioni evidence-based Trastuzumab emtansine (TDM-1) nel carcinoma della mammella avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.33 (Pubblicato a ) Aggiornato
nel carcinoma a cellule squamose del tratto testa e collo ricorrente e/o metastatico (I linea di terapia)
 Raccomandazioni evidence-based Cetuximab nel carcinoma a cellule squamose del tratto testa e collo ricorrente e/o metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Raccomandazioni evidence-based Cetuximab nel carcinoma a cellule squamose del tratto testa e collo ricorrente e/o metastatico (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Doxorubicina liposomiale dopo almeno una linea di terapia
 Raccomandazioni d'uso Mieloma multiplo Doxorubicina liposomiale dopo almeno una linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni evidence based
Raccomandazioni d'uso Mieloma multiplo Doxorubicina liposomiale dopo almeno una linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni evidence based
Abiraterone e cabazitaxel
 Raccomandazioni evidence-based Abiraterone e cabazitaxel nel carcinoma della prostata metastatico (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 18
Raccomandazioni evidence-based Abiraterone e cabazitaxel nel carcinoma della prostata metastatico (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 18
Raccomandazioni evidence-based. Farmaci per il melanoma avanzato, non resecabile o metastatico Prima linea di terapia
 Raccomandazioni evidence-based Farmaci per il melanoma avanzato, non resecabile o metastatico Prima linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 54 Maggio
Raccomandazioni evidence-based Farmaci per il melanoma avanzato, non resecabile o metastatico Prima linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 54 Maggio
BOLOGNA BOLOGNA BOLOGNA WORKSHOP 22 NOVEMBRE 2016
 OSPEDALE e TERRITORIO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO BARI FIRENZE NAPOLI PADOVA ROMA TORINO PALERMO BOLOGNA
OSPEDALE e TERRITORIO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO BARI FIRENZE NAPOLI PADOVA ROMA TORINO PALERMO BOLOGNA
REGORAFENIB - STIVARGA
 giunta regionale Allegato A al Decreto n. 5 del 14 gennaio 2016 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED REGORAFENIB - STIVARGA Indicazione in esame: è indicato
giunta regionale Allegato A al Decreto n. 5 del 14 gennaio 2016 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED REGORAFENIB - STIVARGA Indicazione in esame: è indicato
Raccomandazioni evidence-based. Olaparib. Carcinoma ovarico epiteliale, alle tube di Falloppio, peritoneale primario BRCA mutato
 Raccomandazioni evidence-based Olaparib Carcinoma ovarico epiteliale, alle tube di Falloppio, peritoneale primario BRCA mutato Terapia di mantenimento A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Raccomandazioni evidence-based Olaparib Carcinoma ovarico epiteliale, alle tube di Falloppio, peritoneale primario BRCA mutato Terapia di mantenimento A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
nel carcinoma a cellule chiare del rene avanzato (I e II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Pazopanib nel carcinoma a cellule chiare del rene avanzato (I e II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.32 Direzione
Raccomandazioni evidence-based Pazopanib nel carcinoma a cellule chiare del rene avanzato (I e II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.32 Direzione
Romiplostim Eltrombopag
 Raccomandazioni evidence-based Romiplostim Eltrombopag Nella porpora trombocitopenica immunitaria (PTI) idiopatica A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazioni d uso n. 12 Settembre
Raccomandazioni evidence-based Romiplostim Eltrombopag Nella porpora trombocitopenica immunitaria (PTI) idiopatica A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazioni d uso n. 12 Settembre
Raccomandazioni evidence-based. Farmaci per il melanoma avanzato, non resecabile o metastatico. A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Farmaci per il melanoma avanzato, non resecabile o metastatico A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 54 Maggio 2016 Aggiornato a
Raccomandazioni evidence-based Farmaci per il melanoma avanzato, non resecabile o metastatico A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 54 Maggio 2016 Aggiornato a
Il ruolo delle Reti in tema di Sostenibilità. Giovanna Scroccaro Settore Farmaceutico Regione Veneto
 Il ruolo delle Reti in tema di Sostenibilità Giovanna Scroccaro Settore Farmaceutico Regione Veneto Roma, 23 maggio 2017 Farmaci ospedalieri 2016 Spesa per farmaci oncologici e oncoematologici Italia +8%*
Il ruolo delle Reti in tema di Sostenibilità Giovanna Scroccaro Settore Farmaceutico Regione Veneto Roma, 23 maggio 2017 Farmaci ospedalieri 2016 Spesa per farmaci oncologici e oncoematologici Italia +8%*
nel carcinoma a cellule transizionali del tratto uroteliale avanzato o metastatico (II linea di terapia)
 Raccomandazioni evidence-based Vinflunina nel carcinoma a cellule transizionali del tratto uroteliale avanzato o metastatico (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Raccomandazioni evidence-based Vinflunina nel carcinoma a cellule transizionali del tratto uroteliale avanzato o metastatico (II linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Temsirolimus. nel Linfoma a cellule mantellari refrattario e/o recidivante. Raccomandazioni evidence-based
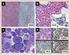 Raccomandazioni evidence-based Temsirolimus nel Linfoma a cellule mantellari refrattario e/o recidivante A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 20 giugno 2012 Direzione
Raccomandazioni evidence-based Temsirolimus nel Linfoma a cellule mantellari refrattario e/o recidivante A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 20 giugno 2012 Direzione
Tumore del polmone (Non Small Cell Lung Cancer) localmente avanzato o metastatico
 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) localmente avanzato o metastatico Gefitinib I e II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione
Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) localmente avanzato o metastatico Gefitinib I e II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione
Raccomandazioni evidence-based. Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia
 Raccomandazioni evidence-based Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d
Raccomandazioni evidence-based Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d
Una nuova visione per un nuovo orizzonte: criticità, proposte ed esperienze in una sanità che cambia Torino, novembre 2015
 Una nuova visione per un nuovo orizzonte: criticità, proposte ed esperienze in una sanità che cambia Torino, 20-21 novembre 2015 Il PTOR quale strumento di governance farmaceutica Maria Trapanese, Anna
Una nuova visione per un nuovo orizzonte: criticità, proposte ed esperienze in una sanità che cambia Torino, 20-21 novembre 2015 Il PTOR quale strumento di governance farmaceutica Maria Trapanese, Anna
Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto
 Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto Metodologia Farmaci Innovativi Metodologia Percorso Valutativo (dr. Alberto Bortolami-Coordinamento Rete Oncologica)
Alberto Bortolami Coordinamento Rete Oncologica del Veneto Istituto Oncologico Veneto Metodologia Farmaci Innovativi Metodologia Percorso Valutativo (dr. Alberto Bortolami-Coordinamento Rete Oncologica)
REGORAFENIB - STIVARGA
 giunta regionale Allegato A al Decreto n. 308 del 12 novembre 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED REGORAFENIB - STIVARGA Indicazione in esame: è indicato
giunta regionale Allegato A al Decreto n. 308 del 12 novembre 2015 pag. 1/9 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED REGORAFENIB - STIVARGA Indicazione in esame: è indicato
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE. Reggio Emilia 4 giugno 2008
 O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
Carcinoma basocellualare metastatico o in stadio localmente avanzato. A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Vismodegib Carcinoma basocellualare metastatico o in stadio localmente avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 42 Direzione
Raccomandazioni evidence-based Vismodegib Carcinoma basocellualare metastatico o in stadio localmente avanzato A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 42 Direzione
Leucemia linfatica cronica (LLC) (I e II linea di terapia). Idelalisib+rituximab Ibrutinib
 Raccomandazioni evidence-based Leucemia linfatica cronica (LLC) (I e II linea di terapia). Idelalisib+rituximab Ibrutinib A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.
Raccomandazioni evidence-based Leucemia linfatica cronica (LLC) (I e II linea di terapia). Idelalisib+rituximab Ibrutinib A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.
Ca della Mammella : Gli strumenti di governo clinico e la vigilanza da parte della farmacia. Paola Fiacchi. Farmacia Puggioli.
 Ca della Mammella : Gli strumenti di governo clinico e la vigilanza da parte della farmacia Paola Fiacchi Farmacia Puggioli 19 ottobre 2010 clinical governance (governo clinico) politica sanitaria orientata
Ca della Mammella : Gli strumenti di governo clinico e la vigilanza da parte della farmacia Paola Fiacchi Farmacia Puggioli 19 ottobre 2010 clinical governance (governo clinico) politica sanitaria orientata
CARCINOMA DELLA MAMMELLA CORSO EDUCAZIONALE INTERATTIVO
 [ Corso Residenziale ] CARCINOMA DELLA MAMMELLA 2009 9 CORSO EDUCAZIONALE INTERATTIVO 12 giugno 2009 1 di 1 [ Programma preliminare] Venerdì 12 giugno ore 09.45 Presentazione Guido Biasco, Andrea Martoni,
[ Corso Residenziale ] CARCINOMA DELLA MAMMELLA 2009 9 CORSO EDUCAZIONALE INTERATTIVO 12 giugno 2009 1 di 1 [ Programma preliminare] Venerdì 12 giugno ore 09.45 Presentazione Guido Biasco, Andrea Martoni,
Jennifer Foglietta Oncologia medica- Perugia
 QUESITO GRADE 3: Nelle pazienti operate con carcinoma mammario HR+ in premenopausa, il trattamento ormonale adiuvante con exemestane +soppressione ovarica è raccomandato rispetto a tamoxifen + soppressione
QUESITO GRADE 3: Nelle pazienti operate con carcinoma mammario HR+ in premenopausa, il trattamento ormonale adiuvante con exemestane +soppressione ovarica è raccomandato rispetto a tamoxifen + soppressione
Farmaci per il carcinoma della prostata metastatico castrazione resistente
 Raccomandazioni evidence-based Farmaci per il carcinoma della prostata metastatico castrazione resistente Abiraterone-Cabazitaxel-Enzalutamide A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
Raccomandazioni evidence-based Farmaci per il carcinoma della prostata metastatico castrazione resistente Abiraterone-Cabazitaxel-Enzalutamide A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
CRITERI PER LA VALUTAZIONE DEI FARMACI C(nn) DA PARTE DELLA COMMISSIONE REGIONALE DEL FARMACO (CRF)
 Direzione Generale Cura della Persona, Salute e Welfare Commissione Regionale Farmaco (D.G.R. 1540/2006 e 392/2015) Documento PTR n. 211 relativo a: CRITERI PER LA VALUTAZIONE DEI FARMACI C(nn) DA PARTE
Direzione Generale Cura della Persona, Salute e Welfare Commissione Regionale Farmaco (D.G.R. 1540/2006 e 392/2015) Documento PTR n. 211 relativo a: CRITERI PER LA VALUTAZIONE DEI FARMACI C(nn) DA PARTE
Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile. Erlotinib II linea di terapia. Raccomandazioni d'uso. Documento PTR n.
 Documento PTR n.131 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile Erlotinib II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Documento PTR n.131 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile Erlotinib II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna
 PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO DELLA FASE AVANZATA DEI TUMORI DEL COLON RETTO E STOMACO RACCOMANDAZIONE sull impiego della chemioterapia locoregionale
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO DELLA FASE AVANZATA DEI TUMORI DEL COLON RETTO E STOMACO RACCOMANDAZIONE sull impiego della chemioterapia locoregionale
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 Presentata da RICHIESTA DI INSERIMENTO IN PTR DI SUNITINIB ATC L01XE04 ( SUTENT ) Componente Commissione per il Prontuario Terapeutico Regionale In data Febbraio 2007 Per le seguenti motivazioni (sintesi):
Presentata da RICHIESTA DI INSERIMENTO IN PTR DI SUNITINIB ATC L01XE04 ( SUTENT ) Componente Commissione per il Prontuario Terapeutico Regionale In data Febbraio 2007 Per le seguenti motivazioni (sintesi):
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR SUNITINIB
 Presentata da RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE04 (SUTENT ) Componente Commissione per il Prontuario Terapeutico Regionale In data Febbraio 2007 Per le seguenti motivazioni (sintesi): Sutent
Presentata da RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE04 (SUTENT ) Componente Commissione per il Prontuario Terapeutico Regionale In data Febbraio 2007 Per le seguenti motivazioni (sintesi): Sutent
Tumore gastrico Metastatico o non operabile. trastuzumab I linea di terapia. Raccomandazioni d'uso. Documento PTR n.132
 Documento PTR n.132 Raccomandazioni d'uso Tumore gastrico Metastatico o non operabile trastuzumab I linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni
Documento PTR n.132 Raccomandazioni d'uso Tumore gastrico Metastatico o non operabile trastuzumab I linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni
PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA
 PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA Unità destinatarie e competenze Urologia (prevenzione, diagnosi e stadiazione), trattamento, riabilitazione,
PERCORSO DIAGNOSTICO TERAPEUTICO ASSISTENZIALE (PDTA) PER I PAZIENTI AFFETTI DA CARCINOMA DELLA PROSTATA Unità destinatarie e competenze Urologia (prevenzione, diagnosi e stadiazione), trattamento, riabilitazione,
Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici. Dr Andrea Rocchi Oncologia-Foligno
 Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici Dr Andrea Rocchi Oncologia-Foligno Carcinoma del colon: Bevacizumab I e II linea Aflibercept II linea Panitumumab I, II, III linea Carcinoma
Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici Dr Andrea Rocchi Oncologia-Foligno Carcinoma del colon: Bevacizumab I e II linea Aflibercept II linea Panitumumab I, II, III linea Carcinoma
BEVACIZUMAB - AVASTIN
 giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
Le principali tappe dell EBM
 Le principali tappe dell EBM 1. La formulazione del quesito clinico in termini chiari; 2. La ricerca sistematica ed esaustiva delle prove nella letteratura medica, 3. La loro interpretazione critica, 4.
Le principali tappe dell EBM 1. La formulazione del quesito clinico in termini chiari; 2. La ricerca sistematica ed esaustiva delle prove nella letteratura medica, 3. La loro interpretazione critica, 4.
Colchicina nella prevenzione degli eventi cardiovascolari
 Revisione Cochrane 2016 Colchicina nella prevenzione degli eventi cardiovascolari Hemkens LG, Ewald H, Gloy VL, et al. Colchicine for prevention of cardiovascular events. Cochrane Database Syst Rev 2016;1:CD011047.
Revisione Cochrane 2016 Colchicina nella prevenzione degli eventi cardiovascolari Hemkens LG, Ewald H, Gloy VL, et al. Colchicine for prevention of cardiovascular events. Cochrane Database Syst Rev 2016;1:CD011047.
Corso: La Ricerca Bibliografica Biomedica con PubMed. La qualità delle pubblicazioni scientifiche
 Corso: La Ricerca Bibliografica Biomedica con PubMed La qualità delle pubblicazioni scientifiche 23 maggio 2012 L organizazzione della documentazione La piramide delle 6 S Sistemi Summaries Sinossi delle
Corso: La Ricerca Bibliografica Biomedica con PubMed La qualità delle pubblicazioni scientifiche 23 maggio 2012 L organizazzione della documentazione La piramide delle 6 S Sistemi Summaries Sinossi delle
REGIONE EMILIA-ROMAGNA Atti amministrativi
 REGIONE EMILIA-ROMAGNA Atti amministrativi GIUNTA REGIONALE Atto del Dirigente: DETERMINAZIONE n 16179 del 13/12/2011 Proposta: DPG/2011/16852 del 05/12/2011 Struttura proponente: Oggetto: Autorità emanante:
REGIONE EMILIA-ROMAGNA Atti amministrativi GIUNTA REGIONALE Atto del Dirigente: DETERMINAZIONE n 16179 del 13/12/2011 Proposta: DPG/2011/16852 del 05/12/2011 Struttura proponente: Oggetto: Autorità emanante:
(Non Small Cell Lung Cancer)
 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Bevacizumab A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni evidence based Direzione Generale
Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Bevacizumab A cura del Gruppo Regionale Farmaci Oncologici (GReFO) per l'elaborazione di raccomandazioni evidence based Direzione Generale
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna
 PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO ADIUVANTE DEI TUMORI DEL COLON RETTO RACCOMANDAZIONE sull utilizzo della chemio-radioterapia nella fase pre-operatoria
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO ADIUVANTE DEI TUMORI DEL COLON RETTO RACCOMANDAZIONE sull utilizzo della chemio-radioterapia nella fase pre-operatoria
Il Metodo GRADE per la formulazione di raccomandazioni
 VI convegno PREVENIRE LE COMPLICANZE DEL DIABETE: DALLA RICERCA DI BASE ALL ASSISTENZA Istituto Superiore di Sanità Roma, 5-6 marzo 2012 Il Metodo GRADE per la formulazione di raccomandazioni L esperienza
VI convegno PREVENIRE LE COMPLICANZE DEL DIABETE: DALLA RICERCA DI BASE ALL ASSISTENZA Istituto Superiore di Sanità Roma, 5-6 marzo 2012 Il Metodo GRADE per la formulazione di raccomandazioni L esperienza
Questione farmaci oncologici ad alto costo
 Per un nuovo Codice di Deontologia Medica Giornata di studio Pistoia, 18 gennaio 2014 Questione farmaci oncologici ad alto costo Giuseppe Traversa Centro Nazionale di Epidemiologia, Sorveglianza e Prevenzione
Per un nuovo Codice di Deontologia Medica Giornata di studio Pistoia, 18 gennaio 2014 Questione farmaci oncologici ad alto costo Giuseppe Traversa Centro Nazionale di Epidemiologia, Sorveglianza e Prevenzione
Raccomandazioni sui farmaci per il diabete: monitoraggio regionale basato su indicatori di prescrizione
 IGEA: dal progetto al sistema L'integrazione delle cure per le persone con malattie croniche Istituto Superiore di Sanità, Roma 22 aprile 2013 Raccomandazioni sui farmaci per il diabete: monitoraggio regionale
IGEA: dal progetto al sistema L'integrazione delle cure per le persone con malattie croniche Istituto Superiore di Sanità, Roma 22 aprile 2013 Raccomandazioni sui farmaci per il diabete: monitoraggio regionale
Finalità della Rete Oncologica Veneta PierFranco Conte Coordinatore ROV
 Finalità della Rete Oncologica Veneta PierFranco Conte Coordinatore ROV Reasons why a new model of governance is needed Quality of Care no «magic» number; volume & speciality are associated with better
Finalità della Rete Oncologica Veneta PierFranco Conte Coordinatore ROV Reasons why a new model of governance is needed Quality of Care no «magic» number; volume & speciality are associated with better
Innovatività per i pazienti
 Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
IX Congresso del Gruppo Oncologico Chirurgico Cooperativo Italiano
 Gruppo Oncologico Chirurgico Cooperativo Italiano IX Congresso del Gruppo Oncologico Chirurgico Cooperativo Italiano Terapie Mediche Innovative in Oncologia Firenze, 21-22 settembre 2017 Aula Magna del
Gruppo Oncologico Chirurgico Cooperativo Italiano IX Congresso del Gruppo Oncologico Chirurgico Cooperativo Italiano Terapie Mediche Innovative in Oncologia Firenze, 21-22 settembre 2017 Aula Magna del
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Allegato A al Decreto n. 139 del 3 giugno 2015 pag. 1/10. Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED AFLIBERCEPT ZALTRAP
 giunta regionale Allegato A al Decreto n. 139 del 3 giugno 2015 pag. 1/10 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED AFLIBERCEPT ZALTRAP Indicazione in esame: Aflibercept (Zaltrap
giunta regionale Allegato A al Decreto n. 139 del 3 giugno 2015 pag. 1/10 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED AFLIBERCEPT ZALTRAP Indicazione in esame: Aflibercept (Zaltrap
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Le prescrizioni terapeutiche cambiano con lo screening mammografico? Studio osservazionale a Reggio Emilia
 Le prescrizioni terapeutiche cambiano con lo screening mammografico? Studio osservazionale a Reggio Emilia Pamela Mancuso 1,2, Massimo Vicentini 1,2, Francesca Ferrari 1,2, Moira Ragazzi 3, Stefania Caroli
Le prescrizioni terapeutiche cambiano con lo screening mammografico? Studio osservazionale a Reggio Emilia Pamela Mancuso 1,2, Massimo Vicentini 1,2, Francesca Ferrari 1,2, Moira Ragazzi 3, Stefania Caroli
Uso appropriato e sicuro dei medicinali nei pazienti anziani trattati in ambito territoriale o istituzionalizzati in case residenza per anziani
 Progetto Multicentrico Regionale di Farmacovigilanza Attiva (Fondi AIFA 2010-2011) Uso appropriato e sicuro dei medicinali nei pazienti anziani trattati in ambito territoriale o istituzionalizzati in case
Progetto Multicentrico Regionale di Farmacovigilanza Attiva (Fondi AIFA 2010-2011) Uso appropriato e sicuro dei medicinali nei pazienti anziani trattati in ambito territoriale o istituzionalizzati in case
Linfoma Mantellare, recidivato o refrattario, dopo una prima linea di terapia Ibrutinib, temsirolimus
 Raccomandazioni evidence-based Linfoma Mantellare, recidivato o refrattario, dopo una prima linea di terapia Ibrutinib, temsirolimus A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
Raccomandazioni evidence-based Linfoma Mantellare, recidivato o refrattario, dopo una prima linea di terapia Ibrutinib, temsirolimus A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione
decitabina Leucemia mieloide acuta (LMA) (I linea di terapia) Raccomandazioni evidence-based A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based decitabina Leucemia mieloide acuta (LMA) (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 43 Aprile 2015 Direzione Generale
Raccomandazioni evidence-based decitabina Leucemia mieloide acuta (LMA) (I linea di terapia) A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n. 43 Aprile 2015 Direzione Generale
PROTOCOLLI GOIRC-SPONSORED FARM6PMFJM
 PROTOCOLLI -SPONSORED FARM6PMFJM Multicenter phase III randomized study of cisplatin and etoposide with or without bevacizumab as first-line treatment in extensive stage (ED) small cell lung cancer (SCLC).
PROTOCOLLI -SPONSORED FARM6PMFJM Multicenter phase III randomized study of cisplatin and etoposide with or without bevacizumab as first-line treatment in extensive stage (ED) small cell lung cancer (SCLC).
Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia
 Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia Gruppo di Studio sul carcinoma del colon-retto Coordinatore: Patrizia Racca Comitato Estensore: F. Leone, P. Racca,
Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia Gruppo di Studio sul carcinoma del colon-retto Coordinatore: Patrizia Racca Comitato Estensore: F. Leone, P. Racca,
Gestione del Pap test anormale
 Ferrara 10 giugno 2009 Gestione del Pap test anormale PAOLA GARUTTI Azienda Ospedaliera Universitaria S.Anna Ferrara Clinica Ostetrica e Ginecologica Direttore Prof. A. Patella Gestione del Pap test anormale
Ferrara 10 giugno 2009 Gestione del Pap test anormale PAOLA GARUTTI Azienda Ospedaliera Universitaria S.Anna Ferrara Clinica Ostetrica e Ginecologica Direttore Prof. A. Patella Gestione del Pap test anormale
Diagnosi precoce: utopia o realtà?
 Diagnosi precoce: utopia o realtà? Valter Torri Laboratorio di Metodologia per la Ricerca Clinica Dipartimento di Oncologia Istituto di Ricerche Farmacologiche Mario Negri IRCCS, Milano è il 3% del totale
Diagnosi precoce: utopia o realtà? Valter Torri Laboratorio di Metodologia per la Ricerca Clinica Dipartimento di Oncologia Istituto di Ricerche Farmacologiche Mario Negri IRCCS, Milano è il 3% del totale
PROGETTO DI RIORGANIZZAZIONE DELLE ATTIVITA DI RADIOTERAPIA IN AMBITO METROPOLITANO
 PROGETTO DI RIORGANIZZAZIONE DELLE ATTIVITA DI RADIOTERAPIA IN AMBITO METROPOLITANO Giovanni Frezza Direttore UO di Radioterapia Oncologica Azienda USL di Bologna Documento presentato, discusso ed approvato
PROGETTO DI RIORGANIZZAZIONE DELLE ATTIVITA DI RADIOTERAPIA IN AMBITO METROPOLITANO Giovanni Frezza Direttore UO di Radioterapia Oncologica Azienda USL di Bologna Documento presentato, discusso ed approvato
I dati dell Emilia-Romagna sul fine vita in pazienti oncologici
 I dati dell Emilia-Romagna sul fine vita in pazienti oncologici Rossana De Palma, Daniela Fortuna Regione Emilia-Romagna Firenze 18 luglio 2017 L assistenza nel fine vita uno studio regionale basato su
I dati dell Emilia-Romagna sul fine vita in pazienti oncologici Rossana De Palma, Daniela Fortuna Regione Emilia-Romagna Firenze 18 luglio 2017 L assistenza nel fine vita uno studio regionale basato su
PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO. Fausto Roila Oncologia Medica, Perugia
 PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO Fausto Roila Oncologia Medica, Perugia LA NECESSITA DI UNA RICERCA INDIPENDENTE L industria promuove studi di sviluppo del farmaco per registrarlo (talora
PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO Fausto Roila Oncologia Medica, Perugia LA NECESSITA DI UNA RICERCA INDIPENDENTE L industria promuove studi di sviluppo del farmaco per registrarlo (talora
Novità in tema di neoplasia mammaria
 Cattolica Sala Snaporaz sabato 17 maggio 2014 Novità in tema di neoplasia mammaria Sezione Regionale Emilia Romagna Cattolica Sala Snaporaz sabato 17 maggio 2014 Novità in tema di neoplasia mammaria scheda
Cattolica Sala Snaporaz sabato 17 maggio 2014 Novità in tema di neoplasia mammaria Sezione Regionale Emilia Romagna Cattolica Sala Snaporaz sabato 17 maggio 2014 Novità in tema di neoplasia mammaria scheda
I Registri Tumori un patrimonio per la Sanità Pubblica e la Ricerca in Oncologia. Carmine Pinto
 XX Riunione Scientifica Annuale AIRTUM Reggio Emilia, 13 Aprile 1016 I Registri Tumori un patrimonio per la Sanità Pubblica e la Ricerca in Oncologia Carmine Pinto Presidente Nazionale AIOM Oncologia Medica
XX Riunione Scientifica Annuale AIRTUM Reggio Emilia, 13 Aprile 1016 I Registri Tumori un patrimonio per la Sanità Pubblica e la Ricerca in Oncologia Carmine Pinto Presidente Nazionale AIOM Oncologia Medica
PierFranco Conte Coordinatore
 PierFranco Conte Coordinatore Rete Oncologica del Veneto Istituita dalla Regione Veneto con Deliberazione della Giunta Regionale n. 2067 del 19.11.2013. Con Decreto n. 23 del 17.3.2016 la Regione Veneto
PierFranco Conte Coordinatore Rete Oncologica del Veneto Istituita dalla Regione Veneto con Deliberazione della Giunta Regionale n. 2067 del 19.11.2013. Con Decreto n. 23 del 17.3.2016 la Regione Veneto
Ricette di ricerca Come fare una ricerca bibliografica di successo ADE. Corso di laurea B a.a. 2013/2014
 Ricette di ricerca Come fare una ricerca bibliografica di successo ADE Corso di laurea B a.a. 2013/2014 Prof. V. Trischitta Dott. E. Giannetta RICERCA BIBLIOGRAFICA 1.QUESITO CLINICO: Effetti del sildenafil
Ricette di ricerca Come fare una ricerca bibliografica di successo ADE Corso di laurea B a.a. 2013/2014 Prof. V. Trischitta Dott. E. Giannetta RICERCA BIBLIOGRAFICA 1.QUESITO CLINICO: Effetti del sildenafil
Principali criteri per valutare la qualità di una revisione sistematica
 Principali criteri per valutare la qualità di una revisione sistematica A cura di Luca Ronfani Adattato da: Oxman AD, et al. Users' guides to the medical literature. VI. How to use an overview. JAMA 1994;
Principali criteri per valutare la qualità di una revisione sistematica A cura di Luca Ronfani Adattato da: Oxman AD, et al. Users' guides to the medical literature. VI. How to use an overview. JAMA 1994;
Progetti di Ricerca Regionale sugli indicatori di monitoraggio
 Progetti di Ricerca Regionale sugli indicatori di monitoraggio Paolo Morandi U.O.C. Oncologia Medica Mestre Venezia Alberto Bortolami ROV-Istituto Oncologico Veneto, Padova Emilio Bria Dipartimento di
Progetti di Ricerca Regionale sugli indicatori di monitoraggio Paolo Morandi U.O.C. Oncologia Medica Mestre Venezia Alberto Bortolami ROV-Istituto Oncologico Veneto, Padova Emilio Bria Dipartimento di
Studio SENIORS Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza
 Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
MEDICINA BASATA SULL EVIDENZA (EBM)
 www.fisiokinesiterapia.biz MEDICINA BASATA SULL EVIDENZA (EBM) JAMA 1992;268:2420-2425 Evidence-Based Medicine Working Group Evidence-based medicine. A new approach to teaching the practice of medicine.
www.fisiokinesiterapia.biz MEDICINA BASATA SULL EVIDENZA (EBM) JAMA 1992;268:2420-2425 Evidence-Based Medicine Working Group Evidence-based medicine. A new approach to teaching the practice of medicine.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs
 Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
L aggiornamento pubblicato nel marzo del 2007 è stato integrato con la pubblicazione della prima lista di farmaci essenziali ad uso pediatrico
 Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Requisiti essenziali per la gestione integrata del diabete mellito di tipo 2 nell'adulto AGGIORNAMENTO 2010 ASPETTI METODOLOGICI.
 Requisiti essenziali per la gestione integrata del diabete mellito di tipo 2 nell'adulto AGGIORNAMENTO 2010 ASPETTI METODOLOGICI Francesco Nonino Documento di indirizzo 2008 Il trattamento intensivo mirato
Requisiti essenziali per la gestione integrata del diabete mellito di tipo 2 nell'adulto AGGIORNAMENTO 2010 ASPETTI METODOLOGICI Francesco Nonino Documento di indirizzo 2008 Il trattamento intensivo mirato
La produzione di raccomandazioni cliniche con il metodo GRADE
 3. Il metodo GRADE La breve presentazione del metodo GRADE contenuta in questo Capitolo è di necessità schematica. In particolare nel testo e negli esempi che vengono presentati ci si è concentrati sull
3. Il metodo GRADE La breve presentazione del metodo GRADE contenuta in questo Capitolo è di necessità schematica. In particolare nel testo e negli esempi che vengono presentati ci si è concentrati sull
Screening neonatale della DISPLASIA EVOLUTIVA DELL ANCA (D.E.A) Raccomandazioni
 Screening neonatale della DISPLASIA EVOLUTIVA DELL ANCA (D.E.A) Raccomandazioni Aprile 2010 Gruppo di studio per l elaborazione delle raccomandazioni: Paola Dalla Casa Dante Baronciani Giuseppe Atti Fabrizio
Screening neonatale della DISPLASIA EVOLUTIVA DELL ANCA (D.E.A) Raccomandazioni Aprile 2010 Gruppo di studio per l elaborazione delle raccomandazioni: Paola Dalla Casa Dante Baronciani Giuseppe Atti Fabrizio
DECRETO N. 02 DEL 9 marzo Nomina Commissione per il Prontuario Terapeutico Regionale.
 L Assessore DECRETO N. 02 DEL 9 marzo 2006 Oggetto: Nomina Commissione per il Prontuario Terapeutico Regionale. VISTO lo Statuto Speciale per la Regione Sarda e le relative norme di attuazione; VISTO l
L Assessore DECRETO N. 02 DEL 9 marzo 2006 Oggetto: Nomina Commissione per il Prontuario Terapeutico Regionale. VISTO lo Statuto Speciale per la Regione Sarda e le relative norme di attuazione; VISTO l
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine
 Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
