Lezione 7. Cenni di struttura della materia.
|
|
|
- Eva Conte
- 6 anni fa
- Visualizzazioni
Transcript
1 Lezione 7 Cenni di struttura della materia.
2 Particelle La materia è costituita da particelle (atomi e molecole), legate da forze di natura elettromagnetica per formare i corpi materiali. I corpi materiali, a loro volta, si differenziano poi a seconda dell entità di tali forze.
3 I mattoni della materia: p,n,e Protoni (p), neutroni (n) ed elettroni (e) sono i mattoni più grossolani di cui è fatta la materia. Essi si aggregano formando atomi, ovvero strutture più o meno stabili presenti nel nostro universo. In realtà oggi sappiamo che n,p non sono costituenti elementari ma sono composti di quark (3 quark per ciascuno), i veri mattoni elementari di cui è costituita la materia.
4 Composizione a quark p = u u d n = u d d
5 Proprietà dei quark
6 Carica elettrica p ed e sono elettricamente carichi e possono quindi interagire elettricamente. n sono neutri e la loro presenza nell atomo è necessaria per assicurarne la stabilità. Gli atomi sono elettricamente neutri (non privi di cariche ma con cariche positive e negative presenti in ugual numero).
7 Elementi naturali Attualmente gli elementi naturali (cioè presenti in natura) sono 92. Ad essi, fino ad oggi, bisogna aggiungere altri 15 elementi (transuranici) creati dall uomo, l ultimo dei quali, l elemento 107, è stato sintetizzato solo nel 1977 (Flerov, Dubna, Russia). Poiché gli elementi sono circa 100 anche le specie atomiche sono circa 100. Esempio: potete pensare alle specie atomiche come alle lettere dell alfabeto: le prime si compongono a formare ogni varietà di materia; con le ultime possiamo formare ogni parola.
8 Struttura atomica degli elementi In natura esistono elementi (es. i gas nobili) il cui macroelemento chimico è formato da un solo atomo ed altri (es. zolfo, fosforo, etc.) per cui è formato da due o più atomi della stessa specie; altri ancora (es. sostanze organiche) il cui macroelemento chimico è formato da migliaia o milioni di atomi, anche di specie diversa. L unione di due o più atomi della stessa specie o di specie diverse si chiama molecola.
9 Molecole A seconda della propria struttura (disposizione elettronica) gli atomi possono legarsi (legame chimico) tra loro a formare le molecole. In generale, una molecola si può ancora considerare una parte elementare del corpo che risulta pertanto formato da un grandissimo numero di molecole identiche.
10 Interazione molecolare In generale, le molecole si attraggono o respingono reciprocamente con forze che dipendono dalla distanza, per effetto delle forze elettriche agenti a livello atomico.
11 Modello di interazione molecolare: particelle immobili Tra due molecole che interagiscono esiste una distanza di equilibrio d 0 che rappresenta la condizione in cui forze attrattive e repulsive si equivalgono. Il tentativo di avvicinarle fa nascere forze repulsive subito molto intense; quello di allontanarle fa nascere forze attrattive, di intensità però decrescente all aumentare della distanza.
12 Solidi I solidi sono quei corpi in cui le molecole sono effettivamente in tale condizione: le forze tra le varie molecole mantengono le molecole mediamente alla stessa distanza. Pertanto il corpo conserva forma e volume. Inoltre, se soggetto ad una sollecitazione esterna il corpo subisce una deformazione elastica, ovvero terminata l azione esterna il corpo tende a riportarsi nella configurazione iniziale.
13 Agitazione termica Il modello esposto rappresenta una schematizzazione drastica della situazione. A livello microscopico infatti tutte le particelle costituenti il corpo sono animate da un moto disordinato detto di agitazione termica. N.B. A causa dell agitazione termica non possiamo osservare direttamente le singole molecole.
14 Temperatura Dal punto di vista macroscopico l agitazione termica è misurabile mediante la temperatura. Maggiore agitazione termica Maggiore energia cinetica delle molecole Maggiore temperatura.
15 Critica al modello delle particelle immobili Il modello delle particelle immobili è praticamente irrealizzabile. La distanza di equilibrio deve essere considerata una distanza media attorno alla quale le molecole realizzano il loro moto di agitazione termica. Se aumenta l agitazione termica, aumenta pure il valore della distanza media di equilibrio: le molecole possono avvicinarsi tra loro però con maggiore difficoltà di quanto è invece consentito per allontanarsi. Segue un aumento delle dimensioni del corpo che è noto come dilatazione termica.
16 Stati di aggregazione della materia L aumentare (con l agitazione termica) della distanza media tra le particelle porta alla situazione in cui le forze di richiamo (attrattive) perdono di intensità e le particelle stesse possono considerarsi autonome cioè poco o addirittura non interagenti. Il corpo perde così le caratteristiche del solido e può passare agli stati di liquido prima e di aeriforme o gas poi. Dunque: la materia si presenta in tre stati: solido, liquido e aeriforme a seconda della diversa intensità delle forze che si esercitano tra le molecole che costituiscono il corpo.
17 Stato solido:i Rappresentazione schematica di aggregazione molecolare allo stato solido.
18 Stato solido:ii I solidi hanno forma e volume proprio. Nei solidi il moto molecolare si riduce ad una serie di rapide oscillazioni attorno ad alcuni particolari centri di equilibrio (punti nodali).
19 Stato liquido: I Rappresentazione schematica di aggregazione molecolare allo stato liquido.
20 Stato liquido: II I liquidi hanno volume proprio e forma dipendente dal sistema che li contiene. Nei liquidi le molecole, mantenendo praticamente invariate le distanze mutue, possono scorrere a gruppi, mescolandosi continuamente e riuscendo talvolta anche a sfuggire dal recipiente che li contiene (evaporazione).
21 Stato gassoso: I Rappresentazione schematica di aggregazione molecolare allo stato gassoso.
22 Stato gassoso: II I gas hanno forma e volume dipendenti dal sistema che li contiene. Nei gas le molecole sono molto distanziate tra loro e sono in moto rapidissimo e disordinato (agitazione termica).
23 Plasma In realtà, oltre alle 3 fasi (S,L,G) esiste un quarto stato di aggregazione detto plasma, corrispondente alla situazione per cui a causa di elevetissime temperature gli atomi si scindono nei loro costituendi, nuclei, protoni, elettroni. Il plasma è dunque un insieme di particelle con carica totale nulla che è molto difficile da mantenere in laboratorio ma che costituisce lo stato più diffuso di materia stellare.
24 Fluidi = liquidi e gas Liquidi e gas si dicono genericamente fluidi. La differenza fondamentale tra solidi e fluidi è che nel primo caso le molecole hanno una disposizione definita (reticolo) mentre nel secondo caso no. Mentre per descrivere il moto di un solido si puo pensare di adattare la descrizione vista per un punto materiale (tutti i punti materiali costituenti sono rigidamente collegati) per descrivere il moto di un fluido occorre pensare a modalità diverse di azione di forze (esempio non applicate ad un singolo punto ma applicate a tutta una superficie o un volume).
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
LA STRUTTURA DELLA MATERIA
 LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 4 Le teorie 1. L atomo e la sua storia 2. La nascita della moderna teoria atomica: da Lavoiser
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 4 Le teorie 1. L atomo e la sua storia 2. La nascita della moderna teoria atomica: da Lavoiser
Fenomeno fisico. Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici
 Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Chimica. Gli stati di aggregazione della materia
 Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
Chimica Gli stati di aggregazione della materia La materia si presenta in natura in tre modelli di aggregazione dei suoi costituenti (atomi, molecole o ioni): solido, liquido, aeriforme. Da un punto di
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
FONDAMENTI DI CHIMICA
 FONDAMENTI DI CHIMICA LA CHIMICA E UNA BRANCA DELLA SCIENZA CHE STUDIA LA COMPOSIZIONE DELLA MATERIA E DELLE SOSTANZE, LE LORO PROPRIETA E LE LORO TRASFORMAZIONI IN ALTRE SOSTANZE ED ELEMENTI E/O IN ENERGIA
FONDAMENTI DI CHIMICA LA CHIMICA E UNA BRANCA DELLA SCIENZA CHE STUDIA LA COMPOSIZIONE DELLA MATERIA E DELLE SOSTANZE, LE LORO PROPRIETA E LE LORO TRASFORMAZIONI IN ALTRE SOSTANZE ED ELEMENTI E/O IN ENERGIA
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 4 Le teorie della materia 3 Sommario 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 4 Le teorie della materia 3 Sommario 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI
 ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
Corso di CHIMICA LEZIONE 1
 Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
IL CALORE LA TEMPERATURA E I PASSAGGI DI STATO
 IL CALORE LA TEMPERATURA E I PASSAGGI DI STATO IL CALORE Se metti a contatto un oggetto meno caldo (acqua) con uno più caldo (chiodo), dopo un po di tempo quello meno caldo tende a scaldarsi e quello più
IL CALORE LA TEMPERATURA E I PASSAGGI DI STATO IL CALORE Se metti a contatto un oggetto meno caldo (acqua) con uno più caldo (chiodo), dopo un po di tempo quello meno caldo tende a scaldarsi e quello più
Elettrizzazione Progetto creato da: Alessandro Stracqualursi, Loriga Davide, Evangelio Giancarlo e Nistor Massimo
 Elettrizzazione Progetto creato da: Alessandro Stracqualursi, Loriga Davide, Evangelio Giancarlo e Nistor Massimo Elettrizzazione definizione: L elettrizzazione è un fenomeno che avviene tra due corpi
Elettrizzazione Progetto creato da: Alessandro Stracqualursi, Loriga Davide, Evangelio Giancarlo e Nistor Massimo Elettrizzazione definizione: L elettrizzazione è un fenomeno che avviene tra due corpi
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Chimica. La Chimica è la scienza che cerca di comprendere il comportamento della materia studiando il comportamento di atomi e molecole
 Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica. La Chimica è la scienza che cerca di comprendere il comportamento della materia studiando il comportamento di atomi e molecole
 Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello
 Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
Atomi e molecole. Gli atomi degli elementi si trovano in natura generalmente combinati tra loro in molecole o composti ionici
 IL LEGAME CHIMICO Atomi e molecole È estremamente difficile trovare in natura una sostanza formata da singoli atomi isolati Solo i gas nobili sono presenti in natura come gas monoatomici Gli atomi degli
IL LEGAME CHIMICO Atomi e molecole È estremamente difficile trovare in natura una sostanza formata da singoli atomi isolati Solo i gas nobili sono presenti in natura come gas monoatomici Gli atomi degli
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
A1.1 Elettrostatica. Particella Carica elettrica Massa. Elettrone 1,602 x C 9,108 x kg. Protone 1,602 x C 1,672 x kg
 A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
14. Transizioni di Fase_a.a. 2009/2010 TRANSIZIONI DI FASE
 TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
10. LA MISURA DELLA TEMPERATURA
 1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno 5. Legami a confronto
 Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
LE TEORIE DELLA MATERIA
 IL CONCETTO DIATOMO HA RADICI ANTICHE LE TEORIE DELLA MATERIA FILOSOFI GRECI: LEUCIPPO circa 450 a.c. La materia non è continua ma è formata da particelle piccolissime. DEMOCRITO circa 400 a.c. discepolo
IL CONCETTO DIATOMO HA RADICI ANTICHE LE TEORIE DELLA MATERIA FILOSOFI GRECI: LEUCIPPO circa 450 a.c. La materia non è continua ma è formata da particelle piccolissime. DEMOCRITO circa 400 a.c. discepolo
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia
 Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
LA CARICA ELETTRICA E LA LEGGE DI COULOMB V CLASSICO PROF.SSA DELFINO M. G.
 LA CARICA ELETTRICA E LA LEGGE DI COULOMB 1 V CLASSICO PROF.SSA DELFINO M. G. UNITÀ 1 - LA CARICA ELETTRICA E LA LEGGE DI COULOMB 1. Le cariche elettriche 2. La legge di Coulomb 2 LEZIONE 1 - LE CARICHE
LA CARICA ELETTRICA E LA LEGGE DI COULOMB 1 V CLASSICO PROF.SSA DELFINO M. G. UNITÀ 1 - LA CARICA ELETTRICA E LA LEGGE DI COULOMB 1. Le cariche elettriche 2. La legge di Coulomb 2 LEZIONE 1 - LE CARICHE
La CHIMICA, come tutte le scienze, ha un suo LINGUAGGIO e un METODO
 La CHIMICA, come tutte le scienze, ha un suo LINGUAGGIO e un METODO La Chimica è lo studio delle trasformazioni della materia La materia è Tutto ciò che ha massa Tutto ciò che occupa spazio Tutto ciò che
La CHIMICA, come tutte le scienze, ha un suo LINGUAGGIO e un METODO La Chimica è lo studio delle trasformazioni della materia La materia è Tutto ciò che ha massa Tutto ciò che occupa spazio Tutto ciò che
La Dinamica. Principi fondamentali. Le Forze. Lezione 4
 La Dinamica. Principi fondamentali. Le Forze. Lezione 4 Dinamica La Dinamica studia il movimento indagandone le cause, ovvero considera quali sono le cause che determinano qualche effetto sul movimento.
La Dinamica. Principi fondamentali. Le Forze. Lezione 4 Dinamica La Dinamica studia il movimento indagandone le cause, ovvero considera quali sono le cause che determinano qualche effetto sul movimento.
Introduzione alla Chimica. Paolo Mazza
 Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Gli stati di aggregazione della materia.
 Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto
 1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
La misura della temperatura
 Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Capitolo 4 Le teorie della materia
 Atomo: Prime Teorie Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria atomica spiega le leggi ponderali 4. La teoria atomica e le
Atomo: Prime Teorie Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria atomica spiega le leggi ponderali 4. La teoria atomica e le
Per esempio, possiamo osservare il legame ionico nella molecola di cloruro di sodio. Il cloro e il sodio hanno le seguenti strutture di Lewis:
 IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA
 http://www.youtube.com/watch?v=q4ki1fa4yj0 PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA 1 Gli elettroni ruotano intorno al nucleo, trattenuti dalla loro carica elettrica negativa,
http://www.youtube.com/watch?v=q4ki1fa4yj0 PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA 1 Gli elettroni ruotano intorno al nucleo, trattenuti dalla loro carica elettrica negativa,
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO
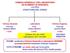 CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
Capitolo 16 L energia si trasferisce
 Capitolo 16 L energia si trasferisce 1. L «ABC» dei trasferimenti energetici 2. Le reazioni scambiano energia con l ambiente 3. Durante le reazioni varia l energia chimica del sistema 4. L energia chimica
Capitolo 16 L energia si trasferisce 1. L «ABC» dei trasferimenti energetici 2. Le reazioni scambiano energia con l ambiente 3. Durante le reazioni varia l energia chimica del sistema 4. L energia chimica
La temperatura. La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso
 1 La temperatura La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso Qualunque sia lo stato di aggregazione, le particelle (molecole o atomi) di cui è fatta
1 La temperatura La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso Qualunque sia lo stato di aggregazione, le particelle (molecole o atomi) di cui è fatta
Atomo: modello microscopico
 Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
LEGAMI INTERMOLECOLARI LEGAMI INTERMOLECOLARI
 I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
I legami (o forze) intermolecolari sono le forze attrattive tra particelle: molecola - molecola, molecola - ione, ione - ione In assenza di queste interazioni tutti i composti sarebbero gassosi NB: attenzione
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
Lo stato liquido. Un liquido non ha una forma propria, ma ha la forma del recipiente che lo contiene; ha però volume proprio e non è comprimibile.
 I liquidi Lo stato liquido Lo stato liquido rappresenta una condizione intermedia tra stato aeriforme e stato solido, tra lo stato di massimo disordine e quello di perfetto ordine Un liquido non ha una
I liquidi Lo stato liquido Lo stato liquido rappresenta una condizione intermedia tra stato aeriforme e stato solido, tra lo stato di massimo disordine e quello di perfetto ordine Un liquido non ha una
PROPRIETA DEI MATERIALI
 PROPRIETA DEI MATERIALI Una proprietà è la risposta di un materiale ad una sollecitazione esterna. Per i materiali solidi le proprietà possono raggrupparsi in sei differenti categorie: 1. Meccaniche 2.
PROPRIETA DEI MATERIALI Una proprietà è la risposta di un materiale ad una sollecitazione esterna. Per i materiali solidi le proprietà possono raggrupparsi in sei differenti categorie: 1. Meccaniche 2.
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
CORPO RIGIDO MOMENTO DI UNA FORZA EQUILIBRIO DI UN CORPO RIGIDO CENTRO DI MASSA BARICENTRO
 LEZIONE statica-1 CORPO RIGIDO MOMENTO DI UNA FORZA EQUILIBRIO DI UN CORPO RIGIDO CENTRO DI MASSA BARICENTRO GRANDEZZE SCALARI E VETTORIALI: RICHIAMI DUE SONO LE TIPOLOGIE DI GRANDEZZE ESISTENTI IN FISICA
LEZIONE statica-1 CORPO RIGIDO MOMENTO DI UNA FORZA EQUILIBRIO DI UN CORPO RIGIDO CENTRO DI MASSA BARICENTRO GRANDEZZE SCALARI E VETTORIALI: RICHIAMI DUE SONO LE TIPOLOGIE DI GRANDEZZE ESISTENTI IN FISICA
ELETTRICITÀ. In natura esistono due tipi di elettricità: positiva e negativa.
 Elettricità 1 ELETTRICITÀ Quando alcuni corpi (vetro, ambra, ecc.) sono strofinati con un panno di lana, acquistano una carica elettrica netta, cioè essi acquistano la proprietà di attrarre o di respingere
Elettricità 1 ELETTRICITÀ Quando alcuni corpi (vetro, ambra, ecc.) sono strofinati con un panno di lana, acquistano una carica elettrica netta, cioè essi acquistano la proprietà di attrarre o di respingere
L1 - Come si conclude questa serie di simboli? ><, <>, <<, ][, [], [[, )(,...
![L1 - Come si conclude questa serie di simboli? ><, <>, <<, ][, [], [[, )(,... L1 - Come si conclude questa serie di simboli? ><, <>, <<, ][, [], [[, )(,...](/thumbs/51/27413874.jpg) Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di simboli? >
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come si conclude questa serie di simboli? >
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 19 L energia si trasferisce 3 Sommario (I) 1. L «ABC» dei trasferimenti energetici 2. Durante le reazioni varia l energia chimica
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 19 L energia si trasferisce 3 Sommario (I) 1. L «ABC» dei trasferimenti energetici 2. Durante le reazioni varia l energia chimica
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
STRUTTURA DELL'ATOMO
 STRUTTURA DELL'ATOMO L'atomo è costituito da un nucleo centrale costituito da protoni (carica positiva 1,62*10-19 coulomb) e neutroni (privi di carica), intorno al quale ruotano uno o più elettroni (carica
STRUTTURA DELL'ATOMO L'atomo è costituito da un nucleo centrale costituito da protoni (carica positiva 1,62*10-19 coulomb) e neutroni (privi di carica), intorno al quale ruotano uno o più elettroni (carica
Intro & Stechiometria
 CHIMICA Studio della materia (composizione, stru7ura e proprietà) e dei suoi cambiamen; (trasformazioni) Azione: su due livelli macroscopico (proprietà e trasformazioni della materia visibile) microscopico
CHIMICA Studio della materia (composizione, stru7ura e proprietà) e dei suoi cambiamen; (trasformazioni) Azione: su due livelli macroscopico (proprietà e trasformazioni della materia visibile) microscopico
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
L elettrizzazione. Progetto: Istruzione di base per giovani adulti lavoratori 2 a opportunità
 1 L elettrizzazione Si può notare che corpi di materiale differente (plastica, vetro ecc.) acquisiscono la proprietà di attirare piccoli pezzetti di carta dopo essere stati strofinati con un panno di stoffa
1 L elettrizzazione Si può notare che corpi di materiale differente (plastica, vetro ecc.) acquisiscono la proprietà di attirare piccoli pezzetti di carta dopo essere stati strofinati con un panno di stoffa
Le trasformazioni chimiche e fisiche della materia. Lezioni d'autore di Giorgio Benedetti
 Le trasformazioni chimiche e fisiche della materia Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) La comprensione delle proprietà delle sostanze e le trasformazioni che
Le trasformazioni chimiche e fisiche della materia Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) La comprensione delle proprietà delle sostanze e le trasformazioni che
FORZE INTERMOLECOLARI
 FORZE INTERMOLECOLARI Le forze intermolecolari sono forze di attrazione che si stabiliscono tra le molecole che costituiscono una sostanza Determinano la tendenza delle molecole ad avvicinarsi. Per ogni
FORZE INTERMOLECOLARI Le forze intermolecolari sono forze di attrazione che si stabiliscono tra le molecole che costituiscono una sostanza Determinano la tendenza delle molecole ad avvicinarsi. Per ogni
Cenni sulla struttura della materia
 Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
Cenni sulla struttura della materia Tutta la materia è costituita da uno o più costituenti fondamentali detti elementi Esistono 102 elementi, di cui 92 si trovano in natura (i rimanenti sono creati in
ATOMI E MOLECOLE. Psicobiologia Lezione nr. 1. Prof. Lasaponara
 ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 15 Le forze intermolecolari e gli stati condensati della materia 3 Sommario 1. Le forze intermolecolari 2. Molecole polari e
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 15 Le forze intermolecolari e gli stati condensati della materia 3 Sommario 1. Le forze intermolecolari 2. Molecole polari e
Lezione 6. Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. WWW.SLIDETUBE.IT
 Lezione 6 Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. Classificazione delle Forze Distinguiamo tra: Forze attive Forze passive Forze attive Le 4 forze fondamentali:
Lezione 6 Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. Classificazione delle Forze Distinguiamo tra: Forze attive Forze passive Forze attive Le 4 forze fondamentali:
Elementi di Chimica. Lezione 03
 Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
L Atomo e le Molecole
 L Atomo e le Molecole La materia Tutti i corpi che ci circondano, (rocce, aria, nubi, sabbia, ) sono fatti di materia. Materia è tutto ciò che occupa uno spazio, cioè ha un volume, e ha una massa, quindi
L Atomo e le Molecole La materia Tutti i corpi che ci circondano, (rocce, aria, nubi, sabbia, ) sono fatti di materia. Materia è tutto ciò che occupa uno spazio, cioè ha un volume, e ha una massa, quindi
Studiamo le stelle su modelli che si basano su due presupposn principali:
 - - 0 Introduzione. Le forze che agiscono nelle stelle. La stru9ura della materia (approfondimento) 3. Le reazioni di fusione nucleare Le fasi della vita di una stella: 4. La nascita delle stelle 5. Le
- - 0 Introduzione. Le forze che agiscono nelle stelle. La stru9ura della materia (approfondimento) 3. Le reazioni di fusione nucleare Le fasi della vita di una stella: 4. La nascita delle stelle 5. Le
UNITÀ 1 LA CARICA ELETTRICA E L'ELETTRIZZAZIONE. I corpi possono acquisire (prendere) una proprietà che si chiama carica elettrica.
 UNITÀ 1 Prerequisiti: conoscere le caratteristiche del modello atomico conoscere e operare con le potenze: prodotto e divisione tra potenze con stessa base, potenze di 10, potenze ad esponente negativo
UNITÀ 1 Prerequisiti: conoscere le caratteristiche del modello atomico conoscere e operare con le potenze: prodotto e divisione tra potenze con stessa base, potenze di 10, potenze ad esponente negativo
TERMODINAMICA. Studia le trasformazioni dei sistemi in relazione agli scambi di calore e lavoro. GENERALITÀ SUI SISTEMI TERMODINAMICI
 TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
TERMODINAMICA Termodinamica: scienza che studia le proprietà e il comportamento dei sistemi, la loro evoluzione e interazione con l'ambiente esterno che li circonda. Studia le trasformazioni dei sistemi
Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) A cura del Prof S. Giannitto
 Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) APPUNTI DI TDP- TEORIA 3 ANNO A cura del Prof S. Giannitto La molecola è la più piccola parte che si può ottenere da un corpo conservandone
Istituto d Istruzione Secondaria Superiore M.BARTOLO PACHINO (SR) APPUNTI DI TDP- TEORIA 3 ANNO A cura del Prof S. Giannitto La molecola è la più piccola parte che si può ottenere da un corpo conservandone
Appunti di storia della fisica: l atomo
 Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro
 Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro Trovare una bilancia che possa pesare un atomo è un sogno irrealizzabile. Non potendo determinare
Aspetti quali-quantitativi delle reazioni chimiche unità 1, modulo B del libro unità 2, modulo E del libro Trovare una bilancia che possa pesare un atomo è un sogno irrealizzabile. Non potendo determinare
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Il Calore e la Temperatura
 Il Calore e la Temperatura Gloria Nuzzolo è l energia lenergia termica che si trasferisce da un oggetto a temperatura più alta a un oggetto con temperatura più bassa. Il flusso di calore è dovuto alla
Il Calore e la Temperatura Gloria Nuzzolo è l energia lenergia termica che si trasferisce da un oggetto a temperatura più alta a un oggetto con temperatura più bassa. Il flusso di calore è dovuto alla
Legame Chimico. Legame Chimico
 Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
delle curve isoterme dell anidride carbonica
 COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti.
 1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
LA STRUTTURA DELL ATOMO
 Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Il Gas Ideale. Il gas ideale é un'astrazione
 Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
GAIALAB:INCONTRIAMO L AMBIENTE IN LABORATORIO
 LABORATORIO DI FISICA Le forze che governano la natura La forza ha carattere vettoriale, cioè caratterizzata da un intensità, una direzione e un verso oltre che da un punto di applicazione. Rappresentazione
LABORATORIO DI FISICA Le forze che governano la natura La forza ha carattere vettoriale, cioè caratterizzata da un intensità, una direzione e un verso oltre che da un punto di applicazione. Rappresentazione
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Il Legame Ionico. Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B -
 Il Legame Ionico Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B - A + B - Le coppie di ioni si attraggono elettrostaticamente Il
Il Legame Ionico Quando la differenza di elettronegatività fra atomi A e B è molto grande le coppie AB possono essere considerate A + B - A + B - Le coppie di ioni si attraggono elettrostaticamente Il
Fenomeni elettrici e magnetici
 Fenomeni elettrici e magnetici Le forze elettromagnetiche sono percepibili nella maggior parte dei fenomeni che avvengono in natura Caricamento elettrostatico di un corpo per strofinamento Fulmine Magnetismo
Fenomeni elettrici e magnetici Le forze elettromagnetiche sono percepibili nella maggior parte dei fenomeni che avvengono in natura Caricamento elettrostatico di un corpo per strofinamento Fulmine Magnetismo
A_Test di valutazione di CHIMICA:
 COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi
 SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
Capitolo Cariche elettriche, forze 23 e campi
 Capitolo Cariche elettriche, forze 23 e campi 1 Capitolo 23 - Contenuti 1. Carica elettrica 2. Isolanti e conduttori 3. La legge di Coulomb 4. Il campo elettrico 5. Le linee del campo elettrico 6. La schermatura
Capitolo Cariche elettriche, forze 23 e campi 1 Capitolo 23 - Contenuti 1. Carica elettrica 2. Isolanti e conduttori 3. La legge di Coulomb 4. Il campo elettrico 5. Le linee del campo elettrico 6. La schermatura
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
I LEGAMI CHIMICI. Configurazione elettronica stabile: è quella in cui tutti i livelli energetici dell atomo sono pieni di elettroni
 I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
Lezione 12 Tensione superficiale. Deformabilità.
 Lezione 12 Tensione superficiale. Deformabilità. Fenomeni di interazione molecolare residua Abbiamo schematizzato i liquidi come insiemi di particelle poco interagenti tra loro. Tuttavia gli effetti di
Lezione 12 Tensione superficiale. Deformabilità. Fenomeni di interazione molecolare residua Abbiamo schematizzato i liquidi come insiemi di particelle poco interagenti tra loro. Tuttavia gli effetti di
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
