Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
|
|
|
- Dante Vanni
- 5 anni fa
- Visualizzazioni
Transcript
1 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu, disperato pilota, frangi ora fra gli scogli la mia barca già stanca e squassata per tante tempeste! A te accanto, mio amore! Oh schietto farmacista! Efficace è la tua droga. Con questo bacio io muoio. W. Shakespeare. Giulietta e Romeo, Atto 5, Scena 3. Ultima revisione: 4 novembre 2015 Lezione 08 5 novembre 2015
2 Scala di operazione A seconda della quantità di sostanza che viene impiegata per l analisi, è possibile distinguere: -lamacroanalisi (~ 1 g oppure 50 ml); -lasemimicroanalisi (~ 0,1 g oppure 5 ml); -lamicroanalisi (~ 10 mg oppure 0,5 ml).
3 Scala di operazione Il procedimento generale è più o meno lo stesso per i 3 tipi di analisi. Le reazioni di riconoscimento sono generalmente le stesse per la macro- e la semimicroanalisi, mentre per la microanalisi si ricorre generalmente ad apparecchiature e a reazioni dedicate. Anche la concentrazione della sostanza in soluzione è la medesima per tutti e 3 i tipi di analisi: varia soltanto la quantità di sostanza impiegata.
4 Corredo di laboratorio per ciascun studente Per un corretto svolgimento dell analisi è necessario operare con apparecchi sempre ben puliti. I recipienti devono essere lavati e sgrassati con acidi o con miscela cromica (soluzione satura di bicromato potassico, K 2 Cr 2 O 7, in acido solforico concentrato), poi si risciacquano con acqua distillata.
5 Apparecchiatura per l Analisi Lampada Bunsen Da sinistra. Lampada di Bunsen semplice, con rubinetto, con rubinetto e blocco di sicurezza.
6 Apparecchiatura per l Analisi Lampada Bunsen La lampada di Bunsen o becco Bunsen (Robert Wilhelm Eberhard Bunsen, ) costituisce il mezzo di riscaldamento ordinariamente usato per le operazioni analitiche. La lampada è costituita da un tubo di ottone in cui il gas entra attraverso un raccordo porta-gomma che si trova vicino alla base. Girando opportunamente un apposito anello forato, che è sul collo della lampada, si può graduare l afflusso dell aria.
7 Apparecchiatura per l Analisi Lampada Bunsen Se l anello è disposto in modo da impedire totalmente l afflusso dell aria si ottiene una fiamma con proprietà riducenti, non molto calda e luminosa. Questo tipo di fiamma è ricca di particelle di carbonio incandescenti, che non bruciano completamente per difetto di aria.
8 Apparecchiatura per l Analisi Lampada Bunsen Se, invece, l anello è regolato in modo che attraverso il foro si abbia il massimo afflusso di aria, il carbonio che si separa dagli idrocarburi contenuti nel gas brucia completamente. Si ottiene così una fiamma in cui si possono distinguere varie zone, più o meno calde, ossidanti o riducenti.
9 Apparecchiatura per l Analisi Lampada Bunsen
10 Operazioni Analitiche Generali Evaporazione ed ebollizione L evaporazione consiste nel trasformare un liquido in vapore allo scopo di eliminare tutto o parte del liquido. Se da una soluzione il liquido viene evaporato completamente si dice che la soluzione è stata portata a secchezza. Se invece il liquido viene evaporato solo in parte si parla di concentrazione. Questa operazione viene eseguita mediante riscaldamento, cioè approfittando del fatto che un aumento di temperatura fa aumentare la tensione di vapore dei liquidi.
11 Operazioni Analitiche Generali Evaporazione ed ebollizione Il riscaldamento può essere spinto fino alla temperatura di ebollizione, ma talvolta può essere sufficiente una temperatura inferiore. Durante l ebollizione o l evaporazione di una soluzione, si eliminano, oltre al solvente, anche le sostanze disciolte che hanno una volatilità maggiore o poco diversa da quella del solvente stesso. I gas, la cui solubilità diminuisce con l aumentare della temperatura, vengono eliminati per primi.
12 Operazioni Analitiche Generali Evaporazione ed ebollizione L evaporazione, o anche il semplice riscaldamento dei liquidi, si fa in becher o in capsula, sul treppiede sormontato da una reticella, oppure in provetta, su fiamma libera. I liquidi alcalini, che corrodono il vetro, devono essere riscaldati di norma in recipienti di porcellana. Per il riscaldamento si usa la fiamma di una lampada Bunsen. Qualora non si vogliano superare i 100 ºC si usa il bagnomaria, cioè il riscaldamento mediante vapore acqueo o immersione in acqua bollente.
13 Operazioni Analitiche Generali Evaporazione ed ebollizione
14 Operazioni Analitiche Generali Calcinazione La calcinazione è l operazione con cui si eliminano i componenti volatili da una sostanza solida, mediante riscaldamento a temperature generalmente elevate. Un esempio di calcinazione frequente nell analisi si ha nel riscaldamento di miscele saline da cui si vogliono eliminare i sali ammoniacali, i quali volatilizzano a temperature di ºC.
15 Operazioni Analitiche Generali Calcinazione La calcinazione si esegue in recipienti di porcellana o di platino (capsule, crogioli), riscaldando direttamente sulla fiamma di una lampada Bunsen (sino a 800 ºC) o di una soffieria (sino a 1000 ºC). Prima di calcinare occorre esser certi che l operazione non presenti pericoli (presenza di clorati con sostanze organiche, ecc.). In genere, poiché nella calcinazione si possono sviluppare sostanze tossiche, si opera sotto cappa.
16 Operazioni Analitiche Generali Calcinazione
17 Operazioni Analitiche Generali Fusione Per portare in soluzione alcune sostanze (solfati alcalino-terrosi, ossidi di metalli tri- e tetravalenti, ecc.), che sono insolubili in acqua e negli acidi, si può ricorrere alla fusione. La fusione si esegue mescolando la sostanza con il reagente (fondente) e riscaldando gradatamente fino alla temperatura di fusione. Sostanze molto usate come fondenti sono Na 2 CO 3, Na 2 CO 3 /K 2 CO 3,KHSO 4.
18 Operazioni Analitiche Generali Fusione La miscela Na 2 CO 3 /K 2 CO 3 (1:1) ha il vantaggio di fondere ad una temperatura più bassa di quella a cui fondono i 2 singoli carbonati. Tale miscela viene usata, per esempio, per far reagire il solfato di bario, il solfato di piombo, vari ossidi metallici. Il bisolfato potassico, riscaldato alla temperatura di fusione, dà luogo alla reazione: 2KHSO 4 K 2 SO 4 + H 2 O + SO 3
19 Operazioni Analitiche Generali Fusione L anidride solforica libera è molto reattiva e capace di attaccare vari ossidi metallici inerti (es., Cr 2 O 3,Fe 2 O 3, ecc.) trasformandoli in solfati solubili: Cr 2 O 3 + 3SO 3 Cr 2 (SO 4 ) 3 Se si vuole che nella fusione la sostanza subisca una ossidazione o una riduzione, si adoperano come fondenti sostanze o miscele di sostanze ossidanti o riducenti.
20 Operazioni Analitiche Generali Fusione Una delle sostanze ossidanti più usate è la miscela Na 2 CO 3 /KNO 3, che deve il suo potere ossidante alla presenza del nitrato e che si usa, ad esempio, per ossidare i sali di cromo a cromati e i sali di manganese a manganati. Una miscela riducente è quella costituita Na 2 CO 3 /C, che deve il suo potere riducente alla presenza del carbone e si usa, ad esempio, per ridurre il solfato di bario a solfuro.
21 Operazioni Analitiche Generali Fusione La fusione si esegue, a seconda dei casi, in crogioli di platino, di argento, di nichel o anche di porcellana. Quest ultima viene facilmente attaccata dagli alcali, con separazione di Al 2 O 3 e SiO 2, che possono interferire nelle operazioni successive. In molti casi, dopo la fusione, la massa fusa viene lisciviata, cioè viene ripresa con un liquido opportuno, eventualmente riscaldando all ebollizione; se necessario, poi si filtra.
22 Esecuzione delle reazioni di riconoscimento La maggior parte delle reazioni analitiche macro e semimicro si eseguono in provette. Per piccole quantità di sostanza si usano preferibilmente microprovette e provette per centrifuga. In generale, le reazioni di precipitazione si eseguono aggiungendo il reattivo precipitante goccia a goccia nella soluzione in esame, fino a completa precipitazione.
23 Esecuzione delle reazioni di riconoscimento Per accelerare la reazione, si può agitare la miscela; in molti casi è anche utile riscaldare. In alcuni casi, è necessario sfregare la parete interna della provetta con una bacchetta di vetro a spigolo vivo, per innescare la precipitazione. Spesso, quando le soluzioni sono diluite, la formazione del precipitato si riduce ad un intorbidimento. In taluni casi, può essere utile ripetere la prova sul liquido in esame, dopo averlo concentrato.
24 Esecuzione delle reazioni di riconoscimento Le reazioni molto sensibili e quelle in cui si formano prodotti colorati si possono eseguire in vetrini da orologio o su piattelli di porcellana. In questo caso, i reagenti vengono aggiunti con il contagocce e mescolati con una bacchetta di vetro. Tale procedura prende il nome di reazione alla tocca o stillireazione o spot test.
25 Esecuzione delle reazioni di riconoscimento
26 Esecuzione delle reazioni di riconoscimento Alcune reazioni micro e semimicroanalitiche si possono eseguire anche versando i reagenti con il contagocce su strisce di carta da filtro in modo da sfruttare i fenomeni di capillarità. A tale scopo si usa generalmente carta da filtro molto spessa e molto adsorbente, il più possibile esente da impurezze. La carta da filtro non può essere usata con soluzioni molto acide perché si rompe, né con soluzioni molto basiche perché si rigonfia.
27 Filtrazione e centrifugazione Un precipitato può essere separato dalle acque madri in 2 modi: - per filtrazione; - per centrifugazione. La filtrazione si esegue mediante dischi di carta porosa. Quando si vuole recuperare un precipitato, la grandezza del filtro da usare deve dipendere non dalla quantità del liquido da filtrare, bensì dalla quantità del precipitato: il filtro deve essere piccolo quanto più è possibile per evitare una dispersione della sostanza.
28 Filtrazione e centrifugazione
29 Filtrazione e centrifugazione Il disco di carta (a) viene piegato prima esattamente a metà (b), poi in 4 parti (c), indi si aprono 2 lembi per formare un cono (d) che viene adattato in un imbuto, mantenendolo con le dita sino a che, bagnandolo con acqua distillata, non resti aderente al vetro (e). Quando il filtro è riempito di acqua, il gambo dell imbuto deve riempirsi di una colonna di liquido che deve persistere anche durante la filtrazione, senza che si formino bolle per risucchio.
30 Filtrazione e centrifugazione Il cono dell imbuto deve essere poco più grande del filtro. Il liquido filtrante provoca sotto il filtro un aspirazione proporzionale all altezza della colonna liquida. Per aumentare la velocità di filtrazione conviene usare imbuti dal gambo molto lungo. Il liquido deve riempire il filtro fino a circa 5 mm dal bordo.
31 Filtrazione e centrifugazione Se si debbono filtrare precipitati gelatinosi (es., idrossidi), si può usare una carta da filtro a pori larghi (filtri rapidi). Per precipitati molto fini è opportuno usare una carta a pori più stretti (filtri per analisi qualitativa). Nell analisi semimicro e micro, la filtrazione è spesso sostituita dalla centrifugazione, che si esegue con appositi apparecchi, detti centrifughe, rotanti ad alta velocità. La centrifugazione ha il vantaggio di essere più rapida e permette separazioni senza perdite.
32 Filtrazione e centrifugazione
33 Filtrazione e centrifugazione Per centrifugare una sospensione, che deve essere contenuta nell apposita provetta di forma cilindro-conica, si introduce quest ultima in uno dei tubi portaprovette. Nel tubo opposto si colloca un altra provetta contenente un egual peso di acqua per evitare vibrazioni e sbilanciamenti dell apparecchio. Si fa ruotare la centrifuga, prima lentamente, poi alla velocità massima, per qualche minuto (2 min a 3000 giri).
34 Filtrazione e centrifugazione Per azione della centrifuga, il precipitato viene spinto al fondo della provetta, dove si deposita così compatto che il liquido limpido ne può essere allontanato per decantazione o per aspirazione con un contagocce. Il precipitato rimasto al fondo della provetta può essere prelevato con una bacchettina di vetro o con una spatola.
35 Filtrazione e centrifugazione In qualche caso, dopo la centrifugazione, per rendere perfettamente limpido il liquido centrifugato, si può filtrare questo attraverso un filtro a pori molto stretti. In alcuni casi è possibile indicare a priori se, per separare un precipitato, sia più conveniente la filtrazione o la centrifugazione. In tali casi si prescrive genericamente di filtrare, ma spetta all analista decidere se è il caso di filtrare o di centrifugare.
36 Lavaggio dei precipitati Difficilmente i precipitati si separano puri. In generale, al termine della filtrazione o della centrifugazione, per eliminare le sostanze estranee trattenute dal precipitato è necessario lavare il precipitato con acqua o con altro liquido opportuno. Per lavare un precipitato sul filtro, si spruzza, mediante una spruzzetta, il liquido di lavaggio sul precipitato facendo in modo che questo si raccolga al fondo del filtro stesso.
37 Lavaggio dei precipitati Per lavare un precipitato in una provetta da centrifuga, si aggiungono alcune gocce del liquido di lavaggio, si agita con una bacchettina e si centrifuga nuovamente. L operazione va ripetuta più volte. In genere la prima acqua di lavaggio si può unire al filtrato che servirà per ulteriori ricerche. Le acque di lavaggio successive, invece, si possono gettare per non diluire eccessivamente la soluzione.
38 Lavaggio dei precipitati Per rimuovere o per raccogliere il precipitato che si trova sul filtro, si può bucare il filtro con la punta di bacchetta di vetro e trasferire il precipitato, servendosi del getto di una spruzzetta, in un altro recipiente posto sotto l imbuto. Si può anche aprire il filtro, stendendolo su di un vetrino ad orologio, e raccogliere il precipitato con l aiuto di una spatola o di una bacchetta di vetro, oppure rimuoverlo mediante il getto di una spruzzetta.
39 Lavaggio dei precipitati Talvolta, quando il precipitato è scarso, può essere conveniente sciogliere il precipitato sul filtro stesso (senza toglierlo dall imbuto) aggiungendo con un contagocce la quantità di solvente strettamente necessaria.
40 Gorgogliamento e sviluppo di gas Per far gorgogliare un gas in un liquido, si pone il liquido in un recipiente opportuno (beuta o provetta). Vi si fa gorgogliare il gas per mezzo di un tubetto di vetro opportunamente piegato. Un estremità del tubetto è immersa nel liquido, mentre l altra è collegata al generatore del gas, cioè ad una bombola oppure ad un Kipp.
41 Gorgogliamento e sviluppo di gas
42 Gorgogliamento e sviluppo di gas
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI:
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Analisi Chimico Farmaceutica e Tossicologica con Laboratorio
 Analisi Chimico Farmaceutica e Tossicologica con Laboratorio corso di Laurea in Farmacia canale A-L anno accademico 2015-2016 Dr. Antonio Coluccia Dipartimento di Chimica e Tecnologie del Farmaco Sapienza
Analisi Chimico Farmaceutica e Tossicologica con Laboratorio corso di Laurea in Farmacia canale A-L anno accademico 2015-2016 Dr. Antonio Coluccia Dipartimento di Chimica e Tecnologie del Farmaco Sapienza
Analisi Chimico Farmaceutica e Tossicologica con Laboratorio
 Analisi Chimico Farmaceutica e Tossicologica con Laboratorio corso di Laurea in Farmacia canale A-L anno accademico 2018-2019 Dr. Antonio Coluccia Dipartimento di Chimica e Tecnologie del Farmaco Sapienza
Analisi Chimico Farmaceutica e Tossicologica con Laboratorio corso di Laurea in Farmacia canale A-L anno accademico 2018-2019 Dr. Antonio Coluccia Dipartimento di Chimica e Tecnologie del Farmaco Sapienza
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
IL LABORATORIO CHIMICO ) 1
 IL LABORATORIO CHIMICO ) 1 ATTREZZATURA DI UN LABORATORIO CHIMICO Beker: bicchieri dotati di beccuccio nella parte superiore per facilitare il travaso dei liquidi. varia capacità (25-100-250-400-600..ml)
IL LABORATORIO CHIMICO ) 1 ATTREZZATURA DI UN LABORATORIO CHIMICO Beker: bicchieri dotati di beccuccio nella parte superiore per facilitare il travaso dei liquidi. varia capacità (25-100-250-400-600..ml)
CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale
 CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale ESERCITAZIONE N 4 bis Stati di ossidazione del manganese Il manganese è un tipico elemento di transizione del blocco d.
CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale ESERCITAZIONE N 4 bis Stati di ossidazione del manganese Il manganese è un tipico elemento di transizione del blocco d.
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Parte Terza Principi Teorici
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Dott. Giuseppe La Regina Parte
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2017/2018 Dott. Giuseppe La Regina Parte
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica organica I corso. Dott.ssa Alessandra Operamolla
 La vetreria Laboratorio di chimica organica I corso Dott.ssa Alessandra Operamolla alessandra.operamolla@uniba.it Lavaggio e cura 1. La vetreria deve essere sempre fissata agli stativi con pinze e sostegni
La vetreria Laboratorio di chimica organica I corso Dott.ssa Alessandra Operamolla alessandra.operamolla@uniba.it Lavaggio e cura 1. La vetreria deve essere sempre fissata agli stativi con pinze e sostegni
Sostanza pura. Il termine sostanza indica il tipo di materia di cui è fatto un corpo.
 Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
TECNICHE DI PURIFICAZIONE. Cristallizzazione
 TECNICHE DI PURIFICAZIONE Cristallizzazione I composti organici solidi ottenuti nel corso delle reazioni non sono quasi mai puri, per cui è necessario adottare delle tecniche di purificazione in grado
TECNICHE DI PURIFICAZIONE Cristallizzazione I composti organici solidi ottenuti nel corso delle reazioni non sono quasi mai puri, per cui è necessario adottare delle tecniche di purificazione in grado
Isolamento della caffeina dalle foglie di tè
 SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
CRISTALLIZZAZIONE. Scelta del solvente: Affinché la cristallizzazione possa essere efficace, è necessario scegliere il solvente più
 CRISTALLIZZAZIONE La cristallizzazione è stata a lungo utilizzata nella purificazione delle sostanze. Si tratta essenzialmente di una tecnica di separazione solido-liquido molto importante per ricavare
CRISTALLIZZAZIONE La cristallizzazione è stata a lungo utilizzata nella purificazione delle sostanze. Si tratta essenzialmente di una tecnica di separazione solido-liquido molto importante per ricavare
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Dott. Giuseppe La Regina Tu,
IL LABORATORIO CHIMICO
 IL LABORATORIO CHIMICO 1 ATTREZZATURA DI UN LABORATORIO CHIMICO Beaker: bicchieri dotati di beccuccio nella parte superiore per facilitare il travaso dei liquidi. varia capacità (25-100-250-400-600..ml)
IL LABORATORIO CHIMICO 1 ATTREZZATURA DI UN LABORATORIO CHIMICO Beaker: bicchieri dotati di beccuccio nella parte superiore per facilitare il travaso dei liquidi. varia capacità (25-100-250-400-600..ml)
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
MATERIALE IN DOTAZIONE
 MATERIALE IN DOTAZIONE Dotazione per due studenti: 2 porta provette 8 provette per centrifuga 8 provette 12/120 6 contagocce 6 becker (250, 100, 100, 50, 50, 25 ml) 1 becker da 400 ml con supporto provette
MATERIALE IN DOTAZIONE Dotazione per due studenti: 2 porta provette 8 provette per centrifuga 8 provette 12/120 6 contagocce 6 becker (250, 100, 100, 50, 50, 25 ml) 1 becker da 400 ml con supporto provette
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ESTRAZIONE SOLVENTI. tecnica di separazione e purificazione
 ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
A) Determinazione gravimetrica di manganese(ii) e di zinco(ii)
 UNIVERSITA DEGLI STUDI DI NAPOLI FEDERICO II A.A. 2015/16 Laurea triennale in CHIMICA ANALITICA I E LABORATORIO CHIMICA INDUSTRIALE Determinazione della percentuale di manganese(ii) e Esercitazione n 15
UNIVERSITA DEGLI STUDI DI NAPOLI FEDERICO II A.A. 2015/16 Laurea triennale in CHIMICA ANALITICA I E LABORATORIO CHIMICA INDUSTRIALE Determinazione della percentuale di manganese(ii) e Esercitazione n 15
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
Estrazione. Il processo di estrazione con solventi è impiegato per l isolamento di
 Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Se si mescolano 24,50 g. di NaCl in polvere e 100,00 g. di acqua:
 A. Si mescolano 15,30 g. di zucchero con 5,65 g. di NaCl dopo averli pesati. Determinare: A. Le percentuali dei due componenti B. Gli errori assoluti e relativi compiuti sulle due pesate C. L errore assoluto
A. Si mescolano 15,30 g. di zucchero con 5,65 g. di NaCl dopo averli pesati. Determinare: A. Le percentuali dei due componenti B. Gli errori assoluti e relativi compiuti sulle due pesate C. L errore assoluto
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
LABORATORIO DI CHIMICA
 LABORATORIO DI CHIMICA MANUALE PRATICO AD USO DELLE CLASSI DEGLI ISTITUTI TECNICI DI CARMELO GRECO ATTREZZATURA DI LABORATORIO Le attrezzature e gli utensili che si trovano in un laboratorio chimico possono
LABORATORIO DI CHIMICA MANUALE PRATICO AD USO DELLE CLASSI DEGLI ISTITUTI TECNICI DI CARMELO GRECO ATTREZZATURA DI LABORATORIO Le attrezzature e gli utensili che si trovano in un laboratorio chimico possono
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
Attività laboratoriale di «Trasformazione dei prodotti»
 Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Il Rame a Scuola, per esempio Una proposta didattica per gli Istituti Tecnici Tecnologici
 Il Rame a Scuola, per esempio Sentire parlare di riciclo, sostenibilità, ambiente...è noioso Fare riciclo, sostenibilità, ambiente...è avventuroso Molti Istituti tecnici o professionali del settore elettronico
Il Rame a Scuola, per esempio Sentire parlare di riciclo, sostenibilità, ambiente...è noioso Fare riciclo, sostenibilità, ambiente...è avventuroso Molti Istituti tecnici o professionali del settore elettronico
Prima esperienza di Laboratorio. Alcune reazioni del rame
 Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Sostanze grasse o lipidi
 Sostanze grasse o lipidi I lipidi (in greco significa sostanze grasse ) sono composti ternari formati da carbonio, idrogeno e ossigeno e sono caratterizzati dalla proprietà di essere insolubili in acqua
Sostanze grasse o lipidi I lipidi (in greco significa sostanze grasse ) sono composti ternari formati da carbonio, idrogeno e ossigeno e sono caratterizzati dalla proprietà di essere insolubili in acqua
5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica
 NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
1 Gruppo: Ag + ; Hg 2 2+ ; Pb ++ Reattivo precipitante: HCl dil (2N).
 1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
QUARTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO Le attrezzature e gli utensili che si trovano in un laboratorio chimico possono essere di materiale diverso: porcellana, plastica, sughero, gomma, vetro. Il vetro Parlando di
ATTREZZATURA DI LABORATORIO Le attrezzature e gli utensili che si trovano in un laboratorio chimico possono essere di materiale diverso: porcellana, plastica, sughero, gomma, vetro. Il vetro Parlando di
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico
 3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo)
 4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
Sintesi verde malachite
 Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
PRINCIPIO TESTATO: reazioni di sintesi, doppio scambio con precipitazione, eso-endotermiche e di ossido-riduzione.
 TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) H 2 SO 4. Quantità: Acido salicilico 5.0 g (PM = 138.
 ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
Classe 5 ch B a.s.2007/08 ANALISI DELLA BIRRA
 ANALISI DELLA BIRRA DETRMINAZIONE DELL ACIDITÀ L acidità della birra è dovuta in parte ad acidi organici vari (specialmente lattico), in parte a fosfati acidi, e, specialmente nelle birre mal conservate,
ANALISI DELLA BIRRA DETRMINAZIONE DELL ACIDITÀ L acidità della birra è dovuta in parte ad acidi organici vari (specialmente lattico), in parte a fosfati acidi, e, specialmente nelle birre mal conservate,
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2014/2015
 Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE
 2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni
 Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Corso di Chimica Analitica II e Laboratorio Docenti: Davide Atzei e Antonella Rossi
 Corso di Chimica Analitica II e Laboratorio Docenti: Davide Atzei e Antonella Rossi Analisi elettrogravimetrica del rame in composti, leghe e minerali contenenti rame 1 OBIETTIVI I metodi dell analisi
Corso di Chimica Analitica II e Laboratorio Docenti: Davide Atzei e Antonella Rossi Analisi elettrogravimetrica del rame in composti, leghe e minerali contenenti rame 1 OBIETTIVI I metodi dell analisi
ESPERIENZA 4. Permanganometria
 ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA
 ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA Per effettuare una reazione chimica correttamente, si deve eseguire un certo numero di operazioni: 1. Si purificano (se necessario) reagenti e solventi.
ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA Per effettuare una reazione chimica correttamente, si deve eseguire un certo numero di operazioni: 1. Si purificano (se necessario) reagenti e solventi.
Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico.
 Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Esercitazione 6. Chimica biologica del Fe. Il Ferro ) 2 (SO 4 6H 2. Fe(NH 4
 Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
3016 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico
 6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
Appunti del corso di Istituzioni di tecnologia alimentare Parte 8 Separazione meccanica - 1 ZEPPA G. Università degli Studi di Torino
 Appunti del corso di Istituzioni di tecnologia alimentare Parte 8 Separazione meccanica - 1 ZEPPA G. Università degli Studi di Torino Separazione meccanica Vagliatura separare solidi in funzione delle
Appunti del corso di Istituzioni di tecnologia alimentare Parte 8 Separazione meccanica - 1 ZEPPA G. Università degli Studi di Torino Separazione meccanica Vagliatura separare solidi in funzione delle
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
Crogioli. Crogioli. Porcellana Haldenwanger. Crogioli. In metallo - quarzo. Filtranti. Accessori
 Crogioli In metallo - quarzo Accessori Crogioli 422 Le caratteristiche principali di questo tipo di porcellana sono: - Conforme alle norme DIN 40685 tipo 110, con ottima resistenza all'attacco chimico
Crogioli In metallo - quarzo Accessori Crogioli 422 Le caratteristiche principali di questo tipo di porcellana sono: - Conforme alle norme DIN 40685 tipo 110, con ottima resistenza all'attacco chimico
Analisi Chimico-Farmaceutiche e Tossicologiche 1
 Analisi Chimico-Farmaceutiche e Tossicologiche 1 Corso A (A H) Prof.ssa Alessia Carocci E-mail: alessia.carocci@uniba.it Studio: stanza 429, III Piano Tel: 080/5442745 Ricevimento studenti: lunedì, mercoledì,
Analisi Chimico-Farmaceutiche e Tossicologiche 1 Corso A (A H) Prof.ssa Alessia Carocci E-mail: alessia.carocci@uniba.it Studio: stanza 429, III Piano Tel: 080/5442745 Ricevimento studenti: lunedì, mercoledì,
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
5007 Reazione dell anidride ftalica con la resorcina per formare fluoresceina
 57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
Virt&l-Comm
 La Materia: I miscugli e le sostanze ilaria FRAOLiNi 1 OBIETTIVI Conoscere la differenza tra miscuglio eterogeneo e soluzione Conoscere i principali metodi per separare i componenti di un miscuglio eterogeneo
La Materia: I miscugli e le sostanze ilaria FRAOLiNi 1 OBIETTIVI Conoscere la differenza tra miscuglio eterogeneo e soluzione Conoscere i principali metodi per separare i componenti di un miscuglio eterogeneo
COSTITUENTI INORGANICI NON METALLICI
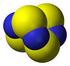 4140. Solfato I solfati presenti in natura derivano in larga misura dalla trasformazione dei solfuri naturali. Si ritrovano prevalentemente nei sedimenti evaporitici come gesso (Ca 2H 2 O) o anidride (Ca
4140. Solfato I solfati presenti in natura derivano in larga misura dalla trasformazione dei solfuri naturali. Si ritrovano prevalentemente nei sedimenti evaporitici come gesso (Ca 2H 2 O) o anidride (Ca
CARATTERISTICHE. In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee.
 In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide
 1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
Acido 3,5-dinitrosalicilico Glucosio Acido 3-amino-5-nitrosalicilico Acido gluconico (Incolore-giallo leggero)
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
Laboratorio PLS-Chimica SEPARAZIONE DEI COMPONENTI DI MISCUGLI DI SOLIDI
 Laboratorio PLS-Chimica Esercitazione (per Docenti) n. 1 SEPARAZIONE DEI COMPONENTI DI MISCUGLI DI SOLIDI PREMESSA. La materia che ci circonda è formata di corpi, per lo più diversi per composizione e/o
Laboratorio PLS-Chimica Esercitazione (per Docenti) n. 1 SEPARAZIONE DEI COMPONENTI DI MISCUGLI DI SOLIDI PREMESSA. La materia che ci circonda è formata di corpi, per lo più diversi per composizione e/o
Chimica Organica II - Laboratorio A.A. 2008/09 2. H 3 O+
 Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
specie chimiche. in quantità maggiore presente nella soluzione, e tutti gli altri componenti che sono detti soluti. Un componente di una soluzione
 Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico. estere dietilico dell acido adipico (pe 245 C)
 NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
