Introduzione alla Chimica organica
|
|
|
- Silvano Napolitano
- 5 anni fa
- Visualizzazioni
Transcript
1 Introduzione alla Chimica organica Definizione di Jacob Berzelius (1807): I composti organici sono quelli elaborati dagli organismi viventi (animali e vegetali) e costituiti prevalentemente da carbonio e la chimica organica è quella scienza che studia i comportamenti chimici e fisici dei composti organici. Nel 1828 il chimico tedesco Friedrich Wöhler per primo riuscì nella sintesi di un composto organico (l urea) a partire da composti inorganici. La definizione più corretta di chimica organica diventa: La scienza che si occupa delle caratteristiche chimiche e fisiche delle molecole organiche. Si definiscono convenzionalmente composti organici i composti del carbonio con eccezione del monossido di carbonio e dell anidride carbonica.
2 Il carbonio Cosa rende l elemento carbonio così particolare da dovergli riservare una chimica a parte rispetto a quella di tutti gli altri elementi messi insieme (chimica inorganica)? Il carbonio occupa un posto centrale nella Tavola Periodica. Ha un elettronegatività tale da preferire legami covalenti con gli altri non metalli, formando milioni di composti stabili.
3 Infatti l atomo di carbonio: Il carbonio forma fino a 4 legami covalenti singoli, doppi o tripli ha piccole dimensioni; non ha elevata elettronegatività, che permette la formazione di legami stabili con elementi come l idrogeno e l ossigeno e altri non-metalli forma, con altri atomi di carbonio, catene, corte o assai lunghe, lineari o ramificate, oppure chiuse ad anello, con una varietà di combinazioni quasi infinita; forma un elevatissimo numero di isomeri (molecole costituite dagli stessi atomi, che però sono disposti in modo differente nello spazio) Il carbonio (simbolo C) è un non metallo del gruppo VI A del sistema periodico; è presente in natura, allo stato elementare, in due differenti forme cristalline: la grafite e il diamante. Nella crosta terrestre è presente in una piccola percentuale nei carbonati, nel petrolio, nel carbone e nel gas naturale; nell atmosfera si trova soprattutto come monossido (CO) e diossido (CO 2 ) di carbonio (o anidride carbonica), ma la percentuale maggiore di carbonio si trova come costituente delle strutture di base degli organismi.
4 Il carbonio In che modo il carbonio forma 4 legami covalenti? Nella sua configurazione elettronica fondamentale ha solo 2 elettroni spaiati! C Z=6 1s 2 2s 2 2p 2 Se uno degli elettroni nell orbitale 2s è promosso nel 2p vuoto, abbiamo 4 elettroni spaiati e quindi la possibilità di formare 4 legami covalenti. Ma i 4 legami con l idrogeno non sarebbero equivalenti!
5 Gli orbitali ibridi: Ibridazione sp 3 Il carbonio Dalla combinazione di un orbitale atomico di tipo s e 3 orbitali atomici di tipo p si generano 4 orbitali atomici ibridi di tipo sp 3. I 4 orbitali hanno una forma che ricorda gli orbitali di tipo p, con i 2 lobi di dimensioni diverse. Un orbitale sp 3 ha il 25% di carattere s e il 75% di carattere p.
6 Gli orbitali ibridi: Ibridazione sp 3 Il carbonio In questo modo i 4 elettroni del guscio più esterno del C diventano perfettamente equivalenti, si dispongono lungo un tetraedro, a 109 l uno dall altro e possono far formare al Carbonio stesso 4 legami identici tra loro. Metano CH 4
7 Gli orbitali ibridi: Ibridazione sp3
8 L ibridazione sp 3 non spiega la struttura di composti come l etilene 8
9 Gli orbitali ibridi: Ibridazione sp 2 Il carbonio Nell ibridzione sp 2 solo questi tre orbitali generano orbitali ibridi identici mentre l orbitale p z rimane invariato
10 Gli orbitali ibridi: Ibridazione sp 2 Lo stato di ibridazione sp 2 è tipico degli atomi di carbonio impegnati in un doppio legame C=C o
11 Gli orbitali ibridi: Ibridazione sp Nell ibridzione sp solo questi due orbitali generano orbitali ibridi identici mentre gli orbitali p y e p z rimangono invariati
12 Gli orbitali ibridi: Ibridazione sp
13 E come spieghiamo la struttura dell etino o acetilene? ETINO 13
14 Ricapitolando IBRIDAZIONE 1s + 3p 4 sp 3 (tetraedro) 1s + 2p IBRIDAZIONE 3 sp 2 (triangolare planare) 1s + 1p IBRIDAZIONE 2 sp (lineare) 14
15 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
16 Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra loro mediante legami singoli (C n H 2n+2 ) -Gli alcani sono insolubili in acqua: sono apolari, pertanto non formano legami idrogeno con le molecole d acqua
17 Tutti gli alcani si indicano con la desinenza: -ano Numero atomi di carbonio crescente
18
19 Isomeria Gli idrocarburi Isomeri di struttura: composti con la stessa composizione chimica ma in cui gli atomi sono legati in modo diverso Esempio: butano e isobutano
20 Isomeria Gli idrocarburi All aumentare del numero di atomi di carbonio aumenta il numero di possibili isomeri
21 Isomeria ISOMERI CONFORMAZIONALI
22 Isomeria + STABILE
23 Isomeria
24 Isomeria
25 Propietà fisiche degli Alcani
26
27
28
29
30
31 Gli idrocarburi Cicloalcani Alcani a catena ciclica Rappresentazione a stecche e sfere
32 Gli idrocarburi I cicloalcani, ad eccezione del ciclopropano (3 atomi di carbonio), non sono piani ma adottano delle conformazioni ripiegate tridimensionali che consentono di diminuire la tensione di anello. Es. Cicloesano
33 Isomeria
34 Gli idrocarburi ALCHENI o olefine. Sono caratterizzati dalla presenza di un doppio legame nella molecola Tutti gli alcheni si indicano con la desinenza: -ene indicando il numero del primo atomo di carbonio partecipante al doppio legame Gli atomi di carbonio si numerano partendo dall estremità più vicina al doppio legame CH3 CH=CH CH2 CH3 CH3 CH2 CH =CH CH3 2-pentene 2-pentene
35 Gli idrocarburi CICLO ALCHENI Conformazione cicloesene
36 Isomeria geometrica cis-trans Questi due composti hanno la stessa formula molecolare e gli atomi sono legati nello stesso ordine ma la disposizione nello spazio è diversa: sono diasteromeri Reazioni degli alcheni: addizione al doppio legame CH 2 CH 2 + H 2 CH 3 CH 3
37 Addizione elettrofila agli alcheni Regola di Markovnikov: in un addizione elettrofila di acidi alogenidrici ad un alchene asimmetrico, l elettrofilo si lega al carbonio meno sostituito
38 In una molecola possono essere presenti 2 (dieni) o più (trieni, tetraeni ) legami multipli Maggiore stabilità degli isolati. Perché?
39 Gli idrocarburi ALCHINI Sono caratterizzati dalla presenza di un triplo legame nella molecola Tutti gli alchini si indicano con la desinenza: -ino indicando il numero del primo atomo di carbonio partecipante al triplo legame GLI ALCHINI NON POSSONO FORMARE CICLI
40
41 IDROCARBURI AROMATICI Sono caratterizzati dalla presenza di delocalizzazione elettronica che conferisce particolare stabilià. Immaginiamo la struttura molecolare che vede ogni atomo di C con 3 orbitali atomici ibridizzati sp 2 ed un orbitale p non ibrido:
42 IDROCARBURI AROMATICI Gli idrocarburi BENZENE Non si può dire con precisione quali siano gli orbitali p che si uniscono per formare il doppio legame, perché si possono avere entrambe le strutture in risonanza: Grazie alla delocalizzazione degli elettroni negli orbitali p z l anello benzenico è un anello AROMATICO. Il concetto di Aromaticità non è confinato solo al benzene, in quanto un affinché composto viene considerato aromatico se presenta una particolare configurazione elettronica.
43
44 I composti aromatici policiclici NB:Nelle strutture chimiche gli atomi di carbonio (e gli atomi di idrogeno ad essi legati) spesso non sono indicati ma vengono rappresentati solo i segmenti dei legami che li uniscono
45 I gruppi funzionali E possibile catalogare tutti i composti organici in poche decine di famiglie. La collocazione di una molecola in una famiglia dipende dalla presenza di un caratteristico gruppo di atomi definito gruppo funzionale. Es1 : Etene (o etilene) e limonene appartengono alla stessa famiglia, quella degli alcheni, perché possiedono lo stesso gruppo funzionale, il doppio legame C=C, e la loro reattività chimica sarà molto simile indipendentemente dalle loro dimensioni o dalla loro complessità Es2: Colesterolo ed etanolo: due alcoli strutturalmente molto diversi, ma possiedono entrambi il gruppo funzionale -OH
46 I gruppi funzionali
47 I gruppi funzionali
48 ALCOLI Formula generale R OH SUFFISSO: -OLO Es. METANOLO alcoli possono essere classificati come primari (1 ), secondari (2 ) o terziari (3 ) a seconda che il gruppo OH sia legato ad un carbonio primario, secondario o terziario. Si indica con gruppo generico R una catena di 1 o più atomi di carbonio Es: METANOLO Es: 2- BUTANOLO Es: 2- METIL 2-PROPANOLO
49 Il punto di ebollizione degli alcoli è più alto rispetto a quello degli alcani con peso molecolare simile. Ciò dovuto alla polarità delle molecole di alcol che si associano allo stato liquido grazie ai legami idrogeno. A causa di questi legami è richiesta una ulteriore energia, rispetto agli alcani, per separare le molecole una dall altra. L aumento di solubilità in acqua degli alcoli rispetto agli alcani, dipende dai legami idrogeno che il gruppo OH stabilisce con le molecole di acqua
50 Alcoli con più di un ossidrile Reazioni degli alcoli: Disidratazione Ossidazione
51 AMMINE R NH2 SUFFISSO: AMMINA METILAMMINA AMMINA PRIMARIA AMMINA SECONDARIA AMMINA TERZIARIA Alta importanza biologica dovuta alla loro reattività con acqua, acidi carbossilici e aldeidi
52 ALDEIDI SUFFISSO: ALE METANALE o aldeide formica PROPANALE o aldeide propionica CHETONI SUFFISSO: ONE DIMETIL CHETONE METIL-PROPIL CHETONE Alta importanza biologica dovuta alla loro reattività con alcoli e ammine SI OTTENGONO PER OSSIDAZIONE DA ALCOLI PRIMARI E SECONDARI
53 ACIDI CARBOSSILICI PREFISSO: ACIDO SUFFISSO: OICO SI OTTENGONO PER OSSIDAZIONE DI ALDEIDI ESTERI SUFFISSO: ATO alla catena R + di R SI OTTENGONO PER REAZIONE DI UN ACIDO CARBOSSILICO CON UN ALCOL propanoato di metile
54 ETERI R O R SUFFISSO: ETERE DIMETIL ETERE METIL ISOBUTIL ETERE più volatili e meno solubili degli alcoli TIOLI R SH SUFFISSO: TIOLO METANTIOLO
55 Elementi costitutivi della materia vivente: 20 aminoacidi proteine, ormoni, porfirine, substrati energetici 5 basi nucleotidiche DNA, RNA, coenzimi, trasportatori di energia meno di dieci tipi di zuccheri substrati energetici, elementi di riconoscimento cellulare acidi grassi costituenti delle membrane, substrati energetici Le macromolecole sono composti multimerici assemblati a partire da un certo numero di subunità più semplici: Proteine aminoacidi Acidi nucleici nucleotidi Polisaccaridi monosaccaridi Lipidi acidi grassi, alcoli
56 SUBUNITA MONOMERICHE Lettere dell alfabeto (26 tipi diversi) Deossiribonucleotidi (4 tipi diversi) Aminoacidi (20 tipi diversi) A L M H I G F E D C B R Q P O N S T U V Z X W K J Y M E S S A G G I M A S S A G G I P A S S A G G I C T G A G A T T A C C A A G T T T C C G G A C C A T T G Thr Tyr Phe Asn Gly Ser Met Asp Lys Gln Leu Ile Arg Val Ala His Pro Trp Cys Glu Gly Val Ser Asp Phe Arg Glu Ala Arg Gly Leu Pro Cys Asn Phe Glu Asp Gly Leu Pro Gly Lys Trp Cys SEQUENZE LINEARI ORDINATE
57 Formula generale (CH 2 O) n Monosaccaridi sono aldeidi o chetoni poliossidrilici; sono solidi cristallini inodori, incolori, idrosolubili. Contengono uno o più atomi di C asimmetrici e quindi sono presenti in natura sotto forma di vari isomeri. Si dividono in: Aldosi (ribosio, glucosio, galattosio, ) Chetosi (fruttosio, )
58
59 Legame O- glicosidico : gruppo ossidrilico di uno zucchero che reagisce con l atomo di C anomerico di un altro zucchero. Può essere di tipo α o β
60 Polimeri ad alto peso molecolare formati da numerose unità di monosaccaridi. Si distinguono in omopolisaccaridi e eteropolisaccaridi Omopolisaccaridi con funzione di riserva energetica: AMIDO Polisaccaride di riserva delle cellule vegetali formato da unità di glucosio. GLICOGENO Polisaccaride formato da unità di glucosio. Ha funzione di riserva nelle cellule animali ed è presente in particolare nel fegato e nel muscolo scheletrico.
61
62
63
64 Componenti strutturali degli acidi nucleici Trasportatori di energia chimica (ATP ) Cofattori enzimatici (NAD, FAD,..)
65 RNA Polimero di ribonucleotidi DNA Polimero di deossiribonucleotidi
66 DNA: -depositario dell informazione genetica della cellula (genoma) - costituito da due filamenti antiparalleli avvolti uno attorno all altro a formare una doppia elica destrorsa - estremamente stabile
67 Scoperta nel 1953 da Watson e Crick
68 Le proteine sono macromolecole di peso molecolare compreso fra 5000 e daltons costituite da un certo numero di aminoacidi legati fra loro in modo covalente in sequenze lineari caratteristiche. Gli aminoacidi si differenziano in base alla struttura della catena laterale; gli aminoacidi che compongono le proteine sono solamente 20 e sono tutti nella forma L-
69 ossia:
70
71 Catena laterale apolare Catena laterale polare Catena laterale carica
72 Ogni proteina contiene un unico gruppo amminico libero e un unico gruppo carbossilico libero Il legame peptidico è un legame di tipo amidico che unisce il gruppo carbossilico di un aminoacido con il gruppo amminico dell aminoacido successivo
73 Struttura primaria È la sequenza aminoacidica della proteina a partire dall estremità N-terminale; è determinata dal codice genetico e si basa sul legame covalente fra gli aminoacidi. Struttura secondaria, terziaria e quaternaria Dipendono dalla struttura primaria; si basano su interazioni deboli non covalenti come legami idrogeno, interazioni idrofobiche,
74
75 Fonte di energia Riserva di energia Lipidi Sostanze organiche molto eterogeneee dal punto di vista chimico, caratterizzate da dimensioni molecolari modeste, insolubili in acqua ma solubili nei solventi organici. Si distinguono in grassi e oli. Funzione strutturale: membrane biologiche Ormoni steroidei,... Protezione termica, meccanica, elettrica
76 ACIDI GRASSI Sono l unità costituente di altri lipidi. Sono acidi carbossilici a lunga catena (da 4 a 36 atomi di carbonio). Le proprietà fisiche dipendono dalla lunghezza della catena idrocarburica e dalla presenza di doppi legami Acido stearico 18:0 Acido oleico 18:1 ( 9 )
77 Alcuni acidi grassi presenti in natura
78 L impacchettamento degli acidi grassi dipende dal loro grado di saturazione Gli acidi grassi saturi nella forma completamente estesa si impacchettano con una disposizione quasi cristallina (consistenza cerosa). La presenza di uno o più doppi legami interferisce con questa disposizione e produce aggregati meno stabili (liquidi oleosi)
79 I lipidi nell alimentazione Gli acidi grassi saturi sono solidi a temperatura ambiente e si trovano nei grassi animali (formaggi, carni, salumi, burro ecc.); essi possono essere dannosi se assunti in quantità eccessiva. Gli acidi grassi insaturi sono liquidi a temperatura ambiente e si trovano per esempio negli oli vegetali (olio d oliva e di semi) e nel pesce. Un importante acido grasso monoinsaturo è l acido oleico che si trova nell olio d oliva. Come tutti gli acidi grassi insaturi esso agisce positivamente nella prevenzione dell aterosclerosi. Gli acidi grassi insaturi possono distinguersi in monoinsaturi, se hanno un doppio legame lungo la catena carboniosa, e polinsaturi, se hanno due o più doppi legami. I più importanti acidi grassi polinsaturi sono: 1) acido linoleico, della serie omega-6 (olio d oliva, di mais, di vinaccioli e di soia) 2) acido linolenico, della serie omega-3. (pesce azzurro, semi di soia e olio di soia) Sono detti anche acidi grassi essenziali perché l organismo umano non è in grado di sintetizzarli, per cui devono essere introdotti con gli alimenti. sono i costituenti della membrana cellulare; ostacolano la deposizione di colesterolo nelle arterie prevenendo l aterosclerosi; da essi derivano le prostaglandine, sostanze prodotte dal nostro organismo che svolgono numerose funzioni.
80 3 acidi grassi legati ad una molecola di glicerolo mediante legame estere Non polari, idrofobici, insolubili in acqua Presenti nella cellula come gocce nel citosol (in particolare negli adipociti) Funzione di riserva energetica In alcuni animali usati anche come isolamento termico
81 I costituenti del fosfato di calcio [Ca 3 (PO 4 ) 2 ] hanno le seguenti masse molari espresse in g/mol: Ca = 40, P = 31, O = 16. Si può affermare che 0,125 moli di tale composto: A) Contengono una massa di calcio superiore a quella dell ossigeno B) Contengono 7,525 *10 24 molecole C) Contengono 1 mole di atomi di ossigeno D) Hanno massa 155g E) Dissociandosi completamente liberano 0,25 moli di cationi
82
83 Calcolare quanti grammi di idrogeno gassoso si formano per reazione di 39 grammi di potassio metallico (peso atomico: 39 u.m.a.) con acqua (reagente in eccesso), dopo aver bilanciato la seguente reazione: K + H 2 O --> KOH + H 2 A)4.5 B)0.5 C)2.0 D)3.0 E)1.0 Nei trigliceridi gli acidi grassi sono legati a: A)Glicerolo B)Propanolo C)Acido glicerico D)Glicerofosfato E)Propandiolo
84 Dati i seguenti acidi: (1) H 2 SO 4 ; (2) CH 3 COOH; (3) H 2 S; (4) HCN; (5) HClO 4 ; (6) HNO 3 ; (7) H 3 PO 4 ; (8) HF, individuare la serie che indica solamente quelli poliprotici. A) (1), (2), (3), (7) B) (3), (4), (8) C) (2), (4), (6) D) (1), (3), (7) E) (1), (5) Quanti grammi di H 2 SO 4 (P.M. = 98 u.m.a.) sono contenuti in 250 ml di una soluzione acquosa 2 M di H 2 SO 4? A) 57 g B) 98 g C) 24,5 g D) 49 g E) 13 g
85 Quanti grammi di una sostanza avente peso molecolare pari a 100 u.m.a. sono necessari per preparare 10 ml di una soluzione 2,5 M? A) 5,00 B) 250,00 C) 10,00 D)2,50 E) 1,25 Qual è lo stato di ibridazione degli orbitali del carbonio nel cicloesano (C 6 H 12 )? A) sp 3 B) sp C) sp 2 D) sp 4
86 Il ph di una soluzione tampone di un acido debole corrisponde al pk dell acido quando: A) nel tampone è presente anche una base forte B) nel tampone è presente anche un acido forte C) il rapporto tra la concentrazione dell acido debole e la concentrazione del suo sale è pari a 10 D) la concentrazione dell acido debole è uguale alla concentrazione del suo sale E) la concentrazione dell acido debole è uguale alla metà della concentrazione del suo sale Quale delle seguenti sostanze può comportarsi sia da acido che da base secondo Brønsted-Lowry? A) CO 2-3 B) H 2 PO 4 - C) H 3 O + D) NH 4 + E) CH 4
87 Qual è il volume minimo di ossigeno per la combustione completa di 400ml di propano se consideriamo i due gas nelle stesse condizioni di temperatura e pressione? A) 1000 ml B) 1200 ml C) 1600 ml D) 2000 ml E) 4000 ml Quando un catalizzatore è aggiunto ad una reazione chimica, quale/i dei seguenti eventi accade/ono? 1. L'energia di attivazione viene abbassata 2. La quantità finale di prodotto aumenta 3. Aumenta la velocità di formazione dei prodotti A) Solo 1 e 3 B) Solo 3 C) Solo 1 D) Solo 1 e 2 E) Solo 2
88 Durante la fusione di un corpo che si trova allo stato solido quale delle seguenti grandezze del sistema non cambia? A) Il volume B) La densità C) L energia termica D) La velocità media con cui si muovono le sue particelle E) La temperatura Quale è la formula bruta del dimetilchetone? A) C 3 H 3 O 2 B) C 3 H 4 O C) C 3 H 3 O D) C 3 H 2 O E) C 3 H 6 O
89 Per quanti atomi di idrogeno il benzene differisce dal cicloesano? A) 4 B) 3 C) 5 D) 6 E) 2 In 100 ml di una soluzione 2M sono presenti 6 grammi di soluto. Qual è il peso molecolare del soluto in u.m.a.? A) 60 B) 30 C) 120 D) 3 E) 12
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Aspetti generali dei lipidi
 7.3 I lipidi Aspetti generali dei lipidi I lipidi, anche detti grassi, sono composti organici ternari, ovvero formati da tre elementi chimici C, H, O (possono contenere anche P, N). Caratteristiche: -
7.3 I lipidi Aspetti generali dei lipidi I lipidi, anche detti grassi, sono composti organici ternari, ovvero formati da tre elementi chimici C, H, O (possono contenere anche P, N). Caratteristiche: -
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Di cosa è fatta una cellula?
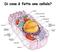 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
CARBOIDRATI SEMPLICI
 CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
Problemi 1 PROPEDEUTICITÀ
 Problemi 1 PROPEDEUTICITÀ Da manifesto degli studi del corso per sostenere l esame di Chimica Biologica bisogna aver superato: Citologia e Istologia Chimica Organica (Chimica generale) Non vale questa
Problemi 1 PROPEDEUTICITÀ Da manifesto degli studi del corso per sostenere l esame di Chimica Biologica bisogna aver superato: Citologia e Istologia Chimica Organica (Chimica generale) Non vale questa
CHIMICA delle MACROMOLECOLE BIOLOGICHE
 Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
Fig. 1. Fig. 3. Fig. 4
 Cap. 9 La chimica del carbonio saperi essenziali 9.1 L atomo di carbonio L atomo di carbonio ha la possibilità di formare 4 legami covalenti e i composti che può formare possono essere tridimensionali
Cap. 9 La chimica del carbonio saperi essenziali 9.1 L atomo di carbonio L atomo di carbonio ha la possibilità di formare 4 legami covalenti e i composti che può formare possono essere tridimensionali
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
CHIMICA ORGANICA. 2 a D. Novembre Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14. Ponte Felcino Perugia.
 CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Il carbonio è l elemento più abbondante nelle molecole biologiche
 Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
I composti del carbonio
 Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) colesterolo
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) colesterolo
Caratteristiche generali
 Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
Caratteristiche generali I lipidi (o grassi) sono un gruppo di sostanze, costituite prevalentemente da carbonio, idrogeno e ossigeno (in proporzioni ovviamente diverse da quelle dei glucidi) con la caratteristica
La massa è la quantità di materia di cui è fatta una qualsiasi cosa
 Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
Cos è la chimica organica
 Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Di cosa è fatta una cellula?
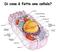 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Cos è la chimica organica
 Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
R = GRUPPO FUNZIONALE Atomo o raggruppamento atomico
 GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
LIPIDI. Steroidi Acidi grassi Trigliceridi Fosfolipidi Prostaglandine Vitamine liposolubili
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte.
 Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
Aspetti generali. Caratteristiche: I lipidi, anche detti grassi, sono composti ternari C, H, O (possono contenere anche P, N)
 Lipidi Aspetti generali I lipidi, anche detti grassi, sono composti ternari C, H, O (possono contenere anche P, N) Caratteristiche: sono untuosi al tatto sono insolubili in acqua sono solubili in solventi
Lipidi Aspetti generali I lipidi, anche detti grassi, sono composti ternari C, H, O (possono contenere anche P, N) Caratteristiche: sono untuosi al tatto sono insolubili in acqua sono solubili in solventi
Sostanze grasse o lipidi
 Sostanze grasse o lipidi I lipidi (in greco significa sostanze grasse ) sono composti ternari formati da carbonio, idrogeno e ossigeno e sono caratterizzati dalla proprietà di essere insolubili in acqua
Sostanze grasse o lipidi I lipidi (in greco significa sostanze grasse ) sono composti ternari formati da carbonio, idrogeno e ossigeno e sono caratterizzati dalla proprietà di essere insolubili in acqua
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
LIPIDI. Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
04/10/17 I LEGAMI DEL CARBONIO. Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole
 04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
Struttura e legami dei composti organici. VIDEOLEZIONE L ibridazione dell atomo di carbonio. Alcani e cicloalcani
 III 1 Struttura e legami dei composti organici 1.1 La nascita della chimica organica 2 1.2 Struttura elettronica degli atomi 3 1.3 Regola dell ottetto e simbolismo di Lewis 5 1.4 Elettronegatività e legami
III 1 Struttura e legami dei composti organici 1.1 La nascita della chimica organica 2 1.2 Struttura elettronica degli atomi 3 1.3 Regola dell ottetto e simbolismo di Lewis 5 1.4 Elettronegatività e legami
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
ESERCIZI AGGIUNTIVI DI FINE CAPITOLO
 Phelan, Pignocchino Le scienze naturali Osservare i viventi ESERCIZI AGGIUNTIVI DI FINE CAPITOLO Capitolo 2 L IDENTITÀ DEGLI ATOMI 1. Con quale relazione si ricava il numero massimo di elettroni in ciascun
Phelan, Pignocchino Le scienze naturali Osservare i viventi ESERCIZI AGGIUNTIVI DI FINE CAPITOLO Capitolo 2 L IDENTITÀ DEGLI ATOMI 1. Con quale relazione si ricava il numero massimo di elettroni in ciascun
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli Alcheni. Ibridazione sp 2. I legami chimici degli alcheni
 Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza.
 Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza. La costante di Avogadro. La massa molare. Relazione tra massa di una sostanza
Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza. La costante di Avogadro. La massa molare. Relazione tra massa di una sostanza
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Classificazione. In base alla composizione chimica i lipidi si classificano in: Lipidi semplici (costituiti da CHO)
 1 2 LIPIDI Lipidi significa grasso. Sono composti ternari C, H, O. Sono detti anche grassi. Nel corpo umano costituiscono circa il 17% del peso corporeo (ma variano in funzione del grasso accumulato).
1 2 LIPIDI Lipidi significa grasso. Sono composti ternari C, H, O. Sono detti anche grassi. Nel corpo umano costituiscono circa il 17% del peso corporeo (ma variano in funzione del grasso accumulato).
I doppi legami sono in genere nella forma stereoisomera cis
 GLI ACIDI GRASSI SONO CLASSIFICATI IN BASE ALLA STRUTTURA DELLA CATENA IDROCARBURICA SATURI - senza doppi legami catena satura in H, completamente ridotta MONOINSATURI - un doppio legame POLINSATURI -
GLI ACIDI GRASSI SONO CLASSIFICATI IN BASE ALLA STRUTTURA DELLA CATENA IDROCARBURICA SATURI - senza doppi legami catena satura in H, completamente ridotta MONOINSATURI - un doppio legame POLINSATURI -
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica -aminoacidi
 Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica α-aminoacidi (17.1) subunità che costituiscono le proteine formatei da un carbonio-α
Katherine J. Denniston, Joseph J. Topping, Robert L. Caret Chimica generale - Chimica organica - Propedeutica biochimica α-aminoacidi (17.1) subunità che costituiscono le proteine formatei da un carbonio-α
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
