Allestire un unità di Fase I in Piemonte: WORK IN PROGRESS
|
|
|
- Ruggero Marra
- 5 anni fa
- Visualizzazioni
Transcript
1 Allestire un unità di Fase I in Piemonte: WORK IN PROGRESS (L ESPERIENZA DELL AOU San Luigi) Francesca Arizio Coordinatore della Ricerca Clinica francesca.arizio@unito.it Oncologia Polmonare AOU San Luigi-Orbassano (TO)
2 Determina AIFA del 19 Giugno 2015 Determina inerente i requisiti minimi necessari per le strutture sanitarie che seguono sperimentazioni di FASEI: -Articolo 1- Definizioni Sperimentazione Clinica di Fase I o studio di Fase I Unità, centro o struttura di Fase I: struttura, incluso il laboratorio di analisi, che conduce sperimentazioni di FASE I in maniera esclusiva o parziale, permanente o temporanea Deviazioni critiche delle GCP -Articolo 2- Requisiti Tutte le Unità, Centri o Strutture di Fase I devono essere in possesso dei requisiti dettagliati nell allegato 1 e nelle appendici Allegato 1 Aspetti generali Requisiti delle Unità Cliniche per le Sperimentazioni di Fase I (appendice 1) Requisiti dei laboratori per le sperimentazioni di Fase I (appendice 2) Lista delle procedure operative standard SOP( appendice 3)
3 -Articolo 3- Riconoscimento dei requisiti Riconoscimento dei requisiti-> autocertificazione Deviazioni riscontrate durante la conduzione dello studio e notifica all ufficio Ricerca e Sperimentazioni cliniche e Attività Ispettive GCO dell AIFA Richiesta di Ispezioni all Unità/Centro all ufficio -Articolo 4- Aggiornamento requisiti DM per Unita /Centri Privati (Competenza delle ASL) Conformità alle norme vigenti in materia igienico-sanitaria e di sicurezza per le attività che vengono compiute Possesso dei requisiti minimi per l esercizio delle attività sanitarie di cui al DPR14 gennaio Articolo 5- Sperimentazioni di FASE I eseguite all estero Le sperimentazioni di FASE I eseguite all estro i cui risultati vengono presentati all AIFA quali parte di un dossier per l autorizzazione alla immissione in commercio, debbono essere condotte in strutture, inclusi i laboratori, con i requisiti almeno equivalenti a quelli della determina 809/2015 dell AIFA -Articolo 6- Revisione dei requisiti
4 La Determina in Struttura Pubblica In tali strutture le sperimentazioni di Fase I possono essere condotte in singole Unità dedicate alle sperimentazioni di Fase I e in possesso dei requisiti di cui al presente documento o in alternativa i reparti specialistici che per il periodo della sperimentazione utilizzano strutture, SOP e personale in possesso dei requisiti della determina
5 Da dove partiamo?
6 PROGETTO Si decide di presentare alla Direzione Sanitaria un progetto congiunto di autocertificazione dell Oncologia e dell Ematologia La struttura che si autocertificherà sarà l ONCOEMATOLOGIA
7 La determina nei centri di Oncologia -Già organizzati per curare -Già organizzati per fare ricerca -Già strutturati per «subire» Audit o Ispezioni e quindi già abituati a confrontarsi su controlli che vengono normalmente effettuati per studi clinici Profit (e non solo)
8 ..ENTRIAMO NEL VIVO DI COSA TUTTO QUESTO SIGNIFICHI NELLA PRATICA DOVE SIAMO, ma soprattutto, DA DOVE PARTIAMO?.E SOPRATTUTTO DOVE DOBBIAMO ARRIVARE?
9 I Requisiti delle Unità Cliniche APPENDICE I A) Requisiti di carattere generale B) Requisiti per interventi di emergenza avanzata C) Requisiti di qualità A Organizzazione della struttura Attrezzature mediche B -La struttura di fase I deve essere collocata all interno di un ospedale con rianimazione -Reperibilità H24 del personale dedicato alle emergenze -Formazione adeguata del personale: fomazione BLS & ALS Gestione delle Emergenze Personale in servizio presso l Unità C L Unità deve avere un appropriato sistema di assicurazione di Qualità (QA) e designare un responsabile della gestione di questo sistema
10 Organizzazione della struttura: A -struttura adeguata dell edificio, rispetto norme igieniche -controllo telecamere (sia dell unità sia dei pazienti) -area per registrazione screening esame medico pazienti -area ricovero adeguata (letti inclinabili e adattabili al peso, Testate dei letti attrezzate) -area ricreativa -area preparazione pasti -servizi igienici adeguati -area conservazione farmaci dedicata -area dedicata alla conservazione campioni biologici -area Archivio con armadi ignifughi (misure antincendio,antiallagamanto ecc) -gruppo elettrogeno con reperibilità h24 Attrezzature mediche -apparecchiature per rianimazione -strumenti visita medica -Elettrocardigrafo con monitoraggio -Monitoraggio centralizzato in continuo -Frigoriferi -strumenti per trattamento campioni -servizi di radiologia,tac,rmn -PET e medicina nucleare -ecografo Emergenze -Fondamentale la collocazione dell Unità all interno dell ospedale. -Formazione in emergenze del personale (ALS, BLS -Carrello emergenze (assistenza ventilatoria,circolatoria,farmaci per emergenze, defibrillatore con ECG sia a rete sia a batteria, misuratore pressione) -Pulsanti di allarme nelle aree dei soggetti -Numeri di contatto per i pazienti h24 -Presenza di antidoti per IMP -
11 Personale in servizio presso l Unità -Direttore medico (laurea da almeno 8 aa responsabile della supervisione degli studi clinici, conoscenza della Metodologia Generale della sperimentazione clinica -Medico farmacologo -Uno o più medici laureati da almeno 5 anni -Almeno un laureato in farmacia o CTF per gestione farmaci -Almeno un infermiere con conoscenze in rianimazione e GCP (Infermiere di ricerca) -Persona con laurea idonea per trattamento e conservazione materiali biologici raccolti durante lo studio -PI con esperienza clinica rilevante e specializzazione attinente alla patologia trattata: tutto documentato -Responsabile QA -Monitor interno alla struttura o fornito da sponsor -»figura di raccordo» tra Unità e Promotore e AC
12 SOP-PROCEDURE OPERATIVE STANDARD
13 -23 gennaio 2017: 1 mail di contatto con la struttura di Ematologia. -fine marzo 2017: 1 TC con società che segue la certificazione -luglio 2017:invio di bozza di contratto di supporto per l ottenimento dell abilitazione necessaria ai centri per seguire le sperimentazioni di Fase 1, completo della fornitura del servizio di QA e Auditing. -inizio agosto 2017 primo incontro -conferimento definitivo dell incarico con firma contratto gennaio Febbraio 2018 COMINCIANO I LAVORI! Si procede dal centro con revisioni di SOP e pianificazione di incontri con strutture coinvolte -13 Giugno 2018: incontro per valutazione avanzamento lavori -2 ottobre 2018: nuovo incontro (in concomitanza del quale si decide di procedere con certificazione laboratorio)
14 COSA RESTA DA FARE? -Acquisto armadi per archivio -Acquisto apparecchi per telemetria -Servizio di Quality Assurance -Definizione delle SOP e manuale di qualità TEMPISTICHE Fine Aprile?
15 Grazie per l attenzione!
Nuove Sfide - prepararsi a condurre sperimentazioni di fase I. Valentina Sinno Coordinatore del CTC Fondazione IRCCS Istituto Nazionale dei Tumori
 Nuove Sfide - prepararsi a condurre sperimentazioni di fase I Valentina Sinno Coordinatore del CTC Fondazione IRCCS Istituto Nazionale dei Tumori Milano 14-15 Giugno 2018 Determina AIFA del 19 Giugno
Nuove Sfide - prepararsi a condurre sperimentazioni di fase I Valentina Sinno Coordinatore del CTC Fondazione IRCCS Istituto Nazionale dei Tumori Milano 14-15 Giugno 2018 Determina AIFA del 19 Giugno
Studi di Fase I e requisiti minimi dei centri sperimentali: la Determina AIFA
 Sperimentazione Clinica in Neurologia Studi Clinici Innovativi Milano, 30 giugno 2016 Studi di Fase I e requisiti minimi dei centri sperimentali: la Determina AIFA Marino Gobetti QA Consultant marinogobetti1@alice.it
Sperimentazione Clinica in Neurologia Studi Clinici Innovativi Milano, 30 giugno 2016 Studi di Fase I e requisiti minimi dei centri sperimentali: la Determina AIFA Marino Gobetti QA Consultant marinogobetti1@alice.it
REQUISITI DELLA UNITA CLINICHE
 REQUISITI DELLA UNITA CLINICHE Giovanni Apolone Direttore Scientifico Fondazione IRCCS Istituto Nazionale dei Tumori Valentina Sinno Coordinatore del CTC Fondazione IRCCS Istituto Nazionale dei Tumori
REQUISITI DELLA UNITA CLINICHE Giovanni Apolone Direttore Scientifico Fondazione IRCCS Istituto Nazionale dei Tumori Valentina Sinno Coordinatore del CTC Fondazione IRCCS Istituto Nazionale dei Tumori
Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza. XXV CONGRESSO NAZIONALE GIQAR Parma, 19 maggio 2016
 Determina AIFA 2015 sui requisiti minimi necessari per le strutture sanitarie che eseguono sperimentazioni di fase I: scopi ed aspetti generali, parte clinica Angela Del Vecchio Direttore Ufficio Attività
Determina AIFA 2015 sui requisiti minimi necessari per le strutture sanitarie che eseguono sperimentazioni di fase I: scopi ed aspetti generali, parte clinica Angela Del Vecchio Direttore Ufficio Attività
ALLESTIRE UNA UNITA' DI FASE I IN PIEMONTE - WORK IN PROGRESS
 ALLESTIRE UNA UNITA' DI FASE I IN PIEMONTE - WORK IN PROGRESS L'esperienza dell'oncologia1 dell'aou Città della Salute e della Scienza Cristiana Taverniti Coordinatore della Ricerca Clinica Oncologia Medica
ALLESTIRE UNA UNITA' DI FASE I IN PIEMONTE - WORK IN PROGRESS L'esperienza dell'oncologia1 dell'aou Città della Salute e della Scienza Cristiana Taverniti Coordinatore della Ricerca Clinica Oncologia Medica
Determina AIFA n. 809/2015 del 19 giugno 2015 Sperimentazione clinica di fase I Requisiti minimi
 del 19 giugno 2015 Sperimentazione clinica di fase I Requisiti minimi M.P. Trojniak Settore Farmaceutico- Protesica-Dispositivi medici, Venezia del 19 giugno 2015 Determina inerente i requisiti minimi
del 19 giugno 2015 Sperimentazione clinica di fase I Requisiti minimi M.P. Trojniak Settore Farmaceutico- Protesica-Dispositivi medici, Venezia del 19 giugno 2015 Determina inerente i requisiti minimi
Requisiti dei laboratori per le sperimentazioni di fase I
 Requisiti dei laboratori per le sperimentazioni di fase I Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza Corso AIOM: studi di fase I Milano, 17 maggio 2016 Dichiarazione
Requisiti dei laboratori per le sperimentazioni di fase I Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza Corso AIOM: studi di fase I Milano, 17 maggio 2016 Dichiarazione
Analisi della Determina AIFA
 Analisi della Determina AIFA Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza Sperimentazione clinica di Fase I in Italia Roma, 30 marzo 2016 Dichiarazione di trasparenza/interessi*
Analisi della Determina AIFA Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza Sperimentazione clinica di Fase I in Italia Roma, 30 marzo 2016 Dichiarazione di trasparenza/interessi*
Determina AIFA 2015 sui requisiti minimi necessari per le strutture sanitarie che eseguono sperimentazioni di fase I: scopi ed aspetti generali
 Determina AIFA 2015 sui requisiti minimi necessari per le strutture sanitarie che eseguono sperimentazioni di fase I: scopi ed aspetti generali Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP
Determina AIFA 2015 sui requisiti minimi necessari per le strutture sanitarie che eseguono sperimentazioni di fase I: scopi ed aspetti generali Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP
Ispezioni alle CRO. Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza
 Ispezioni alle CRO Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza XXV CONGRESSO NAZIONALE GIQAR Parma, 19 maggio 2016 Dichiarazione di trasparenza/interessi* Le opinioni
Ispezioni alle CRO Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di Farmacovigilanza XXV CONGRESSO NAZIONALE GIQAR Parma, 19 maggio 2016 Dichiarazione di trasparenza/interessi* Le opinioni
Modena, 22 Marzo 2016
 Modena, 22 Marzo 2016 Newsletter AIFA 04 Dicembre 2011 Normativa di riferimento: Fase I DPR 439, 21 settembre 2001 Procedure di accertamento della composizione e dell innocuità dei prodotti medicinali
Modena, 22 Marzo 2016 Newsletter AIFA 04 Dicembre 2011 Normativa di riferimento: Fase I DPR 439, 21 settembre 2001 Procedure di accertamento della composizione e dell innocuità dei prodotti medicinali
Agenzia Italiana del Farmaco
 Schema sulla verifica delle Norme di Buona Pratica Clinica presso i Comitati etici e i siti sperimentali, secondo gli orientamenti europei in materia 1 Principali riferimenti normativi Linee guida ICH
Schema sulla verifica delle Norme di Buona Pratica Clinica presso i Comitati etici e i siti sperimentali, secondo gli orientamenti europei in materia 1 Principali riferimenti normativi Linee guida ICH
IL MINISTRO DELLA SALUTE
 GAZZETTA UFFICIALE N. 279 DEL 28 NOVEMBRE 2008 MINISTERO DELLA SALUTE Decreto 31 Marzo 2008 DEFINIZIONE DEI REQUISITI MINIMI PER LE ORGANIZZAZIONI DI RICERCA A CONTRATTO (CRO) NELL AMBITO DELLE SPERIMENTAZIONI
GAZZETTA UFFICIALE N. 279 DEL 28 NOVEMBRE 2008 MINISTERO DELLA SALUTE Decreto 31 Marzo 2008 DEFINIZIONE DEI REQUISITI MINIMI PER LE ORGANIZZAZIONI DI RICERCA A CONTRATTO (CRO) NELL AMBITO DELLE SPERIMENTAZIONI
Il monitoraggio degli studi clinici. Il punto di vista dello Sperimentatore. 10 giugno 2014
 Il monitoraggio degli studi clinici Il punto di vista dello Sperimentatore 10 giugno 2014 Lo Sperimentatore GCP 4.1 Qualifiche dello sperimentatore ed accordi 4.1.3 Lo sperimentatore deve conoscere le
Il monitoraggio degli studi clinici Il punto di vista dello Sperimentatore 10 giugno 2014 Lo Sperimentatore GCP 4.1 Qualifiche dello sperimentatore ed accordi 4.1.3 Lo sperimentatore deve conoscere le
D.M. CONCERNENTE I CRITERI PER IL RICONOSCIMENTO DELLA IDONEITA'DEI CENTRI PER LA SPERIMENTAZIONE CLINICA DEI MEDICINALI
 D.M. CONCERNENTE I CRITERI PER IL RICONOSCIMENTO DELLA IDONEITA'DEI CENTRI PER LA SPERIMENTAZIONE CLINICA DEI MEDICINALI pubblicato sulla G.U. n. 122 del 28 maggio 1998 Il Ministro della Sanità VISTO l'art.
D.M. CONCERNENTE I CRITERI PER IL RICONOSCIMENTO DELLA IDONEITA'DEI CENTRI PER LA SPERIMENTAZIONE CLINICA DEI MEDICINALI pubblicato sulla G.U. n. 122 del 28 maggio 1998 Il Ministro della Sanità VISTO l'art.
La Determina AIFA sulle strutture di FASE I Ispezioni risultanze - chiarimenti - quesiti
 La Determina AIFA sulle strutture di FASE I Ispezioni risultanze - chiarimenti - quesiti Fabrizio Galliccia (Ispettore Senior GCP) 25 maggio 2017 XXVI CONGRESSO NAZIONALE GIQAR Dichiarazione di trasparenza/interessi*
La Determina AIFA sulle strutture di FASE I Ispezioni risultanze - chiarimenti - quesiti Fabrizio Galliccia (Ispettore Senior GCP) 25 maggio 2017 XXVI CONGRESSO NAZIONALE GIQAR Dichiarazione di trasparenza/interessi*
HIGH RESEARCH. DM 21 dicembre CTA e nuovo Osservatorio Sperimentazione Clinica
 srl DM 21 dicembre 2007- CTA e nuovo Osservatorio Sperimentazione Clinica Dr, General Manager HIGH RESERACH srl AriSla- Milano 16 Febbraio 2015 DM 21/12/2007-CTA Modalità di inoltro di richiesta di autorizzazione
srl DM 21 dicembre 2007- CTA e nuovo Osservatorio Sperimentazione Clinica Dr, General Manager HIGH RESERACH srl AriSla- Milano 16 Febbraio 2015 DM 21/12/2007-CTA Modalità di inoltro di richiesta di autorizzazione
Nuovi requisiti minimi per condurre studi di Fase I. Cosa è cambiato Celeste Cagnazzo
 Nuovi requisiti minimi per condurre studi di Fase I. Cosa è cambiato Celeste Cagnazzo Unità di Ricerca e Sviluppo Clinico S.C. Oncoematologia Pediatrica AOU Città della Salute e della Scienza Presidio
Nuovi requisiti minimi per condurre studi di Fase I. Cosa è cambiato Celeste Cagnazzo Unità di Ricerca e Sviluppo Clinico S.C. Oncoematologia Pediatrica AOU Città della Salute e della Scienza Presidio
Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di DAY SURGERY (Lista di controllo n. 4.9)
 Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di Y SURGERY (Lista
Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di Y SURGERY (Lista
Il Coordinamento della Ricerca 1 Corso ISG di Formazione per la Ricerca Clinica 28-Set-2015
 Qualità del dato e monitoraggio Il Coordinamento della Ricerca 1 Corso ISG di Formazione per la Ricerca Clinica 28-Set-2015 1 Qualità del dato 5.18.1b I dati riguardanti la sperimentazione debbono essere
Qualità del dato e monitoraggio Il Coordinamento della Ricerca 1 Corso ISG di Formazione per la Ricerca Clinica 28-Set-2015 1 Qualità del dato 5.18.1b I dati riguardanti la sperimentazione debbono essere
GCP Livello Investigatore PROGRAMMA. Durata: 2 giorni. Modalità di svolgimento: Obiettivi
 Formazione CTU-EOC Mercoledì 24 ottobre e 14 novembre 2018 Ospedale Italiano di Lugano 4 Piano Aula 3 Dalle 9.00 alle 17.30 (si prega di verificare nel programma l orario esatto) PROGRAMMA GCP Livello
Formazione CTU-EOC Mercoledì 24 ottobre e 14 novembre 2018 Ospedale Italiano di Lugano 4 Piano Aula 3 Dalle 9.00 alle 17.30 (si prega di verificare nel programma l orario esatto) PROGRAMMA GCP Livello
HIGH RESEARCH. DM 15 Novembre 2011 sostituisce DM 31 marzo CRO
 srl DM 15 Novembre 2011 sostituisce DM 31 marzo 2008- CRO Dr, President- General Manager HIGH RESERACH srl AriSla, 16 Febbraio 2015 premesse Visto il Decreto Presidente della Repubblica 18nov110 (Consiglio
srl DM 15 Novembre 2011 sostituisce DM 31 marzo 2008- CRO Dr, President- General Manager HIGH RESERACH srl AriSla, 16 Febbraio 2015 premesse Visto il Decreto Presidente della Repubblica 18nov110 (Consiglio
Proseguendo con i fondamentali: la normativa Italiana ed Europea
 Proseguendo con i fondamentali: la normativa Italiana ed Europea Manuela Monti Clinical Research Coordinator IRST-IRCCS Meldola manuela.monti@irst.emr.it Regolamento: si applica in tutti i paesi dell
Proseguendo con i fondamentali: la normativa Italiana ed Europea Manuela Monti Clinical Research Coordinator IRST-IRCCS Meldola manuela.monti@irst.emr.it Regolamento: si applica in tutti i paesi dell
Nomi: Bianca M. Francucci: Segreteria Scientifica Comitato Etico Giovanni Apolone: Direttore Scientifico
 Nomi: Bianca M. Francucci: Segreteria Scientifica Comitato Etico Giovanni Apolone: Direttore Scientifico Ente: Fondazione IRCCS Istituto Nazionale dei Tumori Titolo Comitati Etici e nuovi approcci alla
Nomi: Bianca M. Francucci: Segreteria Scientifica Comitato Etico Giovanni Apolone: Direttore Scientifico Ente: Fondazione IRCCS Istituto Nazionale dei Tumori Titolo Comitati Etici e nuovi approcci alla
MANUALE DEL CLINICAL RESEARCH COORDINATOR. Bologna, 13 Maggio 2016
 MANUALE DEL CLINICAL RESEARCH COORDINATOR SCOPI Essere uno strumento guida per chi muove i primi passi in questo mestiere Essere un testo di riferimento per chi ha già esperienza di ricerca clinica ma
MANUALE DEL CLINICAL RESEARCH COORDINATOR SCOPI Essere uno strumento guida per chi muove i primi passi in questo mestiere Essere un testo di riferimento per chi ha già esperienza di ricerca clinica ma
SPERIMENTAZIONE CLINICA DEI MEDICINALI DI TIPO COMMERCIALE
 SPERIMENTAZIONE CLINICA DEI MEDICINALI DI TIPO COMMERCIALE MODULISTICA A CURA DELLO SPERIMENTATORE RESPONSABILE E DEL DIRETTORE DELL UNITÀ OPERATIVA COINVOLTA Per ulteriori informazioni consultare la segreteria
SPERIMENTAZIONE CLINICA DEI MEDICINALI DI TIPO COMMERCIALE MODULISTICA A CURA DELLO SPERIMENTATORE RESPONSABILE E DEL DIRETTORE DELL UNITÀ OPERATIVA COINVOLTA Per ulteriori informazioni consultare la segreteria
Procedure Operative Standard
 Procedure Operative Standard Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di farmacovigilanza CORSO AIOM Studi Fase I Milano, 17 maggio 2016 Dichiarazione di trasparenza/interessi* Le
Procedure Operative Standard Angela Del Vecchio Direttore Ufficio Attività Ispettive GCP e di farmacovigilanza CORSO AIOM Studi Fase I Milano, 17 maggio 2016 Dichiarazione di trasparenza/interessi* Le
Determina AIFA n. 809/2015 del 19 giugno 2015
 Determina AIFA n. 809/2015 del 19 giugno 2015 1) Requisiti di Qualità derivanti da norme di carattere generale 2) Requisiti di qualità per i CTs no profit:il CTQT Dott. Umberto Filibeck Docente a contratto
Determina AIFA n. 809/2015 del 19 giugno 2015 1) Requisiti di Qualità derivanti da norme di carattere generale 2) Requisiti di qualità per i CTs no profit:il CTQT Dott. Umberto Filibeck Docente a contratto
ASPETTI GESTIONALI E DI COORDINAMENTO LEGATI ALLA FIGURA DELLA STUDY NURSE
 ASPETTI GESTIONALI E DI COORDINAMENTO LEGATI ALLA FIGURA DELLA STUDY NURSE Monica Bianchi Research Nurse Coordinator Fondazione Istituto Neurologico Nazionale Casimiro Mondino I.R.C.C.S. 1 CLINICAL TRIAL
ASPETTI GESTIONALI E DI COORDINAMENTO LEGATI ALLA FIGURA DELLA STUDY NURSE Monica Bianchi Research Nurse Coordinator Fondazione Istituto Neurologico Nazionale Casimiro Mondino I.R.C.C.S. 1 CLINICAL TRIAL
AZIENDA OSPEDALIERO - UNIVERSITARIA DI MODENA
 AZIENDA OSPEDALIERO - UNIVERSITARIA DI MODENA COPIA DAL REGISTRO DEGLI ATTI DEL DIRETTORE GENERALE N.16/0000091/DG Del 4 Luglio 2016 DELIBERA N. 16/0000091/DG OGGETTO: Istituzione dell Unità Centrale di
AZIENDA OSPEDALIERO - UNIVERSITARIA DI MODENA COPIA DAL REGISTRO DEGLI ATTI DEL DIRETTORE GENERALE N.16/0000091/DG Del 4 Luglio 2016 DELIBERA N. 16/0000091/DG OGGETTO: Istituzione dell Unità Centrale di
Applicazione del Risk Management nella Sperimentazione Clinica: il punto di vista del Quality Assurance
 Applicazione del Risk Management nella Sperimentazione Clinica: il punto di vista del Quality Assurance Roma 21 ottobre 2015 1 Documenti FDA e EMA Guidance FDA (August 2013) «Guidance for Industry: Oversight
Applicazione del Risk Management nella Sperimentazione Clinica: il punto di vista del Quality Assurance Roma 21 ottobre 2015 1 Documenti FDA e EMA Guidance FDA (August 2013) «Guidance for Industry: Oversight
LE SINERGIE DEL GRUPPO OPERATORI PAZIENTE ONCOLOGICO
 LE SINERGIE DEL GRUPPO OPERATORI PAZIENTE ONCOLOGICO MARIA, SIGNORA 54 ANNI, GIUNGE ALL'ATTENZIONE DEL C.A.S. VISITA PRENOTATA AL C.A.S. DA UN ALTRO OSPEDALE DOVE ERA STATA OPERATA ED ERA POI STATA TRASFERITA
LE SINERGIE DEL GRUPPO OPERATORI PAZIENTE ONCOLOGICO MARIA, SIGNORA 54 ANNI, GIUNGE ALL'ATTENZIONE DEL C.A.S. VISITA PRENOTATA AL C.A.S. DA UN ALTRO OSPEDALE DOVE ERA STATA OPERATA ED ERA POI STATA TRASFERITA
REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA
 REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA Processo Sequenza di processo Area di Attività Qualificazione regionale SETTORE ECONOMICO PROFESSIONALE 1 Chimica Chimica farmaceutica
REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA Processo Sequenza di processo Area di Attività Qualificazione regionale SETTORE ECONOMICO PROFESSIONALE 1 Chimica Chimica farmaceutica
Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di AREA DI DEGENZA OSPEDALIERA (Lista di controllo n. 4.
 Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di AREA DI DEGENZA
Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di AREA DI DEGENZA
REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA
 REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA QUALIFICAZIONE PROFESSIONALE Denominazione qualificazione Tecnico della progettazione e realizzazione di studi clinici e dello sviluppo
REPERTORIO DELLE QUALIFICAZIONI PROFESSIONALI DELLA REGIONE CAMPANIA QUALIFICAZIONE PROFESSIONALE Denominazione qualificazione Tecnico della progettazione e realizzazione di studi clinici e dello sviluppo
CHECK LIST - CHIRURGIA REFRATTIVA CON LASER AD ECCIMERI REQUISITO
 ENTE DI CERTIFICAZIONE DI QUALITA S.O.I. S.r.l. con socio unico V.I del 1-REQUISITI STRUTTURALI OBBLIGATORI CONSIGLIATI 1.1- Generali 1.1.1 E' garantita una facile accessibilità Autorizzazione dall'esterno
ENTE DI CERTIFICAZIONE DI QUALITA S.O.I. S.r.l. con socio unico V.I del 1-REQUISITI STRUTTURALI OBBLIGATORI CONSIGLIATI 1.1- Generali 1.1.1 E' garantita una facile accessibilità Autorizzazione dall'esterno
Proposta Formativa Corsi di Aggiornamento Professionale/Formazione Permanente LA REVISIONE DEI PROCESSI DI CURA IN TERAPIA INTENSIVA
 Scopo e campo d applicazione Lo scopo del corso è orientato allo sviluppo continuo professionale, attraverso l aggiornamento degli strumenti operativi attualmente in uso in Terapia Intensiva. Il corso
Scopo e campo d applicazione Lo scopo del corso è orientato allo sviluppo continuo professionale, attraverso l aggiornamento degli strumenti operativi attualmente in uso in Terapia Intensiva. Il corso
DECRETI E DELIBERE DI ALTRE AUTORITÀ
 DECRETI E DELIBERE DI ALTRE AUTORITÀ AGENZIA ITALIANA DEL FARMACO DETERMINA 19 giugno 2015. Determina inerente i requisiti minimi necessari per le strutture sanitarie, che eseguono sperimentazioni di fase
DECRETI E DELIBERE DI ALTRE AUTORITÀ AGENZIA ITALIANA DEL FARMACO DETERMINA 19 giugno 2015. Determina inerente i requisiti minimi necessari per le strutture sanitarie, che eseguono sperimentazioni di fase
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere
 Sperimentazione Clinica: ruolo e responsabilità dell Infermiere I diversi ruoli e responsabilità nella ricerca clinica Sergio Scaccabarozzi, Head of Clinical Operations-Roche S.p.A. Davide Ausili, RN,MSN,PhD.
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere I diversi ruoli e responsabilità nella ricerca clinica Sergio Scaccabarozzi, Head of Clinical Operations-Roche S.p.A. Davide Ausili, RN,MSN,PhD.
Studi FARMACOLOGICI PROFIT
 CEI FONDAZIONE PTV POLICLINICO TOR VERGATA SOP Procedure Operative Standard U.O.C. Farmacia clinica Studi FARMACOLOGICI PROFIT COMPILARE E ALLEGARE ALLA DOCUMENTAZIONE DELLO STUDIO L APPENDICE 2 ALLA DOMANDA
CEI FONDAZIONE PTV POLICLINICO TOR VERGATA SOP Procedure Operative Standard U.O.C. Farmacia clinica Studi FARMACOLOGICI PROFIT COMPILARE E ALLEGARE ALLA DOCUMENTAZIONE DELLO STUDIO L APPENDICE 2 ALLA DOMANDA
Il Nuovo Regolamento Aziendale per. sperimentazioni. Collegio di Direzione Board Aziendale Ricerca e Innovazione 22 maggio 2013
 Il Nuovo Regolamento Aziendale per la conduzione di ricerche e sperimentazioni Collegio di Direzione Board Aziendale Ricerca e Innovazione 22 maggio 2013 DGR 1066/2009 Le funzioni della Ricerca Esplorativa/conoscitiva
Il Nuovo Regolamento Aziendale per la conduzione di ricerche e sperimentazioni Collegio di Direzione Board Aziendale Ricerca e Innovazione 22 maggio 2013 DGR 1066/2009 Le funzioni della Ricerca Esplorativa/conoscitiva
Richiesta di parere in ordine all autorizzazione di sperimentazione interventistica
 PROCEDURE PER PRESENTARE UNA RICHIESTA DI PARERE alla Segreteria STS del CE INRCA La documentazione di cui si richiede la valutazione al CE INRCA deve essere presentata tramite l'invio: 1. del CD-ROM o
PROCEDURE PER PRESENTARE UNA RICHIESTA DI PARERE alla Segreteria STS del CE INRCA La documentazione di cui si richiede la valutazione al CE INRCA deve essere presentata tramite l'invio: 1. del CD-ROM o
AVVISO PUBBLICO N. 12
 Servizio Sanitario Nazionale - Regione Veneto AZIENDA ULSS N. 8 BERICA Viale F. Rodolfi n. 37 36100 VICENZA COD.FISC. E P.IVA 02441500242 Cod. ipa AUV Tel. 0444 753111 - Fax 0444 753809 Mail protocollo@aulss8.veneto.it
Servizio Sanitario Nazionale - Regione Veneto AZIENDA ULSS N. 8 BERICA Viale F. Rodolfi n. 37 36100 VICENZA COD.FISC. E P.IVA 02441500242 Cod. ipa AUV Tel. 0444 753111 - Fax 0444 753809 Mail protocollo@aulss8.veneto.it
Telefono Fax
 INFORMAZIONI PERSONALI Nome Indirizzo STELLA ROBERTO VIA CASTIGLIONI, 10 21052 BUSTO ARSIZIO VARESE (ITALIA) Telefono +390331321870 - +393318829418 Fax +390331630763 E-mail stellart@tin.it; roberto.stella@snamid.it
INFORMAZIONI PERSONALI Nome Indirizzo STELLA ROBERTO VIA CASTIGLIONI, 10 21052 BUSTO ARSIZIO VARESE (ITALIA) Telefono +390331321870 - +393318829418 Fax +390331630763 E-mail stellart@tin.it; roberto.stella@snamid.it
La nuova legislazione sulla Farmacovigilanza. Il sistema di qualità di farmacovigilanza in AIFA. Pietro Erba. Roma, 13 settembre 2012
 La nuova legislazione sulla Farmacovigilanza Il sistema di qualità di farmacovigilanza in AIFA Pietro Erba Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa
La nuova legislazione sulla Farmacovigilanza Il sistema di qualità di farmacovigilanza in AIFA Pietro Erba Roma, 13 settembre 2012 Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa
Strumenti di consultazione, reportistica e messaggistica automatica
 Corso sull Osservatorio Nazionale sulla Sperimentazione Clinica dei Medicinali (OsSC) rivolto ai Comitati Etici Febbraio 2009 Strumenti di consultazione, reportistica e messaggistica automatica Alice Ramenghi
Corso sull Osservatorio Nazionale sulla Sperimentazione Clinica dei Medicinali (OsSC) rivolto ai Comitati Etici Febbraio 2009 Strumenti di consultazione, reportistica e messaggistica automatica Alice Ramenghi
IL DIRETTORE GENERALE Dr. Pierluigi Tosi
 IL DIRETTORE GENERALE Dr. Pierluigi Tosi coadiuvato dal: - Direttore Amministrativo Dr. Giacomo Centini - Direttore Sanitario Dr.ssa Silvia Briani Richiamato l art. 3 del D. Lgs. del 30 dicembre 1992,
IL DIRETTORE GENERALE Dr. Pierluigi Tosi coadiuvato dal: - Direttore Amministrativo Dr. Giacomo Centini - Direttore Sanitario Dr.ssa Silvia Briani Richiamato l art. 3 del D. Lgs. del 30 dicembre 1992,
La nuova legislazione sulla Farmacovigilanza
 La nuova legislazione sulla Farmacovigilanza Responsabilità e compiti dell Azienda Farmaceutica Alessandra Del Porto MSD Italia S.r.l., GdL Farmacovigilanza Farmindustria Auditorium Confindustria Roma,
La nuova legislazione sulla Farmacovigilanza Responsabilità e compiti dell Azienda Farmaceutica Alessandra Del Porto MSD Italia S.r.l., GdL Farmacovigilanza Farmindustria Auditorium Confindustria Roma,
Attività sanitarie di medicina specialistica e diagnostica svolte in mezzi mobili
 Allegato n. 2 alla Delib.G.R. n. 23/7 del 29.5.2012 Attività sanitarie di medicina specialistica e diagnostica svolte in mezzi mobili I mezzi mobili sono strutture sanitarie costituite da automezzi dove
Allegato n. 2 alla Delib.G.R. n. 23/7 del 29.5.2012 Attività sanitarie di medicina specialistica e diagnostica svolte in mezzi mobili I mezzi mobili sono strutture sanitarie costituite da automezzi dove
UN ESEMPIO DI GESTIONE INTEGRATA OSPEDALE TERRITORIO. Piero Luigi GIULIANO
 GLI ACCESSI VENOSI: COME MIGLIORARNE LA GESTIONE COINVOLGENDO I SERVIZI TERRITORIALI TORINO 17 OTTOBRE 2018 UN ESEMPIO DI GESTIONE INTEGRATA OSPEDALE TERRITORIO Piero Luigi GIULIANO keyword Rete oncologica
GLI ACCESSI VENOSI: COME MIGLIORARNE LA GESTIONE COINVOLGENDO I SERVIZI TERRITORIALI TORINO 17 OTTOBRE 2018 UN ESEMPIO DI GESTIONE INTEGRATA OSPEDALE TERRITORIO Piero Luigi GIULIANO keyword Rete oncologica
ASSESSORATO DELL IGIENE E SANITA E DELL ASSISTENZA SOCIALE
 L osservazione Breve Intensiva (OBI) è uno strumento per l osservazione e la gestione clinica temporanea in regime di non ricovero la cui durata è limitata a 24 ore. Nell ambito di tale attività possono
L osservazione Breve Intensiva (OBI) è uno strumento per l osservazione e la gestione clinica temporanea in regime di non ricovero la cui durata è limitata a 24 ore. Nell ambito di tale attività possono
Prima Giornata Nazionale sulla Macrodattilia. La ricerca clinica e le malattie rare
 Prima Giornata Nazionale sulla Macrodattilia La ricerca clinica e le malattie rare Lorenzo Cottini President- General Manager HIGH RESEARCH srl AFI (Associazione Farmaceutici dell Industria) Monza, 16
Prima Giornata Nazionale sulla Macrodattilia La ricerca clinica e le malattie rare Lorenzo Cottini President- General Manager HIGH RESEARCH srl AFI (Associazione Farmaceutici dell Industria) Monza, 16
RESPONSABILITA DELL ESPERTO IN AFFARI REGOLATORI TITOLARI AIC (MAH) OFFICINA DI PRODOTTO FINITO OFFICINA DI API
 REGOLATORI TITOLARI AIC (MAH) OFFICINA DI PRODOTTO FINITO OFFICINA DI API REGOLATORI: TITOLARI A.I.C. (MAH); OFFICINA PRODOTTO FINITO E API In considerazione del continuo evolvere del panorama normativo,
REGOLATORI TITOLARI AIC (MAH) OFFICINA DI PRODOTTO FINITO OFFICINA DI API REGOLATORI: TITOLARI A.I.C. (MAH); OFFICINA PRODOTTO FINITO E API In considerazione del continuo evolvere del panorama normativo,
Rapporto. Ispezioni GCP Classificazione e analisi delle deviazioni alla Good Clinical Practice AGENZIA ITALIANA DEL FARMACO
 Rapporto Ispezioni GCP 2015-2017 Classificazione e analisi delle deviazioni alla Good Clinical Practice AGENZIA ITALIANA DEL FARMACO Citare il presente Rapporto come segue: Rapporto Ispezioni GCP 2015-2017.
Rapporto Ispezioni GCP 2015-2017 Classificazione e analisi delle deviazioni alla Good Clinical Practice AGENZIA ITALIANA DEL FARMACO Citare il presente Rapporto come segue: Rapporto Ispezioni GCP 2015-2017.
Il ruolo delle reti in tema di APPROPRIATEZZA E QUALITA
 Il ruolo delle reti in tema di APPROPRIATEZZA E QUALITA Gianmauro Numico ASO SS Antonio e Biagio e C. Arrigo, Alessandria Rete Oncologica del Piemonte e della Valle d Aosta Gli snodi clinico-organizzativi
Il ruolo delle reti in tema di APPROPRIATEZZA E QUALITA Gianmauro Numico ASO SS Antonio e Biagio e C. Arrigo, Alessandria Rete Oncologica del Piemonte e della Valle d Aosta Gli snodi clinico-organizzativi
Prevenzione degli errori in terapia con farmaci antineoplastici
 Fornitura braccialetti (pdf - 720 KB) Gestione penne contenenti insulina (pdf - 292 KB) Prevenzione degli errori in terapia con farmaci antineoplastici Raccomandazione ministeriale n. 14 per la prevenzione
Fornitura braccialetti (pdf - 720 KB) Gestione penne contenenti insulina (pdf - 292 KB) Prevenzione degli errori in terapia con farmaci antineoplastici Raccomandazione ministeriale n. 14 per la prevenzione
Medico di Medicina Generale Convenzionato con il SSN Gestione di 1500 pazienti di varie classi ed età
 INFORMAZIONI PERSONALI Nome Indirizzo STELLA ROBERTO VIA CASTIGLIONI,10 21052 BUSTO ARSIZIO VARESE (ITALIA) Telefono +390331321870 - +393387058653 Fax +390331630763 E-mail stellart@tin.it; stella@snamid.org
INFORMAZIONI PERSONALI Nome Indirizzo STELLA ROBERTO VIA CASTIGLIONI,10 21052 BUSTO ARSIZIO VARESE (ITALIA) Telefono +390331321870 - +393387058653 Fax +390331630763 E-mail stellart@tin.it; stella@snamid.org
CONFERIMENTO INCARICO DIRETTORE DI STRUTTURA COMPLESSA - SCIENZA DELL ALIMENTAZIONE E DIETETICA - CURRICULA CANDIDATI AMMESSI
 Dott. Mauro BRUGNANI CONFERIMENTO INCARICO DIRETTORE DI STRUTTURA COMPLESSA - SCIENZA DELL ALIMENTAZIONE E DIETETICA - CURRICULA CANDIDATI AMMESSI TITOLI DI AMMISSIONE - Laurea in Medicina e Chirurgia
Dott. Mauro BRUGNANI CONFERIMENTO INCARICO DIRETTORE DI STRUTTURA COMPLESSA - SCIENZA DELL ALIMENTAZIONE E DIETETICA - CURRICULA CANDIDATI AMMESSI TITOLI DI AMMISSIONE - Laurea in Medicina e Chirurgia
Curriculum Vitae Europass
 Curriculum Vitae Europass Informazioni personali Nome / Cognome Indirizzo Luigi Seghezzi Via Campagna 10, 21041 Albizzate (VA) Telefono +39 0331.992026 Cellulare: +39 328.2026743 E-mail luigi.seghezzi@aogallarate.it
Curriculum Vitae Europass Informazioni personali Nome / Cognome Indirizzo Luigi Seghezzi Via Campagna 10, 21041 Albizzate (VA) Telefono +39 0331.992026 Cellulare: +39 328.2026743 E-mail luigi.seghezzi@aogallarate.it
La Scuola di Specialità in Medicina di Emergenza e Urgenza
 Convegno: "Dipartimento Emergenza Oggi e Domani" La Scuola di Specialità in Medicina di Emergenza e Urgenza Nicola Montano Dipartimento di Scienze Cliniche Ospedale Luigi Sacco Universita degli Studi di
Convegno: "Dipartimento Emergenza Oggi e Domani" La Scuola di Specialità in Medicina di Emergenza e Urgenza Nicola Montano Dipartimento di Scienze Cliniche Ospedale Luigi Sacco Universita degli Studi di
F O R M A T O E U R O P E O
 F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome COSTA DANIELA Indirizzo 6/E VIA OSVALDO REMOTTI SAN MICHELE, 15121 ALESSANDRIA Telefono 0131-207329 cell.338-9904335
F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome COSTA DANIELA Indirizzo 6/E VIA OSVALDO REMOTTI SAN MICHELE, 15121 ALESSANDRIA Telefono 0131-207329 cell.338-9904335
Centro Accoglienza e Servizi: ruolo di regia nel percorso di cura
 Centro Accoglienza e Servizi: ruolo di regia nel percorso di cura Gianmauro Numico AO SS Antonio e Biagio e C Arrigo Alessandria gianmauro.numico@ospedale.al.it Come accedono i pazienti in ospedale? In
Centro Accoglienza e Servizi: ruolo di regia nel percorso di cura Gianmauro Numico AO SS Antonio e Biagio e C Arrigo Alessandria gianmauro.numico@ospedale.al.it Come accedono i pazienti in ospedale? In
CURRICULUM FORMATIVO E PROFESSIONALE DEL DR. CARLO FINELLI
 1 CURRICULUM FORMATIVO E PROFESSIONALE DEL DR. CARLO FINELLI 2 DATI ANAGRAFICI - Nato il 7/7/1954 a Bologna - Diploma di Maturità Classica presso il Liceo Statale "Marco Minghetti" di Bologna nel 1973
1 CURRICULUM FORMATIVO E PROFESSIONALE DEL DR. CARLO FINELLI 2 DATI ANAGRAFICI - Nato il 7/7/1954 a Bologna - Diploma di Maturità Classica presso il Liceo Statale "Marco Minghetti" di Bologna nel 1973
ASSESSORATO DELL IGIENE E SANITA E DELL ASSISTENZA SOCIALE
 La terapia semi-intensiva riguarda pazienti per lo più con insufficienza multiorgano che necessitano di una intensità di interventi ad alta tecnologia e nursing minori alla terapia intensiva (400 minutia
La terapia semi-intensiva riguarda pazienti per lo più con insufficienza multiorgano che necessitano di una intensità di interventi ad alta tecnologia e nursing minori alla terapia intensiva (400 minutia
Profilo Professionale
 Profilo Professionale Addetto al Controllo del Sistema Qualità Roma 02 Marzo 2016 Organizzazione Sviluppo Risorse Umane e Qualità Certificata ISO 9001:2008 Certificata OHSAS 18001:2007 Finalità L addetto
Profilo Professionale Addetto al Controllo del Sistema Qualità Roma 02 Marzo 2016 Organizzazione Sviluppo Risorse Umane e Qualità Certificata ISO 9001:2008 Certificata OHSAS 18001:2007 Finalità L addetto
AMBULATORIO DI ENDOSCOPIA 1) ENDOSCOPIA DI 1 LIVELLO
 L attività di Endoscopia è una procedura invasiva basata sull introduzione di un mezzo ottico, rigido o flessibile, nelle cavità naturali a scopo diagnostico e terapeutico. Nella gestione del processo
L attività di Endoscopia è una procedura invasiva basata sull introduzione di un mezzo ottico, rigido o flessibile, nelle cavità naturali a scopo diagnostico e terapeutico. Nella gestione del processo
Gestione POCT: punto di vista del laboratorio
 Gestione POCT: punto di vista del laboratorio Roma 03 Ottobre 2009 Dr. Paolo Casalino POCT dosaggio eseguito al letto del paziente o vicino al luogo di degenza il cui esito porti alla possibilità di incidere
Gestione POCT: punto di vista del laboratorio Roma 03 Ottobre 2009 Dr. Paolo Casalino POCT dosaggio eseguito al letto del paziente o vicino al luogo di degenza il cui esito porti alla possibilità di incidere
AREA C: SISTEMI INTEGRATI
 AREA C: SISTEMI INTEGRATI Codice Titolo Ore C01 Formazione in merito al Sistema di Gestione per la Qualità UNI EN 28 ISO 9001 C02 Internal Auditing secondo la linea guida UNI EN ISO 19011:2012 28 C03 Formazione
AREA C: SISTEMI INTEGRATI Codice Titolo Ore C01 Formazione in merito al Sistema di Gestione per la Qualità UNI EN 28 ISO 9001 C02 Internal Auditing secondo la linea guida UNI EN ISO 19011:2012 28 C03 Formazione
Ospedale di Treviso. Medicina di Laboratorio Guida ai Servizi
 Ospedale di Treviso Medicina di Laboratorio Guida ai Servizi L Unità Operativa Complessa Medicina di Laboratorio è un struttura del Dipartimento di Patologia Clinica dell Azienda ULSS 9 di Treviso. Essa
Ospedale di Treviso Medicina di Laboratorio Guida ai Servizi L Unità Operativa Complessa Medicina di Laboratorio è un struttura del Dipartimento di Patologia Clinica dell Azienda ULSS 9 di Treviso. Essa
Gara per la fornitura del Servizio di Ristorazione per la Mensa Obbligatoria di Servizio per il personale di Polizia Penitenziaria
 ALLEGATO 6 AL CAPITOLATO MONITORAGGIO ISPETTIVO ED ANALITICO Allegato 6- Monitoraggio ispettivo ed analitico Pagina 1 di 5 SOMMARIO 1. Oggetto delle attività di monitoraggio... 3 2. Soggetti coinvolti
ALLEGATO 6 AL CAPITOLATO MONITORAGGIO ISPETTIVO ED ANALITICO Allegato 6- Monitoraggio ispettivo ed analitico Pagina 1 di 5 SOMMARIO 1. Oggetto delle attività di monitoraggio... 3 2. Soggetti coinvolti
Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di MEDICINA NUCLEARE (Lista di controllo n. 4.
 Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di MEDICINA NUCLEARE
Da allegare alla domanda di autorizzazione all esercizio di attività sanitaria e/o socio-sanitaria Dichiarazione del possesso dei requisiti minimi previsti per l esercizio di attività di MEDICINA NUCLEARE
La gestione del campione di farmaco sperimentale. Dr.ssa Elvia Malo Servizio di Farmacia Nucleo per la Ricerca Clinica
 La gestione del campione di farmaco sperimentale Dr.ssa Elvia Malo Servizio di Farmacia Nucleo per la Ricerca Clinica Negrar, 21/10/2016 Il Medicinale sperimentale Una forma farmaceutica di un principio
La gestione del campione di farmaco sperimentale Dr.ssa Elvia Malo Servizio di Farmacia Nucleo per la Ricerca Clinica Negrar, 21/10/2016 Il Medicinale sperimentale Una forma farmaceutica di un principio
AMBULATORIO DI ENDOSCOPIA 1) ENDOSCOPIA DI 1 LIVELLO
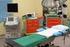 L attività di Endoscopia è una procedura invasiva basata sull introduzione di un mezzo ottico, rigido o flessibile, nelle cavità naturali a scopo diagnostico e terapeutico. Nella gestione del processo
L attività di Endoscopia è una procedura invasiva basata sull introduzione di un mezzo ottico, rigido o flessibile, nelle cavità naturali a scopo diagnostico e terapeutico. Nella gestione del processo
IL RUOLO DEL DATA MANAGER
 Bergamo, 10 giugno 2014 La proposta di regolamento europeo sulle sperimentazioni cliniche. Nuove opportunità per i pazienti e per la ricerca IL RUOLO DEL DATA MANAGER Dr Maria Luisa Ferrari Ematologia
Bergamo, 10 giugno 2014 La proposta di regolamento europeo sulle sperimentazioni cliniche. Nuove opportunità per i pazienti e per la ricerca IL RUOLO DEL DATA MANAGER Dr Maria Luisa Ferrari Ematologia
ASSESSORATO DELL IGIENE E SANITA E DELL ASSISTENZA SOCIALE REQUISITI SPECIFICI. AREA EMERGENZA URGENZA: Osservazione Breve Intensiva
 L osservazione Breve Intensiva (OBI) è uno strumento per l osservazione e la gestione clinica temporanea in regime di non ricovero la cui durata è limitata a 24 ore. Nell ambito di tale attività possono
L osservazione Breve Intensiva (OBI) è uno strumento per l osservazione e la gestione clinica temporanea in regime di non ricovero la cui durata è limitata a 24 ore. Nell ambito di tale attività possono
I CONVEGNO PER INFERMIERI IN ONCOLOGIA Ospedale di S. Polo Monfalcone 20 Novembre La ricerca: Come, dove, quando?
 I CONVEGNO PER INFERMIERI IN ONCOLOGIA Ospedale di S. Polo Monfalcone 20 Novembre 2004 La ricerca: Come, dove, quando? Daniela Grosso, UO di Oncologia Medica, Azienda Ospedaliera di Padova L ASSISTENZA
I CONVEGNO PER INFERMIERI IN ONCOLOGIA Ospedale di S. Polo Monfalcone 20 Novembre 2004 La ricerca: Come, dove, quando? Daniela Grosso, UO di Oncologia Medica, Azienda Ospedaliera di Padova L ASSISTENZA
Triage-linee guida. Obiettivi formativi ECM e acquisizioni di competenze
 Direzione Sanitaria Ufficio Formazione (Provider Regionale n. 2) Dirigente: Dott. Paolo Moscara Programma del Corso ECM: R4076. Galatina - P.O. Ore Corso ai fini ECM 5.30 2 Cred. ECM 5,6 2 Giorno da ore
Direzione Sanitaria Ufficio Formazione (Provider Regionale n. 2) Dirigente: Dott. Paolo Moscara Programma del Corso ECM: R4076. Galatina - P.O. Ore Corso ai fini ECM 5.30 2 Cred. ECM 5,6 2 Giorno da ore
REGIONE VENETO / Segreteria regionale Sanità e Sociale- ARSS Agenzia Regionale Sanitaria e Sociosanitaria
 Lista di verifica REQUITI MINIMI SPECIFICI E DI QUALITA' PER L'AUTORIZZAZIONE RIANIMAZIONE E TERAPIA INTENVA 1 RIANIMAZIONE E TERAPIA INTENVA - REQUITI STRUTTURALI RIAN01.AU.1.1 I locali e gli spazi sono
Lista di verifica REQUITI MINIMI SPECIFICI E DI QUALITA' PER L'AUTORIZZAZIONE RIANIMAZIONE E TERAPIA INTENVA 1 RIANIMAZIONE E TERAPIA INTENVA - REQUITI STRUTTURALI RIAN01.AU.1.1 I locali e gli spazi sono
Luogo di nascita: Zafferana Etnea (CT) Residenza: Vittorio Emanuele 144 Zafferana Etnea CAP 95019
 F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E Carmelo Russo INFORMAZIONI PERSONALI Stato civile: coniugato Nazionalità: italiana Data di nascita: 25/04/1960 Luogo di nascita: Zafferana
F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E Carmelo Russo INFORMAZIONI PERSONALI Stato civile: coniugato Nazionalità: italiana Data di nascita: 25/04/1960 Luogo di nascita: Zafferana
Sperimentazione clinica controllata in medicina generale ed in pediatria di libera scelta. IL MINISTRO DELLA SANITA
 Direzione generale per la valutazione dei medicinali e la farmacovigilanza Ufficio Sperimentazione Clinica dei Medicinali ed Uso Speciale di Farmaci non Autorizzati Decreto Ministeriale 10 maggio 2001
Direzione generale per la valutazione dei medicinali e la farmacovigilanza Ufficio Sperimentazione Clinica dei Medicinali ed Uso Speciale di Farmaci non Autorizzati Decreto Ministeriale 10 maggio 2001
F O R M A T O E U R O P E O
 F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome CASTELLI FRANCESCO Indirizzo VIA LUSIGNANI, 30-16138 GENOVA Telefono +39 010 8355486; +39 010 5553188 Fax
F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome CASTELLI FRANCESCO Indirizzo VIA LUSIGNANI, 30-16138 GENOVA Telefono +39 010 8355486; +39 010 5553188 Fax
Curriculum Vitae di LUCA GIUDITTA
 Curriculum Vitae di LUCA GIUDITTA DATI PERSONALI nato a ROMA il 22-08-1961 Profilo breve Medico presso l' Ospedale di Rovereto, svolge attività di assistenza e di guardia attiva presso la Unità Operativa
Curriculum Vitae di LUCA GIUDITTA DATI PERSONALI nato a ROMA il 22-08-1961 Profilo breve Medico presso l' Ospedale di Rovereto, svolge attività di assistenza e di guardia attiva presso la Unità Operativa
CARTA INTESTATA DEL CENTRO
 CARTA INTESTATA DEL CENTRO Sede, Data Al Comitato Etico Unico Regionale Del Friuli Venezia Giulia c/o Direzione Scientifica CRO Aviano Alla Direzione Generale Azienda (DA COMPLETARE) OGGETTO: Dichiarazione
CARTA INTESTATA DEL CENTRO Sede, Data Al Comitato Etico Unico Regionale Del Friuli Venezia Giulia c/o Direzione Scientifica CRO Aviano Alla Direzione Generale Azienda (DA COMPLETARE) OGGETTO: Dichiarazione
CURRICULUM VITAE INFORMAZIONI PERSONALE. Favale Alessandra Via Pacchiotti Torino. Nome Indirizzo. Stato Civile. Nubile
 CURRICULUM VITAE INFORMAZIONI PERSONALE Nome Indirizzo Stato Civile Favale Alessandra Via Pacchiotti 12 10146 Torino Nubile Telefono 3928279093 oppure 0117743329 E-mail alessandra.favale@libero.it Nazionalità
CURRICULUM VITAE INFORMAZIONI PERSONALE Nome Indirizzo Stato Civile Favale Alessandra Via Pacchiotti 12 10146 Torino Nubile Telefono 3928279093 oppure 0117743329 E-mail alessandra.favale@libero.it Nazionalità
Prospettive occupazionali dei laureati in Scienze del Farmaco Il Manufacturing Farmaceutico
 Prospettive occupazionali dei laureati in Scienze del Farmaco Il Manufacturing Farmaceutico Alessandro Regola Quality Unit Bayer HealthCare Manufacturing Garbagnate /////////// & Segrate, Italy Università
Prospettive occupazionali dei laureati in Scienze del Farmaco Il Manufacturing Farmaceutico Alessandro Regola Quality Unit Bayer HealthCare Manufacturing Garbagnate /////////// & Segrate, Italy Università
Corsi di formazione ed aggiornamento professionale
 Fabiana Carmen Rollo Istruzione Diploma conseguito nel 2007 presso il Liceo Scientifico Giordano Bruno di Torino (progetto brocca maxi linguistico) specializzazione in lingua inglese, francese e tedesca,
Fabiana Carmen Rollo Istruzione Diploma conseguito nel 2007 presso il Liceo Scientifico Giordano Bruno di Torino (progetto brocca maxi linguistico) specializzazione in lingua inglese, francese e tedesca,
INFORMAZIONI. Nome SILVIA SANTORO Indirizzo VIA PANORAMICA DELLO STRETTO MESSINA Telefono Fax
 F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome SILVIA SANTORO Indirizzo VIA PANORAMICA DELLO STRETTO 480 98168 MESSINA Telefono 3489201644 Fax E-mail silvia904@virgilio.it
F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome SILVIA SANTORO Indirizzo VIA PANORAMICA DELLO STRETTO 480 98168 MESSINA Telefono 3489201644 Fax E-mail silvia904@virgilio.it
CARTA INTESTATA DEL CENTRO
 CARTA INTESTATA DEL CENTRO Sede, Data Al Comitato Etico Unico Regionale del Friuli Venezia Giulia c/o Irccs Centro di Riferimento Oncologico via Franco Gallini, 2-33081 Aviano (PN) Alla Direzione Generale
CARTA INTESTATA DEL CENTRO Sede, Data Al Comitato Etico Unico Regionale del Friuli Venezia Giulia c/o Irccs Centro di Riferimento Oncologico via Franco Gallini, 2-33081 Aviano (PN) Alla Direzione Generale
Il clinical trial center dell A.R.N.A.S. Garibaldi il percorso farmaceutico.
 Il clinical trial center dell A.R.N.A.S. Garibaldi il percorso farmaceutico. Giuseppina Emanuela Fassari Responsabile Unità Farmaci Antitumorali ARNAS Garibaldi di Catania Partecipa al Comitato Etico Partecipa
Il clinical trial center dell A.R.N.A.S. Garibaldi il percorso farmaceutico. Giuseppina Emanuela Fassari Responsabile Unità Farmaci Antitumorali ARNAS Garibaldi di Catania Partecipa al Comitato Etico Partecipa
Capo 48. Scuola di specializzazione in farmacologia. Art. 48.1
 Capo 48 Scuola di specializzazione in farmacologia Art. 48.1 E' istituita la scuola di specializzazione in farmacologia presso l'università degli studi di Napoli, afferente alla facoltà di medicina e chirurgia.
Capo 48 Scuola di specializzazione in farmacologia Art. 48.1 E' istituita la scuola di specializzazione in farmacologia presso l'università degli studi di Napoli, afferente alla facoltà di medicina e chirurgia.
MATERIALI E DOTAZIONI
 Pagina 1 di 5 MATERIALI E DOTAZIONI Rev. Data Redazione Verificato Approvato 0 15/03/2012 Resp. Protocolli - S. Dami Coord inf. - S. Brogini UO Assicurazione Qualità Coord. Inf. R. Montalbano Resp. DEU
Pagina 1 di 5 MATERIALI E DOTAZIONI Rev. Data Redazione Verificato Approvato 0 15/03/2012 Resp. Protocolli - S. Dami Coord inf. - S. Brogini UO Assicurazione Qualità Coord. Inf. R. Montalbano Resp. DEU
A relazione dell'assessore Monferino:
 REGIONE PIEMONTE BU45 08/11/2012 Deliberazione della Giunta Regionale 15 ottobre 2012, n. 41-4751 Controllo sugli atti delle AA.SS.RR.- l.r. 31/92 s.m.i. - DGR 18-23906 del 2.2.1998. Sessione istruttoria
REGIONE PIEMONTE BU45 08/11/2012 Deliberazione della Giunta Regionale 15 ottobre 2012, n. 41-4751 Controllo sugli atti delle AA.SS.RR.- l.r. 31/92 s.m.i. - DGR 18-23906 del 2.2.1998. Sessione istruttoria
Curriculum Vitae di GIOVANNI LUCA SEMERARO
 Curriculum Vitae di GIOVANNI LUCA SEMERARO DATI PERSONALI nato a TARANTO il 22-03-1957 Profilo breve Dirigente medico di area di Medicina e Chirurgia di Accettazione e di Urgenza con incarico professionale
Curriculum Vitae di GIOVANNI LUCA SEMERARO DATI PERSONALI nato a TARANTO il 22-03-1957 Profilo breve Dirigente medico di area di Medicina e Chirurgia di Accettazione e di Urgenza con incarico professionale
Claudia Runci. Supporto alla Didattica per il C.d.L. in Infermieristica Pediatrica
 INFORMAZIONI PERSONALI Claudia Runci ESPERIENZA PROFESSIONALE Settembre 2015 marzo 2016 informazioni docenti e studenti; pianificazione tirocini; certificati per docenti e studenti; consegna divise per
INFORMAZIONI PERSONALI Claudia Runci ESPERIENZA PROFESSIONALE Settembre 2015 marzo 2016 informazioni docenti e studenti; pianificazione tirocini; certificati per docenti e studenti; consegna divise per
REQUISITI SPECIFICI DI AUTORIZZAZIONE E ACCREDITAMENTO AMBULATORIO CHIRURGICO
 Per ambulatorio chirurgico (o ambulatorio per interventi chirurgici) si intende la struttura intra o extra-ospedaliera nella quale sono eseguiti interventi chirurgici o anche procedure diagnostiche o terapeutiche
Per ambulatorio chirurgico (o ambulatorio per interventi chirurgici) si intende la struttura intra o extra-ospedaliera nella quale sono eseguiti interventi chirurgici o anche procedure diagnostiche o terapeutiche
Incontro regionale "Sperimentazione Clinica di Fase I"
 Incontro regionale "Sperimentazione Clinica di Fase I" 23 maggio 2016 Studi di fase I nei centri di oncologia Dott. Gian luca De Salvo, Istituto Oncologico Veneto, IRCCS Servizio Sperimentazioni Cliniche
Incontro regionale "Sperimentazione Clinica di Fase I" 23 maggio 2016 Studi di fase I nei centri di oncologia Dott. Gian luca De Salvo, Istituto Oncologico Veneto, IRCCS Servizio Sperimentazioni Cliniche
Ospedale Ca Foncello di Treviso. Oncologia Guida ai Servizi
 Ospedale Ca Foncello di Treviso Oncologia Guida ai Servizi RICOVERO Il giorno del ricovero il paziente deve presentarsi alle ore 7.30, a digiuno, per eseguire i prelievi ematochimici e deve portare con
Ospedale Ca Foncello di Treviso Oncologia Guida ai Servizi RICOVERO Il giorno del ricovero il paziente deve presentarsi alle ore 7.30, a digiuno, per eseguire i prelievi ematochimici e deve portare con
DOMANDA PER L'AUTORIZZAZIONE ALLA SPERIMENTAZIONE CLINICA
 Modello 1 DOMANDA PER L'AUTORIZZAZIONE ALLA SPERIMENTAZIONE CLINICA Al Presidente del Comitato Etico dell Azienda Sanitaria Locale Viterbo via S.Lorenzo,101 VITERBO Il sottoscritto Prof./Dr. Della Unità
Modello 1 DOMANDA PER L'AUTORIZZAZIONE ALLA SPERIMENTAZIONE CLINICA Al Presidente del Comitato Etico dell Azienda Sanitaria Locale Viterbo via S.Lorenzo,101 VITERBO Il sottoscritto Prof./Dr. Della Unità
