Equilibrio acido-base
|
|
|
- Gerardo Fantoni
- 9 anni fa
- Просмотров:
Транскрипт
1 Equilibrio acidobase
2 ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = ph urina 4.5 8
3 Effetti delle alterazioni ph Alterazioni eccitabilità cellule nervose e muscolari ph depressione SNC (disorientamento e coma) ph ipereccitabilità SNP (sistemi afferenti, formicolii, sistemi efferenti, scosse muscolari, spasmi) e SNC (convulsioni) Alterazioni attività enzimatiche Alterazioni concentrazione K ph escrezione renale H secrezione K
4 Produzione H Acidi volatili ( mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili (0.2%, 210 mmol/dì): Acido solforico (metabolismo proteico: metionina, cisteina, cistina) Acido fosforico (metabolismo fosfolipidi) Acido cloridrico (conversione Cloruro di ammonio in Urea) Acido lattico Corpi chetonici (Acido acetoacetico, βidrossibutirrico, acetone) Consumo H ( 140 mmol/dì) Reazioni metaboliche Ossidazione anioni (citrato, lattato, acetato) Bilancio H (dieta mista) = 1 mmol/kg/d /Kg/dì ( 70 mmol/d /dì, adulto 70 Kg) Richiede: Tamponamento immediato Eliminazione renale
5 Dieta: Acidi grassi Aminoacidi Assunzione H CO 2, acido lattico, chetoacidi Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione: CO 2 Eliminazione H Rene: H
6 Sistemi di regolazione del ph Risposta immediata Sistemi tampone dei liquidi corporei Si combinano istantaneamente con acidi e basi per impedire variazioni consistenti del ph Risposta rapida Sistema respiratorio Viene regolata in pochi minuti la ventilazione e quindi l eliminazione di CO 2 Risposta lenta Rene Elimina gli acidi o le basi in eccesso
7 Potere tampone: Quantità (moli) di acido o base che occorre aggiungere ad 1l di soluzione tampone per variare il ph di 1 unità Equazione di HendersonHasselbalch permette di calcolare il ph di una soluzione tampone ed è descritta dalla cinetica della reazione: HA K 1 H A All equilibrio K 1 = K 2 Per la Legge dell azione delle masse: K 1 [HA] = K 2 [H ] [A ] K 1 [H ] [A ] K = 1 K 2 [HA] K 2 K [H ] [A ] = [HA] K 2 [H ] = K [A ] = K costante di equilibrio [HA] log [H ] = log K log [HA] [A ] ph = pk log [A ] [HA]
8 Rappresentazione grafica dell equazione equazione di HendersonHasselbalch Hasselbalch Curva di titolazione di un acido debole Aggiunta di H HA pk = 6,5 Rimozione di H A ph Quando il valore del ph è uguale al valore del pk, le concentrazioni di HA ed A sono uguali. Il sistema tampone è più efficiente nella parte centrale della curva (entro oscillazioni di 1 unità di ph in più o in meno del valore di pk) Il tampone è efficace se: il suo pk è vicino al ph desiderato è presente in elevate concentrazioni
9 Sistema tampone del Bicarbonato E formato dalla coppia tampone HCO 3 /H 2 CO 3 Quando viene aggiunto un acido forte come HCl, l H liberato viene tamponato da HCO 3 con formazione di H 2 CO 3 secondo la reazione: K1 K2 H HCO 3 H 2 CO 3 H 2 O CO 2 Quando viene aggiunta una base forte, come NaOH, l OH liberato si combina con H 2 CO 3 formando HCO 3. La concentrazione di H 2 CO 3 diminuisce e la reazione è spostata verso sinistra. Secondo l equazione l di HendersonHasselbalch Hasselbalch: ph = pk log [HCO 3 ] /[H 2 CO 3 ] dove H 2 CO 3 può essere sostituito da CO 2 ph = pk log [HCO 3 ] /[CO 2 ] pk = 6.1 ph = 6.1 log 24 mmol/l /1.2 mmol/l ph = 6.1 log 20 (1.3) = 7.4 [HCO 3 ] ph, equilibrio acidobase spostato verso alcalosi [CO 2 ] ph, equilibrio acidobase spostato verso acidosi
10 Punto al quale normalmente opera nell organismo questo sistema tampone Aggiunta di H % tampone sotto forma di H 2 CO 3 eco pk = 6, % tampone sotto forma di HCO 3 Aggiunta di OH ph Curva di titolazione del sistema bicarbonato Il sistema tampone non sembra essere particolarmente efficiente perché pk = 6.1 (ph sangue 7.4). La parte del tampone sotto forma di HCO 3 è 20 volte > di quella sotto forma di CO 2. Inoltre le concentrazioni di HCO 3 e CO 2 sono basse.
11 Il sistema tampone Bicarbonato è il sistema tampone extracellulare più potente dell organismo, perché è un sistema aperto, cioè un sistema nel quale i componenti possono essere regolati: CO 2 dalla respirazione e HCO 3 dal rene. ph = 6.1 log 24mmol/l /1.2mmol/l L aggiunta di 5 mmol HCl, in un sistema chiuso: ph = 6.1 log (24 5)/(1.2 5) ph = 6.1 log 19/6.5 = 6.6 L aggiunta di 5 mmol HCl, in un sistema aperto, in cui CO 2 è costantemente controllata: ph = 6.1 log 19/1.2 = 7.3
12 Sistema tampone Fosfato HPO 4 2 /H 2 PO 4 pk = 6.8 E meno efficace perché: meno concentrato (12 meq/l) la forma acida non può essere eliminata come la CO 2 E comunque essenziale per la regolazione del ph del liquido extracellulare e del liquido tubulare renale perché: il fosfato è molto concentrato nei tubuli renali il liquido tubulare ha un ph più vicino al pk del tampone Sistema tampone delle Proteine Le proteine sono i sistemi tampone più abbondanti dell organismo. La loro capacità tampone è legata all esistenza di gruppi imidazolici dell istidina (pk = ) e αaminici (pk = ). Nei globuli rossi, l emoglobina ha una funzione tampone molto importante
13 Tamponi intracellulari Il ph intracellulare (6 7.4) è leggermente inferiore a quello del LEC, ma segue, anche se lentamente, le sue variazioni, perché CO 2 diffonde nelle cellule e H entra con anioni organici e in scambio con il K. I sistemi tampone intracellulari contribuiscono ad impedire variazioni del ph del LEC, anche se agiscono lentamente. Sono rappresentati dalle proteine e dai fosfati inorganici (ATP, ADP, AMP, Glucosio1 monofosfato e 2,3DPG).
14 Il principio isoidrico: Quando varia la concentrazione di H nel LEC, cambia, contemporaneamente, l equilibrio di tutto il sistema tampone Ogni condizione che altera l equilibrio di uno dei sistemi tampone, cambia anche l equilibrio di tutti gli altri.
15 Basi tampone totali: Somma di tutti gli anioni (proteinati e bicarbonati) con effetto tampone La concentrazione totale delle basi tampone nel sangue è circa 48 mmol/l e non si modifica se varia la pco 2. Infatti, pco 2 HCO 3 ma proteinati (utilizzati in questo caso per tamponare l H ). La concentrazione totale delle basi tampone è quindi un buon indice per il riconoscimento delle alterazioni dell equilibrio acidobase dovute ad aumento o diminuzione degli acidi fissi nel sangue (acidosi nonrespiratorie) L aumento della concentrazione delle basi tampone, rispetto al normale, viene definito eccesso di basi (BE) o BE positivo. In caso di riduzione, si parla di BE negativo.
16 Gap anionico Utile nella diagnosi differenziale dell'acidosi metabolica GA = [Na ] ([Cl ] [HCO 3 ]) Range di normalità 5 11 meq/l. Riflette le cariche negative associate alle proteine plasmatiche in quanto gli altri cationi (K, Ca 2 e Mg 2 ) sono bilanciate da fosfati, solfati ed anioni organici. Gap anionico elevato: acidosi metabolica da accumulo di anioni non misurati (solfato nell'insufficienza renale, corpi chetonici nel diabete o chetoacidosi alcolica, lattato o agenti tossici esogeni come il glicole etilenico o i salicilati). Gap anionico normale: acidosi metabolica ipercloremica, perchè l'anione acido è il cloro che entra nel calcolo del gap anionico. Le perdite renali o extrarenali di HCO 3 determinano acidosi metabolica ipercloremica (senza gap anionico), poiché i meccanismi renali conservano il cloro nel tentativo di mantenere il volume del LEC. Acidosi con gap anionico normale segnalano alterazione dell'escrezione renale di H (acidosi tubulare renale: Renal Tubular Acidosis, RTA, nefropatia interstiziale).
17 Regolazione respiratoria dell equilibrio equilibrio acidobase La seconda linea di difesa dalle alterazioni dell equilibrio acidobase è costituita dal controllo polmonare della concentrazione di CO 2 pco 2 ph pco 2 ph Attraverso modificazioni della ventilazione, che regolano la pco 2 il sistema respiratorio può regolare il ph: ph ventilazione pco 2 ph vicino ai valori normali ph ventilazione pco 2 ph vicino ai valori normali
18 Rene ed equilibrio acidobase
19 Per mantenere l equilibrio l acidobase i reni devono: Eliminare con le urine ioni H in quantità equivalente a quella prodotta. Impedire la perdita con le urine di HCO 3 riassorbendolo quasi totalmente (carico filtrato: VFG x [HCO 3 ] p = 180 l/dì x 24 mmol/l = 4320 mmol/dì).
20 70 mmol/dì di H liberi in 1.5 l/dì di urina determinerebbero una [H ] nelle urine di 0.07 mol/1.5 l = M ph 1.3. Poiché il ph minimo urinario è 4 4.5, [H ] u deve essere 3 volte inferiore. Il rene abbassa la [H ] u tamponando H con tamponi presenti nel filtrato (HCO 3, HPO 4 ), o prodotti nel rene (NH 3 /NH 4 ).
21 Ioni H sono secreti a livello tubulare (4400 mmol/dì). Gran parte di H secreti (4320 mmol/dì) vengono utilizzati per il riassorbimento di HCO 3. La parte rimanente ( 80 mmol/dì) è escreta con le urine, in gran parte associata a tamponi urinari (fosfato ed ammoniaca) ed in piccola parte in forma libera.
22 Riassorbimento degli HCO mmol/dì 10% 432 mmol/dì Riassorbimento 99.99% > 4.9% 215 mmol/dì 1 mmol/dì
23 Il riassorbimento di HCO 3 filtrato dipende dalla secrezione di ioni H
24 Secrezione di H e riassorbimento di HCO 3 nel tubulo prossimale ANG, PKC PKA Cellule tubulari ANG, PKC PKA Filtrazione Sangue HCO 3 S1 S3 Na ATP K HCO 3 Na HCO 3 Cl H 2 CO 3 H 2 O CO 2 H Anidrasi carbonica (CAII) NHE3 GPI H Na Anidrasi carbonica (CAIV) HCO 3 H 2 CO 3 CO 2 H 2 O Liquido interstiziale Per ogni H secreto nel lume, un HCO 3 viene riassorbito e passa nel sangue Lume tubulare
25 volume del LEC riassorbimento HCO 3 Angiotensina II Aldosterone riassorbimento Na riassorbimento Na secrezione H Meccanismo alla base dell alcalosi da riduzione del LEC (Terapia con diuretici, vomito)
26 Il riassorbimento di HCO 3 non porta ad escrezione netta di H. La secrezione di H serve fondamentalmente ad impedire la perdita di HCO 3.
27 Il sistema tampone del fosfato Cellule tubulari Filtrazione Sangue Na ATP S1 K HCO 3 Na H NHE3 Na H HPO 4 2 HPO 4 2 S3 HCO 3 Cl H 2 CO 3 H 2 PO 4 ACII H 2 O CO 2 CO 2 NaH 2 PO 4 Liquido interstiziale Per ogni H secreto nel lume che si combina con un tampone diverso da HCO 3, un nuovo ione HCO 3 viene immesso nel sangue. Lume tubulare
28 In condizioni normali, la maggior parte del fosfato filtrato è riassorbita (cotrasporto Na /fosfato), solo 3040 mmol/dì sono utilizzabili come tampone urinario. Il cotrasporto Na /fosfato è inibito da ph luminale basso (minor riassorbimento in caso di acidosi). Il carrier Na /fosfato trasporta meglio H 2 PO 2 4 rispetto ad H 2 PO 4 (è facilitata l escrezione di H ). In condizioni di acidosi, il sistema tampone prevalente è quello dell NH 3
29 Liquido interstiziale Escrezione NH 3 nel tubulo prossimale Cellule tubulo prossimale Lume tubulare Sangue Glutamina Na ½ Glucosio GLUT ATP Na K 2HCO 3 2CO 2 Glutamina Glutaminasi NH 4 Glutamato Glutamatodeidrogenasi αchetoglutarato 2H H 2 CO 3 ACII H 2 O Per ogni molecola di glutamina metabolizzata nei tubuli prossimali 2NH 4 vengono secreti nel tubulo e 2HCO 3 di nuova formazione vengono immessi nel sangue. NH 4 2NH 4 H Glutamina 2NH 3 2NH 3 Na H 2NH 4 Cl Cl NH 4 1) Riassorbito nell ansa di Henle, in scambio con K, rientra poi nel lume del tubulo collettore come NH 3 2) Escreto con le urine
30 Escrezione NH 3 nei tubuli collettori Sangue Na CO 2 NH 3 Liquido interstiziale ATP K Cl Cellule intercalate HCO 3 ACII H 2 CO 3 H 2 O CO 2 NH 3 H H H ATP ATP Per ogni NH 4 escreto nell urina un nuovo HCO 3 viene immesso nel sangue. K Favorisce riassorbimento K in caso di ridotta assunzione NH 3 H NH 4 Cl Cl Lume tubulare
31 L acidosi stimola la sintesi della glutaminasi e quindi incrementa il metabolismo renale della glutamina Nell acidosi cronica, l escrezione di NH 4 aumenta notevolmente e diventa il meccanismo prevalente per l eliminazione dell eccesso di H.
32 Ruolo delle cellule intercalate del nefrone distale nell acidosi e nell alcalosi In caso di acidosi le cellule intercalate di tipo α secernono H e riassorbono HCO 3 (pompa ATPasi H e pompa ATPasi H /K membrana apicale) In caso di alcalosi le cellule intercalate di tipo β riassorbono H ed eliminano HCO 3 (pompa ATPasi H e pompa ATPasi H /K membrana basolaterale) L acidosi stimola l inserimento della pompa ATPasi H /K nella membrana apicale. La pompa rappresenta il punto di contatto tra H e K che può creare alterazioni nella kaliemia, parallele a quelle dell equilibrio acidobase. Acidosi associata ad iperkaliemia Alcalosi associata ad ipokaliemia
33 Trasporto attivo primario di H a livello delle cellule intercalate Acidosi: secrezione di H (5%) a livello delle cellule intercalate di tipo α Liquido interstiziale Cellule intercalate α Lume tubulare Sangue CO 2 HCO 3 K Cl ACII H 2 CO 3 H 2 O CO 2 Per ogni ione H secreto nel lume, uno ione HCO 3 viene riassorbito e passa nel sangue H H H ATP ATP Cl H H K Favorisce riassorbimento K in caso di ridotta assunzione H Escrezione nell urina Concentra ioni H fino a 900 volte e abbassa il ph fino a (minimo possibile).
34 Alcalosi: riassorbimento di H a livello delle cellule intercalate di tipo β Liquido interstiziale Cellule intercalate β Lume tubulare Cl Cl H ATP H HCO 3 H HCO 3 Sangue CO 2 ATP H K ACII H 2 CO 3 H 2 O CO 2 K Escrezione nell urina Per ogni ione H riassorbito uno ione HCO 3 viene secreto ed escreto nell urina
35 La secrezione di H è stimolata da Aldosterone: Azione diretta sulle cellule intercalate (meccanismo non ancora chiarito). Azione indiretta, associata al riassorbimento di Na a livello delle cellule principali, che aumenta il voltaggio negativo del lume, favorendo la secrezione di H da parte delle cellule intercalate. Acidosi stimola espressione ed inserimento pompa H nella membrana apicale cellule α, alcalosi ha effetto opposto.
36 Quando si ha un eccesso di HCO 3 rispetto ad H (alcalosi) gli HCO 3 in eccesso non possono essere riassorbiti e vengono escreti (compensazione dell alcalosi) Quando si ha un eccesso di H rispetto ad HCO 3 (acidosi), HCO 3 viene completamente riassorbito e gli H in eccesso passano nell urina, dove sono tamponati da fosfato ed ammoniaca ed escreti in forma di sali (compensazione dell acidosi) Nell acidosi, il metabolismo renale della glutamina (formazione di NH 3 ) è stimolato, perché aumenta la sintesi della glutaminasi Nell acidosi cronica aumenta notevolmente l escrezione di NH 4 che diventa il meccanismo prevalente per l eliminazione di acido
37 Acido netto escreto Il carico escreto di HCO 3 (U HCO3 x V) è un indice della rimozione di HCO 3 dal sangue (o della immissione di H nel sangue). La quantità di H escreta sotto forma di tamponi diversi da HCO 3 : NH 4 acidità titolabile (valutata in base alla quantità di base, NaOH, necessaria a riportare il ph a 7.4) è un indice della quantità di HCO 3 di nuova formazione. Acido netto escreto = NH 4 escreto Acido titolabile urinario HCO 3 escreto In acidosi si ha aggiunta netta di HCO 3 NH 4 ed acidi titolabili nelle urine al sangue ed aumento di In alcalosi l escrezione urinaria di NH 4 ed acidi titolabili scende a 0, mentre aumenta l escrezione di HCO 3
38 I reni ripristinano l equilibrio l acidobase in condizioni di alterazione attraverso: Riassorbimento di tutto l HCO 3 filtrato (acidosi) o di quantità minori di HCO 3 filtrato (alcalosi) Secrezione di quantità maggiori (acidosi) o minori (alcalosi) di H Produzione di nuovi HCO 3 (acidosi)
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
ph = log 1/[H + ] = log [H + ]
![ph = log 1/[H + ] = log [H + ] ph = log 1/[H + ] = log [H + ]](/thumbs/49/24977942.jpg) ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio
 Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra ). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE
 LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE 1 ALDOSTERONE Ormone steroideo rilasciato dalla corticale surrenale l aldosterone stimola: riassorbimento di Na +
LEZIONE 29: REGOLAZIONE NEUROORMONALE MECCANISMI NEUROORMONALI DI REGOLAZIONE DEL RENE 1 ALDOSTERONE Ormone steroideo rilasciato dalla corticale surrenale l aldosterone stimola: riassorbimento di Na +
Escrezione renale di Na + e sua regolazione
 Escrezione renale di e sua regolazione L escrezione di dipende dal carico filtrato (e quindi dalla VFG) e dal carico riassorbito Il riassorbimento di avviene in tutti i segmenti del nefrone e nel nefrone
Escrezione renale di e sua regolazione L escrezione di dipende dal carico filtrato (e quindi dalla VFG) e dal carico riassorbito Il riassorbimento di avviene in tutti i segmenti del nefrone e nel nefrone
Rene ed equilibrio acido base. La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica. Principali funzioni renali
 Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Rene ed equilibrio acido base La fisiologia e l'acidosi metabolica in corso di insufficienza renale cronica Savi Umberto Scuola di Specializzazione in Nefrologia S.C. di Nefrologia e Dialisi Cattinara
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
EQUILIBRIO ACIDO BASE Le reazioni metaboliche sono molto sensibili a cambiamenti del ph: il ph dei liquidi dell organismo è mantenuto entro un range di valori molto stretto. ph intracellulare è generalmente
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Sistema urinario: la funzione renale
 Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
Sistema urinario: la funzione renale FUNZIONI: Regolazione della composizione ionica del sangue: aumentando o diminuendo l escrezione di ioni specifici, i reni ne regolano la concentrazione plasmatica
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
La eliminazione dei protoni nelle urine permette il ripristino di bicarbonato nel circolo sistemico.
 ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
ESCREZIONE URINARIA DI ACIDI : 1-1,5 meq/l Es. produzione endogena di ac. solforico o cloridrico, formazione di sodio solfato o cloruro, eliminazione urinaria di ammonio legato ai sali. La eliminazione
DISORDINI DELL EQUILIBRIO ACIDO - BASE
 DISORDINI DELL EQUILIBRIO ACIDO - BASE Equilibrio acido-base e potassio Nel tubulo distale e dotto collettore il riassorbimento del bicarbonato è legato a quello del potassio Il riassorbimento del bicarbonato
DISORDINI DELL EQUILIBRIO ACIDO - BASE Equilibrio acido-base e potassio Nel tubulo distale e dotto collettore il riassorbimento del bicarbonato è legato a quello del potassio Il riassorbimento del bicarbonato
Funzioni. Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto
 La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
La Funzione Renale Funzioni Regola composizione ionica plasmatica Volume plasmatico Osmolarità ph Rimuove I prodotti di scarto Il Nefrone Distinguiamo un tubulo renale (trasporto) ed un corpuscolo renale
Sodio. L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria
 Sodio L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria E elemento principale per il controllo dell osmolalità
Sodio L introduzione giornaliera con la dieta di sodio (200 meq/l) è maggiore del nostro fabbisogno (20 meq/l): è necessaria l escrezione urinaria E elemento principale per il controllo dell osmolalità
2.Controllo dell equilibrio acido-base - II. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
In base all equazione di Henderson-Hasselbalch
 Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
equilibrio acido base
 Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Fisiologia Renale Equilibrio acido-base: Fisiologia e fisiopatologia Obiettivi Produzione e bilancio degli idrogenioni Regolazione respiratoria e renale del ph Riassorbimento del bicarbonato e secrezione
Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali:
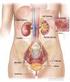 Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali: 1) Secerne Idrogenioni; 1a) Riassorbe il Bicarbonato Filtrato; 1b) Produce Nuovo Bicarbonato. 4320 meq/die
Il Rene Regola la Concentrazione di Idrogenioni nel LEC attraverso Tre Meccanismi Fondamentali: 1) Secerne Idrogenioni; 1a) Riassorbe il Bicarbonato Filtrato; 1b) Produce Nuovo Bicarbonato. 4320 meq/die
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI
 EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
L'EQUILIBRIO ACIDO-BASE
 L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
ph = log 1/[H+] = - log [H+]
![ph = log 1/[H+] = - log [H+] ph = log 1/[H+] = - log [H+]](/thumbs/34/16948015.jpg) ph = log 1/[H+] = log [H+] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = inizio 7,36 max 6.8) ph superiori = alcalosi (limite ph inizio 7,44 max 7.8) ph intracellulare
ph = log 1/[H+] = log [H+] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = inizio 7,36 max 6.8) ph superiori = alcalosi (limite ph inizio 7,44 max 7.8) ph intracellulare
LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE
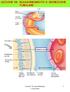 LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE 1 2 capillare peritubulare 80% >19% : riassorbito 20% Frazione di filtrazione riassorbimento = movimento di soluti filtrati e di acqua dal lume tubulare
LEZIONE 28: RIASSORBIMENTO E SECREZIONE TUBULARE 1 2 capillare peritubulare 80% >19% : riassorbito 20% Frazione di filtrazione riassorbimento = movimento di soluti filtrati e di acqua dal lume tubulare
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Riassorbimento tubulare
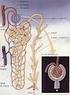 Riassorbimento tubulare Riassorbimento Secrezione Qtr = Qf- Qe Qts = Qe Qf Qtr = VFG*P UV Qts = UV VFG*P Le urine si formano mediante tre processi: Filtrazione glomerulare Riassorbimento di acqua e soluti
Riassorbimento tubulare Riassorbimento Secrezione Qtr = Qf- Qe Qts = Qe Qf Qtr = VFG*P UV Qts = UV VFG*P Le urine si formano mediante tre processi: Filtrazione glomerulare Riassorbimento di acqua e soluti
Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento.
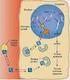 Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento. Lungo i tubuli renali viene riassorbita la maggior parte dei soluti e il
Il rene regola l escrezione dei diversi soluti indipendentemente l uno dall altro, controllandone la velocità di riassorbimento. Lungo i tubuli renali viene riassorbita la maggior parte dei soluti e il
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
acqua, CO 2, O 2, sali e ioni H +
 Legge dell Equilibrio di Massa Se la quantità di una sostanza nell organismo deve rimanere costante, ad ogni sua acquisizione deve corrispondere una perdita di eguale entità acqua, CO 2, O 2, sali e ioni
Legge dell Equilibrio di Massa Se la quantità di una sostanza nell organismo deve rimanere costante, ad ogni sua acquisizione deve corrispondere una perdita di eguale entità acqua, CO 2, O 2, sali e ioni
17/05/2010. Equilibrio idrico. Variazioni del volume ematico indicono risposte omeostatiche
 Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
Equilibrio idrico Variazioni del volume ematico indicono risposte omeostatiche 1 Ruolo del rene nel bilancio idrico Variazioni dell osmolarità attraverso la midollare 2 Scambio per controcorrente nella
PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA. Il paziente non ha problemi cardiaci ma iperpotassiemia
 PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA Il paziente non ha problemi cardiaci ma iperpotassiemia Cause: Prolungato utilizzo del laccio emostatico Rottura delle cellule, durante il prelievo di sangue
PSEUDOIPERKALEMIA o IPERPOTASSIEMIA SPURIA Il paziente non ha problemi cardiaci ma iperpotassiemia Cause: Prolungato utilizzo del laccio emostatico Rottura delle cellule, durante il prelievo di sangue
Riassorbimento dell acqua lungo il nefrone
 Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE. Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta
 CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta Equilibrio acido-base Ph normale: 7.35-7.45 Acidemia per ph < 7.35 Alcalemia per ph >
CHIRURGIA III ED EMERGENZE MEDICO - CHIRURGICHE Sezione di Anestesia e Rianimazione Dir. Prof. Carlo Alberto Volta Equilibrio acido-base Ph normale: 7.35-7.45 Acidemia per ph < 7.35 Alcalemia per ph >
Trasporto epiteliale
 Trasporto epiteliale Rivestono le cavità e le superfici corporee: interfaccia tra gli spazi interni dell organismo e l ambiente Semplice rivestimento o funzione di regolazione (es:osmoregolazione) Trasporto
Trasporto epiteliale Rivestono le cavità e le superfici corporee: interfaccia tra gli spazi interni dell organismo e l ambiente Semplice rivestimento o funzione di regolazione (es:osmoregolazione) Trasporto
I tre sistemi per la regolazione del ph
 I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
Omeostasi idro-elettrolitica
 Omeostasi idro-elettrolitica Riassorbimento idrico isoosmotico o obbligatorio Riassorbimento idrico non-isoosmotico o facoltativo Il bilancio idrico richiede l azione integrata di molteplici sistemi 1
Omeostasi idro-elettrolitica Riassorbimento idrico isoosmotico o obbligatorio Riassorbimento idrico non-isoosmotico o facoltativo Il bilancio idrico richiede l azione integrata di molteplici sistemi 1
I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg
 LEZIONE RENE 6 I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg BL 4.2mM 150mM BILANCIO DEL POTASSIO 4 moli di K nei compartimenti liquidi Liquido intracellulare
LEZIONE RENE 6 I VOLUMI DEI PRINCIPALI COMPARTIMENTI IDRICI DELL ORGANISMO CALCOLATI PER UN INDIVIDUO DI 70 Kg BL 4.2mM 150mM BILANCIO DEL POTASSIO 4 moli di K nei compartimenti liquidi Liquido intracellulare
Anatomia funzionale del rene
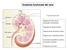 Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
Alterazione della capacità tampone nell'organismo. Alterazione capacità tampone rev. 0 - data: 5 luglio
 Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
Alterazione della capacità tampone nell'organismo Alterazione capacità tampone rev. 0 - data: 5 luglio 2008 1 Il ph fisiologico dell'organismo è compreso tra 7.38 e 7.44 Nel liquido extracellulare sono
OSMOREGOLAZIONE DEI LIQUIDI CORPOREI
 OSMOREGOLAZIONE DEI LIQUIDI CORPOREI Lezione 25 1 Distribuzione dei liquidi corporei L H 2 O contenuta nel corpo è circa il 60% del peso totale ed è così ripartita: 67% 33% EXTRACELLULARE 33% INTRACELLULARE
OSMOREGOLAZIONE DEI LIQUIDI CORPOREI Lezione 25 1 Distribuzione dei liquidi corporei L H 2 O contenuta nel corpo è circa il 60% del peso totale ed è così ripartita: 67% 33% EXTRACELLULARE 33% INTRACELLULARE
Emogasanalisi in t.i.
 Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
45. Fisiologia dell'equilibrio acido-base
 Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
Lezioni di Patologia generale Capitolo 45. Fisiologia dell'equilibrio acido-base 1465 45. Fisiologia dell'equilibrio acido-base III edizione ebook Luigi Barbieri (opzionale) 45. Fisiologia dell'equilibrio
L anatomia dell apparato urinario
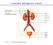 L anatomia dell apparato urinario Le funzioni del rene Secrezione (escrezione) Equilibrio idrico (controllo della pressione arteriosa) Equilibrio salino (controllo della composizione elettrolitica) Endocrina
L anatomia dell apparato urinario Le funzioni del rene Secrezione (escrezione) Equilibrio idrico (controllo della pressione arteriosa) Equilibrio salino (controllo della composizione elettrolitica) Endocrina
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
 Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Fisiologia Renale 8. Bilancio idro-elettrolitico III. Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona
 Fisiologia Renale 8. Bilancio idro-elettrolitico III Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona Obiettivi Bilancio del sodio e regolazione del volume extracellulare
Fisiologia Renale 8. Bilancio idro-elettrolitico III Carlo Capelli, Fisiologia Generale e dell Esercizio Facoltà di Scienze Motorie di Verona Obiettivi Bilancio del sodio e regolazione del volume extracellulare
Riassorbimento tubulare
 Riassorbimento tubulare Le urine si formano mediante tre processi: Ultrafiltrazione (glomerulo) Riassorbimento (tubuli) di acqua e soluti dall ultrafiltrato Secrezione (tubuli) selettiva di alcune sostanze,
Riassorbimento tubulare Le urine si formano mediante tre processi: Ultrafiltrazione (glomerulo) Riassorbimento (tubuli) di acqua e soluti dall ultrafiltrato Secrezione (tubuli) selettiva di alcune sostanze,
Equilibri acido-base, ph e sistemi tampone
 Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Il sistema urinario. Regolazione della concentrazione di sali e acqua, del volume e osmolarità del sangue
 Il sistema urinario Regolazione della concentrazione di sali e acqua, del volume e osmolarità del sangue Funzioni dei reni Regolazione del volume del liquido extracellulare e plasmatico per evitare che
Il sistema urinario Regolazione della concentrazione di sali e acqua, del volume e osmolarità del sangue Funzioni dei reni Regolazione del volume del liquido extracellulare e plasmatico per evitare che
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori:
 Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Il processo di ultrafiltrazione è interamente passivo e dipende sostanzialmente da tre fattori: 1) Dalla differenza netta di pressione tra il lume del capillare ed il lume della capsula di Bowman; 2) dalla
Unidirezionalità del trasporto di una sostanza è assicurata dalla polarizzazione morfologica e funzionale delle cellule epiteliali
 Unidirezionalità del trasporto di una sostanza è assicurata dalla polarizzazione morfologica e funzionale delle cellule epiteliali Lume tubulare (lato apicale, microvilli) Lume interstiziale/capillare
Unidirezionalità del trasporto di una sostanza è assicurata dalla polarizzazione morfologica e funzionale delle cellule epiteliali Lume tubulare (lato apicale, microvilli) Lume interstiziale/capillare
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua
 FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
SOLUZIONE TAMPONE. Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti
 SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE
 EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
Raffaele Alvisi 14 gennaio 1916
 Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Anatomia funzionale del rene
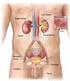 Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
Anatomia funzionale del rene Funzione dei reni: Regolazione del volume del liquido extracellulare Regolazione dell osmolarità Mantenimento del bilancio idrico Regolazione omeostatica del ph Escrezione
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
Bilancio Sodio e Potassio
 Bilancio Sodio e Potassio Sodio E l elemento fondamentale per: Controllo osmolalità Mantenimento volume del LEC Mantenimento Pressione arteriosa L introduzione giornaliera di sodio con la dieta (200 meq/l)
Bilancio Sodio e Potassio Sodio E l elemento fondamentale per: Controllo osmolalità Mantenimento volume del LEC Mantenimento Pressione arteriosa L introduzione giornaliera di sodio con la dieta (200 meq/l)
Equilibrio Acido-Base: interpretazione dati emogasanalitici
 Equilibrio Acido-Base: interpretazione dati emogasanalitici Dott.ssa M. Martino Corso di medicina generale Anno 2010 L EMOGASANALISI è stata definita dall OMS come l esame in assoluto con il miglior rapporto
Equilibrio Acido-Base: interpretazione dati emogasanalitici Dott.ssa M. Martino Corso di medicina generale Anno 2010 L EMOGASANALISI è stata definita dall OMS come l esame in assoluto con il miglior rapporto
Acqua: nutriente essenziale
 Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + +
 Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI
 CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI Il rene è responsabile del controllo dell escrezione di acqua. Altre vie che consentono l eliminazione di acqua dall organismo includono sudorazione, feci
CONTROLLO DELL OSMOLALITA DEI LIQUIDI CORPOREI Il rene è responsabile del controllo dell escrezione di acqua. Altre vie che consentono l eliminazione di acqua dall organismo includono sudorazione, feci
Processi di formazione dell urina
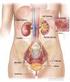 Processi di formazione dell urina Formazione dell urina Filtrazione glomerulare (urina primaria, ultrafiltrato). Riassorbimento (trasporto attivo). Secrezione. Escrezione = Filtrazione glomerulare - Riassorbimento
Processi di formazione dell urina Formazione dell urina Filtrazione glomerulare (urina primaria, ultrafiltrato). Riassorbimento (trasporto attivo). Secrezione. Escrezione = Filtrazione glomerulare - Riassorbimento
PRINCIPALI SISTEMI TAMPONE
 SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
LEZIONE 1_TRASPORTI DI MEMBRANA
 LEZIONE 1_TRASPORTI DI MEMBRANA 1 2 I TRASPORTI DI MEMBRANA Diffusione semplice Diffusione facilitata Trasporto attivo 3 La diffusione semplice Lezione_1_trasporti 4 La diffusione semplice Relazione tra
LEZIONE 1_TRASPORTI DI MEMBRANA 1 2 I TRASPORTI DI MEMBRANA Diffusione semplice Diffusione facilitata Trasporto attivo 3 La diffusione semplice Lezione_1_trasporti 4 La diffusione semplice Relazione tra
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
EQUILIBRIO ACIDO - BASE da appunti del dott. Claudio Italiano, internista ospedaliero Che significa? Vuol dire che l organismo ha un suo equilibrio, detto omeòstasi, cioè il sangue deve necessariamente
Funzioni del Rene. Escrezione prodotti di scarto del metabolismo (urea, creatinina, acido urico) e di sostanze estranee (farmaci, additivi alimentari)
 Il sistema urinario Funzioni del Rene Corticale Nefroni Escrezione prodotti di scarto del metabolismo (urea, creatinina, acido urico) e di sostanze estranee (farmaci, additivi alimentari) Midollare Pelvi
Il sistema urinario Funzioni del Rene Corticale Nefroni Escrezione prodotti di scarto del metabolismo (urea, creatinina, acido urico) e di sostanze estranee (farmaci, additivi alimentari) Midollare Pelvi
www.slidetube.it Il nefrone è costituito dal corpuscolo renale e dal tubulo
 Il nefrone è costituito dal corpuscolo renale e dal tubulo Il corpuscolo renale è formato da : a) il glomerulo arterioso b) la capsula di Bowman www.slidetube.it Zona corticale Zona midollare Dall arteria
Il nefrone è costituito dal corpuscolo renale e dal tubulo Il corpuscolo renale è formato da : a) il glomerulo arterioso b) la capsula di Bowman www.slidetube.it Zona corticale Zona midollare Dall arteria
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE
 FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei Mantenere costanti volume ed osmolarità dei liquidi corporei è essenziale per l omeostasi. Questo è possibile solo se assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei Mantenere costanti volume ed osmolarità dei liquidi corporei è essenziale per l omeostasi. Questo è possibile solo se assunzione ed eliminazione di H 2
FUNZIONE RENALE. Rene: maggiore controllore della composizione del sangue
 FUNZIONE RENALE Rene: maggiore controllore della composizione del sangue Meccanismo di base: eliminazione specifica (selettiva) di soluti e H 2 O dal sangue 0 completa ritenzione sostanze non gradite massima
FUNZIONE RENALE Rene: maggiore controllore della composizione del sangue Meccanismo di base: eliminazione specifica (selettiva) di soluti e H 2 O dal sangue 0 completa ritenzione sostanze non gradite massima
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Riassorbimento dell acqua lungo il nefrone
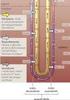 Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
Riassorbimento dell acqua lungo il nefrone La quota escreta di acqua varia fra 0.25% (0.5 L/giorno, massima antidiuresi) ed il 13% (24 L/giorno, massima diuresi), attestandosi in condizioni normali intorno
