Strisce analitiche per determinazioni semi-quantitative
|
|
|
- Niccolina Mauri
- 9 anni fa
- Просмотров:
Транскрипт
1 Strisce analitiche QUANTOFIX per determinazioni ni semiquantitative di ioni e di altre sostanze QUANTOFIX strisce analitiche che rispondono ai più importanti requisiti di un test rapido moderno: Rapido: Si immerge e si legge. Conveniente: L analisi può essere effettuata senza alcun apparecchio, è necessaria solo una striscia QUANTOFIX. Specifico: Le strisce QUANTOFIX sono altamente specifiche; se vi sono interferenze si può precipitarle o mascherarle. Conservabilità: 2 anni e mezzo sotto i +30 C. Confezione: Scatola contenente 100 strisce 6 x 95 mm. Tipo Intervallo e graduazioni Variazione di colore Cod. art. QUANTOFIX Acido ascorbico mg/l vitamina C MN 17 da giallo a verde blu CM QUANTOFIX Alluminio mg/l Al 3+ da rosa a rosso CM QUANTOFIX Ammonio mg/l NH 4 + da giallo ad arancio CM QUANTOFIX Arsenico 10 00,010,0250,050,10,5 mg/l As 3+/5+ da bianco a giallomarrone CM QUANTOFIX Arsenico 50 00,050,10,511,73,0 mg/l As 3+/5+ da bianco a giallomarrone CM QUANTOFIX Calcio mg/l Ca 2+ da giallo a rosso CM ) QUANTOFIX Cianuri mg/l CN da bianco a viola CM QUANTOFIX Cloro mg/l Cl 2 da bianco a rosso viola CM QUANTOFIX Cloruri mg/l Cl da marrone a giallo CM QUANTOFIX Cobalto mg/l Co 2+ da bianco a verdeblu CM QUANTOFIX Cromati mg/l CrO 4 da bianco a viola CM QUANTOFIX Durezza carbonatica d da verde chiaro a blu CM QUANTOFIX EDTA mg/l EDTA da rosso a viola CM QUANTOFIX Ferro mg/l Fe 2+/3+ da bianco a blu viola CM QUANTOFIX Ferro mg/l Fe 2+/3+ da bianco a rosso scuro CM QUANTOFIX Formaldeide mg/l HCHO da marrone chiaro a blu viola CM QUANTOFIX Fosfati mg/l PO 4 da bianco a verdeblu CM QUANTOFIX LubriCheck mmol/l KOH da giallo a blu CM QUANTOFIX Molibdeno mg/l Mo 6+ da bianco a verde CM QUANTOFIX Nichel mg/l Ni 2+ da bianco a rosso chiaro CM QUANTOFIX Nitrati/Nitriti mg/l NO mg/l No 2 da bianco a rossoviola da bianco a rossoviola CM QUANTOFIX Nitriti mg/l NO 2 da bianco a rosso violetto CM QUANTOFIX Nitriti ,10,0,613 mg/l NO 2 da giallo a rosso CM QUANTOFIX Nitriti/pH mg/l NO 2 ph 6,06,46,77,07,7,67,98,8,48,68,89,09,9,6 da bianco a rossoviola da gialloarancio a violarosso CM QUANTOFIX Perossidi 25 00, mg/l H 2 O 2 da bianco a blu CM QUANTOFIX Perossidi mg/l H 2 O 2 da bianco a blu CM QUANTOFIX Perossidi mg/l H 2 O 2 da bianco a marrone CM QUANTOFIX Potassio mg/l K + da giallo ad arancio CM QUANTOFIX QUAT mg/l cloruro di belzanconio da giallo a verdeblu CM QUANTOFIX Rame mg/l Cu +/2+ da bianco a rossoviola CM QUANTOFIX Solfati <200>400>800>1200>1600 mg/l SO 4 da rosso a giallo CM QUANTOFIX Solfiti mg/l SO 3 da bianco a salmone CM QUANTOFIX Stagno mg/l Sn 2+ da bianco a blu scuro CM QUANTOFIX Zinco mg/l Zn 2+ da arancio a rosso CM QUANTOFIX Strisce mult. per acquari d durezza totale da verde a rosso CM QUANTOFIX Strisce multiple per acquari 1) Scatola contenente 60 strisce 2) Scatola contenente 25 strisce d durezza carbonatica ph 6,46,87,7,68,08,4 da verde chiaro a blu da giallo a rosso CM )
2 Sistemi analitici QUANTOFIX QUANTOFIX Acido ascorbico Cod. CM Questa cartina permette di determinare in modo rapido e affidabile l'acido ascorbico (vitamina C) negli alimenti. Si può effettuare la determinazione sia nei succhi di frutta che su superfici di frutta e verdura tagliate di fresco. Nota: conservare le strisce per l acido ascorbico in un posto fresco e asciutto al riparo dalla luce. Intervallo: mg/l vitamina C. Viraggio colore: da giallo a verdeblu. QUANTOFIX Alluminio Cod. CM dell alluminio nelle soluzioni: Nota: dopo aver immerso la striscia in soluzioni fortemente alcaline (ph 13,514) immergere la parte terminale in soluzione di acido acetico al 10% prima della valutazione per circa un minuto. Il berillio interferisce. Anche il rame > 10 mg/l interferisce ma può essere precipitato con ioduro di potassio o con polvere di cadmio. I seguenti anioni interferiscono abbassando il risultato >100 mg/l MnO 4, PO 4, SO 3, S >500 mg/l B 4 O 7, F, Fe (CN) 6, S 2 O 4, S 2 O 5, SiO 4 4, citrati e tartrati. QUANTOFIX Arsenico 50 Cod. CM Cartine e reattivi per la determinazione semiquantitativa dell'arsenico. L'aggiunta di zinco e di un acido solido comporta la formazione di arsina da qualsiasi composto dell'arsenico presente nella soluzione campione. L'arsina reagisce nella fase gassosa, con bromuro di mercurio, nella zona di reazione della striscia per formare alogenuri misti di arsenico/mercurio che in funione della concentrazione da colore giallo diviene colore marrone. Intervallo: 0,053 mg/l As 3+/5+. Viraggio colore: da bianco a giallomarrone. Intervallo: mg/l Al 3+. Viraggio colore: da rosa a rosso. QUANTOFIX Ammonio Cod. CM Strisce e reattivi per la determinazione semiquantitativa dello ione ammonio in soluzione. Intervallo: mg/l NH 4+. Viraggio colore: da giallo brillante ad arancio. QUANTOFIX Arsenico 10 Cod. CM Cartine e reattivi per la determinazione semiquantitativa dell'arsenico. L'aggiunta di zinco e di un acido solido comporta la formazione di arsina da qualsiasi composto dell'arsenico presente nella soluzione campione. L'arsina reagisce nella fase gassosa, con bromuro di mercurio, nella zona di reazione della striscia per formare alogenuri misti di arsenico/mercurio che in funzione della concentrazione danno un viraggio del colore al giallomarrone. QUANTOFIX Calcio Cod. CM Strisce analitiche e reattivi per la determinazione semiquantitativa del calcio in soluzione. I seguenti ioni interferiscono solo al di sopra delle concentrazioni indicate: > di 1000 mg/l: Al 3+, As 3+, NH 4+, Sb 3+, K +, Na +, Bi 3+, Br, Cl, CN, CrO 4, [Fe(CN) 6 ], [Fe(CN) 6 ] 4, I, NO, NO, PO 4, SCN, S 2 O 5, acetati, ascorbati, citrati, tartrati; di 500 mg/l: Ba 2+, Mg 2+ ; di 250 mg/l: Sr 2+, di 100 mg/l: MnO 4. I metalli pesanti interferiscono al di sopra delle seguenti concentrazioni: di 100 mg/l: Mn 2+ ; di 50 mg/l: Ni 2+ ; di 25 mg/l: Fe 2+, Fe 3+, Pb 2+ ; di 10 mg/l: Cr 3+, Co 2+, Cu 2+, Hg 2+, Zn 2+. Intervallo: mg/l Ca 2+. Sufficiente per: 60 analisi. Viraggio colore: da giallo a rosso. Intervallo: 0,010,0250,050,10,5 mg/l As 3+/5+. Viraggio colore: da bianco a giallomarrone. 18 MN
3 QUANTOFIX Cianuri Cod. CM Strisce analitiche e reattivi per la determinazione semiquantitativa dei cianuri in soluzione. Vengono rilevati solo i cianuri liberi o i cianuri complessi che possono essere decomposti dal cloro. Le soluzioni fortemente alcaline, con ph maggiore di 10, devono essere portate a ph 67 con acido solforico diluito. I solfocianuri (tiocianati) a più di 1 mg/l danno luogo ad una colorazione simile. Gli ioduri e i bromuri a più di 5 mg/l, i solfuri a più di 20 mg/l provocano un indebolimento del colore sviluppato. Intervallo: mg/l CN. Viraggio colore: da bianco a viola. QUANTOFIX Cloro Cod. CM Strisce analitiche e reattivi per la determinazione semiquantitativa del cloro libero nelle soluzioni. I bromuri e gli ioduri sopra 5 mg/l indeboliscono il colore sviluppato. A concentrazioni più elevate provocano una completa decolorazione. Anche i nitriti abbassano il valore della misura. Le soluzioni fortemente alcaline (ph maggiore di 10) devono essere portate a ph 67 con acido solforico diluito. Intervallo: mg/l Cl 2. Viraggio colore: da bianco a rossoviola. QUANTOFIX Cloruri Cod. CM dei cloruri (Cl ). Le strisce QUANTOFIX Cloruri utilizzano lo stesso principio generale delle strisce AQUADUR (vedere pagina 26). Nell intervallo di ph 12 la reazione non risente del ph. Soluzioni fortemente acide vanno portate a ph tra 5 e 7 con soluzione di idrato sodico. Soluzioni fortemente alcaline vanno portate nello stesso ambito di ph con acido nitrico. Si possono valutare concentrazioni di cloruri superiori a 3000 mg/l diluendo il campione con acqua distillata. I seguenti ioni interferiscono solo sopra le concentrazioni indicate: > di 1000 mg/l: Al 3+, Ca 2+, Cd 2+, Ce 4+, Cu 2+, K+, Mg 2+, Mn 2+, Na+, NH 4+, Ni 2+, Pb 2+, Sn 2+, Zn 2+, BO, CO 3, CrO 4, NO, NO, PO 4, SO 3, SO 4, acetati, citrati, ossalati, tartrati, EDTA; > di 500 mg/l: Fe 2+, Fe 3+ ; > di 200 mg/l: I ; > di 100 mg/l: Ag +, Br, SCN, > di 75 mg/l: Hg 2+ ; > di 20 mg/l: CN, S 2 O 3 ; > di 10 mg/l: S, ascorbati. Le strisce QUANTOFIX Cloruri risultano particolarmente utili per la valutazione preliminare dell eventuale interferenza da cloruri in soluzioni da sottoporre alla determinazione del COD. Le strisce dovrebbero essere conservate in luogo fresco e asciutto, protette dalla luce solare e dall umidità. Si consiglia di conservare in frigorifero le confezioni non ancora aperte. QUANTOFIX Cobalto Cod. CM del cobalto in soluzione. Se il colore della reazione non compare sulla scala colorata, sono presenti grandi quantità di altri ioni (Cu 2+, Hg + ). Per eliminare queste interferenze seguire le istruzioni indicate sulla confezione. Intervallo: mg/l CO 2+. Shelflife: almeno 2.5 anni dopo la produzione. Viraggio colore: da bianco a verdeblu. QUANTOFIX Cromati Cod. CM dei cromati in soluzione. Le interferenze dovute a Fe 3+, Cu 2+ e ai molibdati vengono eliminate mediante aggiunta di acido ossalico cristallino o in soluzione concentrata. Intervallo: mg/l CrO 4. Shelflife: almeno 2 anni dalla produzione. Viraggio colore: da bianco a viola. QUANTOFIX Durezza carbonatica Cod. CM della durezza da carbonati e bicarbonati. Questa durezza è quella frazione delle durezza totale che è dovuta al contenuto di ioni alcalino terrosi (Ca e Mg) corrispondenti agli ioni carbonato e bicarbonato presenti nell acqua. La durezza carbonatica è la parte di durezza totale che dà luogo alla formazione di incrostazioni di carbonati alcalino terrosi nelle caldaie. Basi forti e altre sostanze che consumano acido provocano risultati errati. Intervallo: d (50360 mg/l CaCO 3 ). Viraggio colore:da verde brillante a blu. Intervallo: mg/l Cl. Shelflife: almeno 2.5 anni dalla produzione, a 8 C. Viraggio colore: da marrone a giallo. MN 19
4 QUANTOFIX EDTA Cod. CM Striscia per la rilevazione veloce e semplice di EDTA, NTA ed altri agenti complessanti in soluzione. Agenti complessanti come EDTA (etilendiamminotetracetato) o NTA (acido nitrilotriacetico) hanno sostituito i fosfati come additivi nelle soluzioni di lavaggio e detergenti. Questa striscia è la soluzione ideale per controllare la concentrazione di tali soluzioni. Nei laboratori di proteomica l'edta viene anche impiegato per rigenerare le colonne cromatografiche precaricate con Co e Ni, utilizzate per purificare le proteine ricombinanti. Prima della successiva analisi, la striscia viene utilizzata per controllare se l'edta è stato risciacquato via completamente. Si possono determinare anche i seguenti agenti complessanti: acido nitrilotriacetico (NTA), acido cicloesandinitrilo(1,2) tetraacetico, acido dietiltrinitrilopentaacetico, acido bis (aminoetil) glicoleteren,n,n',n'tetraacetico. Fattore di conversione: 1 mg/l EDTA=0.7 mg/l NTA. Intervallo: mg/l EDTA. Viraggio colore: da rosso a giallo. QUANTOFIX Ferro 100 Cod. CM di ferro (II) e ferro (III) in soluzione. Il cobalto >50 mg Co 2+ /l forma un colore giallo marrone. Questo può venir eliminato bollendo la soluzione con ditionito di sodio. Non si può determinare il ferro sotto forma di esacianoferrato. Questi complessi devono venir decomposti con acido solforico concentrato prima della determinazione del ferro. QUANTOFIX Formaldeide Cod. CM Strisce analitiche per determinazioni semiquantitative in soluzioni acquose. Utilizzo: la formaldeide è un gas incolore, solubile in acqua, di odore pungente. E sospettata di essere cancerogena, irrita le mucose e provoca allergie. Le soluzioni acquose di formaldeide vengono usate nella produzione di materie plastiche (es. resine urea formaldeide), rivestimenti, adesivi, tessuti, pannelli truciolari, ecc. Vengono anche utilizzate come conservanti in prodotti cosmetici, prodotti biologici e preparati istologici. Le strisce analitiche sono adatte all esame di soluzioni acquose e di estratti acquosi di prodotti solidi (es. truciolati). Per l esame di prodotti detergenti, disinfettanti, shampoo e cosmetici è consigliabile diluire il campione. Metodo: la reazione della formaldeide con un derivato del triazolo dà luogo a un colore da marrone chiaro a blu violetto. La sola interferenza possibile è data da concentrazioni elevate di altre aldeidi che provocano colorazioni diverse da quelle riportate sulla scala colorata. Intervallo: mg/l HCHO. Viraggio colore: da beige a bluviola. Intervallo: mg/l Fe 2+ /Fe 3+. Viraggio colore: da bianco a bluviola. QUANTOFIX Ferro 1000 Cod. CM di Fe 2+ /Fe 3+ in soluzione. Alcuni ioni di metalli pesanti se presenti in forti quantità provocano leggere variazioni di colore. Questo può venire eliminato mediante aggiunta di una piccola quantità di cadmio in polvere. Intervallo: mg/l Fe 2+ /Fe 3+. Viraggio colore: da bianco a rosso scuro. 20 MN
5 QUANTOFIX Fosfati Cod. CM degli ortofosfati (PO 4 ) in soluzione. Vengono rilevati solo gli ortofosfati. Altri fosfati, quali i poli, i piro e i metafosfati devono essere decomposti se si vuole determinare il fosforo totale. Contenuti di silice (SiO 2 ) maggiori di 10 mg/l reagiscono nello stesso modo dando una colorazione azzurra e simulando una concentrazione di fosfati superiore al reale. Concentrazioni elevate di ioni solfuro (S ) producono una colorazione marrone nel campo di misura, mentre a concentrazioni più basse danno luogo a risultati inferiori al reale. I seguenti ioni non interferiscono: < di 1000 mg/l: Ag+, Al 3+, Cd 2+, Co 2+, Cr 3+, Mg 2+, Mn 2+, NH 4+, Ni 2+, Zn 2+, Cl, F, NO, SO 4, citrati, ossalati, tartrati; < di 500 mg/l: Ca 2+ ; < di 250 mg/l: Pb 2+ ; < di 50 mg/l: Cu 2+ ; < di 25 mg/l: Fe 3+ ; < di 5 mg/l: Fe 2+ ; < di 2 mg/l: NO. Intervallo: mg/l PO 4 (solo ortofosfato). Viraggio colore: da bianco a bluverde. QUANTOFIX Lubricheck Cod. CM Utilizzando questa striscia la concentrazione dei lubrificanti di raffreddamento può essere determinata velocemente. La concentrazione viene fornita come mmol KOH/l. Utilizzando un fattore, il risultato può facilmente essere convertito in concentrazione di lubrificante di raffreddamento. Intervallo: mmol/l KOH. Viraggio colore: da giallo a blu. QUANTOFIX Molibdeno Cod. CM Strisce analitiche e reagenti per la determinazione semi quantitativa del molibdeno. Conservare le strisce in luogo fresco ed asciutto, al riparo dalla luce solare e a temperature inferiori a 30 C. Intervallo: mg/l Mo 6+. Viraggio colore: da bianco a verde. QUANTOFIX Nichel Cod. CM Strisce analitiche per la determinazione semi quantitativa del nichel in soluzione. Se il colore della reazione non compare sulla scala colorata sono presenti forte quantità di altri ioni (Co 2+, Hg + ). Per eliminare queste interferenze seguire le istruzioni fornite con la confezione. Intervallo: mg/l Ni 2+. Viraggio colore: da bianco a rosso brillante. QUANTOFIX Nitrati/Nitriti Cod. CM dei nitrati e dei nitriti. Nota: I nitriti interferiscono con la determinazione dei nitrati e perciò le strisce contengono un settore in più per i nitriti. Se questo settore diventa rosso, indicando la presenza di nitriti l NO 2 deve essere decomposto con acido solfammico (acido ammidosolfonico) (Cod. CM ). Dopo la decomposizione dei nitriti si deve ripetere, la determinazione dei nitrati con un altra striscia. Seguendo questo procedimento si possono misurare 10 mg/l (10 ppm) di nitrati anche in presenza di 1000 mg/l (1000 ppm) di nitriti. Conservare le strisce in un luogo fresco e asciutto al riparo dalla luce. Intervallo: Nitrati mg/l NO. Nitriti mg/l NO. Viraggio colore: da bianco a rossoviola. MN 21
6 QUANTOFIX Nitriti Cod. CM dei nitriti in soluzione. Tra ph 1 e 13 la reazione non risente del valore di ph della soluzione in esame. Soluzioni fortemente acide devono venir tamponate con acetato di sodio mentre quelle fortemente alcaline con acido citrico ad un ph tra 3 e 5. Nota: Conservare le strisce analitiche per i nitriti in un luogo fresco e asciutto al riparo dalla luce. Intervallo: mg/l NO. Viraggio colore: da bianco a rossoviola. QUANTOFIX Nitriti/pH Cod. CM La striscia permette la determinazione veloce e semplificata del nitrito e del ph nei lubrificanti di raffreddamento, due parametri molto importanti. Intervallo: mg/l NO. ph Viraggio colore: da bianco a rossoviola (NO ) da giallo/arancio a viola/rosso (ph). QUANTOFIX Nitriti 3000 Cod. CM di concentrazioni elevate di nitriti (NO ) in soluzione. Tra ph 2 e 12 la reazione non risente del valore di ph. Modificare il ph a 4 6 delle soluzioni fortemente acide con soluzione diluita di idrato sodico e quello delle soluzioni fortemente basiche con acido solforico diluito. Nota: Conservare le strisce per nitriti il luogo fresco e asciutto, al riparo dalla luce solare. Intervallo: 00,10,0,613 g/l NO. Viraggio colore: da giallo a rosso. NEW! 22 MN
7 QUANTOFIX Perossidi 25 Cod. CM del perossido di idrogeno (acqua ossigenata; H 2 O 2 ) e dei perossidi in soluzione. Adatte anche per la valutazione di altri idroperossidi inorganici e organici. Per la determinazione degli idroperossidi nei solventi organici si deve bagnare la zona reattiva con una goccia d acqua dopo che il solvente sia evaporato. Nell intervallo di ph tra 2 e 12 la reazione non risente del valore di ph. Soluzioni fortemente acide vanno tamponate con acetato di sodio. Soluzioni fortemente basiche vanno portate a ph 5 7 con acido citrico. Solo agenti ossidanti forti sono in grado di dare risultati falsamente positivi. Intervallo: 00, mg/l H 2 O 2. (Limite di sensibilità per acido peracetico: 1 mg/l). Viraggio colore: da bianco a blu. QUANTOFIX Perossidi 100 Cod. CM dell acqua ossigenata (perossido di idrogeno) in soluzione. Le strisce sono adatte anche per la determinazione di altri idroperossidi inorganici e organici. Per la determinazione di idroperossidi in solventi organici si deve bagnare la zona reattiva con una goccia d acqua dopo che il solvente sia evaporato. Tra ph 2 e 9 la reazione non dipende dal valore del ph. Soluzioni fortemente acide devono venir tamponate con acetato di sodio e quelle fortemente alcaline con acido citrico a ph 57. Oltre a questo solo i forti ossidanti possono interferire. (limite di sensibilità per l'acido peracetico: 2 mg/l) Intervallo: mg/l H 2 O 2. Shelflife: almeno 2.5 anni dalla produzione a 8 C. Viraggio colore: da bianco a blu. QUANTOFIX Perossidi 1000 Cod. CM dell acqua ossigenata (perossido di idrogeno) in soluzione. Le strisce sono adatte anche per la determinazione di altri idroperossidi inorganici e organici. Per la determinazione di idroperossidi in solventi organici si deve bagnare la zona reattiva con una goccia d acqua dopo che il solvente sia evaporato. Tra ph 2 e 9 la reazione non dipende dal valore del ph. Soluzioni fortemente acide devono venir tamponate con acetato di sodio e quelle fortemente alcaline con acido citrico a ph 57. Oltre a questo solo i forti ossidanti possono interferire. Intervallo: mg/l H 2 O 2. Shelflife: almeno 2.5 anni dalla produzione a 8 C. Viraggio colore: da bianco a marrone. QUANTOFIX Potassio Cod. CM Strisce analitiche e reattivo per determinare semiquantitativamente il potassio nelle soluzioni. Concentrazioni di ioni sodio superiori a 3000 mg/l abbassano i risultati. Le seguenti concentrazioni di ioni non interferiscono: < di 1000 mg/l: Al 3+, Ba 2+, Bi 3+, Ca 2+, Fe 2+/3+, Mg 2+, Mn 2+, Sr 2+, Zn 2+ ; < di 200 mg/l: NH 4+, Hg +/2+, Ti + ; < di 25 mg/l S. Proteggere le strisce dalla luce solare e dall'umidità. Conservare sotto i 30 C. Intervallo: mg/l K +. Viraggio colore: da giallo ad arancio. MN 23
8 QUANTOFIX QUAT Cod. CM La striscia è adatta alla determinazione veloce ed affidabile dei composti dell'ammonio quaternario (QUAT) nelle soluzioni. I QUAT sono usati di frequente per la disinfezione di dispositivi medici e superfici. Il test è calibrato per il cloruro di Benzalconio. Vengono forniti anche i fattori di conversione per molti altri composti dell'ammonio quaternario. Intervallo: mg/l cloruro di benzalconio. Viraggio colore: da giallo a bluverde. QUANTOFIX Solfati Cod. CM dei solfati in soluzione. Le strisce QUANTOFIX Solfati si basano sugli stessi principi generali delle strisce AQUADUR (vedere pag. 26). Tra ph 4 e 8 la reazione è indipendente dal ph della soluzione. Campioni fortemente acidi vanno regolati con acetato sodico, mentre per le soluzioni fortemente alcaline si usa acido tartarico. I seguenti ioni interferiscono solo al di sopra delle concentrazioni indicate: >1000 mg/l: BrO, ClO, CrO 4, SO 3, S 2 O 5, SeO 3. >500 mg/l: S 2 O 4. >100 mg/l: CN, S Intervallo: <200>400>800>1200>1600 mg/l SO 4 Viraggio colore: da rosso a giallo. QUANTOFIX Solfiti Cod. CM dei solfiti in soluzione. Questo test viene utilizzato per controllare la concentrazione di solfiti in alimenti trattati con composti dello zolfo per aumentarne la shelflife. Nel settore enologico il controllo dei solfiti è importante per monitorare la produzione e la qualità dei vini. Soluzioni fortemente o anche debolmente acide devono venir tamponate con acetato di sodio prima del saggio in quanto la reazione con i solfiti non avviene in soluzione acida. I solfuri interferiscono in quanto anch essi fanno sviluppare un colore rosso in soluzione neutra.questa interferenza può essere eliminata aggiungendo un eccesso di ioni nichel. Il solfuro di nichel che si forma può venire eliminato mediante filtrazione. Forti quantità di sostanze riducenti quali l acido ascorbico o il cloruro di idrossilammonio interferiscono abbassando il valore dei solfiti. QUANTOFIX Rame Cod. CM del rame in soluzione. Intervallo: mg/l SO 3. Viraggio colore: da bianco a salmone. Intervallo: mg/l Cu + /Cu 2+. Viraggio colore: da bianco a rossoviola. 24 MN
9 QUANTOFIX Stagno Cod. CM dello stagno in soluzione. Nell'industria alimentare questa striscia viene utilizzata per controllare succhi di frutta o conserve. In funzione delle condizioni di conservazione e della qualità del rivestimento interno dell'imballaggio, quantità significative di stagno possono migrare nel prodotto, con effetti negativi sul sapore dell'alimento. Il controllo dello stagno quindi assicura un'ottima qualità dell'alimento. Intervallo: mg/l Sn 2+. Viraggio colore: da bianco a blu scuro. QUANTOFIX Zinco Cod. CM Strisce analitiche e reattivi per la determinazione semiquantitativa dello zinco (Zn 2+ ) in soluzione. I seguenti ioni interferiscono solo a concentrazioni superiori a: > di 1000 mg/l: Ag +, Al 3+, Bi 3+, Ca 2+, Cd 2+, Co 2+, Fe 2+, Fe 3+, Mn 2+, NH 4+, Pb 2+, Sn 2+, Sn 4+, Cl, CrO 4, NO, NO, PO 4, SCN, SO 3, SO 4, acetati, ascorbati, citrati, ossalati, tartrati. I seguenti ioni abbassano i risultati: > di 500 mg/l Cr 3+ ; > di 200 mg/l CN ; > di 100 mg/l Mg 2+ ; > di 50 mg/l S 2 > di 25 mg/l Ni 2+. La presenza di Cu 2+, > di 10 mg/l di Hg + / 2+ (si precipita con polvere di ferro o di cadmio in soluzione debolmente acida) e > di 50 mg/l MnO 4 (si distrugge con cloruro di idrossilammonio in soluzione acida) provocano una colorazione marrone della zona reattiva. Intervallo: mg/l Zn 2+. Viraggio colore: da arancio a rosso. QUANTOFIX Acquari Strisce multiple Cod. CM /27 della durezza totale (Ca 2+, Mg 2+ ), della durezza carbonatica (HCO, CO 3 ) e del ph nell acqua degli acquari. La durezza totale dell acqua è dovuta al suo contenuto di sali di calcio e di magnesio (Ca 2+, Mg 2+ ). La misura della durezza totale è data dalla somma di questi sali. La durezza carbonatica è solo una frazione della durezza totale ed è dovuta alla parte di elementi alcalino terrosi (Ca e Mg) corrispondenti agli ioni carbonato e bicarbonato (CO 3 e HCO ) presenti nell acqua. La durezza carbonatica rappresenta una misura della capacità tampone di un acqua. Un acqua con un basso contenuto di durezza carbonatica non è sufficientemente tamponata e di conseguenza il valore del ph può presentare ampie fluttuazioni. Il valore del ph indica se l acqua è acida, neutra o alcalina (basica). Se il valore del ph è uguale a 7 l acqua è neutra. Con valori inferiori a 7 l acqua è acida. Per valori superiori a 7 la reazione è alcalina (basica). Le strisce multiple QUANTOFIX consentono di ottenere facilmente misure orientative dei tre parametri molto importanti per un acqua da acquario. Intervalli: durezza totale d durezza carbonatica d ph 6,46,87,7,68,08,4 Sufficiente per: 100 (CM ) o 25 analisi (CM ). Viraggio colore: da verde a rosso (durezza totale) da verde brillante a blu (durezza carbonatica) da giallo a rosso (ph). MN 25
3. Strumenti di misura Misura del ph/carta
 . Strumenti di Misura del /Carta GENERAL CATALOGUE EDITION 8 LLG-Cartina indicatrice universale di, rotolo Per la determinazione dei valori di. Rocchetto dispensatore in plastica con rotolo da m. - - 9.9
. Strumenti di Misura del /Carta GENERAL CATALOGUE EDITION 8 LLG-Cartina indicatrice universale di, rotolo Per la determinazione dei valori di. Rocchetto dispensatore in plastica con rotolo da m. - - 9.9
Catalogo Prodotti Labware. a b c d e f g h i j k l m n o p q r s T u v w x y z. 38 Test rapidi. Parametri ambientali e di qualità...
 Catalogo Prodotti Labware 38 Parametri ambientali e di qualità... 302 a b c d e f g h i j k l m n o p q r s T u v w x y z 301 38 Parametri ambientali e di qualità Idrimeter Mc - Manuali colorimetrici Catalogo
Catalogo Prodotti Labware 38 Parametri ambientali e di qualità... 302 a b c d e f g h i j k l m n o p q r s T u v w x y z 301 38 Parametri ambientali e di qualità Idrimeter Mc - Manuali colorimetrici Catalogo
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
Total P Total S Ammonio NH 4
 2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) 3 bianco gelatinoso.
 Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
ossidazione/riduzione, ossidante/riducente
 ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox +6-1 -1 +3-1 K 2 Cr 2 O 7 (aq) + HI(aq) KI(aq) + CrI 3 (aq) + I 2 (s) + H 2 O(l) 0 K 2 Cr 2 O 7 (aq) + 6HI(aq) KI(aq) + 2CrI
ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox +6-1 -1 +3-1 K 2 Cr 2 O 7 (aq) + HI(aq) KI(aq) + CrI 3 (aq) + I 2 (s) + H 2 O(l) 0 K 2 Cr 2 O 7 (aq) + 6HI(aq) KI(aq) + 2CrI
HYDROCHECK. Oggetto: INFORMAZIONI PER L ACQUISTO IN data:
 INFORMAZIONE GENERALE Per tutti i kit HYDROCHECK possono essere forniti ricambi dei vari reagenti, che consentono di realizzare un risparmio nel costo per analisi. TITRATEST Ogni kit TITRATEST contiene
INFORMAZIONE GENERALE Per tutti i kit HYDROCHECK possono essere forniti ricambi dei vari reagenti, che consentono di realizzare un risparmio nel costo per analisi. TITRATEST Ogni kit TITRATEST contiene
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
ossidazione/riduzione, ossidante/riducente
 ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox 0 +5 +2 +4 Cu(s) + HNO 3 (aq) Cu(NO 3 ) 2 + NO 2 (g) + H 2 O(l) Determinazione dei numeri di ossidazione Cu(s) + 2HNO 3 (aq)
ossidazione/riduzione, ossidante/riducente Esercizio tipo: bilanciamento redox 0 +5 +2 +4 Cu(s) + HNO 3 (aq) Cu(NO 3 ) 2 + NO 2 (g) + H 2 O(l) Determinazione dei numeri di ossidazione Cu(s) + 2HNO 3 (aq)
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
KIT DI ANALISI HYDROCHECK COLORTEST
 KIT DI ANALISI HYDROCHECK COLORTEST NOME DEL KIT : HCK COLORTEST AMMONIACA Cod.N 6102 TIPO DI ANALISI: COLORIMETRICA METODO DI ANALISI: Indofenolo SENSIBILITA : 0,25 ppm NH3 2 flaconi reagente Ammoniaca
KIT DI ANALISI HYDROCHECK COLORTEST NOME DEL KIT : HCK COLORTEST AMMONIACA Cod.N 6102 TIPO DI ANALISI: COLORIMETRICA METODO DI ANALISI: Indofenolo SENSIBILITA : 0,25 ppm NH3 2 flaconi reagente Ammoniaca
Chimica Generale. Reazioni Chimiche. Reazioni Chimiche
 Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
La fertilità chimica
 La fertilità chimica La fertilità chimica di un suolo è la capacità continuata nel tempo di fornire gli elementi della nutrizione minerale delle piante in forma disponibile ed in quantità bilanciate Indicatori
La fertilità chimica La fertilità chimica di un suolo è la capacità continuata nel tempo di fornire gli elementi della nutrizione minerale delle piante in forma disponibile ed in quantità bilanciate Indicatori
SCHEDE TECNICHE fornitura prodotti chimici e reagenti
 SCHEDA TECNICA N. 1 IPOCLORITO DI SODIO AL 14-15 % (COME CLORO ATTIVO) PER LA DEPURAZIONE DELL ACQUA, CONFORME ALLA NORMA ONORM C9902 Aspetto: Titolo: Colorazione: Soluzione acquosa 14 15 % (come cloro
SCHEDA TECNICA N. 1 IPOCLORITO DI SODIO AL 14-15 % (COME CLORO ATTIVO) PER LA DEPURAZIONE DELL ACQUA, CONFORME ALLA NORMA ONORM C9902 Aspetto: Titolo: Colorazione: Soluzione acquosa 14 15 % (come cloro
ESERCIZI DI RIEPILOGO GENERALE
 ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole e fontanelle cittadine.
 Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
NUMERO DI OSSIDAZIONE NOMENCLATURA CHIMICA
 NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
LE SOSTANZE PRESENTI NELL ACQUA SI POSSONO SUDDIVIDERE IN: sostanze in sospensione sostanze in soluzione gas disciolti
 LE SOSTANZE PRESENTI NELL ACQUA SI POSSONO SUDDIVIDERE IN: sostanze in sospensione sostanze in soluzione gas disciolti Tipi di acque Acque Per Uso Industriale (I) Le acque impiegate dalle industrie per
LE SOSTANZE PRESENTI NELL ACQUA SI POSSONO SUDDIVIDERE IN: sostanze in sospensione sostanze in soluzione gas disciolti Tipi di acque Acque Per Uso Industriale (I) Le acque impiegate dalle industrie per
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE
 PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
ESERCIZI. 1. Completa le seguenti reazioni e, se necessario, bilanciale: b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore!
 ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml.
 Compito di Analisi dei farmaci I Bari,3 febbraio 1999 1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml. 1)Quale deve essere la sensibilità della bilancia
Compito di Analisi dei farmaci I Bari,3 febbraio 1999 1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml. 1)Quale deve essere la sensibilità della bilancia
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
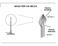 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
APPLICAZIONE DI RIDUCENTI IN VOLUMETRICA
 APPLICAZIONE DI RIDUCENTI IN VOLUMETRICA Le sostanze riducenti reagiscono con l O 2 dell aria, per questo motivo è meglio conservarle in atmosfera inerte. Metodo: agente riducente non standardizzato +
APPLICAZIONE DI RIDUCENTI IN VOLUMETRICA Le sostanze riducenti reagiscono con l O 2 dell aria, per questo motivo è meglio conservarle in atmosfera inerte. Metodo: agente riducente non standardizzato +
Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA. Prof. Antonino Mamo
 Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA Prof. Antonino Mamo 1) Scrivere le formule di struttura dei seguenti sali: a) permanganato di
Università di Catania Facoltà di Ingegneria CdL Ingegneria Recupero Edilizio Ambientale ESERCIZI DI CHIMICA Prof. Antonino Mamo 1) Scrivere le formule di struttura dei seguenti sali: a) permanganato di
Sostanze organiche: determinazioni qualitative
 Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Titolazioni Redox. Analisi volumetrica basata su una reazione di ossido-riduzione. La somma delle due coppie coniugate ossido-riduttive
 Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
NOMENCLATURA E REAZIONI
 NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
Sommario della lezione 7. Misure di concentrazione. Nomenclatura
 Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
Esame (0) classei - Codice Prova:
 1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
1) Il diossido di zolfo reagirà con l acqua secondo la reazione: SO 2 (g) + H 2 O (l) H 2 SO 3 (l) Quanto diossido di zolfo è necessario per preparare 27.86 g di H 2 SO 3 (l)? A. 27.86 g B. 0.3394 g C.
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
Metodi e apparecchiature
 Metodi e apparecchiature Matrici gassose Temperatura media Velocità media Tenore volumetrico di ossigeno Umidità Monossido di carbonio Ammoniaca Ossidi di azoto Ossidi di zolfo Protossido d azoto Ammine
Metodi e apparecchiature Matrici gassose Temperatura media Velocità media Tenore volumetrico di ossigeno Umidità Monossido di carbonio Ammoniaca Ossidi di azoto Ossidi di zolfo Protossido d azoto Ammine
DICHIARA DI OFFRIRE PER LA FORNITURA DI REAGENTI - LOTTO 1
 ALLEGATO 7 - MODULO OFFERTA - LOTTO 1 AFFIDAMENTO FORNITURA TRIENNALE REAGENTI PER LABORATORI ARPAS l sottoscritt, titolare/legale rappresentante della con sede in, via partita IVA DICHIARA DI OFFRIRE
ALLEGATO 7 - MODULO OFFERTA - LOTTO 1 AFFIDAMENTO FORNITURA TRIENNALE REAGENTI PER LABORATORI ARPAS l sottoscritt, titolare/legale rappresentante della con sede in, via partita IVA DICHIARA DI OFFRIRE
* * *TESTPC* * *
 Pagina 1 di 5 Dati Anagrafici Campione di: Prelevatore: Richiesta/Verbale n : Data Prelievo: Campione Formale: Punto Prelievo: Ditta/Struttura prelievo Comune di Prelievo: Cliente: Indirizzo cliente: Quesito:
Pagina 1 di 5 Dati Anagrafici Campione di: Prelevatore: Richiesta/Verbale n : Data Prelievo: Campione Formale: Punto Prelievo: Ditta/Struttura prelievo Comune di Prelievo: Cliente: Indirizzo cliente: Quesito:
Numero di ossidazione
 Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Armadio Scaffale Sostanza CAS number Scheda Quantità
 Acidi 1 Acido acetico 64-19-7 A1 2 314 226 Acidi 1 Acido oleico 70 % 112-80-1 A2 1 335 319 315 Acidi 1 Acido ossalico 144-62-7 A3 2 312 302 Acidi 1 Acido formico 64-18-6 A4 1 314 226 Acidi 1 Acido fluoridrico
Acidi 1 Acido acetico 64-19-7 A1 2 314 226 Acidi 1 Acido oleico 70 % 112-80-1 A2 1 335 319 315 Acidi 1 Acido ossalico 144-62-7 A3 2 312 302 Acidi 1 Acido formico 64-18-6 A4 1 314 226 Acidi 1 Acido fluoridrico
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI. Dr. Francesco Musiani
 REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
REAZIONI DI OSSIDO-RIDUZIONE: ESERCIZI RISOLTI Dr. Francesco Musiani Versione aggiornata al 20.12.2011 Zn (s) + NO 3 - Zn 2+ + NH 4 + Zn (s) Ý Zn 2+ (1) NO - + 3 Ý NH 4 (2) - Bilanciamento di (1): In questa
PROCHEM. Certificato di analisi (Certificato valido ai sensi del R.D. 842/28)
 Numero Certificato: 249/12 Campione: Acqua piezometro n.1 ph 7,79 - APAT 2060/2003 Conducibilità elettrica us/cm a 20 C 3260 - APAT 2030/2003 Ossidabilità mg/l O 2 1,9 - UNI EN ISO 8467:1997 Azoto ammoniacale
Numero Certificato: 249/12 Campione: Acqua piezometro n.1 ph 7,79 - APAT 2060/2003 Conducibilità elettrica us/cm a 20 C 3260 - APAT 2030/2003 Ossidabilità mg/l O 2 1,9 - UNI EN ISO 8467:1997 Azoto ammoniacale
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
H N. Mn 2+ +.. Fe 3+ +.. H 2 O
 CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
ISTRUZIONE OPERATIVA N. 04 INCOMPATIBILITA. Revisione 00 - Gennaio A cura di: Servizio Ambiente e Progettazione per la Sicurezza
 ISTRUZIONE OPERATIVA N. 04 Revisione 00 - Gennaio 2015 A cura di: Servizio Ambiente e Progettazione per la Sicurezza ISTRUZIONE OPERATIVA N.04. Scopo e campo di applicazione Il rifiuto, prima di essere
ISTRUZIONE OPERATIVA N. 04 Revisione 00 - Gennaio 2015 A cura di: Servizio Ambiente e Progettazione per la Sicurezza ISTRUZIONE OPERATIVA N.04. Scopo e campo di applicazione Il rifiuto, prima di essere
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali 1 Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
prendono parte alla reazione.
 REAZIONI CHIMICHE A + B = C + D A, B = reagenti C, D = prodotti Es. C 3 H 8 (g) + O 2 (g) = CO 2 (g) + H 2 O (g) propano BILANCIAMENTO DELL EQUAZIONE DI REAZIONE (principio di conservazione della massa)
REAZIONI CHIMICHE A + B = C + D A, B = reagenti C, D = prodotti Es. C 3 H 8 (g) + O 2 (g) = CO 2 (g) + H 2 O (g) propano BILANCIAMENTO DELL EQUAZIONE DI REAZIONE (principio di conservazione della massa)
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
REGISTRO PRODOTTI CHIMICI LABORATORIO DI CHIMICA REV. 07 A.S.2012/2013 XN-NOCIVO VETRO R H225 ML.900 F-FACILMENTE INFIAMMABILE
 1 ACETONE XN-NOCIVO R-11-36-66-67 H225 ML.900 F-FACILMENTE INFIAMMABILE S-9-16-26 2 ACQUA OSSIGENATA C-CORROSIVO R-8-34 H271 ML.300 O-COMBURENTE S-3-28-36/39-45 H314 ML.2000 3 ACQUA DI BARITE ML.650 4
1 ACETONE XN-NOCIVO R-11-36-66-67 H225 ML.900 F-FACILMENTE INFIAMMABILE S-9-16-26 2 ACQUA OSSIGENATA C-CORROSIVO R-8-34 H271 ML.300 O-COMBURENTE S-3-28-36/39-45 H314 ML.2000 3 ACQUA DI BARITE ML.650 4
MODULO MOD 01.1 LISTINO PREZZI
 Pag. 1 di 11 Matrice acque di scarico parametro Metodo prezzo #*aldeidi APAT CNR IRSA 5010 A Man 29 2003 16,50 *aldeidi (come HCHO) MtdI 18 Rev. 00 2016 20,00 Anioni preparativa 6,60 #*azoto ammoniacale
Pag. 1 di 11 Matrice acque di scarico parametro Metodo prezzo #*aldeidi APAT CNR IRSA 5010 A Man 29 2003 16,50 *aldeidi (come HCHO) MtdI 18 Rev. 00 2016 20,00 Anioni preparativa 6,60 #*azoto ammoniacale
Soluzioni. 12 a. La soluzione più acida è la soluzione A. b. La soluzione con il ph maggiore è la soluzione B.
 Soluzioni capitolo 21 VERIFICA LE TUE CONOSCENZE IL PRODOTTO IONICO DELL ACQUA 1 Concentrazione degli ioni H 3 O + : a. [H 3 O + ] = 1 $ 10-1 mol/l b. [H 3 O + ] = 1 $ 10 0 mol/l 2 Concentrazione degli
Soluzioni capitolo 21 VERIFICA LE TUE CONOSCENZE IL PRODOTTO IONICO DELL ACQUA 1 Concentrazione degli ioni H 3 O + : a. [H 3 O + ] = 1 $ 10-1 mol/l b. [H 3 O + ] = 1 $ 10 0 mol/l 2 Concentrazione degli
 ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
Compito di analisi dei farmaci I. Bari,9 settembre 1998
 Compito di analisi dei farmaci I Bari,9 settembre 1998 1) L acido formico in una soluzione 0.1 M è dissociato per il 4.6%.50 ml di questa soluzione si diluiscono a 250 ml con acqua e si titolano con NaOH
Compito di analisi dei farmaci I Bari,9 settembre 1998 1) L acido formico in una soluzione 0.1 M è dissociato per il 4.6%.50 ml di questa soluzione si diluiscono a 250 ml con acqua e si titolano con NaOH
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 5 Maggio 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
NANOCOLOR 500D Cod
 16 Analisi acque» FOTOMETRI MULTIPARAMETRO NANOCOLOR 500D Cod. 22.3215.88 Descrizione Fotometro digitale adatto per analisi di routine, particolarmente indicato per analisi di acque e acque di scarico,
16 Analisi acque» FOTOMETRI MULTIPARAMETRO NANOCOLOR 500D Cod. 22.3215.88 Descrizione Fotometro digitale adatto per analisi di routine, particolarmente indicato per analisi di acque e acque di scarico,
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
