La termodinamica studia i flussi/trasformazioni di energia. Bioenergetica: termodinamica applicata ai sistemi biologici
|
|
|
- Albana Brunelli
- 6 anni fa
- Visualizzazioni
Transcript
1 LA CAPACITÀ DI USARE ENERGIA È CARATTERISTICA DEI SISTEMI VIVENTI Bisogni degli esseri viventi: Energia (luce, molecole organiche) Catalizzatori biologici (enzimi) La termodinamica studia i flussi/trasformazioni di energia Bioenergetica: termodinamica applicata ai sistemi biologici
2 Energia: capacità di compiere un lavoro o meglio Capacità di causare specifici cambiamenti 1. Lavoro di sintesi: cambiamenti nei legami chimici (turnover, crescita) 2. Lavoro meccanico: cambiamenti nella localizzazione o nell orientamento di una cellula o di una sua parte 3. Lavoro di concentrazione: movimento di molecole attraverso una membrana contro gradiente di concentrazione 4. Lavoro elettrico: movimento di ioni attraverso una membrana contro un gradiente elettrochimico. 5. Calore: aumento di temperatura (utile negli animali a sangue caldo,omeotermi). 6. Bioluminescenza: produzione di luce
3 Gli organismi viventi ottengono E dalla luce del sole (fototrofi) o dalle molecole organiche del cibo (chemiotrofi). ENTROPIA: disordine (S) ENTALPIA: calore (H) Flusso di energia attraverso la biosfera è unidirezionale: sole biosfera entropia universo Flusso di materia è ciclico Il nitrato ( inorganico ) è trasformato dalle piante in ammoniaca e lo usano per la sintesi di Aa, proteine, nucleotidi, ac. nucleici.
4 Tutte le forme di energia possono essere di due tipi: CINETICA o energia di movimento (movimento di elettroni, onde, atomi etc; es: E. elettrica, E. Termica, suono, velocità, ) POTENZIALE o energia di posizione (o energia immagazzinata; es energia chimica, nucleare, molla compressa, )
5 Concetto di sistema in termodinamica Sistema: porzione di universo considerato relativamente agli scambi di energia (sotto forma di calore o lavoro) con ambiente circostante. NB: Chiuso: scambia solo E Aperto: sia E che massa
6 Gli esseri viventi sono sistemi aperti!
7 I legge della termodinamica: Legge della conservazione dell E. L energia può essere convertita da una forma all altra, ma non può mai essere creata né distrutta. Nel caso delle reazioni e dei processi biologici si è maggiormente interessati al cambiamento di ENTALPIA o contenuto di calore (H). H = E + PV Nelle reazioni biologiche P e V = 0 Becker et al. H = H prodotti H reagenti H negativo : reazione esotermica; H positivo: reazione endotermica
8 II legge della termodinamica:aumento dell entropia S In ogni cambiamento chimico e fisico il disordine complessivo del sistema e dell ambiente (universo) aumenta sempre. In base al I e II principio della termodinamica Energia libera = G H = G + T S G = H T S Ogni reazione spontanea è caratterizzata da una diminuzione di E libera ( G sistema < 0) e da un aumento di entropia ( S universo > 0). Tutte le reazioni che avvengono spontaneamente hanno come conseguenza una diminuzione nel contenuto di Energia libera del sistema. Le reazioni esoergoniche liberano energia ( G negativo) spontanee Una reazione endoergonica richiede E ( G positivo) non spontanee
9 La variazione di energia libera ( G) indica se la reazione è spontanea G negativo spontanea G positivo non spontanea Nei viventi metabolismo include reazioni sia esoergoniche che endoergoniche Strategia dell accoppiamento delle reazioni! in modo che G complessivo<0
10 L accoppiamento tra 2 reazioni/processi in una cellula può avvenire: tra reazioni diverse ma con intermedio comune Formazione di proteina in stato/conformazione attivato (es proteine motrici) Uso di gradienti elettrochimici Es. energia potenziale sotto forma di gradiente di concentrazione
11 Luce solare Ossidazione nutrienti fototrofi chemiotrofi ATP L ATP è la molecola più usata dai viventi per accoppiare reazioni esoergoniche ed endoergoniche. ATP ha alta energia potenziale nei legami dei gruppi P la rimozione/idrolisi del P è fortemente esoergonica Cioè ha un alto potenziale di trasferimento del gruppo P
12 L ATP libera energia utile per le reazioni endoergoniche attraverso il trasferimento del gruppo fosfato. ATP Lavoro chimico Lavoro meccanico Lavoro di trasporto Membrana della proteina P + Proteina motrice P Soluto Reagenti P P P Prodotto Molecola formata Proteina mobile Soluto trasportato P ADP + P
13 Becker et al. Diminuzione della stabilizzazione per risonanza dei gruppi carbossilato e fosfato in seguito alla formazione di legami. (b) Un legame anidridico dà come risultato una maggiore delocalizzazione elettronica in entrambi i prodotti, quindi ha una maggiore energia di idrolisi
14 Becker et al. Perché l idrolisi dell ATP è tanto esoergonica? L idrolisi dell ATP a ADP + Pi è esoergonica a causa della -repulsione di carica tra gruppi fosfato e -della stabilizzazione per risonanza di entrambi i prodotti dell idrolisi. -Quindi il prodotto di reazione è + stabile e favorito termodinamicamente La vera struttura dei gruppi fosfato è in realtà la media delle strutture che vi contribuiscono, detta IBRIDO DI RISONANZA, nel quale gli e in eccesso sono delocalizzati su tutti i possibili legami
15 Becker et al. Importante: l ATP è un composto fosforilato ad E intermedia! La coppia ATP/ADP rappresenta un mezzo reversibile per conservare, trasferire e rilasciare E all interno della cellula. L E libera rilasciata al momento dell idrolisi dell ATP fornisce la forza per trascinare i numerosi processi necessari per la vita.
16 Ciclo dell ATP Catabolismo respirazione cellulare L ATP è continuamente consumata e rigenerata Lavoro cellulare (anabolismo, trasporto molecole, attivazione proteine,..)
17 Anche i coenzimi trasportatori di elettroni (NAD, FAD, NADP) sono molecole con alto contenuto di energia potenziale potenziale di trasf. di e-
18 In una reazione reversibile all equilibrio la tendenza a dare prodotti o reagenti è la stessa L equilibrio è influenzato dalla concentrazione di reagenti e prodotti Nei sistemi biologici le reazioni sono quasi sempre tenute lontane dall equlibrio! L energia libera associata al sistema è minima all equilibrio e aumenta quando ci si sposta dall equilibrio in una delle 2 direzioni! dg<0 reazione procede vs dx dg=0 reazione all equilibrio dg>0 reazione procede vs sx
19 R: costante dei gas T: 298Kelvin=25 C
20 G dice solo se una reazione può avvenire, ma non dice se avverrà (valore assoluto =energia scambiata; segno: spontaneità, direzione del processo). NB: le uniche reazioni che avvengono a velocità apprezzabile in una cellula sono quelle per le quali sono presenti e attivi i catalizzatori proteici (enzimi) o ad RNA (ribozimi) appropriati. Il ruolo di un catalizzatore è quello di abbassare l energia di attivazione (E a ) richiesta per fare avvenire una reazione. In questo modo la reazione è accelerata L accelerazione della velocità di reazione è detta CATALISI
21 L energia di attivazione (EA) è la quantità minima di E cinetica che le molecole di reagente devono possedere per consentire il verificarsi delle collisioni, che portano alla formazione del prodotto. Attivazione termica frazione molecole con alta energia (b) Il numero di molecole con sufficiente energia per superare la barriera dell (EA) e collidere può aumentare alzando la temperatura da T1 a T2. non realizzabile nei viventi Catalisi EA l Ea può essere abbassata da un catalizzatore, aumentando in tal modo il numero di molecole da N1 a N 2
22 Che cosa fa un catalizzatore? Legando i reagenti ad una sorta di superficie in modo da giustapporre le parti potenzialmente reattive di molecole adiacenti, è favorita la loro interazione ed effettivamente ridotta l E di attivazione. Fornire questa superficie reattiva è compito del CATALIZZATORE. NB: Il catalizzatore non è permanentemente modificato o consumato al procedere della reazione. Es di catalizzatori: enzimi, ribozimi, metalli UN CATALIZZATORE: 1) la velocità di una reazione ( volte) 2) Forma complessi transitori con le molecole di substrato, legandosi ad esse in modo da facilitarne interazione 3) Cambia solo la velocità con cui si raggiunge l equilibrio, ma non può in alcun modo far avvenire una reazione endoergonica.
23 Gli enzimi sono proteine che agiscono come catalizzatori biologici: accelerano la velocità delle reazioni senza alterare il G. Con la catalisi l enzima abbassa l Energia di attivazione richiesta affinchè la reazione inizi
24 Ogni enzima contiene un SITO ATTIVO che riconosce e lega specificamente il substrato e dove avviene l evento catalitico. Sito attivo: tasca molecolare in cui si inserisce specificamente il substrato
25 Gli aa del sito attivo generalmente non sono contigui lungo la sequenza primaria, ma vengono portati vicini col ripiegamento 3D della catena polipeptidica. Tipico è anche il coinvolgimento di Aa in posizioni distanti lungo la struttura primaria. Dei 20 Aa solo pochi sono implicati nei siti attivi: cisteina, istidina, serina, aspartato, glutammato, lisina. Alcuni enzimi includono componenti NON proteiche: i cofattori COFATTORI= piccole molecole organiche (coenzimi) oppure ioni metallici che spesso partecipano alla catalisi in modo determinante.
26 Grazie al sito attivo gli enzimi hanno un elevato grado di specificità di substrato. ENZIMI x sintesi o degradazione: specificità di gruppo ( più economico per la cellula).
27 Gli ENZIMI sono altamente specifici nell interazione col substrato e per il tipo di reazione catalizzata Ogni cellula possiede migliaia di enzimi specifici per diverse reazioni La catalisi avviene favorendo lo stato di transizione: 1. Portare vicine tra loro molecole dei reagenti 2. Orientarle come nello stato di transizione 3. Creare microambiente che ne agevola reazione Caratteri degli enzimi 1. Elevata specificità 2. Regolazione 3. Sensibilità a T, ph, forza ionica,..
28
29 Interazione enzima-substrato a)modello chiave serratura- rigido b)modello adattam.indotto distorsione di enzima e substrato reazione favorita Le reazioni catalizzate da enzimi sono volte più veloci!
30 L attività degli enzimi è influenzata da temperatura e ph. T elevata denatura l enzima stomaco intestino La DIPENDENZA DAL PH è generalmente dovuta alla presenza di uno o più Aa carichi nel sito attivo e riflette l ambiente fisiologico in cui l enzima opera. Sensibilità ad altri fattori: substrati alternativi Ambiente ionico.
31 a) V reazione aumenta con aumento di enzima (eccesso di substrato) b) V reazione aumenta fino ad un MAX se la conc. di enzima è costante saturazione
32 Inibizione degli enzimi Inibizione reversibile e irreversibile a) Inib revers. competitiva b) Inib revers. non competitiva
33 Inibitori enzimatici come farmaci specifici e selettivi Es. Sulfonammidi, antibiotici, farmaci antitumorali,
34 Regolazione allosterica L Enzima esiste in due forme attiva /non attiva, determinate dal legame con effettore allosterico (positivo o negativo) su sito allosterico (diverso dal sito attivo) Enzimi multimerici; subunità catalitiche e regolatorie; cooperatività
35 Inibitori e/o effettori allosterici possono regolare l attività enzimatica Es: inibizione a feed-back (o da prodotto finale). Un prodotto metabolico inibisce uno degli enzimi coinvolti nella catena metabolica che porta alla sintesi del prodotto.
36 Oltre alla regolazione allosterica molti E sono anche soggetti a controllo mediante modificazione chimica. A) Aggiunta/rimozione di gruppi P a) Fosforilazione ad opera delle protein- chinasi: trasferimento di un gruppo fosfato dall ATP al gruppo OH di una serina, treonina o tirosina. b) Defosforilazione ad opera delle protein-fosfatasi Es: glicogeno fosforilasi regolata mediante fosforilazione/defosforilazione
37 B) Taglio proteolitico Es: proteasi pancreatiche sintetizzate come precursori inattivi
38 Non tutti gli enzimi sono proteine! Ribozima Auto-excisione e splicing dell introne dal pre-rrna: Una molecola precursore di rrna di Tetraymena contiene un introne in grado di catalizzare la propria excisione dalla molecola di pre.rrna. Altri es.: ribonucleasi P, ribosomi
39 A seguito del preciso adattamento chimico tra il sito attivo di un enzima e i suoi substrati, gli enzimi sono molto efficaci quali catalizzatori. Le reazioni catalizzate da enzimi sono volte più veloci.
40 Attivazione del substrato. Il ruolo del sito attivo non è solo quello di riconoscere e legare l opportuno substrato, ma è anche quello di attivare il substrato. 1) Il cambiamento nella conformazione dell enzima, indotto dal legame iniziale del substrato al sito attivo, causa non solo una migliore complementarietà e un più stretto adattamento E-S, ma anche distorce 1 o più legami del substrato indebolendoli e rendendoli più suscettibili all attacco catalitico. 2) L Enzima può anche accettare o donare protoni, aumentando la reattività chimica del substrato. 3) Gli Enzimi possono anche accettare o donare e -, formando in tal modo legami covalenti temporanei tra E e S.
La capacità di usare energia è caratteristica dei sistemi viventi
 La capacità di usare energia è caratteristica dei sistemi viventi Bisogni degli esseri viventi Energia (luce, molecole organiche) Catalizzatori biologici (enzimi) La termodinamica studia i flussi/trasformazioni
La capacità di usare energia è caratteristica dei sistemi viventi Bisogni degli esseri viventi Energia (luce, molecole organiche) Catalizzatori biologici (enzimi) La termodinamica studia i flussi/trasformazioni
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Termodinamica ENTALPIA...6
 Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Lo scopo della biochimica è la comprensione della vita in termini molecolari.
 Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Capitolo 5 L energia e il trasporto
 Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Introduzione allo studio del metabolismo Parte I
 Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO
 L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Fonte diretta di Energia è l ATP.
 Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti
 ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
B. Classificazione degli organismi 1. Autotrofi - si nutrono da soli a. ottengono il carbonio dalla CO 2 b. fonte di energia - fotosintetica: uso
 Outline Classificazione degli organismi Energia e metabolismo Energia libera Composti ad alta energia Ossidazione, riduzione e trasferimento energetico Ruolo degli enzimi Introduzione A. La vita è organica
Outline Classificazione degli organismi Energia e metabolismo Energia libera Composti ad alta energia Ossidazione, riduzione e trasferimento energetico Ruolo degli enzimi Introduzione A. La vita è organica
Enzimi: catalizzatori biologici
 Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Il metabolismo cellulare
 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. a.a
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Introduzione al Metabolismo
 Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Il paradosso (termodinamico) degli organismi viventi e la soluzione bioenergetica
 Università di Modena & Reggio Emilia DIPARTIMENTO di BIOLOGIA ANIMALE Laboratorio di Biochimica Il paradosso (termodinamico) degli organismi viventi e la soluzione bioenergetica Nicola Volpi, Prof. Associato
Università di Modena & Reggio Emilia DIPARTIMENTO di BIOLOGIA ANIMALE Laboratorio di Biochimica Il paradosso (termodinamico) degli organismi viventi e la soluzione bioenergetica Nicola Volpi, Prof. Associato
Le reazioni chimiche biologiche e gli enzimi
 Le reazioni chimiche biologiche e gli enzimi LEZIONE NR. 6 - PSICOBIOLOGIA Le reazioni chimiche consistono in interazioni interatomiche che si svolgono a livello dei loro orbitali, e quindi differenti
Le reazioni chimiche biologiche e gli enzimi LEZIONE NR. 6 - PSICOBIOLOGIA Le reazioni chimiche consistono in interazioni interatomiche che si svolgono a livello dei loro orbitali, e quindi differenti
Termodinamica dei sistemi biologici
 Bioenergetica Termodinamica dei sistemi biologici La bioenergetica è lo studio quantitativo delle trasduzioni energetiche, cioè dei cambiamenti di energia da una forma ad un altra Le trasformazioni biologiche
Bioenergetica Termodinamica dei sistemi biologici La bioenergetica è lo studio quantitativo delle trasduzioni energetiche, cioè dei cambiamenti di energia da una forma ad un altra Le trasformazioni biologiche
La materia vivente è costituita da un numero relativamente piccolo di elementi
 La materia vivente è costituita da un numero relativamente piccolo di elementi Circa il 98% : C, N, O, Ca, H, P,K, S Circa il 70 % è Acqua La prima evidenza fossile risale a circa 3,5 miliardi di anni
La materia vivente è costituita da un numero relativamente piccolo di elementi Circa il 98% : C, N, O, Ca, H, P,K, S Circa il 70 % è Acqua La prima evidenza fossile risale a circa 3,5 miliardi di anni
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
G i l i A ut u otro r fi G i l i E t E ero r tro r fi I F ototro r fi I C he h mo m tro r fi i us u a s no C e h moete t ro r tr t o r fi
 Organismi differenti utilizzano differenti modalità per ottenere carbonio ed energia: carbonio: Gli Autotrofi usano CO 2 Gli Eterotrofi usano carbonio organico energia: I Fototrofi usano la luce I Chemotrofi
Organismi differenti utilizzano differenti modalità per ottenere carbonio ed energia: carbonio: Gli Autotrofi usano CO 2 Gli Eterotrofi usano carbonio organico energia: I Fototrofi usano la luce I Chemotrofi
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed.
 Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Energia di attivazione
 Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
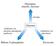 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE
 BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi
 Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
La catalisi enzimatica. Copyright 2013 Zanichelli editore S.p.A.
 La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Concetti chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Concetti chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Cinetica Chimica. Cinetica chimica
 Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia
 I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana
 la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana Forme di energia L energia è la capacità di trasferire calore o compiere un lavoro.
la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana Forme di energia L energia è la capacità di trasferire calore o compiere un lavoro.
Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la
 Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica
 Brevetti Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Committente:
Brevetti Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Committente:
CHIUSO: scambia con. solo energia. ENERGIA IN TRANSITO tra SISTEMA e AMBIENTE. POSITIVO Il sistema assorbe calore dall ambiente
 Analisi quantitativa delle modalità con cui gli organismi ottengono, incanalano e utilizzano l ENERGIA ISOLATO : non scambia né energia né materia con l ambiente CALORE (q) LAVORO (w) CHIUSO: scambia con
Analisi quantitativa delle modalità con cui gli organismi ottengono, incanalano e utilizzano l ENERGIA ISOLATO : non scambia né energia né materia con l ambiente CALORE (q) LAVORO (w) CHIUSO: scambia con
Proprietà di permeabilità della membrana
 Proprietà di permeabilità della membrana Il Trasporto attraverso le membrane La fase lipidica delle membrane le rende impermeabili alla maggior parte degli ioni e delle sostanze polari. Questi composti
Proprietà di permeabilità della membrana Il Trasporto attraverso le membrane La fase lipidica delle membrane le rende impermeabili alla maggior parte degli ioni e delle sostanze polari. Questi composti
INTRODUZIONE ALLA BIOCHIMICA
 INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
Organismi viventi ed energia
 Termodinamica ORGANISMI VIVENTI ED ENERGIA...2 Primo principio della termodinamica...5 Secondo principio della termodinamica...6 energia libera di Gibbs (G)...9 Variazione di energia libera in una reazione
Termodinamica ORGANISMI VIVENTI ED ENERGIA...2 Primo principio della termodinamica...5 Secondo principio della termodinamica...6 energia libera di Gibbs (G)...9 Variazione di energia libera in una reazione
Limiti del criterio della variazione entropia
 Limiti del criterio della variazione entropia S universo = S sistema + S ambiente > 0 (nei processi irreversibili) S universo = S sistema + S ambiente = 0 (nei processi reversibili) Dalla valutazione di
Limiti del criterio della variazione entropia S universo = S sistema + S ambiente > 0 (nei processi irreversibili) S universo = S sistema + S ambiente = 0 (nei processi reversibili) Dalla valutazione di
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono:
 Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Termodinamica. Scienza che studia le relazioni tra il calore e le altre forme di energia coinvolte in un processo fisico o chimico
 Termodinamica Scienza che studia le relazioni tra il calore e le altre forme di energia coinvolte in un processo fisico o chimico La termodinamica fa uso di modelli astratti per rappresentare sistemi e
Termodinamica Scienza che studia le relazioni tra il calore e le altre forme di energia coinvolte in un processo fisico o chimico La termodinamica fa uso di modelli astratti per rappresentare sistemi e
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
IL METABOLISMO ENERGETICO
 IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
Energia e trasformazioni spontanee
 Energia e trasformazioni spontanee Durante le trasformazioni (sia chimiche che fisiche) la materia acquista o cede energia. La termodinamica è quella scienza che studia le variazioni di energia in una
Energia e trasformazioni spontanee Durante le trasformazioni (sia chimiche che fisiche) la materia acquista o cede energia. La termodinamica è quella scienza che studia le variazioni di energia in una
I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente
 I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente regolata, detta metabolismo dell organismo. Questa rete
I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente regolata, detta metabolismo dell organismo. Questa rete
Il metabolismo microbico
 Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
Dinamica delle reazioni chimiche (attenzione: mancano i disegni)
 Dinamica delle reazioni chimiche (attenzione: mancano i disegni) Primo principio della termodinamica L energia non si può creare o distruggere, ma solo convertire da una forma all altra. Questo significa
Dinamica delle reazioni chimiche (attenzione: mancano i disegni) Primo principio della termodinamica L energia non si può creare o distruggere, ma solo convertire da una forma all altra. Questo significa
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
Prof. Giorgio Sartor. Il metabolismo. Metabolismo. È il processo che permette di ricavare energia da legami chimici (sottoforma di
 Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Capitolo 16 L energia si trasferisce
 Capitolo 16 L energia si trasferisce 1. L «ABC» dei trasferimenti energetici 2. Le reazioni scambiano energia con l ambiente 3. Durante le reazioni varia l energia chimica del sistema 4. L energia chimica
Capitolo 16 L energia si trasferisce 1. L «ABC» dei trasferimenti energetici 2. Le reazioni scambiano energia con l ambiente 3. Durante le reazioni varia l energia chimica del sistema 4. L energia chimica
Il ciclo di Krebs e la fosforilazione ossidativa
 Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
Il ciclo di Krebs e la fosforilazione ossidativa La respirazione cellulare Sono i processi molecolari in cui è coinvolto il consumo di O 2 e la formazione di CO 2 e H 2 O da parte della cellula. E suddivisa
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
FATTORI DI CRESCITA COME MESSAGGERI
 RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
COMPOSTI AD ALTA ENERGIA
 MPSTI AD ALTA ENERGIA ENTALPIA: misura della variazione di energia di una reazione condotta a pressione costante H = E + P V ENTRPIA: misura del grado di disordine S = k lnw (k=cos di Boltzmann, cioè la
MPSTI AD ALTA ENERGIA ENTALPIA: misura della variazione di energia di una reazione condotta a pressione costante H = E + P V ENTRPIA: misura del grado di disordine S = k lnw (k=cos di Boltzmann, cioè la
