La Fisica Applicata ai Beni Culturali: l'effetto fotoelettrico per l'analisi non distruttiva di campioni di interesse storico-artistico
|
|
|
- Gabriella Pozzi
- 6 anni fa
- Visualizzazioni
Transcript
1 La Fisica Applicata ai Beni Culturali: l'effetto fotoelettrico per l'analisi non distruttiva di campioni di interesse storico-artistico Giovanni BUCCOLIERI Università del SALENTO
2 L effetto fotoelettrico (Einstein -1905) Un raggio di luce consiste di piccoli pacchetti di energia chiamati quanti di luce o fotoni. L energia di un fotone è proporzionale alla sua frequenza secondo la relazione: E=h h costante di Planck (6, J s). Quando un fotone interagisce con la materia può trasferire la sua energia ad un elettrone: parte di tale energia, indicata con, viene utilizzata dall elettrone per vincere le forze che lo tengono legato e la rimanente costituisce l energia cinetica dell elettrone rimosso. Energia del fotone = h = + ½ m e v 2 Questo significa che il processo può avvenite a patto che: h >
3 Effetto fotoelettrico Se h >, aumentando la frequenza della luce gli elettroni che vengono emessi hanno energie cinetiche maggiori: ½ m e v 2 = h - = h -h 0 = h ( - 0 ) L energia cinetica degli elettroni espulsi varia linearmente con la frequenza della radiazione incidente. I metalli che cedono più facilmente elettroni sono i metalli alcalini (I gruppo). La luce rossa, avendo elevata lunghezza d onda (bassa frequenza) produce effetto fotoelettrico nel rubidio (Rb) ma non nel sodio (Na).
4 Effetto fotoelettrico Aumentando l energia della luce con cui illumino il campione è possibile rimuovere elettroni con energia di legame maggiore! Cosa accade se uso luce ad energia ben più elevata di quella visibile?
5 Osservare un oggetto Luce visibile occhio Oggetto
6 Osservare un oggetto Luce non visibile Altro sistema di rivelazione Oggetto
7 Osservare con raggi X I raggi X sono radiazioni elettromagnetiche con energia comprese tra alcuni ev (ev=elettronvolt) e circa 100 kev. L elettronvolt rappresenta l unità di misura dell energia (lavoro) più usata in fisica delle radiazioni. Un ev è uguale al lavoro compiuto su una particella di carica e (carica dell elettrone C) quando viene spostata tra due punti la cui differenza di potenziale è pari ad 1 Volt. 1eV= J I raggi X sono prodotti dall interazione con la materia di elettroni (o particelle cariche in generale) o fotoni (luce).
8 Lo spettro elettromagnetico
9 Tubo a raggi X
10 Interazione tra materia ed elettroni accelerati Produzione di raggi X Meccanismi attraverso i quali l elettrone perde energia: 1. l elettrone eccita un atomo della sostanza colpita spostando un elettrone su un orbitale ottico. L atomo torna poi allo stato fondamentale con emissione di radiazione nel visibile (perdita di energia di qualche ev); 2. l elettrone ionizza l atomo rimuovendo un elettrone esterno (perdita di energia di centinaia di ev); 3. l elettrone interagisce con un elettrone interno della sostanza colpita (shell K o L) con relativa espulsione di quest ultimo (con energia cinetica E C ). Se W KL indica l energia di legame dell elettrone all orbita K o L, l energia richiesta per il processo è E C +W KL. Un elettrone più esterno va a sostituire quello espulso con emissione della radiazione caratteristica della sostanza colpita; 4. l elettrone interagisce con il nucleo atomico: in questo caso l elettrone orbita parzialmente intorno al nucleo e perde energia per decelerazione con produzione di una banda di lunghezza d onda continuamente variabile il cui limite inferiore è determinato dalla energia degli elettroni incidenti (bremsstrahlung). Quando dei fotoni interagiscono la materia i fenomeni 1, 2 e 3 continuano a verificarsi (interazione luce - materia)
11 Conteggi Spettro prodotto da un tubo a raggi X con anodo di tungsteno alimentato a 80 kv W-L 8.4 kev W-L 9.8 kev W-K kev W-K kev Energia (kev)
12 Atomo tungsteno
13 Label Orbital ev K 1s L I 2s L II 2p 1/ L III 2p 3/ M I 3s 2820 M II 3p 1/ M III 3p 3/ M IV 3d 3/ M V 3d 5/ N I 4s N II 4p 1/ N III 4p 3/ N IV 4d 3/ N V 4d 5/ N VI 4f 5/ N VII 4f 7/ O I 5s 75.6] O II 5p 1/ O III 5p 3/2 36.8
14 Fluorescenza a raggi X I raggi X, se di sufficiente energia, possono interagire con la materia rimuovendo elettroni interni (shell K, L o M) Fotoelettrone Fotoelettr one Radiazione incidente
15 Fluorescenza a raggi X L elettrone rimosso è poi sostituito da uno più esterno. Tale processo è accompagnato dall emissione di un fotone caratteristico dell atomo bersaglio
16 Elemento Simbolo Energia (kev) Zolfo S 2.3 Cloro Cl 2.6 Argon Ar 2.9 Calcio Ca Titanio Ti Cromo Cr Manganese Mn Ferro Fe Cobalto Co Nichel Ni Rame Cu Zinco Zn Arsenico As Mercurio Hg Piombo Pb Argento Ag Stagno Sn Oro Au Righe di emissione di alcuni elementi
17
18
19
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Un nuovo spettrometro XRF portatile: prima applicazione a un bronzo dorato del Battistero di Firenze
 Un nuovo spettrometro XRF portatile: prima applicazione a un bronzo dorato del Battistero di Firenze A. Migliori a,b, P. Bonanni a, L. Carraresi a, N. Grassi a, P.A. Mandò a a Dipartimento di Fisica dell
Un nuovo spettrometro XRF portatile: prima applicazione a un bronzo dorato del Battistero di Firenze A. Migliori a,b, P. Bonanni a, L. Carraresi a, N. Grassi a, P.A. Mandò a a Dipartimento di Fisica dell
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
LEGAME METALLICO PROPRIETA METALLICHE NON METALLI SEMIMETALLI METALLI
 LEGAME METALLICO LEGAME METALLICO NON METALLI PROPRIETA METALLICHE Elevata conducibilità elettrica ( 1/ T) Bassa energia di ionizzazione Elevata duttilità e malleabilità Non trasparenza Lucentezza Strutture
LEGAME METALLICO LEGAME METALLICO NON METALLI PROPRIETA METALLICHE Elevata conducibilità elettrica ( 1/ T) Bassa energia di ionizzazione Elevata duttilità e malleabilità Non trasparenza Lucentezza Strutture
Elettronica II Legame covalente e bande di energia nei solidi p. 2
 Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Elettronica II Legame covalente e bande di energia nei solidi Valentino Liberali Dipartimento di Tecnologie dell Informaione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Chimica. 1) Il simbolo del Carbonio è: A) C B) Ca. C) Ce D) Cu. 2) Secondo il principio della conservazione della materia:
 Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Il progetto di biomonitoraggio ambientale con le api all interno del Parco Nazionale della Majella: risultati sui metalli pesanti
 Il progetto di biomonitoraggio ambientale con le api all interno del Parco Nazionale della Majella: risultati sui metalli pesanti Dott. Alessandro Ubaldi Istituto Zooprofilattico Sperimentale delle Regioni
Il progetto di biomonitoraggio ambientale con le api all interno del Parco Nazionale della Majella: risultati sui metalli pesanti Dott. Alessandro Ubaldi Istituto Zooprofilattico Sperimentale delle Regioni
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
La Teoria dei Quanti e la Struttura Elettronica degli Atomi. Capitolo 7
 La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
3. Strumenti di misura Misura del ph/carta
 . Strumenti di Misura del /Carta GENERAL CATALOGUE EDITION 8 LLG-Cartina indicatrice universale di, rotolo Per la determinazione dei valori di. Rocchetto dispensatore in plastica con rotolo da m. - - 9.9
. Strumenti di Misura del /Carta GENERAL CATALOGUE EDITION 8 LLG-Cartina indicatrice universale di, rotolo Per la determinazione dei valori di. Rocchetto dispensatore in plastica con rotolo da m. - - 9.9
Energia elettrica. L atomo nel suo complesso è neutro perché ha l equilibrio tra protoni ed elettroni presenti nello stesso numero.
 Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Struttura Elettronica degli Atomi
 Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Na (T 1/2 =15 h), che a sua volta decade β - in 24 12
 Esercizio 1 Il 24 10 Ne (T 1/2 =3.38 min) decade β - in 24 11 Na (T 1/2 =15 h), che a sua volta decade β - in 24 12 Mg. Dire quali livelli sono raggiungibili dal decadimento beta e indicare lo schema di
Esercizio 1 Il 24 10 Ne (T 1/2 =3.38 min) decade β - in 24 11 Na (T 1/2 =15 h), che a sua volta decade β - in 24 12 Mg. Dire quali livelli sono raggiungibili dal decadimento beta e indicare lo schema di
Le particelle dell atomo
 La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
03 - Unità di misura, tabelle di conversione
 0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Gli elementi di transizione
 Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
MICRONUTRIENTI. Oligoelementi. Macroelementi. Ca= Calcio Mg= Magnesio P= Fosforo Na= Sodio Cl= Cloro K= Potassio S= Zolfo

Facoltà di Medicina e Chirurgia. Corso di Diagnostica per Immagini
 Facoltà di Medicina e Chirurgia Corso di Diagnostica per Immagini I raggi X sono onde elettromagnetiche la cui lunghezza d'onda è molto più piccola di quella delle radiazioni visibili. Furono scoperti
Facoltà di Medicina e Chirurgia Corso di Diagnostica per Immagini I raggi X sono onde elettromagnetiche la cui lunghezza d'onda è molto più piccola di quella delle radiazioni visibili. Furono scoperti
U.M.A. e le masse ATOMICHE
 U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO INTERAZIONI TRA RADIAZIONI E MATERIA Quando una radiazione elettromagnetica interagisce con la materia, può verificarsi un trasferimento di energia dalla radiazione
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO INTERAZIONI TRA RADIAZIONI E MATERIA Quando una radiazione elettromagnetica interagisce con la materia, può verificarsi un trasferimento di energia dalla radiazione
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA
 ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
11 Spettroscopia di fluorescenza ai raggi X SKOOG et al. Cap.12(12A,12B,12C), Cap.4(4C-7) RUBINSON et al. Cap.9(9C)
 11 Spettroscopia di fluorescenza ai raggi X SKOOG et al. Cap.12(12A,12B,12C), Cap.4(4C-7) RUBINSON et al. Cap.9(9C) 11.1. Principi della spettroscopia di fluorescenza ai raggi X (XRF) La spettroscopia
11 Spettroscopia di fluorescenza ai raggi X SKOOG et al. Cap.12(12A,12B,12C), Cap.4(4C-7) RUBINSON et al. Cap.9(9C) 11.1. Principi della spettroscopia di fluorescenza ai raggi X (XRF) La spettroscopia
Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici.
 I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
La tavola periodica. 1- Introduzione
 La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
SCHEDE TECNICHE fornitura prodotti chimici e reagenti
 SCHEDE TECNICHE fornitura prodotti chimici e reagenti SCHEDA TECNICA N. 1 IPOCLORITO DI SODIO al 14,5-15% (come cloro attivo) Aspetto: liquido Colore: giallo paglierino Odore: caratteristico Densità a
SCHEDE TECNICHE fornitura prodotti chimici e reagenti SCHEDA TECNICA N. 1 IPOCLORITO DI SODIO al 14,5-15% (come cloro attivo) Aspetto: liquido Colore: giallo paglierino Odore: caratteristico Densità a
Risultati della caratterizzazione dei fumi
 Progetto Produzione di energia e sostanza organica dai sottoprodotti del vigneto Risultati della caratterizzazione dei fumi Paolo Giandon ARPAV Dipartimento Provinciale di Treviso Biella, 24 settembre
Progetto Produzione di energia e sostanza organica dai sottoprodotti del vigneto Risultati della caratterizzazione dei fumi Paolo Giandon ARPAV Dipartimento Provinciale di Treviso Biella, 24 settembre
Natura della luce. Qualsiasi tipo di onda è caratterizzato da:
 Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
PARTE SESTA. Le modificazioni fisiche all interno della materia irradiata
 PARTE SESTA Le modificazioni fisiche all interno della materia irradiata 135 INTRODUZIONE ALLA BIOFISICA DELLE RADIAZIONI Tavola VI Cinetica di dissociazione radioindotta delle basi A e T nella doppia
PARTE SESTA Le modificazioni fisiche all interno della materia irradiata 135 INTRODUZIONE ALLA BIOFISICA DELLE RADIAZIONI Tavola VI Cinetica di dissociazione radioindotta delle basi A e T nella doppia
TECNICHE SPETTROSCOPICHE PER I BENI CULTURALI: SPETTROMETRIA DI FLUORESCENZA X
 Dipartimento di Scienze Chimiche TECNICHE SPETTROSCOPICHE PER I BENI CULTURALI: SPETTROMETRIA DI FLUORESCENZA X Analisi superficiali via XRF: Le misure sono effettuate in tempi dell ordine di qualche centinaio
Dipartimento di Scienze Chimiche TECNICHE SPETTROSCOPICHE PER I BENI CULTURALI: SPETTROMETRIA DI FLUORESCENZA X Analisi superficiali via XRF: Le misure sono effettuate in tempi dell ordine di qualche centinaio
LEZIONE 2. Configurazioni elettroniche e tavola periodica
 LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
CHIMICA ANALITICA SPETTROSCOPIA ATOMICA
 CHIMICA ANALITICA SPETTROSCOPIA ATOMICA Carlo I.G. Tuberoso Appunti didattici uso laboratorio ver. 00 La spettroscopia atomica (di assorbimento, AAS o di emissione, AES) è ancora oggi una tecnica analitica
CHIMICA ANALITICA SPETTROSCOPIA ATOMICA Carlo I.G. Tuberoso Appunti didattici uso laboratorio ver. 00 La spettroscopia atomica (di assorbimento, AAS o di emissione, AES) è ancora oggi una tecnica analitica
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Laboratorio Biomasse - Elenco delle analisi
 Laboratorio Biomasse - Elenco delle analisi 1 - Analisi per la caratterizzazione energetica e chimico-fisica dei materiali 1.1 - Biomasse solide * 1 Umidità CEN/TS 14774 Ceneri a 550 C CEN/TS 14775 Potere
Laboratorio Biomasse - Elenco delle analisi 1 - Analisi per la caratterizzazione energetica e chimico-fisica dei materiali 1.1 - Biomasse solide * 1 Umidità CEN/TS 14774 Ceneri a 550 C CEN/TS 14775 Potere
Il metodo scientifico
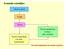 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
LEZIONE 2 ( Interazione delle particelle con la materia)
 LEZIONE 2 ( Interazione delle particelle con la materia) INTERAZIONE DELLE RADIAZIONI FOTONICHE La materia viene ionizzata prevalentemente ad opera degli elettroni secondari prodotti a seguito di una interazione
LEZIONE 2 ( Interazione delle particelle con la materia) INTERAZIONE DELLE RADIAZIONI FOTONICHE La materia viene ionizzata prevalentemente ad opera degli elettroni secondari prodotti a seguito di una interazione
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I blocchi s, p, d ed f della Tavola Periodica
 I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietä degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietä degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
Il sistema periodico degli elementi
 Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Approccio storico-epistemologico alla tavola periodica. E. Roletto, A. Regis, CnS Chimica nella Scuola, 2004, 5, 161-171
 Approccio storico-epistemologico alla tavola periodica E. Roletto, A. Regis, CnS Chimica nella Scuola, 2004, 5, 161-171 Approccio storico-epistemologico Obiettivi dell approccio: 1) Condurre gli allievi
Approccio storico-epistemologico alla tavola periodica E. Roletto, A. Regis, CnS Chimica nella Scuola, 2004, 5, 161-171 Approccio storico-epistemologico Obiettivi dell approccio: 1) Condurre gli allievi
La tavola periodica. Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici
 La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici Si possono classificare gli elementi secondo la loro configurazione elettronica: Gas nobili. Elementi
La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici Si possono classificare gli elementi secondo la loro configurazione elettronica: Gas nobili. Elementi
ARPA FVG. Monitoraggio della qualità dell aria. Rilievi effettuati a centrale termoelettrica spenta ed accesa nel comune di Monfalcone
 Monitoraggio della qualità dell aria Rilievi effettuati a centrale termoelettrica spenta ed accesa nel comune di Monfalcone Mercoledì 19 novembre 2014 Comune di Monfalcone Durata del monitoraggio A2A FERMA
Monitoraggio della qualità dell aria Rilievi effettuati a centrale termoelettrica spenta ed accesa nel comune di Monfalcone Mercoledì 19 novembre 2014 Comune di Monfalcone Durata del monitoraggio A2A FERMA
SPETTROSCOPIA ATOMICA (estratto dal file ipertestuale distribuito a lezione) La spettroscopia atomica comprende un insieme di tecniche analitiche
 SPETTROSCOPIA ATOMICA (estratto dal file ipertestuale distribuito a lezione) La spettroscopia atomica comprende un insieme di tecniche analitiche basate sull'assorbimento, l'emissione o la fluorescenza
SPETTROSCOPIA ATOMICA (estratto dal file ipertestuale distribuito a lezione) La spettroscopia atomica comprende un insieme di tecniche analitiche basate sull'assorbimento, l'emissione o la fluorescenza
INTRODUZIONE ALLA SPETTROMETRIA
 INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
ELENCO PROVE ACCREDITATE - CATEGORIA: 0
 Scheda 1 di 5 ELENCO PROVE ACCREDITATE - CATEGORIA: 0 Acciai e Ghise non legati e legati. Alluminio, Piombo, Stagno, Titanio, Vanadio e Tungsteno mediante spettrofotometria d'assorbimento atomico nella
Scheda 1 di 5 ELENCO PROVE ACCREDITATE - CATEGORIA: 0 Acciai e Ghise non legati e legati. Alluminio, Piombo, Stagno, Titanio, Vanadio e Tungsteno mediante spettrofotometria d'assorbimento atomico nella
4) 8 g di idrogeno reagiscono esattamente con 64 g di ossigeno secondo la seguente reazione:
 Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Esercizi Gli esercizi sulla legge di Lavoisier che seguono si risolvono ricordando che la massa iniziale, prima della reazione, deve equivalere a quella finale, dopo la reazione. L uguaglianza vale anche
Da Newton a Planck. La struttura dell atomo. Da Newton a Planck. Da Newton a Planck. Meccanica classica (Newton): insieme
 Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Laboratorio di sistemi 3 A Meccanica Energia. Resistività ρ Resistori e resistenza elettrica Ω
 Laboratorio di sistemi 3 A Meccanica Energia Resistività ρ Resistori e resistenza elettrica Ω Resistività elettrica La resistività elettrica (ρ), anche detta resistenza elettrica specifica, è l'attitudine
Laboratorio di sistemi 3 A Meccanica Energia Resistività ρ Resistori e resistenza elettrica Ω Resistività elettrica La resistività elettrica (ρ), anche detta resistenza elettrica specifica, è l'attitudine
23/03/2016. Signature Not Verified. Firma Digitale. a cura del servizio prelevatore. Dati Anagrafici. Accettazione a cura dello Sportello di: BOLOGNA
 Sezione Provinciale di Bologna Laboratorio Integrato Resp.: Dott.ssa Maria Antonietta Bucci Sabattini via F.Rocchi,19 40138 Bologna tel. 051.396211 fax. 051.342642 e-mail aoobo@cert.arpa.emr.it Signature
Sezione Provinciale di Bologna Laboratorio Integrato Resp.: Dott.ssa Maria Antonietta Bucci Sabattini via F.Rocchi,19 40138 Bologna tel. 051.396211 fax. 051.342642 e-mail aoobo@cert.arpa.emr.it Signature
La quantità chimica LA MOLE
 La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
30.7.2008 Gazzetta ufficiale dell Unione europea L 201/37
 30.7.2008 Gazzetta ufficiale dell Unione europea L 201/37 ALLEGATO «Bosnia-Erzegovina Nota: in virtù dell'articolo 1 del presente regolamento, l'articolo 18 del regolamento (CE) n. 1013/2006 si applica
30.7.2008 Gazzetta ufficiale dell Unione europea L 201/37 ALLEGATO «Bosnia-Erzegovina Nota: in virtù dell'articolo 1 del presente regolamento, l'articolo 18 del regolamento (CE) n. 1013/2006 si applica
26/10/2012. Onde elettromagnetiche. b) proprietà periodiche C) configurazione elettronica. f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν
 Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
Onde elettromagnetiche Struttura atomica: a) riempimento orbitali b) proprietà periodiche C) configurazione elettronica ONDE onde armoniche f(x,t)=a sin(kx+ωt+φ) k=2π/λ; ω=2π/t= 2πν Energia di un fotone
Prove di combustione
 Giornata Dimostrativa del Progetto BioTec Analisi delle tecniche di combustione e ricerca sui processi di produzione di biocombustibili da biomasse agro-forestali Prove di combustione Andrea Cristoforetti
Giornata Dimostrativa del Progetto BioTec Analisi delle tecniche di combustione e ricerca sui processi di produzione di biocombustibili da biomasse agro-forestali Prove di combustione Andrea Cristoforetti
STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO
 UNIVERSITA CA FOSCARI VENEZIA DIPARTIMENTO DI SCIENZE AMBIENTALI STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO Prof. Rampazzo Giancarlo CHE COS E LA GEOCHIMICA 1.La geochimica studia la composizione chimica
UNIVERSITA CA FOSCARI VENEZIA DIPARTIMENTO DI SCIENZE AMBIENTALI STUDIO GEOCHIMICO DEL PARTICOLATO ATMOSFERICO Prof. Rampazzo Giancarlo CHE COS E LA GEOCHIMICA 1.La geochimica studia la composizione chimica
Galvanostegia. Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo
 Galvanostegia Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo Che cos è la Galvanostegia? Un processo elettrochimico in cui
Galvanostegia Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo Che cos è la Galvanostegia? Un processo elettrochimico in cui
IL MODELLO ATOMICO DI BOHR
 IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
Istituzioni di fisica della materia I Lezione 3. S. Solimeno lezione 3 1
 Istituzioni di fisica della materia I Lezione 3 S. Solimeno lezione 3 1 S. Solimeno lezione 3 2 S. Solimeno lezione 3 3 S. Solimeno lezione 3 4 S. Solimeno lezione 3 5 spettroscopia gamma di colori che
Istituzioni di fisica della materia I Lezione 3 S. Solimeno lezione 3 1 S. Solimeno lezione 3 2 S. Solimeno lezione 3 3 S. Solimeno lezione 3 4 S. Solimeno lezione 3 5 spettroscopia gamma di colori che
SPETTROFOTOMETRIA UV/VIS
 SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
Modelli atomici. Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle.
 Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
CaO+H 2 O Ca(OH) 2. metallo + ossigeno (danno origine ad idrossidi o basi per reazione con l'acqua)
 ESERCITAZINE 1 NMENCLATURA E REAZINI Esame della Tavola Periodica. Suddivisione degli elementi fra METALLI E NN METALLI e loro caratteristiche. Reazione dei metalli con ossigeno ossidi basici Reazione
ESERCITAZINE 1 NMENCLATURA E REAZINI Esame della Tavola Periodica. Suddivisione degli elementi fra METALLI E NN METALLI e loro caratteristiche. Reazione dei metalli con ossigeno ossidi basici Reazione
Le tecnologie per l acquisizione delle immagini digitali
 Le tecnologie per l acquisizione delle immagini digitali Mauro Gambaccini Dipartimento di Fisica dell Università di Ferrara Sezione INFN di Ferrara CORSO ITINERANTE DI MAMMOGRAFIA DIGITALE Udine, 27 Gennaio
Le tecnologie per l acquisizione delle immagini digitali Mauro Gambaccini Dipartimento di Fisica dell Università di Ferrara Sezione INFN di Ferrara CORSO ITINERANTE DI MAMMOGRAFIA DIGITALE Udine, 27 Gennaio
Calcolare quante moli di zinco sono contenute in 5,50 g di Zn. (Massa molare (m.m.) Zn = 65,409 g mol -1 ).
 Calcolare quante moli di zinco sono contenute in 5,50 g di Zn. (Massa molare (m.m.) Zn = 65,409 g mol -1 ). moli Zn = massa Zn / m.m. Zn = 5,50 / 65,409 g mol -1 = 8,41 10-2 mol Calcolare a quante moli
Calcolare quante moli di zinco sono contenute in 5,50 g di Zn. (Massa molare (m.m.) Zn = 65,409 g mol -1 ). moli Zn = massa Zn / m.m. Zn = 5,50 / 65,409 g mol -1 = 8,41 10-2 mol Calcolare a quante moli
CHIMICA QUANTITATIVA. Massa atomica. Unità di massa atomica. Massa molare
 CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
Unità di misura di lunghezza usate in astronomia
 Unità di misura di lunghezza usate in astronomia In astronomia si usano unità di lunghezza un po diverse da quelle che abbiamo finora utilizzato; ciò è dovuto alle enormi distanze che separano gli oggetti
Unità di misura di lunghezza usate in astronomia In astronomia si usano unità di lunghezza un po diverse da quelle che abbiamo finora utilizzato; ciò è dovuto alle enormi distanze che separano gli oggetti
FERRO E SUE LEGHE. Il Ferro (Fe) è un metallo: Duttile Malleabile Magnetizzabile Facilmente ossidabile
 FERRO E SUE LEGHE Il Ferro (Fe) è un metallo: Duttile Malleabile Magnetizzabile Facilmente ossidabile E' uno degli elementi più abbondanti della superficie terrestre. Si utilizza fin dalla preistoria.
FERRO E SUE LEGHE Il Ferro (Fe) è un metallo: Duttile Malleabile Magnetizzabile Facilmente ossidabile E' uno degli elementi più abbondanti della superficie terrestre. Si utilizza fin dalla preistoria.
TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici.
 TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici. Se per esempio, facciamo l'analisi di un oggetto di rame,
TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici. Se per esempio, facciamo l'analisi di un oggetto di rame,
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia. Francesco Nobili
 Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
Introduzione alle tecniche spettroscopiche e all interazione radiazione/materia Francesco Nobili TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tecniche analitiche basate sull interazione tra
Definizione rigorosa di Mole. Definizione rigorosa di u.m.a. = Dalton. 1 u.m.a. = 1/12 della massa di un atomo di 12 C
 Definizione rigorosa di Mole Quantità di sostanza di un sistema che contiene un numero di entità elementari pari al numero di atomi presente in 0.012 kg di carbonio(12). Quant è grande questo numero? N
Definizione rigorosa di Mole Quantità di sostanza di un sistema che contiene un numero di entità elementari pari al numero di atomi presente in 0.012 kg di carbonio(12). Quant è grande questo numero? N
STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA
 pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
La metodologia per il recupero dei Metalli Nobili dai RAEE
 Università degli Studi di Cagliari Dipartimento di Chimica Inorganica ed Analitica Dipartimento di Ingegneria Elettrica ed Elettronica Dott. Angela Serpe Prof. Paola Deplano Prof. Massimo Vanzi La metodologia
Università degli Studi di Cagliari Dipartimento di Chimica Inorganica ed Analitica Dipartimento di Ingegneria Elettrica ed Elettronica Dott. Angela Serpe Prof. Paola Deplano Prof. Massimo Vanzi La metodologia
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Laser in medicina 28/2/2004
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Laser in medicina 28/2/2004 Laser Sviluppo moderne tecniche di comunicazione fasci molto intensi di onde radio coerenti in bande di frequenza molto
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Laser in medicina 28/2/2004 Laser Sviluppo moderne tecniche di comunicazione fasci molto intensi di onde radio coerenti in bande di frequenza molto
LEZIONE 4 INTERAZIONE DEI RAGGI X E GAMMA CON LA MATERIA
 LZION 4 INTRZION DI RGGI X GMM CON L MTRI I raggi X hanno generalmente energie comprese fra i 5KeV e i 500 kev. Interagendo con la materia i raggi X (interazione primaria) producono elettroni secondari
LZION 4 INTRZION DI RGGI X GMM CON L MTRI I raggi X hanno generalmente energie comprese fra i 5KeV e i 500 kev. Interagendo con la materia i raggi X (interazione primaria) producono elettroni secondari
RAPPORTO DI PROVA N. 702/14
 Data emissione: 23 settembre 2014 Committente: RUGGERI SERVICE SpA - Strada Statale 275 Maglie Leuca, Muro Leccese(LE) Sito di provenienza: Stabilimento di Muro Leccese Matrice dichiarata: Emissioni in
Data emissione: 23 settembre 2014 Committente: RUGGERI SERVICE SpA - Strada Statale 275 Maglie Leuca, Muro Leccese(LE) Sito di provenienza: Stabilimento di Muro Leccese Matrice dichiarata: Emissioni in
Spettroscopia atomica
 Spettroscopia atomica La spettroscopia atomica è una tecnica di indagine qualitativa e quantitativa, in cui una sostanza viene decomposta negli atomi che la costituiscono tramite una fiamma, un fornetto
Spettroscopia atomica La spettroscopia atomica è una tecnica di indagine qualitativa e quantitativa, in cui una sostanza viene decomposta negli atomi che la costituiscono tramite una fiamma, un fornetto
MATERIALI METALLICI. Piombo ( Pb ) Nichel ( Ni ) al carbonio o comuni
 MATERIALI METALLICI Sono i materiali costituiti da metalli e loro leghe, ricavati dalla lavorazione di minerali attraverso dei processi metallurgici. Sono caratterizzati da una struttura chimica cristallina
MATERIALI METALLICI Sono i materiali costituiti da metalli e loro leghe, ricavati dalla lavorazione di minerali attraverso dei processi metallurgici. Sono caratterizzati da una struttura chimica cristallina
Appendice A: tabelle descrittive residenti
 Appendice A: tabelle descrittive residenti 1. PARAMETRI EMATOCHIMICI DI BASE Nelle tabelle 1-12 sono riportati in dettaglio i risultati delle analisi descrittive riguardanti i parametri ematochimici di
Appendice A: tabelle descrittive residenti 1. PARAMETRI EMATOCHIMICI DI BASE Nelle tabelle 1-12 sono riportati in dettaglio i risultati delle analisi descrittive riguardanti i parametri ematochimici di
DEFINIZIONE DI RADIANZA La radiazione è caratterizzata tramite la Radianza Spettrale, I (λ, θ, φ, T), definita come la densità di potenza per unità di
 SISTEMI PASSIVI Ogni corpo a temperatura T diversa da 0 K irradia spontaneamente potenza elettromagnetica distribuita su tutto lo spettro Attraverso un elemento da della superficie del corpo, fluisce p
SISTEMI PASSIVI Ogni corpo a temperatura T diversa da 0 K irradia spontaneamente potenza elettromagnetica distribuita su tutto lo spettro Attraverso un elemento da della superficie del corpo, fluisce p
Scheda tecnica prodotto
 Progetto: Lavello leva clinica Area di vendita: Italia Designer: / Data di lancio: Autore: MZ Revisioni 1.0 Informazioni generali 1.1 Prodotti trattati e codici 1.2 Finitura superficiale 1.3 Materiali
Progetto: Lavello leva clinica Area di vendita: Italia Designer: / Data di lancio: Autore: MZ Revisioni 1.0 Informazioni generali 1.1 Prodotti trattati e codici 1.2 Finitura superficiale 1.3 Materiali
Esperienze di caratterizzazione delle componenti inorganiche in deposizioni umide e secche nei pressi di un impianto di incenerimento
 Esperienze di caratterizzazione delle componenti inorganiche in deposizioni umide e secche nei pressi di un impianto di incenerimento Brescia, Auditorium del Museo Civico di Scienze Naturali 5 giugno 2014
Esperienze di caratterizzazione delle componenti inorganiche in deposizioni umide e secche nei pressi di un impianto di incenerimento Brescia, Auditorium del Museo Civico di Scienze Naturali 5 giugno 2014
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
Caratterizzazione chimico fisica delle biomasse legnose
 Caratterizzazione chimico fisica delle biomasse legnose Rossana Cerioni SIBE Srl Spin-Off dell Università Politecnica delle Marche BIOENERGY - Verona, 4 febbraio 2010 COMPONENTI DELLA BIOMASSA SOLIDA Aspetti
Caratterizzazione chimico fisica delle biomasse legnose Rossana Cerioni SIBE Srl Spin-Off dell Università Politecnica delle Marche BIOENERGY - Verona, 4 febbraio 2010 COMPONENTI DELLA BIOMASSA SOLIDA Aspetti
VL-4.C (*) VL-6.C (*) VL-8.C VL-115.C VL-215.C
 Lampade UV La luce ultravioletta è una parte delle radiazioni invisibili che confina con lo spettro visibile. Inizia al di là del violetto, dove termina la rivelazione all occhio umano. Lo spettro ultravioletto
Lampade UV La luce ultravioletta è una parte delle radiazioni invisibili che confina con lo spettro visibile. Inizia al di là del violetto, dove termina la rivelazione all occhio umano. Lo spettro ultravioletto
La spettroscopia di fotoemissione:
 La spettroscopia di fotoemissione: La spettroscopia di fotoemissione e' una tecnica di indagine molto usata per studiare le proprietà dei materiali, sia nell ambito della ricerca scientifica, sia in ambito
La spettroscopia di fotoemissione: La spettroscopia di fotoemissione e' una tecnica di indagine molto usata per studiare le proprietà dei materiali, sia nell ambito della ricerca scientifica, sia in ambito
grado di fornire i propri servizi Dal 1959 la ditta E.L.B.A., con grande tempestività su Emporio, Lingotto, Bronzo, tutto il territorio nazionale,
 Dal 1959 la ditta E.L.B.A., Emporio, Lingotto, Bronzo, Alluminio, inizia la commercializzazione di barre in bronzo a colata continua nella 1 sede del centro cittadino, fornendo i clienti della zona che
Dal 1959 la ditta E.L.B.A., Emporio, Lingotto, Bronzo, Alluminio, inizia la commercializzazione di barre in bronzo a colata continua nella 1 sede del centro cittadino, fornendo i clienti della zona che
