METABOLISMO DI BASI AZOTATE E NUCLEOTIDI
|
|
|
- Taddeo Lorenzo Barbato
- 5 anni fa
- Visualizzazioni
Transcript
1 METABOLISMO DI BASI AZOTATE E NUCLEOTIDI Le basi azotate si dividono in purine e pirimidine. Le purine sono l adenina e la guanina. La xantina e la ipoxantina sono considerati due intermedi della sintesi dell adenina e guanina. Le pirimidine sono invece l uracile, la citosina e la timina. I nucleosidi sono costituita dalle basi azotate legate a uno zucchero, il ribosio. Purinici Pirimidinici 112
2 I nucleotidi sono molecole costitute invece da una base azotata, uno zucchero (il ribosio o il desossiribosio) e i gruppi fosfati (massimo 3). NUCLEOTIDI La biosintesi dei nucleotidi può procedere attraverso due processi che avvengono nel citoplasma: 1. Sintesi de novo: combinando insieme i vari precursori si sintetizza l intero nucleotide. I precursori nella sintesi de novo sono la CO 2, l NH 3, gli amminoacidi glicina (essenziale per la sintesi delle purine), aspartato (essenziale per la sintesi delle pirimidine), glutammina (partecipa a entrambe le vie metaboliche donando il gruppo ammidico); il ribosio 5- fosfato derivante dalla via dei pentosi. Il ribosio 5-fosfato deve essere attivato nel composto 5-fosforibosil-1-pirofosfato (PRPP). Questa reazione reazione è catalizzata dalla PRPP sintetasi e il pirofosfato è donato da una molecola di ATP. La disponibilità di questo composto e del fosfato inorganico determina la velocità della sintesi dei vari nucleotidi. Gli inibitori competitivi di questa via metabolica sono l ADP e il 2,3-bisfosfoglicerato che competono per ATP e ribosio 5-fosfato. ciclo dei pentosi PRPP sintetasi I livelli di PRPP sono bassi in cellule confluenti quando non si dividono e aumentano rapidamente all entrata nel ciclo cellulare. Questo enzima può essere mutato e causare la malattia di von Gierke (deficit di glucosio 6- fosfato fosfatasi; aumento della PRPP, aumento della purine; iperuricemia e acidosi lattica). 2. Vie di salvataggio: riciclano le basi azotate e i nucleotidi che sono resi disponibili dal catabolismo degli acidi nucleici. Il 5-fosforibosil-1-pirofosfato 113
3 Sintesi de novo delle purine La sintesi de novo delle purine include dieci reazioni che portano alla sintesi di nucleotidi monofosfato, AMP e GMP. Si parte dal ribosio attivato (PPRP) e sono aggiunti sullo zucchero tutti i gruppi che formeranno l anello delle purine. Una volta formato l anello si ottiene l inosinato (IMP), dal quale verranno sintetizzati successivamente AMP e GMP. Buchanan ha identifato l origine di tutti gli atomi che compongono l anello aromatico. La glicina fornisce la maggior parte di atomi. 8/61 1. Commiting step: il ribosio amminato è indirizzato alla sintesi delle purine tramite la glutammina- PRPP amidotransferasi. È il principale sito di regolazione della sintesi de novo. L amminazione avviene sul carbonio anomerico dello zucchero con rimozione del pirofosfato. Si ottiene una 5-fosfo-β-D -ribosilammina. 114
4 2. Entra la glicina attraverso la GAR sintetasi (enzima trifunzionale) e si forma il glicinammide ribonucleotide (GAR). Viene consumata ATP e inserita la glicina. (trifunctional protein) 3. Viene aggiunto un terzo carbonio sotto forma di formile ceduto dal tetraidrofolato tramite la GAR transformilasi e si ottiene la formilglinamide ribonucleotide (FGAR). protein) (trifunctional protein) 4. Interviene ora una ammidotransferasi che inserisce il gruppo ammidico, preso dalla glutammina entrante, sul gruppo carbossilico della glicina del FGAR. Si è formata la formilglicinamidine ribonucleotide (FGAM). (trifunctional protein) 115
5 5. Avviene la ciclizzazione: si chiude il primo anello, l imidazolo. Si forma il 5-aminoimidazolo ribonucleotide (AIR). 6. Sull AIR avviene una carbossilazione, ovvero viene inserito un gruppo carbossilico fornito dall anidride carbonica. Il composto ottenuto è un imidazolo con gruppo carbossilico e amminico, il carbossiamino-imidazolo ribonucleotide (CAIR). 7. Entra in gioco l aspartato che dona il gruppo amminico. Le reazioni che avvengono sono uguali a quelle avvenute nel ciclo dell urea. Su questo composto si inserisce l aspartato per intero. Il gruppo amminico dell aspartato reagisce con il gruppo carbossilico appena inserito. Si forma il N Succinil-5-amonoimidasolo-4-carbossamide ribonucleotide (SAICAR). 116
6 8. Lo scheletro carbonioso dell aspartato viene rimosso da una liasi ed esce come fumarato. Si ottiene il composto 5-aminoimidazole-4-carboammide ribonucleotide (AICAR). 9. Viene inserito un ultimo C sotto forma di formile donato dall N 10 formile tetraidrofolato. Si è formato il N-formiaminoimidazolo-4-carbossamide ribonucleotide. 10. Il secondo anello si ciclizza e si forma l inosinato (IMP). Viene sintetizzato il primo nucleotide purinico come nucleotide monofosfato. 117
7 L inositato è il precursore della sintesi di AMP e GMP attraverso due reazioni. Dall inositato si ha una biforcazione. Sintesi di AMP Bisogna sostituire il chetone dell IMP con un ammina. L azoto per l ammina viene donato dall aspartato con lo stesso meccanismo del ciclo dell urea. 1. L enzima adenilosuccinato sintetasi lega l aspartato al carbonio chetonico dell IMP e si forma l adenilosuccinato. Questa reazione richiede energia. Il nucleotide trifosfato usato è il GTP. 2. L enzima adenilato liasi rimuove lo scheletro carbonioso dell aspartato che esce come fumarato. Si produce così adenilato (AMP). Sintesi di GMP Il guanilato contiene un gruppo ammidico. 1. Viene introdotto un gruppo chetonico per formare il nucleotide xantilato (XMP). Si impiega NAD + per ossidare, che diventa NADH, e H 2 O per ottenere il gruppo chetonico. 2. Il chetone viene dunque sostituito da una ammina. Il donatore di questo gruppo ammidico è la glutammina. La reazione è catalizzata dalla xantilato-glutammina amidotransferasi. È richiesta energia tramite l ATP. Si produce così il guanilato (GMP). Regolazione della sintesi delle purine Questa via metabolica viene regolata da una regolazione allosterica retroattiva sequenziale perché si ha prima la sintesi di un intermedio comune, IMP, e poi la sintesi di AMP e GMP (i veri nucleotidi finali). È importante che la disponibilità di nucleotidi sia bilanciata. L AMP o il GMP inibisce la sua stessa sintesi quando la sua quantità è sufficiente. Contemporaneamente questi due nucleotidi inibiscono la glutammina PRPP ammidotransferasi che porta alla sintesi di IMP. L IMP inibisce a sua volta la glutammina PRPP ammidotransferasi. Per bloccare completamente l enzima sono necessari tutti i composti (GMP, AMP e IMP), se è presente solo IMP l enzima rallenta solamente. 118
8 L AMP per diventare un nucleotide da inserire nel DNA o RNA deve essere fosforilato. Il primo passaggio è la sua fosforilazione da AMP a ADP. La produzione di grandi quantità di ADP inibisce la sintesi di ribosio 5-fosfato. L ADP segnala l adeguata quantità di purine a disposizione. Sintesi de novo delle pirimidine Per la loro sintesi prima vien costruita la base azotata che ha una struttura molto più semplice delle purine. L aspartato costituisce più della metà dell anello fornendo gli atomi , l azoto è fornito dalla glutammina e l altro atomo di carbonio da HCO 3. Una volta sintetizzato è coniugato con PRPP. I prodotti ottenuti sono nucleotidi trifosfato. Verrà sintetizzata una prima base azotata intermedia che sarà poi modificata. 1. La carbamilfosfato sintetasi II (CPS II) catalizza la reazione che produce carbamilfosfato a partire dalla glutammina. La CPS II è un isoforma presente nel citosol delle cellule. Essa non sa usare ione ammonio libero, ma glutammina che cede il gruppo ammidico alla CO 2. Questo enzima è inibito da UTP e attivato da ATP. Sono quindi inseriti i primi due atomi di carbonio che faranno parte dell anello delle basi pirimidiniche. 119
9 2. Viene inserito l aspartato sul carbamilfosfato tramite l enzima aspartato transcarbamoilasi. Si ottiene il N-carbamoilaspartato. 3. L anello si ciclizza tramite l enzima didroorotasi. Si forma il legame fra gruppo amminico e carbossilico e si chiude l anello. Si forma così il L-diidroorato. 4. Viene inserita l insaturazione tramite una diidrorato deidrogenasi che trasforma un legame singolo in un legame doppio usando il NAD per produrre NADH. Si ottiene orato o acido orotico. 5. La base azotata viene coniugata con il PRPP e si ottiene il nucleotide monofosfato orotidilato. 120
10 6. Da qua si parte per la sintesi di uridilato (UMP) e citidina (CTP). Si tratta di una sintesi sequenziale. L orotidilato subisce una decarbossilazione e viene convertito in uridilato. 7. Interviene una chinasi che fosforila sequenzialmente l UMP prima a UDP e poi UTP ottenendo l uridina 5 -trisfosfato. 8. La citidilato sintetasi ammina l anello, partendo da glutammina, e si ottiene il composto citidina 5 -trifosfato (CTP). Il CTP va a inibire l aspartato transcarbamilasi, tramite meccanismo retrogrado. 121
11 Regolazione della sintesi delle pirimidine È una regolazione allosterica a feedback negativo e positivo: gli enzimi regolati sono la carbamilsintetasi II e la OMP decarbossilasi. I modulatori allosterici sono l uridilato nelle sue forme fosforilate: l UMP funziona con feedback negativo sulla OMP decarbossilasi. UDP e UTP inibiscono la CPSII. L ATP e il 5 fosforibosil-1-pirofosfato invece promuove la sintesi. Sintesi dei nucleotidi trifosfati Sia le purine che le pirimidine devo essere trasformate nella forma difosfata. Le pirimidine devono essere convertite alla forma trifosforilata. Nella cellula esistono due chinasi: la nucleoside monofosfato chinasi base-specifica e la nucleoside difosfato chinasi. La prima, consumando ATP, trasforma le purine monofosfato nella corrispondete forma difosfata. La seconda invece fosforila il prodotto del primo enzima, consumando ATP, per produrre i nucleotidici trifosfati che la cellula può usare per sintetizzare i vari RNA. Sono enzimi reversibili. 122
12 Sintesi de novo dei deossiribonucleotidi Si parte dai corrispondenti ribonucleotidi ed esiste un enzima, la ribonucleotide reduttasi, che catalizza la loro sintesi. Viene ridotto ed eliminato il gruppo -OH per dare i deossiribonucleotidi. Questo enzima utilizza nucleotidi difosfati. Si ottiene il deossiribonucleotidi in forma difosfato. L enzima contiene due tioli liberi che si ossidano e diventano ponti disolfuro permettendo la catalisi. Affinché la proteina possa riprendere il suo ciclo è necessario che il ponte disofluro ritorni alla forma ridotta: gli equivalenti riducenti provengono dal NADPH e viene liberata acqua. Esistono due sistemi tramite i quali l enzima nucleotide reduttasi agisce: uno impiega la tioredossina, l altro la glutaredossina. Sistema tioredossina: l enzima fornisce gli equivalenti riducenti, ossidandosi a ponte disolfuro. Per ridurre il ponte disolfuro gli equivalenti riducenti sono forniti dalla tioredossina, che si ossida a sua volta con il ponte disolfuro. A questo punto è necessario ridurre la tioredossina, associata alla tioredossina reduttasi, che contiene un FAD covalentemente legato (che può essere nella forma ossidata o ridotta). La tioredossina reduttasi funzionante contiene FADH 2, che si ossida a FAD per ridurre la tioredossina. Il FAD deve essere ridotto nuovamente per ricominciare il ciclo: gli equivalenti riducenti sono forniti dal NADPH. Sistema glutaredossina: funziona con lo stesso meccanismo dell altro sistema. Il NADPH riduce il glutatione, che a sua volta riduce la glutaredossina che riduce la ribonucleotide reduttasi. 123
13 La ribonucleotide reduttasi è un unico enzima che può usare come substrati tutti i 4 ribonucleotidi in forma difosfato. È costituita da due dimeri R1 e R2. Il sito attivo si crea quando l enzima è assemblato correttamente ed è creato dalla struttura quaternaria, in esso sporgono le due cisteine, che si ridurranno ed ossideranno per la catalisi, e il residuo HX. Il residuo HX è un identità non identificata fondamentale nella catalisi. È presente anche una tirosina che lega il cofattore binucleare ferrico nella sua forma radicalica. nucleare izza il silico Meccanismo catalitico della ribonucleotide reduttasi Il residuo di tirosina radicalico nel sito attivo è stabilizzato dal ferro e può interagire con il residuo HX e trasferire il radicale sull amminoacido X. Si rigenera la tirosina generando il radicale X nel sito attivo attraverso una reazione catalitica. A questo punto entra il NDP, il radicale X reagisce con il carbonio 3 dello zucchero, rimuovendone un idrogeno e generando un radicale sul carbonio. La catalisi passa a carico dei due tioli e uno dei due tioli protona il gruppo ossidrilico in posizione 2, generando un solfuro. Il gruppo ossidrilico protonato viene liberato come acqua e si genera un catione sul carbonio 2. Questo carbocatione e questo solfuro si riorganizzano: il solfuro mette in compartecipazione il doppietto elettronico con lo zolfo e il carbocatione recupera lo ioduro dalla cisteina; si forma quindi un ponte disolfuro e avviene la protonazione del carbonio 2. Il radicale in 3 recupera l idrogeno, rigenerando il radicale X nel sito attivo. È completato il deossiribonucleotide difosfato che esce dal sito attivo. L enzima deve quindi essere rigenerato attraverso le reazioni precedentemente descritte tramite il trasferimento di elettroni (si rigenerano i due tioli liberi nel sito attivo). L enzima può così continuare i due cicli di riduzione. 124
14 125
15 Gli altri siti ne permettono la regolazione dell enzima: 1. Allosterica: controlla la velocità di riduzione dei ribonucleotidi. I modulatori sono l ATP e il deossiatp che si legano nel sito di regolazione primaria nella subunità R1. 2. Il sito di regolazione per la specificità di substrato: a seconda del nucleotide legato, l enzima scegli il substrato da ridurre. Il datp con un meccanismo a feedback negativo inibisce l attività dell enzima, mentre l ATP attiva l enzima. Questa regolazione avviene con meccanismo particolare: l enzima funzionante è un tetramero α2β2 e il suo stato attivo si trova in equilibrio tra lo stato dissociato e lo stato ad anello. I fattori che determinano lo spostamento dell equilibrio (lo stato dissociato o lo stato attivo) sono le concentrazioni proteiche: a basse concentrazioni prevale lo stato dissociato, a concentrazioni elevate prevale la forma attiva. Ad elevate concentrazioni di deossiatp i dimeri si organizzano in una struttura ad anello, a concentrazioni basse di deossiatp e alte di ATP cambia forma e passa allo stato più attivo e può catalizzare la riduzione. Quando l enzima ha la struttura ad anello, il sito attivo non è presente. Quando si ha la struttura ad anello, le subunità α e β si trovano nella stessa localizzazione, interagiscono le une con le altre. ATP dntp alte [datp] basse [datp] alte [ATP] Regolazione della ribonucleotide reduttasi I siti di specificità del substrato agiscono attraverso il seguente meccanismo: i substrati che entrano (CDP, UDP, GDP, ADP) vengono convertiti grazie all enzima nei corrispondenti deossiribonucleotidi difosfati (deossicdp, deossiudp, deossigdp, deossiadp). I ribonucleotidi difosfati devono essere fosforilati per formare dctp, dttp, dgtp, datp. Il dudp subisce un meccanismo diverso perché l uracile prima deve essere trasformato in timina per poi diventare dttp. I modulatori allosterici sono i nucleotidi trifosfato. Il dttp è sia modulatore allosterico positivo, in quanto attiva la riduzione di dgdp, che negativo in quanto inibisce la riduzione del CDP e dell UDP. Il dgtp così prodotto va a stimolare la riduzione a datp. Il datp stimola positivamente la sintesi delle deossipirimidine. La scelta del ribonucleotide da ridurre dipende dalla concentrazione dei deossiribonucleotidi dell altra classe presenti (purinici o pirimidinici). 126
16 Sintesi di timidilato (dtmp) Il deossitimidilato può essere ottenuto a partire da dctp e dutp. Il dctp viene convertito a dutp, che viene convertito dal dutpasi a dump, substrato della timidato sintasi che lo converte in dtmp. Se il timidilato non è sufficiente le cellule possono inserire dump invece di dtmp nel DNA creando delle alterazioni. È essenziale che ci sia il timidilato. Esiste un altra via che utilizza il CDP per la sintesi del timidilato: il dctp può essere deaminato e convertito in dutp, utilizzato per la sintesi di timidilato. Quindi la sintesi dipende dalla concentrazione di nucleotidi sia purinici che pirimidinici. La timidilato sintasi metila la base azotata del dump per convertirlo in dtmp: il donatore del gruppo metilico è una forma di tetraidrofolato, che trasferisce un atomo di idrogeno. Il tetraidrofolato cambia lo stato di ossidazione: passa da N 5, N 10 -metilene-tetraidrofolato a 7,8-diidrofolato. È necessario ridurre nuovamente il diidrofolato, grazie alla diidrofolato reduttasi che consuma NADPH. A questo punto il tetraidrofolato deve essere ricaricato del gruppo metilenico che deve trasportare, che è quello che proviene dalla catena laterale della serina. Il secondo enzima che serve si chiama, infatti, serina idrossimetil-transferasi; la serina viene convertita in glicina. Questa sintesi richiede un adeguata quantità di purine e pirimidine, così come una grande quantità di folati. Meccanismo d azione di timidilato sintasi 127
17 CATABOLISMO DELLE BASI PURINICHE Si parte dalle forme monofosfato dei nucleotidi purinici e si ottiene acido urico. 1. La prima reazione è la separazione tra lo zucchero e la base. Partendo da GMP il primo enzima che agisce è una 5 -nucleotidasi che rimuove la guanosina e il fosfato inorganico; il secondo enzima è una nucleosidasi che rimuove lo zucchero dal nucleoside. Per la degradazione dell AMP. La 5 nucleosidasi rimuove il fosfato (è una fosfatasi); l adenosina deaminasi ha come substrato l adenosina ottenuta e libera il gruppo amminico come ione ammonio: si ottiene l inosina. Sull inosina agisce la nucleosidasi che rimuove il ribosio e la basa azotata (ipoxantina). 2. Le due basi ottenute (guanina e ipoxantina) sono convertite in xantina. La guanina è deaminata dall enzima guanina deaminasi, che genera xantina liberando ammoniaca. L ipoxantina è substrato della xantina ossidasi; ossidasi che utilizza ossigeno e lo inserisce sull anello aromatico; il restante ossigeno esce come acqua ossigenata. Sono necessari sistemi per eliminare l ammoniaca (usata dalla glutammina sintetasi) e l acqua ossigenata (catalasi o glutatione reduttasi). 3. La xantina è nuovamente substrato della xantina ossidasi (contenente molipteno e 14 centri ferro-zolfo), che inserisce un nuovo ossigeno ottenendo acido urico. Xantina ossidasi: Enzima dimerico FAD Mo 4 centri Fe-S 128
18 Vie di recupero per la sintesi di nucleotidi purinici Circa il 90% delle purine sono recuperate e riutilizzate. PRPP + base à nucleotide. L enzima ipoxantina-guanina fosforibosiltransferasi (HGPRT) regola il riciclaggio di ipoxantina e guanina. Se l enzima è mutato non avviene il riciclo di ipoxantina e guanina, che vengono degradati. L acido urico si forma nella forma chetonica e nella forma enolica. È una molecola poco solubile in una soluzione acquosa (massima solubilità 7mg/100 ml) e presente in sali solidi, che quando precipitano si depositano preferenzialmente nelle articolazioni (infiammazione per cui le articolazioni si gonfiano, gotta). La gotta si genera in condizioni di iperuceremia: questa è attribuita a un errore congenito nel metabolismo, oppure a malattie renali per cui si riduce la clearance, ad alcuni tumori, all alterazione dell HGPRT, della glucosio -6P fosfatasi e a un aumentata sintesi di PRPP. La sindrome di Lesch-Nyhan è una disfunzione ereditaria recessiva legata al cromosoma X associata a una mancanza quasi totale della HGPRT. In questi casi di carenze enzimatiche l organismo risponde utilizzando molte riserve energetiche per la sintesi de novo di basi azotate. La gotta viene curata dal farmaco allopurinolo: è un inibitore competitivo della xantina ossidasi, che quindi non utilizza ipoxantina. Conseguentemente la xantina e l ipoxantina si accumulano, ma sono più solubili dell acido urico e quindi non si accumulano. L allopurinolo forma una forma idrossilata eliminata con le urine. L acido urico ha un ruolo nell eliminazione dei radicali liberi. La mancanza di adenosina deaminasi induce l insorgenza di immunodeficienza combinata grave, che comporta una disfunzione ai linfociti T, accumulo di datp a livello dei globuli rossi e quindi in circolo. 129
Nucleotide. Fosfato. Pentosio. Purina o pirimidina
 AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
METABOLISMO DEI NUCLEOTIDI
 METABOLISMO DEI NUCLEOTIDI SOSTANZE UBIQUITARIE COSTITUISCONO UNITA MONOMERICHE ACIDI NUCLEICI NUCLEOSIDI TRIFOSFATI (ATP) SONO PRODOTTI TERMINALI RICCHI DI ENERGIA MAGGIOR PARTE DELLE VIE METABOLICHE
METABOLISMO DEI NUCLEOTIDI SOSTANZE UBIQUITARIE COSTITUISCONO UNITA MONOMERICHE ACIDI NUCLEICI NUCLEOSIDI TRIFOSFATI (ATP) SONO PRODOTTI TERMINALI RICCHI DI ENERGIA MAGGIOR PARTE DELLE VIE METABOLICHE
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
BIOSINTESI DI AMMINOACIDI E NUCLEOTIDI
 BIOSINTESI DI AMMINOACIDI E NUCLEOTIDI La biosintesi degli amminoacidi ha molto in comune con quella dei nucleotidi, perché entrambe le classi di composti contengono azoto, ma anche perché le due vie di
BIOSINTESI DI AMMINOACIDI E NUCLEOTIDI La biosintesi degli amminoacidi ha molto in comune con quella dei nucleotidi, perché entrambe le classi di composti contengono azoto, ma anche perché le due vie di
Nucleotidi 26/10/2014. Nucleotidi (1)
 I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
Nucleotidi 04/11/2015
 Base azotata Nucleotidi Qualsiasi composto che manifesta proprietà basiche per via della presenza di una doppietta di elettroni non condivisi su un atomo di azoto (come nell ammoniaca e nelle ammine).
Base azotata Nucleotidi Qualsiasi composto che manifesta proprietà basiche per via della presenza di una doppietta di elettroni non condivisi su un atomo di azoto (come nell ammoniaca e nelle ammine).
Nucleotidi 20/12/2013. Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
Sintesi de novo dei ribonucleotidi purinici
 Sintesi de novo dei ribonucleotidi purinici origine metabolica dei nove atomi dell anello purinico: a differenza delle pirimidine, le basi puriniche vengono costruite sull anello di ribosio fosfato: sono
Sintesi de novo dei ribonucleotidi purinici origine metabolica dei nove atomi dell anello purinico: a differenza delle pirimidine, le basi puriniche vengono costruite sull anello di ribosio fosfato: sono
Nucleotidi 24/10/2012. Studenti: Biotec _ Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi Studenti: Biotec _ 2012 Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un composto ad anello contenente azoto (N) legato
I Nucleotidi Hanno Tre Componenti Nucleotidi Studenti: Biotec _ 2012 Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un composto ad anello contenente azoto (N) legato
Metabolismo. dei nucleotidi. Citosina Uracile Timina. Adenina Guanina
 Metabolismo dei nucleotidi Adenina Guanina Citosina Uracile Timina 1 I nucleotidi sono esteri fosforici di un pentosio (ribosio o desossiribosio) in cui una base purinica o pirimidinica è legata all atomo
Metabolismo dei nucleotidi Adenina Guanina Citosina Uracile Timina 1 I nucleotidi sono esteri fosforici di un pentosio (ribosio o desossiribosio) in cui una base purinica o pirimidinica è legata all atomo
Nucleotidi e Acidi Nucleici
 Nucleotidi e Acidi Nucleici https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Componenti degli acidi nucleici Collegato al fosfato Collegato alla base azotata Collegato allo zucchero
Nucleotidi e Acidi Nucleici https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Componenti degli acidi nucleici Collegato al fosfato Collegato alla base azotata Collegato allo zucchero
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Modulo 8: I nucleotidi e gli acidi nucleici
 Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Respirazione cellulare: processi molecolari medianti i quali le cellule consumano O 2 e producono CO 2
 AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Aerobiosi C A T A B O L I S M O. Lez 4A. Schema generale del metabolismo dei glucidi
 Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Seminario. Ciclo di Krebs 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A
 Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH
 Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Prima di essere ossidati. gli ACIDI GRASSI devono essere attivati. (cioè legati al CoA) e poi entrare nel mitocondrio
 Prima di essere ossidati gli ACIDI GRASSI devono essere attivati (cioè legati al CoA) e poi entrare nel mitocondrio L enzima acil CoA sintetasi (= acido grasso tiokinasi) sta sulla membrana mitocondriale
Prima di essere ossidati gli ACIDI GRASSI devono essere attivati (cioè legati al CoA) e poi entrare nel mitocondrio L enzima acil CoA sintetasi (= acido grasso tiokinasi) sta sulla membrana mitocondriale
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Metabolismo glucidico
 Metabolismo glucidico Glicogeno glicogenolisi Riboso-5P (NADPH) Colesterolo glicogenosintesi shunt pentoso fosfati Glucoso Glucoso-6P glicolisi Piruvato gluconeogenesi CO 2 -ossidazione Trigliceridi Acidi
Metabolismo glucidico Glicogeno glicogenolisi Riboso-5P (NADPH) Colesterolo glicogenosintesi shunt pentoso fosfati Glucoso Glucoso-6P glicolisi Piruvato gluconeogenesi CO 2 -ossidazione Trigliceridi Acidi
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
N H. 9H-purine. Le pirimidine che si trovano nel DNA sono citosina e timina: mentre nell RNA ritroviamo citosina e uracile:
 Lezione del 5 Maggio 2009 ucleotidi ed acidi nucleici Pirimidine e Purine Al fine di comprendere la struttura e le proprietà del DA e del RA, abbiamo bisogno di guardare in dettaglio ai loro componenti
Lezione del 5 Maggio 2009 ucleotidi ed acidi nucleici Pirimidine e Purine Al fine di comprendere la struttura e le proprietà del DA e del RA, abbiamo bisogno di guardare in dettaglio ai loro componenti
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
UNIVERSITÀ DI PISA. Facoltà di Farmacia. Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche
 UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Esercitazione Esempi di domande del 2 test
 Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
Esercitazione Esempi di domande del 1 test
 Esercitazione Esempi di domande del 1 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Esercitazione Esempi di domande del 1 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
La materia vivente è costituita da molecole, che costruiscono strutture ordinate partendo da materiali disordinati, tramite una spesa energetica
 LA LOGICA DELLA VITA La materia vivente è costituita da molecole, che costruiscono strutture ordinate partendo da materiali disordinati, tramite una spesa energetica G = H - T S Le reazioni dei processi
LA LOGICA DELLA VITA La materia vivente è costituita da molecole, che costruiscono strutture ordinate partendo da materiali disordinati, tramite una spesa energetica G = H - T S Le reazioni dei processi
METABOLISMO OSSIDATIVO
 METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
Metabolismo delle purine e delle pirimidine
 Metabolismo delle purine e delle pirimidine BASI AZTATE PIRIMIDIA PURIA citosina timina (DA) uracile (RA) adenina guanina Monomero ucleotide zucchero + base azotata + gruppo fosfato ucleoside gruppo fosfato
Metabolismo delle purine e delle pirimidine BASI AZTATE PIRIMIDIA PURIA citosina timina (DA) uracile (RA) adenina guanina Monomero ucleotide zucchero + base azotata + gruppo fosfato ucleoside gruppo fosfato
scaricato da www.sunhope.it
 CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CELLULA PROCARIOTICA PROCARIOTE
 CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
Biosintesi dei carboidrati
 Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
GLUCONEOGENESI fegato, corteccia renale
 GLUCONEOGENESI fegato, corteccia renale Glucosio 6 fosfato Energia Fosfoenolpiruvato Ciclo dell acido citrico Piruvato Glicerolo Lattato Amminoacidi glucogenici Triacilgliceroli Esochinasi (Glucochinasi)
GLUCONEOGENESI fegato, corteccia renale Glucosio 6 fosfato Energia Fosfoenolpiruvato Ciclo dell acido citrico Piruvato Glicerolo Lattato Amminoacidi glucogenici Triacilgliceroli Esochinasi (Glucochinasi)
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato
 2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
Una panoramica del ciclo dell acido ciclico
 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Se la biosintesi del glicogeno dipendesse unicamente dalla glicogeno sintasi il glicogeno sarebbe costituito da lunghe catene lineari simili a quelle
 Se la biosintesi del glicogeno dipendesse unicamente dalla glicogeno sintasi il glicogeno sarebbe costituito da lunghe catene lineari simili a quelle dell'amilosio. Ma nelle cellule devolute all'accumulo
Se la biosintesi del glicogeno dipendesse unicamente dalla glicogeno sintasi il glicogeno sarebbe costituito da lunghe catene lineari simili a quelle dell'amilosio. Ma nelle cellule devolute all'accumulo
I processi metabolici cellulari
 I processi metabolici cellulari 1 Metabolismo E l insieme delle reazioni chimiche che avvengono in una cellula o, più in generale, in qualsiasi organismo. Le sostanze coinvolte in tali reazioni sono dette
I processi metabolici cellulari 1 Metabolismo E l insieme delle reazioni chimiche che avvengono in una cellula o, più in generale, in qualsiasi organismo. Le sostanze coinvolte in tali reazioni sono dette
Cap.16 GLICOLISI. Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP H 2 O 2 NAD + 2 NADH + 2H +
 Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Casi più complicati. inibizione mista (competitiva e non competitiva)
 Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP. Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico
 Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Introduzione allo studio del metabolismo Parte I
 Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
scaricato da 1
 scaricato da www.sunhope.it 1 La decarbossilazione ossidativa del piruvato rappresenta il legame tra glicolisi e ciclo di Krebs Questa reazione, come tutto il ciclo di Krebs, avviene nella matrice mitocondriale
scaricato da www.sunhope.it 1 La decarbossilazione ossidativa del piruvato rappresenta il legame tra glicolisi e ciclo di Krebs Questa reazione, come tutto il ciclo di Krebs, avviene nella matrice mitocondriale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
Respirazione cellullare
 Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
METABOLISMO DEL GLICOGENO
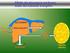 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
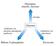 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NUCLEOTIDI. Hanno la funzione di conservare, trasmettere e modulare l informazione genetica e di tradurla nella sintesi di proteine.
 NUCLEOTIDI RUOLI BIOLOGICI: a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e di intermedi metabolici c) Costituiscono
NUCLEOTIDI RUOLI BIOLOGICI: a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e di intermedi metabolici c) Costituiscono
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Caratteristiche generali
 Caratteristiche generali Sono così chiamati perché hanno caratteristiche acide e si trovano prevalentemente nel nucleo delle cellule, dove svolgono la funzione informazionale. Gli acidi nucleici sono infatti
Caratteristiche generali Sono così chiamati perché hanno caratteristiche acide e si trovano prevalentemente nel nucleo delle cellule, dove svolgono la funzione informazionale. Gli acidi nucleici sono infatti
NUCLEOTIDI. Hanno la funzione di conservare, trasmettere e modulare l informazione genetica e di tradurla nella sintesi proteica.
 NUCLEOTIDI a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e intermedi metabolici c) Costituiscono gli ACIDI
NUCLEOTIDI a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e intermedi metabolici c) Costituiscono gli ACIDI
Il metabolismo dei lipidi
 Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Capitolo B2 Il metabolismo energetico: dal glucosio all ATP
 Capitolo B2 Il metabolismo energetico: dal glucosio all ATP Quesiti e problemi 1 Le funzioni del metabolismo cellulare sono: ricavare energia utile per la cellula attraverso la degradazione di sostanze
Capitolo B2 Il metabolismo energetico: dal glucosio all ATP Quesiti e problemi 1 Le funzioni del metabolismo cellulare sono: ricavare energia utile per la cellula attraverso la degradazione di sostanze
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
DNA: Struttura e caratteristiche
 DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
Regolazione del Ciclo di Krebs 8 reazioni
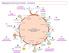 Regolazione del Ciclo di Krebs 8 reazioni Stechiometria del Ciclo Acetil-CoA + 3NAD + + FAD + GDP + Pi + 2H 2 O 2 CO 2 + HS-CoA + 3NADH + 2H + + FADH2 + GTP (GTP ATP) 1 NADH 2,5 ATP 1 FADH 2 1,5 ATP Per
Regolazione del Ciclo di Krebs 8 reazioni Stechiometria del Ciclo Acetil-CoA + 3NAD + + FAD + GDP + Pi + 2H 2 O 2 CO 2 + HS-CoA + 3NADH + 2H + + FADH2 + GTP (GTP ATP) 1 NADH 2,5 ATP 1 FADH 2 1,5 ATP Per
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
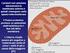 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Gluconeogenesi sintesi di glucosio da precursori non glucidici
 GLUCONEOGENESI Gluconeogenesi sintesi di glucosio da precursori non glucidici Precursori: Lattato, ossalacetato, glicerolo Amminoacidi (scheletro carbonioso) Usa le reazioni glicolitiche in direzione
GLUCONEOGENESI Gluconeogenesi sintesi di glucosio da precursori non glucidici Precursori: Lattato, ossalacetato, glicerolo Amminoacidi (scheletro carbonioso) Usa le reazioni glicolitiche in direzione
GLICOLISI ADP ATP. Condizioni aerobiche. Condizioni anaerobiche ATP
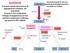 GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
LE REAZIONI DI FISSAZIONE DEL CARBONIO
 LE REAZIONI DI FISSAZIONE DEL CARBONIO Reazioni al buio ogni anno 200 miliardi di tonnellate di CO 2 vengono convertite in biomassa 40% fitoplancton CICLO DI CALVIN ciclo riduttivo dei pentosi fosfati,
LE REAZIONI DI FISSAZIONE DEL CARBONIO Reazioni al buio ogni anno 200 miliardi di tonnellate di CO 2 vengono convertite in biomassa 40% fitoplancton CICLO DI CALVIN ciclo riduttivo dei pentosi fosfati,
Biologia. La cellula al lavoro
 Biologia La cellula al lavoro Capitolo 5 La cellula al lavoro 1. Il metabolismo cellulare: come le cellule ricavano energia 2. La glicolisi è la prima fase della demolizione del glucosio 3. La respirazione
Biologia La cellula al lavoro Capitolo 5 La cellula al lavoro 1. Il metabolismo cellulare: come le cellule ricavano energia 2. La glicolisi è la prima fase della demolizione del glucosio 3. La respirazione
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
Introduzione alla biologia della cellula. Lezione 3 Le biomolecole DNA e RNA
 Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI
 METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
