Corso di Laurea in Chimica. Laboratorio di Chimica Generale
|
|
|
- Paolina Scognamiglio
- 5 anni fa
- Visualizzazioni
Transcript
1 Corso di Laurea in Chimica Laboratorio di Chimica Generale Prof. Claudia Caltagirone Anno Accademico 2018/2019
2 Prof. Claudia Caltagirone Tel (uff) (lab)
3 Date importanti: Compito Compito Compito Inizio Laboratorio
4 Materiale per lezione: Calcolatrice Tavola periodica
5 Materiale per il laboratorio: Camice Occhiali protezione (facoltativi) Pennarello vetro
6 Svolgimento delle lezioni Stechiometria: - lucidi/power point di materiale grafico di supporto - Esercitazioni in aula con supporti «social» Testi consigliati: Chimica. Principi generali con esercizi (Vito Lippolis, Nelsi Zaccheroni, Luca Giorgi, Vieri Fusi) Ed. Idelson-Gnocchi Laboratorio: -esperienze di laboratorio Le esperienze si devono scaricare da internet La prova di esame consiste in una verifica scritta. Entra nella valutazione finale anche il COMPORTAMENTO IN LABORATORIO durante il semestre.
7 Prova di esame La prova di esame consiste in un compito scritto. Durante il semestre verranno svolte 3 prove parziali ad esclusione. Gli studenti che supereranno le tre prove con un voto pari o superiore ai 18/30 non dovranno fare l esame finale. Le prove parziali prevedono 10 esercizi ciascuno su argomenti selezionati. Ogni domanda vale 3 punti La prova di esame finale prevede 5 esercizi che vertono su tutto il programma svolto. Ogni domanda vale 6 punti. La valutazione del laboratorio verrà effettuata considerando il comportamento in laboratorio e con una prova scritta che riguarderà le esperienze svolte durante il semestre
8 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa molare. Formula chimica: empirica e molecolare. Nomenclatura dei composti inorganici. Equazioni chimiche. Bilanciamento delle equazioni chimiche. Bilanciamento delle reazioni redox con il metodo delle semireazioni. Calcolo stechiometrico delle quantità molari e delle masse. Reagente limitante. Resa di reazione. Soluzioni e loro concentrazione. Metodi di separazione delle componenti di una miscela. Acidi e Basi. Reazioni di ossidoriduzione e loro bilanciamento. Equilibrio chimico gassoso ed in soluzione acquosa. Legge di azione di massa. Principio di Le Chatelier e quoziente di reazione. Equilibri Acido- Base: autoprotolisi dell acqua; ph; idrolisi di sali; soluzioni tampone; titolazioni acido-base (cenni). Equilibrio di solubilità: solubilità e prodotto di solubilità; previsione di precipitazione; effetto dello ione in comune, del ph, della temperatura. Elettrochimica: serie elettrochimica; celle galvaniche.
9 1.Proprietà della Materia Materia: Occupa volume, possiede massa ed inerzia Omogenea e eterogenea Sostanze e miscele Composti e elementi Composizione: H 2 O, 11.9% idrogeno e 88.81% ossigeno Proprietà: Fisiche e chimiche
10 Stati della Materia I solidi sono rigidi ed hanno forma e volume definito. Poche variazioni con P e T. I liquidi prendono la forma del contenitore. Hanno un volume proprio I gas assumono il volume e la forma del contenitore.
11 La Classificazione Schematica della Materia sostanza pura composto materia miscela omogenea eterogenea elemento
12 Elementi ed atomi Elementi: contengono un solo tipo di atomo; organizzati nella tavola periodica caratterizzati da un simbolo Atomo: particella più piccola di un elemento che conserva le proprietà chimiche dell elemento stesso
13 La Tavola Periodica
14 Composti e molecole Composto: sostanza pura costituita da uno o più elementi tenuti insieme da un legame chimico. Ogni composto è caratterizzato dalla sua formula chimica H 2 O : composto binario Composti organici e inorganici Molecole: le più piccole unità discrete neutre che conservano la composizione e le caratteristiche chimiche del composto: H 2 O, CO 2, NH 3, CH 4 Ioni : atomi o molecole carichi
15 Proprietà Fisiche caratteristiche proprie della materia caratteristiche che si possono osservare direttamente e misurare senza variare l identità della sostanza es. stato, dimensione, massa, volume, colore, odore, punto di fusione (T m ), punto di ebollizione (T b ), densità, solubilità...
16 Proprietà Chimiche Caratteristiche che descrivono il comportamento (reattività) della materia eg. infiammabilità, potere ossidante, acidità/basicità...
17 Misura della Materia Unità di Misura
18 Misurazioni Si sta effettuando una misura quando: Leggete l ora Prendete la vostra temperatura Pesate un oggetto
19 Alcuni Strumenti di Misura
20 Misure in Chimica In chimica si fanno esperimenti misurano quantità si usano numeri per riportare le misure
21 Il Sistema Internazionale delle Unità (SI) lunghezza metro m massa kilogrammo kg temperatura Kelvin K quantità di sostanza mole mol tempo secondi s Intensità di corrente ampere A Intensità luminosa candela cd
22 Temperatura La temperatura è la proprietà che caratterizza lo stato termico di due sistemi in relazione alla direzione del flusso di calore che si instaurerebbe fra di essi. Si misura utilizzando un termometro.
23 Scale di Temperatura Sono Fahrenheit, Celsius, e Kelvin. Punti di riferimento comune sono la temperatura di fusione ed ebollizione dell acqua.
24 Temperatura Scala Kelvin (K) e scala Celsius ( C) Le due scale hanno la stessa ampiezza (DK = D C) 0 K = C K = C La normale temperatura del corpo umano può oscillare nel corso della giornata da 36 C a 37 C. Esprimere queste due temperature e la loro variazione utilizzando la scala Kelvin Secondo il sito web della NASA la temperatura media dell Universo è 2.7 K. Convertire questa temperatura in C
25 Volume 1 m = 10 dm (1m) 3 = (10 dm) 3 1m 3 = 1000 dm 3 = 1000 L 1 dm = 10 cm (1dm) 3 = (10 cm) 3 1dm 3 = 1000 cm 3 = 1000mL
26 Densità massa (g) massa (g) Densità = = volume (cm 3 ) volume (ml) densità di H 2 O è 1.00 g/cm 3 (a ~ 4 C) 1cm 3 = 1mL Mercurio Platino Alluminio liquido 13.6 g/cm g/cm g/cm 3
27 La densità dell aria priva di umidità è 1.18 x 10-3 g/cm 3. Quale volume di aria, in cm 3, ha una massa di 1.50g?
28 Incertezze nelle Misure Scientifiche Ogni strumento è caratterizzato da: sensibilità, accuratezza, precisone Errori sistematici. Termometro costantemente 2 C più basso. Errori casuali Legati alla lettura della misura. Precisione Riproducibilità di una misura. Accuratezza Quanto vicino è la misura al valore reale.
29 Sensibilità
30 Precisione e Accuratezza Buona precisione Buona accuratezza Buona precisione Scarsa accuratezza Scarsa precisione Scarsa accuratezza
31 Deviazione standard Determinazione Massa misurata (g) Differenza tra media e misura (g) Quadrato della differenza x x x x x 10-5 Media = g Somma dei quadrati della differenza= 26 x 10-5 Deviazione standard= (26 x 10-5 /5) 1/2 = La deviazione standard valuta l errore indeterminato che non può essere controllato dall operatore. Il 68% dei valori ottenuti è dentro la deviazione standard
32 Riportare una Misura In ogni misura si deve esprimere un Numero Seguito dalla sua Unità
33 Notazione esponenziale o scientifica Il numero è espresso come prodotto di due numeri N x 10 n n numero di posti di cui il punto decimale è spostato per ottenere il numero in notazione scientifica Es. 1234= x 10 1 x 10 1 x 10 1 = x = 1.234/10 1 x 10 1 = x 10-1 x 10-1 = x 10-2
34 Cifre Significative: cifre di un valore numerico alle quali si assegna un valore certo (riflettono l accuratezza della misura). Non ha senso esprimere una misura con un numero di cifre decimali superiori a quelle dello strumento usato Tutti i numeri diversi da zero sono significativi kg 4 cifre significative Gli zero tra numeri diversi da zero sono significativi 606 m 3 cifre significative Gli zero alla sinistra di numeri diversi da zero NON sono significativi 0.08 L 1 cifra significativa Se un numero è maggiore di 1, gli zero alla sua destra sono significativi 2.0 mg 2 cifre significative Se un numero è minore di 1, solo gli zero terminali o che si trovano tra i numeri sono significativi g 3 cifre significative
35 Cifre Significative Cifre diverse da zero a partire da sinistra. Nelle addizioni e sottrazioni. Numero 6.29 g g g = Cifre significative Usare lo stesso numero di decimali della quantità con il più basso numero di decimali varie
36 Cifre Significative Nelle moltiplicazioni e divisioni. Usare il numero di cifre significative relative alla precisione più bassa = = Arrotondamento la 3 a cifra è incrementata se la 4 a cifra 5 Arrotondare a 3 cifre
37 Unità Unità S.I. Lunghezza metro, m Massa chilogrammo, kg Tempo secondo, s Temperatura Kelvin, K Quantità Mole, mol -1 Unità derivate Forza Newton, kg m s -2 Pressione Pascal, kg m -1 s -2 Energia Joule, kg m 2 s -2 Altre unità Lunghezza Angstrom, Å, 10-8 cm Volume Litro, L, 10-3 m 3 Energia Caloria, cal, J Pressione 1 Atm = x 10 2 kpa 1 Atm = 760 mm Hg
38 Sottomultipli per le grandezze fisiche frazione prefisso simbolo 10-1 deci d 10-2 centi c 10-3 milli m 10-6 micro 10-9 nano n pico p femto f atto a Multipli per le grandezze fisiche multiplo prefisso simbolo 10 1 deca da 10 2 etto h 10 3 chilo K 10 6 mega M 10 9 giga G tera T
39 Es. Il glicol etilenico, C 2 H 6 O 2, ha una densità di 1.11 g/cm 3 a 20 C. (1cm 3 = 1 ml) Si devono utilizzare 500 ml di questo liquido, quanti grammi di questo composto si devono pesare? d = m (g) / V (ml) 1.11 g 500 ml = 555 g 1 ml 3 cifre significative
40 Es. Si devono utilizzare 2.00 g di un liquido avente densità g/cm 3. Determinare il volume del composto? d = m (g) / V (ml) 1 cm g = 2.79 cm g 3 cifre significative
41 Es. Un campione di 37.5 g di un metallo è posto in un cilindro graduato contenente acqua. Il volume dell acqua passa da 7.0 a 20.5 ml. Utilizzando i dati di densità stabilire di quale metallo si tratti. Metallo d(g/ml) Metallo d(g/ml) Mg 1.74 Al 2.70 Fe 7.87 Cu 8.96 Ag 10.5 Pb 11.3 Volume del campione = volume di acqua spostata nel cilindro = = 13.5 ml
42
43 d = m (g) / V (ml) m 37.5 g d = = = 2.78 g/ml V 13.5 ml 3 cifre significative Il metallo è l alluminio.
44 La densità del mercurio a 0 C è g/cm 3, a 10 C è g/cm 3, e a 20 C g/cm 3. Stimare la densità del mercurio a 30 C. Un pezzo d argento ha una massa di 2.365g. Se la densità dell argento è 10.5 g/cm 3 qual è il volume dell argento? La pirite è spesso chiamata l oro degli sciocchi poiché ha l aspetto dell oro. Si supponga di avere un solido che ha l aspetto dell oro di massa 23.5g. Quando il campione viene immerso in acqua in un cilindro graduato il livello dell acqua sale da 47.5 a 52.2 ml. Il campione è pirite (d = 5g/cm 3 ) o oro (d = 19.3 g/cm 3 )?
45 La mina di una matita misura 19 cm. Qual è la sua lunghezza in millimetri? E in metri? Alcune bibite analcoliche sono vendute in bottiglie che hanno un volume di 1.5L. Quant è questo volume in millilitri, in centimetri cubici e in decimetri cubici? Una moneta ha una massa di g. Quanto vale questa massa in chilogrammi e in milligrammi? La lega utilizzata un tempo per saldare I tubi di rame è formata dal 67% di piombo e dal 33% di stagno. Qual è la massa del piombo in un blocco di lega da 250g?
L Atomo Nucleare. Rutherford protoni James Chadwick neutroni 1932
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Alcune informazioni utili
 Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2015/2016
 Corso di Laurea in Biologia Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2015/2016 Prof Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it Svolgimento
Corso di Laurea in Biologia Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2015/2016 Prof Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it Svolgimento
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE
 CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2018/2019
 Corso di Laurea in Biologia Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2018/2019 Prof Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it In
Corso di Laurea in Biologia Laboratorio di Chimica Prof. Claudia Caltagirone Anno Accademico 2018/2019 Prof Claudia Caltagirone Tel. 070 6754452 (uff) 070 6754495 (lab) E-mail ccaltagirone@unica.it In
Reazioni di ossido-riduzione (redox) - Come stabilire il verso di una redox? -
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Corso di Chimica Generale e Inorganica
 Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
Corso di Chimica Generale e Inorganica Prof. Manuel Sergi Testi consigliati: QUALSIASI TESTO UNIVERSITARIO DI CHIMICA GENERALE VA BENE! Sacco, Pasquali, Marchetti Chimica generale e inorganica Casa Editrice
Grandezze fisiche fondamentali
 Grandezze fisiche fondamentali La grandezza fisica rappresenta la proprietà di un corpo. Le grandezze fisiche fondamentali sono 7. La differenza rispetto a quelle derivate è che quelle derivate presentano
Grandezze fisiche fondamentali La grandezza fisica rappresenta la proprietà di un corpo. Le grandezze fisiche fondamentali sono 7. La differenza rispetto a quelle derivate è che quelle derivate presentano
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Chimica Generale ed Inorganica
 CCS-Biologia CCS- Scienze Geologiche A.A. 2016-2017 Chimica Generale ed Inorganica Prof. Francesco Isaia Prof. Vito Lippolis Dipartimento di Scienze Chimiche e Geologiche Cittadella Universitaria Email:
CCS-Biologia CCS- Scienze Geologiche A.A. 2016-2017 Chimica Generale ed Inorganica Prof. Francesco Isaia Prof. Vito Lippolis Dipartimento di Scienze Chimiche e Geologiche Cittadella Universitaria Email:
GRANDEZZE FONDAMENTALI E DERIVATE
 GRANDEZZE FONDAMENTALI E DERIVATE GRANDEZZA FISICA = sostanza o corpo che può essere misurata Il Sistema Internazionale (SI) delle unità di misura classifica le grandezze fisiche in: GRANDEZZE FONDAMENTALI
GRANDEZZE FONDAMENTALI E DERIVATE GRANDEZZA FISICA = sostanza o corpo che può essere misurata Il Sistema Internazionale (SI) delle unità di misura classifica le grandezze fisiche in: GRANDEZZE FONDAMENTALI
CHIMICA GENERALE ED INORGANICA
 Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
Corso di Laurea in Biotecnologie CHIMICA GENERALE ED INORGANICA Autori: Nivaldo J. Tro Chimica Un approccio molecolare EdiSES Per gli esercizi Autori : Rossi, Tesauro, Saviano, Randazzo Casa Editrice :
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
La Pressione. Convertire una pressione di 635 mm Hg nel suo corrispondente valore in atm, bar e kpa 635 mmhg/760 mmhg = atm. 1atm.
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Le unità fondamentali SI
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Misure e Unità di Misura
 2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
Laboratorio di Chimica Generale ed Inorganica. Lezione 2. Misura della materia
 Laboratorio di Chimica Generale ed Inorganica Lezione 2 Misura della materia Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale ed Inorganica UniFe
Laboratorio di Chimica Generale ed Inorganica Lezione 2 Misura della materia Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale ed Inorganica UniFe
Laboratorio di Fisica-Chimica
 Laboratorio di Fisica-Chimica Lezione n.1. Che cos'è la Fisica? La Fisica è una scienza che si occupa dello studio dei fenomeni che avvengono in natura. Questo studio viene compiuto tramite la definizione
Laboratorio di Fisica-Chimica Lezione n.1. Che cos'è la Fisica? La Fisica è una scienza che si occupa dello studio dei fenomeni che avvengono in natura. Questo studio viene compiuto tramite la definizione
APPUNTI delle lezioni prof. Celino PARTE 1
 APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
Argomenti per il Recupero di Fisica
 Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze Fondamentali e Derivate
Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze Fondamentali e Derivate
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Le Grandezze e il Sistema Internazionale di misura
 Le Grandezze e il Sistema Internazionale di misura Si dice GRANDEZZA tutto ciò ce si può misurare. Esempio L altezza di una torre, il volume di una stanza, la superficie di un muro, l ampiezza di un angolo,
Le Grandezze e il Sistema Internazionale di misura Si dice GRANDEZZA tutto ciò ce si può misurare. Esempio L altezza di una torre, il volume di una stanza, la superficie di un muro, l ampiezza di un angolo,
Sommario. Note di metodo. Dentro la materia: miscugli e sostanze. Le trasformazioni della materia. Capitolo. Capitolo
 Sommario Note di metodo 1 Misurare in chimica IX 2 Le grandezze X 3 Multipli e sottomultipli XI 4 Notazione scientifica XII 5 Gli errori nelle misure XIII 6 Accuratezza e precisione XIV 7 Sensibilità e
Sommario Note di metodo 1 Misurare in chimica IX 2 Le grandezze X 3 Multipli e sottomultipli XI 4 Notazione scientifica XII 5 Gli errori nelle misure XIII 6 Accuratezza e precisione XIV 7 Sensibilità e
Tutte le altre grandezze fisiche derivano da queste e sono dette grandezze DERIVATE (es. la superficie e il volume).
 Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
LA MISURA DELLE GRANDEZZE FISICHE. Prof Giovanni Ianne
 LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
GRANDEZZE FISICHE E MISURA
 GRANDEZZE FISICHE E MISURA 1 Una grandezza è la proprietà di un fenomeno, corpo o sostanza, che può essere espressa quantitativamente mediante un numero e un riferimento Quindi il colore delle matite non
GRANDEZZE FISICHE E MISURA 1 Una grandezza è la proprietà di un fenomeno, corpo o sostanza, che può essere espressa quantitativamente mediante un numero e un riferimento Quindi il colore delle matite non
Calcoli applicati alla chimica analitica. Unità di misura del Sistema Internazionale
 Calcoli applicati alla chimica analitica Unità di misura del Sistema Internazionale Soluzioni e loro concentrazioni Stechiometria chimica 1 Unità di misura SI Il Sistema Internazionale delle Unità (SI)
Calcoli applicati alla chimica analitica Unità di misura del Sistema Internazionale Soluzioni e loro concentrazioni Stechiometria chimica 1 Unità di misura SI Il Sistema Internazionale delle Unità (SI)
Esperienze di Fisica
 Esperienze di Fisica Dr. Alen Khanbekyan Tel.: 057734665 E-mail: khanbekyan@unisi.it Relazioni. Per ogni prova pratica deve essere preparata una relazione scritta strutturata nel modo seguente:. Introduzione
Esperienze di Fisica Dr. Alen Khanbekyan Tel.: 057734665 E-mail: khanbekyan@unisi.it Relazioni. Per ogni prova pratica deve essere preparata una relazione scritta strutturata nel modo seguente:. Introduzione
Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2
 Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2 Esercizio Risposta PAG 40 ES 1 Per permettere un confronto quantitativo tra i dati raccolti da operatori diversi.
Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2 Esercizio Risposta PAG 40 ES 1 Per permettere un confronto quantitativo tra i dati raccolti da operatori diversi.
Materia. Tutto ciò che occupa spazio e ha massa
 ISBN: 9788879476539 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore.
ISBN: 9788879476539 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore.
Materia. Tutto ciò che occupa spazio e ha massa
 Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore. Hanno un volume
Materia Tutto ciò che occupa spazio e ha massa Gli Stati della Materia Solido Liquido Gas I solidi sono rigidi ed hanno forma e volume definito. I liquidi prendono la forma del contenitore. Hanno un volume
I.T.C.G. Hodierna. Corso per Geometri. Materia: Fisica. Prof. Giuseppe Frangiamore
 I.T.C.G. Hodierna Corso per Geometri Materia: Fisica Prof. Giuseppe Frangiamore CAPITOLO I Che cosa studia la fisica La fisica studia tutti i fenomeni naturali ricercando le leggi che li governano. Grazie
I.T.C.G. Hodierna Corso per Geometri Materia: Fisica Prof. Giuseppe Frangiamore CAPITOLO I Che cosa studia la fisica La fisica studia tutti i fenomeni naturali ricercando le leggi che li governano. Grazie
Corso di Laurea in Fisica
 Anno accademico 2016/2017 Corso di Laurea in Fisica Laboratorio 1 Docente: Prof. Annalisa D Angelo Esercitatori: Cristina Morone, Alessandro Rizzo, Lucilla Lanza, Valeria Di Felice, Massimo Bassan people.roma2.infn.it/~annalisa/lab1
Anno accademico 2016/2017 Corso di Laurea in Fisica Laboratorio 1 Docente: Prof. Annalisa D Angelo Esercitatori: Cristina Morone, Alessandro Rizzo, Lucilla Lanza, Valeria Di Felice, Massimo Bassan people.roma2.infn.it/~annalisa/lab1
fenomeni na- turali grandezze fisiche principi leggi metodo scientifico modello
 La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
Il metodo scientifico
 Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
Nei laboratori scientifici si parla di misurare, calcolare, determinare, aggiungere, togliere, mescolare, prelevare, pesare, sperimentare, provare,
 02.10.17 Nei laboratori scientifici si parla di misurare, calcolare, determinare, aggiungere, togliere, mescolare, prelevare, pesare, sperimentare, provare, si effettuano esperienze, si misurano grandezze,...
02.10.17 Nei laboratori scientifici si parla di misurare, calcolare, determinare, aggiungere, togliere, mescolare, prelevare, pesare, sperimentare, provare, si effettuano esperienze, si misurano grandezze,...
DISCIPLINA: SCIENZE INTEGRATE (CHIMICA) PIANO DELLE UDA 1 ANNO CHIMICA, MATERIALI E BIOTECNOLOGIE ITIS. Anno 2018/2019
 ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it https://isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 DISCIPLINA: SCIENZE INTEGRATE
ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it https://isisfacchinetti.gov.it Rev. 1.1 del 26/07/17 DISCIPLINA: SCIENZE INTEGRATE
Richiami di matematica per lo studio delle discipline scientifiche
 Richiami di matematica per lo studio delle discipline scientifiche La misura in chimica : Misurare significa confrontare una grandezza in rapporto con un altra ad essa omogenea, scelta come campione.i
Richiami di matematica per lo studio delle discipline scientifiche La misura in chimica : Misurare significa confrontare una grandezza in rapporto con un altra ad essa omogenea, scelta come campione.i
Gli strumenti della Chimica Quantitativa (cap. 1)
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Gli strumenti della Chimica Quantitativa (cap. 1) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Gli strumenti della Chimica Quantitativa (cap. 1) Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
UNITA DI MISURA. Le unità di misura sono molto importanti
 Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Le unità di misura sono molto importanti UNITA DI MISURA 1000 è solo un numero 1000 LIRE unità di misura monetaria 1000 EURO unità di misura monetaria ma il valore di acquisto è molto diverso! 1000 Euro/mese
Chimica Generale ed Inorganica. Lezione 1
 Chimica Generale ed Inorganica Lezione 1 Implicazioni della Chimica nella Vita Quotidiana Salute e Medicina Sistemi di disinfettazione Anestesia Vaccini e antibiotici Terapia genica Energia ed Ambiente
Chimica Generale ed Inorganica Lezione 1 Implicazioni della Chimica nella Vita Quotidiana Salute e Medicina Sistemi di disinfettazione Anestesia Vaccini e antibiotici Terapia genica Energia ed Ambiente
APPUNTI DI CHIMICA GENERALE
 APPUNTI DI CHIMICA GENERALE Curati dal Prof. Miceli Gli appunti che seguiranno sono frutto di anni di esperienza, di tanta passione per questa disciplina e dell amore nato dall insegnamento in gran parte
APPUNTI DI CHIMICA GENERALE Curati dal Prof. Miceli Gli appunti che seguiranno sono frutto di anni di esperienza, di tanta passione per questa disciplina e dell amore nato dall insegnamento in gran parte
SISTEMA INTERNAZIONALE (S.I.) Le grandezze che si possono misurare sono dette grandezze fisiche.
 1. GRANDEZZE FONDAMENTALI SISTEMA INTERNAZIONALE (S.I.) Le grandezze che si possono misurare sono dette grandezze fisiche. Secondo il Sistema Internazionale (SI) ci sono sette grandezze fondamentali. 2.
1. GRANDEZZE FONDAMENTALI SISTEMA INTERNAZIONALE (S.I.) Le grandezze che si possono misurare sono dette grandezze fisiche. Secondo il Sistema Internazionale (SI) ci sono sette grandezze fondamentali. 2.
fenomeni na- turali grandezze fisiche principi leggi metodo scientifico modello
 La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
La fisica è la scienza che studia i fenomeni naturali (ossia tutti gli eventi che possono essere descritti, o quantificati, attraverso grandezze fisiche opportune) al fine di stabilire principi e leggi
Chimica Generale ed Inorganica
 Dipartimento di Ecologia e Biologia Chimica Generale ed Inorganica Prof.ssa Giorgia Botta Contatti Tel: 0761-357314 Dipartimento DEB Facoltà di Agraria, lab 08 e-mail: botta.giorgia@gmail.com Proprietà,
Dipartimento di Ecologia e Biologia Chimica Generale ed Inorganica Prof.ssa Giorgia Botta Contatti Tel: 0761-357314 Dipartimento DEB Facoltà di Agraria, lab 08 e-mail: botta.giorgia@gmail.com Proprietà,
UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE. UdM 1
 UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE UdM 1 Lo studio dei fenomeni naturali si basa sulle osservazioni sperimentali e richiede la misura di certe grandezze fisiche. Ai fini della misurazione
UNITA di MISURA e DIMENSIONI delle OSSERVABILI FISICHE UdM 1 Lo studio dei fenomeni naturali si basa sulle osservazioni sperimentali e richiede la misura di certe grandezze fisiche. Ai fini della misurazione
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301»
 Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze
Grandezze e Misure 1
 Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
IL SISTEMA INTERNAZIONALE DI MISURA
 IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
Gli Stati della Materia
 John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Capitolo 1 Materia e Misure 1 Benvenuti nel Mondo della Chimica 2 Versione italiana a cura di Giaime Marongiu e Guido Ennas
John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Capitolo 1 Materia e Misure 1 Benvenuti nel Mondo della Chimica 2 Versione italiana a cura di Giaime Marongiu e Guido Ennas
Corso di FISICA. Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci
 Anno accademico 2003/2004 Corso di Laurea in Biologia Cellulare e Molecolare Corso di FISICA Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci LEZIONI martedi ore 9-11
Anno accademico 2003/2004 Corso di Laurea in Biologia Cellulare e Molecolare Corso di FISICA Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci LEZIONI martedi ore 9-11
Strumenti Matematici per la Fisica.
 Strumenti Matematici per la Fisica www.fisicaxscuola.altervista.org 2 Strumenti Matematici per la Fisica Potenze di Prefissi: Multipli e Sottomultipli Sistema Metrico Decimale Equivalenze Proporzioni e
Strumenti Matematici per la Fisica www.fisicaxscuola.altervista.org 2 Strumenti Matematici per la Fisica Potenze di Prefissi: Multipli e Sottomultipli Sistema Metrico Decimale Equivalenze Proporzioni e
Algebra. Considera la formula: esplicita rispetto a r e rispetto a Q. Considera la formula: esplicita rispetto a h.
 Algebra Considera la formula: F 1 qq 2 4 r esplicita rispetto a r e rispetto a Q. Considera la formula: p p 0 gh esplicita rispetto a h. Proprietà potenze Operazione di elevamento a potenza: Esempi 10
Algebra Considera la formula: F 1 qq 2 4 r esplicita rispetto a r e rispetto a Q. Considera la formula: p p 0 gh esplicita rispetto a h. Proprietà potenze Operazione di elevamento a potenza: Esempi 10
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica CH 3
 Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Introduzione alla Chimica. Paolo Mazza
 Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Programma di CHIMICA E LABORATORIO
 «IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti di misura: portata e sensibilità,
«IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti di misura: portata e sensibilità,
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Le reazioni chimiche 2
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Appunti di Stechiometria per Chimica GRANDEZZE FISICHE
 Appunti di Stechiometria per Chimica GRANDEZZE FISICHE Una grandezza fisica è una qualunque proprietà della materia che può essere misurata (quantificata). Misurare significa confrontare (rapportare) due
Appunti di Stechiometria per Chimica GRANDEZZE FISICHE Una grandezza fisica è una qualunque proprietà della materia che può essere misurata (quantificata). Misurare significa confrontare (rapportare) due
3 Le grandezze fisiche
 3 Le grandezze fisiche Grandezze fondamentali e grandezze derivate Tra le grandezze fisiche è possibile individuarne alcune (fondamentali) dalle quali è possibile derivare tutte le altre (derivate) Le
3 Le grandezze fisiche Grandezze fondamentali e grandezze derivate Tra le grandezze fisiche è possibile individuarne alcune (fondamentali) dalle quali è possibile derivare tutte le altre (derivate) Le
Grandezze e unità di misura
 Grandezze e unità di misura La misura di una grandezza è costituita da un valore numerico e un appropriata unità di misura Esiste un sistema metrico denominato Sistema Internazionale di Unità (SI) basato
Grandezze e unità di misura La misura di una grandezza è costituita da un valore numerico e un appropriata unità di misura Esiste un sistema metrico denominato Sistema Internazionale di Unità (SI) basato
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO
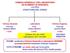 CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
grandezze fisiche leggi fisiche
 INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
1 - GRANDEZZE E MISURE
 1 - GRANDEZZE E MISURE INDICE Grandezze fisiche e loro misure: 2 Notazione: 3 Prefissi: 4 Grandezze fondamentali e unità di misura: 5 Grandezze derivate: 9 Valori ed errori, incertezza di misura: 12 Come
1 - GRANDEZZE E MISURE INDICE Grandezze fisiche e loro misure: 2 Notazione: 3 Prefissi: 4 Grandezze fondamentali e unità di misura: 5 Grandezze derivate: 9 Valori ed errori, incertezza di misura: 12 Come
Programma di CHIMICA E LABORATORIO
 Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Plesso «ALESSANDRO VOLTA» Programma di CHIMICA E LABORATORIO Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA Anno Scolastico
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Plesso «ALESSANDRO VOLTA» Programma di CHIMICA E LABORATORIO Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA Anno Scolastico
Didattica delle scienze (FIS/01)
 Facoltà di Studi Classici, Linguistici e della Formazione SCIENZE DELLA FORMAZIONE PRIMARIA (LM-85 bis) Lucia Quattrocchi Didattica delle scienze (FIS/01) Qualche informazione utile Testo consigliato Halliday
Facoltà di Studi Classici, Linguistici e della Formazione SCIENZE DELLA FORMAZIONE PRIMARIA (LM-85 bis) Lucia Quattrocchi Didattica delle scienze (FIS/01) Qualche informazione utile Testo consigliato Halliday
CHIMICA GENERALE ED INORGANICA I E LABORATORIO M - Z
 DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea in Chimica Anno accademico 2016/2017-1 anno CHIMICA GENERALE ED INORGANICA I E LABORATORIO M - Z 12 CFU - 1 semestre Docente titolare dell'insegnamento
DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea in Chimica Anno accademico 2016/2017-1 anno CHIMICA GENERALE ED INORGANICA I E LABORATORIO M - Z 12 CFU - 1 semestre Docente titolare dell'insegnamento
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301»
 «IIS Via Silvestri 301» Programma di CHIMICA E LABORATORIO Classe 1 a B Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti
«IIS Via Silvestri 301» Programma di CHIMICA E LABORATORIO Classe 1 a B Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti
Capitolo 1 Misure e grandezze
 Capitolo 1 Misure e grandezze 1. Il Sistema Internazionale di Unità di misura 2. Grandezze estensive e grandezze intensive 3. Energia, lavoro e calore 4. Temperatura e calore 5. Misure precise e misure
Capitolo 1 Misure e grandezze 1. Il Sistema Internazionale di Unità di misura 2. Grandezze estensive e grandezze intensive 3. Energia, lavoro e calore 4. Temperatura e calore 5. Misure precise e misure
SCIENZE BIOLOGICHE CHIMICA GENERALE CON ESERCITAZIONI A Discipline chimiche. 1 semestre Facoltativa Voto in trentesimi
 DIPARTIMENTO SCUOLA ANNO ACCADEMICO OFFERTA 2018/2019 ANNO ACCADEMICO EROGAZIONE 2018/2019 CORSO DILAUREA INSEGNAMENTO TIPO DI ATTIVITA' AMBITO CODICE INSEGNAMENTO 18246 SETTORI SCIENTIFICO-DISCIPLINARI
DIPARTIMENTO SCUOLA ANNO ACCADEMICO OFFERTA 2018/2019 ANNO ACCADEMICO EROGAZIONE 2018/2019 CORSO DILAUREA INSEGNAMENTO TIPO DI ATTIVITA' AMBITO CODICE INSEGNAMENTO 18246 SETTORI SCIENTIFICO-DISCIPLINARI
A.S. 2016/2017 PROGRAMMA SVOLTO E INDICAZIONI PER IL RECUPERO ESTIVO. Proff. ZANNI PAOLO e FRANCHINI MANUELA. docenti di ANALISI CHIMICA STRUMENTALE
 A.S. 2016/2017 PROGRAMMA SVOLTO E INDICAZIONI PER IL RECUPERO ESTIVO Proff. ZANNI PAOLO e FRANCHINI MANUELA docenti di ANALISI CHIMICA STRUMENTALE Classe 3^B Moduli Contenuti Mod. 1 L atomo e la mole,
A.S. 2016/2017 PROGRAMMA SVOLTO E INDICAZIONI PER IL RECUPERO ESTIVO Proff. ZANNI PAOLO e FRANCHINI MANUELA docenti di ANALISI CHIMICA STRUMENTALE Classe 3^B Moduli Contenuti Mod. 1 L atomo e la mole,
Corso di Chimica Dott.ssa Fioravanti
 Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Grandezze e Misure.
 Grandezze e Misure www.fisicaxscuola.altervista.org Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Strumenti di misura Misure dirette
Grandezze e Misure www.fisicaxscuola.altervista.org Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Strumenti di misura Misure dirette
METODO SPERIMENTALE. Per la comprensione di un fenomeno è importante individuare i fattori essenziali e distinguerli da quelli secondari.
 INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
INTRODUZIONE Scopo della Fisica è quello di fornire una descrizione quantitativa di tutti i fenomeni naturali, individuandone le proprietà significative (grandezze fisiche) ed analizzandone la loro interdipendenza
NUMERI. Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali
 NUMERI Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali N NUMERI Per contare i soldi del proprio conto in banca! 0,+1, 1,+2, 2,+3, 3,... Numeri interi Z NUMERI Per tagliare le torte! 0,1,-1,1/2,-1/2,2,-2,1/3,-1/3,2/3.-2/3,...
NUMERI Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali N NUMERI Per contare i soldi del proprio conto in banca! 0,+1, 1,+2, 2,+3, 3,... Numeri interi Z NUMERI Per tagliare le torte! 0,1,-1,1/2,-1/2,2,-2,1/3,-1/3,2/3.-2/3,...
CHIMICA. Primo anno. 1. Misure e grandezze. Abilità/Capacità Contenuti Tempi. disciplinari
 CHIMICA Primo anno 1. Misure e grandezze T 1 Osservare, descrivere ed riconoscere nelle sue varie forme i concetti di sistema e Applicare le unità di misura del Sistema Internazionale, i relativi prefissi
CHIMICA Primo anno 1. Misure e grandezze T 1 Osservare, descrivere ed riconoscere nelle sue varie forme i concetti di sistema e Applicare le unità di misura del Sistema Internazionale, i relativi prefissi
REGISTRO DELLE LEZIONI 2004/2005. Tipologia. Addì Tipologia. Addì Tipologia
 Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Unità di misura. Grandezze fisiche. Unità di Misura. Strumenti di misura. Grandezza fisica: qualsiasi proprietà della materia che può essere misurata
 Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Unità di misura Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Unità di misura Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO STATE TRATTE DAL LIBRO FONDAMENTI DI FISICA DI D. HALLIDAY,
CORSO DI BIOFISICA IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO STATE TRATTE DAL LIBRO FONDAMENTI DI FISICA DI D. HALLIDAY,
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Argomenti per il Recupero di Fisica
 Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica ed il Metodo Scientifico Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze
Argomenti per il Recupero di Fisica (I Quadrimestre) Lo scopo della Fisica ed il Metodo Scientifico Definizioni di Grandezza Fisica, Misura, Unità di Misura Sistemi di misura e Sistema Internazionale Grandezze
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
La materia e le sostanze. Trasformazioni fisiche e trasformazioni chimiche. Sommario
 1 La materia e le sostanze 2 Trasformazioni fisiche e trasformazioni chimiche 1 La materia attorno a noi 2 2 Dai miscugli alle sostanze 5 3 Le grandezze e la loro misurazione 8 4 Massa, volume e densità
1 La materia e le sostanze 2 Trasformazioni fisiche e trasformazioni chimiche 1 La materia attorno a noi 2 2 Dai miscugli alle sostanze 5 3 Le grandezze e la loro misurazione 8 4 Massa, volume e densità
1 Misurare una grandezza
 1 Misurare una grandezza DEFINIZIONE. Misurare una grandezza significa confrontarla con una grandezza dello stesso tipo, assunta come unità di misura, per stabilire quante volte quest ultima è contenuta
1 Misurare una grandezza DEFINIZIONE. Misurare una grandezza significa confrontarla con una grandezza dello stesso tipo, assunta come unità di misura, per stabilire quante volte quest ultima è contenuta
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 1 Misure e grandezze 3 Sommario 1. Le origini della chimica 2. Il metodo scientifico 3. Il Sistema Internazionale di unità di
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 1 Misure e grandezze 3 Sommario 1. Le origini della chimica 2. Il metodo scientifico 3. Il Sistema Internazionale di unità di
Capitolo 1 Misure e grandezze
 Capitolo 1 Misure e grandezze 1. Il Sistema Internazionale di Unità di misura 2. Grandezze estensive e grandezze intensive 3. Energia, lavoro e calore 4. Temperatura e calore 5. Misure precise e misure
Capitolo 1 Misure e grandezze 1. Il Sistema Internazionale di Unità di misura 2. Grandezze estensive e grandezze intensive 3. Energia, lavoro e calore 4. Temperatura e calore 5. Misure precise e misure
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012
 CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 U01 U.01 Fondamenti U.01 Fondamenti 1/29 SISTEMI TERMODINAMICI E LORO PROPRIETA U.01 Fondamenti 2/29 1 CONCETTI FONDAMENTALI DELLA TERMODINAMICA
CONTROLLO TERMICO DEI SISTEMI DI CALCOLO A.A. 2011/2012 U01 U.01 Fondamenti U.01 Fondamenti 1/29 SISTEMI TERMODINAMICI E LORO PROPRIETA U.01 Fondamenti 2/29 1 CONCETTI FONDAMENTALI DELLA TERMODINAMICA
Scienza dei Materiali 1 Esercitazioni
 Scienza dei Materiali 1 Esercitazioni 1. Introduzione ver. 1.1 Errori più comuni Errori di concetto Non si è capito il problema Errori di memoria Non si ricorda la formula Errori di precisione/accuratezza
Scienza dei Materiali 1 Esercitazioni 1. Introduzione ver. 1.1 Errori più comuni Errori di concetto Non si è capito il problema Errori di memoria Non si ricorda la formula Errori di precisione/accuratezza
Sistemi di unità di Misura
 Sistemi di unità di Misura Costruzione di un sistema di unità di misura: 1) Scegliere un particolare gruppo ( 4) di grandezze fisiche (lunghezza, tempo, massa, velocità, accelerazione, energia, potenza,
Sistemi di unità di Misura Costruzione di un sistema di unità di misura: 1) Scegliere un particolare gruppo ( 4) di grandezze fisiche (lunghezza, tempo, massa, velocità, accelerazione, energia, potenza,
Unità di misura. Grandezze fisiche. Unità di Misura. Grandezza fisica: qualsiasi proprietà della materia che può essere misurata
 Unità di misura Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Unità di misura Grandezze fisiche Grandezza fisica: qualsiasi proprietà della materia che può essere misurata Grandezze estensive: dipendono dalle quantità di materia ADDITIVE Es: volume, massa, calore
Grandezze e Misure.
 Grandezze e Misure www.fisicaxscuola.altervista.org Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Strumenti di misura Misure dirette
Grandezze e Misure www.fisicaxscuola.altervista.org Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Strumenti di misura Misure dirette
GRANDEZZE FISICHE UNITÀ DI MISURA E CALCOLI
 Capitolo 1 GRANDEZZE FISICHE UNITÀ DI MISURA E CALCOLI N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof.
Capitolo 1 GRANDEZZE FISICHE UNITÀ DI MISURA E CALCOLI N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof.
