Gli strumenti della Chimica Quantitativa (cap. 1)
|
|
|
- Mariangela Lia Bondi
- 6 anni fa
- Visualizzazioni
Transcript
1 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale CCS CHI e MAT Gli strumenti della Chimica Quantitativa (cap. 1) Prof. Dipartimento CMIC Giulio Natta
2 Misure e Calcoli Scientifici: Cifre Significative e Accuratezza/Precisione 2 Misure Ottenute con specifiche strumentazioni Si determinano i valori in unità di misura Si determina l'incertezza della misura Accuratezza e precisione errore vs. deviazione regole diverse ; + e - ; x e / ; log e 10 x numeri esatti - possiedono un numero infinito di cifre significative. Metodo del fattore etichetta fattori di conversione sono uguali a uno usati per cambiare le unità di misura
3 Unità di Misura 3 Osservazione qualitativa vs. quantitativa Tutte le quantità misurate si compongono di un numero e di una unità. I rapporti tra grandezze portano a rapporti tra numeri, p.es. km/ora. Per minimizzare gli errori, bisogna includere le unità in TUTTI i calcoli. Nel rispondere ad un problema, specificare le unità! Esempi: Un tetto di 3 m per 4 m copre un area di (3 m) (4 m) = 12 m 2 Un auto che percorre 700 chilometri in 7 ore ha una velocità di: (700 km) : (7 ore) = 100 km/ora (o meglio km h -1 adottato nel corso). unità base : Unità SI - m, kg, s, L, K, mol, cd unità derivate: J, C, N, atm, pascal * Il sistema SI è stato adottato nel Per i dettagli vedere:
4 Sistema Internazionale (SI) 4 UNITA' BASE SISTEMA S.I. GRANDEZZA NOME SIMBOLO S. dimens. Lunghezza Metro m L Massa Chilogrammo kg M Tempo Secondo s T Corrente elettrica Ampere A I Temperatura Kelvin K Θ Quantità di sostanza Mole mol N Intensità luminosa Candela cd J
5 Campioni di Riferimento 5 CAMPIONI DI RIFERIMENTO NEL SISTEMA S.I. Entità Fisica Massa (kg) Lunghezza (m) Tempo (s) Temperatura (K) Valore Definito (S.I.) 1 Kg = massa di un cilindro di lega platino-iridio (1900) 1 m = distanza percorsa dalla luce nel vuoto in 1 / sec (1983) 1 s = tempo intercorso per l'isotopo 133 Cs per effettuare vibrazioni (1967) Assumendo 0 K allo zero assoluto e al punto triplo dell'acqua (1967)
6 Prefissi S.I. e loro Simboli 6 PREFISSI S.I. E LORO SIMBOLI FRAZIONI Simbolo MULTIPLI Simbolo 10-1 d (deci-) 10 d (deca-) 10-2 c (centi-) 10 2 h (etto-) 10-3 m (milli-) 10 3 k (chilo-) 10-6 µ (micro-) 10 6 M (mega-) 10-9 n (nano-) 10 9 G (giga-) p (pico-) T (tera-) f (femto-) P (peta-) Tera Giga Mega Chilo - Milli Micro Nano T 1,000,000,000,000 bilione (e: trillion) G 1,000,000,000 miliardo (e: billion) M 1,000,000 milione k 1,000 migliaia - 1 uno m millesimo µ 0.000,001 milionesimo n 0.000,000,001 miliardesimo
7 Unità Derivate e Notazione Dimensionale 7 Tutte le altre grandezze misurabili sono definite mediante relazioni matematiche - leggi fisiche sperimentali - e per esse vengono definite delle unità derivate (che sottostanno alle stesse operazioni dei numeri coinvolti nelle relazioni/leggi). 2 Area = lunghezza lunghezza; m = m m distanza metri m Velocità = = ; v= = m s tempo secondo s Ogni grandezza misurabile è pertanto caratterizzata da un fattore di conversione (relazione fra diverse unità di misura) Convenzione usata: si adotta la notazione esponenziale!!! massa = volume 3 densità ( kg m ) 1
8 Fattori di Conversione 8 Molto spesso bisogna passare da una unità all altra. Per esempio, per convertire gli Angstrom (una distanza tipica di due atomi legati) in metri, vale l eguaglianza: m = 1 Å Si può costruire il così detto fattore di conversione in due modi: m Å = 1Å 1Å m 1Å o 1Å 10 = 10 m 10 1Å 10 m = 1 = 10 Si può moltiplicare ogni numero per questo fattore di conversione e ciò corrisponde a moltiplicare per m m
9 Strategia per Problemi di Conversione delle Unità 9 1. Identificare la destinazione, incluse le unità 2. Scegliere un punto di partenza 3. Elencare i fattori di conversione richiesti 4. Moltiplicare le misure di partenza per i fattori di conversione 5. Controllare se la risposta ottenuta ha senso.
10 Un Esempio di Fattore di Conversione 10 Esempio: Qual è il volume in cm 3 di un recipiente di 0.6 litri (L)? Si parte scrivendo quanto si vuol calcolare sul lato sinistro del segno =, e mettendo sulla destra le informazione in possesso? cm 3 = 0.6 litri Si decide quindi quale fattore di conversione si deve usare. Scegliere quello che fornisce l adatta cancellazione delle unità cm? cm = 0.6 1litro = 600 cm 3 litri Notare come le unità si elidono, lasciando il risultato nell unità desiderata di cm 3
11 Relazioni di Volume in S.I ml = 1 cm 3 = 10-3 dm 3 = 10-3 L = 10-6 m 3
12 Esempio di Conversione Sistema Inglese - Sistema Metrico 12 Una montagna è alta 3212 ft. Qual è l altezza in unità di metri? Il fattore di conversione fra miglia (mi) e chilometri (km) si può dedurre impiegando due fattori di conversione: 1 ft = mi km = 1 mi 1 km = 1000 m Fase I: scrivere le informazioni sulla destra? m = 3212 ft Fase II: moltiplicare per 3 successivi fattori di conversione.
13 Esempio (con.) mi km 1000 m? m = 3212 ft = 979 m 1ft 1mi 1km ft mi km m L uso dei fattori di conversione nei problemi si chiama Analisi Dimensionale.
14 Unità di Misura dell Energia 14 L energia si esprime in due forme principali: Calore e Movimento L unità fondamentale SI dell energia è il joule joule (J) = N m = kg m 2 s 2 Il joule è una energia molto piccola; 1 J è sufficiente ad innalzare la temperatura di 1 ml di acqua di ~0.25 C La caloria (cal) è una unità opzionale, vale 4.18 J 3000 kcal per una dieta giornaliera = J = 12.5 MJ Tutti i tipi di attività fisiche si possono valutare in termini di energia Combustione di combustibili 1 m 3 di gas naturale = J Lavoro fisico umano 1 ora di duro lavoro = J Produzione di un prodotto Energia in un veicolo = J kg -1
15 Classificazioni della Materia 15 Sostanze Pure - composizioni fisse Atomi Elementi Molecole Composti Miscele - ampia varietà di composizioni Leghe Soluzioni Conglomerati, ecc.
16 Massa 16 La massa di un oggetto si riferisce alla quantità di materia che contiene. L Unità S.I. è il chilogrammo (kg). Il peso di un oggetto è la forza esercitata da una massa dovuta al campo gravitazionale locale. La massa di uno specifico oggetto sarà la stessa sulla terra e sulla luna, ed è indipendente dalla gravità. Il peso di tale oggetto può però differire, poiché sulla luna la costante gravitazionale è 1/6 di quella della terra.
17 Esempio di Conversione di Unità di Massa 17 Problema: Se una goccia di pioggia pesa 65 mg in media, e cadono ogni minuto su un area di 10 m gocce, quale è la massa totale di pioggia (in kg) che cade su un area di 50 m 2 in 1.5 ore? Fase I: Assemblare il problema. 4? kg gocce 65 mg 1 kg 60 min = m hr min 10 m 1 goccia 1 10 mg hr Fase II: Risolvere kg kg hr m kg m hr 2? = = = 20 kg 2 m hr
18 Densità e Gravità Specifica 18 Densià t = massa volume volume = massa densità Si può riarrangiare: massa = densità volume L unità SI della densità è il kg m -3 (!! g dm -3 ) Gravità specifica = densità della sostanza densità dell'acqua
19 Calcoli sulla Densità - Esempio 19 Problema. Se un pezzo rettangolare di litio metallico di dimensioni 29.0 mm, 11.1 mm e 11.9 mm ha una massa di mg, quale è la densità del litio in g cm -3? Usare densità = massa volume volume = 11.1 mm 29.0 mm 11.9 mm = mm 3 = 3.83 cm 3 1 g? g = mg = 1.49 g 1000 mg 1.49 g densità = = g cm cm 3 3
20 Densità di Sostanze Comuni 20 Sostanza Stato Fisico Densità (g cm -3 ) Idrogeno gas Ossigeno gas Alcol etilico liquido Acqua liquido Sale da cucina solido 2.16 Alluminio solido 2.70 Piombo solido 11.3 Oro solido 19.3 A temperatura ambiente (20 C) e pressione atmosferica normale (1 atm).
21 Temperatura 21 La Temperatura è la misura di quanto calda o fredda è una sostanza rispetto ad un altra. Il calore è l energia che fluisce fra oggetti che si trovano a temperature differenti. Il termometro misura la temperatura, non il calore. Unità di Misura: Kelvin (K), (si noti: non preceduto dal segno di grado ). La scala Kelvin è una scala assoluta. Non esiste T < 0 K. Scala Celsius ( C) : definizione (è una scala relativa!) 0 C pari al punto di congelamento del ghiaccio. 100 C pari al punto di ebollizione dell acqua a 1 atm.
22 Unità e Fattori di Conversione della Temperatura 22 Scala Fahrenheit : T(in C) = T(in K) T(in K) = T(in C) F definita come il punto di congelamento dell acqua 212 F definita come il punto di ebollizione dell acqua. 9 T(in F) = T(in C) T(in C) = T(in F) 32 9
23 Unità di Misura della Temperatura: le Tre Scale 23 Temperatura L acqua bolle Intervallo di 100 gradi Intervallo di 100 gradi Intervallo di 100 gradi Temperatura corporea normale L acqua ghiaccia Scala Kelvin Scala Celsius Scala Fahrenheit
24 Alcune Temperature Significative K 10 3 K 10 2 K 10 1 K 0 K : Superficie del Sole (interno ~10 7 K) 3683: Il più alto punto di fusione di un elemento (tungsteno)) 1337: Punto di fusione dell oro 600: Punto di fusione del Piombo 373: Punto di ebollizione dell acqua H 2 O 370: Giorno sulla Luna 273: Punto di fusione di H 2 O 140: Macchia estesa di Giove 120: Notte sulla Luna 90: Punto di ebollizione dell Ossigeno 27: Punto di ebollizione del Neon Zero Assoluto (temperatura più bassa raggiunta ~10-6 K)
25 Unità di Misura Derivate 25 Grandezza Definizione Dimensione Unità di misura cgs SI Lunghezza I L cm Metro (m) Superficie S = l 2 L 2 cm 2 m 2 Volume V = l 3 L 3 cm 3 m 3 Tempo t t s Secondo (s) Frequenza t -1 t -1 Hertz (s -1 ) Hertz (s -1 ) Accelleraz. a = v t -1 L t -2 cm s -2 m s -2
26 Unità di Misura 26 Unità di misura Grandezza Definizione Dimensione cgs SI Chilogrammo Massa m M g (kg) Densità m d = M L -3 g cm -3 Kg m -3 V Forza F = m a M L t -2 Dine (g cm s -2 ) Pressione Lavoro o Energia Newton (N) (Kg m s -2 ) F P = M L -1 t -2 dine cm -2 Pascal (Pa) S (Newton m -2 ) w = F l 1 E = mv 2 2 M L 2 t -2 erg (dine cm) Joule (J) (Newton m)
27 Unità di Misura 27 Grandezza Definizione Dimensione Corrente elettrica Carica elettrica q = I t I t Unità di misura (SI) I I Ampere (A) Coulomb (C) (A s) Forza elettromotrice Resistenza elettrica Potenza f. e. m. = R E q M L 2 t -3 I -1 Volt (V) (J A -1 s -1 ) f. e. m. I (V A -1 ) w P = M L 2 t -3 Watt (W) t (J s -1 ) = M L 2 t -3 I -2 Ohm (Ω)
28 Unità di Misura 28 Grandezza Definizione Dimensione Sistema SI Temperatura T T Kelvin (K) Capacità termica Calore specifico Quantità di materia Intensità luminosa E C = T C c = m M L 2 t -2 T -1 J K -1 L2 t-2 T-1 J Kg-1 K-1 n n Mole (mol) I v I v Candela (cd)
29 Alcuni Fattori di Conversione 29 Grandezza Nome Simbolo Espressione unità SI Lunghezza... Peso... Peso Ångstrom grammo gamma Å g γ m 10-3 kg kg Volume... Forza... litro dina l dine 10-3 m N Pressione... Pressione... atmosfera mm di Hg atm mm Hg (Torr) Pa Pa Energia... Energia, calore... Energia... erg caloria kilocaloria elettron-volt erg cal kcal ev 10-7 J J J = kj J Temperatura... grado Celsius C 0 K = C Handbook of Chemistry and Physics, CRC Press.
30 Incertezza nelle Misure 30 Una certa incertezza è associata a tutte le misure. La nostra capacità di saper misurare una quantità esattamente è limitata da molti fattori: I dispositivi di misura sono realizzati con specifiche limitate. I sensi e l abilità nel leggere i dispositivi di misura è imperfetta. L incertezza si può esprimere usando il segno ± per delimitare l intervallo della quantificazione: per es ± kg di un composto chimico. Spesso, il segno ± viene eliminato, e il valore si scrive in modo che il numero di cifre nel numero implica l incertezza (2.036 indica che l imprecisione è sulla 4 a cifra significativa).
31 Cifre Significative 31 Una misura viene annotata in modo tale da risultare incerta l ultima cifra (quella più a destra). Significativo nella scienza è sinonimo di misurato. Il numero di cifre significative in un numero è proprio il numero di cifre nel numero registrato, inclusa quella incerta (quella più a destra). Il numero kg possiede 4 cifre significative, implicando una incertezza di 1 g. Il numero 2.0 kg ha 2 cifre significative, anche se l ultimo numero è uno zero. Poiché si include lo zero, vuol dire che si sa per certo che la misura sperimentale è compresa tra 1.9 e 2.1 (con un errore di ± 0.1) per cui la cifra zero è significativa.
32 Il Numero di Cifre Significative in una Misura 32 Gradazione più precisa sul dispositivo A B
33 Determinazione del N di Cifre Significative 33 In generale, tutte le cifre sono significative eccetto quelle usate per posizionare il punto decimale.* 1. Accertare se il numero ha un punto decimale. 2. Partire dalla sinistra e spostarsi a destra fino a raggiungere la prima cifra diversa da zero. 3. Contare le cifre e ogni cifra alla destra come significative. A) gli zero dopo o prima (interni) del decimale si contano come significativi. B) se non c è il punto,* gli zero non sono significativi e cifre sig mg 5 cifre sig e g K ml m L * Virgola nella notazione italiana comune
34 Numeri Esatti 34 I numeri esatti possono far parte della definizione di unità: ci sono esattamente 60 secondi in 1 minuto. Qui, il numero 60 si può considerare avere un numero infinito di cifre significative. Altri numeri esatti sono quelli deputati al conteggio di singoli oggetti, Ci sono 120 studenti in questa classe. Ci sono 24 capitoli nel testo di Chimica. In un calcolo, 120 e 24 si possono considerare avere un numero infinito di cifre significative.
35 Cifre Significative nei Calcoli 35 Se un calcolo fornisce un numero con troppe cifre, lo si deve arrotondare. Le seguenti regole ci forniscono le relative cifre significative. Ricordarsi! 1. Moltiplicazione e divisione: il risultato contiene lo stesso numero di cifre significative della misura con il minor numero di cifre significative 9.2 cm 6.80 cm cm = cm 3 = 23 cm 3 2. Addizione e sottrazione: il risultato ha lo stesso numero di decimali della misura con il minor numero di decimali ml ml = ml = ml
36 Regole di Arrotondamento Se la cifra rimossa è superiore a 5, il numero che la precede viene aumentato di 1. Così si arrotonda a 5.38 con 3 cifre significative. 2. Se la cifra rimossa è inferiore a 5, il numero che la precede non si modifica. Così, si arrotonda a Se la cifra rimossa è pari a 5, seguita solo da zeri: a) se quella che precede è pari, non si cambia. b) se quella che precede è dispari, si aumenta di Se la cifra rimossa è pari a 5, senza cifre non zero successive: quella che precede si aumenta di 1. Tenere sempre 2 o 3 cifre significative extra nel corso di calcoli successivi, quindi arrotondare alla fine.
37 Precisione, Accuratezza e Errore 37 Precisione: si riferisce a quanto vicine sono le misure tra loro in una serie. Accuratezza: si riferisce a quanto vicina è una misura al numero reale. Errore Casuale: errori nelle singole misure che sono sia superiori che inferiori al valore vero. Errore Sistematico: errori che producono valori che sono o sempre superiori o inferiori al valore vero.
38 Precisione vs. Accuratezza 38 A C Massa (g) di acqua Massa (g) di acqua Numero di prove Numero di prove B D Massa (g) do acqua Massa (g) di acqua Numero di prove Numero di prove A) alta precisione e alta accuratezza B) alta precisione e bassa accuratezza C) bassa precisione e alta accuratezza D) bassa precisione e accuratezza
39 Precisione vs. Accuratezza 39 Precisione Riproducibilità Verificata con misure ripetute Una scarsa precisione deriva da strumentazione di prestazioni modeste Accuratezza Correttezza Verificata tramite metodi diversi Una scarsa accuratezza deriva da inadeguate procedure o difetti di strumentazione
40 Deviazione Standard 40 Il grado di dispersione dei valori sperimentali per una stessa grandezza fornisce una serie di misure più o meno accorpate attorno ad un valore. Ciò è legato ad un insieme di errori "sistematici" o "casuali" che possono essere contenuti ma mai annullati. Un modo tipico per valutare il grado di dispersione di una serie di misure è il calcolo della deviazione standard secondo la formula: N i= 1 σ = ( x µ ) i N * dove: σ = deviazione standard x i = singola misura (i) m = media delle misure N = numero totale delle misure N* = N-1 (se poche) ed N (se molte) Detto in parole: data una distribuzione statistica X composta da N valori numerici, la deviazione standard è la radice quadrata della media aritmetica degli scarti assoluti tra i valori della distribuzione { x 1, x 2,..., x N } e un valore medio (μ).
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Cifre significative delle misure di grandezze fisiche
 Cifre significative delle misure di grandezze fisiche Si definiscono grandezze fisiche tutte quelle entità con cui vengono descritti i fenomeni fisici e che sono suscettibili di una definizione quantitativa,
Cifre significative delle misure di grandezze fisiche Si definiscono grandezze fisiche tutte quelle entità con cui vengono descritti i fenomeni fisici e che sono suscettibili di una definizione quantitativa,
Misure e Unità di Misura
 2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
1 - GRANDEZZE E MISURE
 1 - GRANDEZZE E MISURE INDICE Grandezze fisiche e loro misure: 2 Notazione: 3 Prefissi: 4 Grandezze fondamentali e unità di misura: 5 Grandezze derivate: 9 Valori ed errori, incertezza di misura: 12 Come
1 - GRANDEZZE E MISURE INDICE Grandezze fisiche e loro misure: 2 Notazione: 3 Prefissi: 4 Grandezze fondamentali e unità di misura: 5 Grandezze derivate: 9 Valori ed errori, incertezza di misura: 12 Come
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 1 Misure e grandezze 3 Sommario 1. Le origini della chimica 2. Il metodo scientifico 3. Il Sistema Internazionale di unità di
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 1 Misure e grandezze 3 Sommario 1. Le origini della chimica 2. Il metodo scientifico 3. Il Sistema Internazionale di unità di
ANALISI CHIMICO FARMACEUTICA I
 Prof. Gianluca Sbardella : 089 969770 : gsbardella@unisa.it L INCERTEZZA E LE CIFRE SIGNIFICATIVE Tutte le misure sono affette da un certo grado di incertezza la cui entità può dipendere sia dall operatore
Prof. Gianluca Sbardella : 089 969770 : gsbardella@unisa.it L INCERTEZZA E LE CIFRE SIGNIFICATIVE Tutte le misure sono affette da un certo grado di incertezza la cui entità può dipendere sia dall operatore
UNITA DI MISURA BASE
 Revisione del 2/9/15 ISTITUTO TECNICO INDUSTRIALE V.E.MARZOTTO Valdagno (VI) Corso di Fisica prof. Nardon UNITA DI MISURA BASE Richiami di teoria Il Sistema Internazionale (S.I.) di unità di misura è composto
Revisione del 2/9/15 ISTITUTO TECNICO INDUSTRIALE V.E.MARZOTTO Valdagno (VI) Corso di Fisica prof. Nardon UNITA DI MISURA BASE Richiami di teoria Il Sistema Internazionale (S.I.) di unità di misura è composto
Corso di Chimica Dott.ssa Fioravanti
 Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Unità di Misura Unità di misura LA MISURA "La misura è la determinazione delle dimensioni, della capacità, della quantità o dell estensione di qualcosa" NUMERI ESATTI E APPROSSIMATI Un numero esatto ha
Importanza delle incertezze nelle misure fisiche
 Importanza delle incertezze nelle misure fisiche La parola errore non significa equivoco o sbaglio Essa assume il significato di incertezza da associare alla misura Nessuna grandezza fisica può essere
Importanza delle incertezze nelle misure fisiche La parola errore non significa equivoco o sbaglio Essa assume il significato di incertezza da associare alla misura Nessuna grandezza fisica può essere
NUMERI. q Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali
 Contare, misurare. q Quanti denti ha un cane? Da adulto 42, se cucciolo 28 q Quanto è lunga la coda di una marmotta? Circa 20 cm q Quanto liquido contiene un cucchiaio da minestra? Circa 15 ml q Quanto
Contare, misurare. q Quanti denti ha un cane? Da adulto 42, se cucciolo 28 q Quanto è lunga la coda di una marmotta? Circa 20 cm q Quanto liquido contiene un cucchiaio da minestra? Circa 15 ml q Quanto
SINTESI 0. Grandezze e unità di misura
 Le grandezze fisiche Per studiare la composizione e la struttura della materia e le sue trasformazioni, la chimica e le altre scienze sperimentali si basano sulle grandezze fisiche, cioè su proprietà che
Le grandezze fisiche Per studiare la composizione e la struttura della materia e le sue trasformazioni, la chimica e le altre scienze sperimentali si basano sulle grandezze fisiche, cioè su proprietà che
Le Grandezze Fisiche e la loro Misura
 FISICA: Le Grandezze Fisiche e la loro Misura Giancarlo Zancanella (2009) 1 1 Le Grandezze Fisiche Si chiamano grandezze fisiche le proprietà dei corpi che possono essere misurate La forma, la bellezza
FISICA: Le Grandezze Fisiche e la loro Misura Giancarlo Zancanella (2009) 1 1 Le Grandezze Fisiche Si chiamano grandezze fisiche le proprietà dei corpi che possono essere misurate La forma, la bellezza
La Misura Esercizi guida con soluzioni
 La misura Esercizi guida (UbiMath) - 1 La Misura Esercizi guida con soluzioni Grandezze e sistema metrico decimale Scrivi in forma di numerica e come potenza di dieci i seguenti prefissi SI. 1. mega- =
La misura Esercizi guida (UbiMath) - 1 La Misura Esercizi guida con soluzioni Grandezze e sistema metrico decimale Scrivi in forma di numerica e come potenza di dieci i seguenti prefissi SI. 1. mega- =
FORMULE INVERSE. Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso.
 FORMULE INVERSE FORMULE INVERSE Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso. FORMULE INVERSE Nello studio della fisica si incontrano
FORMULE INVERSE FORMULE INVERSE Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso. FORMULE INVERSE Nello studio della fisica si incontrano
Costruiamo la STRISCIA DELLE MISURE. decametro metro decimetro. Tm Gm Mm km hm dam m dm cm mm µm nm pm
 Terametro Gigametro Megametro chilometro ettometro decametro metro decimetro micrometro millimetro milcrometro nanometro picometro Costruiamo la STRISCIA DELLE MISURE. Tm Gm Mm km hm dam m dm cm mm µm
Terametro Gigametro Megametro chilometro ettometro decametro metro decimetro micrometro millimetro milcrometro nanometro picometro Costruiamo la STRISCIA DELLE MISURE. Tm Gm Mm km hm dam m dm cm mm µm
Cifre significative. Andrea Bussani. 4 novembre 2012
 Cifre significative Andrea Bussani 4 novembre 2012 Numero di cifre significative Valore misura Cifre significative Numero di cifre significative (evidenziate in rosso) 12 12 2 12,5 12,5 3 1,25 1,25 3 125
Cifre significative Andrea Bussani 4 novembre 2012 Numero di cifre significative Valore misura Cifre significative Numero di cifre significative (evidenziate in rosso) 12 12 2 12,5 12,5 3 1,25 1,25 3 125
MODULO 1 Le grandezze fisiche
 MODULO 1 Le grandezze fisiche Quante volte, ogni giorno, utilizziamo il metro, i secondi, i kilogrammi Ma forse non sappiamo quante menti di uomini ingegnosi hanno dato un senso a quei simboli per noi
MODULO 1 Le grandezze fisiche Quante volte, ogni giorno, utilizziamo il metro, i secondi, i kilogrammi Ma forse non sappiamo quante menti di uomini ingegnosi hanno dato un senso a quei simboli per noi
Metodologie informatiche per la chimica
 Metodologie informatiche per la chimica Dr. Sergio Brutti Metodologie di analisi dei dati Strumenti di misura Uno strumento di misura e un dispositivo destinato a essere utilizzato per eseguire una misura,
Metodologie informatiche per la chimica Dr. Sergio Brutti Metodologie di analisi dei dati Strumenti di misura Uno strumento di misura e un dispositivo destinato a essere utilizzato per eseguire una misura,
IIS Moro Dipartimento di matematica e fisica
 IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
Accuratezza, precisione, tipi di errori e cifre significative dei dati analitici.
 Accuratezza, precisione, tipi di errori e cifre significative dei dati analitici. Indice: 1. Lettura della buretta pag.2 2. Precisione ed Accuratezza pag.3 3. Tipi di errori pag.4 4. Affidabilità di una
Accuratezza, precisione, tipi di errori e cifre significative dei dati analitici. Indice: 1. Lettura della buretta pag.2 2. Precisione ed Accuratezza pag.3 3. Tipi di errori pag.4 4. Affidabilità di una
Richiami di aritmetica(2)
 Richiami di aritmetica() Frazioni definizioni, operazioni, espressioni Numeri decimali Rapporti e proporzioni Percentuali Materia Matematica Autore Mario De Leo Le frazioni La frazione è un operatore che
Richiami di aritmetica() Frazioni definizioni, operazioni, espressioni Numeri decimali Rapporti e proporzioni Percentuali Materia Matematica Autore Mario De Leo Le frazioni La frazione è un operatore che
Tabella 1: Denominazioni dei principali multipli e sottomultipli decimali delle grandezze fisiche
 Unità di misura e fattori di conversione; potenze del 10; notazione scientica La misura di una grandezza va sempre riferita ad una data unità di misura: il metro(m), il grammo (g), e il secondo (s). A
Unità di misura e fattori di conversione; potenze del 10; notazione scientica La misura di una grandezza va sempre riferita ad una data unità di misura: il metro(m), il grammo (g), e il secondo (s). A
MODULO 1. Conoscere e misurare le grandezze
 Prof. M. C. Capizzo MODULO 1 Conoscere e misurare le grandezze Cos è la Fisica? Indagine sulla natura con gli strumenti matematici MECCANICA TERMODINAMICA ELETTROMAGNETISMO movimento dei corpi fenomeni
Prof. M. C. Capizzo MODULO 1 Conoscere e misurare le grandezze Cos è la Fisica? Indagine sulla natura con gli strumenti matematici MECCANICA TERMODINAMICA ELETTROMAGNETISMO movimento dei corpi fenomeni
Somma di numeri floating point. Algoritmi di moltiplicazione e divisione per numeri interi
 Somma di numeri floating point Algoritmi di moltiplicazione e divisione per numeri interi Standard IEEE754 " Standard IEEE754: Singola precisione (32 bit) si riescono a rappresentare numeri 2.0 10 2-38
Somma di numeri floating point Algoritmi di moltiplicazione e divisione per numeri interi Standard IEEE754 " Standard IEEE754: Singola precisione (32 bit) si riescono a rappresentare numeri 2.0 10 2-38
UNIVERSITA DEGLI STUDI DI CAGLIARI FACOLTÁ DI INGEGNERIA E ARCHITETTURA. Laurea in Scienze dell Archite?ura. FISICA TECNICA AMBIENTALE a.a.
 UNIVERSITA DEGLI STUDI DI CAGLIARI FACOLTÁ DI INGEGNERIA E ARCHITETTURA Laurea in Scienze dell Archite?ura FISICA TECNICA AMBIENTALE a.a. 2013-2014 Grandezze e Unità di Misura Docente: Indice: Grandezze
UNIVERSITA DEGLI STUDI DI CAGLIARI FACOLTÁ DI INGEGNERIA E ARCHITETTURA Laurea in Scienze dell Archite?ura FISICA TECNICA AMBIENTALE a.a. 2013-2014 Grandezze e Unità di Misura Docente: Indice: Grandezze
Lezione 4. Sommario. L artimetica binaria: I numeri relativi e frazionari. I numeri relativi I numeri frazionari
 Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Lezione 4 L artimetica binaria: I numeri relativi e frazionari Sommario I numeri relativi I numeri frazionari I numeri in virgola fissa I numeri in virgola mobile 1 Cosa sono inumeri relativi? I numeri
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Lezione 2 - Grandezze e Unità di misura -
 Insegnamento di OPERAZIONI UNITARIE DELLA TECNOLOGIA ALIMENTARE Corso di Laurea in Scienze e Tecnologie Alimentari Prof. Marco Poiana Lezione 2 - Grandezze e Unità di misura - Grandezza fisica: Entità
Insegnamento di OPERAZIONI UNITARIE DELLA TECNOLOGIA ALIMENTARE Corso di Laurea in Scienze e Tecnologie Alimentari Prof. Marco Poiana Lezione 2 - Grandezze e Unità di misura - Grandezza fisica: Entità
codifica in virgola mobile (floating point)
 codifica in virgola mobile (floating point) Del tutto simile a cosiddetta notazione scientifica o esponenziale Per rappresentare in modo compatto numeri molto piccoli o molto grandi e.g. massa dell elettrone
codifica in virgola mobile (floating point) Del tutto simile a cosiddetta notazione scientifica o esponenziale Per rappresentare in modo compatto numeri molto piccoli o molto grandi e.g. massa dell elettrone
METODI DI CONVERSIONE FRA MISURE
 METODI DI CONVERSIONE FRA MISURE Un problema molto frequente e delicato da risolvere è la conversione tra misure, già in parte introdotto a proposito delle conversioni tra multipli e sottomultipli delle
METODI DI CONVERSIONE FRA MISURE Un problema molto frequente e delicato da risolvere è la conversione tra misure, già in parte introdotto a proposito delle conversioni tra multipli e sottomultipli delle
PIANO DI LAVORO DEL DOCENTE prof. Rossi Manuela A.S. 2015/2016 CLASSE: 1ALL MATERIA: Scienze Naturali
 PIANO DI LAVORO DEL DOCENTE prof. Rossi Manuela A.S. 2015/2016 CLASSE: 1ALL MATERIA: Scienze Naturali Modulo n.1 - Introduzione alle scienze: il metodo scientifico e misure e grandezze. Collocazione temporale:
PIANO DI LAVORO DEL DOCENTE prof. Rossi Manuela A.S. 2015/2016 CLASSE: 1ALL MATERIA: Scienze Naturali Modulo n.1 - Introduzione alle scienze: il metodo scientifico e misure e grandezze. Collocazione temporale:
Numeri frazionari. sistema posizionale. due modi: virgola fissa virgola mobile. posizionale, decimale
 Numeri frazionari sistema posizionale due modi: virgola fissa virgola mobile posizionale, decimale 0,341=tre decimi più quattro centesimi più un millesimo cifre dopo la virgola: decimi centesimi millesimi
Numeri frazionari sistema posizionale due modi: virgola fissa virgola mobile posizionale, decimale 0,341=tre decimi più quattro centesimi più un millesimo cifre dopo la virgola: decimi centesimi millesimi
Sistemi di unità di misura
 Sistemi di unità di misura L Assemblea Nazionale Francese avvia nel 1790 l adozione di un sistema di unità di misura, che possa essere comune per tutto il genere umano. Prima di questa data ( e anche dopo
Sistemi di unità di misura L Assemblea Nazionale Francese avvia nel 1790 l adozione di un sistema di unità di misura, che possa essere comune per tutto il genere umano. Prima di questa data ( e anche dopo
INCERTEZZA DI MISURA SECONDO NORME CEI
 CORSO DI FORMAZIONE AMBIENTALE TECNICHE DI MISURA DEI CAMPI ELETTROMAGNETICI IN ALTA E BASSA FREQUENZA INCERTEZZA DI MISURA SECONDO NORME CEI Ing. Valeria Canè Servizio Agenti Fisici 1 UNA MISURA E un
CORSO DI FORMAZIONE AMBIENTALE TECNICHE DI MISURA DEI CAMPI ELETTROMAGNETICI IN ALTA E BASSA FREQUENZA INCERTEZZA DI MISURA SECONDO NORME CEI Ing. Valeria Canè Servizio Agenti Fisici 1 UNA MISURA E un
Richiami di aritmetica
 Richiami di aritmetica I numeri naturali L insieme dei numeri naturali, che si indica con N, comprende tutti i numeri interi maggiori di zero. Operazioni fondamentali OPERAZIONE SIMBOLO RISULTATO TERMINI
Richiami di aritmetica I numeri naturali L insieme dei numeri naturali, che si indica con N, comprende tutti i numeri interi maggiori di zero. Operazioni fondamentali OPERAZIONE SIMBOLO RISULTATO TERMINI
La quantità chimica LA MOLE
 La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
 Misurazione di una grandezza fisica Definizione operativa: Grandezza fisica Proprietà misurabile Sensazione di caldo/freddo Temperatura NO (soggettiva, diversa per ciascuno) SI (oggettiva, uguale per tutti)
Misurazione di una grandezza fisica Definizione operativa: Grandezza fisica Proprietà misurabile Sensazione di caldo/freddo Temperatura NO (soggettiva, diversa per ciascuno) SI (oggettiva, uguale per tutti)
1) Il grafico rappresenta la quantità di acqua contenuta in una vasca da bagno al passare del tempo.
 ESERCIZI DI SCIENZE 1) Il grafico rappresenta la quantità di acqua contenuta in una vasca da bagno al passare del tempo. A quale delle seguenti situazioni corrisponde il grafico? A. Il rubinetto è aperto
ESERCIZI DI SCIENZE 1) Il grafico rappresenta la quantità di acqua contenuta in una vasca da bagno al passare del tempo. A quale delle seguenti situazioni corrisponde il grafico? A. Il rubinetto è aperto
Esercizi sulla conversione tra unità di misura
 Esercizi sulla conversione tra unità di misura Autore: Enrico Campanelli Prima stesura: Settembre 2013 Ultima revisione: Settembre 2013 Per segnalare errori o per osservazioni e suggerimenti di qualsiasi
Esercizi sulla conversione tra unità di misura Autore: Enrico Campanelli Prima stesura: Settembre 2013 Ultima revisione: Settembre 2013 Per segnalare errori o per osservazioni e suggerimenti di qualsiasi
Massa assoluta e relativa e mole
 Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
LE GRANDEZZE FISICHE
 LE GRANDEZZE FISICHE 1. 2. Grandezze fondamentali e derivate 3. Sistemi di unità di misura 4. Multipli e sottomultipli 5. Ordini di grandezza 6. Errori e cifre significative pag.1 Misura di una grandezza
LE GRANDEZZE FISICHE 1. 2. Grandezze fondamentali e derivate 3. Sistemi di unità di misura 4. Multipli e sottomultipli 5. Ordini di grandezza 6. Errori e cifre significative pag.1 Misura di una grandezza
Distribuzioni di probabilità
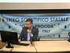 Distribuzioni di probabilità Distribuzioni di probabilità L analisi statistica spesso studia i fenomeni collettivi confrontandoli con modelli teorici di riferimento. Tra di essi, vedremo: la distribuzione
Distribuzioni di probabilità Distribuzioni di probabilità L analisi statistica spesso studia i fenomeni collettivi confrontandoli con modelli teorici di riferimento. Tra di essi, vedremo: la distribuzione
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza?
 Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il Metodo Scientifico
 Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
Unita Naturali Il Metodo Scientifico La Fisica si occupa di descrivere ed interpretare i fenomeni naturali usando il metodo scientifico. Passi del metodo scientifico: Schematizzazione: modello semplificato
04 - Numeri Complessi
 Università degli Studi di Palermo Scuola Politecnica Dipartimento di Scienze Economiche, Aziendali e Statistiche Appunti del corso di Matematica 04 - Numeri Complessi Anno Accademico 2015/2016 M. Tumminello,
Università degli Studi di Palermo Scuola Politecnica Dipartimento di Scienze Economiche, Aziendali e Statistiche Appunti del corso di Matematica 04 - Numeri Complessi Anno Accademico 2015/2016 M. Tumminello,
CdS Ingegneria Industriale: Corso di Chimica
 CdS Ingegneria Industriale: Corso di Chimica Docente : Informazioni generali Candida MILONE cmilone@ingegneria.unime.it Ricevimento Mar e Gio 15:00-17:00 Struttura del corso: Verifiche: 54 ore di lezioni
CdS Ingegneria Industriale: Corso di Chimica Docente : Informazioni generali Candida MILONE cmilone@ingegneria.unime.it Ricevimento Mar e Gio 15:00-17:00 Struttura del corso: Verifiche: 54 ore di lezioni
AISR ASSOCIAZIONE ITALIANA STAMPAGGIO ROTAZIONALE TABELLE DI CONVERSIONE DELLE UNITA DI MISURA
 AISR ASSOCIAZIONE ITALIANA STAMPAGGIO ROTAZIONALE TABELLE DI CONVERSIONE DELLE UNITA DI MISURA TABELLE DI CONVERSIONE DELLE UNITA' DI MISURA Le grandezze nelle tabelle sono riportate in forma esponenziale:
AISR ASSOCIAZIONE ITALIANA STAMPAGGIO ROTAZIONALE TABELLE DI CONVERSIONE DELLE UNITA DI MISURA TABELLE DI CONVERSIONE DELLE UNITA' DI MISURA Le grandezze nelle tabelle sono riportate in forma esponenziale:
CHIMICA QUANTITATIVA. Massa atomica. Unità di massa atomica. Massa molare
 CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
CHIMICA QUANTITATIVA Unità di massa atomica Massa atomica Mole Massa molare 1 L unità di misura della massa è pari a 1/12 della massa dell isotopo 12 6C Questa quantità si chiama unità di massa atomica
LE PROPRIETA DELLA MATERIA
 LE PROPRIETA DELLA MATERIA Gli aspetti macroscopico, microscopico e particellare della materia La materia è tutto ciò che possiede una massa e occupa un volume, cioè una porzione di spazio Un campione
LE PROPRIETA DELLA MATERIA Gli aspetti macroscopico, microscopico e particellare della materia La materia è tutto ciò che possiede una massa e occupa un volume, cioè una porzione di spazio Un campione
i fenomeni nell universo fisico seguono precise regole, i risultati degli esperimenti devono essere riproducibili a piacere
 Metodo scientifico il metodo scientifico comporta l uso sistematico: del dubbio e dello scetticismo, intesi in senso costruttivo dei principi della logica della classificazione rigorosa delle osservazioni
Metodo scientifico il metodo scientifico comporta l uso sistematico: del dubbio e dello scetticismo, intesi in senso costruttivo dei principi della logica della classificazione rigorosa delle osservazioni
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
La fisica e la misura
 La fisica e la misura La fisica è una scienza fondamentale che ha per oggetto la comprensione dei fenomeni naturali che accadono nel nostro universo. È basata su osservazioni sperimentali e misure quantitative
La fisica e la misura La fisica è una scienza fondamentale che ha per oggetto la comprensione dei fenomeni naturali che accadono nel nostro universo. È basata su osservazioni sperimentali e misure quantitative
Verifica della conservazione dell energia meccanica mediante rotaia a cuscino d aria
 Verifica della conservazione dell energia meccanica mediante rotaia a cuscino d aria Lo scopo dell esperimento L esperimento serve a verificare il principio di conservazione dell energia meccanica, secondo
Verifica della conservazione dell energia meccanica mediante rotaia a cuscino d aria Lo scopo dell esperimento L esperimento serve a verificare il principio di conservazione dell energia meccanica, secondo
Sintesi dei dati in una tabella. Misure di variabilità (cap. 4) Misure di forma (cap. 5) Statistica descrittiva (cap. 6)
 Sintesi dei dati in una tabella Misure di variabilità (cap. 4) Misure di forma (cap. 5) Statistica descrittiva (cap. 6) Sintesi dei dati Spesso si vuole effettuare una sintesi dei dati per ottenere indici
Sintesi dei dati in una tabella Misure di variabilità (cap. 4) Misure di forma (cap. 5) Statistica descrittiva (cap. 6) Sintesi dei dati Spesso si vuole effettuare una sintesi dei dati per ottenere indici
CURRICOLO VERTICALE MATEMATICA RELAZIONI/ DATI E PREVISIONI/ MISURA
 CURRICOLO VERTICALE MATEMATICA / DATI E PREVISIONI/ MISURA SCUOLA PRIMARIA CONOSCENZE (Concetti) ABILITA Classe 1^ - Classificazione - in situazioni concrete, classificare persone, oggetti, figure, numeri
CURRICOLO VERTICALE MATEMATICA / DATI E PREVISIONI/ MISURA SCUOLA PRIMARIA CONOSCENZE (Concetti) ABILITA Classe 1^ - Classificazione - in situazioni concrete, classificare persone, oggetti, figure, numeri
Corso di Fisica. DOCENTE: Marina COBAL: Tel
 Corso di Fisica DOCENTE: Marina COBAL: marina.cobal@cern.ch Tel. 339-2326287 TESTO di RIFERIMENTO: Mazzoldi, Nigro, Voci: Elementi di fisica,meccanica e Termodinamica Ed. EdiSES FONDAMENTI DI FISICA -
Corso di Fisica DOCENTE: Marina COBAL: marina.cobal@cern.ch Tel. 339-2326287 TESTO di RIFERIMENTO: Mazzoldi, Nigro, Voci: Elementi di fisica,meccanica e Termodinamica Ed. EdiSES FONDAMENTI DI FISICA -
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA. Lezione n 4 2016
 METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 4 2016 GLI INSIEMI NUMERICI N Numeri naturali Z : Numeri interi Q : Numeri razionali R : Numeri reali Q A meno di isomorfismi!!! R 5 π
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 4 2016 GLI INSIEMI NUMERICI N Numeri naturali Z : Numeri interi Q : Numeri razionali R : Numeri reali Q A meno di isomorfismi!!! R 5 π
IPSSAR P. ARTUSI - Forlimpopoli (Fc) 1 ANNO MODULO: ACCOGLIENZA
 MODULO: ACCOGLIENZA - Il programma di Fisica da svolgere assieme - Conoscere gli alunni - Il metodo di lavoro e di valutazione - Far conoscere agli alunni il metodo di lavoro - Esporre il metodo di valutazione
MODULO: ACCOGLIENZA - Il programma di Fisica da svolgere assieme - Conoscere gli alunni - Il metodo di lavoro e di valutazione - Far conoscere agli alunni il metodo di lavoro - Esporre il metodo di valutazione
DETERMINAZIONI SPERIMENTALI ED ERRORI. confrontare quella grandezza con un'altra di riferimento, ad essa omogenea, detta unità di misura.
 DETERMINAZIONI SPERIMENTALI ED ERRORI MISURARE UNA GRANDEZZA = confrontare quella grandezza con un'altra di riferimento, ad essa omogenea, detta unità di misura. LUNGHEZZA metro (m) distanza percorsa dalla
DETERMINAZIONI SPERIMENTALI ED ERRORI MISURARE UNA GRANDEZZA = confrontare quella grandezza con un'altra di riferimento, ad essa omogenea, detta unità di misura. LUNGHEZZA metro (m) distanza percorsa dalla
Stati della materia. Esempio. Fusione e solidificazione. Esempio. Stati di aggregazione della materia
 Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
= < < < < < Matematica 1
 NUMERI NATURALI N I numeri naturali sono: 0,1,2,3,4,5,6,7,8,9,10,11,12,13,... L insieme dei numeri naturali è indicato con la lettera. Si ha cioè: N= 0,1,2,3,4,5,6,7,.... L insieme dei naturali privato
NUMERI NATURALI N I numeri naturali sono: 0,1,2,3,4,5,6,7,8,9,10,11,12,13,... L insieme dei numeri naturali è indicato con la lettera. Si ha cioè: N= 0,1,2,3,4,5,6,7,.... L insieme dei naturali privato
Codice binario. Codice. Codifica - numeri naturali. Codifica - numeri naturali. Alfabeto binario: costituito da due simboli
 Codice La relazione che associa ad ogni successione ben formata di simboli di un alfabeto il dato corrispondente è detta codice. Un codice mette quindi in relazione le successioni di simboli con il significato
Codice La relazione che associa ad ogni successione ben formata di simboli di un alfabeto il dato corrispondente è detta codice. Un codice mette quindi in relazione le successioni di simboli con il significato
Capitolo 5. La misura. (Ob. 1, 11) 5.1 Le grandezze e la misura 5.2 Il Sistema Internazionale 5.3 Le grandezze derivate 5.4 La misura dell ampiezza
 (Ob. 1, 11) 5.1 Le grandezze e la misura 5.3 Le grandezze derivate 5.4 La misura dell ampiezza 5.1 Le grandezze e la misura 5.1 Le grandezze e la misura Grandezza = qualità di un oggetto che può essere
(Ob. 1, 11) 5.1 Le grandezze e la misura 5.3 Le grandezze derivate 5.4 La misura dell ampiezza 5.1 Le grandezze e la misura 5.1 Le grandezze e la misura Grandezza = qualità di un oggetto che può essere
Corso zero CHIMICA Ingegneria Meccanica Ingegneria Elettrica A.A. 2009/2010
 Corso zero CHIMICA Ingegneria Meccanica Ingegneria Elettrica A.A. 2009/2010 Prof.ssa Giovanna Di Pasquale 1 2 1 Il mondo della chimica abbraccia tutto ciò che intorno a noi ha natura materiale 3 4 2 Il
Corso zero CHIMICA Ingegneria Meccanica Ingegneria Elettrica A.A. 2009/2010 Prof.ssa Giovanna Di Pasquale 1 2 1 Il mondo della chimica abbraccia tutto ciò che intorno a noi ha natura materiale 3 4 2 Il
Appendice B Esempi di item di matematica
 Appendice B Esempi di item di matematica Esempi di item di matematica Classe quarta primaria 1 Osserva la seguente sequenza di numeri. 100, 1, 99, 2, 98, C, C, C Quali numeri devono andare nei tre riquadri?
Appendice B Esempi di item di matematica Esempi di item di matematica Classe quarta primaria 1 Osserva la seguente sequenza di numeri. 100, 1, 99, 2, 98, C, C, C Quali numeri devono andare nei tre riquadri?
Classe Prima. Concetti topologici. Confronti Classificazioni Grafici. Confronti, ordinamenti e grandezze misurabili
 apprendimento ISTITUTO COMPRENSIVO STATALE Classe Prima ABILITA' Leggere e scrivere i numeri, usarli per contare ed eseguire semplici operazioni di addizione e sottrazione I numeri naturali nel loro aspetto
apprendimento ISTITUTO COMPRENSIVO STATALE Classe Prima ABILITA' Leggere e scrivere i numeri, usarli per contare ed eseguire semplici operazioni di addizione e sottrazione I numeri naturali nel loro aspetto
La legge dei gas perfetti
 La legge dei gas perfetti In condizioni normali l aria ambiente secca contiene approssimativamente 78,08% di azoto (N2), 20,94% di ossigeno (O2), 0,93% di argon (Ar), 0,04% di biossido di carbonio (CO2)
La legge dei gas perfetti In condizioni normali l aria ambiente secca contiene approssimativamente 78,08% di azoto (N2), 20,94% di ossigeno (O2), 0,93% di argon (Ar), 0,04% di biossido di carbonio (CO2)
1 L estrazione di radice
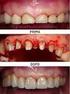 1 L estrazione di radice Consideriamo la potenza 3 2 = 9 di cui conosciamo: Esponente 3 2 = 9 Valore della potenza Base L operazione di radice quadrata consiste nel chiedersi qual è quel numero x che elevato
1 L estrazione di radice Consideriamo la potenza 3 2 = 9 di cui conosciamo: Esponente 3 2 = 9 Valore della potenza Base L operazione di radice quadrata consiste nel chiedersi qual è quel numero x che elevato
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
CONCETTO di GRANDEZZA
 CONCETTO di GRANDEZZA Le GRANDEZZE FISICHE sono qualità misurabili di un corpo o di un fenomeno Esempi di grandezze Per misurare una grandezza occorre un adeguato strumento di misura GRANDEZZA Lunghezza
CONCETTO di GRANDEZZA Le GRANDEZZE FISICHE sono qualità misurabili di un corpo o di un fenomeno Esempi di grandezze Per misurare una grandezza occorre un adeguato strumento di misura GRANDEZZA Lunghezza
MATEMATICA CLASSE NUMERO Contare sia in senso progressivo sia in senso regressivo.
 MATEMATICA OB. FORMATIVI COMPETENZE CLASSE 1 1. NUMERO Contare sia in senso progressivo sia in senso regressivo..2 Usare il numero per contare, confrontare, ordinare raggruppamenti di oggetti..3 Leggere
MATEMATICA OB. FORMATIVI COMPETENZE CLASSE 1 1. NUMERO Contare sia in senso progressivo sia in senso regressivo..2 Usare il numero per contare, confrontare, ordinare raggruppamenti di oggetti..3 Leggere
GRIGLIA DI CORREZIONE Matematica Classe I Scuola secondaria di I grado
 GRIGLIA DI CORREZIONE Matematica Classe I Scuola secondaria di I grado LEGENDA AMBITI: NU (Numeri), SF (Spazio e figure), DP (Dati e previsioni), RF (Relazioni e funzioni) LEGENDA PROCESSI: 1. Conoscere
GRIGLIA DI CORREZIONE Matematica Classe I Scuola secondaria di I grado LEGENDA AMBITI: NU (Numeri), SF (Spazio e figure), DP (Dati e previsioni), RF (Relazioni e funzioni) LEGENDA PROCESSI: 1. Conoscere
FISICA Corso di laurea in Informatica e Informatica applicata
 FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
FISICA Corso di laurea in Informatica e Informatica applicata I semestre AA 2004-2005 G. Carapella Generalita Programma di massima Testi di riferimento Halliday Resnick Walker CEA Resnick Halliday Krane
2. E L E M E N T I S T R U T T U R A L I E T E R R I T O R I A L I D I U N A Z I E N D A A G R A R I A
 2. E L E M E N T I S T R U T T U R A L I E T E R R I T O R I A L I D I U N A Z I E N D A A G R A R I A Capitolo 2 - Elementi strutturali e territoriali di un azienda agraria 2. 1. G r a n d e z z e e u
2. E L E M E N T I S T R U T T U R A L I E T E R R I T O R I A L I D I U N A Z I E N D A A G R A R I A Capitolo 2 - Elementi strutturali e territoriali di un azienda agraria 2. 1. G r a n d e z z e e u
Tab 2/1. Grandezze e unità SI fondamentali e supplementari.
 2. UNITA' DI MISURA. R. Mi ha detto che avremmo incontrato spesso la sigla SI. Di che cosa si tratta, esattamente? D. SI è la sigla di Sistema internazionale di unità di misura, in vigore, nei Paesi dell
2. UNITA' DI MISURA. R. Mi ha detto che avremmo incontrato spesso la sigla SI. Di che cosa si tratta, esattamente? D. SI è la sigla di Sistema internazionale di unità di misura, in vigore, nei Paesi dell
Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto grandi e molto piccoli.
 Elevamento a potenza Potenze del 10, SI e potenze del 2 (UbiMath) - 1 Potenze del 10 e SI Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto
Elevamento a potenza Potenze del 10, SI e potenze del 2 (UbiMath) - 1 Potenze del 10 e SI Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto
Prof.ssa Laura Salvagno
 Prof.ssa Laura Salvagno Nella vita di tutti i giorni abbiamo spesso a che fare con il concetto di rapporto, partiamo perciò da alcuni esempi per introdurre l argomento. Consideriamo tutte le gare combattute
Prof.ssa Laura Salvagno Nella vita di tutti i giorni abbiamo spesso a che fare con il concetto di rapporto, partiamo perciò da alcuni esempi per introdurre l argomento. Consideriamo tutte le gare combattute
Esercizi di termologia
 Esercizi di termologia L. Paolucci 4 dicembre 2009 Sommario Termologia: esercizi e problemi con soluzioni. Per la classe seconda. Anno Scolastico 2009/0. Versione: v Si ricordi che cal 4,86. Quindi il
Esercizi di termologia L. Paolucci 4 dicembre 2009 Sommario Termologia: esercizi e problemi con soluzioni. Per la classe seconda. Anno Scolastico 2009/0. Versione: v Si ricordi che cal 4,86. Quindi il
Determinazione del calore di combustione specifico di un pellet vegetale
 Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
D. Sono cifre significative: *Le cifre di un numero diverse da zero.
 1. RICHIAMI DI MATEMATICA D. Per comprendere quanto studieremo insieme, è necessario richiamare alla memoria alcuni concetti di fisica e matematica, dimenticati o mai appresi. Si faccia coraggio. Si definiscono
1. RICHIAMI DI MATEMATICA D. Per comprendere quanto studieremo insieme, è necessario richiamare alla memoria alcuni concetti di fisica e matematica, dimenticati o mai appresi. Si faccia coraggio. Si definiscono
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
03 - Unità di misura, tabelle di conversione
 0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
Lezione 4 a - Misure di dispersione o di variabilità
 Lezione 4 a - Misure di dispersione o di variabilità Abbiamo visto che la media è una misura della localizzazione centrale della distribuzione (il centro di gravità). Popolazioni con la stessa media possono
Lezione 4 a - Misure di dispersione o di variabilità Abbiamo visto che la media è una misura della localizzazione centrale della distribuzione (il centro di gravità). Popolazioni con la stessa media possono
12) Metodo dei minimi quadrati e linea di tendenza
 12) Metodo dei minimi quadrati e linea di tendenza 43 Si supponga di avere una tabella di dati {y exp i} i=1,,n in funzione di altri dati {x i } i=1,,n che siano il risultato di una qualche misura sperimentale.
12) Metodo dei minimi quadrati e linea di tendenza 43 Si supponga di avere una tabella di dati {y exp i} i=1,,n in funzione di altri dati {x i } i=1,,n che siano il risultato di una qualche misura sperimentale.
Scuola Statale Italiana di Madrid Anno scolastico 2014-2015. PROGRAMMAZIONE CURRICOLARE DI MATEMATICA Classe quarta B Insegnante: Adriano Adamo
 Scuola Statale Italiana di Madrid Anno scolastico 2014-2015 PROGRAMMAZIONE CURRICOLARE DI MATEMATICA Classe quarta B Insegnante: Adriano Adamo INDICATORI OBIETTIVI SPECIFICI DI APPRENDIMENTO (Conoscenze
Scuola Statale Italiana di Madrid Anno scolastico 2014-2015 PROGRAMMAZIONE CURRICOLARE DI MATEMATICA Classe quarta B Insegnante: Adriano Adamo INDICATORI OBIETTIVI SPECIFICI DI APPRENDIMENTO (Conoscenze
Laboratorio di sistemi 3 A Meccanica Energia. Resistività ρ Resistori e resistenza elettrica Ω
 Laboratorio di sistemi 3 A Meccanica Energia Resistività ρ Resistori e resistenza elettrica Ω Resistività elettrica La resistività elettrica (ρ), anche detta resistenza elettrica specifica, è l'attitudine
Laboratorio di sistemi 3 A Meccanica Energia Resistività ρ Resistori e resistenza elettrica Ω Resistività elettrica La resistività elettrica (ρ), anche detta resistenza elettrica specifica, è l'attitudine
Classe ALLENAMENTO INVALSI MATEMATICA (4) - Numeri (2) Cognome e Nome Classe Data
 Classe 1-3 - ALLENAMENTO INVALSI MATEMATICA (4) - Numeri (2) Cognome e Nome Classe Data 1. Quale valore deve avere il perché la seguente uguaglianza sia vera? 24,5 : 100 = 2,45 : [ ] B. 1 [ ] C. 0,1 [
Classe 1-3 - ALLENAMENTO INVALSI MATEMATICA (4) - Numeri (2) Cognome e Nome Classe Data 1. Quale valore deve avere il perché la seguente uguaglianza sia vera? 24,5 : 100 = 2,45 : [ ] B. 1 [ ] C. 0,1 [
La divisione esatta fra a e b è l operazione che dati i numeri a e b (con a multiplo di b) permette di trovare un terzo numero c tale che c b = a.
 Significato Significato della divisione esatta La divisione esatta fra a e b è l operazione che dati i numeri a e b (con a multiplo di b) permette di trovare un terzo numero c tale che c b = a. Descrivendo
Significato Significato della divisione esatta La divisione esatta fra a e b è l operazione che dati i numeri a e b (con a multiplo di b) permette di trovare un terzo numero c tale che c b = a. Descrivendo
Esame di Statistica (10 o 12 CFU) CLEF 11 febbraio 2016
 Esame di Statistica 0 o CFU) CLEF febbraio 06 Esercizio Si considerino i seguenti dati, relativi a 00 clienti di una banca a cui è stato concesso un prestito, classificati per età e per esito dell operazione
Esame di Statistica 0 o CFU) CLEF febbraio 06 Esercizio Si considerino i seguenti dati, relativi a 00 clienti di una banca a cui è stato concesso un prestito, classificati per età e per esito dell operazione
L indagine statistica
 1 L indagine statistica DEFINIZIONE. La statistica è quella disciplina che si occupa della raccolta di dati quantitativi relativi a diversi fenomeni, della loro elaborazione e del loro utilizzo a fini
1 L indagine statistica DEFINIZIONE. La statistica è quella disciplina che si occupa della raccolta di dati quantitativi relativi a diversi fenomeni, della loro elaborazione e del loro utilizzo a fini
La corrente alternata
 La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
STATISTICHE DESCRITTIVE Parte II
 STATISTICHE DESCRITTIVE Parte II INDICI DI DISPERSIONE Introduzione agli Indici di Dispersione Gamma Differenza Interquartilica Varianza Deviazione Standard Coefficiente di Variazione introduzione Una
STATISTICHE DESCRITTIVE Parte II INDICI DI DISPERSIONE Introduzione agli Indici di Dispersione Gamma Differenza Interquartilica Varianza Deviazione Standard Coefficiente di Variazione introduzione Una
Incertezza di Misura: Concetti di Base
 Incertezza di Misura: Concetti di Base Roberto Ottoboni Dipartimento di Elettrotecnica Politecnico di Milano 1 Il concetto di misura Nella sua accezione più comune si è sempre inteso come misura di una
Incertezza di Misura: Concetti di Base Roberto Ottoboni Dipartimento di Elettrotecnica Politecnico di Milano 1 Il concetto di misura Nella sua accezione più comune si è sempre inteso come misura di una
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
SISTEMA INTERNAZIONALE DI UNITÀ
 LE MISURE DEFINIZIONI: Grandezza fisica: è una proprietà che può essere misurata (l altezza di una persona, la temperatura in una stanza, la massa di un oggetto ) Misurare: effettuare un confronto tra
LE MISURE DEFINIZIONI: Grandezza fisica: è una proprietà che può essere misurata (l altezza di una persona, la temperatura in una stanza, la massa di un oggetto ) Misurare: effettuare un confronto tra
Metodi e tecniche di analisi dei dati nella ricerca psico-educativa Parte III
 Laboratorio Metodi e tecniche di analisi dei dati nella ricerca psico-educativa Parte III Laura Palmerio Università Tor Vergata A.A. 2005/2006 MISURAZIONE Misurare le variabili Assegnazione di valori numerici
Laboratorio Metodi e tecniche di analisi dei dati nella ricerca psico-educativa Parte III Laura Palmerio Università Tor Vergata A.A. 2005/2006 MISURAZIONE Misurare le variabili Assegnazione di valori numerici
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA. Lezione n 14
 METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 14 L equivalenza di figure piane Due figure piane si dicono equivalenti (o equiestese) se hanno la stessa estensione nel piano. L area
METODI E TECNOLOGIE PER L INSEGNAMENTO DELLA MATEMATICA Lezione n 14 L equivalenza di figure piane Due figure piane si dicono equivalenti (o equiestese) se hanno la stessa estensione nel piano. L area
CUOCERE ILLUMINARE SCALDARSI
 IL CALORE Pagine per l insegnante Portiamo a scuola vari tipi di termometri: ambientale, medico... Iniziamo l attività spiegando che il calore è un energia. L energia è qualcosa che permette a un corpo
IL CALORE Pagine per l insegnante Portiamo a scuola vari tipi di termometri: ambientale, medico... Iniziamo l attività spiegando che il calore è un energia. L energia è qualcosa che permette a un corpo
Stati di aggregazione della materia unità 2, modulo A del libro
 Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
