GUARIGIONE DEGLI INNESTI OSSEI LIBERI
|
|
|
- Luigina Pace
- 5 anni fa
- Visualizzazioni
Transcript
1 GUARIGIONE DEGLI INNESTI OSSEI LIBERI Il processo di guarigione degli innesti ossei liberi presenta similitudini ai processi riparativi e di guarigione delle fratture ossee, mentre si differenzia da queste per la presenza da un lato di un sito ricevente e dall all altro di tessuto osseo trapiantato avascolare. I meccanismi biologici della riparazione sono comunque indipendenti dai segmenti ossei coinvolti, e la sequenza cronologica degli eventi appare comune e controllata da meccanismi a cascata, fattori locali e sistemici e bioumorali. Il processo di guarigione degli innesti di osso è diviso in due fasi: una fase precoce ed una fase tardiva. La fase precoce, la quale avviene nelle prime 4 settimane, è caratterizzata da: Emostasi e danno anossico Infiammazione ed induzione cellulare Rimozione dei tessuti necrotici Proliferazione cellulare (blastema fibrocellulare) Osteogenesi e rimodellamento La fase tardiva, rappresenta il proseguo del processo di guarigione, dove il processo di rimodellamento e di riassorbimento continua con la crescita di nuovi vasi. La fine di tale fase è rappresentata dalla completa sostituzione dell innesto con osso neo-formato, che avviene in circa 6 mesi dall innesto. 148 EMOSTASI E DANNO ANOSSICO (PRIME ORE) Il posizionamento chirurgico dell innesto, a seguito di uno scollamento di un lembo muco-periostale, porta ad uno stravaso emorragico che vengono obliterati dalla formazione di un ematoma. L interruzione della circolazione e il ristagno ematico, portano ad una diminuzione locale della po 2, accompagnata da un aumento della pco 2 ed un abbassamento del ph, producendo un danno anossico nei tessuti circostanti INFIAMMAZIONE ED INDUZIONE CELLULARE (DALLE PRIME ORE PER I SUCCESSIVI 2-4 GIORNI) Inseguito alla formazione dell ematoma si innesca la reazione flogistica (prima fase della riparazione). La vasodilatazione che ne consegue, consente l ingresso nel focolaio infiammatorio di elementi cellulari maturi e di differente derivazione. Questi 72
2 ultimi, sotto l azione di stimoli umorali e biomeccanici, si differenziano in popolazioni di diverso significato funzionale, responsabili delle fasi successive dei processi riparativi. La reazione infiammatoria conduce, quindi, all invasione cellulare dell ematoma e dei tessuti circostanti; a questo punto numerose biomolecole regolatrici e morfologiche vengono prodotte e liberate durante questa fase, stimolando così l induzione cellulare (Fig 53). 148,149 Fig. 53: Immagine di coagulo ematico che mostra un ammasso cellulare composto da globuli rossi imbrigliato dalla fibrina RIMOZIONE DELL EMATOMA E DEI TESSUTI NECROTICI Una volta arrestata l emorragia, il coagulo stabilizzato viene progressivamente dissolto grazie all azione fibrinolitica. Alla fibrinolisi si accompagna anche la degradazione dei tessuti necrotici, con la mobilizzazione di numerosi elementi cellulari della serie bianca. In particolare tra queste cellule i linfociti giocano un ruolo molto importante per l attivazione delle altre cellule che popolano la regione dell ematoma. Granulociti ad attività macrofagica, sotto lo stimolo di linfochine e di interleuchine presidiano la rimozione dei detriti cellulari e del coagulo. Linfochine specifiche, quali il fattore di fusione dei macrofagi e quello attivante gli osteoclasti inducono a dei precursori degli osteoclasti a costituire degli aggregati sinciziali che agendo su 73
3 frammenti lesionati producono il riassorbimento delle porzioni ossee necrotiche (Fig 54). 148,149 Fig. 54: Porzione di ematoma in una frattura sperimentale al microscopio ottico; rimozione di cellule e materiale interstiziale per opera dei macrofagi 149. BLASTEMA FIBROCELLULARE Gettoni cordonali endoteliali, in origine dai vasi che circondano l area della lesione, proliferano in modo continuo durante la rimozione del coagulo. Infatti, si viene a formare una rete vascolare altamente anastomizzata, che in breve termine tempo ristabilisce la circolazione ematica all interno della regione lesionata. La neoangiogenesi e il conseguente ripristino dei valori locali normali di po 2, di poc 2 e di ph costituiscono la premessa fondamentale per l inizio dei processi rigenerativi. Attorno alle anse dei capillari neoformati comincia a svilupparsi una nuova popolazione cellulare, formata da elementi mesenchimali di tipo fibroblastico. Queste cellule sono circondate da sostanza intercellulare nella quale sono presenti fibre collagene che costituiscono una delicata trama di sostegno. In breve si costituisce un tessuto connettivo lasso avente molteplici possibilità rigenerative, che viene propriamente definito blastema fibrocellulare. Durante la fase di invasione e di induzione, oltre a i numerosi elementi emopoietici, nell area della lesione vengono riversate anche cellule mesenchimali di tipo fibroblastico; queste potenzialmente, possono seguire linee differenziative diverse nell ambito dei tessuti di origine mesenchimale come fibroblasti, 74
4 condroblasti o osteblasti. L orientamento fenotipico di tali elementi è diretto dall azione di fattori morfogenetici e delle condizioni meccaniche locali, alcuni dei quali hanno una azione specifica sulla proliferazione del substrato mesenchimale, altri invece sembrano indirizzare il destino degli elementi mesenchimali verso il fenotipo osteoblastico (Fig 55). 148,149 Fig. 55: Blastema fibrocellulare in una frattura sperimentale al microscopio ottico; elementi cellulari di tipo fibroblastico uniti a formare un connettivo di tipo lasso e iniziale deposizione di materiale osteoide. OSTEOGENESI E RIMODELLAMENTO L osso neodeposto ha una struttura piuttosto primitiva, ma i processi neoangiogenesi, rigenerazione e consolidamento hanno ricostituito nel segmento lesionato le condizioni metaboliche e strutturali sufficienti a far fronte alle sollecitazioni meccaniche a cui il segmento è sottoposto. Questo adattamento permette l organizzazione traiettoriale dell attività di modellamento e rimodellamento che si verificano successivamente. Alla quarta settimana dall evento traumatico (Fig. 56), l osteogenesi rigenerativa ha raggiunto l acme della sua attività cominciando a perdere inerzia; al contrario l attività cellulare viceversa è aumentata in correlazione all adattamento della struttura. I fattori meccanici assumono una grande importanza, condizionando sia la fase di orientamento del segmento lesionato, sia la fase successiva strutturale di modellamento e rimodellamento. 150,151 75
5 Fig. 56: Osteogenesi e rimodellamento osseo (ematossilina -eosina). (Acocella Colafranceschi, Università degli Studi di Firenze) ASPETTI MOLECOLARI DELLA GUARIGIONE DELLE FRATTURE Le molecole coinvolte nel processo di guarigione delle fratture, possono essere classificati in tre gruppi 152 : le citochine pro-infiammatorie, il fattore di crescita trasformante-beta (TGF-b) e fattori di crescita appartenete a tale superfamiglia, fattori angiogenici Le citochine pro-infiammatorie, come l interleuchina-1 (IL-1) e l interleuchina-6 (IL-6), nonché il fattore di necrosi tumorale alfa (TNF-a) svolgono un ruolo importante nel promuovere la riparazione per mezzo di attivazione a cascata 153. Essi sono secreti non solo dai macrofagi e dalle cellule infiammatorie, ma anche da cellule di origine mesenchimali presenti nel periostio, svolgendo funzioni importanti nell'induzione di risposte a valle della lesione. Infatti, avendo un azione di tipo chemiotattica su altre cellule infiammatorie, migliorando la sintesi della matrice extracellulare, stimolando l'angiogenesi, e il reclutamento di cellule endogene fibrogeniche nel sito coinvolto nella frattura. (Tab. III, IV, V) Il picco di concentrazione massima di tali molecole (IL-1, Il-6, TNF-a) è entro le prime 24 ore dopo la frattura aumentando di nuovo durante il rimodellamento osseo. Le 76
6 citochine regolano anche la formazione delle ossa e il rimodellamento endocondrale. Il TNF-a promuovere il reclutamento di cellule staminali mesenchimali, induce l'apoptosi di condrociti ipertrofici durante ossificazione endocondrale e stimolndo la funzione osteoclastica. Assenza di TNF-a determina un ritardo nel riassorbimento della cartilagine mineralizzata impedendo così la neoformazione ossea FATTORI DI CRESCITA E DIFFERENZIAZIONE I fattori di crescita e di differenziamenti più importanti, nei processi riparativi delle fratture, sono rappresentati dalla superfamiglia dei fattori di crescita trasformantebeta (TGF-b) Tabella 3. La superfamiglia TGF-b è una grande famiglia di fattori di crescita e di differenziazione a cui appartengono anche le proteine morfogenetiche ossee (BMP). Almeno 34 membri sono stati identificati nel genoma umano. Provengono da precursori alto peso molecolare e sono attivati da enzimi proteolitici. Essi agiscono su i recettori di membrana serina / treonina chinasi delle cellule bersaglio Componenti specifiche di questa superfamiglia compresa proteine morfogenetiche ossee (BMP 1-8), i fattori di crescita (GDF-1, 5, 8, 10) e il fattore trasformante beta (TGF-b1, b2-,-b3), promuovono varie fasi dell ossificazione intramembranosa e del processo di guarigione ossa durante la frattura 159. Essential molecules during fracture healing Cytokines (IL-1, IL-6, TNF-a) Source: macrophages and other inflammatory cells, cells of mesenchymal origin Chemotactic effect on other inflammatory cells, stimulation of extracellular matrix synthesis, angiogenesis, recruitment of endogenous fibrogenic cells to the injury site, and at later stages bone resorption Increased levels from days 1 to 3 and during bone remodelling TGF-b Source: degranulating platelets, inflammatory cells, endothelium, extracellular matrix, chondrocytes, osteoblasts Targeted cells: MSCs, osteoprogenitors cells, osteoblasts, chondrocytes Potent mitogenic and chemotactic for bone forming cells, chemotactic for macrophages Expressed from very early stages throughout fracture healing 77
7 PDGF Source: degranulating platelets, macrophages, monocytes (during the granulation stage) and endothelial cells, osteoblasts (at later stages) Targeted cells: mesenchymal and inflammatory cells, osteoblasts Mitogenic for mesenchymal cells and osteoblasts, chemotactic for inflammatory and mesenchymal cells Released at very early stages of fracture healing BMPs Source: osteoprogenitors and mesenchymal cells, osteoblasts, bone extracellular matrix and chondrocytes Targeted cells: mesenchymal and osteoprogenitor cells, osteoblasts Differentiation of undifferentiated mesenchymal cells into chondrocytes and osteoblasts and osteoprogenitors into osteoblasts Various temporal expression patterns FGFs Source: monocytes, macrophages, mesenchymal cells, osteoblasts, chondrocytes Targeted cells: mesenchymal and epithelial cells, osteoblasts and chondrocytes Angiogenic and mitogenic for mesenchymal and epithelial cells, osteoblasts, chondrocytes a-fgf mainly effects chondrocyte proliferation, b-fgf (more potent) involved in chondrocytes maturation and bone resorption Expressed from the early stages until osteoblasts formation IGFs Source: bone matrix, endothelial and mesenchymal cells (in granulation stage) and osteoblasts and non-hyperthrophic chondrocytes (in bone and cartilage formation) Targeted cells: MSCs, endothelial cells, osteoblasts, chondrocytes IGF-I: mesenchymal and osteoprogenitor cells recruitment and proliferation, expressed throughout fracture healing IGF-II: cell proliferation and protein synthesis during endochondral ossification Metalloproteinases Source: the extracellular matrix Degradation of the cartilage and bone allowing the invasion of blood vessels during the final stages of endochondral ossification and bone remodelling VEGFs Potent stimulators of endothelial cell proliferation Expressed during endochondral formation and bone formation Angiopoietin (1 and 2) Formation of larger vessel structures, development of co-lateral branches from existing vessels Expressed from the early stages throughout fracture healing Tabella III: Fattori di crescita e loro funzione durante la guarigione ossea 78
8 Time Event Molecular signal Day 1 Haematoma formation, inflammation Recruitment of mesenchymal cells Osteogenic differentiation of MSCs from bone marrow Cytokines: IL-1, IL-6, TNF-a released by inflammatory cells PDGF, TFG-beta released from degranulating platelets BMP-2 expression and restricted to day 1 expression of GDF-8 Day 3 MSCs proliferation begins Proliferation and differentiation of preosteoblasts and osteoblasts in regions of intramembranous ossification Angiogenesis begins Decline of cytokines levels Expression of TGF-b2, - b3, GDF-10, BMP-5, -6 Angiopoietin-1 is induced Day 7 Peak of cell proliferation in intramembranous ossification between days 7 and 10, Chondrogenesis and endochondral ossification begins (days 9 14 maturation of chondrocytes) Peak of TGF-b2 and -b3 expression Expression of GDF-5 and probably GDF-1 Day 14 Cessation of cell proliferation in intramembranous ossification, but osteoblastic activity continues Mineralization of the soft callus, cartilage resorption, and woven bone formation Phase of most active osteogenesis until day 21 Decreased levels of expression for TGF-b2, GDF-5, and probably GDF-1 Expression of BMP-3, - 4, -7, and -8 VEGFs expression Second increase of IL-1 and TNF-a which continues during bone remodelling Day 21 Woven bone remodelled and subsequently replaced by lamellar bone Decreased expression of TGF-b1 and TGF-b3, GDF-10, and BMPs (2 8) Tabella IV: Distribuzione temporale della produzione dei fattori di crescita e loro funzioni. 79
9 PROTEINE MORFOGENETICHE OSSEE I membri della famiglia BMP sono divisi in almeno quattro sottogruppi distinti a seconda della loro sequenza aminoacidica primaria. Il primo gruppo è costituito dalle proteine morfogenetiche BMP-2 BMP-4, e il secondo gruppo comprende le proteine morfogenetiche BMP-5, -6 e -7. Il terzo gruppo comprende GDF-5 (o BMP-14), GDF-6 (o BMP-13) e GDF-7 (o BMP-12); e infine, il quarto gruppo include BMP-3 (o osteogenina) e GDF-10 (o BMP-3b) 160. La proteina morfogenetica BMP-1 non è un membro della superfamiglia TGF-b, ma ha un ruolo importante nel modulare le azioni delle altre BMP dalla proteolisi degli antagonisti BMP.63 Le BMP si legano al recettore tipo II della serina / treonina chinasi che successivamente attiva la cascata di segnali intracellulari Smad, regolando la trascrizione dei geni bersaglio nel nucleo 156. Le BMP sono svolgono un ruolo critico nella regolazione della crescita e differenziazione nonché l apoptosi di vari tipi di cellule, tra cui osteoblasti, condroblasti, le cellule neuronali, e cellule epiteliali. Inoltre, è stato dimostrato che eterodimeri BMP, come BMP-4/-7 e BMP-2/-7 hanno una maggiore attività osteoinduttiva che regolano in modo più efficiente differenziazione e la proliferazione delle cellule mesenchimali in osteoblasti in vitro e in vivo 160,161. Studi sul ruolo delle BMP nella guarigione della frattura nel ratto hanno mostrato una varietà di effetti osteogenici, espressioni temporali, e capacità mitogena In una analisi generale delle attività osteogenico di 14 tipi di BMPS, Cheng et al. 163 hanno suggerito un modello gerarchico osteogenico di BMPS. Le BMP-2, -6 e -9 possono essere il più potente fattore di differenziamento che induce le cellule progenitrici mesenchimali a differenziarsi in osteoblasti. Inoltre le BMP possono anche stimolare la sintesi e la secrezione di altre ossa e fattori di crescita angiogenetici come il fattore di crescita insulino-simile (IGF) e rispettivamente anche il fattore di crescita vascolare endoteliale (VEGF). Esse possono anche stimolare la formazione di osso da azionare direttamente le cellule endoteliali a stimolare angiogenesis 163,164. IL FATTORE DI CRESCITA DERIVATO DALLE PIASTRINE (PDGF) Il PDGF è un polipeptide omo-o eterodimerico composto da due catene A e B. L effetto PDGF viene esercitata attraverso i recettori che hanno l'attività tirosin-chinasi. Le IL-1, TNF-alfa, TGF-b1 e influenzare il legame del PDGF. Il fattore di crescita derivato dalle piastrine (PDGF) è sintetizzato da piastrine, monociti, macrofagi, cellule 80
10 endoteliali e osteoblasti, ed ha una potente azione mitogena per le cellule di origine mesenchimale. Il PDGF viene rilasciato dalle piastrine durante le prime fasi della guarigione della frattura, ed è ha una potente azione chemiotattica per le cellule infiammatorie oltre ad avere uno stimolo proliferativo per le cellule staminali mesenchimali e per gli osteoblasti. Tuttavia, attualmente, il suo potenziale terapeutico rimane poco chiaro 165,166. FATTORE DI CRESCITA FIBROBLASTICO (FGF) La famiglia di FGFs si compone di nove polipeptidi strutturalmente simili. La loro azione è mediata dal legame sui recettori della tirosin-chinasi. Durante la guarigione ossea, FGFs sono sintetizzati dai monociti, macrofagi, cellule mesenchimali, osteoblasti e condrociti. La loro azione è quella di promuovere la crescita e la differenziazione di diverse cellule come fibroblasti, miociti, osteoblasti, e condrociti. Il fattore di crescita fibroblastico ha un ruolo fondamentale durante le fasi iniziali della guarigione della frattura promuovendo la neoangiogenesi e la mitogenesi delle cellule mesenchimali da i siti coinvolti nel processo di guarigione INSULINO SIMILE FATTORI DI CRESCITA (IGF) Le fonti di IGF-I (o somatomedina-c) e IGF-II (o fattore di crescita scheletrica), sono rappresentate dalla matrice ossea, dalle cellule endoteliali, dagli osteoblasti e dai condrociti. La concentrazione sierica di IGF-I è principalmente regolata dalla ormone della crescita. Le azioni biologiche dell IGF sono modulati in modo cellulo-specifico. L IGF-I promuove la formazione ossea matrice (collagene di tipo I e le proteine della matrice non collageniche) e del completamente dei processi di differenziazione degli osteoblasti 167,168. METALLOPROTEINASI E FATTORI ANGIOGENICI Una rigenerazione ossea ottimale richiede un adeguato flusso di sangue e durante le fasi finali di ossificazione endocondrale così come durante il rimodellamento, specifiche matrici metalloproteinasi degradano le cartilagine e l osso, permettendo l'invasione dei vasi sanguigni. Si ritiene che due percorsi distinti regolano l'angiogenesi: un vascolare endoteliale fattore dipendente e uno angiopoietinadipendente Si è ipotizzato che entrambe le vie sono funzionali durante la riparazione della frattura. VEGF sono mediatori essenziali della neo-angiogenesi e delle 81
11 cellule endoteliali specificmitogens. Considerando che, angiopoietin1e 2 sono molecole correlate alla formazione di grandi vasi e allo sviluppo di rami co-laterale da parte di vasi esistenti. Tuttavia, il loro contributo in riparazione ossea non è ben compreso. Street et al. ha dimostrato che la riparazione della frattura è stata rafforzata dalla somministrazione esogena di VEGF. Recenti studi hanno inoltre dimostrato che le BMP stimolano l'espressione del VEGF da parte degli osteoblasti 171. Member of the TGF-b Superfamily Time of expression Specific responses in vivo and in vitro GDF-8 Restricted to day 1 Potential function as a negative regulator of skeletal muscle growth BMP-2 Days 1-21 (the earliest gene to be induced and second elevation during osteogenesis Recruitmnt of mesenchymal cells hondrogenesis ay initiate the fracture healing ascade and regulate the expression of ther BMPs MP-2, -6, -9 may be the most potent to induce osteoblast lineagespecific differentiation of MSCs BMP-3, -8 Days (restricted expression during osteogenesis) Temporaldata suggest a role in the regulation of osteogenesis BMP-4 Transient increased expression in the surrounding soft tissues 6 h to day 5 Days Throughout fracture healing Involvement in the formation of callus at a very early stage in the healing process. In vitro: BMP-3 and -4 stimulate the migration of human blood monocytes BMP-7 Days From the early stages of fracture Regulatory role in both types of ossification in healing vitro: stimulation of relative mature osteoblasts GDF-10, BMP-5, -6 Days 3-21 Regulatory role in both 82
12 types of ossification BMP- 6 may initiate chondrocyte saturation20 GDF-5, -1 Day 7 (maximal) to day 14 (restricted expression during chondrogenic phase) GDF-1 at extremely low levels GDF-5 an exclusive involvement in hondrogenesis is suggested stimulation of mesenchymal aggregation and induction of angiogenesis through nhemotaxis of endothelial cells and egradation of matrix proteins GDF-3, GDF-6, -9 No detectable levels within the fracture callus GDF-6 may be expressed only in articular cartilage and with GDF-5, 7 more efficiently induce cartilage and endon-like structures in vivo TGF-b1, -b2, -b3 Days 1-21 Days 3-14 Days 3 21 Potent chemotactic for bone forming cells and macrophages proliferation of undifferentiated esenchymal and osteoprogenitor cells, osteoblasts, chondrocytes Tabella V: Fattori di crescita e di differenziamenti più importanti DIFFERENZE DEI MECCANISMI DI GUARIGIONE DI DIVERSI INNESTI OSSEI Al di là della cascata degli eventi sopradescritti esistono differenze sostanziali nel meccanismo di attecchimento delle varie tipologie di innesto in chirurgia ricostruttiva pre-implantare. Le capacità di integrazione, rivascolarizzazione, stabilità volumetrica dell innesto, qualità istologica, tempi di guarigione dipendono strettamente dal tipo di innesto utilizzato (particolato, blocco, microarchitettura corticale o midollare, sostituti ossei), dal sito ricevente, dalle stimolazioni meccaniche che avvengono in cavità orale durante la guarigione. Da un lato evento fondamentale è costituito dal processo di rivascolarizzazione poiché la formazione di neo-vasi nel contesto del sito di innesto è necessario per l apporto di ossigeno, nutrienti cellulari, fattori di crescita e cellule in 83
13 grado di differenziarsi in senso osteoblastico e partecipare direttamente alla formazione di nuovo tessuto osseo, nonché cellule osteoclastiche per la rimozione del tessuto innestato e sostituzione di questo con un nuovo tessuto osseo (Fig.57). Per questo esistono differenze tra un sito ricevente mascellare in cui la presenza di osso midollare e vasi è maggiore rispetto ad un sito di innesto mandibolare in cui la presenza di vasi e di midollare è più scarsamente rappresentata. Dall altro lato esistono le capactà intrinseche dell innesto che sottendono alla rigenerzione ossea mediante tre meccanismi ormai codificati: Osteogenesi, Osteoinduzione e Osteoconduzione. Per Osteogenesi si intende la capacità intrinseca dell innesto di neogenesi ossea da parte delle cellule osteoprogenitrici (cellule mesenchimali indifferenziate, preosteoblasti, osteoblasti), che sopravvivono al danno anossico derivato dal prelievo e che sono in grado di produrre direttamente tessuto osseo nel sito di innesto. Per Osteoinduzione si intende la capacità intrinseca dell innesto di partecipare attivamente al rilascio di fattori di crescita ossei che stimolano il differenziamento e la proliferazione di cellule osteoblastiche. Per osteoconduzione si intende la capacità dell innesto di creare un supporto strutturale tridimensionale (scaffold) alla crescita delle e alla formazione di neovasi nel contesto dell innesto. E chiaro quindi che questa triade di proprietà sono racchiuse soltanto nel tessuto osseo autologo che rappresenta il gold standard e il materiale di riferimento per tutti i sostituti ossei ed è chiaro che questa triade sia alla base dell attuale e futuro sviluppo dell ingegneria tissutale per ottenere rigenerazioni ossee evitando prelievi ossei autologhi. Queste capacità sono state descritte maggiormente per i vari materiali da innesto comunque ciò che differenzia sostanzialmente gli innesti utilizzabili a scopo pre-implantare è la macro-morfologia dell innesto (particolato o blocco) e la microarchitettura (corticale, midollare). Nel processo di guarigione di un innesto particolato tutti i processi di neoangiogenesi e di sviluppo delle fasi sopradescritte di formazione del coagulo, sostituzione con tessuto di granulazione e formazione di nuovo osso, si sviluppano nello spazio tra le particelle dell innesto (Fig. 58). Si evince come la rivascolarizzazione di questo tipo di innesto, in realtà del sito di innesto più che dell innesto in sé, sia più pronta e rapida (circa due settimane) rispetto agli innesti sotto forma di blocchi. Inoltre giocano fattore essenziale la dimensione delle particelle e lo zeppamento più o meno consistente di queste particelle. 84
14 Fig. 57: Schema della guarigione ossea: in seguito alla formazione di neo-vasi le cellule osteoclastiche rimuovono il tessuto osseo innestato. Questo processo porta alla liberazione di fattori di crescita che stimolano la differenziazione di cellule osteoblastiche che producono nuovo tessuto osseo a ridosso dell innesto. Se l innesto particolato è molto condensato, esiste poco spazio per la rigenerazione ossea. Il nuovo tessuto osseo si forma a diretto contatto delle particelle innestate che fungono da impalcatura alle cellule osteogenetiche (osteoconduzione). In caso di chips osse autologhe, queste vengono progressivamente riassorbite da cellule osteoclastiche o per le porzioni corticali mediante progressiva sostituzione con nuovo tessuto osseo (creeping substitution) fino alla totale scomparsa in pochi mesi delle particelle innestate (Fig. 59). Fig. 58: Schema di attecchimento di innesto osseo particolato: i neovasi si formano dal sito ricevente all innesto inserendosi nello spazio tra le particelle dell innesto apportando cellule staminali che si differenziano in osteoblasti che depongono osso a diretto contatto con le particelle innestate e osteoclasti che riassorbono lee particelle stesse liberando fattori di crescita che stimolano il processo di sostituzione delle particelle con nuovo tessuto osseo. 85
15 Fig. 59: Immagine istologica di riassorbimento e sostituzione tramite creeping substitution di chips corticale di osso autologo (privo di osteociti vitali) da parte di osso vitale neoformato (ricco di osteociti). (Acocella Colafranceschi, Università degli Studi di Firenze) Questo processo è più o meno lento in base alla dimensione delle porzioni corticali dell innesto poiché la componente midollare di questi viene rimaneggiata più velocemente. Durante questa fase di riassorbimento le chips ossee liberano in situ fattori di crescita come le BMPs che stimolano la rigenerazione ossea (osteoinduzione) velocizzando la guarigione dell innesto particolato osseo autologo che è in media di sei mesi. Per quanto riguarda la capacità osteogenetica dipende dalla presenza di cellule all interno delle chips ossee che nel caso di chips corticali sono molto basse e dalla capacità comunque scarsa di sopravvivenza delle cellule al prelievo, soprattutto dopo il processo di triturazione ossea che si effettua per ricavarle (Fig. 60). Nel caso dell utilizzo di particolato ad opera di biomateriali sostitutivi dell osso il processo di guarigione è sostanzialmente il medesimo le particelle di biomateriale fungono da impalcatura (osteoconduzione) e l osso si forma tra una particella e l altra del biomateriale o nel contesto delle particelle se queste sono dotate di micropori. Nel caso di materiali riassorbibili alla fine del processo di rimodellamento tutto il materiale innestato viene sostituito da nuovo osso in tempi variabili a seconda del materiale, mentre nel caso di materiali non riassorbibili le particelle dell innesto permangono nel contesto del sito e il risultato istologico è costituito da un amalgama di tessuto osseo e materiale da innesto (Fig. 61). 86
16 Alessandro Acocella Fig. 60: Immagine istologica di chips cortico-midollari appena prelevate e triturate con un trita-osso: l osso ha risentito del processo di triturazione, la componente midollare appare schiacciata ed è evidente la ipocellularità presente. (Acocella Colafranceschi, Università degli Studi di Firenze). Fig. 61: Processo di guarigione di sito innestatato con osso bovino deproteinizzato: La formazione del coagulo e il progressivo differenziamento in tessuto osseo avviene tra una particella e l altra di innesto le quali alla fine rimangono nel contesto del tessuto osseo maturo. Per l innesto a blocco il meccanismo di attecchimento e guarigione è sostanzialmente diverso. Non esistendo spazio fisico per la neo-vascolarizzzione, i 87
17 nuovi vasi si devono formare dal sito ricevente nel contesto del blocco e il tessuto osseo si deve formare prima a ponte per ricostruire una continuità tra sito ricevente e blocco osseo con un meccanismo simile alla formazione del callo osseo dopo una frattura (Fig. 62). Solo successivamente col progredire della vascolarizzazione si instaurano processi di riassorbimento e rimodellamento osseo nel conteso del blocco che funge di per sé come grosso scaffold per la rigenerazione ossea. A seconda dell architettura dell innesto questo processo può essere più o meno veloce. I blocchi ossei cortico-midollari presentano una capacità di rivasolarizzazione molto veloce (Fig. 63) anche se più lenta Fig. 62: Schema di attecchimento di un innesto a blocco cortico-midollare: formazione di coagulo all interfaccia, formazione del callo osseo, rimodellamento dell innesto con particolare istologico delle unità multicellulari di base (si nota un osteoclasta con alle spalle un vaso e linee osteoblastiche)
18 del particolato, per la presenza di lacune al suo interno, inoltre posseggono capacità osteogenetiche superiori per la presenza di un elevato contenuto cellulare che se sopravvive al trapianto può contribuire efficacemente alla neoformazione ossea. Di conseguenza se l innesto viene prelevato correttamente, e trapiantato velocemente soprattutto in un sito ricevente molto vascolarizzato la probabilità di mantenere vitali le cellule nel suo contesto è elevata. Fig. 63: Frammento di prelievo cortico-midollare da sinfisi mentoniera: la presenza di una midollare ricca di midollo emopoietico tra trabecole di osso lamellare denso consente se innestata una rivascolarizzazione più rapida. (Acocella Colafranceschi, Università degli Studi di Firenze) Fig. 64: Immagine istologica di innesto a blocco da cresta iliaca a distanza di 20 gg dall innesto con particolare dell interfaccia col sito ricevente (osso mascellare): si nota una intensa presenza di neovasi e osso vitale (pieno di osteociti) di saldatura a ponte. (Acocella e coll) 89
19 Studi da noi effettuati hanno mostrato come già a distanza di tre mesi dall innesto i blocchi cortico-midollari siano già caratterizzati da una intensa vascolarizzazione, presenza di osseo neo-formato vitale a ponte tra le trabecole ossee del sito ricevente e quelle dell innesto e dalla presenza di cellule vitali nel contesto dell innesto (Fig. 64). Queste cellule osteoblastiche vitali sono costituite da cellule sopravvissute alla procedura di innesto e da cellule osteoblastiche derivate dalla differenziazione di cellule mesenchimali indifferenziate derivate dal comparto vascolare.l attecchimento e la guarigione delle stecche corticali sono fortemente condizionate dalla compatta struttura di osso lamellare denso che le caratterizza (Fig. 65). Fig. 65: Frammento di innesto prelevato dal ramo mandibolare: è evidente la struttura estremamente compatta con poche lacune vascolari.( Acocella Colafranceschi, Università degli Studi di Firenze) Affinchè la rivascolarizzazione avvenga, è infatti necessario dapprima nu processo di riassorbimento osteoclastico mediante unità multicellulari di base al fine di permettere alle strutture vascolari di invadere o produrre ex-novo i canali di Havers o di Volkmann. Una volta completata l angiogenesi può iniziare il processo di rimaneggiamento secondo la cosiddetta sostituzione strisciante con un fronte progressivo di riassorbimento e neo-apposizione ossea a partire dall interfaccia tra osso ed innesto. Studi da noi effettuati, i cui dati non sono stati ancora pubblicati, hanno utilizzato l individuazione immuno-istochimica del VEGF (vascular endothelial growth factor) come marcatore di rivascolarizzazione degli innesti a blocco confermando come la struttura midollare degli innesti a blocco sia più rivascolarizzata e ricca di cellule 90
20 osteoblastiche vitali, rispetto ai blocchi essenzialmente corticali (Fig. 60). E quindi ragionevole pensare che i processi di sostituzione e rimodellamento degli innesti a blocco autologhi richiedano un periodo superiore ai sei mesi e questo aspetto farà parte integrante dello studio di questa tesi. Fig. 66: Positività al VEGF all interfaccia e nel contesto di un innesto corticomidollare a ridosso di trabecole ossee neoformate (a) e scarsa positività nel contesto di innesto coticale (b) a 20 giorni dopo l innesto. (Acocella Vannelli, Università degli Studi di Firenze) 91
Bergamo, Humanitas Gavazzeni. Biotecnologie. A. Rossi U.O.Ortopedia e Traumatologia Resp. Dr. F.Cividini Humanitas Gavazzeni Bergamo
 Bergamo, 17.11.2010 Humanitas Gavazzeni Biotecnologie A. Rossi U.O.Ortopedia e Traumatologia Resp. Dr. F.Cividini Humanitas Gavazzeni Bergamo COSA SERVE ALL OSSO PER GUARIRE? Popolazione locale osteoblastica
Bergamo, 17.11.2010 Humanitas Gavazzeni Biotecnologie A. Rossi U.O.Ortopedia e Traumatologia Resp. Dr. F.Cividini Humanitas Gavazzeni Bergamo COSA SERVE ALL OSSO PER GUARIRE? Popolazione locale osteoblastica
Osso e cicatrizzazione ossea. Patologia chirurgica veterinaria
 Osso e cicatrizzazione ossea Patologia chirurgica veterinaria Tessuto osseo n Componente essenziale dell organismo Funzioni: 1. Impalcatura per l ancoraggio di muscoli, tendini e legamenti 2. Protezione
Osso e cicatrizzazione ossea Patologia chirurgica veterinaria Tessuto osseo n Componente essenziale dell organismo Funzioni: 1. Impalcatura per l ancoraggio di muscoli, tendini e legamenti 2. Protezione
Lo scheletro ha origine dal mesoderma, pertanto, segue linee differenziative di tipo mesenchimale.
 Lo scheletro ha origine dal mesoderma, pertanto, segue linee differenziative di tipo mesenchimale. www.fisiokinesiterapia.biz Linee differenziative della cellula mesenchimale a cellula mesenchimale Le
Lo scheletro ha origine dal mesoderma, pertanto, segue linee differenziative di tipo mesenchimale. www.fisiokinesiterapia.biz Linee differenziative della cellula mesenchimale a cellula mesenchimale Le
OSTEOGENESI. intramembranosa) Formazione di tessuto osseo su una preesistente, pericondrio, osso) Formazione di tessuto osseo su una preesistente
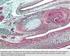 OSTEOGENESI OSSIFICAZIONE DIRETTA (intramembranosa( intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima,(, pericondrio, osso) ( ossa del cranio, mandibola,
OSTEOGENESI OSSIFICAZIONE DIRETTA (intramembranosa( intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima,(, pericondrio, osso) ( ossa del cranio, mandibola,
OSTEOGENESI. OSSIFICAZIONE DIRETTA (intramembranosa) Formazione di tessuto osseo su una preesistente, pericondrio, osso)
 OSSIFICAZIONE DIRETTA (intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima,(, pericondrio, osso) (dove? ossa del cranio, mandibola, clavicola) OSSIFICAZIONE
OSSIFICAZIONE DIRETTA (intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima,(, pericondrio, osso) (dove? ossa del cranio, mandibola, clavicola) OSSIFICAZIONE
Riparazione. Rigenerazione o Risoluzione
 GUARIGIONE GUARIGIONE È l insieme dei fenomeni e dei meccanismi che l organismo attua per ripristinare le condizioni di equilibrio cioè per ritornare allo stato normale. Rigenerazione o Risoluzione Ricostruzione
GUARIGIONE GUARIGIONE È l insieme dei fenomeni e dei meccanismi che l organismo attua per ripristinare le condizioni di equilibrio cioè per ritornare allo stato normale. Rigenerazione o Risoluzione Ricostruzione
TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE
 TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE COMPONENTE AMORFA: GAG, PROTEOGLICANI GLICOPROTEINE LEGANTI IL CALCIO SALI DI
TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE COMPONENTE AMORFA: GAG, PROTEOGLICANI GLICOPROTEINE LEGANTI IL CALCIO SALI DI
Università degli Studi di Teramo
 Università degli Studi di Teramo CORSO di LAUREA in BIOTECNOLOGIE Corso Integrato di CITOLOGIA e ISTOLOGIA Modulo LABORATORIO TECNICHE CITOLOGICHE ED ISTOLOGICHE Dr.ssa A. MAURO Tessuti connettivi specializzati
Università degli Studi di Teramo CORSO di LAUREA in BIOTECNOLOGIE Corso Integrato di CITOLOGIA e ISTOLOGIA Modulo LABORATORIO TECNICHE CITOLOGICHE ED ISTOLOGICHE Dr.ssa A. MAURO Tessuti connettivi specializzati
Processo riparativo La capacità dell organismo di rigenerare le cellule danneggiate o morte e di riparare i tessuti è un evento cruciale per la
 Processo riparativo La capacità dell organismo di rigenerare le cellule danneggiate o morte e di riparare i tessuti è un evento cruciale per la sopravvivenza. Diverse cause esogene ed endogene provocano
Processo riparativo La capacità dell organismo di rigenerare le cellule danneggiate o morte e di riparare i tessuti è un evento cruciale per la sopravvivenza. Diverse cause esogene ed endogene provocano
SEGMENTI SCHELETRICI (o ossa)
 SEGMENTI SCHELETRICI (o ossa) Costituiti prevalentemente da tessuto osseo Cellule: osteoblasti osteociti osteoclasti Sostanza intercellulare: matrice fibrosa sostanza amorfa matrice inorganica Le cellule
SEGMENTI SCHELETRICI (o ossa) Costituiti prevalentemente da tessuto osseo Cellule: osteoblasti osteociti osteoclasti Sostanza intercellulare: matrice fibrosa sostanza amorfa matrice inorganica Le cellule
Tessuto osseo. L osso è al contempo resistente e leggero
 Tessuto osseo Forma specializzata di connettivo caratterizzata dalla mineralizzazione della matrice extracellulare che conferisce al tessuto una notevole resistenza e durezza L osso è al contempo resistente
Tessuto osseo Forma specializzata di connettivo caratterizzata dalla mineralizzazione della matrice extracellulare che conferisce al tessuto una notevole resistenza e durezza L osso è al contempo resistente
Ossa piatte. Ossa piatte del cranio si sviluppano con modalità diverse dalle lunghe
 Ossa piatte Ossa piatte del cranio si sviluppano con modalità diverse dalle lunghe Tavolato interno e Tavolato esterno di osso compatto, racchiudono uno strato di osso spugnoso centrale, Diploe Pericranio
Ossa piatte Ossa piatte del cranio si sviluppano con modalità diverse dalle lunghe Tavolato interno e Tavolato esterno di osso compatto, racchiudono uno strato di osso spugnoso centrale, Diploe Pericranio
Tessuto Osseo. Tessuto osseo. Tessuto osseo Tessuto osseo. Tessuto di sostegno (ma dinamico!!!!)
 Tessuto Osseo Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno (ma dinamico!!!!) Organizzato
Tessuto Osseo Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno (ma dinamico!!!!) Organizzato
Cartilagine. Funzione: sostegno scheletro embrionale allungamento delle ossa (piastra metafisaria) movimento dei capi articolari.
 Funzione: Cartilagine sostegno scheletro embrionale allungamento delle ossa (piastra metafisaria) movimento dei capi articolari Caratteristiche: resistente, elastica, deformabile MATRICE fibre sostanza
Funzione: Cartilagine sostegno scheletro embrionale allungamento delle ossa (piastra metafisaria) movimento dei capi articolari Caratteristiche: resistente, elastica, deformabile MATRICE fibre sostanza
04-07/10 Tessuti fondamentali, struttura degli organi.
 Programma settimanale 04-07/10 Tessuti fondamentali, struttura degli organi. Tessuti epiteliali (di rivestimento, ghiandolari) Tessuti connettivi (propriamente detti, liquidi o a funzione trofica, di sostegno)
Programma settimanale 04-07/10 Tessuti fondamentali, struttura degli organi. Tessuti epiteliali (di rivestimento, ghiandolari) Tessuti connettivi (propriamente detti, liquidi o a funzione trofica, di sostegno)
OSTEOGENESI. ( ossa del cranio, mandibola, clavicola ) OSSIFICAZIONE INDIRETTA (endocondrale)
 OSTEOGENESI DIRETTA (intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima, pericondrio, osso) ( ossa del cranio, mandibola, clavicola ) INDIRETTA (endocondrale)
OSTEOGENESI DIRETTA (intramembranosa) Formazione di tessuto osseo su una preesistente matrice connettivale (mesenchima, pericondrio, osso) ( ossa del cranio, mandibola, clavicola ) INDIRETTA (endocondrale)
TESSUTI CONNETTIVI. 2) connettivi a funzione trofica (sangue, linfa) 3) T. connettivi di sostegno (cartilagine, osso) SANGUE FUNZIONI
 TESSUTI CONNETTIVI 1) T. connettivo propriamente detto (TCPD) 2) connettivi a funzione trofica (sangue, linfa) 3) T. connettivi di sostegno (cartilagine, osso) SANGUE SOSTANZA INTERCELLULARE fluida: il
TESSUTI CONNETTIVI 1) T. connettivo propriamente detto (TCPD) 2) connettivi a funzione trofica (sangue, linfa) 3) T. connettivi di sostegno (cartilagine, osso) SANGUE SOSTANZA INTERCELLULARE fluida: il
Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Le cellule sono immerse in una matrice mineralizzata
 Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno (ma dinamico!!!!) Organizzato in
Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno (ma dinamico!!!!) Organizzato in
Tessuto osseo. Tessuto osseo. Tessuto osseo. Tessuto di sostegno (ma dinamico!!!!) Ca ++
 Tessuto osseo Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Protegge i visceri Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno
Tessuto osseo Tessuto osseo Tessuto connettivo specializzato (Cellule + Fibre + Matrice organica e minerale) Protegge i visceri Le cellule sono immerse in una matrice mineralizzata Tessuto di sostegno
Guarigione delle ferite
 Guarigione delle ferite Possono essere riconosciute tre componenti in parte funzionalmente e temporaneamente distinte, ma intimamente interconnesse: Emostasi Infiammazione Riparazione Emostasi L emorragia
Guarigione delle ferite Possono essere riconosciute tre componenti in parte funzionalmente e temporaneamente distinte, ma intimamente interconnesse: Emostasi Infiammazione Riparazione Emostasi L emorragia
Osteogenesi formativa diretta o intramembranosa
 Osteogenesi formativa diretta o intramembranosa Dal tessuto connettivo Cellule mesenchimali > osteoblasti Produzione di matrice mucoproteica e fibre collagene Sostanza osteoide Deposizione d idrossiapatite
Osteogenesi formativa diretta o intramembranosa Dal tessuto connettivo Cellule mesenchimali > osteoblasti Produzione di matrice mucoproteica e fibre collagene Sostanza osteoide Deposizione d idrossiapatite
14/10 Tessuti fondamentali, struttura degli organi.
 14/10 Tessuti fondamentali, struttura degli organi. Tessuti connettivi (propriamente detti, liquidi o a funzione trofica, di sostegno) Tessuti muscolari (striato scheletrico e cardiaco, liscio) Tessuto
14/10 Tessuti fondamentali, struttura degli organi. Tessuti connettivi (propriamente detti, liquidi o a funzione trofica, di sostegno) Tessuti muscolari (striato scheletrico e cardiaco, liscio) Tessuto
Carmen Ciavarella, PhD
 Le MSC vascolari determinano lo sviluppo e la progressione della patologia aterosclerotica, mediante iper-espressione di MMP-9 e pronunciato differenziamento osteogenico in condizioni infiammatorie Carmen
Le MSC vascolari determinano lo sviluppo e la progressione della patologia aterosclerotica, mediante iper-espressione di MMP-9 e pronunciato differenziamento osteogenico in condizioni infiammatorie Carmen
1. INTRODUZIONE 1.1. Struttura del tessuto osseo
 1. INTRODUZIONE 1.1. Struttura del tessuto osseo Il tessuto osseo è costituito dagli osteociti, derivanti dagli elementi che sintetizzano la matrice ossea (osteoblasti) e da sostanza fondamentale costituita
1. INTRODUZIONE 1.1. Struttura del tessuto osseo Il tessuto osseo è costituito dagli osteociti, derivanti dagli elementi che sintetizzano la matrice ossea (osteoblasti) e da sostanza fondamentale costituita
I FATTORI DI CRESCITA IN ORTOPEDIA
 I FATTORI DI CRESCITA IN ORTOPEDIA Dott. VINICIO L. G. PERRONE Medico Chirurgo Specialista in Ortopedia e Traumatologia Divisione Ortopedia e Traumatologia Ospedale S. Cuore di Gesù Gallipoli (LE) L ingegneria
I FATTORI DI CRESCITA IN ORTOPEDIA Dott. VINICIO L. G. PERRONE Medico Chirurgo Specialista in Ortopedia e Traumatologia Divisione Ortopedia e Traumatologia Ospedale S. Cuore di Gesù Gallipoli (LE) L ingegneria
IL TESSUTO OSSEO. (resistenza e leggerezza)
 IL TESSUTO OSSEO (resistenza e leggerezza) Il tessuto osseo è un tessuto connettivo caratterizzato dalla matrice intercellulare mineralizzata Forma le ossa dello scheletro Lo scheletro umano adulto è formato
IL TESSUTO OSSEO (resistenza e leggerezza) Il tessuto osseo è un tessuto connettivo caratterizzato dalla matrice intercellulare mineralizzata Forma le ossa dello scheletro Lo scheletro umano adulto è formato
TESSUTO OSSEO funzione
 TESSUTO OSSEO è un tipo particolare di tessuto connettivo in quanto è mineralizzato questo gli conferisce particolari caratteristiche: è un tessuto resistente, presenta un certo grado di flessibilità e
TESSUTO OSSEO è un tipo particolare di tessuto connettivo in quanto è mineralizzato questo gli conferisce particolari caratteristiche: è un tessuto resistente, presenta un certo grado di flessibilità e
composizione: 65% di cristalli di Ca sotto forma di cristalli di idrossiapatite 25% di proteine collageniche 2% di proteine non collageniche 10% di
 TESSUTO OSSEO è un tipo particolare di tessuto connettivo in quanto è mineralizzato questo gli conferisce particolari caratteristiche: è un tessuto resistente, ma presenta un certo grado di flessibilità
TESSUTO OSSEO è un tipo particolare di tessuto connettivo in quanto è mineralizzato questo gli conferisce particolari caratteristiche: è un tessuto resistente, ma presenta un certo grado di flessibilità
TESSUTO OSSEO. CARATTERISTICHE: Denso Compatto Solido Leggero Elastico Basso peso specifico
 CARATTERISTICHE: Denso Compatto Solido Leggero Elastico Basso peso specifico TESSUTO OSSEO Resistente alle azioni meccaniche (trazione, compressione, torsione e flessione) OSSO (tessuto connettivo) matrice
CARATTERISTICHE: Denso Compatto Solido Leggero Elastico Basso peso specifico TESSUTO OSSEO Resistente alle azioni meccaniche (trazione, compressione, torsione e flessione) OSSO (tessuto connettivo) matrice
INTRODUZIONE ALLE REAZIONI FLOGISTICHE
 INTRODUZIONE ALLE REAZIONI FLOGISTICHE INCONTRO FRA CELLUA E NOXA PATOGENA: SEQUENZA DEGLI EVENTI noxa patogena adattamento cellula danno irreversibile danno reversibile - stress proteins - enzimi di riparazione
INTRODUZIONE ALLE REAZIONI FLOGISTICHE INCONTRO FRA CELLUA E NOXA PATOGENA: SEQUENZA DEGLI EVENTI noxa patogena adattamento cellula danno irreversibile danno reversibile - stress proteins - enzimi di riparazione
T I S S O U R E G E N E R A T I V E C O M P A N Y
 T I S S REGENERATIVE COMPANY O U IMMUNITÀ INNATA E RIGENERAZIONE Il sistema immunitario gioca un ruolo critico nello sviluppo, nell omeostasi e nella riparazione dei tessuti. I monociti e i macrofagi rispondono
T I S S REGENERATIVE COMPANY O U IMMUNITÀ INNATA E RIGENERAZIONE Il sistema immunitario gioca un ruolo critico nello sviluppo, nell omeostasi e nella riparazione dei tessuti. I monociti e i macrofagi rispondono
Il tessuto cartilagineo
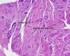 Il tessuto cartilagineo CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: Condroblasti, Condrociti, Condroclasti (che derivano dai monociti del sangue) La ECM è compatta e contiene: fibre,
Il tessuto cartilagineo CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: Condroblasti, Condrociti, Condroclasti (che derivano dai monociti del sangue) La ECM è compatta e contiene: fibre,
Struttura del tessuto osseo
 Struttura del tessuto osseo Classificazione in base alla forma: Ossa lunghe Zona allungata posta fra due teste globose (tibia) Ossa corte Lunghezza e larghezza uguali (carpali del polso) Ossa piatte Sottili,
Struttura del tessuto osseo Classificazione in base alla forma: Ossa lunghe Zona allungata posta fra due teste globose (tibia) Ossa corte Lunghezza e larghezza uguali (carpali del polso) Ossa piatte Sottili,
Il tessuto cartilagineo
 Il tessuto cartilagineo CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: Condroblasti, Condrociti, Condroclasti (derivano dai monociti del sangue) La ECM è compatta e contiene: Fibre (soprattutto
Il tessuto cartilagineo CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: Condroblasti, Condrociti, Condroclasti (derivano dai monociti del sangue) La ECM è compatta e contiene: Fibre (soprattutto
Immunologia e Immunopatologia. LINFOCITI T HELPER: Citochine dell Immunità Specifica
 Immunologia e Immunopatologia LINFOCITI T HELPER: Citochine dell Immunità Specifica Linfociti T effettori T helper: regolazione dell immunità specifica Attivazione macrofagi Secrezione Ab, scambio isotipico
Immunologia e Immunopatologia LINFOCITI T HELPER: Citochine dell Immunità Specifica Linfociti T effettori T helper: regolazione dell immunità specifica Attivazione macrofagi Secrezione Ab, scambio isotipico
Sviluppo del tessuto osseo. Osteogenesis and reparative osteogenesis muscle tissue. Giuseppe M. Peretti
 Osteogenesis and reparative osteogenesis muscle tissue Giuseppe M. Peretti I testi e le immagini che verranno presentati sono un sussidio didattico alle lezioni del corso di Morfologia Umana riguardanti
Osteogenesis and reparative osteogenesis muscle tissue Giuseppe M. Peretti I testi e le immagini che verranno presentati sono un sussidio didattico alle lezioni del corso di Morfologia Umana riguardanti
Regolazione endocrina della crescita
 Regolazione endocrina della crescita Determinazione genica Dieta adeguata Assenza di malattie croniche e condizioni ambientali stressanti (che inducono rilascio di cortisolo attività catabolica) Livelli
Regolazione endocrina della crescita Determinazione genica Dieta adeguata Assenza di malattie croniche e condizioni ambientali stressanti (che inducono rilascio di cortisolo attività catabolica) Livelli
Immunità cellulo-mediata
 Immunità cellulo-mediata Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari Immunità cellulo-mediata
Immunità cellulo-mediata Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari Immunità cellulo-mediata
Cartilagine. connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno
 Cartilagine connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno nell individuo adulto, la cartilagine si trova Superfici articolari Cartilagini costali Orecchio
Cartilagine connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno nell individuo adulto, la cartilagine si trova Superfici articolari Cartilagini costali Orecchio
Connettivi Specializzati. Cartilagine Osso Sangue
 Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata Funzione: - Fornisce impalcatura per la protezione e il movimento - Riserva di
Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata Funzione: - Fornisce impalcatura per la protezione e il movimento - Riserva di
Tessuto osseo. Caratteristiche generali: -Colore, leggerezza, resistenza. COMPONENTI: -Cellule e matrice extracellulare
 Tessuto osseo Varietà di tessuto connettivo a prevalente funzione meccanica, di sostegno e di protezione, ma anche metabolica ( riserva di minerali) e di movimento (dando attacco ai muscoli) Caratteristiche
Tessuto osseo Varietà di tessuto connettivo a prevalente funzione meccanica, di sostegno e di protezione, ma anche metabolica ( riserva di minerali) e di movimento (dando attacco ai muscoli) Caratteristiche
ISOLAMENTO E CARATTERIZZAZIONE DI ms-hsc (MUSCLE DERIVED HEMATOPOIETIC STEM CELLS) IN HIRUDO MEDICINALIS
 UNIVERSITA DEGLI STUDI DELL INSUBRIA FACOLTA DI SCIENZE MATEMATICHE, FISICHE E NATURALI VARESE Corso di Laurea Triennale in Biologia Sanitaria ISOLAMENTO E CARATTERIZZAZIONE DI ms-hsc (MUSCLE DERIVED HEMATOPOIETIC
UNIVERSITA DEGLI STUDI DELL INSUBRIA FACOLTA DI SCIENZE MATEMATICHE, FISICHE E NATURALI VARESE Corso di Laurea Triennale in Biologia Sanitaria ISOLAMENTO E CARATTERIZZAZIONE DI ms-hsc (MUSCLE DERIVED HEMATOPOIETIC
LESIONI DELL APPARATO EFFETTORE DEL MOVIMENTO
 LESIONI DELL APPARATO EFFETTORE DEL MOVIMENTO APPARATO EFFETTORE DEL MOVIMENTO Insieme di organi ed apparati che realizzano il movimento: Apparato osteo-articolare Muscoli e tendini SNP PROCESSO INFIAMMATORIO
LESIONI DELL APPARATO EFFETTORE DEL MOVIMENTO APPARATO EFFETTORE DEL MOVIMENTO Insieme di organi ed apparati che realizzano il movimento: Apparato osteo-articolare Muscoli e tendini SNP PROCESSO INFIAMMATORIO
cartilagine connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno
 cartilagine connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno nell individuo adulto, la cartilagine si trova Superfici articolari Cartilagini costali Orecchio
cartilagine connettivo a carattere solido costituisce, insieme all osso, i cosiddetti tessuti di sostegno nell individuo adulto, la cartilagine si trova Superfici articolari Cartilagini costali Orecchio
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Dr. Alessandro Lorusso Fisioterapista. Docente di: Patologia ortopedica
 Dr. Alessandro Lorusso Fisioterapista Docente di: Patologia ortopedica Patologia Ortopedica: Fratture Ossee Frattura e Contusione TRAUMA: Forza diretta o indiretta applicata ad un determinato segmento
Dr. Alessandro Lorusso Fisioterapista Docente di: Patologia ortopedica Patologia Ortopedica: Fratture Ossee Frattura e Contusione TRAUMA: Forza diretta o indiretta applicata ad un determinato segmento
Regolazione endocrina della crescita
 Regolazione endocrina della crescita Determinazione genica Dieta adeguata Assenza di malattie croniche e condizioni ambientali stressanti (che inducono rilascio di cortisolo attività catabolica) Livelli
Regolazione endocrina della crescita Determinazione genica Dieta adeguata Assenza di malattie croniche e condizioni ambientali stressanti (che inducono rilascio di cortisolo attività catabolica) Livelli
Lezione n. 2: Biologia dei tumori
 CORSO INTEGRATO: PROBLEMI DI SALUTE III (ONCOLOGICI) Lezione n. 2: Biologia dei tumori Franco Testore Argomenti Principi di proliferazione cellulare Meccanismi di regolazione della crescita e della proliferazione
CORSO INTEGRATO: PROBLEMI DI SALUTE III (ONCOLOGICI) Lezione n. 2: Biologia dei tumori Franco Testore Argomenti Principi di proliferazione cellulare Meccanismi di regolazione della crescita e della proliferazione
FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE
 FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE Carboidrati proteine Glicolipide Regione ad a-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di membrana
FUNZIONE CELLULARE E TRAFFICO INTRACELLULARE Carboidrati proteine Glicolipide Regione ad a-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di membrana
Il tessuto cartilagineo (t. connettivo specializzato)
 Il tessuto cartilagineo (t. connettivo specializzato) -plasticità ed elasticità superficie ammortizzante per le articolazioni; levigatezza scorrimento superfici articolari -modello per la formazione del
Il tessuto cartilagineo (t. connettivo specializzato) -plasticità ed elasticità superficie ammortizzante per le articolazioni; levigatezza scorrimento superfici articolari -modello per la formazione del
TESSUTO CARTILAGINEO. Le principali caratteristiche di questo tessuto sono la solidità,, la flessibilità e la capacità di deformarsi limitatamente
 TESSUTO CARTILAGINEO I tessuti scheletrici, cartilagine e osso,, sono essenzialmente tessuti connettivi specializzati costituiti dai medesimi tre componenti: Cellule immerse in una matrice extracellulare
TESSUTO CARTILAGINEO I tessuti scheletrici, cartilagine e osso,, sono essenzialmente tessuti connettivi specializzati costituiti dai medesimi tre componenti: Cellule immerse in una matrice extracellulare
Schema delle citochine
 Schema delle citochine 13 gennaio 2011 1 Risposta innata TNF - Tumor Necrosis Factor Fonti principali: fagociti attivati, NK e mastociti. Struttura e recettore: inizialmente proteina di membrana, poi tagliata
Schema delle citochine 13 gennaio 2011 1 Risposta innata TNF - Tumor Necrosis Factor Fonti principali: fagociti attivati, NK e mastociti. Struttura e recettore: inizialmente proteina di membrana, poi tagliata
I MEDIATORI CHIMICI DELLA FLOGOSI
 I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
I MEDIATORI CHIMICI DELLA FLOGOSI I mediatori chimici della flogosi attualmente noti sono numerosissimi e la loro conoscenza dettagliata va ben oltre gli obiettivi del corso. Punteremo, pertanto, l attenzione
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Infiammazione (flogosi)
 Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Calor Rubor Tumor Dolor Functio laesa Equilibrio dei fluidi
Infiammazione (flogosi) Reazione di un tessuto vascolarizzato ad un danno locale Componente vascolare Componente cellulare Infiammazione acuta Calor Rubor Tumor Dolor Functio laesa Equilibrio dei fluidi
TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE
 TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE Carboidrati proteine Glicolipide Regione ad α-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di
TRAFFICO INTRACELLULARE E COMUNICAZIONE TRA LE CELLULE Carboidrati proteine Glicolipide Regione ad α-elica di proteina transmembrana Acido grasso Doppio strato Fosfolipidico 5-8 nm Proteina integrale di
TCR e maturazione linfociti T
 ATTENZIONE: questi file compresi testo ed immagini in essi contenuti sono destinati esclusivamente agli studenti del corso per favorirne lo studio. Nessun file, che potrebbe contenere materiale soggetto
ATTENZIONE: questi file compresi testo ed immagini in essi contenuti sono destinati esclusivamente agli studenti del corso per favorirne lo studio. Nessun file, che potrebbe contenere materiale soggetto
Tipi di TESSUTO CONNETTIVO. Tessuto connettivo propriamente detto e connettivi specializzati
 Tipi di TESSUTO CONNETTIVO Tessuto connettivo propriamente detto e connettivi specializzati Connettivi di sostegno Tessuto osseo: mineralizzato -> rigido/duro vascolarizzato Cartilagine: leggera e flessibile
Tipi di TESSUTO CONNETTIVO Tessuto connettivo propriamente detto e connettivi specializzati Connettivi di sostegno Tessuto osseo: mineralizzato -> rigido/duro vascolarizzato Cartilagine: leggera e flessibile
Tessuto osseo. Costituzione del tessuto osseo
 Tessuto osseo Tessuto connettivo a prevalente funzione meccanica, di sostegno e di protezione, ma anche metabolica ( riserva di calcio) Caratteristiche generali: Durezza, resistenza meccanica a trazione
Tessuto osseo Tessuto connettivo a prevalente funzione meccanica, di sostegno e di protezione, ma anche metabolica ( riserva di calcio) Caratteristiche generali: Durezza, resistenza meccanica a trazione
TCR e maturazione linfociti T
 TCR e maturazione linfociti T Il recettore per l Ag dei linfociti T, T-Cell Receptor (TCR) eterodimero composto da catene a e b o g e d TCR a/b presente in 95% delle cellule T periferiche eterodimero legato
TCR e maturazione linfociti T Il recettore per l Ag dei linfociti T, T-Cell Receptor (TCR) eterodimero composto da catene a e b o g e d TCR a/b presente in 95% delle cellule T periferiche eterodimero legato
La vita media delle cellule del sangue è breve
 La vita media delle cellule del sangue è breve Eritrociti: 120 giorni Neutrofili: 6 ore in circolo; pochi giorni nei tessuti Eosinofili: 8-12 giorni Monociti: 14 ore in circolo; mesi-anni nei tessuti (macrofagi)
La vita media delle cellule del sangue è breve Eritrociti: 120 giorni Neutrofili: 6 ore in circolo; pochi giorni nei tessuti Eosinofili: 8-12 giorni Monociti: 14 ore in circolo; mesi-anni nei tessuti (macrofagi)
LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors)
 LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors) PERCHE QUESTA TERAPIA? Il corpo umano è fatto in modo di autodifendersi dai danni che possono colpirlo, e soprattutto
LA TECNICA DEL PRGF: IL PLASMA RICCO DI FATTORI di CRESCITA (Plasma Riched of Growth Factors) PERCHE QUESTA TERAPIA? Il corpo umano è fatto in modo di autodifendersi dai danni che possono colpirlo, e soprattutto
Meccanismi effettori dei linfociti T citotossici
 Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
immunità adattativa o acquisita
 immunità adattativa o acquisita L immunità adattativa è dovuta all attività dei linfociti che, a seguito del contatto con un antigene, producono risposte effettrici specifiche, cioè dirette solo contro
immunità adattativa o acquisita L immunità adattativa è dovuta all attività dei linfociti che, a seguito del contatto con un antigene, producono risposte effettrici specifiche, cioè dirette solo contro
Evoluzione del focolaio di frattura
 Evoluzione del focolaio di frattura Necrosi delle estremità dei monconi Per interruzione dei canali vascolari Attivazione della neoangiogenesi Compenetrazione del tessuto necrotico Attivazione del processo
Evoluzione del focolaio di frattura Necrosi delle estremità dei monconi Per interruzione dei canali vascolari Attivazione della neoangiogenesi Compenetrazione del tessuto necrotico Attivazione del processo
Connettivi Specializzati. Cartilagine Osso Sangue
 Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata ed imprigiona le cellule che l hanno prodotta Funzione: Fornisce impalcatura
Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata ed imprigiona le cellule che l hanno prodotta Funzione: Fornisce impalcatura
Biomaterials Catalog 2012
 dx Biomaterials Division Biomaterials Catalog 2012 Stampato da: Tipo-lito ABALTI G.F. - Creazzo (VI) Dental X...un partner con molta esperienza. Dental X da più di 20 anni ha legato il suo nome al mondo
dx Biomaterials Division Biomaterials Catalog 2012 Stampato da: Tipo-lito ABALTI G.F. - Creazzo (VI) Dental X...un partner con molta esperienza. Dental X da più di 20 anni ha legato il suo nome al mondo
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare
 Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
Deposizione tessuto connettivo. Risoluzione Cicatriziale Fibroblasti Fibrosi cronica
 7 fibrosi Deposizione tessuto connettivo Risoluzione Cicatriziale Fibroblasti Fibrosi cronica Riparazione tessutale 1. Rigenerazione 1. Cellulare 2. Tessutale 2. Deposizione di tessuto connettivo 1. Cicatrice
7 fibrosi Deposizione tessuto connettivo Risoluzione Cicatriziale Fibroblasti Fibrosi cronica Riparazione tessutale 1. Rigenerazione 1. Cellulare 2. Tessutale 2. Deposizione di tessuto connettivo 1. Cicatrice
La Cute: definizione
 LA CUTE La Cute: definizione Organo che ricopre la superficie corporea Protezione contro le aggressioni esterne, termoregolazione e protezione immunologica Barriera fra i tessuti, gli organi interni e
LA CUTE La Cute: definizione Organo che ricopre la superficie corporea Protezione contro le aggressioni esterne, termoregolazione e protezione immunologica Barriera fra i tessuti, gli organi interni e
REGOLAZIONE DEL CICLO CELLULARE
 REGOLAZIONE DEL CICLO CELLULARE Il sistema di controllo che regola la progressione del ciclo cellulare deve: 1) Garantire che tutti i processi associati con le diverse fasi siano portati a termine al tempo
REGOLAZIONE DEL CICLO CELLULARE Il sistema di controllo che regola la progressione del ciclo cellulare deve: 1) Garantire che tutti i processi associati con le diverse fasi siano portati a termine al tempo
Forma specializzata di connettivo: la ECM è mineralizzata per cui il tessuto ha notevole resistenza e durezza
 Tessuto osseo Forma specializzata di connettivo: la ECM è mineralizzata per cui il tessuto ha notevole resistenza e durezza L osso è al contempo resistente e leggero Non è un tessuto statico; è continuamente
Tessuto osseo Forma specializzata di connettivo: la ECM è mineralizzata per cui il tessuto ha notevole resistenza e durezza L osso è al contempo resistente e leggero Non è un tessuto statico; è continuamente
Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari
 Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari La gran parte delle citochine sono per convenzione chiamate interleuchine ad indicare che queste sono prodotte dai
Piccole proteine (15-30kDal) Riconosciute da recettori Secrete da diversi tipi cellulari La gran parte delle citochine sono per convenzione chiamate interleuchine ad indicare che queste sono prodotte dai
Caratteristiche biologiche degli emocomponenti ad uso non trasfusionale. Marina Buzzi
 Caratteristiche biologiche degli emocomponenti ad uso non trasfusionale Marina Buzzi adult newt can regenerate: Jaws Lens Retina Large sections of the heart Limbs Tail Regeneration might be a primordial
Caratteristiche biologiche degli emocomponenti ad uso non trasfusionale Marina Buzzi adult newt can regenerate: Jaws Lens Retina Large sections of the heart Limbs Tail Regeneration might be a primordial
Leading regeneration: qualità, affidabilità, e convenienza.
 SOSTITUTO OSSEO Leading regeneration: qualità, affidabilità, e convenienza. La produzione secondo i più elevati standard qualitativi, e le peculiarità innovative del prodotto vi conducono alla scelta ottimale
SOSTITUTO OSSEO Leading regeneration: qualità, affidabilità, e convenienza. La produzione secondo i più elevati standard qualitativi, e le peculiarità innovative del prodotto vi conducono alla scelta ottimale
FLOGOSI CRONICA: CAUSE
 FLOGOSI CRONICA FLOGOSI CRONICA: CAUSE inadeguatezza della risposta flogistica acuta nell eliminare la noxa caratteristiche della noxa che inducono reazione cronica 1- infezioni a basso potenziale proflogistico
FLOGOSI CRONICA FLOGOSI CRONICA: CAUSE inadeguatezza della risposta flogistica acuta nell eliminare la noxa caratteristiche della noxa che inducono reazione cronica 1- infezioni a basso potenziale proflogistico
Connettivi Specializzati. Cartilagine Osso Sangue
 Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata ed imprigiona le cellule che l hanno prodotta Funzione: Fornisce impalcatura
Connettivi Specializzati Cartilagine Osso Sangue Osso Connettivo specializzato, la cui matrice extracellulare è calcificata ed imprigiona le cellule che l hanno prodotta Funzione: Fornisce impalcatura
INTRODUZIONE. La riabilitazione orale di tipo fisso mediante impianti osseointegrati nei
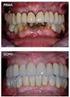 INTRODUZIONE La riabilitazione orale di tipo fisso mediante impianti osseointegrati nei pazienti totalmente o parzialmente edentuli è una tecnica che presenta follow-up ormai soddisfacenti nell odontoiatria
INTRODUZIONE La riabilitazione orale di tipo fisso mediante impianti osseointegrati nei pazienti totalmente o parzialmente edentuli è una tecnica che presenta follow-up ormai soddisfacenti nell odontoiatria
Osteoporosi Post Menopausale. Ruolo degli estrogeni ed attuali orientamenti di condotta clinica sul loro
 Osteoporosi Post Menopausale Ruolo degli estrogeni ed attuali orientamenti di condotta clinica sul loro utilizzo. OSTEOPOROSI: DEFINIZIONE Affezione caratterizzata da riduzione della massa ossea E alterazione
Osteoporosi Post Menopausale Ruolo degli estrogeni ed attuali orientamenti di condotta clinica sul loro utilizzo. OSTEOPOROSI: DEFINIZIONE Affezione caratterizzata da riduzione della massa ossea E alterazione
RIFLESSIONI SU CASI PARTICOLARI
 AZIENDA OSPEDALIERA Istituti Clinici di Perfezionamento -C.T.O.- CLINICA ORTOPEDICA Direttore: Prof. R. Facchini Università degli Studi di Milano Società italiana di ortopedia e traumatologia pediatrica
AZIENDA OSPEDALIERA Istituti Clinici di Perfezionamento -C.T.O.- CLINICA ORTOPEDICA Direttore: Prof. R. Facchini Università degli Studi di Milano Società italiana di ortopedia e traumatologia pediatrica
QUALE È LA COMPOSIZIONE DEL SANGUE?
 QUALE È LA COMPOSIZIONE DEL SANGUE? 1/2 COMPOSIZIONE DEL SANGUE 45% FORMATO DA CELLULE 55% FORMATO DAL PLASMA IL SANGUE CHE CIRCOLA NELL ORGANISMO CORRISPONDE ALL 8% CIRCA del PESO CORPOREO 1/3 IL PLASMA
QUALE È LA COMPOSIZIONE DEL SANGUE? 1/2 COMPOSIZIONE DEL SANGUE 45% FORMATO DA CELLULE 55% FORMATO DAL PLASMA IL SANGUE CHE CIRCOLA NELL ORGANISMO CORRISPONDE ALL 8% CIRCA del PESO CORPOREO 1/3 IL PLASMA
G1: marcato accrescimento della cellula, che sintetizza componenti strutturali ed enzimi per la duplicazione del DNA.
 Il ciclo cellulare G1: marcato accrescimento della cellula, che sintetizza componenti strutturali ed enzimi per la duplicazione del DNA. S: duplicazione del DNA e sintesi di proteine cromosomiche G2:
Il ciclo cellulare G1: marcato accrescimento della cellula, che sintetizza componenti strutturali ed enzimi per la duplicazione del DNA. S: duplicazione del DNA e sintesi di proteine cromosomiche G2:
APPARATO LOCOMOTORE. Sistema scheletrico: Ossa, Cartilagini ed Articolazioni. Sistema muscolare scheletrico: Muscoli Scheletrici e Tendini
 APPARATO LOCOMOTORE Sistema scheletrico: Ossa, Cartilagini ed Articolazioni (Osteoartrologia) Sistema muscolare scheletrico: Muscoli Scheletrici e Tendini (Miologia) Nessun sistema lavora isolatamente..
APPARATO LOCOMOTORE Sistema scheletrico: Ossa, Cartilagini ed Articolazioni (Osteoartrologia) Sistema muscolare scheletrico: Muscoli Scheletrici e Tendini (Miologia) Nessun sistema lavora isolatamente..
Trasduzione del segnale
 Trasduzione del segnale Modalità di segnalazione tra cellule JUXTACRINA proteine transmembrana mediatori locali ormoni Il legame di una sostanza al suo recettore di membrana porta la cellula a cambiare
Trasduzione del segnale Modalità di segnalazione tra cellule JUXTACRINA proteine transmembrana mediatori locali ormoni Il legame di una sostanza al suo recettore di membrana porta la cellula a cambiare
Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad
 Esotossine ed Endotossine prof. Vincenzo Cuteri Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad attività
Esotossine ed Endotossine prof. Vincenzo Cuteri Esotossina: definizione Prodotto del metabolismo di alcuni batteri che viene riversato nel mezzo in cui essi sono posti a sviluppare Glicoproteine ad attività
ISTOLOGIA ED EMBRIOLOGIA - canale 1
 DIPARTIMENTO DI CHIRURGIA GENERALE E SPECIALITÀ MEDICO-CHIRURGICHE Corso di laurea magistrale in Medicina e chirurgia Anno accademico 2016/2017-1 anno ISTOLOGIA ED EMBRIOLOGIA - canale 1 7 CFU - 2 semestre
DIPARTIMENTO DI CHIRURGIA GENERALE E SPECIALITÀ MEDICO-CHIRURGICHE Corso di laurea magistrale in Medicina e chirurgia Anno accademico 2016/2017-1 anno ISTOLOGIA ED EMBRIOLOGIA - canale 1 7 CFU - 2 semestre
FATTORI DI CRESCITA COME MESSAGGERI
 RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
RECETTORI ASSOCIATI A PROTEINE CHINASI Sono proteine che hanno sia funzione di recettore che attività enzimatica chinasica. L interazione con il ligando specifico stimola l attività della chinasi e il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI
 Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata. Ciclo Cellulare
 Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
La biologia: fattori di crescita, cellule staminali A Vitullo
 La biologia: fattori di crescita, cellule staminali A Vitullo Introduzione La patologia della cuffia dei rotatori è la condizione più frequente per cui il paziente richiede un trattamento per la spalla;
La biologia: fattori di crescita, cellule staminali A Vitullo Introduzione La patologia della cuffia dei rotatori è la condizione più frequente per cui il paziente richiede un trattamento per la spalla;
A.A.: 2016/2017 Infermieristica Polo A. Anno di corso: I Semestre: I Insegnamento: ISTOLOGIA Coordinatore: Prof. PAOLA CASTROGIOVANNI CFU: 2.
 A.A.: 2016/2017 Infermieristica Polo A. Anno di corso: I Semestre: I Insegnamento: ISTOLOGIA Coordinatore: Prof. PAOLA CASTROGIOVANNI CFU: 2 Italiano Testi consigliati Obiettivi formativi Adamo, Comoglio,
A.A.: 2016/2017 Infermieristica Polo A. Anno di corso: I Semestre: I Insegnamento: ISTOLOGIA Coordinatore: Prof. PAOLA CASTROGIOVANNI CFU: 2 Italiano Testi consigliati Obiettivi formativi Adamo, Comoglio,
Tessuto Cartilagineo e Osseo
 Tessuti connettivi specializzati: Tessuti di sostegno Tessuto Cartilagineo Tessuti connettivi specializzati: Tessuti di sostegno Tessuto Osseo e Osseo Matrice: lastica Cellule: Condroblasti, Condrociti
Tessuti connettivi specializzati: Tessuti di sostegno Tessuto Cartilagineo Tessuti connettivi specializzati: Tessuti di sostegno Tessuto Osseo e Osseo Matrice: lastica Cellule: Condroblasti, Condrociti
La vita media delle cellule del sangue è breve
 La vita media delle cellule del sangue è breve Eritrociti: 120 giorni Neutrofili: 6 ore in circolo; pochi giorni nei tessuti Eosinofili: 8-12 giorni Monociti: 14 ore in circolo; mesi-anni nei tessuti (macrofagi)
La vita media delle cellule del sangue è breve Eritrociti: 120 giorni Neutrofili: 6 ore in circolo; pochi giorni nei tessuti Eosinofili: 8-12 giorni Monociti: 14 ore in circolo; mesi-anni nei tessuti (macrofagi)
CARTILAGINE. NON sono presenti vasi sanguigni
 CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: condrociti circondati da una ECM compatta, contenente: fibre, proteoglicani, glicoproteine I condrociti sono situati in cavità dette lacune
CARTILAGINE Tessuto connettivo di sostegno costituito da cellule: condrociti circondati da una ECM compatta, contenente: fibre, proteoglicani, glicoproteine I condrociti sono situati in cavità dette lacune
COME FUNZIONA IL SISTEMA IMMUNITARIO
 COME FUNZIONA IL COME FUNZIONA IL SISTEMA IMMUNITARIO I vertebrati possiedono complessi meccanismi difensivi che costituiscono il sistema immunitario, che li protegge dall invasione di microrganismi patogeni,
COME FUNZIONA IL COME FUNZIONA IL SISTEMA IMMUNITARIO I vertebrati possiedono complessi meccanismi difensivi che costituiscono il sistema immunitario, che li protegge dall invasione di microrganismi patogeni,
Recettori di superficie
 Recettori di superficie Esistono 3 classi principali di recettori di superficie 1. Recettori annessi a canali ionici 2. Recettori accoppiati alle proteine G 3. Recettori associati ad enzimi Recettori
Recettori di superficie Esistono 3 classi principali di recettori di superficie 1. Recettori annessi a canali ionici 2. Recettori accoppiati alle proteine G 3. Recettori associati ad enzimi Recettori
