CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU)
|
|
|
- Niccoletta Cirillo
- 5 anni fa
- Visualizzazioni
Transcript
1 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU) Roberto Giacominelli Stuffler
2 IL CORSO MONODISCIPLINARE DI BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) LE MOLECOLE BIOLOGICHE B) ENZIMOLOGIA ED ELEMENTI DI BIOLOGIA MOLECOLARE 2
3 L UNITÀ DIDATTICA LE MOLECOLE BIOLOGICHE COMPRENDE: 1) I LIPIDI 2) I CARBOIDRATI 3) GLI AMMINOACIDI E LE PROTEINE 4) LE PROTEINE DEL CONNETTIVO 5) LA MIOGLOBINA E L EMOGLOBINAL 3
4 L UNITÀ DIDATTICA ENZIMOLOGIA ED ELEMENTI DI BIOLOGIA MOLECOLARE COMPRENDE: 1) ENZIMOLOGIA 2) LA BIOLOGIA MOLECOLARE DEI PROCARIOTI 3) LA BIOLOGIA MOLECOLARE DEGLI EUCARIOTI 4) L EVOLUZIONEL 4
5 UNITÀ DIDATTICA LE MOLECOLE BIOLOGICHE 5
6 UNITÀ BIOTEC. DIDATTICA LE MOLECOLE BIOLOGICHE LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA. Roberto Giacominelli Stuffler
7 IL COLLAGENO 7
8 IL COLLAGENO E una famiglia di proteine fibrose con ruolo strutturale, nei vertebrati costituisce ~ il 25% delle proteine totali, forma fibre insolubili che hanno una elevata resistenza alla tensione. 8
9 -elica della cheratina passo 5.1Å c g d a e b avvolgimento avvolto f b e a d g c f protofilamento cellule e filamento intermedio protofibrilla protofibrilla protofilamento LE PROTEINE FIBROSE avvolgimento avvolto -elica della cheratina 9
10 IL COLLAGENO È presente in tutti gli organismi multicellulari: - nelle ossa e nei denti é un polimero di fosfato di calcio, - nella cornea dell occhio é così ordinato da risultare trasparente, - nei tendini é organizzato in fibre simili a funi, - nella pelle é in fibre poco intrecciate rivolte in ogni direzione, - nei vasi sanguigni é organizzato in fibre disposte in reti elicoidali elastiche. 10
11 L UNITÀ STRUTTURALE DEL COLLAGENO É IL TROPOCOLLAGENO Esso é formato da tre catene polipeptidiche a elica sinistrorsa, avvolte l una attorno all altra a formare una superelica destrorsa, così lo svolgimento delle prime é impedito dalla seconda. Ogni catena contiene circa 1000 residui. Le principali caratteristiche passo dell elica : 0,31 nm lunghezza: 300 nm diametro: 1,5 nm massa: 285 kda 11
12 I TIPI DI COLLAGENO TIPO COMPOSIZIONE DISTRIBUZIONE I [α 1 (I)] 2 α 2 (I) Pelle, tendini, ossa, cornea II [α 1 (II)] 3 Cartilagine, dischi intervertebrali, corpo vitreo III [α 1 (III)] 3 Pelle fetale, sistema cardiovascolare, fibre reticolari IV [α 1 (IV)] 2 α 2 (IV) Membrana basale V [α 1 (V)] 2 α 2 (V) Placenta, pelle 12
13 IL COLLAGENO b) Modello spaziale dell elica sinistrorsa (3,3 residui per giro), c) tre catene di collageno si arrotolano insieme con un andamento destrorso, d) rappresentazione a palle-ebastoncini della superelica a tre catene di collageno vista dall alto. 13
14 IL TROPOCOLLAGENO In esso non sono presenti legami idrogeno intra-catena; sono invece presenti legami idrogeno inter-catena. 14
15 La struttura primaria del collageno è insolita: (Gly-X-Y) n X è molto spesso Pro, Y è molto spesso Hyp, 1/3 degli aminoacidi è costituito da Gly, 1/4 degli aminoacidi è costituito da Pro, vi è una elevata presenza di 5-idrossilisina e di 4-idrossiprolina (25%). 15
16 LA PROLINA Avendo una flessibilità conformazionale molto limitata, essa conferisce rigidità alle catene, quindi alle fibre; i loro anelli si respingono a vicenda, costringendo la catena ad assumere una struttura ad elica sottile e distesa. Pro 16
17 IL COLLAGENO Nel collageno, è diffusa la idrossilazione della prolina in idrossiprolina ad opera della prolinidrossilasi, la prolina è idrossilata solo se è situata sul lato amminico di un residuo di glicina, la 4-idrossiprolina forma legami H tra le catene di tropocollageno; le idrossilazioni coinvolgono la vitamina C (ac. Ascorbico) che mantiene il Fe dell enzima a Fe +2, la sua mancanza provoca lo scorbuto, che causa lesioni cutanee, fragilità dei vasi, emorragie gengivali, ecc. 17
18 IL COLLAGENO I legami H stabilizzano il collageno e sono perpendicolari all asse longitudinale del bastoncino di tropocollageno. 18
19 IL COLLAGENO E E UNA GLICOPROTEINA Una piccola percentuale di lisina é idrossilata a livello del C-5 ad opera dell enzima lisinidrossilasi, la 5-idrossilisina rappresenta il sito d attacco per i polisaccaridi. 19
20 IL COLLAGENO E UNA GLICOPROTEINA Il numero di unità saccaridiche legate per molecola di tropocollageno varia in funzione del tipo di tessuto. Gli enzimi, che intervengono prima che le catene assumano una struttura elicoidale, sono: 1) la galattosiltransferasi, 2) la glucosiltransferasi. 20
21 LA SEZIONE TRASVERSALE DEL TROPOCOLLAGENO L interno del cavo elicoidale della tripla elica é molto compatto, il solo residuo amminoacidico che può adattarsi ad una posizione interna dell elica é la glicina, poiché vi sono 3 residui per giro, un residuo ogni 3 di ciascuna catena deve essere glicina. 21
22 La T m (TEMPERATURA DI FUSIONE) La forma ad elica é la conseguenza di molti legami che si rinforzano l un l altro, la tripla elica é stabilizzata da interazioni cooperative; se una soluzione di tropocollageno viene scaldata, raggiunta una certa temperatura, la struttura elicoidale viene distrutta ( gelatina) e la viscosità diminuisce. 22
23 La T m (TEMPERATURA DI FUSIONE) I movimenti termici, ad una certa temperatura, superano le forze che stabilizzano l elica a tripla catena, questa transizione strutturale avviene bruscamente; la T m (temperatura di fusione) é la temperatura a cui metà della struttura elicoidale viene persa. 23
24 La T m (TEMPERATURA DI FUSIONE) La T m del collageno é correlata alla temperatura corporea della specie da cui deriva il collageno; la tripla elica é fortemente stabilizzata dalla idrossilazione dei residui di prolina che formano legami idrogeno, il contenuto in imminoacidi (prolina e idrossiprolina) aumenta nell evoluzione. 24
25 LA MATURAZIONE DEL COLLAGENO Il procollageno é il precursore del tropocollageno. Le catene che costituiscono il tropocollageno vengono sintetizzate in forma di precursori più grandi. I propeptidi vengono rimossi, al di fuori della cellula, da parte delle procollageno peptidasi (sia per i propeptidi amino-, sia per i propeptidi carbossi-terminali). 25
26 LA PROCOLLAGENO PEPTIDASI La rimozione difettosa dei propeptidi determina la Sindrome di Ehlers Danlos : pelle tesa, giunture ipermobili, bassa statura associata a fragilità cutanea, lassità articolare. 26
27 LA MATURAZIONE DEL COLLAGENO 27
28 IL COLLAGENO AL M.E. Si alternano bande scure a bande chiare ad intervalli regolari; lo spessore della banda scura è di 35 nm, lo spessoredi bandascurae bandachiaraèdi 67 nm. 28
29 LA STRUTTURA DELLA FIBRA DI COLLAGENO Le molecole di tropocollageno hanno una disposizione sfalsata, ogni molecola é spostata di ¼ della propria lunghezza rispetto a quelle vicine, si ha la completa sovrapposizione solo ad intervalli di 5 molecole, la distanza tra l estremità C-terminale di una molecola e l estremità N-terminale di quella adiacente é di 40 nm; nell osso, questo spazio é occupato da un fosfato di calcio: l idrossiapatite. 29
30 LA STRUTTURA DELLA FIBRA DI COLLAGENO 30
31 IL COLLAGENO I legami trasversali covalenti aumentano la resistenza meccanica del collageno. Sono presenti i legami intramolecolari tra le catene di ogni singola tripla elica, i legami intermolecolari tra eliche di tropocollageno di una microfibrilla. 31
32 I LEGAMI CROCIATI INTRAMOLECOLARI Essi si formano in regioni vicine al terminale amminico. 32
33 I LEGAMI CROCIATI INTERMOLECOLARI La regione amminoterminale di una molecola si lega alla regione carbossiterminale di un altra molecola di una fila adiacente; il numero dei legami trasversali varia con la funzione fisiologica e l età del tessuto. 33
34 LE COLLAGENASI Sono enzimi che degradano i legami peptidici nelle regioni a tripla elica del collageno, es. le collagenasi del Clostridium Histolyticum (batterio patogeno). Le collagenasi tessutali Esse sono responsabili della metamorfosi negli anfibi e della riorganizzazione dell utero dopo la gravidanza, nei mammiferi. Le collagenasi dei fibroblasti umani (52KD) sono metalloproteasi contenenti Ca +2 e Zn
35 L ELASTINA 35
36 L ELASTINA È presente in molti tessuti che devono essere elastici: parete dei vasi, cute, legamenti, ecc, ha un elevato contenuto in prolina, valina, glicina (1/3) ed alanina, è povera di idrossiprolina e priva di idrossilisina, le fibre di elastina si formano quando le catene laterali dei polipeptidi adiacenti formano legami trasversali covalenti, che sono: 1) lisinorleucina (1 residuo di lisina + 1 residuo di allisina), 2) desmosina (3 residui di allisina + 1 residuo di lisina); la allisina si forma dalla lisina ad opera dell enzima lisinossidasi. 36
37 LA CONFORMAZIONE E L AVVOLGIMENTO L CASUALE DELL ELASTINA ELASTINA 37
38 LA LISINORLEUCINA É UN LEGAME L TRASVERSALE STABILE 38
39 LA DESMOSINA (3 RESIDUI DI ALLISINA, 1 RESIDUO DI LISINA) 39
40 I LEGAMI CROCIATI Essi riportano l elastina alle sue dimensioni e forma originali dopo l allungamento, danno stabilità, infatti la resistenza delle fibre di elastina alla trazione aumenta con l aumentare del numero di tali legami, sono responsabili anche della sua insolubilitá. 40
41 LA RESISTENZA DELLE FIBRE ALLA TRAZIONE AUMENTA CON IL NUMERO DEI LEGAMI TRASVERSALI 41
LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA.
 UNITÀ BIOTEC. DIDATTICA DI BIOCHIMICA GENERALE LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA. Roberto Giacominelli Stuffler IL COLLAGENO 2 IL COLLAGENO E una famiglia di proteine fibrose con ruolo
UNITÀ BIOTEC. DIDATTICA DI BIOCHIMICA GENERALE LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA. Roberto Giacominelli Stuffler IL COLLAGENO 2 IL COLLAGENO E una famiglia di proteine fibrose con ruolo
Polimorfismo genetico del collageno
 COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
RUOLI BIOLOGICI DELLE PROTEINE. Biochimica
 RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
IL COLLAGENO. E la specie proteica più abbondante nella maggior parte dei vertebrati, in tutti gli organi è presente la molecola di collageno.
 IL COLLAGENO E la specie proteica più abbondante nella maggior parte dei vertebrati, in tutti gli organi è presente la molecola di collageno. Fibre di collageno formano la matrice dell osso su cui precipitano
IL COLLAGENO E la specie proteica più abbondante nella maggior parte dei vertebrati, in tutti gli organi è presente la molecola di collageno. Fibre di collageno formano la matrice dell osso su cui precipitano
Sinistrorsa. destrorso
 Sinistrorsa destrorso Collageno Glicoproteina insolubile del tessuto connettivo, tendini, denti, cartilagine, matrice organica, osso, cornea L unità strutturale del collageno è il TROPOCOLLAGENO costituito
Sinistrorsa destrorso Collageno Glicoproteina insolubile del tessuto connettivo, tendini, denti, cartilagine, matrice organica, osso, cornea L unità strutturale del collageno è il TROPOCOLLAGENO costituito
α-cheratine (α-elica) collageni e cheratine β-cheratine (conformazione β) M.N. Gadaleta
 Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
ECM matrice extra-cellulare
 ECM matrice extra-cellulare I tessuti biologici possono essere considerati come materiali compositi costituiti da un numero variabile di cellule legate ad una sostanza complessa denominata matrice extracellulare
ECM matrice extra-cellulare I tessuti biologici possono essere considerati come materiali compositi costituiti da un numero variabile di cellule legate ad una sostanza complessa denominata matrice extracellulare
Collagene, Emoglobina e
 Collagene, Emoglobina e Mioglobina WWW.SUNHOPE.IT Vit. C WWW.SUNHOPE.IT a a a (vitc) WWW.SUNHOPE.IT Idrossilazione di prolina Per garantire la privacy, è stato impedito il download
Collagene, Emoglobina e Mioglobina WWW.SUNHOPE.IT Vit. C WWW.SUNHOPE.IT a a a (vitc) WWW.SUNHOPE.IT Idrossilazione di prolina Per garantire la privacy, è stato impedito il download
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare
 generalità La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare La sostanza intercellulare a sua volta è costituita da fibre e sostanza
generalità La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare La sostanza intercellulare a sua volta è costituita da fibre e sostanza
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
OLIGOMERICHE Sono costituite cioè da più catene polipeptidiche PROTOMERI O SUBUNITÀ
 Scaricato da Le proteine con peso molecolare superiore a 50.000 sono OLIGOMERICHE Sono costituite cioè da più catene polipeptidiche PROTOMERI O SUBUNITÀ SunHope.it 1 Scaricato da Le proteine oligomeriche
Scaricato da Le proteine con peso molecolare superiore a 50.000 sono OLIGOMERICHE Sono costituite cioè da più catene polipeptidiche PROTOMERI O SUBUNITÀ SunHope.it 1 Scaricato da Le proteine oligomeriche
 TESSUTO CONNETTIVO PROPRIAMENTE DETTO CELLULE + SOSTANZA INTERCELLULARE CELLULE Fibroblasti: secernono tutti i componenti dellasostanzaintercellulare. Fusati o stellati Cellule provenienti dal sangue:
TESSUTO CONNETTIVO PROPRIAMENTE DETTO CELLULE + SOSTANZA INTERCELLULARE CELLULE Fibroblasti: secernono tutti i componenti dellasostanzaintercellulare. Fusati o stellati Cellule provenienti dal sangue:
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
STRUTTURA TERZIARIA. H 3 N + COO - β-foglietto
 STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
Scaricato da
 1 2 3 4 www.sunhope.it 1 Sinistrorsa destrorso 5 6 7 8 www.sunhope.it 2 9 10 11 12 www.sunhope.it 3 13 14 15 16 www.sunhope.it 4 17 18 19 20 www.sunhope.it 5 Idrossilazione della lisina 21 22 23 24 www.sunhope.it
1 2 3 4 www.sunhope.it 1 Sinistrorsa destrorso 5 6 7 8 www.sunhope.it 2 9 10 11 12 www.sunhope.it 3 13 14 15 16 www.sunhope.it 4 17 18 19 20 www.sunhope.it 5 Idrossilazione della lisina 21 22 23 24 www.sunhope.it
Modificazioni delle proteine
 Modificazioni delle proteine POST-TRADUZIONALI = avvengono dopo la sintesi proteica CO-TRADUZIONALI = avvengono durante la sintesi proteica Sono modificazioni chimiche della catena polipeptidica ad opera,
Modificazioni delle proteine POST-TRADUZIONALI = avvengono dopo la sintesi proteica CO-TRADUZIONALI = avvengono durante la sintesi proteica Sono modificazioni chimiche della catena polipeptidica ad opera,
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
L organizzazione sfalsata dà origine alla tipica striatura di una fibrilla vista al ME in colorazione negativa.
 Le unità di tropocollageno si dispongono testa-coda su file parallele, sfalsandosi di circa 1/4 della loro lunghezza (60-70 nm). In ciascuna fila le unità sono separate da spazi di 35-40 nm, che nell osso
Le unità di tropocollageno si dispongono testa-coda su file parallele, sfalsandosi di circa 1/4 della loro lunghezza (60-70 nm). In ciascuna fila le unità sono separate da spazi di 35-40 nm, che nell osso
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
TESSUTI CONNETTIVI. Gruppo di tessuti con caratteristiche comuni: Origine embrionale (mesoderma mesenchima)
 TESSUTI CONNETTIVI Gruppo di tessuti con caratteristiche comuni: Origine embrionale (mesoderma mesenchima) Organizzazione strutturale Funzioni: connessione di altri tessuti, fz. meccanica (sostegno), fz.
TESSUTI CONNETTIVI Gruppo di tessuti con caratteristiche comuni: Origine embrionale (mesoderma mesenchima) Organizzazione strutturale Funzioni: connessione di altri tessuti, fz. meccanica (sostegno), fz.
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare
 generalità La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare La sostanza intercellulare a sua volta è costituita da fibre e sostanza
generalità La caratteristica fondamentale del tessuto connettivo è quella di essere costituito da cellule e sostanza intercellulare La sostanza intercellulare a sua volta è costituita da fibre e sostanza
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 9
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
L'importanza dei legami crociati dovuti alla lisil ossidasi. - è somministrato l'inibitore β-aminopropionitrile.
 L'importanza dei legami crociati dovuti alla lisil ossidasi è dimostrata da studi su animali a cui: - non è fornito con la dieta il Cu 2+ o - è somministrato l'inibitore β-aminopropionitrile. Le conseguenze
L'importanza dei legami crociati dovuti alla lisil ossidasi è dimostrata da studi su animali a cui: - non è fornito con la dieta il Cu 2+ o - è somministrato l'inibitore β-aminopropionitrile. Le conseguenze
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Sinistrorsa. destrorso
 Sinistrorsa destrorso P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Collageno Glicoproteina insolubile del tessuto connettivo, tendini, denti,
Sinistrorsa destrorso P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006 Collageno Glicoproteina insolubile del tessuto connettivo, tendini, denti,
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
AMMINOACIDI. Gli amminoacidi si distinguono in base alla diversità della catena laterale R in ciascuno di essi.
 AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
 COMPOSIZIONE: - Semplici - Coniugate: Apolipoproteine Glicoproteine Nucleoproteine Metalloproteine Cromoproteine STRUTTURA: - Fibrose forma molecolare allungata struttura II - Globulari: forma molecolare
COMPOSIZIONE: - Semplici - Coniugate: Apolipoproteine Glicoproteine Nucleoproteine Metalloproteine Cromoproteine STRUTTURA: - Fibrose forma molecolare allungata struttura II - Globulari: forma molecolare
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
I TESSUTI CONNETTIVI. Tessuti connettivi propriamente detti; Tessuto adiposo; Sangue; Tessuto cartilagineo; Tessuto osseo. A cura di Tiziano Baroni
 I TESSUTI CONNETTIVI 1) 2) 3) 4) 5) Tessuti connettivi propriamente detti; Tessuto adiposo; Sangue; Tessuto cartilagineo; Tessuto osseo A cura di Tiziano Baroni TESSUTI CONNETTIVI Gruppo di tessuti con
I TESSUTI CONNETTIVI 1) 2) 3) 4) 5) Tessuti connettivi propriamente detti; Tessuto adiposo; Sangue; Tessuto cartilagineo; Tessuto osseo A cura di Tiziano Baroni TESSUTI CONNETTIVI Gruppo di tessuti con
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Il Collageno tessuto connettivo
 Il Collageno Costituente del tessuto connettivo, insieme a elastina, fibrillina e proteoglicani, tutti prodotti da fibroblasti, condroblasti, osteoblasti La proteina + abbondante nei mammiferi (25% del
Il Collageno Costituente del tessuto connettivo, insieme a elastina, fibrillina e proteoglicani, tutti prodotti da fibroblasti, condroblasti, osteoblasti La proteina + abbondante nei mammiferi (25% del
TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE
 TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE COMPONENTE AMORFA: GAG, PROTEOGLICANI GLICOPROTEINE LEGANTI IL CALCIO SALI DI
TESSUTO OSSEO ELEMENTI CELLULARI: CELLULE OSTEOPROGENITRICI OSTEOBLASTI OSTEOCITI OSTEOCLASTI COMPONENTE FIBROSA: COLLAGENE COMPONENTE AMORFA: GAG, PROTEOGLICANI GLICOPROTEINE LEGANTI IL CALCIO SALI DI
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Corso di Biomeccanica
 Corso di Laurea in Ingegneria Biomedica Corso di Biomeccanica Parte 7: legami costitutivi F. Auricchio auricchio@unipv.it http://www.unipv.it/dms/auricchio Università degli Studi di Pavia Dipartimento
Corso di Laurea in Ingegneria Biomedica Corso di Biomeccanica Parte 7: legami costitutivi F. Auricchio auricchio@unipv.it http://www.unipv.it/dms/auricchio Università degli Studi di Pavia Dipartimento
I TESSUTI CONNETTIVI
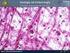 I TESSUTI CONNETTIVI 1) Tessuti connettivi propriamente detti; 2) Tessuto adiposo; 3) Sangue; 4) Tessuto cartilagineo; 5) Tessuto osseo A cura di Tiziano Baroni TESSUTO CONNETTIVO Gruppo di tessuti con
I TESSUTI CONNETTIVI 1) Tessuti connettivi propriamente detti; 2) Tessuto adiposo; 3) Sangue; 4) Tessuto cartilagineo; 5) Tessuto osseo A cura di Tiziano Baroni TESSUTO CONNETTIVO Gruppo di tessuti con
STRUTTURA TERZIARIA. H 3 N + COO - β-foglietto. La catena polipeptidica delle proteine globulari oltre ad organizzarsi in
 STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine globulari oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore RIPIEGAMENTO sino
STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine globulari oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore RIPIEGAMENTO sino
Riepilogo di Emoglobina, collagene, elastina e antitripsina
 Riepilogo di Emoglobina, collagene, elastina e antitripsina Vi sono altri fattori che possono influire sulla capacità dell emoglobina di legarsi all ossigeno, uno di questi è la concentrazione di
Riepilogo di Emoglobina, collagene, elastina e antitripsina Vi sono altri fattori che possono influire sulla capacità dell emoglobina di legarsi all ossigeno, uno di questi è la concentrazione di
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
I TESSUTI CONNETTIVI connettono altri tessuti tra di loro nella formazione degli organi, danno sostegno alle parti molli, intervengono negli scambi
 I TESSUTI CONNETTIVI connettono altri tessuti tra di loro nella formazione degli organi, danno sostegno alle parti molli, intervengono negli scambi nutritizi e presentano elementi specializzati nella difesa
I TESSUTI CONNETTIVI connettono altri tessuti tra di loro nella formazione degli organi, danno sostegno alle parti molli, intervengono negli scambi nutritizi e presentano elementi specializzati nella difesa
Principi di Citologia e Istologia. Prof. Pucci, La Matrice Extracellulare
 Principi di Citologia e Istologia. Prof. Pucci, 2003 La Matrice Extracellulare La matrice extracellulare è composta da quattro classi di macromolecole Collageni Proteoglicani Elastina Glicoproteine Essa
Principi di Citologia e Istologia. Prof. Pucci, 2003 La Matrice Extracellulare La matrice extracellulare è composta da quattro classi di macromolecole Collageni Proteoglicani Elastina Glicoproteine Essa
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
Corso di recupero Fisiologia cellulare/ Laboratorio di colture cellulari
 Corso di laurea magistrale in BIOTECNOLOGIE DELLA RIPRODUZIONE UNIVERSITA DEGLI STUDI DI TERAMO Corso di recupero Fisiologia cellulare/ Laboratorio di colture cellulari Prof.ssa Luisa Gioia Matrice ExtraCellulare
Corso di laurea magistrale in BIOTECNOLOGIE DELLA RIPRODUZIONE UNIVERSITA DEGLI STUDI DI TERAMO Corso di recupero Fisiologia cellulare/ Laboratorio di colture cellulari Prof.ssa Luisa Gioia Matrice ExtraCellulare
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE C.M. BIOCHIMICA (6 CFU) DOCENTE: ROBERTO GIACOMINELLI STUFFLER
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE C.M. BIOCHIMICA (6 CFU) DOCENTE: ROBERTO GIACOMINELLI STUFFLER IL CORSO MONODISCIPLINARE È SUDDIVISO IN DUE UNITÀ DIDATTICHE: 1) BIOCHIMICA
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE C.M. BIOCHIMICA (6 CFU) DOCENTE: ROBERTO GIACOMINELLI STUFFLER IL CORSO MONODISCIPLINARE È SUDDIVISO IN DUE UNITÀ DIDATTICHE: 1) BIOCHIMICA
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA
 PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
a differenza degli epiteli
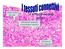 cellule molto più rade a differenza degli epiteli abbondante materiale extracellulare (matrice) presenza di vasi sanguigni I tessuti connettivi Gruppo di tessuti con caratteristiche comuni: Organizzazione
cellule molto più rade a differenza degli epiteli abbondante materiale extracellulare (matrice) presenza di vasi sanguigni I tessuti connettivi Gruppo di tessuti con caratteristiche comuni: Organizzazione
Le proteine o protidi
 Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Le strutture extracellulari consistono principalmente di macromolecole secrete dalla cellula stessa. La natura chimica di queste molecole differisce
 Le strutture extracellulari consistono principalmente di macromolecole secrete dalla cellula stessa. La natura chimica di queste molecole differisce tra i vari organismi, ma le strutture extracellulari
Le strutture extracellulari consistono principalmente di macromolecole secrete dalla cellula stessa. La natura chimica di queste molecole differisce tra i vari organismi, ma le strutture extracellulari
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
TESSUTI ANIMALI, MATRICE EXTRACELLULARE E GIUNZIONI CELLULARI MATRICE EXTRACELLULARE MATRICE EXTRACELLULARE COLLAGENI ED ELASTINA
 TESSUTI ANIMALI, MATRICE EXTRACELLULARE E GIUNZIONI CELLULARI CELLULE E TESSUTI Negli organismi pluricellulari, le cellule sono organizzate in tessuti. Nei vertebrati abbiamo 4 principali tessuti: epiteliale,
TESSUTI ANIMALI, MATRICE EXTRACELLULARE E GIUNZIONI CELLULARI CELLULE E TESSUTI Negli organismi pluricellulari, le cellule sono organizzate in tessuti. Nei vertebrati abbiamo 4 principali tessuti: epiteliale,
Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei.
 DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Macromolecole Biologiche. La struttura secondaria (I)
 La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
Daniela Carotti. Dipartimento di Scienze Biochimiche III piano - stanza 310.
 Daniela Carotti Dipartimento di Scienze Biochimiche III piano - stanza 310 06 49910969 daniela.carotti@uniroma1.it organismo cellula componenti biochimiche acqua ioni carboidrati riserva di energia ruolo
Daniela Carotti Dipartimento di Scienze Biochimiche III piano - stanza 310 06 49910969 daniela.carotti@uniroma1.it organismo cellula componenti biochimiche acqua ioni carboidrati riserva di energia ruolo
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
I Tessuti Trofomeccanici. By A. Pirola
 I Tessuti Trofomeccanici By A. Pirola Classificazione dei tessuti trofomeccanici Sono formati prevalentemente da sostanza fondamentale Svolgono funzioni di tipo Meccanico e Trofico T. Connettivo T. Cartilagineo
I Tessuti Trofomeccanici By A. Pirola Classificazione dei tessuti trofomeccanici Sono formati prevalentemente da sostanza fondamentale Svolgono funzioni di tipo Meccanico e Trofico T. Connettivo T. Cartilagineo
FUNZIONI DELLE PROTEINE
 FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Macromolecole Biologiche. La struttura secondaria (III)
 La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
Protidi. Protidi 16/01/2019
 Protidi I protidi sono macromolecole costituite dall unione di amminoacidi tra loro. I protidi, a seconda del numero di amminoacidi che li costituiscono, sono distinti in: oligopeptidi, formati da pochi
Protidi I protidi sono macromolecole costituite dall unione di amminoacidi tra loro. I protidi, a seconda del numero di amminoacidi che li costituiscono, sono distinti in: oligopeptidi, formati da pochi
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU) Roberto Giacominelli Stuffler IL CORSO MONODISCIPLINARE DI BIOCHIMICA È SUDDIVISO IN DUE UNITÀ
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU) Roberto Giacominelli Stuffler IL CORSO MONODISCIPLINARE DI BIOCHIMICA È SUDDIVISO IN DUE UNITÀ
Macromolecole Biologiche. La struttura secondaria (II)
 La struttura secondaria (II) Nello stesso anno (1951) in cui proposero l α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo l α elica,
La struttura secondaria (II) Nello stesso anno (1951) in cui proposero l α elica, Pauling e Corey postularono anche l esistenza di un altra struttura secondaria: il foglietto β (β-sheet). Dopo l α elica,
Fisiologia cellulare e Laboratorio di Colture cellulari
 Corso di laurea BIOTECNOLOGIE UNIVERSITA DEGLI STUDI DI TERAMO Fisiologia cellulare e Laboratorio di Colture cellulari Prof.ssa Luisa Gioia Corso di laurea BIOTECNOLOGIE Fisiologia cellulare e Laboratorio
Corso di laurea BIOTECNOLOGIE UNIVERSITA DEGLI STUDI DI TERAMO Fisiologia cellulare e Laboratorio di Colture cellulari Prof.ssa Luisa Gioia Corso di laurea BIOTECNOLOGIE Fisiologia cellulare e Laboratorio
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
TESSUTO MUSCOLARE TESSUTO NERVOSO TESSUTO CONNETTIVO TESSUTO EPITELIALE
 TESSUTO MUSCOLARE TESSUTO NERVOSO TESSUTO CONNETTIVO TESSUTO EPITELIALE TESSUTO EPITELIALE poca matrice extracellulare (lamina basale) TESSUTO CONNETTIVO abbondante matrice extracellulare ADESIONE: fenomeno
TESSUTO MUSCOLARE TESSUTO NERVOSO TESSUTO CONNETTIVO TESSUTO EPITELIALE TESSUTO EPITELIALE poca matrice extracellulare (lamina basale) TESSUTO CONNETTIVO abbondante matrice extracellulare ADESIONE: fenomeno
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Il legame peptidico è un ibrido di risonanza: scaricato da
 Il legame peptidico è un ibrido di risonanza: - O ha una parziale carica negativa - - la coppia di e - del legame C=O è parzialmente spostata verso O - N ha una parziale carica positiva + - la coppia di
Il legame peptidico è un ibrido di risonanza: - O ha una parziale carica negativa - - la coppia di e - del legame C=O è parzialmente spostata verso O - N ha una parziale carica positiva + - la coppia di
 http://digilander.libero.it/glampis64 Il corpo umano è organizzato in livelli gerarchici Un organismo è costituito da un insieme di sistemi, formati a loro volta da organi, tessuti e cellule. I tessuti
http://digilander.libero.it/glampis64 Il corpo umano è organizzato in livelli gerarchici Un organismo è costituito da un insieme di sistemi, formati a loro volta da organi, tessuti e cellule. I tessuti
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
Alterazioni di proteine struturali
 Alterazioni di proteine struturali Patologia del Collageno Collageno: 25% (come massa) di tutte le proteine del corpo. Alta resistenza alla trazione. Resistenza alle proteasi comuni (proteasi a serina
Alterazioni di proteine struturali Patologia del Collageno Collageno: 25% (come massa) di tutte le proteine del corpo. Alta resistenza alla trazione. Resistenza alle proteasi comuni (proteasi a serina
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
LE FIBRE ELASTICHE ISTOLOGIA ISTOLOGIA. Azan Mallory. Fibre collagene (fasci) Colorazione di Weigert- Van Gieson
 LE FIBRE ELASTICHE Azan Mallory Fibre collagene (fasci) Colorazione di Weigert- Van Gieson ARTERIA ELASTICA: AORTA ARTERIA DI TIPO MUSCOLARE TONACA AVVENTIZIA TONACA MEDIA Le fibre elastiche Microfibrille
LE FIBRE ELASTICHE Azan Mallory Fibre collagene (fasci) Colorazione di Weigert- Van Gieson ARTERIA ELASTICA: AORTA ARTERIA DI TIPO MUSCOLARE TONACA AVVENTIZIA TONACA MEDIA Le fibre elastiche Microfibrille
STRUTTURA E FUNZIONI
 STRUTTURA E FUNZIONI Typical Cell Membrana plasmatica Chiamata anche membrana cellulare Circonda ogni cellula Separa il contenuto cellulare dal cio che la circonda Separa il LIC dal LEC Controlla il movimento
STRUTTURA E FUNZIONI Typical Cell Membrana plasmatica Chiamata anche membrana cellulare Circonda ogni cellula Separa il contenuto cellulare dal cio che la circonda Separa il LIC dal LEC Controlla il movimento
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
Struttura degli Amminoacidi
 Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
La struttura della cromatina
 La struttura della cromatina Istoni e nucleosomi La cromatina Il DNA all interno del nucleo eucariotico è associato a delle proteine. Il complesso DNA-proteina si chiama cromatina. Se nuclei interfasici
La struttura della cromatina Istoni e nucleosomi La cromatina Il DNA all interno del nucleo eucariotico è associato a delle proteine. Il complesso DNA-proteina si chiama cromatina. Se nuclei interfasici
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Connettivi Specializzati. Cartilagine Osso Sangue
 Connettivi Specializzati Cartilagine Osso Sangue Cartilagine Funzione di sostegno Tessuto molto elastico Resistente alle sollecitazioni meccaniche Correlato al tessuto osseo Composizione della Cartilagine
Connettivi Specializzati Cartilagine Osso Sangue Cartilagine Funzione di sostegno Tessuto molto elastico Resistente alle sollecitazioni meccaniche Correlato al tessuto osseo Composizione della Cartilagine
I carboidrati. (CH 2 O)n n>3. Mono-, oligo-, polisaccaridi. n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi
 I carboidrati (CH 2 O)n n>3 Mono-, oligo-, polisaccaridi n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi I monosaccaridi sono derivati aldeidici e chetonici di alcoli poliossidrilici a catena lineare,
I carboidrati (CH 2 O)n n>3 Mono-, oligo-, polisaccaridi n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi I monosaccaridi sono derivati aldeidici e chetonici di alcoli poliossidrilici a catena lineare,
CLASSIFICAZIONE DEI PEPTIDI
 terminale). PEPTIDI Gli amminoacidi si legano tra di loro attraverso una reazione che coinvolge COOH di un amminoacido e NH 2 di un altro amminoacido, con la liberazione di una molecola di acqua per ogni
terminale). PEPTIDI Gli amminoacidi si legano tra di loro attraverso una reazione che coinvolge COOH di un amminoacido e NH 2 di un altro amminoacido, con la liberazione di una molecola di acqua per ogni
