Polarizzazione della luce
|
|
|
- Concetta Oliva
- 7 anni fa
- Visualizzazioni
Transcript
1 Polarizzazione della luce Fu discepolo di Furier. Studiò all Ecole Politecniche. Entrò nel corpo del genio militare. Partecipò alla campagna di Egitto e Siria con Napoleone nel Le sue indagini di ottica riguardarono la rifrazione dei materiali. Nel 1808, osservando la luce riflessa dalle finestre del palazzo del Lussemburgo che faceva passare attraverso un cristallo di calcite, scopre il fenomeno della polarizzazione della luce, a cui dette appunto il nome. Diviene membro dell Accademia di Francia. Muore nel 1812 a 37 anni, forse di tubercolosi contratta nelle campagne militari.
2 Jean Baptiste Biot Parigi Fisico e matematico francese. Fu nominato professore di fisica al Collège di France e eletto all accademia delle scienze all età di 29 ani. Nel 804 compì con Louis Gay-Lussac la prima ascensione scientifica in pallone aerostatico fino a 5000 metri
3 La prima ascensione scientifica in pallone aerostatico 1804 Gay-Lussac e Biot J.-L. Gay-Lussac ( )
4 Questa immagine d epoca rappresenta l evento della partenza di una mongolfiera, seguita dalla curiosità di un numeroso pubblico. Museo della scienza di Monaco di Baviera
5 La scoperta di Biot 1815 Lamine di quarzo tagliate da cristalli differenti ruotavano il piano di polarizzazione della luce alcune a destra, mentre altre a sinistra ma la la sua più grande scoperta in questo campo è che certe sostanze organiche ruotano il piano di polarizzazione, come l olio di trementina, soluzioni di zucchero, canfora e acido tartarico, perfino allo stato gassoso.. Biot giunge alla conclusione che l azione dei corpi organici era una caratteristica delle molecole ed era dovuta alla costituzione individuale di queste più piccole particelle. Mentre con il quarzo il fenomeno era dovuto al particolare modo di organizzazione delle particelle cristalline. Da : L asimmetria di composti organici naturali di Luis Pasteur Paris 1860
6 Cristallo di silice
7 Cristalli di silice speculari
8 Cristalli di silice speculari
9 Critalli di silice speculari
10 Pasteur, nel suo libro, cita una comunicazione di Mitscherlich, letta da Biot alla Accademia delle Scienze, che lui conobbe quando era studente a l Ecòle Normale: Nel 1819 il chimico tedesco conia la formula << stesso cristallo, st essa chimica >> introducendo la teoria dell isomorfismo, per cui l aspetto dei cristalli chimici si riflette nelle loro molecole costitutive Eilhard Mitscherlich << l acido racemico e l acido tartarico hanno la stessa composizione chimica, la stessa forma cristallina con angoli e facce uguali, lo stesso peso specifico, lo stesso comportamento alla rifrazione della luce. Le loro soluzioni acquose hanno lo stesso indice di rifrazione. Ma l acido tartarico disciolto ruota il piano di polarizzazione della luce e l acido racemico è indifferente, ma la natura e il numero di atomi, la loro disposizione e la loro distanza uno dall altro sono gli stessi in tutti e due i corpi >>
11 Le origini del suo lavoro sorgono da dubbi <<. Ero a quel tempo uno studente all Ecòle Normale. Questa comunicazione sconvolse le mie idee. Quale rassomiglianza sotto ogni punto di vista! Ci possono essere due corpi le cui proprietà sono state più attentamente e completamente confrontate? La scienza può comprendere in questo momento perchè due corpi sono completamente simili senza essere identici? In questo caso che ne è della chiara definizione di specie chimica, così fondamentale in questo momento, che fu enunciata da Chevreul nell anno 1823? corpi composti sono tra loro identici quando la natura, le proporzioni e la disposizione degli atomi sono gli stessi In breve questa comunicazione di Mitscherlich divenne nella mia mente la principale difficoltà nella comprensione dei corpi. >>
12 La Rivoluzione francese e le nuove istituzioni educative e scientifiche École normale supérieure 1794
13 Cosa si deposita dentro le botti
14 Questa superficie rugosa è la parte che aderisce alla parete interna della botte
15 La parte che è esposta verso il lume della botte è ricoperta di cristalli di tartrato cresciuti insieme ai cristalli di calcite. L aspetto rosso è dovuto alla enocianina.
16
17
18
19
20 I cristalli sono solo di un tipo? I cristalli che si possono separare sono due : acido tartarico acido paratartarico o racemo Si distinguono solo perché la soluzione dei cristalli di acido tartarico devia il piano di polarizzazione della luce, mentre la soluzione dei cristalli di acido paratartarico non modifica il piano di polarizzazione
21 Inizia il lavoro di Pasteur <<. Lasciai cristallizzare l acido tartarico e i suoi sali e poi determinai la loro forma cristallina. Ma durante il lavoro osservai un fatto che era importante e che era sfuggito a fisici preparati >> Pasteur nota che la forma dei cristalli di acido tartarico si presenta asimmetrica. Tutti presentavano la stessa asimmetria, come nel quarzo l attività ottica era legata alla forma asimmetrica dei cristalli. E i cristalli di acido paratartarico o racemo? Se i cristalli di acido paratartarico o racemo non presentavano attività ottica allora la forma dei loro cristalli doveva essere simmetrica. Pasteur cristallizza l acido paratartarico dalle sue soluzioni e scopre che si presenta in due forme cristalline che egli riesce a separare con delle pinzette e lente di ingrandimento.entrambe hanno forme asimmetriche, ma l una è speculare all altra. Una delle due è l acido tartarico che già conosceva, l altro il cristallo di acido tartarico speculare.l uno devia il piano della luca a sinistra, l altro a destra. Nell acido paratartarico trovandosi insieme annullano a vicenda la loro azione sulla luce. Acido tartarico destro e sinistro ottenuti separando l acido racemo. Sono l uno immagine speculare dell altro, non sovrapponibili
22 I cristalli contenuti nelle vetrinette provengono dalla collezione di Pasteur, sono conservati nel suo laboratorio all istituto Pasteur di Parigi Nei flaconi sono conservati cristalli di acido paratartarico o racemo provenienti dall industria di Kestner, a Thann. L industriale Kestner fu il primo nel 1820 a constatare l esistenza di questo acido che tanta importanza ha avuto nella scoperta della origine della attività ottica di Pasteur
23 Pasteur lavorò per molti mesi alla formazione di cristalli di varie sostanze. Qui sono raccolti dei cristalli di quarzo levogiro da lui prodotti.
24
25 In questi flaconi sono conservati cristalli di tartrato di ammonio levogiro che Pasteur ha separato dalla miscela racemica con il metodo da lui inventato, che si basava sulla fermentazione selettiva di uno dei due tartrati. Tutte le etichette sono scritte di sua mano
26 Pasteur è un profondo conoscitore della cristallografia. Qui sono conservati modello di cristalli da lui stesso costruiti.
27 Le conclusioni <<. Rammentate la definizione di specie chimica che io ho dato prima? Una specie chimica è composta dagli stessi elementi, nelle stesse proporzioni e con la stessa disposizione. Tutte le proprietà dei corpi dipendono da questi fattori Nel caso di corpi isomerici gli elementi e le loro proporzioni sono gli stessi, è solo differente la disposizione degli atomi. Il grande interesse dell isomerismo viene dall idea che i corpi possono essere completamente cambiati nelle loro proprietà dalla diversa disposizione degli atomi nella molecola chimica, questo è il nostro caso. Tuttavia non ci sono corpi isomerici nei quali noi conosciamo la reale relazione tra un arrangiamento molecolare rispetto ad un altro. Questa carenza è colmata per la prima volta dalla scoperta della costituzione dell acido racemico e dalla mutua relazione tra i due isomeri destro e sinistro dell acido tartarico. >>
28 La grande intuizione <<.Noi sappiamo che, da una parte, la disposizione di entrambi gli acidi tartarici è asimmetrica, dall altro che essi sono completamente gli stessi, con l eccezione che l asimmetria è mostrata in senso opposto. Sono gli atomi dell acido destro arrangiati nella forma di una spirale destrogira o sono situati ai vertici di un tetraedro irregolare, o essi hanno qualche altra disposizione asimmetrica? Ma senza dubbio gli atomi possiedono una disposizione asimmetrica uguale a quella di un oggetto e la sua immagine riflessa >>
29 Tutti gli oggetti, di seguito, si possono presentare in due forme tra loro speculari ma non sovrapponibili. Allo stesso modo le molecole, otticamente attive, sono come questi oggetti, si possono trovare in due forme speculari, ma non sovrapponibili. E stata l intuizione di Pasteur per spiegare l isomeria ottica. La quarta fila di lettere non ha elementi di simmetria, perciò sono possibili due forme tra loro speculari ma non sovrapponibili. ( questa volta rimanendo nel piano )
30 Queste viti con i rispettivi dadi sono oggetti asimmetrici. Possiamo avere viti con una filettatura che si avvolge in senso contrario. Avremo due tipi di viti speculari ma non sovrapponibili Può esistere un altra forbice che si specchia a questa ma non si sovrappone
31 Oggetti chirali naturali : batteri, piante rampicanti, molluschi
32
33 Dalla natura all architettura
34
35 L esame di Biot Pasteur è entusiasta della sua scoperta,ma prima di presentare la comunicazione all accademia delle scienze gli è richiesto di ripetere la prova. E scelto Biot come esaminatore. La prova viene ripetuta in presenza di Biot. Dopo alcuni giorni il risultato è confermato. I cristalli formatisi vengono separati nelle due forme speculari e viene riconfermata la loro proprietà di ruotare in modo opposto il piano della luce. << allora il vecchio e illustre scienziato, visibilmente commosso, mi prese per un braccio e mi disse : Mio caro ragazzo, ho amato la scienza così tanto nella mia vita che questo mi fa battere il cuore. >>
36 Louis Pasteur
ISOMERIA. Isomeri di struttura O OH C 4 H 10 O C 4 H 10
 ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
28/03/2013. Stereochimica: enantiomeri
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
02/10/2018. di catena. di posizione. strutturali. di gruppo funzionale. isomeri. geometrici. stereoisomeri. ottici
 Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
LICEO SCIENTIFICO TITO LUCREZIO CARO NAPOLI. Classificazione dei minerali
 !1 LICEO SCIENTIFICO TITO LUCREZIO CARO NAPOLI Classificazione dei minerali I MINERALI Cosa sono i minerali? I minerali sono corpi inorganici, naturali e solidi,con una composizione chimica ben definita
!1 LICEO SCIENTIFICO TITO LUCREZIO CARO NAPOLI Classificazione dei minerali I MINERALI Cosa sono i minerali? I minerali sono corpi inorganici, naturali e solidi,con una composizione chimica ben definita
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
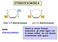 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria :
 Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
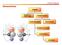 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
le reazioni chimiche asimmetriche
 Struttura molecolare e chiralità: le reazioni chimiche asimmetriche Lezioni d'autore Un video : Clic Chiralità (I) I termini chirale e chiralità, entrambi derivati dal greco χείρ (mano), sono comuni nella
Struttura molecolare e chiralità: le reazioni chimiche asimmetriche Lezioni d'autore Un video : Clic Chiralità (I) I termini chirale e chiralità, entrambi derivati dal greco χείρ (mano), sono comuni nella
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Altre tecniche analitiche ottiche: rifrattometria e polarimetria
 Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente
 Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
CONTENUTI DELLA LEZIONE:
 Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Altre leggi Gay-Lussac Avogadro molecole Cannizzaro
 Altre leggi Nel periodo in cui Dalton formulava la sua teoria atomica, Joseph Louis Gay-Lussac, un chimico francese appassionato di voli in mongolfiera, eseguiva numerosi e accurati esperimenti su reazioni
Altre leggi Nel periodo in cui Dalton formulava la sua teoria atomica, Joseph Louis Gay-Lussac, un chimico francese appassionato di voli in mongolfiera, eseguiva numerosi e accurati esperimenti su reazioni
Soluzioni degli esercizi di fine capitolo
 Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Vito Posca Il carbonio, gli enzimi, il DNA. himica organica, biochimica e biotecnologie 1 Soluzioni
Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Vito Posca Il carbonio, gli enzimi, il DNA. himica organica, biochimica e biotecnologie 1 Soluzioni
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
Cellula batterica. ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6%
 Le macromolecole, assieme, costituiscono la maggior parte del contenuto secco degli organismi viventi Cellula batterica ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6% CLASSIFICAZIONE DEI CARBOIDRATI:
Le macromolecole, assieme, costituiscono la maggior parte del contenuto secco degli organismi viventi Cellula batterica ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6% CLASSIFICAZIONE DEI CARBOIDRATI:
Un oggetto si definisce chirale se non è sovrapponibile alla. propria immagine speculare (mano destra e mano sinistra). Non
 Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
La valenza. 1 Na 1 Cl 1 F 2 O 2 Ca 3 N 3 Al 2 S
 Se una scoperta ha avuto una serie di conseguenze notevoli, fino a rivoluzionarie la chimica organica, questa è stato il fenomeno della isomeria. Esso venne definito per primo da Berzelius. Jons Jacob
Se una scoperta ha avuto una serie di conseguenze notevoli, fino a rivoluzionarie la chimica organica, questa è stato il fenomeno della isomeria. Esso venne definito per primo da Berzelius. Jons Jacob
Piano di oscillazione
 OLARIMETRIA I fenomeni relativi alla polarizzazione della luce possono essere spiegati con la teoria ondulatoria. Secondo Maxwell le oscillazioni elettromagnetiche sono dovute alla pulsazione di un campo
OLARIMETRIA I fenomeni relativi alla polarizzazione della luce possono essere spiegati con la teoria ondulatoria. Secondo Maxwell le oscillazioni elettromagnetiche sono dovute alla pulsazione di un campo
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI
 L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
La FORMA delle MOLECOLE
 La FORMA delle MOLECOLE Quando una molecola è costituita da due soli atomi, non vi è alcun dubbio sulla sua forma: gli atomi sono semplicemente disposti uno accanto all altro. Le molecole formate da tre
La FORMA delle MOLECOLE Quando una molecola è costituita da due soli atomi, non vi è alcun dubbio sulla sua forma: gli atomi sono semplicemente disposti uno accanto all altro. Le molecole formate da tre
Seconda unità didattica. Trasformazioni chimiche
 Seconda unità didattica Trasformazioni chimiche Trasformazioni chimiche Prendono il nome di reazioni chimiche Nelle reazioni chimiche una o più sostanze(reagenti) si trasformano, in una o più, nuove sostanze
Seconda unità didattica Trasformazioni chimiche Trasformazioni chimiche Prendono il nome di reazioni chimiche Nelle reazioni chimiche una o più sostanze(reagenti) si trasformano, in una o più, nuove sostanze
Lezione 39 Chimica organica - stereoisomeria
 Lezione 39 Chimica organica - stereoisomeria 1. La stereoisomeria In un atomo di carbonio ibridato sp 3 i quattro orbitali ibridi, e quindi i quattro legami da essi formati sono orientati, come detto,
Lezione 39 Chimica organica - stereoisomeria 1. La stereoisomeria In un atomo di carbonio ibridato sp 3 i quattro orbitali ibridi, e quindi i quattro legami da essi formati sono orientati, come detto,
OTTICA GEOMETRICA. Ovvero la retta perpendicolare alla superficie riflettente. Figura 1. Figura 2
 OTTICA GEOMETRICA L ottica geometrica si occupa di tutta quella branca della fisica che ha a che fare con lenti, specchi, vetri e cose simili. Viene chiamata geometrica in quanto non interessa la natura
OTTICA GEOMETRICA L ottica geometrica si occupa di tutta quella branca della fisica che ha a che fare con lenti, specchi, vetri e cose simili. Viene chiamata geometrica in quanto non interessa la natura
Diagramma che riassume i diversi tipi di isomeri. N.B. Gli isomeri costituzionali (o isomeri di struttura: es. n-propile /isopropile non sono
 STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2012/2013 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2012/2013 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Lo stato solido. Solido: qualsiasi corpo rigido e incomprimibile che ha forma e volume propri. amorfi. cristallini
 Lo stato solido Solido: qualsiasi corpo rigido e incomprimibile che ha forma e volume propri Solidi amorfi cristallini Cella elementare: la più piccola porzione del reticolo cristallino che ne possiede
Lo stato solido Solido: qualsiasi corpo rigido e incomprimibile che ha forma e volume propri Solidi amorfi cristallini Cella elementare: la più piccola porzione del reticolo cristallino che ne possiede
1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno 5. Legami a confronto
 Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia
 Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 3. LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino
 Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
Massa degli atomi e delle molecole
 Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Polarimetria - Potere Rotatorio Naturale
 Polarimetria - Potere Rotatorio Naturale La polarimetria è la metodica di laboratorio che permette la determinazione del potere rotatorio di sostanze otticamente attive. -1811 J.F.D.Arago scoprì il potere
Polarimetria - Potere Rotatorio Naturale La polarimetria è la metodica di laboratorio che permette la determinazione del potere rotatorio di sostanze otticamente attive. -1811 J.F.D.Arago scoprì il potere
POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della luce p
 POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
TRASFORMAZIONI GEOMETRICHE NEL PIANO. Parte 2
 TRASFORMAZIONI GEOMETRICHE NEL PIANO Parte 2 La simmetria L'etimologia della parola simmetria è greca. = stessa misura Per estensione, se ne amplia il significato ad espressioni del tipo 'equilibrio fra
TRASFORMAZIONI GEOMETRICHE NEL PIANO Parte 2 La simmetria L'etimologia della parola simmetria è greca. = stessa misura Per estensione, se ne amplia il significato ad espressioni del tipo 'equilibrio fra
Cristalli, minerali e loro proprietà
 Cristalli, minerali e loro proprietà 1 2.1 Elementi e composti naturali Un elemento è una sostanza che non può essere separata in tipi più semplici di materia con normali processi chimici. Otto tra gli
Cristalli, minerali e loro proprietà 1 2.1 Elementi e composti naturali Un elemento è una sostanza che non può essere separata in tipi più semplici di materia con normali processi chimici. Otto tra gli
minerale roccia cristallo Abito cristallino Punto di fusione La durezza La sfaldatura
 Minerali e rocce Un minerale è un composto chimico che si trova in natura, come costituente della litosfera, che ha una ben determinata composizione ed una struttura cristallina ben definita. Ad oggi sono
Minerali e rocce Un minerale è un composto chimico che si trova in natura, come costituente della litosfera, che ha una ben determinata composizione ed una struttura cristallina ben definita. Ad oggi sono
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 5 La quantità chimica: la mole 3 Sommario 1. La massa di atomi e molecole: cenni storici 2. Quanto pesa un atomo o una molecola
LA STRUTTURA DELLA MATERIA
 LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
Progetto Nazionale Disciplinare Scienza dei materiali
 Piano Nazionale per le Lauree Scientifiche Progetto Nazionale Disciplinare Scienza dei materiali Università della Calabria Dipartimento di Fisica POLARIZZAZIONE Dipartimento di Fisica Università della
Piano Nazionale per le Lauree Scientifiche Progetto Nazionale Disciplinare Scienza dei materiali Università della Calabria Dipartimento di Fisica POLARIZZAZIONE Dipartimento di Fisica Università della
Cristalli fotonici e loro applicazioni
 Dipartimento di fisica A. Volta, Università degli studi di Pavia 8 maggio 2009 solidi cristallini = reticolo + base Figura: alcuni reticoli di Bravais 3D con 3 vettori primitivi a,b,c; Figura: alcuni reticoli
Dipartimento di fisica A. Volta, Università degli studi di Pavia 8 maggio 2009 solidi cristallini = reticolo + base Figura: alcuni reticoli di Bravais 3D con 3 vettori primitivi a,b,c; Figura: alcuni reticoli
Simmetrie in fisica classica. Sergio Giudici Dip. di Fisica, Università di Pisa
 Simmetrie in fisica classica Sergio Giudici Dip. di Fisica, Università di Pisa Esempio 1 : La macchina di Atwood Dispositivo inventato nel 1784 dal Rev. George Atwood a scopo didattico per lo studio del
Simmetrie in fisica classica Sergio Giudici Dip. di Fisica, Università di Pisa Esempio 1 : La macchina di Atwood Dispositivo inventato nel 1784 dal Rev. George Atwood a scopo didattico per lo studio del
4. Stereoisomeria ottica o enantiomeria
 . Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
. Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
I composti del carbonio
 Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Sostanza pura. Il termine sostanza indica il tipo di materia di cui è fatto un corpo.
 Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
VERIFICA FINALE ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO. Scienziati in erba. Durata della prova: 100 minuti
 VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto. Rete Scuole LSS. a.s. 2016/2017
 Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto Rete Scuole LSS a.s. 2016/2017 ph CHIMICA Classi IV A-B Liceo Linguistico Orbetello a.s. 2016 17 Docente: Carmelina
Iniziativa realizzata con il contributo della Regione Toscana nell ambito del progetto Rete Scuole LSS a.s. 2016/2017 ph CHIMICA Classi IV A-B Liceo Linguistico Orbetello a.s. 2016 17 Docente: Carmelina
Capitolo 8 I LEGAMI CHIMICI Aspetti elettrostatici ed energetici dei legami chimici
 Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
I raggi luminosi. Per secoli si sono contrapposti due modelli della luce. il modello ondulatorio (Christiaan Huygens)
 I raggi luminosi Per secoli si sono contrapposti due modelli della luce il modello corpuscolare (Newton) * la luce è un flusso di particelle microscopiche il modello ondulatorio (Christiaan Huygens) *
I raggi luminosi Per secoli si sono contrapposti due modelli della luce il modello corpuscolare (Newton) * la luce è un flusso di particelle microscopiche il modello ondulatorio (Christiaan Huygens) *
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Appunti di storia della fisica: l atomo
 Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Appunti di storia della fisica: l atomo Dalla filosofia greca all 800 Legge di conservazione della massa (Lavoisier, seconda metà del 700): in una reazione chimica all'interno di un sistema chiuso la massa
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali
 Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2012/13 Test di autovalutazione 2 ottobre 2012 Cognome: Nome: Matematica e logica 1.
Università degli Studi di Perugia Facoltà di Scienze Matematiche Fisiche e Naturali Corso di Laurea in Chimica A.A. 2012/13 Test di autovalutazione 2 ottobre 2012 Cognome: Nome: Matematica e logica 1.
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Gli elettroni della molecola sono quindi descritti da
 IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Le reazioni. Sommario. Equazioni chimiche 13/03/2019
 Le reazioni Sommario Scrittura delle equazioni chimiche Bilanciamento delle reazioni Stechiometria delle reazioni Reagente limitante e reagenti in eccesso Resa di una reazione Tipi diversi di reazioni
Le reazioni Sommario Scrittura delle equazioni chimiche Bilanciamento delle reazioni Stechiometria delle reazioni Reagente limitante e reagenti in eccesso Resa di una reazione Tipi diversi di reazioni
Teoria degli orbitali ibridi
 Legami σ e π Teoria degli orbitali ibridi FORMAZIONE DEI LEGAMI CHIMICI COVALENTI L orbitale della molecola H 2 ha simmetria cilindrica intorno all asse internucleare H-H LEGAME SIGMA Gli orbitali molecolari
Legami σ e π Teoria degli orbitali ibridi FORMAZIONE DEI LEGAMI CHIMICI COVALENTI L orbitale della molecola H 2 ha simmetria cilindrica intorno all asse internucleare H-H LEGAME SIGMA Gli orbitali molecolari
POLIEDRI IN CRISTALLOGRAFIA
 POLIEDRI IN CRISTALLOGRAFIA L'universo è composto di materia, ovviamente. E la materia è composta di particelle: elettroni, neutroni e protoni. Dunque l'intero universo è composto di particelle. Ora, di
POLIEDRI IN CRISTALLOGRAFIA L'universo è composto di materia, ovviamente. E la materia è composta di particelle: elettroni, neutroni e protoni. Dunque l'intero universo è composto di particelle. Ora, di
ISOMERIA. Isomeri costituzionali. Stereoisomeri. Nomenclatura. Importanza biologica della chiralità
 ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Non scrivete nel campo grigio.
 *M15243112I* 2/16 *M15243112I02* *M15243112I03* 3/16 P perforiran list 4/16 *M15243112I04* Pagina vuota *M15243112I05* 5/16 1. Di seguito è rappresentata l'apparecchiatura utilizzata per la distillazione.
*M15243112I* 2/16 *M15243112I02* *M15243112I03* 3/16 P perforiran list 4/16 *M15243112I04* Pagina vuota *M15243112I05* 5/16 1. Di seguito è rappresentata l'apparecchiatura utilizzata per la distillazione.
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
La isomeria in Chimica Organica
 La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
OBIETTIVI SPECIFICI DI APPREDIMENTO IN TERMINI DI COMPETENZE
 OBIETTIVI SPECIFICI DI APPREDIMENTO IN TERMINI DI COMPETENZE CLASSE V Liceo Classico e 2^ Liceo delle scienze Umane Il percorso di Scienze Naturali individuato dal dipartimento di Scienze prevede per le
OBIETTIVI SPECIFICI DI APPREDIMENTO IN TERMINI DI COMPETENZE CLASSE V Liceo Classico e 2^ Liceo delle scienze Umane Il percorso di Scienze Naturali individuato dal dipartimento di Scienze prevede per le
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
nella forma CIS i due gruppi funzionali si trovano dalla stessa parte, mentre nella forma trans si trovano dalla parte opposta.
 http://www. STEREOCHIMICA Considera i due composti 1 forma CIS 2 forma TRANS nella forma CIS i due gruppi funzionali si trovano dalla stessa parte, mentre nella forma trans si trovano dalla parte opposta.
http://www. STEREOCHIMICA Considera i due composti 1 forma CIS 2 forma TRANS nella forma CIS i due gruppi funzionali si trovano dalla stessa parte, mentre nella forma trans si trovano dalla parte opposta.
Istituti Paritari PIO XII
 Istituti Paritari PIO XII RMTD545007 Amministrazione Finanza e Marketing Sistemi Informativi Aziendali 00159 ROMA - via Galla Placidia, 63 RMTL395001 Costruzioni, Ambiente e territorio Tel 064381465 Fax
Istituti Paritari PIO XII RMTD545007 Amministrazione Finanza e Marketing Sistemi Informativi Aziendali 00159 ROMA - via Galla Placidia, 63 RMTL395001 Costruzioni, Ambiente e territorio Tel 064381465 Fax
Legame chimico: covalente polare Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
IL SISTEMA SOLARE IL SISTEMA SOLARE E FORMATO DA: -IL SOLE -I PIANETI -I SATELLITI -GLI ASTEROIDI -LE COMETE -I METEORITI/METEORE
 IL SISTEMA SOLARE HA AVUTO ORIGINE CIRCA 4 MILIARDI E MEZZO DI ANNI FA DA UNA NUBE DI GAS E MINUSCOLE PARTICELLE SOLIDE, CHIAMATE DAGLI SCIENZIATI POLVERE. A CAUSA DELLA FORZA DI GRAVITA QUESTE PARTICELLE
IL SISTEMA SOLARE HA AVUTO ORIGINE CIRCA 4 MILIARDI E MEZZO DI ANNI FA DA UNA NUBE DI GAS E MINUSCOLE PARTICELLE SOLIDE, CHIAMATE DAGLI SCIENZIATI POLVERE. A CAUSA DELLA FORZA DI GRAVITA QUESTE PARTICELLE
Protocollo dei saperi imprescindibili
 Protocollo dei saperi imprescindibili Ordine di scuola: LICEO ARTISTICO DISCIPLINA: CHIMICA DEI MATERIALI RESPONSABILE: MERI TETI CLASSE III / INDIRIZZO: Competenze: correla le grandezze fondamentali e
Protocollo dei saperi imprescindibili Ordine di scuola: LICEO ARTISTICO DISCIPLINA: CHIMICA DEI MATERIALI RESPONSABILE: MERI TETI CLASSE III / INDIRIZZO: Competenze: correla le grandezze fondamentali e
UNITA DIDATTICA. Disciplina: SCIENZE INTEGRATE: CHIMICA
 Disciplina: SCIENZE INTEGRATE: CHIMICA Disciplina: SCIENZE INTEGRATE: CHIMICA Titolo: La mole e il numero di Avogadro. Codice: D1-P-Tec-Gra Ore previste:10 Concetto di massa atomica: come si è arrivati
Disciplina: SCIENZE INTEGRATE: CHIMICA Disciplina: SCIENZE INTEGRATE: CHIMICA Titolo: La mole e il numero di Avogadro. Codice: D1-P-Tec-Gra Ore previste:10 Concetto di massa atomica: come si è arrivati
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
I composti organici e i loro polimeri
 I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
PROGRAMMAZIONE PIANO DI LAVORO SCIENZE CLASSE Prima. Chimica/Fisica
 PROGRMMZIONE PINO I LVORO SCIENZE CLSSE Prima Chimica/Fisica I primi passi nella scienza. B. L osservazione Qualità e quantità Numeri e misure Il metodo scientifico Obiettivi di apprendimento per lo Conosce
PROGRMMZIONE PINO I LVORO SCIENZE CLSSE Prima Chimica/Fisica I primi passi nella scienza. B. L osservazione Qualità e quantità Numeri e misure Il metodo scientifico Obiettivi di apprendimento per lo Conosce
PROGRAMMAZIONE PERSONALE DEL DOCENTE a. s. 2012/2013
 ISTITUTO DI ISTRUZIONE SUPERIORE LEON BATTISTA ALBERTI Via A. Pillon n. 4-35031 ABANO T. (PD) Tel. 049 812424 - Fax 049 810554 Distretto 45 - PD Ovest PDIS017007- Cod. fiscale 80016340285 sito web: http://www.lbalberti.it/
ISTITUTO DI ISTRUZIONE SUPERIORE LEON BATTISTA ALBERTI Via A. Pillon n. 4-35031 ABANO T. (PD) Tel. 049 812424 - Fax 049 810554 Distretto 45 - PD Ovest PDIS017007- Cod. fiscale 80016340285 sito web: http://www.lbalberti.it/
