ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
|
|
|
- Giuliana Pagano
- 9 anni fa
- Просмотров:
Транскрипт
1 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012
2 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno o stereocentro. Una molecola chirale non presenta né un piano, né un centro di simmetria e non è sovrapponibile alla propria immagine speculare.
3 Due stereoisomeri le cui immagini speculari non sono fra loro sovrapponibili sono enantiomeri. Due enantiomeri differiscono solamente nelle proprietà direzionali(o chirali), come ad esempio la capacità di ruotare il piano della luce polarizzata questi composti vengono perciò detti otticamente attivi. Sono diastereoisomeri, due stereoisomeri che non sono enantiomeri. I diastereoisomeri hanno proprietà chimico fisiche diverse. Uno stereocentro può avere configurazione R o S. H COOH * OH OH * COOH H acido (2R,3R) tartarico
4 ATTIVITÀ OTTICA: IL POLARIMETRO Il polarimetro è uno strumento in grado di misurare il potere ottico rotatorio di una soluzione ed è utilizzato per il riconoscimento di enantiomeri nei composti chirali. APPLICAZIONI: consente di misurare la concentrazione e la purezza di sostanze organiche come oli, sostanze zuccherine, sostanze alimentari etc.
5 Laluce,prodottada una sorgentecostituitada una lampadaaivaporidisodio,inbasealla teoria ondulatoria si propagherà su diversi piani lungo la direzione di propagazione. La radiazione luminosa così generata viene fatta passare attraverso un polarizzatore, materiale che lascia passare un unico piano di polarizzazione. Un secondo polarizzatore, detto analizzatore, viene allineato in modo tale che sia perpendicolare al primo filtro polarizzatore la luce giungerà quindi all osservatore che vedrà il campo buio.
6 La sorgente di luce proietta su una lente condensatrice passa attraverso un filtro colorato e poi sul filtro polarizzatore. A questo punto il fascio di luce polarizzata passa attraverso il piano a mezza onda che scompone la luce in 3 campi il fascio illuminante inciderà poi sul campione e attraverserà il filtro analizzatore. OP direzione del piano di vibrazione del campo bipartito OX direzione di vibrazione del filtro analizzatore OP direzione del piano di vibrazione del campo tripartito AA direzione di vibrazione del filtro polarizzatore Ruotare il goniometro di un angolo αper tornare alla condizione Iniziale dove il campo è completamente illuminato.
7 Quando una sostanza chirale viene posta fra i due polarizzatori si osserverà una rotazione del piano della luce incidente e si osserverà perciò un variazione nella luce all uscita dell analizzatore. Le tre diverse situazioni sono qui sotto mostrate: Posizione 0 o sostanza achirale campo illuminato Girare verso sx il goniometro Girare verso dx il goniometro L angolo di rotazione dell analizzatore è la rotazione osservata (α) del campione. Se il campione provoca una rotazione della luce polarizzata verso destra il campione viene detto destrorotatorio, altrimenti è detto levorotatorio. L entità di rotazione del piano della luce polarizzata dipende dal numero di molecole con le quali essa interagisce, quindi dalla concentrazione del campione e dalla lunghezza del cammino ottico: Dove C è la concentrazione in g/ml, l è la lunghezza del cammino ottico in dm e α è la rotazione osservata.
8 [α] λ t è invece la rotazione specifica, ovvero un valore standardizzato per confrontare l attività ottica di diverse sostanze otticamente attive L apice t ed il pedice λindicano che la rotazione ottica è legata alla temperatura e alla lunghezza d onda. Per misurare la rotazione osservata si utilizza poi un goniometro ruotare il filtro analizzatore fino ad ottenere un campo visivo uniforme (situazione iniziale).
9 PROTOCOLLO 1 Avvinare la cella con acqua o etanolo a seconda della molecola da analizzare. Preparare: Una soluzione di acido (2R,3R) tartarico pesare 1.5 g e scioglierli in 15mL di acqua che saranno usati per riempire la cella per la misura al polarimetro (Gruppi pari). Riempire la cella polarimetrica con la soluzione appena preparata. Oppure: Una soluzione di (1R, 2S, 3R) mentolo pesare 1.5 g e scioglierli in 15mL di etanolo che saranno usati per riempire la cella per la misura al polarimetro (Gruppi dispari). Riempire la cella polarimetrica con la soluzione appena preparata. Calcolare la concentrazione della soluzione così preparata sapendo che e [α] C = +12 xml x(g xdm) -1 acido (2R, 3R)tartarico [α] C = -50 xml x(g xdm) -1 acido (1R,2S, 5R)mentolo l = 1dm
10 Idrolisi acida del saccarosio PROTOCOLLO 2 Preparare 15mL di una soluzione di saccarosio al 5%. Aggiungere 1.5mL di soluzione di acido al 10% (che troverete sul banco) e ponete la provetta in acqua bollente per 30minuti. Riempire la cella polarimetrica con la soluzione ottenuta dopo raffreddamento. HCl + Saccarosio Glucosio Fruttosio Nel frattempo effettuate una lettura di una soluzione di saccarosio al 5% (già pronta) in una cella polarimetrica (di l=2 dm). Di ogni soluzione determinare la rotazione osservata e nella relazione evidenziare le differenze. N.B.: attenzione a non rompere le celle per la misura perché sono contate!! Testare la tenuta delle celle per la misura aggiungendovi acqua attenzione poi a coprire la cella con il vetrino senza fare bolle!!
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della luce p
 POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
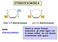 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Esperienza di polarimetria. Dott. Alfonso Zoleo
 Esperienza di polarimetria Dott. Alfonso Zoleo Laboratorio di Metodologie Spettroscopiche per le Biotecnologie AA 2014-2015 Concetti fondamentali La luce possiede una proprietà chiamata polarizzazione.
Esperienza di polarimetria Dott. Alfonso Zoleo Laboratorio di Metodologie Spettroscopiche per le Biotecnologie AA 2014-2015 Concetti fondamentali La luce possiede una proprietà chiamata polarizzazione.
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Altre tecniche analitiche ottiche: rifrattometria e polarimetria
 Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente
 Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
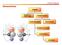 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Diagramma che riassume i diversi tipi di isomeri. N.B. Gli isomeri costituzionali (o isomeri di struttura: es. n-propile /isopropile non sono
 STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
CONTENUTI DELLA LEZIONE DI OGGI:
 CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
4.5 Polarizzazione Capitolo 4 Ottica
 4.5 Polarizzazione Esercizio 98 Un reticolo con N fenditure orizzontali, larghe a e con passo p, è posto perpendicolarmente a superficie di un liquido con n =.0. Il reticolo è colpito normalmente alla
4.5 Polarizzazione Esercizio 98 Un reticolo con N fenditure orizzontali, larghe a e con passo p, è posto perpendicolarmente a superficie di un liquido con n =.0. Il reticolo è colpito normalmente alla
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
LABORATORIO DI FISICA 4 relazione: Saccarometria. De Mauro Giuseppe, Degradi Pablo, Restieri Andrea
 LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
OTTICA ONDE INTERFERENZA DIFFRAZIONE RIFRAZIONE LENTI E OCCHIO
 OTTICA ONDE INTERFERENZA DIFFRAZIONE RIFRAZIONE LENTI E OCCHIO 1 INTERFERENZA Massimi di luminosità Onda incidente L onda prodotta alla fenditura S0, che funge da sorgente, genera due onde alle fenditure
OTTICA ONDE INTERFERENZA DIFFRAZIONE RIFRAZIONE LENTI E OCCHIO 1 INTERFERENZA Massimi di luminosità Onda incidente L onda prodotta alla fenditura S0, che funge da sorgente, genera due onde alle fenditure
Stereochimica. Molecole nello spazio
 Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
I Esperienza laboratorio di Chimica organica Carboidrati riducenti e non riducenti
 I Esperienza laboratorio di Chimica organica 2018-2019 Carboidrati riducenti e non riducenti 1 Carboidrati: ossidazione Come tutte le aldeidi, anche gli aldosi possono ossidarsi per dare acidi carbossilici.
I Esperienza laboratorio di Chimica organica 2018-2019 Carboidrati riducenti e non riducenti 1 Carboidrati: ossidazione Come tutte le aldeidi, anche gli aldosi possono ossidarsi per dare acidi carbossilici.
 La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
Un oggetto si definisce chirale se non è sovrapponibile alla. propria immagine speculare (mano destra e mano sinistra). Non
 Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
La legge. Il colorimetro. L esperienza. Realizzato da. August Beer ( ) Johann Heinrich Lambert ( )
 LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
4. Stereoisomeria ottica o enantiomeria
 . Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
. Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
ISOMERIA. Isomeri costituzionali. Stereoisomeri. Nomenclatura. Importanza biologica della chiralità
 ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
Polarizzazione e potere rotatorio del glucosio
 1 Esperienza del 22/3/2007. Noemi Chirico, Francesca Tedone, Olga Viviana Trumpy Classe 59 Polarizzazione e potere rotatorio del glucosio Materiale a disposizione: un polarimetro, costituito da due lastre
1 Esperienza del 22/3/2007. Noemi Chirico, Francesca Tedone, Olga Viviana Trumpy Classe 59 Polarizzazione e potere rotatorio del glucosio Materiale a disposizione: un polarimetro, costituito da due lastre
DESCRIZIONE DEI MINERALI Clivaggio o sfaldature
 Clivaggio o sfaldature Molti minerali si rompono lungo piani definiti, la posizione dei quali è controllata dalla loro struttura reticolare. Tra i piani di sfaldatura, il legame atomico è più debole rispetto
Clivaggio o sfaldature Molti minerali si rompono lungo piani definiti, la posizione dei quali è controllata dalla loro struttura reticolare. Tra i piani di sfaldatura, il legame atomico è più debole rispetto
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Molecola chirale: esiste in due forme enantiomorfe La molecola chirale può mostrare attività ottica cioè può ruotare il piano della luce polarizzata La luce polarizzata è costituita da due raggi (destrorso
Molecola chirale: esiste in due forme enantiomorfe La molecola chirale può mostrare attività ottica cioè può ruotare il piano della luce polarizzata La luce polarizzata è costituita da due raggi (destrorso
POLARIZZAZIONE. I = < (E 0 cos ϕ) 2 > (1) dove < (E 0 cos ϕ) 2 > è il valore mediato nel tempo.
 POLARIZZAZIONE ESERCIZIO 1 Un fascio di luce naturale attraversa una serie di polarizzatori ognuno dei quali ha l asse di polarizzazione ruotato di 45 rispetto al precedente. Determinare quale frazione
POLARIZZAZIONE ESERCIZIO 1 Un fascio di luce naturale attraversa una serie di polarizzatori ognuno dei quali ha l asse di polarizzazione ruotato di 45 rispetto al precedente. Determinare quale frazione
Esperienza di Polarimetria
 Esperienza di Polarimetria Docente di riferimento: Prof.ssa Marilena Di Valentin Si ringraziano il Dott. Antonio Barbon, Dott. Alfonso Zoleo e Prof.ssa Elisabetta Collini per avere contribuito al materiale
Esperienza di Polarimetria Docente di riferimento: Prof.ssa Marilena Di Valentin Si ringraziano il Dott. Antonio Barbon, Dott. Alfonso Zoleo e Prof.ssa Elisabetta Collini per avere contribuito al materiale
STEREOISOMERIA carbonio ibridizzato sp3 è legato a quattro atomi o gruppi tutti diversi fra loro
 STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
cognome e nome turno banco data Indicare i CALCOLI per ESTESO Nei RIQUADRI TRATTEGGIATI riportare i dati con le CIFRE SIGNIFICATIVE appropriate
 PREPARAZIONE e STANDARDIZZAZIONE di una SOLUZIONE di ACIDO CLORIDRICO densità HCl (aq) conc. (g/ml) % peso prelievo HCl (aq) conc. (ml) mmoli HCl = volume matraccio (ml) titolo previsto HCl (aq) diluito
PREPARAZIONE e STANDARDIZZAZIONE di una SOLUZIONE di ACIDO CLORIDRICO densità HCl (aq) conc. (g/ml) % peso prelievo HCl (aq) conc. (ml) mmoli HCl = volume matraccio (ml) titolo previsto HCl (aq) diluito
Chimica Organica Relazione
 Titolo Sbarbada avide 4 /C I.S.I.I. Marconi -PC- Pagina 1 di 5 26/04/05 Chimica rganica Relazione Esperienza con gli zuccheri (glucosio, fruttosio e saccarosio) biettivo Prerequisiti Analizzare gli zuccheri
Titolo Sbarbada avide 4 /C I.S.I.I. Marconi -PC- Pagina 1 di 5 26/04/05 Chimica rganica Relazione Esperienza con gli zuccheri (glucosio, fruttosio e saccarosio) biettivo Prerequisiti Analizzare gli zuccheri
CD circular dichroism -Misura la differenza di assorbimento della luce polarizzata circolarmente a destra da quella polarizzata a sinistra a
 CD CD circular dichroism -Misura la differenza di assorbimento della luce polarizzata circolarmente a destra da quella polarizzata a sinistra a differenti lunghezze d onda L attività ottica Filtro polarizzatore
CD CD circular dichroism -Misura la differenza di assorbimento della luce polarizzata circolarmente a destra da quella polarizzata a sinistra a differenti lunghezze d onda L attività ottica Filtro polarizzatore
Principio di Huygens
 Ottica fisica La luce è stata considerata una particella da Newton fino a Young (inizi XIX secolo) Nell'800 si sono studiati i fenomeni ondulatori associati alla luce Nel secolo scorso alcuni effetti (fotoelettrico,
Ottica fisica La luce è stata considerata una particella da Newton fino a Young (inizi XIX secolo) Nell'800 si sono studiati i fenomeni ondulatori associati alla luce Nel secolo scorso alcuni effetti (fotoelettrico,
Principio di Huygens
 Ottica fisica La luce è stata considerata una particella da Newton fino a Young (inizi XIX secolo) Nell'800 si sono studiati i fenomeni ondulatori associati alla luce Nel secolo scorso alcuni effetti (fotoelettrico,
Ottica fisica La luce è stata considerata una particella da Newton fino a Young (inizi XIX secolo) Nell'800 si sono studiati i fenomeni ondulatori associati alla luce Nel secolo scorso alcuni effetti (fotoelettrico,
INTERFERENZA - DIFFRAZIONE
 INTERFERENZA - F. Due onde luminose in aria, di lunghezza d onda = 600 nm, sono inizialmente in fase. Si muovono poi attraverso degli strati di plastica trasparente di lunghezza L = 4 m, ma indice di rifrazione
INTERFERENZA - F. Due onde luminose in aria, di lunghezza d onda = 600 nm, sono inizialmente in fase. Si muovono poi attraverso degli strati di plastica trasparente di lunghezza L = 4 m, ma indice di rifrazione
Ottica fisica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Ottica fisica La natura ondulatoria della luce è stata evidenziata da Young ai primi dell 800 usando l interferenza e confutando l idea corpuscolare di Newton Le onde elettromagnetiche sono state previste
Ottica fisica La natura ondulatoria della luce è stata evidenziata da Young ai primi dell 800 usando l interferenza e confutando l idea corpuscolare di Newton Le onde elettromagnetiche sono state previste
7.4 Proprietà delle Molecole Chirali: Attvità Ottica
 7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
ESPERIMENTO DI YOUNG DOPPIA FENDITURA
 ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
ESPERIMENTO DI YOUNG DOPPIA FENDITURA Larghezza fenditure a > d (L = distanza fenditure - schermo; d = distanza tra le fenditure) Evidenza della natura ondulatoria della luce Luce monocromatica
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
ESPERIMENTO 6: OTTICA GEOMETRICA E DIFFRAZIONE
 ESPERIMENTO 6: OTTICA GEOMETRICA E DIFFRAZIONE Scopo dell esperimento: studiare l ottica geometrica e i fenomeni di diffrazione MATERIALE A DISPOSIZIONE: 1 banco ottico 1 blocco di plexiglass 2 lenti con
ESPERIMENTO 6: OTTICA GEOMETRICA E DIFFRAZIONE Scopo dell esperimento: studiare l ottica geometrica e i fenomeni di diffrazione MATERIALE A DISPOSIZIONE: 1 banco ottico 1 blocco di plexiglass 2 lenti con
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata CHO
 Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
Elettromagnetismo (6/6) Onde elettromagnetiche Lezione 24, 8/1/2019, JW , 29.5
 Elettromagnetismo (6/6) Onde elettromagnetiche Lezione 24, 8/1/2019, JW 29.1-29.3, 29.5 1 1. Le onde elettromagnetiche Le equazioni di Maxwell, elaborate nel 1864, prevedono l esistenza nello spazio vuoto
Elettromagnetismo (6/6) Onde elettromagnetiche Lezione 24, 8/1/2019, JW 29.1-29.3, 29.5 1 1. Le onde elettromagnetiche Le equazioni di Maxwell, elaborate nel 1864, prevedono l esistenza nello spazio vuoto
Chimica Organica II - Laboratorio A.A. 2007/08 COOH A(+) (+) Acido Tartarico 2 OH -
 himica Organica II - Laboratorio A.A. 2007/08 Esperienza 1 di una miscela racemica 3 3 OO N 2 2 N + + O O OO B(-)A(+) B(+)A(+) B(-) B(+) A(+) α-metilbenzilammina (+) Acido Tartarico Sali Diasteroisomerici
himica Organica II - Laboratorio A.A. 2007/08 Esperienza 1 di una miscela racemica 3 3 OO N 2 2 N + + O O OO B(-)A(+) B(+)A(+) B(-) B(+) A(+) α-metilbenzilammina (+) Acido Tartarico Sali Diasteroisomerici
La spettrofotometria è una tecnica analitica, qualitativa e quantitativa e permette il riconoscimento e la quantizzazione di una sostanza in base al
 SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
Sperimentazione FT-NIR 2004
 Sperimentazione FT-NIR 2004 Scopo del test L obiettivo della sperimentazione è quello di determinare la possibilità di analizzare i seguenti componenti nei loro range tipici per la applicazioni nell industria
Sperimentazione FT-NIR 2004 Scopo del test L obiettivo della sperimentazione è quello di determinare la possibilità di analizzare i seguenti componenti nei loro range tipici per la applicazioni nell industria
I CARBOIDRATI LA CHIMICA DELLA VITA GSCATULLO
 I CARBOIDRATI LA CHIMICA DELLA VITA GSCATULLO ( I Carboidrati Le biomolecole Cosa sono le biomolecole? Le biomolecole sono quelle molecole presenti negli organismi viventi e da loro sintetizzate. Sono
I CARBOIDRATI LA CHIMICA DELLA VITA GSCATULLO ( I Carboidrati Le biomolecole Cosa sono le biomolecole? Le biomolecole sono quelle molecole presenti negli organismi viventi e da loro sintetizzate. Sono
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
Elementi di Stereochimica
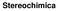 Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Il microscopio: metodi per esaltare il contrasto
 Il microscopio: metodi per esaltare il contrasto La materia vivente è composta principalmente da acqua! Al microscopio risulta TRASPARENTE, se ha uno spessore tale da essere attraversata dalla luce. Altrimenti
Il microscopio: metodi per esaltare il contrasto La materia vivente è composta principalmente da acqua! Al microscopio risulta TRASPARENTE, se ha uno spessore tale da essere attraversata dalla luce. Altrimenti
Legame chimico: covalente polare Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Centri chirali specchio
 entri chirali L atomo centrale ha ibridazione sp 3 ed è legato a quattro sostituenti diversi, esso è detto carbonio chirale. Esiste, un altra molecola nella quale gli stessi atomi sono legati all atomo
entri chirali L atomo centrale ha ibridazione sp 3 ed è legato a quattro sostituenti diversi, esso è detto carbonio chirale. Esiste, un altra molecola nella quale gli stessi atomi sono legati all atomo
Costruiamo un microscopio polarizzatore
 Praticando le Scienze della Terra, Sapienza Università di Roma 26 gennaio 2018 Costruiamo un microscopio polarizzatore Michele Lustrino Dipartimento di Scienze della Terra Sapienza Università di Roma I
Praticando le Scienze della Terra, Sapienza Università di Roma 26 gennaio 2018 Costruiamo un microscopio polarizzatore Michele Lustrino Dipartimento di Scienze della Terra Sapienza Università di Roma I
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
Cosa si intende per onda?
 Fenomeni Ondulatori Cosa si intende per onda? si definisce onda una perturbazione che si propaga non si ha propagazione di materia ma solo di energia onde meccaniche (mezzo) onde elettromagnetiche (vuoto,
Fenomeni Ondulatori Cosa si intende per onda? si definisce onda una perturbazione che si propaga non si ha propagazione di materia ma solo di energia onde meccaniche (mezzo) onde elettromagnetiche (vuoto,
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
Grandezze fotometriche
 Capitolo 3 Grandezze fotometriche 3.1 Intensità luminosa E una grandezza vettoriale di simbolo I. Ha come unità di misura la candela(cd). La candela è l unità di misura fondamentale del sistema fotometrico.
Capitolo 3 Grandezze fotometriche 3.1 Intensità luminosa E una grandezza vettoriale di simbolo I. Ha come unità di misura la candela(cd). La candela è l unità di misura fondamentale del sistema fotometrico.
