4. Stereoisomeria ottica o enantiomeria
|
|
|
- Edmondo Fantoni
- 5 anni fa
- Visualizzazioni
Transcript
1 . Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell ATTIVITA OTTICA capacità di ruotare il piano di vibrazione della luce polarizzata piana. Nel 1875 Vant off e Le Bel deducono da questa proprietà che le valenze del C non sono su un piano, ma si dirigono verso i vertici di un tetraedro regolare. Nel 1880 Pasteur scopre che i composti organici otticamente attivi esistono come coppie di composti che possiedono proprietà chimiche e fisiche identiche con la sola eccezione del segno (+ o -) di rotazione della luce polarizzata piana. Tali coppie di composti vengono denominate: ANTIPODI OTTICI o ENANTIOMERI Uno dei due devia il piano della luce polarizzata in senso destrogiro (o orario), l altro in senso levogiro (o antiorario), ma con identico valore assoluto. Es.: uno dei due +0, l altro
2 .1. Il polarimetro raggio di luce non polarizzata: infiniti piani di vibrazione del campo magnetico () e del campo elettrico (E) ortogonali tra loro. dopo passaggio nel polarizzatore rimane un solo piano di vibrazione del campo elettrico: LUCE POLARIZZATA PIANA Le molecole otticamente attive deviano il piano della luce polarizzata piana. La proprietà è della molecola in sè e non dei cristalli in quanto si osserva anche in soluzione. se nel tubo portacampione sono presenti molecole otticamente attive si ha deviazione del piano di vibrazione della luce polarizzata per ritrovare il piano della luce, l analizzatore deve essere ruotato di α gradi (nell esempio in senso orario) 2
3 .2. Misura dell attività ottica: potere rotatorio osservato e specifico L angolo di deflessione (α) del piano della luce polarizzata piana è una misura del potere rotatorio di una molecola. L angolo osservato sperimentalmente (α oss ) è proporzionale alla lunghezza del tubo polarimetrico utilizzato (L, espressa in dm) e alla concentrazione del campione (c) espressa in g/cm. Si definisce POTERE ROTATORIO SPECIFICO di un composto organico il valore di α oss che si ottiene misurando il potere rotatorio di una soluzione a conc. di 1g/cm mediante un tubo di lunghezza 1 dm. POTERE ROTATORIO SPECIFICO temperatura [α] D 25 = α oss L x C concentrazione = 1 g/cm Lunghezza d onda della riga D del Na λ= 589 nm Lunghezza del tubo polarimetrico = 1 dm Lo [a] D 25 delle varie molecole otticamente attive è una costante chimico-fisica (come il punto d ebollizione) ed è utile per il loro riconoscimento e il loro dosaggio.
4 .. Il potere rotatorio degli antipodi ottici: le configurazioni del carbonio asimmetrico La proprietà dipende dalla struttura molecolare e, in particolare, dall esistenza di asimmetria nella molecola. La geometria tetraedrica del carbonio sp impone che, se i vertici del tetraedro sono occupati da sostituenti diversi, l insieme non possiede alcun elemento di simmetria: è complessivamente ASIMMETRICO. Un C recante sostituenti diversi si definisce asimmetrico e si evidenzia con un asterisco (C*). I sostituenti legati al C* si distribuiscono nello spazio in 2 diversi modi, detti CONFIGURAZIONI, che determinano l esistenza di 2 molecole diverse tra loro solo per la sequenza dei sostituenti nello spazio (enantiomeri o antipodi ottici). Per leggere la parola ALT occorre ruotare lo sguardo in senso orario (molecola di sinistra) o anti-orario (molecola di destra) Le due molecole (antipodi) sono immagini speculari l una dell altra, ma non sono sovrapponibili (come le mani: chiralità) e, quindi, corrispondono a molecole diverse.
5 Nei 2 enantiomeri le distanze interatomiche e gli angoli di legame sono identici e, quindi, tutte le proprietà chimico-fisiche (reattività, costanti di dissociazione, velocità di reazione, bp, mp, ecc.) sono identiche. Conseguenza: i 2 enantiomeri sono inseparabili con i comuni metodi (distillazione, cristallizzazione, ecc.). Gli antipodi si distinguono per 2 sole proprietà: 1. direzione della deviazione del piano della luce polarizzata (orario o anti-orario) 2. proprietà biologiche: un antipodo amaro, l altro dolce (es: aspartame); oppure uno benefico, l altro tossico (es: talidomide) La presenza di C* è condizione sufficiente, ma non necessaria, per il verificarsi del fenomeno. La condizione necessaria è l asimmetria complessiva della molecola. La miscela al 50% di 2 enantiomeri si definisce MISCELA RACEMICA ed è inattiva otticamente. La razionalizzazione del fenomeno di deviazione del piano di polarizzazione della luce è comprensibile utilizzando i modelli molecolari. N.B.: Differenza tra configurazioni e conformazioni delle molecole. La trasformazione di una configurazione del carbonio in quella antipodica comporta la rottura e la riformazione di legami chimici. L energia necessaria è dell ordine delle decine di kcal/mole e la trasformazione non è spontanea: si deve eseguire una reazione. La trasformazione di una conformazione molecolare in un altra necessita di energia inferiore alle 10 kcal/mole ed è spontanea. Di conseguenza, ogni molecola otticamente attiva (configurazione definita) presenta anche tutte le conformazioni possibili. 5
6 .. Rappresentazione degli enantiomeri: proiezioni di FISCER La configurazione del C* negli enantiomeri può essere rappresentata mediante proiezioni di Newman, a cavalletto e di aworth. Oltre ad esse, ed esclusivamente per le molecole a catena aperta, sono utilizzate le proiezioni di Fischer: la posizione nello spazio dei legami (con i relativi sostituenti) che si dipartono da un C* è rappresentata da un croce disegnata rispettando le seguenti condizioni: 1. La catena più lunga deve essere disegnata in verticale 2. il gruppo più ossidato deve essere disegnato in alto. le braccia verticali della croce (catena più lunga) rappresentano legami che si prolungano dietro al foglio di proiezione. le braccia orizzontali della croce rappresentano legami che si protendono verso l osservatore Carbonio asimmetrico * C C 2 C C 2 C -metilesano C 2 C Proiezioni di Fischer C 2 5 nc 7 C C Immagini speculari non sovrapponibili Coppia di enantiomeri C 2 5 nc 7 Per paragonare due proiezioni di Fischer si deve tentare di sovrapporle senza staccarle dal foglio di proiezione. Se sono sovrapponibili: stessa molecola Se non sono sovrapponibili: coppia di antipodi 6
7 ..1. Confronto tra proiezioni di Fischer Talvolta le proiezioni di F. sono ambigue (es.: in mancanza di un sostituente con stato di ossidazione > degli altri) e lo stesso antipodo può essere proiettato in modi diversi. Per riconoscere se 2 diverse proiezioni di F. della stessa molecola corrispondono allo stesso enantiomero o ad enantiomeri diversi, si eseguono scambi successivi dei sostituenti (a coppie) fino a raggiungere la sovrapponibilità delle 2 proiezioni: a. se il numero di scambi necessario è pari le 2 proiezioni rappresentano lo stesso enantiomero: un numero pari di scambi genera una diversa proiezione dello stereoisomero di partenza b. se il numero di scambi necessario è dispari le 2 proiezioni rappresentano 2 diversi enantiomeri: un numero dispari di scambi genera la proiezione dell antipodo dello stereoisomero di partenza Es.: determinare le relazioni di stereoisomeria tra i composti 1, 2 e. 2 si trasforma in con un numero dispari di scambi: 2 e sono tra loro enantiomeri 1 si trasforma in 2 con un numero pari di scambi: 1 e 2 sono due diverse proiezione dello stesso enantiomero 7
8 .5. Nomenclatura degli enantiomeri : configurazioni assolute dei C* Per assegnare un nome ai C* è necessario nominare la configurazione del C*. Tale configurazione può essere RELATIVA (più avanti nel corso) o ASSOLUTA L assegnazione della configurazione assoluta ai C* si esegue, utilizzando le lettere R e S, in base alle regole di Ingold e Prelog: 1. Eseguire una lista di priorità dei sostituenti legati direttamente (primo legame) al C* in base al numero atomico crescente < C < N < O < F < P <S < Cl < Br < I Br > O > C > priorità crescente Es.: C Br C O priorità Se la prima regola lascia delle ambiguità, eseguire la stessa operazione sui secondi legami (e così di seguito) fino a trovare una lista di priorità senza ambiguità. Es.: quale dei 2 gruppi C(C ) 2 o C 2 -C(C ) ha > priorità? a C a C b C* C C b C* C C C c 1 legame (rosso): C 2 legame (blu): C, C, c C 1 legame (rosso): C 2 legame (blu): C,, Il gruppo C(C ) 2 ha > priorità 8
9 N.B.: per l assegnazione delle priorità, legami multipli si considerano (formalmente) doppiamente sostituiti per ciascuno degli atomi coinvolti C C C C 2 C C C 2 C C C C C C C C C C C ; ; N C C C N C C N N C C C O O C C O C Tabella delle priorità più comuni. Orientare il C* al centro di una proiezione di Newmann in modo che il sostituente a priorità minore () sia dietro. Osservare il senso di rotazione dello sguardo nello spostamento dal sostituente a priorità maggiore (1) verso quello a priorità più bassa (): a) se il senso di rotazione è orario: la configurazione assoluta del C* è R (dal latino rectus) b) se il senso di rotazione è anti-orario: la configurazione assoluta del C* è S (dal latino sinister) 9
10 Es.: assegnare la configurazione assoluta all enantiomero del 2,2,-trimetilpentano indicato in proiezione a cavalletto: C C C C 2 C C 2 C C C t. Bu C 2 C C 2 1 a. lista di priorità : < C < C 2 -C < t.bu b. Proiezione di Newmann con dietro c. Si osserva rotazione oraria: la configurazione assoluta del C* è R d. Il nome dell enantiomero è: 2,2,R-trimetilpentano t.bu C C 2 C 10
11 .6. Diastereoisomeri, epimeri e mesoforme Cosa succede se in una molecola c è più di un carbonio asimmetrico? Con 2 C* : entrambi i C* possono avere configurazione S (R nell antipodo), oppure un C* può avere configurazione S e l altro R. Complessivamente: Con 2 C* S,S ; R,R + S,R ; R,S coppia di antipodi coppia di antipodi stereoisomeri totali divisi in 2 coppie di antipodi. Le 2 coppie di antipodi non hanno nessuna relazione di specularità tra loro e si definiscono DIASTEREOISOMERE In generale: si definiscono DIASTEREOISOMERI gli stereoisomeri che non sono immagini speculari l uno dell altro (es.: S,S e S,R) (vedi slides 2 e di lezione ) I DIASTEREOISOMERI hanno proprietà chimiche e fisiche diverse tra loro: sono facilmente separabili con i normali metodi chimico-fisici. Quando 2 (o più) diastereoisomeri differiscono tra loro per la configurazione di un solo C* si dicono EPIMERI (es.: S,S e S,R sono diastereoisomeri ed epimeri) Pertanto: i 2 antipodi della coppia (S,S ; R,R) non sono separabili tra loro (come i 2 antipodi della coppia (S,R ; R,S)), ma la coppia (S,S ; R,R) è separabile dalla coppia di antipodi diastereoisomerici (in particolare, epimerici) (S,R ; R,S). 11
12 Estendiamo l analisi del numero di stereoisomeri possibili ad una molecola con C* Con C* S,S,S ; R,R,R + S,S,R ; R,R,S + S,R,S ; R,S,R + S,R,R ; R,S,S coppia di antipodi coppia di antipodi coppia di antipodi coppia di antipodi 8 stereoisomeri totali divisi in coppie di antipodi tra loro DIASTEREOISOMERE Regola generale: il n massimo di stereoisomeri possibili per una molecola con nc* è dato dalla relazione N max ster = 2 n 12
13 Nomenclatura dei DIASTEREOISOMERI a. nelle molecole cicliche i diastereoisomeri sono identificabili mediante i prefissi cis- e trans- (nelle rappresentazioni planari o nelle proiezioni di aworth). Es. I nomi trans--metil-etilcicloesano e cis--metil-etilcicloesano indicano molecole rappresentabili in due modi, ognuno dei quali costituisce uno dei due possibili antipodi della molecola: 1 1 trans--metil-etilcicloesano oppure 1 1 enantiomero 1S,S enantiomero 1R,R 1 cis--metil-etilcicloesano 1 oppure 1 1 enantiomero 1S,R enantiomero 1R,S 1
14 b. nelle molecole a catena aperta i diastereoisomeri sono identificabili mediante i prefissi sin- e anti- (nelle proiezioni di Noyori : catena più lunga distesa a zig-zag sul piano del foglio e sostituenti orientati verso l osservatore o dalla parte opposta). (S) (S) (R) (R) (S) (R) (R) (S) anti-,-dimetileptano coppia di antipodi Molecole a catena aperta con più di un centro chirale sono rappresentabili anche mediante proiezioni di Fischer. Le Proiezioni di Fischer si eseguono utilizzando una croce a più braccia: tante braccia quanti sono i centri chirali Nel caso dell utilizzo di proiezioni di Fischer, non si usano i prefissi sin e anti, ma solo i simboli R e S (configurazioni assolute dei centri chirali). sin-,-dimetileptano coppia di antipodi C 2 5 S,S-dimetilesano C (S) (S) C 2 5 C S,6S-dimetilottano C (S) (S) C 2 C 2 C C C 2 5 C (C 2 ) 2 C 2 5 C 2 5 C 2 5 1
15 Le MESOFORME Se, pur in presenza di C*, si verificano (in uno o più stereoisomeri) situazioni di simmetria interna alla molecola, viene a cadere la condizione necessaria per l enantiomeria. Pertanto, tali stereoisomeri si definiscono MESOFORME e non sono otticamente attivi. In presenza di mesoforme, il n massimo di stereoisomeri calcolato in base al n di atomi di C* non coincide con il n reale. Il n reale è inferiore a quello calcolato. Es.: quanti stereoisomeri reali ha il,-dimetilesano? In teoria: 2C*= 2 2 = (n massimo) C 2 * C C C C C * C 2 C C C C C piano di simmetria C C C C e D sono sovrapponibili e sono una unica mesoforma (C) che è otticamente inattiva ed è separabile dalla miscela A+B Gli stereoisomeri reali totali sono D C A B A+B è una miscela racemica di antipodi non separabili tra loro, ma separabili da C (diastereoisomero ed epimero). Qualora separati, con metodi che vedremo più avanti, A e B sarebbero otticamente attivi. C Le configurazioni assolute (R,S) delle mesoforme non si assegnano: si usa il prefisso meso. Es.: C=D= meso-,- dimetilesano Le configurazioni assolute (R,S) dei C* nei diastereoisomeri otticamente attivi si assegnano per ogni singolo C*. Es.: A= S,S-dimetilesano; B= R,R-dimetilesano 15
16 Altro esempio: stereoisomeri dello 1,-dietilcicloesano (S) 1 (S) (R) 1 trans - 1, - dietilcicloesano coppia di antipodi (R) 1 piano di simmetria cis - 1, - dietilcicloesano mesoforma
17 .7. Reazioni in cui si formano carboni asimmetrici A. In qualsiasi reazione in vitro tra reagenti simmetrici in cui si formino 1 o più C* si ottengono tutti i possibili diastereoisomeri (in % diverse) costituiti da miscele racemiche (inseparabili) di antipodi ottici. C C 2 C 2 C non contiene C * è simmetrico * C C C 2 C Cl coppia di antipodi: sistema simmetrico + Cl 2 reagente simmetrico reagente simmetrico * Si è formato un C * : C C C 2 C + Cl 1 coppia di antipodi R, S Cl sistema simmetrico * * + Cl 2 C C C C + Cl Cl Cl Si è formato un secondo C * : stereoisomeri costituiti da 2 coppie di antipodi S, S;R, R + S, R;R, S( meso ) sistema simmetrico N.B.: il carbonio che ha subito la reazione che ha generato il C* si definisce stereogenico. 1 Regola: nelle reazioni tra reagenti simmetrici si generano sempre prodotti simmetrici cioè, la simmetria dei reagenti si trasmette ai prodotti B. In qualsiasi reazione in vitro in cui almeno uno dei reagenti è asimmetrico (cioè è un singolo enantiomero) e in cui si formino nuovi C* si ottengono i possibili diastereoisomeri in forma otticamente attiva (R) C C C 2 C (R) (R) + Cl 2 C C C C (R) (S) + C C C C + Cl Cl 1 solo antipodo (otticamente attivo): sistema asimmetrico reagente simmetrico Cl Cl Cl Cl 2 diastereoisomeri, entrambi otticamente attivi 2 Regola: nelle reazioni in cui almeno uno dei reagenti sia asimmetrico si generano sempre prodotti asimmetrici cioè, la asimmetria dei reagenti si trasmette ai prodotti Le sostanze naturali (es. carboidrati, amminoacidi) sono costituite da singoli antipodi puri: in base alla regola 2, i loro precursori devono essere asimmetrici (antipodi puri). Risalendo all indietro nella catena di reazioni che hanno dato origine alle sostanze naturali, quando e come si è formato il primo antipodo puro, cioè la prima asimmetria? Il problema è ancora aperto. 17
18 .8. RELAZIONE TRA PROIEZIONI DI NOYORI E DI FISCER Le proiezioni di Noyori rappresentano la molecola con la catena più lunga a zig-zag (come se fosse in conformazione tutta anti ) mentre le proiezioni di Fischer la rappresentano come se fosse in conformazione tutta eclissata. La trasformazione di una Noyori in una Fischer è complicata: (S) (S) (S) (S) proiezione di Noyori del S,S-dimetileptano legame, ruotato per portare in eclisse la catena più lunga C Pr proiezione a cavalletto C C Pr C proiezione di Fischer in questo corso useremo solo proiezioni di Fischer.
19 I seguenti aspetti applicativi verranno trattati durante le esercitazioni: 1. come assegnare la configurazione assoluta ad uno (o più) C* a partire dalle proiezione di Fischer 2. come eseguire la proiezione di Fischer di uno (o più) C* nota la configurazione assoluta. come assegnare la configurazione assoluta ai singoli C* in molecole cicliche. come trasformare una proiezione di Fischer in una a cavalletto 5. come trasformare una proiezione a cavalletto in una Fischer Le slides successive riportano materiale esplicativo preliminare alle esercitazioni 19
20 1. Assegnazione della configurazione assoluta ad uno (o più) C* a partire dalla proiezione di Fischer Utilizziamo, come esempio, gli stereoisomeri del,-dimetilesano C C C C C C C di A C C C Eseguire un n pari di scambi per portare il sostituente a priorità minore "in basso" (ciò corrisponde ad averlo "dietro" nella proiezione di Newmann) A C 1 scambio C B 2 scambio C C C C (mesoforma) C osservare la direzione di rotazione dello sguardo ed assegnare la configurazione assoluta C C di A C C C C 1 scambio 2 scambio C Eseguire le stesse operazioni Lo stereoisomero A è il S,S-dimetilesano configurazione S C C C configurazione S Lo stereoisomero B è obbligatoriamente il R,R-dimetilesano. Non ha senso assegnare le config. alla forma meso C: si nomina come meso-,- dimetilesano 20
21 2. Ottenimento della proiezione di Fischer di uno (o più) C* nota la configurazione assoluta Eseguire la proiezione di Fischer del 2,R,S-trimetil--etilesano 2 R S i.pr R S C: disegnare la croce di Fischer e porre il sostituente a priorità minore in basso disporre gli altri sostituenti in senso orario (R) dalla priorità maggiore verso la minore C i.pr C C eseguire un numero pari di scambi per portare in verticale la catena più lunga C i.pr C i.pr C C i.pr C C proiezione del C C i.pr C C: eseguire la stessa sequenza i.pr C C Pr.i C C Pr.i C C Proiezione complessiva proiezione del C 21
22 . Assegnazione della configurazione assoluta ai C* in molecole cicliche 1. Utilizzare proiezioni di aworth e, tramite rotazione sul piano del ciclo, portare il C* da assegnare sulla posizione estrema destra (o sinistra) 2. considerare i 2 sostituenti del C* giacenti sul piano del foglio. evidenziare i legami del ciclo con i simboli e se diretti rispettivamente dietro o davanti al piano del foglio.. se nel C* da assegnare il sostituente a minore priorità si trova sotto, eseguire una proiezione di Newmann osservando da sopra ed assegnare la configurazione. direzione di osservazione 5. se nel C* da assegnare il sostituente a minore priorità si trova sopra, eseguire uno scambio ed assegnare la configurazione come nel punto 5. Poi cambiare la lettera. C C 2 S direzione di osservazione C C C C 2 S R C 2 C 1 2 C La molecola in esempio è lo 1S,2S-dimetilciclopropano C C C 2 scambio 1 2 C C C C C
23 Altro esempio: direzione di osservazione C C 2 R C C 2 C C 1 C C 2 configurazione del C1 1 C C C 2 Il nome dello stereoisomero è 1R,Rdimetilcicloesano C 1 configurazione del C C 2 scambio al C direzione di osservazione C C C 2 C 1 C 2 C 2 C C S R N.B.: il metodo consigliato è solo uno dei possibili. Il punto fondamentale è che la direzione di osservazione dei vari C* della molecola sia sempre la stessa: o sempre da sopra o sempre da sotto. C rotazione sul piano del ciclo 2
24 . Trasformazione di una proiezione di Fischer in una a cavalletto Per definizione, i sostituenti posti in verticale nella Fischer sono orientati dietro al foglio, mentre i sostituenti in orizzontale si dirigono verso l osservatore. Pertanto, guardando la Fischer da sopra, i sostituenti in orizzontale si dirigono in alto, mentre quelli in verticale vanno sotto. In definitiva una Fischer corrisponde ad una cavalletto eclissata in cui i sostituenti che sono in verticale nella Fischer puntano verso il basso. N.B.: nel passaggio Fischer/Cavalletto si rischia di disegnare l enantiomero della molecola assegnata. Per non commettere errori è bene abituarsi a seguire sempre lo stesso criterio: es. far corrispondere sempre il C* in alto nella Fischer con quello di destra nella cavalletto. C C S,S-dimetilesano C conformazione eclissata (poco popolata) C C C conformazione sfalsata (molto popolata) N.B.: nel passaggio eclissata/sfalsata è fondamentale mantenere la configurazione dei C*, cioè, nell esempio, la rotazione oraria nella sequenza --C legati al C e la rotazione antioraria nella sequenza --C legati al C 2
25 5. Trasformazione di una proiezione a cavalletto in una di Fischer Si esegue al contrario la sequenza descritta al punto. 1. Mantenendo le configurazioni dei C*, convertire la cavalletto assegnata nella corrispondente eclissata con la catena più lunga rivolta verso il basso 2. trasformare la cavalletto eclissata nella Fischer curando che: a. il C* di destra nella cavalletto diventi quello in alto nella Fischer b. i sostituenti di sotto nella cavalletto vadano in verticale nella Fischer. C cavalletto assegnata conformazione sfalsata (molto popolata) C C C conformazione eclissata (poco popolata) C C Fischer corrispondente 25
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
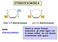 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
ISOMERIA. Isomeri di struttura O OH C 4 H 10 O C 4 H 10
 ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
CONTENUTI DELLA LEZIONE:
 Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria :
 Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
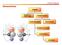 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
02/10/2018. di catena. di posizione. strutturali. di gruppo funzionale. isomeri. geometrici. stereoisomeri. ottici
 Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
28/03/2013. Stereochimica: enantiomeri
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
Diagramma che riassume i diversi tipi di isomeri. N.B. Gli isomeri costituzionali (o isomeri di struttura: es. n-propile /isopropile non sono
 STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
La isomeria in Chimica Organica
 La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
3. Cicloalcani. Formula generale: C n H 2n in serie omologa C 9 C 10 C 11 C 12 >C 12. Es.: 1,1-dimetilciclopropano. Anelli. piccoli. Anelli.
 . Cicloalcani Formula generale: C n 2n in serie omologa ciclopropano ciclobutano ciclopentano Anelli piccoli C 9 C 10 C 11 C 12 cicloottano ciclononano ciclodecano cicloundecano ciclododecano Anelli medi
. Cicloalcani Formula generale: C n 2n in serie omologa ciclopropano ciclobutano ciclopentano Anelli piccoli C 9 C 10 C 11 C 12 cicloottano ciclononano ciclodecano cicloundecano ciclododecano Anelli medi
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
ISOMERI. Stereoisomeri. Isomeri Cos/tuzionali. Conformeri. Geometrici. configurazionali. Enan/omeri. Diastereoisomeri
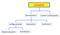 ISOMEI Stereoisomeri Isomeri Cos/tuzionali configurazionali Geometrici Conformeri Diastereoisomeri Enan/omeri Chiralità Dato un Piano di iflessione ( specchio ) è possibile o=enere per qualunque ogge=o
ISOMEI Stereoisomeri Isomeri Cos/tuzionali configurazionali Geometrici Conformeri Diastereoisomeri Enan/omeri Chiralità Dato un Piano di iflessione ( specchio ) è possibile o=enere per qualunque ogge=o
Come scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer
 ome scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer Supponiamo di dover disegnare, usando la rappresentazione tridimensionale
ome scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer Supponiamo di dover disegnare, usando la rappresentazione tridimensionale
Elementi di Stereochimica
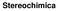 Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica.
 Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2012/2013 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2012/2013 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente
 Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
ISOMERIA. Isomeri costituzionali. Stereoisomeri. Nomenclatura. Importanza biologica della chiralità
 ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
CONTENUTI DELLA LEZIONE DI OGGI:
 CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Un oggetto si definisce chirale se non è sovrapponibile alla. propria immagine speculare (mano destra e mano sinistra). Non
 Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
Altre tecniche analitiche ottiche: rifrattometria e polarimetria
 Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
Altre tecniche analitiche ottiche: rifrattometria e polarimetria Come abbiamo già visto nel primo paragrafo la luce, quando cambia mezzo di propagazione, subisce una deviazione. Questo fenomeno viene detto
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
STEREOISOMERIA carbonio ibridizzato sp3 è legato a quattro atomi o gruppi tutti diversi fra loro
 STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Idrocarburi Saturi. Cicloalcani
 Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Stereochimica. Molecole nello spazio
 Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
CHIMICA ORGANICA I - laboratorio AA 2009/10
 CIMICA ORGANICA I - laboratorio AA 2009/10 Esperienza 1 Costtrruziione dii MODELLII MOLECOLARII La conoscenza della struttura tridimensionale delle molecole è un elemento chiave per la comprensione delle
CIMICA ORGANICA I - laboratorio AA 2009/10 Esperienza 1 Costtrruziione dii MODELLII MOLECOLARII La conoscenza della struttura tridimensionale delle molecole è un elemento chiave per la comprensione delle
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata CHO
 Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie
 1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
Capitolo 15 O C H CH 2 OH. Risposte a Domande ed esercizi di fine capitolo. Tipi di carboidrati
 apitolo 15 Risposte a Domande ed esercizi di fine capitolo Tipi di carboidrati 15.1 Un monosaccaride è lo zucchero più semplice e consiste di una singola unità saccaridica. Un disaccaride è formato da
apitolo 15 Risposte a Domande ed esercizi di fine capitolo Tipi di carboidrati 15.1 Un monosaccaride è lo zucchero più semplice e consiste di una singola unità saccaridica. Un disaccaride è formato da
Configurazione. Conformazione
 Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Idrocarburi Alifatici
 Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
Fondamenti di chimica organica Janice Gorzynski Smith Copyright 2009 The McGraw Hill Companies srl
 Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
Reazioni Stereospecifiche e Stereoselettive
 Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della luce p
 POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
POLARIMETRIA Obiettivi: imparare ad usare un polarimetro POLARIMETRIA La polarimetria è un metodo di analisi non distruttivo che si basa sulla capacità delle molecole chirali di deviare il piano della
Parametri da cui dipendono le costanti di accoppiamento
 Parametri da cui dipendono le costanti di accoppiamento 2 J: può essere negativa o positiva 2 J 12-15 z se Csp 3 ; 2-4 z se Csp 2 Metodi Fisici in Chimica Organica - NMR 3 J: è di solito positiva a) angolo
Parametri da cui dipendono le costanti di accoppiamento 2 J: può essere negativa o positiva 2 J 12-15 z se Csp 3 ; 2-4 z se Csp 2 Metodi Fisici in Chimica Organica - NMR 3 J: è di solito positiva a) angolo
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Carboidrati semplici
 arboidrati semplici ontenuti della lezione: Monosaccaridi aldosi e chetosi Proiezioni di Fischer La reattività dei monosaccaridi: formazione di emiacetaliciclici, ossidazione ad acidi aldonici, riduzione
arboidrati semplici ontenuti della lezione: Monosaccaridi aldosi e chetosi Proiezioni di Fischer La reattività dei monosaccaridi: formazione di emiacetaliciclici, ossidazione ad acidi aldonici, riduzione
 La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
La prova di Fisher La ricerca di Emil Fisher che permise di chiarire la stereochimica del (+)-glucosio (cioè di chiarire in che modo sono orientati i gruppi funzionali attorno ai carboni chirali dello
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
La Chimica Organica idrogeno carbonio azoto ossigeno composti covalenti catene di atomi di carbonio strutture covalenti e debolmente polarizzate
 LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
Stereochimica di alcani e cicloalcani
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
LABORATORIO DI FISICA 4 relazione: Saccarometria. De Mauro Giuseppe, Degradi Pablo, Restieri Andrea
 LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
LABORATORIO DI FISICA 4 relazione: Saccarometria De Mauro Giuseppe, Degradi Pablo, Restieri Andrea Scopo dell'esperienza determinare il potere rotatorio specifico del saccarosio Materiale utilizzato e
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
le reazioni chimiche asimmetriche
 Struttura molecolare e chiralità: le reazioni chimiche asimmetriche Lezioni d'autore Un video : Clic Chiralità (I) I termini chirale e chiralità, entrambi derivati dal greco χείρ (mano), sono comuni nella
Struttura molecolare e chiralità: le reazioni chimiche asimmetriche Lezioni d'autore Un video : Clic Chiralità (I) I termini chirale e chiralità, entrambi derivati dal greco χείρ (mano), sono comuni nella
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Tutor per gli studenti di Farmacia, CTF, e Ing. Chim.: Dott. Simone Serrao
 Testi adottati: - Nelson e Cox, I principi di Biochimica di Lehninger (V o VI ed.) Zanichelli - Horton, Moran, Scrimgeour, Perry, Rawn, Principi di biochimica (IV ed.) Pearson-Prentice Hall (2008). - Voet,
Testi adottati: - Nelson e Cox, I principi di Biochimica di Lehninger (V o VI ed.) Zanichelli - Horton, Moran, Scrimgeour, Perry, Rawn, Principi di biochimica (IV ed.) Pearson-Prentice Hall (2008). - Voet,
c. Disegnate le conformazioni eclissate e sfalsate intermedie
 1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
ALCANI. C n H 2n+2 CH 3 CH 2 CH 2 CH 2 CH 2 CH 3. alcani lineari. alcani ramificati. Cap. 2
 ALANI n 2n+2 2 2 2 2 alcani lineari alcani ramificati ap. 2 1-4 5-10 10-16 15-20 ONFORMAZIONI DEGLI ALANI Ruotando attorno al legame - si individuano alcune posizioni relative dei tetraedri ALTERNATA (SFALSATA)
ALANI n 2n+2 2 2 2 2 alcani lineari alcani ramificati ap. 2 1-4 5-10 10-16 15-20 ONFORMAZIONI DEGLI ALANI Ruotando attorno al legame - si individuano alcune posizioni relative dei tetraedri ALTERNATA (SFALSATA)
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Alcani e Cicloalcani
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
7.9 Reazioni che introducono un centro Stereogenico
 7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
pentosi ed esosi aldosi e chetosi monosaccaridi carboidrati di, tri, tetra saccaridi oligosaccaridi polisaccaridi amido glicogeno cellulosa
 I carboidrati sono composti a base di C, e ; il nome deriva dal fatto che formalmente la formula è (C. 2 ) 6, da cui carboidrati = idrati di carbonio. Si tratta in tutti i casi di poliidrossialdeidi o
I carboidrati sono composti a base di C, e ; il nome deriva dal fatto che formalmente la formula è (C. 2 ) 6, da cui carboidrati = idrati di carbonio. Si tratta in tutti i casi di poliidrossialdeidi o
Alcani. Es. CH 3 CH 2 CH 2 CH 3
 Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
CHIMICA ORGANICA I. Corso di laurea in CHIMICA
 IMIA RGANIA I orso di laurea in IMIA Esercitazione n. 6 - Esercitazione sulla stereoisomeria ottica. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Molecole simmetriche e dissimmetriche.
IMIA RGANIA I orso di laurea in IMIA Esercitazione n. 6 - Esercitazione sulla stereoisomeria ottica. TERMINI ED ARGMENTI PER L SVLGIMENT DEGLI ESERIZI DI QUEST FGLI: Molecole simmetriche e dissimmetriche.
GEOMETRIA MOLECOLARE. Ibridazione La teoria VSEPR
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
12 ESERCITAZIONE A B A+B C+D
 12 ESERCITAZIONE 1. Preparare l enolato cinetico del 2-butanone ed addizionarlo ai seguenti substrati: a) propenoato di metile; b) E-butenoato d etile; c) 1-carboetossicicloesene. Indicare meccanismo e
12 ESERCITAZIONE 1. Preparare l enolato cinetico del 2-butanone ed addizionarlo ai seguenti substrati: a) propenoato di metile; b) E-butenoato d etile; c) 1-carboetossicicloesene. Indicare meccanismo e
Carboidrati. Da un punto di vista della struttura chimica, i carboidrati sono poliidrossi-aldeidi o poliidrossi-chetoni
 Carboidrati C n ( ) m Da un punto di vista della struttura chimica, i carboidrati sono poliidrossi-aldeidi o poliidrossi-chetoni monosaccaridi:, fruttosio, galattosio, mannosio disaccaridi: saccarosio,
Carboidrati C n ( ) m Da un punto di vista della struttura chimica, i carboidrati sono poliidrossi-aldeidi o poliidrossi-chetoni monosaccaridi:, fruttosio, galattosio, mannosio disaccaridi: saccarosio,
Gli elettroni della molecola sono quindi descritti da
 IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Introduzione alla Simmetria Molecolare
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Introduzione alla Simmetria Molecolare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Introduzione alla Simmetria Molecolare Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/general-chemistry-lessons/
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Centri chirali specchio
 entri chirali L atomo centrale ha ibridazione sp 3 ed è legato a quattro sostituenti diversi, esso è detto carbonio chirale. Esiste, un altra molecola nella quale gli stessi atomi sono legati all atomo
entri chirali L atomo centrale ha ibridazione sp 3 ed è legato a quattro sostituenti diversi, esso è detto carbonio chirale. Esiste, un altra molecola nella quale gli stessi atomi sono legati all atomo
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DI COMPOSTI CHIRALI Anno accademico 2013/2014 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
