Stereochimica. Molecole nello spazio
|
|
|
- Gennara Repetto
- 10 anni fa
- Просмотров:
Транскрипт
1 Stereochimica Molecole nello spazio
2 Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri conformazionali: si interconvertono per rotazione attorno a un legame. Stereoisomeri configurazionali: non possono interconvertirsi senza rompere legami: Enantiomeri: stereoisomeri che sono immagini speculari non sovrapponibili. Diastereomeri: stereoisomeri che non sono immagini speculari.
3 Sì A vs B Stessa formula molecolare? No I modelli di A e B sono sovrapponibili? Sì No Non c è relazione tra A e B A e B sono identici Sì A e B sono isomeri No E TIPO DI ISOMERI? A e B differiscono per la rotazione attorno a un legame? A e B sono isomeri conformazionali Sì A e B hanno la stessa formula condensata? No A e B sono stereoisomeri A e B sono isomeri strutturali A e B sono immagini speculari? Sì A e B sono enantiomeri No A e B sono diastereoisomeri
4 Isomeri conformazionali Sono strutture che risultano dalla libera rotazione attorno a un legame singolo. Possono differire in energia. Prevale il conformero a energia più bassa. Le molecole ruotano costantemente attraverso tutte le conformazioni possibili.
5 onformazioni limite dell etano 3-3 staggered sfalsata eclissata Proiezioni di Newman
6 Etano torsional strain Torsional strain: la forza che si oppone alla rotazione di una parte della molecola per portarla in eclissamento. L eccesso di energia presente nella conformazione eclissata.
7 Propano Strain torsionale: 3.3 kcal/mole per il maggior ingombro del metile (rispetto all idrogeno nell etano)
8 Butano
9 Energie relative E 5 5 sin Kcal/mol eclissato sin 3 2 gauche gauche 0 anti anti
10 Stereoisomeria onfigurazionale
11 hiralità Oggetti che non sono sovrapponibili alla loro immagine speculare sono detti chirali. Oggetti che sono sovrapponibili alla loro immagine speculare sono detti achirali. Un oggetto achirale ha almeno un elemento di simmetria.
12 hiralità La molecola non è sovrapponibile alla sua immagine speculare: èchirale La mano destra non è sovrapponibile alla mano sinistra, che è la sua immagine speculare
13 Piano di simmetria Piano di simmetria Nessun piano di simmetria Acido propanoico (achirale) Acido lattico (chirale)
14 Enantiomeri Acido lattico O O O 3 O 3 O O
15 Enantiomeri 3-clorocicloesene l l l
16 Enantiomeri 2-butanolo
17 arbonio stereogenico o stereocentro Un carbonio stereogenico è tetraedrico (sp 3 ) ed ha quattro sostituenti diversi: l l F Br F Br Una molecola chirale ha uno stereocentro, è dissimmetrica. Esiste in due forme, immagini speculari non sovrapponibili, che formano una coppia di enantiomeri (isomero destro e sinistro).
18 Attività ottica Leproprietà fisiche degli enantiomeri sono identiche (punto di ebollizione, punto di fusione, densità, indice di rifrazione, etc.) tranne che per la direzione in cui ruotano il piano della luce piano polarizzata. Gli enantiomeri sono isomeri ottici.
19 Tipi di luce Luceordinariaconsiste di onde che vibrano in tutti i piani perpendicolari alla direzione di propagazione. Luce piano polarizzata consiste di onde che vibrano in un solo piano. pianopolarizzata
20 Polarimetro È lo strumento che misura il grado di rotazione del piano della luce piano polarizzata. destrorotatorio (+) otticamente attivo levorotatorio ( ) otticamente attivo otticamente inattivo
21 Attività ottica omposto otticamente inattivo: a. molecola achirale b. miscela racema, (±), miscela 50/50 dei due enantiomeri omposto otticamente puro: 100% di un enantiomero Purezza ottica (eccesso enantiomerico, e.e.) = percento di un enantiomero percento dell altro es. 80% di un enantiomero e 20% dell altro = 60% e.e. o purezza ottica
22 Attività ottica Rotazione specifica [ α] T D temperatura rotazione osservata (º) [α] T D = α cl cammino ottico (dm) riga D del sodio concentrazione (g/ml soluzione) 27 es. (+)-2-butanolo [α] = º D ( )-2-butanolo 13.5º La rotazione specifica calcolata in questo modo è una proprietà fisica caratteristica di ogni composto otticamente attivo.
23 Rotazioni specifiche di composti bioattivi OMPOSTO [α] D T colesterolo 31.5 cocaina 16 morfina 132 codeina 136 eroina 107 epinefrina 5.0 progesterone testosterone saccarosio β-d-glucosio α-d-glucosio + 112
24 onfigurazioni R e S R e S sono due descrittori che definiscono la configurazione di uno stereocentro attraverso un set di regole. 2-butanolo 3 O O Tale assegnazione non dice quale enantiomero è destrogiro e quale levogiro. Non c è relazione tra la configurazione assoluta di una molecola e il segno della sua rotazione ottica. R ( ) (+) S
25 onvenzione R,S Regole di Priorità (ahn, Ingold, Prelog) Ad ogni atomo legato direttamente allo stereocentro viene assegnata una priorità, sulla base del numero atomico. Più alto è il numero atomico, più alta la priorità N 2 O S l Br I Priorità crescente
26 onvenzione R,S Se non si può assegnare una priorità sulla base del numero atomico dell atomo legato allo stereocentro, si va al set di atomi successivi. La priorità viene assegnata alla prima differenza N 2 2 O Priorità crescente
27 onvenzione R,S Gli atomi che possiedono doppi o tripli legami sono considerati legati ad un numero equivalente di atomi simili con legami singoli. O = O O
28 onvenzione R,S Assegnare la priorità ai quattro sostituenti secondo le Regole di Priorità. Orientare la molecola in modo che il gruppo a priorità più bassa sia lontano dall osservatore. Determinare la direzione di precessione degli altri tre gruppi cominciando da quello con la massima priorità: senso orario = R (rectus) senso antiorario = S (sinister)
29 onvenzione R,S senso orario senso antiorario il sostituente a minor priorità viene posto dietro 3 R (rectus) 3 S (sinister)
30 onvenzione R,S O Et 3 O (R)-2-butanolo O 1 Et O 3 (S)-2-butanolo
31 onvenzione R,S O OO acido (R)-( )-lattico OO O 1 3 acido (S)-(+)-lattico
32 Proiezioni di Fischer A A A D B = D B = D B
33 Proiezioni di Fischer Determinare R e S nelle proiezioni di Fischer 3 O O 2 3 (R)-2-butanolo quando il gruppo a priorità minore è sulla verticale (legame dietro): leggere normalmente (S)-2-butanolo quando il gruppo a priorità minore è orizzontale (legame davanti): leggere all indietro (o leggere normalmente e invertire R con S)
34 Proiezioni di Fischer l Br catena principale in rosso 3 l 3 3 ruotare di 90 o orientare la catena principale verticalmente Br 3 l 3 l 3 Br convertire nella proiezione di Fischer Br 3
35 Proiezione di Fischer orientazione della catena principale e dei sostituenti nella proiezione di Fischer 3 O O 3 O O O 3 3 O
36 Regole di Fischer La catena carboniosa sta sulla linea verticale. Il carbonio più ossidato sta in alto. O 3 < 2 O < < O < OO =O Una rotazione di 180 nel piano non cambia la molecola. Non ruotare di 90! Non ruotare fuori dal piano!
37 omposti con due o più stereocentri Diastereomeri o diastereoisomeri: stereoisomeri che non sono immagini speculari. I diastereomeri hanno differenti proprietà fisiche. n carboni chirali 2 n possibili stereoisomeri
38 omposti con due stereocentri es. 3 3 O Br 2 2 = 4 possibili stereoisomeri 3 3 Br Br 3 Br Br 3 O O O O enantiomeri enantiomeri diastereomeri
39 omposti con due stereocentri Diastereomeri: coppie di enantiomeri eritro e treo A A A A B B B B ' B' B' ' B' ' ' B' A' A' A' A' diastereomero eritro diastereomero treo
40 omposti con più stereocentri 3 carboni chirali 2 3 = 8 possibili stereoisomeri R, R, R : S, S, S R, R, S : S, S, R R, S, R : S, R, S S, R, R : R, S, S diastereomeri enantiomeri
41 omposti con due o più stereocentri uguali: composti meso ontengono carboni chirali ma sono achirali 3 3 Br Br 2 2 = 4 possibili stereoisomeri 3 3 Br Br 3 treo Br 3 3 Br 3 Br Br eritro Br Br 3 3 piano di simmetria enantiomeri stesso composto meso diastereomeri 3 stereoisomeri
42 Acido tartarico OO OO O O 2 2 = 4 possibili stereoisomeri R R, S S, R S, S R O OO R R O OO treo O enantiomeri otticamente attivi OO S S O OO OO R OO O O S O O R OO OO eritro meso otticamente inattivo S piano di simmetria diastereomeri 3 stereoisomeri
43 Acido tartarico acido ( )-tartarico [α] D = 12.0 pf o solubilità di 1 g 0.75 ml 2 O 1.7 ml metanolo 250 ml etere insolubile in l 3 d = g/ml acido (+)-tartarico [α] D = pf o solubilità di 1 g 0.75 ml 2 O 1.7 ml metanolo 250 ml etere insolubile in l 3 d = g/ml acido meso-tartarico [α] D = 0 pf 140 o solubilità di 1 g 0.94 ml 2 O insolubile in l 3 d = g/ml
44 Stereoisomeria geometrica negli alcheni Notazione cis and trans negli alcheni isomeri geometrici diastereomeri cis-2-butene trans-2-butene la rotazione non è possibile
45 Esempi cis O trans cis O cis trans
46 Stereoisomeri geometrici Notazione E-Z per gli alcheni 1. Determinare la priorità più alta fra i due gruppi di sostituenti sui carboni olefinici, secondo le regole.i.p. 2. Se i gruppi a maggior priorità sono: su lati opposti: E (entgegen = opposto) sullo stesso lato: Z (zusammen = insieme) 3 > l > l l (E)-3-cloro-2-pentene (Z)-3-cloro-2-pentene
47 Notazione E-Z per gli alcheni Regole di Priorità: 1. guardare al primo atomo legato al carbonio del doppio legame 2. maggior numero atomico = maggior priorità 3. se gli atomi sono identici, esaminare l atomo successivo fino alla prima differenza. 4. i legami multipli vanno trattati come 2 o 3 legami singoli < 2 3 < < 3 < 2 l 3 3 (,,) (,,) (,,) (,,) (l,,) 3 > 3 O O = 3 = O 3 (,,;,,) (,,;,,)
48 Esempio Z 1 2 l l l E l (2Z,5E)-3,7-dicloro-2,5-ottadiene
49 Stereoisomeria geometrica Anelli disostituiti negli anelli R R entrambi i sostituenti dalla stessa parte del piano medio dell anello: cis R R sostituenti da parti opposte del piano medio dell anello: trans
50 Esempi 3 3 cis trans
51 Risoluzione di Enantiomeri Enantiomeri: identiche proprietà fisiche; non possono essere separati. Diastereomeri: differenti proprietà fisiche, p.f., p.e., solubilità, etc.; possono essere separati per distillazione, ricristallizzazione, cromatografia, etc.
52 Risoluzione di Enantiomeri A miscela racema R + S + B (R) enantiomero puro (agente risolvente) A B (R,R) + A B (S,R) diastereomeri separazione A B (R,R) A (R) si rimuove B A B (S,R) A (S)
53 Risoluzione di Enantiomeri O O + 2 N l racemo (S) O O l O O 3 N + + (R,S) 1) separazione 2) l l (R) O O l O 3 N + (S,S) l (S) O
54 Risoluzione di Enantiomeri
55 Presenza di molti stereocentri Enantiomeri? Diastereomeri? Meso? Assegnare (R) o (S) a ciascuno stereocentro. Gli enantiomeri hanno configurazione opposta in tutti gli stereocentri corrispondenti. I diastereomeri hanno qualche stereocentro della stessa configurazione, qualche altro di configurazione opposta. I composti meso hanno un piano di simmetria interno che riduce il numero di stereoisomeri. Il numero massimo di stereoisomeri è 2 n, con n = numero di stereocentri.
56 E S O S I allo O manno altro O O O O O O O 2 O O O O O 2 O O O O 2 O glucosio O ido O O O O O O O 2 O O O O O O O 2 O O O 2 O gulo galatto O O O O O O 2 O O O O 2 O ENANTIOMERI tutti gli stereocentri sono stati invertiti DIASTEREOMERI O O O solo alcuni stereocentri sono stati invertiti talo O O 2 O
57 onvenzione di Fischer-Rosanoff Prima del 1951, solo le configurazioni relative potevano essere conosciute. Gli zuccheri e gli ammino acidi con la stessa configurazione relativa della (+)-gliceraldeide furono chiamati D e quelli con la stessa configurazione relativa della ( )-gliceraldeide furono chiamati L (con assegnazione arbitraria). Grazie alla cristallografia a raggi X, ora si conoscono le configurazioni assolute della (+)- e della ( )- gliceraldeide: D è (R) e L è (S). Non c è relazione con il segno della rotazione.
58 Assegnazioni D e L O * O 2 O O a destra D-(+)-gliceraldeide (R)-(+)-gliceraldeide OO 2 N 2 2 OO acido L-(+)-glutammico O O 2 O L-( )-gliceraldeide (S)-( )-gliceraldeide carbonio stereocentro più vicino al meno ossidato O O O O O 2 O D-(+)-glucosio O a sinistra più ossidato in alto meno ossidato in basso
STEREOISOMERIA carbonio ibridizzato sp3 è legato a quattro atomi o gruppi tutti diversi fra loro
 STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
7.4 Proprietà delle Molecole Chirali: Attvità Ottica
 7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
7.4 Proprietà delle Molecole Chirali: Attvità Ottica Una sostanza è attiva otticamente se ruota la luce polarizzata Attività Ottica Affinchè una sostanza esibisca attività ottica, essa deve essere chirale
7.9 Reazioni che introducono un centro Stereogenico
 7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
7.9 eazioni che introducono un centro tereogenico Molte reazioni convertono reagenti achirali a prodotti chirali. E importante ricordare, comunque che se tutti i i componenti iniziali (reagenti, catalizzatori,
Polarimetria. Polarimetria
 Polarimetria Polarimetria La radiazione elettromagnetica viene considerata come una forma di energia radiante dotata di una doppia natura, ondulatoria e corpuscolare. In ogni momento il vettore campo elettrico
Polarimetria Polarimetria La radiazione elettromagnetica viene considerata come una forma di energia radiante dotata di una doppia natura, ondulatoria e corpuscolare. In ogni momento il vettore campo elettrico
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI
 L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
L'ATTIVITA' OTTICA DEI COMPOSTI CHIRALI Nei composti inorganici a ogni formula grezza, che esprime la composizione della molecola, corrisponde una sola formula di struttura. Nei composti organici, invece,
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Chimica organica. Biomolecole. Tessuti biologici. Polimeri proprietà funzioni
 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni 1 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni C O N 1 Chimica organica Biomolecole Tessuti biologici
Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni 1 Chimica organica Biomolecole Tessuti biologici Polimeri proprietà funzioni C O N 1 Chimica organica Biomolecole Tessuti biologici
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
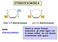 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
STEREOCHIMICA C OH CH 2 CH 3. 180 in questo caso nessuna rotazione è in grado di far sovrapporre perfettamente le due strutture
 TEEIMIA TEEIMEI Due stereoisomeri sono sostanze diverse che hanno in comune sia la formula bruta che la formula di costituzione. osa li rende diversi allora? Una differente orientazione tridimensionale
TEEIMIA TEEIMEI Due stereoisomeri sono sostanze diverse che hanno in comune sia la formula bruta che la formula di costituzione. osa li rende diversi allora? Una differente orientazione tridimensionale
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
La propagazione delle onde luminose può essere studiata per mezzo delle equazioni di Maxwell. Tuttavia, nella maggior parte dei casi è possibile
 Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Diagramma che riassume i diversi tipi di isomeri. N.B. Gli isomeri costituzionali (o isomeri di struttura: es. n-propile /isopropile non sono
 STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
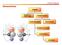 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Elementi di Stereochimica
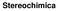 Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Serie completa di Modelli Molecolari per la Chimica Organica
 EdiSES Istruzioni per l utilizzo dei modelli molecolari Serie completa di Modelli Molecolari per la Chimica Organica allegati ai seguenti volumi: Chimica Organica - Paula Y. Bruice Elementi di Chimica
EdiSES Istruzioni per l utilizzo dei modelli molecolari Serie completa di Modelli Molecolari per la Chimica Organica allegati ai seguenti volumi: Chimica Organica - Paula Y. Bruice Elementi di Chimica
Scuola/Classe Cognome Nome Data
 Università di Udine Unità di Ricerca in Didattica della Fisica Scuola/Classe Cognome Nome Data Scheda PotRot Mezzi otticamente attivi Attività A. Riconoscere i mezzi otticamente attivi. Si dispone un puntatore
Università di Udine Unità di Ricerca in Didattica della Fisica Scuola/Classe Cognome Nome Data Scheda PotRot Mezzi otticamente attivi Attività A. Riconoscere i mezzi otticamente attivi. Si dispone un puntatore
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Configurazione. Conformazione
 Configurazione (Mislow,, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: : configurazione opposta Diastereoisomeri: : configurazione diversa
Configurazione (Mislow,, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: : configurazione opposta Diastereoisomeri: : configurazione diversa
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Ragionamento spaziale visivo e percezione
 2 Ragionamento spaziale visivo e percezione Serie e analogie figurali! In alcune batterie di test psicoattitudinali sono ampiamente rappresentati i quesiti che propongono un elenco di figure: in alcuni
2 Ragionamento spaziale visivo e percezione Serie e analogie figurali! In alcune batterie di test psicoattitudinali sono ampiamente rappresentati i quesiti che propongono un elenco di figure: in alcuni
2 FUNZIONI REALI DI VARIABILE REALE
 2 FUNZIONI REALI DI VARIABILE REALE 2.1 CONCETTO DI FUNZIONE Definizione 2.1 Siano A e B due insiemi. Una funzione (o applicazione) f con dominio A a valori in B è una legge che associa ad ogni elemento
2 FUNZIONI REALI DI VARIABILE REALE 2.1 CONCETTO DI FUNZIONE Definizione 2.1 Siano A e B due insiemi. Una funzione (o applicazione) f con dominio A a valori in B è una legge che associa ad ogni elemento
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Teoria in sintesi 10. Attività di sportello 1, 24 - Attività di sportello 2, 24 - Verifica conclusiva, 25. Teoria in sintesi 26
 Indice L attività di recupero 6 Funzioni Teoria in sintesi 0 Obiettivo Ricerca del dominio e del codominio di funzioni note Obiettivo Ricerca del dominio di funzioni algebriche; scrittura del dominio Obiettivo
Indice L attività di recupero 6 Funzioni Teoria in sintesi 0 Obiettivo Ricerca del dominio e del codominio di funzioni note Obiettivo Ricerca del dominio di funzioni algebriche; scrittura del dominio Obiettivo
Retta di calibrazione del polarimetro
 INDICE Generalità Caratteristiche tecniche Componenti dello strumento Metodo operativo Manutenzione Retta di calibrazione del polarimetro Realizzazione Home Caratteristiche tecniche del nostro polarimetro
INDICE Generalità Caratteristiche tecniche Componenti dello strumento Metodo operativo Manutenzione Retta di calibrazione del polarimetro Realizzazione Home Caratteristiche tecniche del nostro polarimetro
A.S. 2012-1013 CLASSE PRIMA SCUOLA PRIMARIA D ISTITUTO COMPETENZA CHIAVE EUROPEA DISCIPLINA
 ISTITUTO COMPRENSIVO STATALE di Scuola dell Infanzia, Scuola Primaria e Scuola Secondaria di 1 grado San Giovanni Teatino (CH) CURRICOLO A.S. 2012-1013 CLASSE PRIMA SCUOLA PRIMARIA OBIETTIVI DI Sviluppa
ISTITUTO COMPRENSIVO STATALE di Scuola dell Infanzia, Scuola Primaria e Scuola Secondaria di 1 grado San Giovanni Teatino (CH) CURRICOLO A.S. 2012-1013 CLASSE PRIMA SCUOLA PRIMARIA OBIETTIVI DI Sviluppa
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE. un atomo compie all atto di formazione di un composto al fine di formare un maggior
 CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE L ibridizzazione o ibridazione è una ricombinazione dei propri orbitali atomici che un atomo compie all atto di formazione di un composto al fine
CHIMICA ORGANICA: IBRIDAZIONE & RISONANZA IBRIDIZZAZIONE L ibridizzazione o ibridazione è una ricombinazione dei propri orbitali atomici che un atomo compie all atto di formazione di un composto al fine
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
MATEMATICA. I numeri relativi. I numeri relativi. il testo:
 01 sono i numeri che hanno davanti il segno + o il segno -. li usano quando devi far capire se un numero sta sopra o sotto dello zero. Se dico che la temperatura è di 30 gradi per te è sicuramente difficile
01 sono i numeri che hanno davanti il segno + o il segno -. li usano quando devi far capire se un numero sta sopra o sotto dello zero. Se dico che la temperatura è di 30 gradi per te è sicuramente difficile
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Formule di Struttura delle Molecole Organiche
 Formule di Struttura delle Molecole Organiche Costituzione L ordine in cui gli atomi di una molecola sono connessi è chiamata costituzione o connettività. La costituzione di una molecola deve essere determinata
Formule di Struttura delle Molecole Organiche Costituzione L ordine in cui gli atomi di una molecola sono connessi è chiamata costituzione o connettività. La costituzione di una molecola deve essere determinata
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
u 1 u k che rappresenta formalmente la somma degli infiniti numeri (14.1), ordinati al crescere del loro indice. I numeri u k
 Capitolo 4 Serie numeriche 4. Serie convergenti, divergenti, indeterminate Data una successione di numeri reali si chiama serie ad essa relativa il simbolo u +... + u +... u, u 2,..., u,..., (4.) oppure
Capitolo 4 Serie numeriche 4. Serie convergenti, divergenti, indeterminate Data una successione di numeri reali si chiama serie ad essa relativa il simbolo u +... + u +... u, u 2,..., u,..., (4.) oppure
Rette e curve, piani e superfici
 Rette e curve piani e superfici ) dicembre 2 Scopo di questo articolo è solo quello di proporre uno schema riepilogativo che metta in luce le caratteristiche essenziali delle equazioni di rette e curve
Rette e curve piani e superfici ) dicembre 2 Scopo di questo articolo è solo quello di proporre uno schema riepilogativo che metta in luce le caratteristiche essenziali delle equazioni di rette e curve
Dalla Chimica Generale
 RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
VERIFICA DELLA LEGGE DI MALUS E MISURA DELLA CONCENTRAZIONE DI UNA SOLUZIONE CON DUE POLAROIDI
 VERIFICA DELLA LEGGE DI MALUS E MISURA DELLA CONCENTRAZIONE DI UNA SOLUZIONE CON DUE POLAROIDI A) VERIFICA DELLA LEGGE DI MALUS L intensità luminosa trasmessa da un sistema costituito da due polaroidi
VERIFICA DELLA LEGGE DI MALUS E MISURA DELLA CONCENTRAZIONE DI UNA SOLUZIONE CON DUE POLAROIDI A) VERIFICA DELLA LEGGE DI MALUS L intensità luminosa trasmessa da un sistema costituito da due polaroidi
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Parte Seconda. Geometria
 Parte Seconda Geometria Geometria piana 99 CAPITOLO I GEOMETRIA PIANA Geometria: scienza che studia le proprietà delle figure geometriche piane e solide, cioè la forma, l estensione e la posizione dei
Parte Seconda Geometria Geometria piana 99 CAPITOLO I GEOMETRIA PIANA Geometria: scienza che studia le proprietà delle figure geometriche piane e solide, cioè la forma, l estensione e la posizione dei
GIROSCOPIO. Scopo dell esperienza: Teoria fisica. Verificare la relazione: ω p = bmg/iω
 GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
RESISTENZA DEI MATERIALI TEST
 RESISTENZA DEI MATERIALI TEST 1. Nello studio della resistenza dei materiali, i corpi: a) sono tali per cui esiste sempre una proporzionalità diretta tra sollecitazione e deformazione b) sono considerati
RESISTENZA DEI MATERIALI TEST 1. Nello studio della resistenza dei materiali, i corpi: a) sono tali per cui esiste sempre una proporzionalità diretta tra sollecitazione e deformazione b) sono considerati
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
Università degli studi di Messina facoltà di Scienze mm ff nn. Progetto Lauree Scientifiche (FISICA) Prisma ottico
 Università degli studi di Messina facoltà di Scienze mm ff nn Progetto Lauree Scientifiche (FISICA) Prisma ottico Parte teorica Fenomenologia di base La luce che attraversa una finestra, un foro, una fenditura,
Università degli studi di Messina facoltà di Scienze mm ff nn Progetto Lauree Scientifiche (FISICA) Prisma ottico Parte teorica Fenomenologia di base La luce che attraversa una finestra, un foro, una fenditura,
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
Condensatore elettrico
 Condensatore elettrico Sistema di conduttori che possiedono cariche uguali ma di segno opposto armature condensatore La presenza di cariche crea d.d.p. V (tensione) fra i due conduttori Condensatore piano
Condensatore elettrico Sistema di conduttori che possiedono cariche uguali ma di segno opposto armature condensatore La presenza di cariche crea d.d.p. V (tensione) fra i due conduttori Condensatore piano
CONTENUTI DELLA LEZIONE DI OGGI:
 CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
9. Urti e conservazione della quantità di moto.
 9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
9. Urti e conservazione della quantità di moto. 1 Conservazione dell impulso m1 v1 v2 m2 Prima Consideriamo due punti materiali di massa m 1 e m 2 che si muovono in una dimensione. Supponiamo che i due
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata CHO
 Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
Configurazione (Mislow, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: configurazione opposta Diastereoisomeri: configurazione diversa Conformazione
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
La propagazione della luce in una fibra ottica
 La propagazione della luce in una fibra ottica La rifrazione della luce Consideriamo due mezzi trasparenti alla luce, separati da una superficie piana. Il primo mezzo ha indice di rifrazione n, il secondo
La propagazione della luce in una fibra ottica La rifrazione della luce Consideriamo due mezzi trasparenti alla luce, separati da una superficie piana. Il primo mezzo ha indice di rifrazione n, il secondo
saccaridi glucidi (CH O) poli-idrossi chetoni aldeidi monosaccaridi oligo- e poli-saccaridi il glucosio amido cellulosa
 I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
l insieme Y è detto codominio (è l insieme di tutti i valori che la funzione può assumere)
 Che cos è una funzione? Assegnati due insiemi X e Y si ha una funzione elemento di X uno e un solo elemento di Y. f : X Y se esiste una corrispondenza che associa ad ogni Osservazioni: l insieme X è detto
Che cos è una funzione? Assegnati due insiemi X e Y si ha una funzione elemento di X uno e un solo elemento di Y. f : X Y se esiste una corrispondenza che associa ad ogni Osservazioni: l insieme X è detto
Limiti e continuità delle funzioni reali a variabile reale
 Limiti e continuità delle funzioni reali a variabile reale Roberto Boggiani Versione 4.0 9 dicembre 2003 1 Esempi che inducono al concetto di ite Per introdurre il concetto di ite consideriamo i seguenti
Limiti e continuità delle funzioni reali a variabile reale Roberto Boggiani Versione 4.0 9 dicembre 2003 1 Esempi che inducono al concetto di ite Per introdurre il concetto di ite consideriamo i seguenti
Poniamo il carbonio al centro, tre idrogeni sono legati al carbonio direttamente e uno attraverso l ossigeno
 Strutture di Lewis E un metodo semplice per ottenere le formule di struttura di composti covalenti nota la formula molecolare, la configurazione elettronica del livello di valenza degli atomi e la connettività
Strutture di Lewis E un metodo semplice per ottenere le formule di struttura di composti covalenti nota la formula molecolare, la configurazione elettronica del livello di valenza degli atomi e la connettività
Speciale SPECCHI RETROVISORI PER VEICOLI Tutto quello che c è da sapere sui: Dispositivi per la visione indiretta * di Franco MEDRI
 Speciale SPECCHI RETROVISORI PER VEICOLI Tutto quello che c è da sapere sui: Dispositivi per la visione indiretta * di Franco MEDRI Con il termine Dispositivi per la visione indiretta (c.d. specchi retrovisori)
Speciale SPECCHI RETROVISORI PER VEICOLI Tutto quello che c è da sapere sui: Dispositivi per la visione indiretta * di Franco MEDRI Con il termine Dispositivi per la visione indiretta (c.d. specchi retrovisori)
15 febbraio 2010 - Soluzione esame di geometria - 12 crediti Ingegneria gestionale - a.a. 2009-2010 COGNOME... NOME... N. MATRICOLA...
 15 febbraio 010 - Soluzione esame di geometria - 1 crediti Ingegneria gestionale - a.a. 009-010 COGNOME.......................... NOME.......................... N. MATRICOLA............. La prova dura
15 febbraio 010 - Soluzione esame di geometria - 1 crediti Ingegneria gestionale - a.a. 009-010 COGNOME.......................... NOME.......................... N. MATRICOLA............. La prova dura
Scelta intertemporale: Consumo vs. risparmio
 Scelta intertemporale: Consumo vs. risparmio Fino a questo punto abbiamo considerato solo modelli statici, cioè modelli che non hanno una dimensione temporale. In realtà i consumatori devono scegliere
Scelta intertemporale: Consumo vs. risparmio Fino a questo punto abbiamo considerato solo modelli statici, cioè modelli che non hanno una dimensione temporale. In realtà i consumatori devono scegliere
GEOMETRIA MOLECOLARE
 GEOMETRIA MOLECOLARE Le molecole hanno geometrie spaziali ben definite caratterizzate da distanze di legame ed angoli di legame. Questi possono essere determinati sperimentalmente (es. raggi X). Si vede
GEOMETRIA MOLECOLARE Le molecole hanno geometrie spaziali ben definite caratterizzate da distanze di legame ed angoli di legame. Questi possono essere determinati sperimentalmente (es. raggi X). Si vede
Elettricità e magnetismo
 E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
INTEGRALI DEFINITI. Tale superficie viene detta trapezoide e la misura della sua area si ottiene utilizzando il calcolo di un integrale definito.
 INTEGRALI DEFINITI Sia nel campo scientifico che in quello tecnico si presentano spesso situazioni per affrontare le quali è necessario ricorrere al calcolo dell integrale definito. Vi sono infatti svariati
INTEGRALI DEFINITI Sia nel campo scientifico che in quello tecnico si presentano spesso situazioni per affrontare le quali è necessario ricorrere al calcolo dell integrale definito. Vi sono infatti svariati
Gruppi funzionali. La maggior parte delle molecole organiche oltre ai legami C-C e C-H possiedono: - Eteroatomi (O, N, Alogeni);
 --- himica rganica - SG --- --- himica rganica - SG --- Gruppi funzionali Il carbonio forma sempre 4 legami, con l eccezione di intermedi di reazione, che possono avere 3 legami, e dei carbeni, che hanno
--- himica rganica - SG --- --- himica rganica - SG --- Gruppi funzionali Il carbonio forma sempre 4 legami, con l eccezione di intermedi di reazione, che possono avere 3 legami, e dei carbeni, che hanno
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
Organic Chemistry. 4 th Edition Paula Yurkanis Bruice. Delocalizzazione degli elettroni e risonanza
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Delocalizzazione degli elettroni e risonanza 1 Elettroni Localizzati contro elettroni delocalizzati localized electrons localized electrons delocalized
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Delocalizzazione degli elettroni e risonanza 1 Elettroni Localizzati contro elettroni delocalizzati localized electrons localized electrons delocalized
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CONTROLLO DELLA RADIAZIONE SOLARE
 CAPITL 4 CTRLL DLLA RADIAZI LAR 4.1 Generalità La localizzazione e l orientamento di un edificio per ridurre l esposizione solare estiva e valorizzare quella invernale, sono obiettivi fondamentali per
CAPITL 4 CTRLL DLLA RADIAZI LAR 4.1 Generalità La localizzazione e l orientamento di un edificio per ridurre l esposizione solare estiva e valorizzare quella invernale, sono obiettivi fondamentali per
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG 27/4/2006 Cuore come dipolo elettrico Il cuore considerato come un generatore elettrico complesso, in cui sono presenti
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 Utilizzo ECG 27/4/2006 Cuore come dipolo elettrico Il cuore considerato come un generatore elettrico complesso, in cui sono presenti
LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE (Regolamento, art.5; O. M. 38 art.6) Anno scolastico 2013-2014
 LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE (Regolamento, art.5; O. M. 38 art.6) Anno scolastico 2013-2014 RELAZIONE FINALE DEL DOCENTE All. A Classe: 5 DSA Indirizzo:
LICEO SCIENTIFICO STATALE "G.B.QUADRI" VICENZA DOCUMENTO DEL CONSIGLIO DI CLASSE (Regolamento, art.5; O. M. 38 art.6) Anno scolastico 2013-2014 RELAZIONE FINALE DEL DOCENTE All. A Classe: 5 DSA Indirizzo:
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
