Introduzione alla Simmetria Molecolare
|
|
|
- Gregorio Angelini
- 8 anni fa
- Просмотров:
Транскрипт
1 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale CCS CHI e MAT Introduzione alla Simmetria Molecolare Prof. Dipartimento CMIC Giulio Natta
2 Introduzione 2 La simmetria molecolare è parzialmente descritta dalla forma molecolare (cioè lineare, trigonale planare, tetraedrica, ecc. ). Le molecole si classificano e raggruppano in base alla loro simmetria. Molecole con simili geometrie sono collocate nello stesso gruppo puntiforme, cioè un gruppo contenete tutti gli oggetti con gli stessi elementi di simmetria. La teoria dei Gruppi è il trattamento matematico più corretto della simmetria molecolare.
3 Operazioni di Simmetria 3 Una operazione di simmetria è una operazione effettuata su un oggetto che lascia la configurazione sovrapponibile all originale. Molecola Simmetrica Molecola Asimmetrica Un elemento di simmetria è una operazione di simmetria effettuata rispetto ad un piano, punto, o linea.
4 Elementi di Simmetria 4 Elemento Operazione di Symmetria Simbolo Identità Asse n-esimo Rotazione di 2π/n C n Piano speculare Riflessione σ Centro di in- Inversione i versione Asse n-esimo di Rotazione di 2π/n S n rotazione seguita da riflessione impropria perpendicolare all'asse di rotazione E
5 Operatore Identità 5 Lasciare la molecola inalterata, è tipico dell operatore identità, E, e identifica la configurazione molecolare. TUTTI gli oggetti (comprese le molecole) contengono l operatore identità Una molecola molto asimmetrica, come un carbonio tetraedrico con legati 4 gruppi differenti, ha solo l'identità come unico elemento di simmetria.
6 Rotazione Attorno ad un Asse di Simmetria 6 Una rotazione lungo un asse di simmetria si indica con il simbolo, C n, dove n è un intero. Angolo di Rotazione I 360 = n Per BF 3, Per H 2 O, I = n n = 3 Possiede un asse C 3 I L'acqua ha un asse binario 2- di rotazione. Quando si ruota di q80 o, gli atomi di idrogeno si scambiano di posto, ma la molecola apparirà inalaterata.
7 Asse n-esimo di Rotazione NH 3 L'ammoniaca ha un asse C 3. Da notare che ci sono due operazioni associate all'asse C 3. La rotazione di 120 o in direzione oraria o antioraria che originano due diverse disposizioni molecolari.
8 Rotazioni Attorno a più Assi di Simmetria 8 Una molecola può avere più di un asse di simmetria rotazionale. L asse di maggiore simmetria molecolare, cioè con il più alto valore di n, è detto l asse principale.
9 Riflessione Attraverso un Piano Speculare 9 Se la riflessione attraverso un piano produce una immagine sovrapponibile, esiste nella molecola un piano di simmetria, denotato da σ. σ h Se il piano di riflessione è perpendicolare all asse principale, esso si denota col simbolo σ h. H 2 O
10 Simmetria di Riflessione 10 Se il piano di simmetria è parallelo all asse C n principale, lo si denota con il simbolo σ v.
11 Simmetria di Riflessione 11 Se un elemento di simmetria σ v taglia a metà l angolo tra due assi C 2 adiacenti, il piano si identifica con il simbolo speciale σ d. σ d. C 6 H 6 σ v. C 6. σ h. XeF 4 L'anello del benzene ha un asse C 6 come asse principale di rotazione. Il piano molecolare è perpendicolare all'asse C 6, e è indicato come piano orizzontale, σ h.
12 Riflessione attraverso un Centro di Inversione 12 Se la riflessione attraverso il centro di una molecola produce una struttura sovrapponibile, allora esiste un centro di inversione, denotato con il simbolo i.
13 Inversione in Complessi Metallici L'operazione di inversione proietta ogni atomo attraverso il centro di inversione, e arriva all'altro lato della molecola. E' tipica di disposizioni atomiche molto simmetriche (per es. Complessi ottaedrici con 6 leganti uguali. inversione Centro di inversione
14 Rotazione Seguita da Riflessione 14 Se una rotazione attraverso l asse C n, seguita dalla riflessione attraverso un piano perpendicolare a tale asse produce una struttura sovrapponibile, si dice che esiste un asse improprio di rotazione, denotato col simbolo S n. L asse taglia a metà l angolo H-C-H A B Rotazione di 90 B A Riflessione attraverso il piano che è perpendicolare all asse di rotazione originario C D C D C D σ h B A C 4
15 Rotazione Impropria La conformazione sfalsata dell'etano ha un asse S 6 che passa attraverso i due atomi di carbonio. E' da notare che un asse S 1 non esiste in quanto l'operazione coincide con quella di un piano speculare. Analogamente, un asse S 2 coincide con un centro di inversione.
16 Operazioni Successive 16 Certe operazioni possono essere una combinazione di due o più operazioni successive. Per NH 3, occorrono tre successivi operatori C 3 per produrre l operazione E. In generale, C 3 3 C n n = = E E
17 Operazioni Successive 17 Altre operazioni si possono scrivere come una combinazione di operazioni successive. Per esempio, S = C σ n n h L asse taglia a metà l angolo H-C-H Rotazione di 90 Riflessione attraverso il piano che è perpendicolare all asse di rotazione originario C 2 σ h
18 Gruppi Puntuali 18 Un gruppo puntuale definisce il numero e la natura degli elementi di simmetria in una data molecola. Un gruppo puntuale è indicato da un simbolo speciale, quale: C s, C i, C n, C nv, C nh, D nh, D nd, T d, O h, e I h. Molecole con gli stessi elementi di simmetria sono posti in gruppi puntuali. Nell'assegnare un gruppo puntuale, tipicamente si ignorano i dettagli finl, quali isomeri conformazionali dei leganti.
19 Gruppi Puntuali 19 Molecola Y Lineare? N Y i? N Y Due o più C n, n > 2? N Y i? N Y C 5? N D h C v I h O h T d Gruppi Lineari Gruppi Cubici
20 Gruppi Puntuali 20 C n? N Y Y σ? N Y Select C n with Y highest n; then, is nc 2 perpendicular to C n? N N Y σ h? σ h? Y i? N N N nσ d? nσ v? Y Y S 2n? N Y D nh D nd D n C n S 2n C nv C nh C i C 1 C s
21 21 Gruppo Puntuale C 1 Non presenta simmetria. Contiene solo un elemento di simmetria C 1 e E. C 1 (rotazione a 360 ) o E LectureNotes/Fall2002/Bonding-Notes5.pdf
22 22 Gruppo Puntuale C v Contiene un asse di rotazione -volte. E' tipica di molecole lineari (per es. HCN, HF). Contiene un numero infinito di piani σ v, ma Nessun σ h o centro di inversione.
23 23 Gruppo Puntuale D h Contiene le stesse caratteristiche di quello C v, con l aggiunta di un piano di simmetria σ h o centro di inversione, i. (per esempio F 2 )
24 24 Gruppo Puntuale T d Contiene molti elementi di simmetria. Contiene quattro vertici e quattro facce equilaterotriangolari. Molecole non polari (µ = 0)
25 25 Gruppo Puntuale O h Contiene molti elementi di simmetria (un piano orizzontale e vari piani verticali). Contiene sei vertici e otto facce equilatero-triangolari. Molti complessi simmetrici di metalli posseggono questa simmetria
26 26 Gruppo Puntuale I h Contiene molti elementi di simmetria. Contiene dodici vertici e venti facce equilaterotriangolari.
27 27 Gruppo Puntuale C nv L'acqua e l'ammoniaca appartengono entrambe alla classe C nv delle molecole. Esse hanno plani verticali di riflessione, ma nessun piano orizzontale.
28 Gruppi Puntuali D nh I Gruppi D nh hanno un piano orizzontale in aggiunta ai piani verticali. Molti complessi inorganici appartengono a questi gruppi di simmetria. X X Y Y X X
29 Determinazione del Gruppo Puntuale 29 Si può usare un approccio sistematico impiegando uno schema a INIZIO flusso. Assegnare T d, O h o I h D h Si Si La molecola ha simmetria T d, O h o I h? No La molecola è lineare? Si C'é un centro di inversione (simmetria)? No No Esiste un asse principale C n? No C'è un piano speculare? Si C s C V Si No C'è un centro di inversione? Si No C i C 1 Ci sono n assi C 2 perpendicolari all'asse C n? No Si C'é un piano σ h (perpendicolare all'asse C n )? Si No Ci sono n piani σ v (contenenti l'asse C n )? (Questi piani σ v sono del tipo σ d ) No D n C'é un piano σ h (perpendicolare all'asse C n )? Si C nh D nh Si No Ci sono n piani σ v (contenenti l'asse C n )? Si No C nv C n D nd
30 Tabelle dei Caratteri Le proprietà di simmetria di ogni gruppo puntuale sono riassunte in una tabella dei caratteri. Questa elenca tutti gli elementi di simmetria del gruppo, assieme ad un completo insieme di rappresentazioni irreducibili. Vedere
31 Tabelle dei Caratteri 31 Ogni gruppo puntuale ha una tabella del carattere associata. Indicatore del gruppo puntuale Operazioni di simmetria In C 2v l ordine è 4: 1 E, 1 C 2, 1 σ v e 1 σ v Simboli della rappresentazione di simmetria C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y x, xz B y, R x y, yz Rappresentazione di B 2 Carattere Simmetria delle funzioni «A» significa simmetrico rispetto alla rotazione attorno all asse principale «B» significa anti-simmetrico rispetto alla rotazione sull asse principale I pedici si usano per differenziare i simboli di simmetria, se necessario «1» indica che l operazione lascia la funzione inalterata, è detta simmetrica «-1» indica che l operazione inverte la funzione; è detta anti-simmetrica
32 Tabella dei Caratteri del Gruppo C 2v Funzioni di simmetria C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz Le funzioni alla destra sono dette le funzioni base. Esse rappresentano funzioni matematiche quali orbitali, rotazioni, ecc.
33 Tabella dei Caratteri del Gruppo C 2v 33 Un orbitale p z ha la stessa simmetria di una freccia che punta lungo l'asse z. z z x y E C 2 σ v (xz) σ' v (yz) x y No variazione Simmetrico 1 in tabella C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
34 Tabella dei Caratteri del Gruppo O 2v Un orbitale p x ha la stessa simmetria di una freccia che punta lungo l'asse x. z z x z y E σ v (xz) x z y No variazione Simmetrico 1 nella tabella x y C 2 σ' v (yz) x y Opposto anti-simmetrico -1 nella tabella C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
35 L'Orbitale p x Se un orbitale p x sull'atomo centrale di una molecola simmetria C 2v viene ruotato attorno all'asse C 2, l'orbitale risulta rovesciato, per cui il carattere sarà -1 C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
36 36 L'Orbitale p x Se un orbitale p x sull'atomo centrale di una molecola simmetria C 2v viene riflesso nel piano yz, l'orbitale risulta rovesciato, per cui il carattere sarà -1 C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
37 L'Orbitale p x Se un orbitale p x sull'atomo centrale di una molecola con simmetria C 2v viene riflesso nel piano xz, l'orbitale è inalterato, per cui il carattere è +1. C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
38 38 L'Orbitale p y Un orbitale p y ha la stessa simmetria di una freccia che punta lungo l'asse y. z z x z y E σ' v (yz) x z y No variazione Simmetrico 1 nella tabella x y C 2 σ' v (xz) x y Opposto anti-simmetrico -1 nella tabella C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
39 L'Orbitale p y La rotazione attorno all'asse R n si può trattare in modo simile. y L'asse z punta fuori dallo schermo Se la rotazione è nella stessa direzione (antioraria) il risultato è considerato simmetrico. y x E C 2 y y x No variazione Simmetrico 1 nella tabella Se la rotazione è nella direzione opposta (oraria) il risultato è considerato antisimmetrico x σ v (yz) σ' v (yz) x Opposto anti-simmetrico -1 nella tabella C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
40 L'Orbitale d xy Le funzioni degli orbitali d si possono trattare in modo simile. y L'asse z punta fuori dallo schermo y x E C 2 y y x No variazione Simmetrico 1 nella tabella x σ v (yz) σ' v (yz) x Opposto anti-simmetrico -1 nella tabella C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
41 Rappresentazioni della Tabella dei Caratteri 1. I caratteri +1 indicano che la funzione base non viene variata nell' operazione di simmetria. 2. I caratteri -1 indicano che la funzione base is invertita dalla operazione di simmetria. 3. I caratteri 0 indicano che la funzione base subisce una variazione più complessa. 4. Una rappresentazione A indica che le funzioni sono simmetriche rispetto alla rotazione attorno all'asse principale di rotazione. 5. Le rappresentazioni B sono asimmetriche rispetto alla rotazione attorno all'asse principale. 6. Le rappresentazioni E sono doppiamente degeneri. 7. Le rappresentazioni T sono triplamente degeneri. 8. SI pedici u e g indicano l'asimmetria (ungerade) o simmetria (gerade) rispetto al centro di inversione.
42 Perché è Utile Identificare gli Elementi di Simmetria? 42 Le applicazioni si riscontrano prevalentemente in quattro categorie principali : Predizione della polarità di molecole (per es. Una molecola non può avere un momento dipolare permanente se essa: a) ha un centro di inversione b) appartiene a uno qualsiasi dei gruppi puntuali D c) appartiene ai gruppi cubici T o O Costruzione degli orbitali molecolari e di quelli ibridi Interpretazione delle proprietà spettroscopiche (movimenti molecolari: rotazioni, vibrazioni, traslazioni) Spettroscopia IR, Raman, UV, Microonde, ecc.) Determinazione della chiralità
43 Spettroscopia Infrarossa 43 Una forma di spettroscopia vibrazionale osservazione dei gradi di libertà vibrazionali I gradi di libertà descrivono i movimenti traslazionali, vibrazionali, e rotazionali delle molecole una molecola di n atomi ha 3n gradi di libertà Movimenti di traslazione nello spazio descritti tramite i 3 gradi di libertà connessi ai 3 assi cartesiani Movimenti rotazionali Molecole non-lineari portano a 3 gradi di libertà rotazionali (numero di vibrazioni molecolari = 3n-3-3 = 3N 6) Le molecole lineari danno 2 gradi di libertà rotazionali (numero di vibrazioni molecolari = 3n-3-2 = 3N 5)
44 Movimento Vibrazionale 44 Per molecole non-lineari, gradi di libertà vibrazionali = 3n-6 Per molecole lineari, gradi di libertà vibrazionali = 3n-5 Esempio: CO 2 n = 3 3 modi traslazionali 2 modi rotazionali 3(3) 5 = 4 modi vibrazionali (a) Stiramento simmetrico IR inattivo (b) Stiramento asimmetrico IR attivo (2349 cm -1 ) (c) Piegamento (deformazione) IR attivo (667 cm -1 ) (c) Piegamento (deformazione) IR attivo (667 cm -1 )
45 Regola di Selezione per l Attività Infrarossa 45 Perché un movimento vibrazionale sia IR attivo, deve cambiare il momento dipolare molecolare. Vero per gli assorbimenti IR fondamentali: comportamenti dominanti di uno spettro IR transizione osservata dallo stato fondamentale vibrazionale al primo stato eccitato Modi di Stiramento e Deformazione Ai modi di Stiramento si attribuisce il simbolo, υ. Ai modi di deformazione o piegamento si attribuisce il simbolo, δ.
46 Molecole Triatomiche Lineari 46 Nella CO 2, si osservano due bande di assorbimento (a) Stiramento simmetrico IR inattivo (b) Stiramento asimmetrico IR attivo (2349 cm -1 ) (c) Piegamento (deformazione) IR attivo (667 cm -1 ) (c) Piegamento (deformazione) IR attivo (667 cm -1 ) una per υ CO a 2349 cm -1 Le altre per i movimenti degeneri δ a 667 cm -1
47 Molecole Triatomiche Angolate 47 Per SO 2, (a) Stiramento simmetrico IR attivo (1151 cm -1 ) (b) Stiramento asimmetrico IR attivo (1362 cm -1 ) (c) Scissoring (allargamento simmetrico) IR attivo (518 cm -1 ) Si devono osservare tre assorbimenti IR υ SO, υ SO, e δ
48 Molecole Planari Trigonali e Piramidali Trigonali 48 Per SO 3, Stiramento simmetrico IR inattivo Deformazione simmetrica IR attivo (498 cm -1 ) stiramento asimmetrico IR attivo (1391 cm -1 ) Modo doppiam. degenere deformazione asimmetrica IR attivo (530 cm -1 ) Modo doppiam. degenere Tre bande di assorbimento attese Specie piramidali trigonali (per es. NH 3 ) mostrano quattro bande di assorbimento.
49 Molecole Tetraedriche 49 Presentano nove modi di vibrazione, sei dei quali sono IR attivi. Stiramento simmetrico IR inattivo Deformazione (dopp. degenere) stiramento (trip. degenere) IR inattivo IR attivo (776 cm -1 ) deformazione (trp. degenere) IR attivo (314 cm -1 ) Solo due bande di assorbimento osservate (a causa della degenerazione).
50 Molecole Planari Quadrato 50 Nove modi di vibrazione Cinque dei quali sono IR attivi (tre osservati). IR inattivo IR inattivo IR inattivo IR inattivo IR attivo 147 cm -1 IR attivo 313 ( dopp. degenere) cm -1 IR attivo 165 ( dopp. degenere) cm -1
51 cis e trans ML 2 (CO) 2 Isomero cis C 2v Isomero trans D 2h
52 cis - ML 2 (CO) 2 C 2v : E C 2 σ xz σ yz Г CO :
53 cis - ML 2 (CO) 2 Г CO si riduce a A 1 + B 1. A 1 è uno stiramento simmetrico, e B 1 è uno stiramento asimmetrico. C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
54 cis - ML 2 (CO) 2 Г CO si riduce a A 1 + B 1. Lo stiramento simmetrico (A 1 ) è sia IR che Raman attivo. C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
55 cis - ML 2 (CO) 2 Г CO si riduce a A 1 + B 1. Lo stiramento asimmetrico (B 1 ) è sia IR che Raman attivo. C 2v E C 2 σ v (xz) σ v (yz) A z z, x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz
56 trans ML 2 (CO) 2 L'isomero trans sta nel piano xy. Il gruppo puntuale D 2h ha i seguenti elementi di simmetria : y x Isomero trans D 2h D 2h E C 2 (z) C 2 (y) C 2 (x) i σ xy σ xz σ yz
57 trans ML 2 (CO) 2 L'isomero trans sta nel piano xy. Г CO si ottiene guardando ai due legami C-O. y x Isomero trans D 2h D 2h E C 2 (z) C 2 (y) C 2 (x) i σ xy σ xz σ yz Г CO
58 trans ML 2 (CO) 2 Г CO si riduce a A g (uno stiramento simmetrico) e B 3u (uno stiramento asimmetrico). y x Isomero trans D 2h
59 trans ML 2 (CO) 2 Г CO si riduce a A g (uno stiramento simmetrico) e B 3u (uno stiramento asimmetrico). y x A g ha come funzioni base x 2, y 2 e z 2, per cui questa vibrazione è Raman attiva. Isomero trans D 2h
60 trans ML 2 (CO) 2 A g ha come funzioni base x 2, y 2 e z 2, per cui questa vibrazione è Raman attiva. y x B 3u ha come funzioni base x, per cui questa vibrazione è IR attiva. Isomero trans D 2h Gli spettri IR e Raman mostreranno entrambi un assorbimento ma a frequenze diverse.
61 Regola di Esclusione Se una molecola ha un centro di simmetria, nessuno dei suoi modi di vibrazione può essere attivo sia nell'infrarosso che nel Raman. Gli isomeri cis e trans del complesso planare quadrato ML 2 (CO) 2 si possono facilmente distinguere mediante spettroscopia. L'isomero cis ha assorbimenti che sono visibili sia negli spettri IR che negli spettri Raman, mentre l'isomero trans non li ha.
62 Molecole Chirali 62 Si definisce chirale una molecola che presenta una immagine speculare non-sovrapponibile. Contengono due differenti conformazioni, normalmente denotate come R e L o d e l. Norme di simmetria: non può contenere un asse improprio di rotazione (S n ) non può contenere un centro di inversione (i) non può contenere un piano di simmetria (σ)
63 Attività Ottica 63 Mostrano attività ottica (ruotano il piano della luce polarizzata) destrorotatorio (d) ruotano la luce a destra levorotatorio (l) ruotano la luce a sinistra Le due immagini speculari prodotte sono dette isomeri ottici o enantiomeri ottici. Gli enantiomeri ruotano la luce ugualmente ma in direzioni opposte.
64 Attività Ottica 64 Entità e segno della rotazione dipendono dalla lunghezza d onda della luce applicata Anche le rotazioni osservate dipendono dall intorno chimico una miscela diseguale di d e l ruoterà la luce nella direzione della forma dominante miscele uguali non mostreranno rotazione e sono detti essere dei racemati o miscele raceme.
65 Rotazione della Luce 65 La rotazione si denota col simbolo, α. si misura mediante un polarimetro L entità della rotazione osservata dipende da: Lunghezza d onda della luce temperatura concentrazione conformazione della molecola Piano della luce polarizzata Piano luce polarizzata dopo rotazione del piano di α Direzione della propagazione dell onda Tubo del polarimetro contenete una soluzione di un composto chirale
66 Rotazione Specifica 66 denotata dal simbolo [α] Si può calcolare in base alla relazione: [ ] α = α cl dove α è la rotazione osservata, l è il percorso ottico, e c è la concentrazione
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
Simmetria Molecolare
 Simmetria Molecolare Chimica Generale ed Inorganica Chimica Inorganica 1 prof. Dario Duca simmetria: artefatti e natura elemento di simmetria operazione di simmetria piano di riflessione riflessione elementi
Simmetria Molecolare Chimica Generale ed Inorganica Chimica Inorganica 1 prof. Dario Duca simmetria: artefatti e natura elemento di simmetria operazione di simmetria piano di riflessione riflessione elementi
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
Esercizi sulle Geometrie Molecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
IBRIDAZIONE e GEOMETRIA MOLECOLARE
 IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
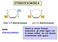 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
Teoria dell Orbitale Molecolare
 Teoria dell Orbitale Molecolare Un orbitale molecolare è il risultato della combinazione lineare degli orbitali atomici appartenenti agli atomi che costituiscono la molecola; questi orbitali molecolari
Teoria dell Orbitale Molecolare Un orbitale molecolare è il risultato della combinazione lineare degli orbitali atomici appartenenti agli atomi che costituiscono la molecola; questi orbitali molecolari
Esercizi sui Complessi Metallici
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Complessi Metallici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizi
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Complessi Metallici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizi
Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) GRUPPO: insieme di elementi correlati dalle seguenti regole:
 APPUNTI DI TEORIA DEI GRUPPI Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) Dr. Andrea G. Marrani DEFINIZIONI GRUPPO: insieme di elementi correlati dalle seguenti regole: 1) PRODOTTO
APPUNTI DI TEORIA DEI GRUPPI Corso di Chimica Inorganica II (A-L) Laurea Triennale in Chimica (L-27) Dr. Andrea G. Marrani DEFINIZIONI GRUPPO: insieme di elementi correlati dalle seguenti regole: 1) PRODOTTO
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
un legame covalente due legami covalenti? tre legami covalenti due legami covalenti un legame covalente
 e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici. Capitolo 10
 Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Esercizi sulle Forze Intermolecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizio
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Fondamenti di chimica organica Janice Gorzynski Smith Copyright 2009 The McGraw Hill Companies srl
 Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
La radiazione infrarossa si trova nella parte dello spettro elettromagnetico tra le regioni del visibile e delle microonde. La porzione di maggiore
 La radiazione infrarossa si trova nella parte dello spettro elettromagnetico tra le regioni del visibile e delle microonde. La porzione di maggiore interesse per la spettroscopia IR è quella compresa tra
La radiazione infrarossa si trova nella parte dello spettro elettromagnetico tra le regioni del visibile e delle microonde. La porzione di maggiore interesse per la spettroscopia IR è quella compresa tra
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
LA STRUTTURA DELLE MOLECOLE. Le Molecole Poliatomiche
 LA STRUTTURA DELLE MOLECOLE Le Molecole Poliatomiche LE MOLECOLE POLIATOMICE Le molecole poliatomiche sono quelle molecole che sono composte da più di due atomi e contengono nella maggior parte dei casi
LA STRUTTURA DELLE MOLECOLE Le Molecole Poliatomiche LE MOLECOLE POLIATOMICE Le molecole poliatomiche sono quelle molecole che sono composte da più di due atomi e contengono nella maggior parte dei casi
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L
 IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Metodi basati sulla meccanica quantistica
 Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
Sostanze otticamente attive POLARIMETRIA
 Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Sostanze otticamente attive POLARIMETRIA COMPOSTI OTTICAMENTE ATTIVI I composti vengono definiti otticamente attivi se sono in grado di fare ruotare il piano della luce polarizzata (stato gassoso, liquido,
Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
 orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
Formule di Lewis e geometria molecolare
 Formule di Lewis e geometria molecolare Formalismo simbolico di Lewis Rappresentazione degli elettroni di valenza; permette di seguire gli elettroni di valenza durante la formazione di un legame Consiste
Formule di Lewis e geometria molecolare Formalismo simbolico di Lewis Rappresentazione degli elettroni di valenza; permette di seguire gli elettroni di valenza durante la formazione di un legame Consiste
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto
 1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
GEOMETRIA MOLECOLARE
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI
 LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
ROTAZIONI OTTICHE DICOMPOSTI CHIRALI
 Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
Corso di Chimica Organica: 6 a esperienza di laboratorio : ROTAZIONI OTTICHE DICOMPOSTI CHIRALI Anno accademico 2011/2012 PRINCIPI GENERALI Un atomo di carbonio legato a 4 gruppi diversi è un centro stereogeno
CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO. Fig. 4
 CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO Fig. 4 1 E PERCE BANDE E NON RIGE? E 3 Nell pratica : E 2 E 1 E 0 4000 600 cm -1 4000 600 cm -1 Tra 2 livelli vibrazionali puliti Sottolivelli rotazionali 2
CLASSIFICAZIONE DELLE BANDE DI ASSORBIMENTO Fig. 4 1 E PERCE BANDE E NON RIGE? E 3 Nell pratica : E 2 E 1 E 0 4000 600 cm -1 4000 600 cm -1 Tra 2 livelli vibrazionali puliti Sottolivelli rotazionali 2
L ONDA ELETTROMAGNETICA UNITA DI MISURA E DEFINIZIONI. ν ν. λ =
 IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
IR: Teoria L ONDA ELETTROMAGNETICA Campo elettrico Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
Reticoli di Bravais e sistemi cristallini
 Reticoli di Bravais e sistemi cristallini Come in 2D, anche in 3D si individuano un motivo, che si ripete in modo periodico nello spazio e un reticolo (disposizione di punti, ciscuno che possiede lo stesso
Reticoli di Bravais e sistemi cristallini Come in 2D, anche in 3D si individuano un motivo, che si ripete in modo periodico nello spazio e un reticolo (disposizione di punti, ciscuno che possiede lo stesso
La struttura di ioni e molecole
 La struttura di ioni e molecole Inizialmente: consideriamo atomi che non danno espansione dell ottetto e non ci interessiamo della geometria delle molecole Alcune regole per individuare la posizione degli
La struttura di ioni e molecole Inizialmente: consideriamo atomi che non danno espansione dell ottetto e non ci interessiamo della geometria delle molecole Alcune regole per individuare la posizione degli
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
La forma delle molecole
 La forma delle molecole Geometria molecolare: disposizione relativa nello spazio degli atomi costituenti una molecola o un composto covalente a struttura infinita La geometria delle molecole si esprime
La forma delle molecole Geometria molecolare: disposizione relativa nello spazio degli atomi costituenti una molecola o un composto covalente a struttura infinita La geometria delle molecole si esprime
I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo
 La polarità I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo L elettronegatività è il parametro di riferimento utilizzato per valutare il trasferimento di carica
La polarità I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo L elettronegatività è il parametro di riferimento utilizzato per valutare il trasferimento di carica
Lezione n. 22. Molecole poliatomiche Metodo VSEPR Orbitali ibridi Coniugazione π. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 22 Molecole poliatomiche Metodo VSEPR Orbitali ibridi Coniugazione π 02/03/2008 Antonino Polimeno 1 Molecole poliatomiche (1) - Siamo ora
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 22 Molecole poliatomiche Metodo VSEPR Orbitali ibridi Coniugazione π 02/03/2008 Antonino Polimeno 1 Molecole poliatomiche (1) - Siamo ora
Simmetrie Cristallografiche A.A Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 A.A. 2009-2010 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Reticolo Cristallino: insieme di punti detti nodi separati da intervalli a, b, e c (reticolo di ripetizione)
A.A. 2009-2010 Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Reticolo Cristallino: insieme di punti detti nodi separati da intervalli a, b, e c (reticolo di ripetizione)
La matematica del CAD. Vettori e Matrici
 La matematica del CAD Vettori e Matrici IUAV Disegno Digitale Camillo Trevisan I programmi CAD riducono tutti i problemi geometrici in problemi analitici: la proiezione di un punto su un piano viene, ad
La matematica del CAD Vettori e Matrici IUAV Disegno Digitale Camillo Trevisan I programmi CAD riducono tutti i problemi geometrici in problemi analitici: la proiezione di un punto su un piano viene, ad
Introduzione alla chimica organica. 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole
 Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente
 Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
Il materiale didattico presentato è di uso esclusivamente personale: NON deve essere trasferito a terzi né diffuso pubblicamente Il materiale didattico non riporta esaurientemente quanto discusso durante
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Elettronegatività Elettronegatività
 Elettronegatività Nel legame covalente tra atomi uguali, la nuvola elettronica è simmetrica rispetto ai due nuclei (es. H 2, Cl 2, F 2 ) legame covalente apolare. Nel legame covalente tra atomi con Z eff
Elettronegatività Nel legame covalente tra atomi uguali, la nuvola elettronica è simmetrica rispetto ai due nuclei (es. H 2, Cl 2, F 2 ) legame covalente apolare. Nel legame covalente tra atomi con Z eff
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi
 Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti).
 4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
1. L energia di legame. 2. I gas nobili e a regola dell ottetto. 3. Il legame covalente. 4. Il legame covalente dativo. 5. Il legame covalente polare
 Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta?
 Specchi piani MPZ 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine
Specchi piani MPZ 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
Lezione n. 26. Principi generali della spettroscopia IR. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
1. L energia di legame
 legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
Idrocarburi Saturi. Cicloalcani
 Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
IBRIDAZIONE. MODELLO DELL ORBITALE di LEGAME
 IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Molecole: Forma e Polarità Orbitali Molecolari
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Molecole: Forma e Polarità Orbitali Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Molecole: Forma e Polarità Orbitali Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
Legame covalente. H 1s un protone e un elettrone
 Legame covalente H 1s un protone e un elettrone Il legame covalente è formato da una coppia di elettroni condivisa fra due atomi. L energia richiesta per separare gli atomi legati è detta energia di legame.
Legame covalente H 1s un protone e un elettrone Il legame covalente è formato da una coppia di elettroni condivisa fra due atomi. L energia richiesta per separare gli atomi legati è detta energia di legame.
Metodi spettroscopici
 Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
Metodi spettroscopici I metodi spettroscopici sono tecniche sperimentali basate sull interazione tra energia e materia per la determinazione di proprietà fisiche e chimiche. Metodi spettroscopici L interazione
CHIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO. energia superiore. energia inferiore. orbitale s
 CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π
 IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
ESPERIENZE CON GLI SPECCHI PIANI
 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine riflessa del cilindro
1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine riflessa del cilindro
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Le simmetrie dei poliedri regolari
 Le simmetrie dei poliedri regolari Le isometrie del piano e dello spazio sono state classificate da due illustri matematici. Per quanto riguarda il piano, il teorema di Chasles, del 8, afferma che nel
Le simmetrie dei poliedri regolari Le isometrie del piano e dello spazio sono state classificate da due illustri matematici. Per quanto riguarda il piano, il teorema di Chasles, del 8, afferma che nel
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II Analisi elementare: formula bruta (C x H y O z N x )? Analisi cromatografica: purezza, confronto con campioni noti Punto di fusione:
Identificazione di un composto organico: Laboratorio di Chimica Organica II Analisi elementare: formula bruta (C x H y O z N x )? Analisi cromatografica: purezza, confronto con campioni noti Punto di fusione:
LE TRASFORMAZIONI GEOMETRICHE
 pag. 1 LE TRASFORMAZIONI GEOMETRICHE Trasformazione geometrica Movimento rigido Traslazione Simmetria Costruzione di due punti simmetrici rispetto ad una retta Poligoni aventi assi di simmetria Rotazione
pag. 1 LE TRASFORMAZIONI GEOMETRICHE Trasformazione geometrica Movimento rigido Traslazione Simmetria Costruzione di due punti simmetrici rispetto ad una retta Poligoni aventi assi di simmetria Rotazione
Il Legame Chimico e la Struttura Molecolare
 A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
Spettroscopia Infrarossa. Lo spettro di assorbimento riflette la struttura di una determinata molecola
 Spettroscopia Infrarossa Lo spettro di assorbimento riflette la struttura di una determinata molecola 1 APPLICAZIONI La spettroscopia IR (vibrazionale( vibrazionale) ) dà informazioni sulle forze di legame
Spettroscopia Infrarossa Lo spettro di assorbimento riflette la struttura di una determinata molecola 1 APPLICAZIONI La spettroscopia IR (vibrazionale( vibrazionale) ) dà informazioni sulle forze di legame
