Metabolismo dei metalli. Ferro e rame
|
|
|
- Bruno Pippi
- 9 anni fa
- Просмотров:
Транскрипт
1 Metabolismo dei metalli. Ferro e rame
2 Ruolo biologico del rame e del ferro Rame e ferro sono metalli essenziali per tutti gli organismi perché si trovano legati a proteine indispensabili alla vita della cellula: respirazione, fotosintesi, fissazione dell azoto, ciclo di Krebs, trasporto dell ossigeno, sintesi del DNA, regolazione genica ecc. Fe citocromo ossidasi proteine a eme (citocromi, emoglobina) proteine con cluster Fe-S (catena di trasporto degli elettroni) proteine a ferro non-eme Cu citocromo ossidasi superossido dismutasi ceruloplasmina lisil ossidasi tirosinasi dopammina β idrossilasi - metallotioneina
3 Il ferro In condizioni fisiologiche il ferro si trova in due stati di ossidazione: Fe 3+ d 5 S=0 oppure S=2 Fe 2+ d 6 S=1/2 oppure S=5/2 Il suo potenziale redox nelle proteine varia da -300 mv a +700 mv Il Fe 2+ è instabile in aerobiosi e viene rapidamente ossidato a ph 7 Il Fe 3+ è insolubile a ph 7 (10-18 M)
4 Strutture di siti di legame del ferro nelle proteine DAOCS Cluster Fe-S Transferrina
5 Il rame In condizioni fisiologiche il rame si trova in due stati di ossidazione: Cu 2+ d 9 Cu + d 10 Il suo potenziale redox nelle proteine varia da +200 mv a +750 mv
6 Strutture di siti di legame del rame nelle proteine CuA citocromo ossidasi Mononucleare Binucleare Trinucleare Metallotioneina
7 Ruolo biologico del rame e del ferro Rame e ferro sono tossici se presenti in quantità eccessive e se non sono complessati a proteine perché reagiscono con O 2 generando specie reattive dell ossigeno (ROS) che sono in grado di danneggiare proteine, DNA e lipidi (membrane) Reazione di Haber-Weiss catalizzata da metalli O 2 + Fe 2+ O Fe 3+ 2 O H + O 2 + H 2 O 2 Fe 2+ + H 2 O 2 Fe 3+ + OH - + OH.
8 Reazioni di ossidazione catalizzate da metalli Proteine: modificazione degli amminoacidi Amminoacido Cisteina Metionina Triptofano Fenilalanina Tirosina Istidina Arginina Lisina Prolina Treonina Glutammato/glutammina Prodotto di ossidazione Disolfuri, acido cisteico Metionina solfossido, solfone Idrossitriptofano, nitrotriptofano, kinurenina 2,3-diidrossifenilalanina, idrossifenilalanina 3,4 diidrossifenilalanina, dimeri di tirosina, dinitrotirosina 2-oxoistidina, asparagina, aspartato Glutammico semialdeide α-amminoadipico semialdeide 2-pirrolidone, idrossiprolina, glutammico semialdeide 2- ammino- 3- ketobutirrato Ossalato, piruvato
9 Reazioni di ossidazione catalizzate da metalli DNA: ossidazione delle basi Lipidi: perossidazione
10 Controllo della tossicità del rame e del ferro Sistemi di detossificazione delle specie reattive dell ossigeno (ROS) Enzimatici: superossido dismutasi, catalasi e perossidasi Non enzimatici: vitamina E e C, glutatione, acido urico, bilirubina ecc. Sistemi di riparo e proteine di deposito Ferritina Metallotioneina I meccanismi cellulari di acquisizione del rame e del ferro sono strettamente regolati per mantenere adeguati livelli intracellulari di questi metalli
11 Trasporto del ferro in batteri I batteri producono siderofori, molecole a basso peso molecolare che agiscono come chelanti del Fe 3+ ad alta affinità (K a >10 30 M). I siderofori formano complessi esadentati ottaedrici con il ferro, mediante gruppi idrossammati, α-idrossi-carbossilati o catecolati. La maggior parte dei siderofori viene prodotta con un meccanismo di sintesi non ribosomiale (NRPS). I siderofori vengono internalizzati attraverso un meccanismo recettore-mediato. I siderofori fanno parte dei fattori di virulenza dei batteri patogeni.
12 Strutture di siderofori Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo. Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo.
13 Sintesi dell enterobactina in E. coli L enterobactina è prodotta da una NRPS a partire da acido 2,3-diidrossibenzoico (DHB) e serina. I geni EntE e EntB sintetizzano il DHB e lo trasferiscono sull NRPS codificata dal gene EntF dove avviene la condensazione con la serina e l assemblaggio del sideroforo.
14 Meccanismi di trasporto dei siderofori in batteri
15 Meccanismi di trasporto dei siderofori in E. coli
16 Trasporto del ferro in batteri. Modello strutturale del complesso FhuA-TonB-FhuD per l internalizzazione del ferricromo
17 Meccanismi di trasporto del ferro in batteri. Trasporto del Fe 2+ : sistema feoab Indotto in anaerobiosi Batteri patogeni: acquisizione anche mediante recettori per ferro-proteine dell ospite Recettori per transferrina e lattoferrina Recettori per l eme Questi recettori sono analoghi a quelli per il trasporto dei siderofori in quanto sono TonB-dipendenti e richiedono un sistema ABC-permeasi
18 Proteine di deposito del ferro batterioferritina e Dps
19 Regolazione del trasporto del ferro in batteri Il repressore Fur è un omodimero che si lega tra le sequenze -35 e -10 dei promotori dei geni regolati, a sequenze consenso NAT(A/T)AT NAT(A/T)AT N AT(A/T)ATN
20 Geni regolati da Fur in E. coli
21 Biosintesi dei cluster Fe-S in E. coli
22 Trasporto del ferro in lievito Nel lievito Saccharomyces cerevisiae il trasporto del ferro all interno della cellula avviene attraverso diversi meccanismi: Trasporto reduttasi-indipendente Recettori/trasportatori di siderofori (Arn1-4) Trasporto reduttasi-dipendente Metalloreduttasi NADPH-dipendenti Fre1 e Fre2 Sistema a bassa affinità (Km 30 µm) Fet4 Sistema ad alta affinità (Km 0.15 µm) Fet3-Ftr1
23 Trasporto del ferro in lievito. Sistema a bassa affinità Fet4 è un trasportatore di metalli bivalenti Fe 2+, Cu 2+, Zn 2+, Co 2+, Ni 2+. È regolato dai livelli di ferro ed è indotto in anaerobiosi.
24 Trasporto del ferro in lievito. Sistema ad alta affinità La ferrossidasi Fet3 catalizza la reazione 4Fe 2+ + O 2 + 4H + 4Fe H 2 O La permeasi Ftr1 trasporta il Fe 3+ all interno della cellula Il sistema di trasporto Fet3-Ftr1 è conservato in diversi lieviti, quali Schizosaccharomyces pombe, Candida albicans e Pichia pastoris. Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo.
25 Il complesso ferrossidasi-permeasi Fet3-Ftr1 Fet3 appartiene alla famiglia delle ossidasi blu multinucleari a rame (MCO), enzimi che legano più atomi di Cu e accoppiano l ossidazione monoelettronica del substrato alla riduzione dell ossigeno ad acqua. Ftr1 è una permeasi che presenterebbe 7 eliche transmembrana. Un motivo di sequenza REGLE nel quarto segmento TM è necessario per la funzionalità della proteina. Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo.
26 Metabolismo del ferro vacuolare e mitocondriale Il vacuolo è il sito di deposito del ferro. Ccc1 è il trasportatore del ferro dal citosol all interno del vacuolo, mentre un complesso ferrossidasi-permeasi formato dalle proteine Fet5 e Fth1 è necessario per la mobilizzazione del metallo. Nel mitocondrio avvengono alcune tappe della sintesi dell eme e la sintesi dei cluster Fe-S. Le proteine Atm1, Mrs3, Mrs4 e Yfh1 sono coinvolte nel trasporto del ferro nel mitocondrio e/o nel trasporto di cluster Fe-S dal mitocondrio al citosol.
27 Regolazione del trasporto del ferro in lievito In S. cerevisiae Aft1 e Aft2 sono fattori trascrizionali che inducono l espressione di numerosi geni in carenza di ferro. Aft1 trasloca dal citoplasma al nucleo quando il ferro è limitante e attiva la trascrizione dei geni bersaglio. Aft1 e Aft2 contengono un motivo Cys-X-Cys nel dominio di legame al DNA. In S. pombe, C. albicans, P. pastoris e altri funghi, la regolazione ferro-dipendente è mediata da repressori trascrizionali appartenenti alla famiglia dei fattori GATA a dita di zinco. Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo.
28 Fattori che regolano Aft1
29 Geni regolati da fattori di trascrizione ferro-dipendenti in lievito Fattore di trascrizione Descrizione Gene Aft1 Trasportatori FET4, FTR1, FTH1, SMF3, MRS4, CCC2, COT1 Cu chaperone Ferrossidasi Metalloreduttasi Proteine della parete cellulare Trasporto di siderofori Biosintesi cluster Fe-S Altri ATX1 FET3, FET5 FRE1, FRE2, FRE3, FRE4, FRE5, FRE6 FIT1, FIT2, FIT3 ARN1, ARN2, ARN3, ARN4 ISU1, ISU2 TIS11, HMX1, AKR1, PCL5, ICY2, PRY1 Aft2 Trasportatori SMF3, MRS4, FTR1, COT1 Cu chaperone Ferrossidasi Metalloreduttasi Proteine della parete cellulare Biosintesi cluster Fe-S Altri ATX1 FET3, FET5 FRE1 FIT1, FIT2, FIT3 ISU1 Fep1 Trasportatori fip1 + Ferrossidasi fio1 + BNA2, ECM4, LAP4, TIS11 Trasporto di siderofori str1 +, str2 +, str3 +
30 Risposta alla carenza di ferro in S. cerevisiae
31 Espressione regolata da metalli in lievito
32 Patologie associate a dismetabolismo del rame o del ferro nell uomo Patologia Gene mutato Sindrome di Menkes ATP7A Carenza di rame (difettoso assorbimento del rame) Morbo di Wilson ATP7B Accumulo di rame nel fegato e nel cervello Emocromatosi di tipo I-IV HFE, TfR2, HJV, HAMP, FPN Accumulo di ferro in diversi organi Atassia di Friedreich Frataxina Neurodegenerazione e Aceruloplasminemia Ceruloplasmina accumulo di ferro in PANK-2 specifiche regioni del cervello Sindrome di Hallevorden- Spatz Neuroferritinopatia Corea di Huntington Morbo di Alzheimer Morbo di Parkinson L-ferritina
33 Metabolismo cellulare del ferro in mammiferi
34 Proteine del metabolismo cellulare del ferro DMT1 è un co-trasportatore di cationi bivalenti e H + espresso in molti tessuti (enterociti, cellule eritroidi, rene, polmone, cervello ). Ha un ruolo nell assorbimento del ferro nel duodeno e nel meccanismo di rilascio del ferro dalla transferrina. L espressione di DMT1 è indotta da carenza di ferro e sono state identificate diverse isoforme della proteina. La Ferritina è la principale proteina di deposito intracellulare del ferro. E formata da 24 subunità di tipo H e di tipo L ed è in grado di legare fino a 4500 atomi di ferro.
35 Ciclo Transferrina-TfR
36 Esporto del ferro dalle cellule: la ferroportina La Ferroportina è l unico esportatore del ferro dalle cellule finora identificato. È espressa sulla membrana basolaterale degli enterociti, nei macrofagi, negli astrociti e negli epatociti. Mutazioni della ferroportina causano accumulo di ferro nel fegato o nei macrofagi reticoloendoteliali.
37 Ferrossidasi: ceruloplasmina ed efestina Le ferrossidasi ceruloplasmina ed efestina appartengono alla famiglia delle MCO e catalizzano l ossidazione del Fe 2+ a Fe 3+ con riduzione dell O 2 ad H 2 O. La ceruloplasmina collabora con la ferroportina ossidando il Fe 2+ esportato da quest ultima e facilitandone l incorporazione nella transferrina. L efestina è una proteina di membrana intracellulare, è espressa principalmente negli enterociti ed ha un ruolo nell assorbimento intestinale del ferro.
38 L attività ferrossidasica della ceruloplasmina è necessaria per mantenere la ferroportina sulla superficie della cellula Una isoforma della ceruloplasmina è ancorata alla membrana mediante un ancora GPI ed è espressa principalmente negli astrociti. La mancanza di ceruloplasmina in queste cellule causa la scomparsa della ferroportina dalla superficie cellulare e ciò potrebbe spiegare l accumulo di ferro riscontrato in pazienti affetti da aceruloplasminemia.
39 Il sistema regolatorio IRE/IRP. Regolazione post-trascrizionale
40 Omeostasi sistemica del ferro Il ferro viene assorbito dagli enterociti nel duodeno, rilasciato nel sangue e trasportato ai diversi organi dalla transferrina. I macrofagi reticoloendoteliali costituiscono il sito principale di riciclaggio del ferro dagli eritrociti senescenti.
41 Regolazione del trasporto del ferro mediata dall epcidina L epcidina è un peptide di 25 amminoacidi prodotto dal fegato. Si lega alla ferroportina causandone l internalizzazione e la degradazione, in questo modo diminuisce l esporto del ferro dagli enterociti e dai macrofagi nella circolazione sanguigna. L espressione dell epcidina è indotta da eccesso di ferro e infiammazione (IL-6), e repressa da anemia e ipossia.
42 Regolazione della sintesi dell epcidina
43 Metabolismo del rame I meccanismi alla base dell omeostasi cellulare del rame sono conservati in batteri (in parte), in lievito e negli eucarioti superiori. Gli studi in lievito si sono rivelati particolarmente utili per identificare e/o caratterizzare proteine umane strutturalmente o funzionalmente omologhe. Il metabolismo del rame negli eucarioti è strettamente connesso con il metabolismo del ferro attraverso le ferrossidasi Cu-dipendenti: difetti nell incorporazione del rame nelle ferrossidasi provocano dismetabolismo del ferro.
44 Trasporto del rame in cellule eucariotiche. Il trasportatore di membrana Ctr1 Ctr1 è il principale trasportatore di Cu + nella cellula (Km 1-5 µm). Ctr1 possiede tre domini transmembrana e una serie di sequenze Met (MX 1-3 M) necessarie per il legame del Cu +. La complementazione funzionale in ceppi di lievito ctr1ctr3δ ha permesso di isolare Ctr1 umano. L importanza di Ctr1 è dimostrata dal fatto che topi knock-out per Ctr1 muoiono allo stadio embrionale. L espressione di Ctr1 è regolata a livello trascrizionale in lievito dal fattore Mac1 e a livello post-traduzionale attraverso endocitosi e degradazione mediata dal rame (in lievito e nei mammiferi).
45 Trasporto intracellulare del rame in lievito. Chaperoni e pompe per lo smistamento del metallo Cuproproteine Cu,ZnSOD e MT citosol Citocromo ossidasi mitocondrio Fet3 membrana plasmatica Chaperoni del rame CCS citosol Cox17 mitocondrio Atx1 Golgi Pompe del rame L ATPasi Ccc2 trasporta il rame all interno del Golgi per l incorporazione in Fet3
46 Trasporto intracellulare del rame in epatociti e neuroni. Chaperoni e pompe per lo smistamento del metallo
47 Gli chaperoni del rame sono proteine di piccole dimensioni (circa amminoacidi) conservate dai batteri all uomo. Il rame viene legato come Cu + da due residui di cisteina con una coordinazione atipica. Chaperoni del rame
48 ATPasi di trasporto del rame Le pompe per il trasporto del rame appartengono alla famiglia delle ATPasi di tipo P o CPx e si trovano in batteri, lievito ed eucarioti superiori. Accoppiano il trasporto del metallo all idrolisi dell ATP con formazione di un intermedio acil-fosfato su un residuo di aspartato. Presentano 8 regioni transmembrana e una regione N-terminale di legame del rame organizzata in domini che contengono sequenze conservate MXCXXC. Nel dominio P e nel dominio N avvengono la fosforilazione dell aspartato e il legame del nucleotide. Nel dominio A avviene la defosforilazione dell aspartato. Batteri CopA, copb Lievito Ccc2 Mammiferi ATP7A, ATP7B
49 Efflusso del rame dalle cellule: Proteine di Menkes (ATP7A) e Wilson (ATP7B) ATP7A possiede sei domini di legame del rame È localizzata nel trans-golgi ed è espressa in enterociti, nell endotelio della barriera emato-encefalica e numerosi altri tessuti. ATP7B possiede sei domini di legame del rame È localizzata nel trans-golgi ed è espressa nel fegato e a bassi livelli nel rene, placenta, cervello e cuore.
50 La localizzazione subcellulare di ATP7A e ATP7B cambia in funzione della concentrazione di rame
51 Gli chaperoni e le pompe del rame. Meccanismo di trasferimento del metallo
52 Struttura di Atx1 e dei domini che legano il rame delle ATPasi di lievito (Ccc2) e umane (Menkes e Wilson). Il riconoscimento specifico è mediato da interazioni di tipo elettrostatico.
53 Complementarietà di carica tra chaperoni e pompe
Metabolismo dei metalli. Ferro e rame
 Metabolismo dei metalli. Ferro e rame Ruolo biologico del rame e del ferro Rame e ferro sono metalli essenziali per tutti gli organismi perché sono cofattori di proteine indispensabili alla vita della
Metabolismo dei metalli. Ferro e rame Ruolo biologico del rame e del ferro Rame e ferro sono metalli essenziali per tutti gli organismi perché sono cofattori di proteine indispensabili alla vita della
Metabolismo del rame e del ferro nell uomo
 Metabolismo del rame e del ferro nell uomo Patologia Patologie associate a dismetabolismo del rame o del ferro Gene mutato Sindrome di Menkes ATP7A Carenza di rame (difettoso assorbimento del rame) Morbo
Metabolismo del rame e del ferro nell uomo Patologia Patologie associate a dismetabolismo del rame o del ferro Gene mutato Sindrome di Menkes ATP7A Carenza di rame (difettoso assorbimento del rame) Morbo
Metabolismo dei metalli. Ferro e rame
 Metabolismo dei metalli. Ferro e rame Ruolo biologico del rame e del ferro Rame e ferro sono metalli essenziali per tutti gli organismi perché si trovano legati a proteine indispensabili alla vita della
Metabolismo dei metalli. Ferro e rame Ruolo biologico del rame e del ferro Rame e ferro sono metalli essenziali per tutti gli organismi perché si trovano legati a proteine indispensabili alla vita della
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Regolazione dell espressione genica nei procarioti: OPERONI
 Regolazione dell espressione genica nei procarioti: OPERONI LA REGOLAZIONE DELL ESPRESSIONE GENICA HA LUOGO A LIVELLO DELLA TRASCRIZIONE OPERONE: insieme di geni che vengono trascritti contemporaneamente
Regolazione dell espressione genica nei procarioti: OPERONI LA REGOLAZIONE DELL ESPRESSIONE GENICA HA LUOGO A LIVELLO DELLA TRASCRIZIONE OPERONE: insieme di geni che vengono trascritti contemporaneamente
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
FOSFORILAZIONE OSSIDATIVA
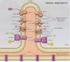 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
La produzione di ROS è catalizzata da metalli legati a proteine
 Stress Ossidativo La produzione di ROS è catalizzata da metalli legati a proteine Reazioni di Fenton e di Haber-Weiss SOD H 2 O 2 + O 2 O 2 - + Fe 3+ Fe 2+ + O 2 Fe 2+ + H 2 O 2 OH - + Fe 3+ + OH Catalasi
Stress Ossidativo La produzione di ROS è catalizzata da metalli legati a proteine Reazioni di Fenton e di Haber-Weiss SOD H 2 O 2 + O 2 O 2 - + Fe 3+ Fe 2+ + O 2 Fe 2+ + H 2 O 2 OH - + Fe 3+ + OH Catalasi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Strutture di alcuni peptidi bioattivi prodotti da batteri e funghi Come vengono prodotti questi peptidi? Hanno strutture complesse (spesso
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Strutture di alcuni peptidi bioattivi prodotti da batteri e funghi Come vengono prodotti questi peptidi? Hanno strutture complesse (spesso
Università di Roma Tor Vergata Scienze della Nutrizione Umana Biochimica della Nutrizione - Prof.ssa Luciana Avigliano A.A.
 Università di Roma Tor Vergata Scienze della Nutrizione Umana Biochimica della Nutrizione - Prof.ssa Luciana Avigliano A.A. 2011-12 Nutrienti quali regolatori delle funzioni cellulari AZIONE REGOLATORIA
Università di Roma Tor Vergata Scienze della Nutrizione Umana Biochimica della Nutrizione - Prof.ssa Luciana Avigliano A.A. 2011-12 Nutrienti quali regolatori delle funzioni cellulari AZIONE REGOLATORIA
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
AGISCONO NEL SISTEMA NAVETTA 2 ISOFORME DELL ENZIMA: UNA FORMA MITOCONDRIALE ( MEMBRANA MIT. INTERNA) FAD-dipendente
 METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
Metabolismo del ferro nell enterocita duodenale
 Assorbimento e rilascio del ferro dall enterocita nel duodeno Metabolismo del ferro nell enterocita duodenale? K + Na + DMT1= Divalent Metal Transporter, un simporto con i protoni Tf = transferrina DCYTB
Assorbimento e rilascio del ferro dall enterocita nel duodeno Metabolismo del ferro nell enterocita duodenale? K + Na + DMT1= Divalent Metal Transporter, un simporto con i protoni Tf = transferrina DCYTB
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI
 GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
FOSFORILAZIONE OSSIDATIVA
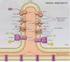 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Metabolismo fermentativo
 Metabolismo fermentativo Anaerobio (non richiede ossigeno) Energeticamente poco efficiente (se confrontata alla respirazione) La catena di trasferimento degli elettroni è molto limitata: donatori ed accettori
Metabolismo fermentativo Anaerobio (non richiede ossigeno) Energeticamente poco efficiente (se confrontata alla respirazione) La catena di trasferimento degli elettroni è molto limitata: donatori ed accettori
Cap.21 CATABOLISMO DEI LIPIDI
 Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
NADH FADH 2 (trasportatori ridotti di elettroni) Catena respiratoria (trasferimento degli
 NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
LIPIDI COMPLESSI E LIPOPROTEINE
 LIPIDI COMPLESSI E LIPOPROTEINE Principali lipidi assunti con la dieta Fosfolipidi e colesterolo (membrane) Triacilgliceroli (olii e grassi) Le cellule importano ACIDI GRASSI e GLICEROLO SATURI MONOINSATURI
LIPIDI COMPLESSI E LIPOPROTEINE Principali lipidi assunti con la dieta Fosfolipidi e colesterolo (membrane) Triacilgliceroli (olii e grassi) Le cellule importano ACIDI GRASSI e GLICEROLO SATURI MONOINSATURI
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa
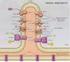 Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
espressione genica processo attraverso cui l informazione di un gene viene decodificata
 espressione genica processo attraverso cui l informazione di un gene viene decodificata regolazione o controllo dell espressione genica meccanismi mediante i quali un gene viene selettivamente espresso
espressione genica processo attraverso cui l informazione di un gene viene decodificata regolazione o controllo dell espressione genica meccanismi mediante i quali un gene viene selettivamente espresso
Biosintesi dei carboidrati
 Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
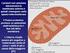 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
MFN0366-A1 (I. Perroteau) - il nucleo. Solo per uso didattico, vietata la riproduzione, la diffusione o la vendita
 1 Cosa contiene il nucleo? Il nucleo non contiene solo DNA, che costituisce solo il 20% del materiale nucleare, ma anche una grande quantità di proteine chiamate nucleoproteine ed RNA. La maggior parte
1 Cosa contiene il nucleo? Il nucleo non contiene solo DNA, che costituisce solo il 20% del materiale nucleare, ma anche una grande quantità di proteine chiamate nucleoproteine ed RNA. La maggior parte
Università degli Studi del Sannio. Facoltà di Scienze MM.FF.NN. - Corso di Laurea in Biotecnologie a.a Programma di Biologia Cellulare
 Università degli Studi del Sannio Facoltà di Scienze MM.FF.NN. - Corso di Laurea in Biotecnologie a.a. 2010-2011 Programma di Biologia Cellulare (Prof Massimo Mallardo, I semestre, I anno) [email protected]
Università degli Studi del Sannio Facoltà di Scienze MM.FF.NN. - Corso di Laurea in Biotecnologie a.a. 2010-2011 Programma di Biologia Cellulare (Prof Massimo Mallardo, I semestre, I anno) [email protected]
COMPARTIMENTI INTRACELLULARI
 COMPARTIMENTI INTRACELLULARI ogni organello è delimitato da una, o due membrane: ciascuna di esse è costituita da un doppio strato fosfolipidico con stessa struttura della membrana plasmatica ma composizione
COMPARTIMENTI INTRACELLULARI ogni organello è delimitato da una, o due membrane: ciascuna di esse è costituita da un doppio strato fosfolipidico con stessa struttura della membrana plasmatica ma composizione
MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine. Solo per uso didattico, vietata la riproduzione, la diffusione o la vendita
 MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine MFN0366-A1 (I. Perroteau) -traduzione delle proteine trna Traduzione: mrna -------> proteine mrna MFN0366-A1 (I. Perroteau) -traduzione
MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine MFN0366-A1 (I. Perroteau) -traduzione delle proteine trna Traduzione: mrna -------> proteine mrna MFN0366-A1 (I. Perroteau) -traduzione
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Ruolo del fegato nella nutrizione
 Ruolo del fegato nella nutrizione Centro di distribuzione dei nutrienti per tutti gli altri organi Annulla le fluttuazioni del metabolismo determinate dall assunzione intermittente del cibo Funge da deposito
Ruolo del fegato nella nutrizione Centro di distribuzione dei nutrienti per tutti gli altri organi Annulla le fluttuazioni del metabolismo determinate dall assunzione intermittente del cibo Funge da deposito
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
FERRO. Il ferro come simbolo di forza e potere risale alla mitologia greca, dove Efesto era il dio del fuoco e del ferro
 FERRO Il ferro come simbolo di forza e potere risale alla mitologia greca, dove Efesto era il dio del fuoco e del ferro E al centro della vita aerobica in quanto media l utilizzo dell ossigeno: metabolismo
FERRO Il ferro come simbolo di forza e potere risale alla mitologia greca, dove Efesto era il dio del fuoco e del ferro E al centro della vita aerobica in quanto media l utilizzo dell ossigeno: metabolismo
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
TRASPORTO VESCICOLARE
 TRASPORTO VESCICOLARE ORIGINE Dalle membrane degli organelli DESTINAZIONE Verso altri organelli (trasporto intracellulare) Verso l ambiente extracellulare (esocitosi) Dalla membrana plasmatica Verso l
TRASPORTO VESCICOLARE ORIGINE Dalle membrane degli organelli DESTINAZIONE Verso altri organelli (trasporto intracellulare) Verso l ambiente extracellulare (esocitosi) Dalla membrana plasmatica Verso l
Biochimica della Nutrizione
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 ferro FERRO Il ferro come simbolo di forza e potere risale alla mitologia greca,
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 ferro FERRO Il ferro come simbolo di forza e potere risale alla mitologia greca,
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Fosforilazione ossidativa
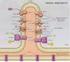 Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
BIOSEGNALAZIONE. La ricezione e la trasmissione delle informazioni extracellulari Parte I
 BIOSEGNALAZIONE La ricezione e la trasmissione delle informazioni extracellulari Parte I La coordinazione delle attività metaboliche nei diversi tessuti e organi dei mammiferi avviene mediante il sistema
BIOSEGNALAZIONE La ricezione e la trasmissione delle informazioni extracellulari Parte I La coordinazione delle attività metaboliche nei diversi tessuti e organi dei mammiferi avviene mediante il sistema
Fosforilazione ossidativa
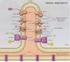 Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
FISIOLOGIA dell ALLENAMENTO. dai processi fisiologici alle metodiche di allenamento
 FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
Membri dell universo microbico
 Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
Membri dell universo microbico Cellule procariote: mancanza di un nucleo ben delimitato all interno della cellula Cellule eucariote: presenza di un compartimento nucleare ben definito, maggiore complessità
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
3. Citologia i. Strutture cellulari comuni tra cellule animali e vegetali
 Strutture cellulari comuni tra cellule animali e vegetali: CITOPLASMA CITOSCHELETRO RIBOSOMI RETICOLO ENDOPLASMATICO APPARATO DEL GOLGI MITOCONDRI NUCLEO PEROSSISOMI CITOPLASMA materiale gelatinoso incolore
Strutture cellulari comuni tra cellule animali e vegetali: CITOPLASMA CITOSCHELETRO RIBOSOMI RETICOLO ENDOPLASMATICO APPARATO DEL GOLGI MITOCONDRI NUCLEO PEROSSISOMI CITOPLASMA materiale gelatinoso incolore
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
METABOLISMO DEL FERRO NEL PAZIENTE NEOPLASTICO
 METABOLISMO DEL FERRO NEL PAZIENTE NEOPLASTICO METABOLISMO DEL FERRO (I) Il ferro partecipa a numerose funzioni come il trasporto di ossigeno (emoglobina e mioglobina) e di elettroni ed è parte della molecola
METABOLISMO DEL FERRO NEL PAZIENTE NEOPLASTICO METABOLISMO DEL FERRO (I) Il ferro partecipa a numerose funzioni come il trasporto di ossigeno (emoglobina e mioglobina) e di elettroni ed è parte della molecola
Lattato. Glicolisi. Piruvato
 Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
06_citologia_SER_golgi 1
 1 La sintesi proteica inizia sempre nello stesso modo: aggancio della piccola subunità ribosomale al estremità 5 dell mrna. si aggancio la grande subunità ribosomale In corrispondenza del codone di inizio
1 La sintesi proteica inizia sempre nello stesso modo: aggancio della piccola subunità ribosomale al estremità 5 dell mrna. si aggancio la grande subunità ribosomale In corrispondenza del codone di inizio
Tutti gli esseri viventi sono formati da cellule
 La cellula La cellula La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. La cellula Sebbene i virus siano in grado
La cellula La cellula La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. La cellula Sebbene i virus siano in grado
Nei batteri non è presente una membrana nucleare
 La cellula procariota (Bacteria e Archaea) Morfologia generale Composizione chimica Le strutture cellulari e le loro funzioni parte 1 L involucro Appendici esterne: Le strutture cellulari e le loro funzioni
La cellula procariota (Bacteria e Archaea) Morfologia generale Composizione chimica Le strutture cellulari e le loro funzioni parte 1 L involucro Appendici esterne: Le strutture cellulari e le loro funzioni
Metabolismo batterico
 Metabolismo batterico La somma di tutte le reazioni chimiche che avvengono nella cellula.questa è resa possibile dal flusso dell energia e dalla partecipazione di enzimi. Funzione principale della cellula
Metabolismo batterico La somma di tutte le reazioni chimiche che avvengono nella cellula.questa è resa possibile dal flusso dell energia e dalla partecipazione di enzimi. Funzione principale della cellula
CELLULA. La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule.
 LA CELLULA CELLULA La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. CELLULA La teoria cellulare Le cellule furono
LA CELLULA CELLULA La cellula è la più piccola unità di un organismo in grado di funzionare in modo autonomo. Tutti gli esseri viventi sono formati da cellule. CELLULA La teoria cellulare Le cellule furono
Diffusione facilitata Trasporti mediati da proteine di membrana: i trasportatori
 Diffusione facilitata Trasporti mediati da proteine di membrana: i trasportatori I trasportatori somigliano agli enzimi: catalizzano la traslocazione dei substrati da una parte all altra della membrana
Diffusione facilitata Trasporti mediati da proteine di membrana: i trasportatori I trasportatori somigliano agli enzimi: catalizzano la traslocazione dei substrati da una parte all altra della membrana
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
COMUNICAZIONE INTERCELLULARE
 COMUNICAZIONE INTERCELLULARE TRASFERIMENTO DIRETTO DI SEGNALI CHIMICI E ELETTRICI ATTRAVERSO GIUNZIONI COMUNICANTI COMUNICAZIONE CHIMICA LOCALE (SOSTANZE PARACRINE E AUTOCRINE) COMUNICAZIONE A LUNGA DISTANZA
COMUNICAZIONE INTERCELLULARE TRASFERIMENTO DIRETTO DI SEGNALI CHIMICI E ELETTRICI ATTRAVERSO GIUNZIONI COMUNICANTI COMUNICAZIONE CHIMICA LOCALE (SOSTANZE PARACRINE E AUTOCRINE) COMUNICAZIONE A LUNGA DISTANZA
La fotosintesi non fornisce energia solo per l organicazione del carbonio METABOLISMO DELL AZOTO
 La fotosintesi non fornisce energia solo per l organicazione del carbonio METABOLISMO DELL AZOTO IL CICLO DELL AZOTO METABOLISMO DELL AZOTO COMPOSTI DELL AZOTO FISSAZIONE BIOLOGICA DELL AZOTO NITROGENASI
La fotosintesi non fornisce energia solo per l organicazione del carbonio METABOLISMO DELL AZOTO IL CICLO DELL AZOTO METABOLISMO DELL AZOTO COMPOSTI DELL AZOTO FISSAZIONE BIOLOGICA DELL AZOTO NITROGENASI
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Complesso Maggiore di Istocompatibilita (MHC)
 Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
Complesso Maggiore di Istocompatibilita (MHC) Scoperta dell MHC I geni dell MHC sono stati inizialmente identificati come responsabili del rapido rigetto dei tessuti trapiantati. I geni dell MHC sono polimorfi:
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
Formazione dei chilomicroni
 Formazione dei chilomicroni I triacilgliceroli forniscono il combustibile per i lunghi voli migratori del Piviere minore. I triacilgliceroli sono riserve di energia molto concentrate essendo ridotti ed
Formazione dei chilomicroni I triacilgliceroli forniscono il combustibile per i lunghi voli migratori del Piviere minore. I triacilgliceroli sono riserve di energia molto concentrate essendo ridotti ed
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) 1 2 Il glucosio viene trasportato all interno della cellula
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia
 I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
Meccanismi effettori dei linfociti T citotossici
 Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
LA REGOLAZIONE GENICA DEI PROCARIOTI.
 LA REGOLAZIONE GENICA DEI PROCARIOTI www.fisiokinesiterapia.biz NON TUTTI I GENI VENGONO UTILIZZATI NELLO STESSO MOMENTO E NON TUTTI CON LA STESSA INTENSITÀ Regolazione genica = la modalità con cui viene
LA REGOLAZIONE GENICA DEI PROCARIOTI www.fisiokinesiterapia.biz NON TUTTI I GENI VENGONO UTILIZZATI NELLO STESSO MOMENTO E NON TUTTI CON LA STESSA INTENSITÀ Regolazione genica = la modalità con cui viene
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
LE METALLOTIONEINE COME BIOMARCATORI DELL INQUINAMENTO DA METALLI
 LE METALLOTIONEINE COME BIOMARCATORI DELL INQUINAMENTO DA METALLI Candidato: Giulia Russo Matricola: 245949 Relatrice: Prof.ssa Maria Marino Anno accademico: 2008/2009 Tavola periodica degli elementi METALLI
LE METALLOTIONEINE COME BIOMARCATORI DELL INQUINAMENTO DA METALLI Candidato: Giulia Russo Matricola: 245949 Relatrice: Prof.ssa Maria Marino Anno accademico: 2008/2009 Tavola periodica degli elementi METALLI
Compartimenti intracellulari
 Compartimenti intracellulari Endosomi: smistamento di materiali assunti per endocitosi Perossisomi: sede di reazioni ossidative per la demolizione di lipidi e di molecole tossiche Lisosomi: contengono
Compartimenti intracellulari Endosomi: smistamento di materiali assunti per endocitosi Perossisomi: sede di reazioni ossidative per la demolizione di lipidi e di molecole tossiche Lisosomi: contengono
Il genoma dei batteri è organizzato in operon. Un operon è una unità trascrizionale indipendente, formata da (2-15) geni regolati da un solo promotore
 Il genoma dei batteri è organizzato in operon Un operon è una unità trascrizionale indipendente, formata da (2-15) geni regolati da un solo promotore I geni di un operon sono diversi, ma concorrono allo
Il genoma dei batteri è organizzato in operon Un operon è una unità trascrizionale indipendente, formata da (2-15) geni regolati da un solo promotore I geni di un operon sono diversi, ma concorrono allo
DESTINI DEL PIRUVATO
 DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
TRANSAMINASI (AMINOTRANSFERASI) agiscono con un meccanismo ping-pong. sono presenti sia nel citosol che nei mitocondri
 TRANSAMINASI (AMINOTRANSFERASI) sono PLP-dipendenti agiscono con un meccanismo ping-pong catalizzano reazioni reversibili sono presenti sia nel citosol che nei mitocondri Seguiamo le fasi di una reazione
TRANSAMINASI (AMINOTRANSFERASI) sono PLP-dipendenti agiscono con un meccanismo ping-pong catalizzano reazioni reversibili sono presenti sia nel citosol che nei mitocondri Seguiamo le fasi di una reazione
