BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
|
|
|
- Leonardo Dino Tommasi
- 8 anni fa
- Просмотров:
Транскрипт
1 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Prof. Augusto Parente Lezione 16
2 - Le peptidasi sono anche note come proteasi, proteinasi, enzimi proteolitici. LE PEPTIDASI PEPTIDASI è il termine raccomandato per ogni proteina enzimatica che idrolizza (scinde con acqua) il legame peptidico. - Enzyme Nomenclature della NC-IUBMB; - Human Gene Nomenclature Committee - MEROPS database - Il termine peptidasi è applicabile a qualsiasi tipo di enzima che scinde il legame peptidico, indipendentemente dalla grandezza del substrato (proteina, oligopeptidi) e dalla posizione del legame idrolizzato (residui terminali, residui interni alla catena polipeptidica). H 2 O
3 IL DATABASE MEROPS DELLE PEPTIDASI Il database MEROPS racchiude le informazione sulle peptidasi e sulle proteine che le inibiscono (inibitori proteici). Industrial Enzymes
4 TIPO DI CATALISI MEROPS divide le peptidasi sulla base del gruppo chimico (nucleofilo) coinvolto nell idrolisi del legame peptidico. Distinguiamo 9 famiglie: 1. Aspartato (aspartil) peptidasi (A) 2. Cisteina (cistein) peptidasi (C) 3. Glutammil peptidasi (G) 4. Metallo peptidasi (M) 5. Asparagin peptidasi (N) 6. Peptidasi miste (P) 7. Serina (serin) peptidasi (S) 8. Treonina (treonin) peptidasi (T) 9. Peptidasi sconosciuta (U)
5 IL SITO ATTIVO delle PEPTIDASI Le strutture cristallografiche delle peptidasi mostrano che il sito attivo è comunemente localizzato sulla superficie delle molecole, tra domini strutturali adiacenti, e le proprietà del sito di legame che si trova nella cavità del sito attivo determinano la specificità per il substrato. Il sito catalitico sarà formato da un residuo che porta il gruppo nucleofilo e da altri residui importanti per la catalisi e il mantenimento della struttura del sito attivo. Questi residui sono altamente conservati tra le peptidasi appartenenti alla stessa FAMIGLIA.
6 In generale, l idrolisi del legame peptidico è una reazione acidobase, in cui un nucleofilo carico agisce come donatore di protoni e un residuo, noto genericamente come base, è l accettore di protoni. Nelle peptidasi a serina, treonina e cisteina, il gruppo reattivo (nucleofilo) è il gruppo ossidrilico (serina e treonina) o il gruppo sulfidrilico (cisteina) della catena laterale dell amminoacido. Nel caso di aspartato e metallo peptidasi, il gruppo reattivo (nucleofilo) è una molecola d acqua attivata. Nelle aspartato-peptidasi, l acqua si lega direttamente alla catena laterale dell amminoacido; Nelle metallo-peptidasi, uno ione metallico divalente (zinco, cobalto, manganese o rame) lega una molecola d acqua e le catene laterali cariche di tre amminoacidi. Alcune metallo-peptidasi utilizzano due ioni metallici: in questo caso legano due molecole d acqua e uno dei residui amminoacidici è legato ad entrambi i metalli.
7 Nelle serin e cistein peptidasi la base accettore di protoni è generalmente un residuo di istidina o di lisina. Quando la base è il residuo di istidina, generalmente interviene un terzo residuo (triade catalitica: Ser-His-Xxx), che orienta l anello imidazolico dell istidina e aiuta a caricare uno degli atomi di azoto dell anello: Nelle serin peptidasi (chimotripsina ) aspartato Nelle cistein peptidasi asparagina (papaina), aspartato o glutammato. Ci sono molte serin e cistein peptidasi che però non utilizzano il terzo residuo. Anche un quarto residuo è importante per la catalisi perché stabilizza l intermedio (ossianione) che si forma nel primo stadio della reazione: Nel caso della chimotripsina è Gly, nella subtilisina è asparagina (Asn) e nella papaina è glutammina (Gln). Le treonin peptidasi utilizzano un solo residuo per la catalisi, posizionato all N-terminale (di conseguenza vengono chiamate Idrolasi con nucleofilo N-terminale). Ne fanno parte anche alcune serin e cistein peptidasi.
8 Aspartato peptidasi Non utilizzano altri residui oltre all aspartato. Metallo peptidasi Altri residui sono coinvolti nella catalisi, ma non si sa esattamente quale sia il loro ruolo. Per le metallo peptidasi che utilizzano due ioni metallici, sono importanti due residui, rappresentati spesso dal glutammato e dall aspartato.
9 Terminologia della specificità delle peptidasi: il sistema di Nomenclatura di Schechter e Berger I residui dell Enzima si indicano con S N-term Sn - S3 - S2 S1 * S1 S2 S3.. - Sn C-term I residui del Substrato con P N-term Pn - P3 - P2 P1 + P1 P2 P3.. - Pn C-term dove: * indica il sito catalitico dell enzima + indica il legame che viene idrolizzato
10 LE PEPTIDASI (EC 3-IDROLASI) H 2 O
11 Classificazione delle peptidasi Attualmente vengono utilizzati tre sistemi per raggruppare le PEPTIDASI. 1. Il Meccanismo catalitico 2. Il Tipo di reazione catalizzata 3. La Struttura Molecolare e la Omologia
12 1. MECCANISMO CATALITICO Il meccanismo catalitico è in relazione ai GRUPPI CHIMICI (di seguito richiamati), responsabili della idrolisi del legame peptidico. 1. Aspartato (aspartil) peptidasi (24 enzimi-a) 2. Cisteina (cistein) peptidasi (98 enzimi-c) 3. Glutammato (glutammil) peptidasi (2 enzimi- G) 4. Metallo peptidasi (102 enzimi-m) 5. Asparagina peptidasi (10 enzimi- N) 6. Peptidasi miste (3 enzimi- P) 7. Serina (serin) peptidasi (67 enzimi-s) 8. Treonina (treonin) peptidasi (6 enzimi- T) 9. Peptidasi con meccanismo catalitico sconosciuto (9 enzimi; U- collagenasi)
13 Consideriamo ad esempio le serin-proteasi e tra queste il meccanismo catalitico della CHIMOTRIPSINA: La reazione catalizzata dalla chimotripsina è un esempio di catalisi acido-basica e catalisi covalente: La prima fase è quella di acilazione: viene rotto il legame peptidico e si forma un legame estereo tra il C carbonilico del substrato e la catena laterale di un residuo di Ser dell enzima. Nella fase di deacilazione il legame estere viene idrolizzato e viene rigenerato l enzima libero. Serina 195 Istidina 57 Aspartico 102
14 GLI AMMINOACIDI DEL SITO CATALITICO Nucleofilo: Ser 195 Quarto residuo (Gly) importante pe la catalisi perché stabilizza l intermedio (ossianione) Base: His57 Terzo residuo: Asp102
15 Carica negativa buco dell ossianione
16 R1= amminoacido aromatico ---Asp102
17 Tuttavia, questa classificazione ha molte limitazioni, in quanto i membri di ciascuna famiglia possono avere strutture molecolari e meccanismi catalitici diversi. Infatti, nel caso delle serin e cistein peptidasi la base è generalmente un residuo di istidina o di lisina. Quando la base è un istidina, generalmente interviene un terzo residuo (triade catalitica), che orienta l anello imidazolico dell istidina e aiuta a caricare uno degli atomi di azoto dell anello: serina peptidasi (chimotripsina ) aspartato cisteina peptidasi asparagina (papaina), aspartato o glutammato. Ci sono molte serin e cistein peptidasi che però non utilizzano il terzo residuo. Anche un quarto residuo è importante per la catalisi perché stabilizza l intermedio (ossianione) che si forma nel primo stadio della reazione: Nel caso della chimotripsina è Gly, nella subtilisina è asparagina (Asn) e nella papaina è glutammina (Gln). Vedi diapositive precedenti
18 2. TIPO DI REAZIONE CATALIZZATA Tutte le peptidasi catalizzano la stessa reazione: idrolisi del legame peptidico. Tuttavia, quello che le rende diverse è: 1. la posizione del legame nella struttura primaria della proteina substrato; 2. la presenza di altri residui vicino al legame idrolizzabile; 3. altre caratteristiche
19 2.1 Endopeptidasi Endopeptidasi (EC ) Catalizzano l idrolisi del legame peptidico internamente alla catena, lontano da N- e C-terminale. Es.: Tripsina Chimotripsina Pepsina NH 2 Papaina (L attività proteolitica del lattice di papaia è nota fin dal 1880 (e.g. Martin, 1884). 1. Alcune endopeptidasi sono attive solo su piccoli substrati oligopeptidasi. 2. Le endopeptidasi iniziano la digestione delle proteine alimentari, generando nuovi N- e C-terminali che rappresenteranno il nuovo substrato per le esopeptidasi che completeranno il processo. Le endopeptidasi inoltre: 3. Rimuovono i peptidi segnale dalle proteine di secrezione; 4. Promuovono la maturazione di proteine precursore COOH
20 5- a seconda di dove avviene il taglio, possono dare prodotti differenti L enzima taglia sul gruppo carbonilico dell amminoacido riconosciuto Sequenza substrato: H 2 N Val Thr Ala Met Phe Val Leu His Gly COOH Prodotti: H 2 N Val Thr Ala Met Phe COOH + H 2 N Val Leu His Gly COOH L enzima taglia sul gruppo ammidico dell amminoacido riconosciuto Sequenza substrato: H 2 N Val Thr Ala Met Phe Val Leu His Gly COOH Prodotti: H 2 N Val Thr Ala Met COOH + H 2 N Phe Val Leu His Gly COOH
21 2.2 Peptidasi omega. Non richiedono residui N- o C-terminali liberi nel substrato. Tuttavia spesso agiscono vicino all una o all altra estremità. Alcune peptidasi omega catalizzano la scissione di legami isopeptidici (catena laterale di Asn nell invecchiamento delle proteine: sequenze Asn-Gly, Asn-Ser, Asn-His); ubiquitinil idrolasi; piroglutammil peptidasi, etc 2.3 Esopeptidasi Richiedono o un gruppo ammino-terminale o uno carbossi-terminale libero, o entrambi, e idrolizzano il legame a non più di tre residui di distanza dal gruppo terminale. Le esopeptidasi vengono ulteriormente suddivise in: 1. Amminopeptidasi 2. Carbossipeptidasi 3. Dipeptidil-peptidasi 4. Tripeptidil-peptidasi 5. Peptidil-dipeptidasi 6. Dipeptidasi
22 2.2.1 Amminopeptidasi Amminopeptidasi (EC ) NH 2 COOH Liberano un singolo residuo amminoacidico a partire dall N-terminale libero Carbossipeptidasi Carbossi peptidasi NH 2 COOH (EC ) Liberano un singolo residuo amminoacidico a partire dal C-terminale libero Dipeptidil-peptidasi Dipeptidil peptidasi NH 2 COOH (EC ) Liberano un dipeptide a partire dall N-terminale libero Tripeptidil-peptidasi Liberano un tripeptide a partire dall N-terminale libero Peptidil-dipeptidasi Peptidil dipeptidasi (EC ) NH 2 COOH Liberano un dipeptide a partire dal C-terminale libero Dipeptidasi Dipeptidasi (EC ) NH 2 COOH Liberano amminoacidi da un dipeptide e richiedono che sia il C- che l Nterminale siano liberi.
23 3. Struttura molecolare e omologia E il tipo di classificazione più recente perché dipende dalla disponibilità di informazioni circa la sequenza amminoacidica e la struttura tridimensionale delle proteasi, informazioni ottenute a partire dagli anni 90. Questo tipo di classificazione è quello adottato dal database MEROPS, che assegnata ogni peptidasi ad una FAMIGLIA sulla base delle omologie, raggruppa le famiglie in CLAN sulla base della stessa origine evolutiva (analoghe strutture terziarie, tipo di residui nel sito catalitico o motivi di sequenza comuni intorno al sito catalitico). FAMIGLIE: 1. Aspartato (aspartil) peptidasi (A) 2. Cisteina (cistein) peptidasi (C) 3. Glutammato (glutammil) peptidasi (G) 4. Metallo peptidasi (M) 5. Asparagina peptidasi (N) 6. Peptidasi mista (P) 7. Serina (serin) peptidasi (S) 8. Treonina (treonin) peptidasi (T) 9. Peptidasi con funzione sconosciuta (U) CLAN: Ogni clan si identifica con due lettere, di cui la prima rappresenta il tipo catalitico delle famiglie incluse nel clan. Alcune famiglie non possono ancora essere assegnate al clan, e, quando è richiesto, una famiglia viene descritta come appartenente al clan A-, C-, G-, M-, N-, P-, S-, T- o U-, a seconda del tipo catalitico.
24
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
3.3.2. ALIMENTI DI ORIGINE VEGETALE. 3.3.2.1. Verdure
 3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
Digestione e assorbimento delle proteine
 Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
Digestione e assorbimento delle proteine Metabolismo delle proteine Le proteine sono formate da catene di α- aminoacidi della serie L uniti tra loro dal legame peptidico Le proteine sono composte da 20
mediante proteasi industriali
 Valorizzazione delle farine disoleate mediante proteasi industriali Alessandra Stefan Unità operativa: CSGI (Consorzio per lo Sviluppo dei Sistemi a Grande Interfase, Firenze) Dipartimento di Farmacia
Valorizzazione delle farine disoleate mediante proteasi industriali Alessandra Stefan Unità operativa: CSGI (Consorzio per lo Sviluppo dei Sistemi a Grande Interfase, Firenze) Dipartimento di Farmacia
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
Traduzione dell informazione genetica (1)
 Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
INTRODUZIONE ALLA PROTEINE BCP 1-2
 INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Digestione delle proteine: 6 fasi
 orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Amminoacidi e Proteine
 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili.
 Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili. La sensibilita delle vie di trasduzione dipende da 3 fattori: -l affinita
Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili. La sensibilita delle vie di trasduzione dipende da 3 fattori: -l affinita
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 18
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 18 I meccanismi di catalisi Concetti chiave: Le catene laterali degli amminoacidi in grado di donare o accettare protoni possono
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 18 I meccanismi di catalisi Concetti chiave: Le catene laterali degli amminoacidi in grado di donare o accettare protoni possono
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CAPITOLO 2 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE
 CAPITOLO 2 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE Analisi della composizione amminoacidica delle proteine La determinazione della composizione amminoacidica di una proteina permette di sapere da
CAPITOLO 2 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE Analisi della composizione amminoacidica delle proteine La determinazione della composizione amminoacidica di una proteina permette di sapere da
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi
 Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
Capitolo 4: Le proteine: ossidazione degli amminoacidi, produzione dell urea e biosintesi degli amminoacidi proteine della dieta nucleotidi, ammine biologiche amminoacidi proteine intracellulari ciclo
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O APPLICAZIONI INDUSTRIALI Gli enzimi sono molto utilizzati nell'industria chimica e in altre applicazioni industriali che richiedono catalizzatori estremamente specifici. Le principali
Continua Peptidasi H 2 O APPLICAZIONI INDUSTRIALI Gli enzimi sono molto utilizzati nell'industria chimica e in altre applicazioni industriali che richiedono catalizzatori estremamente specifici. Le principali
I LIPIDI (GRASSI) Cosa sono
 I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
I LIPIDI (GRASSI) Cosa sono Comunemente chiamati "grassi", i lipidi comprendono una grande varietà di molecole, accomunate dalla caratteristica di essere insolubili in acqua. I lipidi più importanti dal
TRASCRIZIONE DEL DNA, TRADUZIONE DELL RNA
 TRASCRIZIONE DEL DNA, TRADUZIONE DELL RNA TRADUZIONE La traduzione e il processo con cui viene sintetizzata un data proteina, attraverso reazioni chimiche di polimerizzazione di amminoacidi, in una
TRASCRIZIONE DEL DNA, TRADUZIONE DELL RNA TRADUZIONE La traduzione e il processo con cui viene sintetizzata un data proteina, attraverso reazioni chimiche di polimerizzazione di amminoacidi, in una
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
FUNZIONI DELLE PROTEINE
 FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
ALCOLI, ETERI, TIOLI. Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3
 ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Una proteina nella rete: Caccia al tesoro bioinformatica
 Una proteina nella rete: Caccia al tesoro bioinformatica Nel corso di questa attivita utilizzeremo alcune delle piu importanti banche dati disponibili in rete per cercare informazioni su una proteina.
Una proteina nella rete: Caccia al tesoro bioinformatica Nel corso di questa attivita utilizzeremo alcune delle piu importanti banche dati disponibili in rete per cercare informazioni su una proteina.
Lezione 2. Sommario. Bioinformatica. Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine. Mauro Ceccanti e Alberto Paoluzzi
 Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
LE PROTEINE. Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza:
 LE PRTEINE Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza: PRTEINE CATALITICHE PRTEINE REGLATRICI PRTEINE DIFESA PRTEINE
LE PRTEINE Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza: PRTEINE CATALITICHE PRTEINE REGLATRICI PRTEINE DIFESA PRTEINE
Capitolo 6 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE
 Capitolo 6 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE Analisi della composizione amminoacidica delle proteine La determinazione della composizione amminoacidica di una proteina permette di sapere da
Capitolo 6 STUDIO DELLA STRUTTURA PRIMARIA DELLE PROTEINE Analisi della composizione amminoacidica delle proteine La determinazione della composizione amminoacidica di una proteina permette di sapere da
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
I peptidi sono polimeri formati da più amminoacidi, coniugati attraverso legami detti ammidici o peptidici.
 MODULO 5 IL METABOLISMO DEI COMPOSTI AZOTATI RICHIAMI SULLA CHIMICA DI AMMINO ACIDI E PROTEINE Introduzione Gli amminoacidi sono composti organici caratterizzati dalla presenza nella molecola di un gruppo
MODULO 5 IL METABOLISMO DEI COMPOSTI AZOTATI RICHIAMI SULLA CHIMICA DI AMMINO ACIDI E PROTEINE Introduzione Gli amminoacidi sono composti organici caratterizzati dalla presenza nella molecola di un gruppo
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 32
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 32 La degradazione delle proteine Concetti chiave: La digestione delle proteine avviene ad opera di specifiche proteasi. Per
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 32 La degradazione delle proteine Concetti chiave: La digestione delle proteine avviene ad opera di specifiche proteasi. Per
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
MEMBRANE. struttura: fosfolipidi e proteine
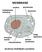 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
METABOLISMO delle PROTEINE
 METABOLISMO delle PROTEINE - Amminoacidi - Nucleotidi AZOTO essenziale per la vita In natura -N 2 atmosferico (N.B. N N triplo legame, molta energia per scinderlo) - ione nitrato NO 3 presente nel suolo
METABOLISMO delle PROTEINE - Amminoacidi - Nucleotidi AZOTO essenziale per la vita In natura -N 2 atmosferico (N.B. N N triplo legame, molta energia per scinderlo) - ione nitrato NO 3 presente nel suolo
26 Aprile 1915, 81 compleanno
 Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
Il dogma centrale della biologia. molecolare
 Il dogma centrale della biologia Cell molecolare Transcription Translation Ribosome DNA mrna Polypeptide (protein) L informazione per la sintesi delle proteine è contenuta nel DNA. La trascrizione e la
Il dogma centrale della biologia Cell molecolare Transcription Translation Ribosome DNA mrna Polypeptide (protein) L informazione per la sintesi delle proteine è contenuta nel DNA. La trascrizione e la
Chaperon molecolari e ripiegamento delle proteine
 UNIVERSITA DEGLI STUDI DI CAGLIARI Facoltà di Scienze Matematiche, Fisiche e Naturali Dipartimento di Scienze Applicate ai Biosistemi Biochimica e Biologia Molecolare Chaperon molecolari e ripiegamento
UNIVERSITA DEGLI STUDI DI CAGLIARI Facoltà di Scienze Matematiche, Fisiche e Naturali Dipartimento di Scienze Applicate ai Biosistemi Biochimica e Biologia Molecolare Chaperon molecolari e ripiegamento
Gli enzimi. Proprietà generali Classificazione e nomenclatura Catalisi enzimatica
 Gli enzimi Proprietà generali Classificazione e nomenclatura Catalisi enzimatica En-zima εν ζυμη nel lievito Enzima termine generico per definire un catalizzatore biologico Tranne che diversamente indicato,
Gli enzimi Proprietà generali Classificazione e nomenclatura Catalisi enzimatica En-zima εν ζυμη nel lievito Enzima termine generico per definire un catalizzatore biologico Tranne che diversamente indicato,
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
UNIWEB- GUIDA STUDENTE INSERIMENTO PIANO DEGLI STUDI ON LINE
 UNIWEB- GUIDA STUDENTE INSERIMENTO PIANO DEGLI STUDI ON LINE In queste pagine vengono illustrate le procedure da seguire per l inserimento del piano degli studi tramite Uniweb per quei corsi di laurea
UNIWEB- GUIDA STUDENTE INSERIMENTO PIANO DEGLI STUDI ON LINE In queste pagine vengono illustrate le procedure da seguire per l inserimento del piano degli studi tramite Uniweb per quei corsi di laurea
Degradazione delle proteine della dieta. Catabolismo degli aminoacidi
 Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
PROTEINE Proteine ed aminoacidi Le proteine o protidi sono composti azotati ad elevato peso molecolare Rappresentano i costituenti fondamentali del
 PROTEINE Proteine ed aminoacidi Le proteine o protidi sono composti azotati ad elevato peso molecolare Rappresentano i costituenti fondamentali del protoplasma Hanno grandissima importanza anche alimentare
PROTEINE Proteine ed aminoacidi Le proteine o protidi sono composti azotati ad elevato peso molecolare Rappresentano i costituenti fondamentali del protoplasma Hanno grandissima importanza anche alimentare
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 8 IL METABOLISMO DEI COMPOSTI AZOTATI 1 Gli amminoacidi sono coinvolti prevalentemente in processi plastici di sintesi e di degradazione, grazie ai quali le cellule
Niccolò Taddei - Biochimica Capitolo 8 IL METABOLISMO DEI COMPOSTI AZOTATI 1 Gli amminoacidi sono coinvolti prevalentemente in processi plastici di sintesi e di degradazione, grazie ai quali le cellule
Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
delegate a conservare e trasmettere l'informazione genetica. Oggi é noto che sono gli acidi
 8. Le proteine Il termine "proteina" (dal greco προτειος: di primaria importanza) fu coniato nel 1838 dal chimico svedese J. Berzelius 1 quando ancora si riteneva che le proteine fossero le molecole delegate
8. Le proteine Il termine "proteina" (dal greco προτειος: di primaria importanza) fu coniato nel 1838 dal chimico svedese J. Berzelius 1 quando ancora si riteneva che le proteine fossero le molecole delegate
Marinella Bosetto Irene Lozzi. Elementi di biochimica agraria
 A07 25 Marinella Bosetto Irene Lozzi Elementi di biochimica agraria Copyright MMVI ARACNE editrice S.r.l. www.aracneeditrice.it [email protected] via Raffaele Garofalo, 133 A/B 00173 Roma (06) 93781065
A07 25 Marinella Bosetto Irene Lozzi Elementi di biochimica agraria Copyright MMVI ARACNE editrice S.r.l. www.aracneeditrice.it [email protected] via Raffaele Garofalo, 133 A/B 00173 Roma (06) 93781065
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n
 Alcani ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n H 2n+1, m/z 43, 57, 71, 85, 99 ), con intensità massima per i cationi a
Alcani ione molecolare poco intenso ma visibile frammentazioni di tutti i legami C-C: serie di picchi separati di 14 u.m.a. (C n H 2n+1, m/z 43, 57, 71, 85, 99 ), con intensità massima per i cationi a
3.3. UMAMI NEGLI ALIMENTI
 3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
Struttura delle proteine
 Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Meccanismo tio-templato delle NRPS
 Meccanismo tio-templato delle NRPS Meccanismo tio-templato delle NRPS Per l attività delle NRPS è necessaria l aggiunta della 4- fosfopanteteina sulla serina del sito attivo del dominio di tiolazione.
Meccanismo tio-templato delle NRPS Meccanismo tio-templato delle NRPS Per l attività delle NRPS è necessaria l aggiunta della 4- fosfopanteteina sulla serina del sito attivo del dominio di tiolazione.
Visualizzazioni 3D. Informatica. Matrice di voxel. Tipi di dato. Dati vettoriali. Tecniche di rappresentazione
 Informatica Lezione VIII Visualizzazione 3D di proteine Visualizzazioni 3D Rappresentazione di strutture/oggetti tridimensionali Risultato di un esperimento modello teorico dati fisici astrazione 1 Lezione
Informatica Lezione VIII Visualizzazione 3D di proteine Visualizzazioni 3D Rappresentazione di strutture/oggetti tridimensionali Risultato di un esperimento modello teorico dati fisici astrazione 1 Lezione
BIOMOLECOLE STRUTTURA E FUNZIONE
 BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
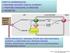 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI Berg et al., BIOCHIMICA 6/E, Zanichelli editore S.p.A. Copyright 2007 PROTEINE INGERITE CON GLI ALIMENTI
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI Berg et al., BIOCHIMICA 6/E, Zanichelli editore S.p.A. Copyright 2007 PROTEINE INGERITE CON GLI ALIMENTI
Replicazione del DNA
 Replicazione del DNA la replicazione del DNA viene effettuata da ENZIMI: DNA-polimerasi (catalizza la formazione del legame fosfodiestere) ogni filamento fa da stampo (enzima diretto dallo stampo) le DNA-polimerasi
Replicazione del DNA la replicazione del DNA viene effettuata da ENZIMI: DNA-polimerasi (catalizza la formazione del legame fosfodiestere) ogni filamento fa da stampo (enzima diretto dallo stampo) le DNA-polimerasi
MODIFICAZIONI POST-TRADUZIONALI DELLE PROTEINE
 MODIFICAZIONI POST-TRADUZIONALI DELLE PROTEINE Nell ultima fase della sintesi proteica la catena polipeptidica neosintetizzata assume spontaneamente la sua conformazione nativa (massimo numero di legami
MODIFICAZIONI POST-TRADUZIONALI DELLE PROTEINE Nell ultima fase della sintesi proteica la catena polipeptidica neosintetizzata assume spontaneamente la sua conformazione nativa (massimo numero di legami
L integrazione proteica nelle diverse fisiopatologie
 Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Arko Enzym. Innovazione con enzimi attivi. Gli Arko Enzym sono frutto della biotecnologia. Perchè gli Enzimi? Interesse degli enzimi specifici.
 Arko Enzym Innovazione con enzimi attivi Perchè gli Enzimi? Gli enzimi sono una soluzione interessante per risolvere numerosi problemi, in particolare nel campo della digestione e sono un ottima alternativa
Arko Enzym Innovazione con enzimi attivi Perchè gli Enzimi? Gli enzimi sono una soluzione interessante per risolvere numerosi problemi, in particolare nel campo della digestione e sono un ottima alternativa
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 7
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Capitolo 17. Risposte alle domande interne al capitolo. 17.1 (p. 501) a. glicina. b. prolina. c. treonina. d. aspartato
 apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
Mutagenesi: introduzione di alterazioni in una sequenza nucleotidica. Mutagenesi random: le mutazioni avvengono a caso su un tratto di DNA.
 Mutagenesi: introduzione di alterazioni in una sequenza nucleotidica Mutagenesi random: le mutazioni avvengono a caso su un tratto di DNA. In genere si ottengono trattando il DNA con agenti chimici (es.
Mutagenesi: introduzione di alterazioni in una sequenza nucleotidica Mutagenesi random: le mutazioni avvengono a caso su un tratto di DNA. In genere si ottengono trattando il DNA con agenti chimici (es.
La reazione da bilanciare è quindi: Cu + HNO 3 CuNO 3 + NO. Le due semireazioni da bilanciare saranno: HNO 3 NO (1) Cu CuNO 3 (2)
 Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
Introducendo rame metallico (Cu) in acido nitrico diluito (HNO 3 ) si forma nitrato di rame (CuNO 3 ) e gas ossido nitrico (NO). Scrivere l equazione chimica bilanciata della reazione. La reazione da bilanciare
METABOLISMO AMINO ACIDI
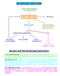 METABOLISMO AMINO ACIDI AMINO ACIDI ESOGENI (ALIMENTAZIONE) POOL AMINO ACIDI PROTEINE DEMOLIZIONE AMINE BIOGENE ORMONI PROTEICI BASI AZOTATE.. SCHELETRO CARBONIOSO NH 3 RESINTESI CICLO KREBS LIPIDI (AA
METABOLISMO AMINO ACIDI AMINO ACIDI ESOGENI (ALIMENTAZIONE) POOL AMINO ACIDI PROTEINE DEMOLIZIONE AMINE BIOGENE ORMONI PROTEICI BASI AZOTATE.. SCHELETRO CARBONIOSO NH 3 RESINTESI CICLO KREBS LIPIDI (AA
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
