aa Proteine Struttura delle Proteine α Amminoacidi
|
|
|
- Giacinta Miele
- 8 anni fa
- Visualizzazioni
Transcript
1 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine, emoglobina ecc.) Protezione (tossine, allergeni ecc.) rmoni (insulina, ormoni della crescita ecc.) Struttura delle Proteine α Amminoacidi 2 C Cα R - 2 sul carbonio adiacente al -C. Glicina, 2 -C 2 -C, è il più semplice. Con -R come catena laterale, essi sono chirali. La maggior parte degli amminoacidi naturali sono L-amminoacidi. 1
2 Stereochimica degli α-amminoacidi Amminoacidi costituenti le proteine Ventidue α-amminoacidi standard. Differiscono nella natura della catena laterale: - o alchile contiene un Contiene lo zolfo Contiene un azoto non basico. Un gruppo C addizionale Un azoto basico Amminoacidi Essenziali Treonina (Thr) Lisina (Lys) Valina (Val) Fenilalanina (Phe) Triptofano (Trp) Metionina (Met) Leucina (Leu) Isoleucina (Ile) 2
3 Proteine Complete forniscono tutti gli amminoacidi essenziali. esempi: quelle nella carne, pesce, latte, uova. Le proteine nei vegetali sono generalmente incomplete. I vegetariani devono mangiare molti tipi differenti di vegetali, oppure supplire la dieta ad esempio con uova o latte. 3
4 Aminoacidi Rari 4-idrossiprolina, 5-idrossilisina presente nel collagene. Acido D-Glutammico nelle pareti cellulari dei batteri. D-Serina nei lombrichi. Acido γ-amminobutirrico, è un neurotrasmettitore. β-alanina, costituente della vitamina acido pantotenico. Zwitterione Gli Amminoacidi esistono come ioni dipolari. -C perde +,mentre - 2 acquista +. La struttura effettiva dipende dal p Proprietà degli Amminoacidi Punti di fusione alti, oltre i 200 C Più solubili in acqua che in solventi non polari. Un momento di dipolo più grande di quello di acidi o ammine semplici. Più acidi della maggior parte degli acidi carbossilici e meno basici di molte ammine. + _ pk a = 10 3 C C pk b = 12 R 4
5 Struttura e p Punto isoelettrico p a cui gli amminoacidi esistono come zwitterione (neutro). Dipende dalla struttura della catena laterale. Amminoacidi acidi, pi ~ 3. Amminoacidi basici, pi ~ 9. Amminoacidi neutri, pi ~ 5-6. Elettroforesi Proteine cariche negativamente si muovono verso l anodo Posizione della miscela originale Proteine cariche positivamente si muovono verso il catodo 5
6 alanina + pk - a =2.35 pk a = C 3 C 3 C pi = 6.11 arginina pk a =2.01 pk a =9.04 pk a = pi =
7 lisina pk a =2.18 pk a =8.95 pk a = pi = 9.74 istidina pk a =1.77 pk a =6.10 pk a = pi = 7.64 Acido aspartico pk + + a =2.10 pk a =3.86 pk a = pi =
8 cisteina S pk a =2.05 pk a =8.00 pk a =10.25 S S - S - pi = 5.02 Tirosina pk + a =2.20 pk a =9.11 pk a = pi = 5.63 Equazione di enderson-asselbalch [ base coniugata] p = pk a + log acido debole [ ] 8
9 Alcune Sintesi di laboratorio degli amminoacidi Amminazione riduttiva Sintesi da a aloacidi Sintesi di Gabriel-estere malonico sintesi di Strecker Amminazionone Riduttiva Questo metodo di sintesi è biomimetico, cioè mima il processo biologico di sintesi. Si fa reagire un α-chetoacido con ammoniaca, poi si riduce l imina con 2 /Pd. el processo di laboratorio si ottiene una miscela racemica! R C C 3 R C C _ Pd R 2 _ C C Sintesi da α-aloacidi La reazione di ell-volhard-zelinsky permette di sintetizzare gli α-bromoacidi. Il bromo può essere sostituito con un gruppo ammino facendo reagire l α-bromoacido con un eccesso di ammoniaca. Si ottiene una miscela racemica. 9
10 Sintesi di Gabriel-Estere Malonico L ammino gruppo viene protetto come ammide. Il gruppo carbossilico viene protetto come estere. La posizione α è attivata ulteriormente dalla presenza del gruppo estereo temporaneo Sintesi di Strecker La prima sintesi nota di un amminoacido risale al La reazione di un aldeide con 3 dà un imina. Lo ione cianuro attacca l immina protonata. Il risultato è un α-ammino nitrile che viene idrolizzato ad acido carbossilico. Meccanismo della sintesi di Strecker Stadio 1: formazione dell immina Stadio 2: attacco dello ione cianuro L idrolisi del nitrile porta all amminoacido. 10
11 Risoluzione degli Amminoacidi solitamente, solo l enantiomero L- e biologicamente attivo. Si converte l amminoacido in un sale, utilizzando un acido o una base chirale. Si ottiene cosi la miscela dei due Sali diastereomerici che possono essere separati Si utilizza un enzima come l deacilasi che reagisce solo con uno dei due enantiomeri. Risoluzione di racemati: alcuni esempi Formazione di esteri diasteromerici R R C C + + R* 3 C C R* + 2 Risoluzione enzimatica Struttura dei Peptidi Il legame peptidico è un legame ammidico. Le ammidi sono composti molto stabili e neutri. 11
12 Alternanza dei piani in un polipeptide Bradichinina Un oligopeptide non proteico. Convenzionalmente le strutture dei peptidi vengono disegnate con l amminoacido -terminale sulla sinistra. Il nome dei peptidi è costruito nominando tutti gli amminoacidi che lo compongono a partire dall amminoacido -terminale: arginilprolilprolil arginina. Legame disolfuro La cisteina può formare ponti disolfuro. 12
13 Determinazione della struttura di un peptide Rottura dei ponti disolfuro Determinazione della composizione in amminoacidi Sequenziazione dall -terminale Analisi dei residui C-terminali Idrolisi parziale Il primo passaggio è la rottura del ponte disolfuro Il passaggio successivo è la determinazione del tipo e del numero degli amminoacidi contenuti Si Separano le catene polipeptidiche. Si mette a bollire con Cl 6 M per 24 ore. Gli amminoacidi si separano con un analizzatore. 13
14 Reazione con la inidrina Utilizzata per visualizzare le macchie o le bande degli amminoacidi separati per cromatografia o elettroforesi. Colore porpora intenso formato con tutti gli amminoacidi La prolina e l idrossiprolina danno una colorazione gialla. 14
15 Sequenziazione dall -terminale Degradazione di Edman: reazione con fenil isotiocianato seguita dall idrolisi rimuove l amminoacido -terminale. La feniltioidantoina viene identificata per via gascromatografica. È utilizzata con buoni risultati per polipeptidi con meno di 30 amminoacidi. Esempio di degradazione di Edman per ossitocina bovina Sequenziazione del residuo C terminale L enzima carbossipeptidasi rompe selettivamente il C-terminale. Riduzione della funzione carbossilica a funzione alcolica Idrazinolisi del peptide. 15
16 Idrolisi parziale Formazione di un legame ammidico 16
17 Sintesi di un dipeptide Sintesi di un peptide in fase liquida Dapprima, si protegge il gruppo terminale. Si attiva il gruppo carbossilico del medesimo amminoacido. Si fa avvenire la reazione con l amminoacido successivo. Per sintetizzare un polipeptide si ripete l operazione di attivazione ed accoppiamento. Terminata la sintesi si rimuove il gruppo protettivo. Sintesi di un tripeptide 17
18 Sintesi di un tripeptide Sintesi di peptidi su fase solida La catena polipeptidica da sintetizzare è ancorata ad un letto di piccoli granuli di polistirene. Gli intermedi non devono essere purificati. I reagenti in eccesso vengono lavati via con un idoneo solvente. Il processo può essere automatizzato. Permette di costruire peptidi più lunghi rispetto alla sintesi in soluzione. Sintesi automatica di Merrifield 1 Stadio 18
19 Sintesi automatica di Merrifield 2 Stadio Sintesi automatica di Merrifield 3 Stadio Sintesi automatica di Merrifield 4 Stadio 19
20 Sintesi automatica di Merrifield 5 Stadio Classificazione delle proteine Semplici: idrolizzano solo ad amminoacidi. Coniugate: sono legate ad un gruppo non proteico come zuccheri, acidi nucleici, lipidi. Fibrose: lunga e filamentosa, insolubile in acqua, funzione strutturale. Globulari: ripiegata in forma sferica, funzione enzimatica, ormonale, o di trasporto ormonale. Proteine fibrose Proteine globulari 20
21 Legame disolfuro Schema di una catena polipeptidica con legami a ponte disolfuro intercatena ed intracatena ote: i ponti disolfuro intracatena legano insieme due parti dello stesso polipeptide, mentre il legame intercatena unisce due catene di polipeptidi differenti. Formazione del legame disolfuro Il ponte disolfuro contribuisce alla forma della proteina 21
22 Livelli delle struttura delle proteine Primaria: la sequenza degli amminoacidi nella catena ed i legami disolfuro. Secondaria: struttura formata dai legami idrogeno. Esempio è l α-elica e il foglietto piegato (struttura β ). Terziaria: la conformazione completa 3-D. Quaternaria: l associazione di due o più catene peptidiche per formare le proteine. Livelli delle struttura delle proteine Alfa elica gni ossigeno carbonilico può formare un legame idrogeno con l - dell avvolgimento successivo dell elica. 22
23 Vista laterale di un segmento di un α elica di una proteina Vista dall alto di un segmento di un α elica di una proteina Foglietti piegati (struttura β ) gni ossigeno carbonilico forma un legame idrogeno con un - di una catena peptidica adiacente. 23
24 STRUTTURA DELLE PRTEIE Struttura primaria: sequenza aminoacidica Struttura secondaria: ripiegamento della catena lungo un asse Cheratine: α- e β-cheratine Collageno: tessuto connettivo Struttura terziaria: ripiegamento tridimensionale delle catene polipeptidiche. Struttura terziaria Spesso determinata per diffrazione ai raggi X Esempi di proteine globulari sono mioglobina, lisozima, ribonucleasi, citocromo C Caratteristiche comuni: Ciascuna proteina ha una struttura caratteristica Ripiegamento compatto con poco spazio all interno Localizzazione all esterno di quasi tutti i gruppi idrofilici Localizzazione all interno dei gruppi idrofobici Possono contenere tratti sia di α-elica sia di β-foglietto 24
25 Mioglobina, una proteina globulare La sequenza determina la struttura La denaturazione dà luogo a conformazioni casuali della catena polipeptidica. Alcune proteine denaturate possono riacquistare la loro attività biologica Esempio classico la ribonucleasi. Denaturazione e rinaturazione della ribonucleasi 25
26 Stabilizzazione della struttura terziaria Legame idrogeno tra gruppi peptidici Legame idrogeno tra residui R polari Interazioni idrofobiche Legame idrogeno tra residui R carichi L interazione predominante è l interazione idrofobica Le interazioni Struttura quaternaria Caratteristica delle proteine oligomeriche La struttura quaternaria designa l interazione tra le varie unità della proteina. Alcune proteine che hanno struttura quaternaria dopo la denaturazione possono essere rinaturate. 26
27 Sommario delle Strutture Alterazioni chimiche negli amminoacidi Alterazioni chimiche negli amminoacidi 27
28 Alterazioni chimiche negli amminoacidi 28
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Amminoacidi e Proteine
 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
AMMINO ACIDI. L equilibrio è regolato dal ph
 AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
PROTEINA GREGGIA (P.G.)
 PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Capitolo 17. Risposte alle domande interne al capitolo. 17.1 (p. 501) a. glicina. b. prolina. c. treonina. d. aspartato
 apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
Lezione 2. Sommario. Bioinformatica. Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine. Mauro Ceccanti e Alberto Paoluzzi
 Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
La biochimica è anche definita la chimica del C :
 Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Peptidi, proteine ed e nzim i i 1
 Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Struttura delle proteine
 Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Traduzione dell informazione genetica (1)
 Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
LE PROTEINE. Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza:
 LE PRTEINE Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza: PRTEINE CATALITICHE PRTEINE REGLATRICI PRTEINE DIFESA PRTEINE
LE PRTEINE Le proteine sono i biopolimeri piu' abbondanti negli organismi viventi e svolgono funzioni biologiche di fondamentale importanza: PRTEINE CATALITICHE PRTEINE REGLATRICI PRTEINE DIFESA PRTEINE
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI
 GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI AMINOACIDI ESSENZIALI Gli aminoacidi indispensabili, noti anche come aminoacidi essenziali, devono essere forniti al corpo con gli alimenti
GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI AMINOACIDI ESSENZIALI Gli aminoacidi indispensabili, noti anche come aminoacidi essenziali, devono essere forniti al corpo con gli alimenti
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 7
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Progetto «Puliamo Garibaldi» Geanina Mihai VD Liceo classico Giulio Cesare
 Progetto «Puliamo Garibaldi» Geanina Mihai VD Liceo classico Giulio Cesare Qual è il rame e qual è lo stagno? E iniziato così questo progetto. Si tratta di «pulire Garibaldi»,quindi di pulire una statua.la
Progetto «Puliamo Garibaldi» Geanina Mihai VD Liceo classico Giulio Cesare Qual è il rame e qual è lo stagno? E iniziato così questo progetto. Si tratta di «pulire Garibaldi»,quindi di pulire una statua.la
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE STRUTTURA E FUNZIONE
 BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
Struttura degli Amminoacidi
 Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 9
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE)
 a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
L E P R O T E I N E. Le proteine sono macromolecole formate dall'unione di molte unità elementari chiamate amminoacidi (AA).
 L E P R O T E I N E ASPETTI GENERALI I protidi o proteine sono i costituenti principali delle cellule, sia animali che vegetali; sono sempre presenti negli esseri viventi dei quali entrano a far parte
L E P R O T E I N E ASPETTI GENERALI I protidi o proteine sono i costituenti principali delle cellule, sia animali che vegetali; sono sempre presenti negli esseri viventi dei quali entrano a far parte
Nota dell editore Presentazione
 00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
Niccolò Taddei - Biochimica apitolo 3 GLI AMMINAOIDI E LE PROTEINE DEGLI ESERIZI 1 Le proteine costituiscono una grande famiglia di biomolecole molto diffuse in natura; sono costituite da unità strutturali
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Competizione tra reazioni di sostituzione e di eliminazione
 Competizione tra reazioni di sostituzione e di eliminazione C δ + δ - CH 2 G Centro elettrofilo δ + H Centro elettrofilo Potenziale buon gruppo uscente Si distinguono due principali meccanismi di eliminazione:
Competizione tra reazioni di sostituzione e di eliminazione C δ + δ - CH 2 G Centro elettrofilo δ + H Centro elettrofilo Potenziale buon gruppo uscente Si distinguono due principali meccanismi di eliminazione:
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
Spettrofotometria e analisi di amminoacidi. Quantizzazione di proteine e di miscele di amminoacidi
 Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
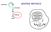 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Aminoacidi. Struttura generale Sono 20 e formano le
 Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE (dal greco proteios, che occupa il primo posto)
 PRTEIE (dal greco proteios, che occupa il primo posto) costituite da una o più catene polipeptidiche; i peptidi sono eteropolimeri lineari formati da 0-50 amminoacidi (aa); si conoscono centinaia di aa
PRTEIE (dal greco proteios, che occupa il primo posto) costituite da una o più catene polipeptidiche; i peptidi sono eteropolimeri lineari formati da 0-50 amminoacidi (aa); si conoscono centinaia di aa
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
AMMINOACIDI. Gli amminoacidi si distinguono in base alla diversità della catena laterale R in ciascuno di essi.
 AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
Marinella Bosetto Irene Lozzi. Elementi di biochimica agraria
 A07 25 Marinella Bosetto Irene Lozzi Elementi di biochimica agraria Copyright MMVI ARACNE editrice S.r.l. www.aracneeditrice.it info@aracneeditrice.it via Raffaele Garofalo, 133 A/B 00173 Roma (06) 93781065
A07 25 Marinella Bosetto Irene Lozzi Elementi di biochimica agraria Copyright MMVI ARACNE editrice S.r.l. www.aracneeditrice.it info@aracneeditrice.it via Raffaele Garofalo, 133 A/B 00173 Roma (06) 93781065
Perché il logaritmo è così importante?
 Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
Si dividono in: N-glicosilate (su Asparagina) O-glicosilate (su Serina o Treonina. Raramente su Tirosina, idrossiprolina, idrossilisina)
 GLICOSILAZIONE La glicosilazione è la modificazione PTM più diffusa. Circa il 50% delle proteine umane sono glicosilate Caratteristica di molte proteine della superficie cellulare e delle d proteine di
GLICOSILAZIONE La glicosilazione è la modificazione PTM più diffusa. Circa il 50% delle proteine umane sono glicosilate Caratteristica di molte proteine della superficie cellulare e delle d proteine di
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
