Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
|
|
|
- Giorgiana Salvatore
- 8 anni fa
- Visualizzazioni
Transcript
1
2 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali
3 LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di riserva proteine contrattili proteine regolatrici proteine di difesa
4 CLASSIFICAZIONE DELLE PROTEINE in base alla funzione biologica che svolgono Classe funzionale Enzimi Esempi Ribonucleasi,catalisi Proteine di regolazione Proteine di trasporto Proteine di riserva Proteine deputate alla mobilità ed alla contrattilità Insulina, tirotropina Emoglobina, albumina sierica Ovoalbumina, ferritina Actina, miosina Proteine strutturali Collagene, fibroina Proteine con funzioni di difesa Anticorpi Proteine particolari Proteina antigelo, resilina
5 CLASSIFICAZIONE DELLE PROTEINE CONIUGATE in base alla natura chimica della componente non - amminoacidica
6 Ogni organismo contiene migliaia di proteine diverse, ognuna con una specifica funzione Gli aminoacidi rappresentano gli elementi costitutivi delle proteine; di tutti gli aminoacidi esistenti in natura solo 20 sono presenti nelle proteine, in quanto espressi dal codice genetico
7 Gli aminoacidi Forma non ionica In soluzione a ph neutro sono in genere ioni dipolari (o anfoioni) tutti gli aminoacidi presentano un gruppo amminico, un gruppo carbossilico ed una catena laterale R variabile nei diversi aminoacidi
8 Gruppi R alifatici, non polari N H 2 H O OH Glicina (gly) N H 2 CH 3 OH O Alanina (ala) H H 3 C N H 2 CH 3 O OH * Valina (val) CH 3 CH 3 CH 3 N H 2 O CH 3 OH N H 2 O OH N H O OH * Leucina (leu) * isoleucina (ile) Prolina (pro)
9 Gruppi R aromatici OH NH N H 2 O OH N H 2 O OH N H 2 O OH * Fenilalanina (phe) Tirosina (tyr) * Triptofano (trp)
10 Gruppi R polari, non carichi OH H 3 C OH SH N H 2 O OH N H 2 O OH N H 2 Serina (ser) * Treonina (thr) Cisteina (cys) O OH S CH 3 O O NH 2 N H 2 O OH * Metionina (met) N H 2 O NH 2 OH Asparagina (asn) N H 2 O OH Glutammina (gln)
11 Gruppi R carichi positivamente NH 3 + NH 2 O OH H N + N H NH 2 * Lisina (lys) *Istidina (hys) Arginina (arg) O OH H 2 N NH+ Gruppi R carichi negativamente N NH 2 O OH O O OH O NH 2 Aspartato (asp) O O O OH NH 2 Glutammato (glu)
12 Come tutte le molecole polimeriche, le proteine possono essere descritte in termini di livelli di organizzazione molecolare : struttura primaria struttura secondaria strutura terziaria struttura quaternaria
13 La sequenza degli AA costituisce la struttura I a delle proteine
14 La struttura primaria di una proteina è la sequenza aminoacidica della sua o delle sue catene polipeptidiche,, se la proteina è costituita da più di un polipeptide; ogni residuo è unito a quello vicino da un legame peptidico. Le proteine sono sintetizzate in vivo legando mediante condensazione uno dopo l altro l i vari aminoacidi in un ordine specificato dalla sequenza nucleotidica di un gene.
15 Le possibilità teoriche di un polipeptide sono illimitate Avendo a disposizione 20 scelte diverse per ogni residuo aminoacidico di una catena polipeptidica, si può immediatamente vedere che è possibile ottenere un numero praticamente infinito di proteine diverse. Chiaramente l evoluzione ha prodotto soltanto un piccolissimo numero di queste proteine teoricamente possibili.
16 Le proteine reali hanno limiti alla dimensioni e alla composizione. In genere le proteine contengono almeno 40 residui; i polipeptidi più piccoli di questa dimensione sono detti semplicemente peptidi. Il polipeptide con le dimensioni più grandi fino ad ora studiato è la TITINA,, una proteina gigantesca contenente residui (2990 kda) ) che partecipa all organizzazione delle strutture ripetitive della fibra muscolare. Ad ogni modo la grande maggioranza dei polipeptidi contiene da 100 a 1000 residui
17 L organizzazione degli atomi in una proteina viene detta conformazione I peptidi presentano regioni, che conferiscono rigidità alla struttura, altre che invece permettono variazioni conformazionali (mediante libera rotaz. intorno ai legami) Le proteine che si trovano nella conformazione più stabile (minore energia libera di Gibbs, G) sono dette proteine native
18 Il gruppo polipeptidico è una struttura rigida e planare, come conseguenza delle interazioni di risonanza che forniscono al legame peptidico circa il 40% di carattere di doppio legame O O - C N C + N H H Lo scheletro o la catena principale di una proteina non è altro che una successione degli atomi che fanno parte dei legami peptidici della catena polipeptidica.
19 Le catene peptidiche non possono assumere strutture 3D casuali L insieme di organizzazioni regolari e ricorrenti nello spazio definiscono la struttura II delle proteine Nelle proteine sono presenti diversi tipi di strutt.ii,, i più rilevanti sono l α-elica e la struttura β-sheet
20 α-elica β-sheet
21 Sia l α-elica sia il foglietto β, sono dette strutture secondarie regolari, in quanto sono composte da residui con valori degli angoli Φ e Ψ che si ripetono. L α-elica è destrorsa. Possiede 3,6 residui per giro e un passo di 5,4 A.
22 Le α-eliche presenti nelle proteine impegnano in media circa 12 residui, che formano più di 3 giri di elica e corrispondono ad una lunghezza di circa 18 A. Questa disposizione porta alla formazione di legami idrogeno molto forti, in quanto, l atomo di idrogeno legato all azoto e l atomo di ossigeno legato al carbonio si trovano alla distanza ottimale di 2,8 A.
23 Foglietto β Come l α-elica il foglietto β utilizza tutta la capacità di formare legami idrogeno dello scheletro del polipeptide. Nel foglietto β i legami ad idrogeno si formano tra catene affiancate invece che tra residui della stessa catena, come nel caso dell α-elica. Si possono avere due tipi di foglietti: Il foglietto β antiparallello in cui le catene vicine che formano legame idrogeno corrono in direzione opposte. Il foglietto β parallelo in cui le catene unite da legame idrogeno corrono invece nella stessa direzione.
24 Un livello ancora più alto di struttura è rappresentato dal dominio Il dominio rappresenta una regione compatta, comprendente aminoacidi, che può essere considerata come un unità strutturale distinta di una catena polipeptidica
25 La diffrazione ai raggi X ha permesso di individuare livelli di organizzazione strutturale superiori alla struttura II delle proteine
26 La struttura III si riferisce alla relazione spaziale tra tutti gli aa di una catena polipeptidica In una struttura III possono trovarsi più strutture II
27 Tra i residui superficiali si stabiliscono legami elettrostatici I legami salini (elettrostatici) uniscono due o più residui i cui gruppi R abbiano carica opposta, ma si stabiliscono anche tra i gruppi ionizzati in posizione α dei residui amminici e carbossi terminali. I ponti disolfuro conferiscono ulteriore stabilità. Questi si stabiliscono tra i residui di cisteina appartenenti alla stessa catena polipeptidica oppure a catene diverse.
28 Le interazioni idrofobiche uniscono i residui posti all interno di una proteina, infatti le catene apolari degli aminoacidi si associano all interno delle proteine globulari. Le interazioni idrofobiche anche se individualmente molto deboli sono presenti in numero talmente elevato da contribuire in maniera fondamentale alla stabilizzazione della struttura della proteina.
29 Le proteine perdono la loro struttura nativa in seguito a denaturazione La denaturazione avviene per azione calore I meccanismi molecolari della denaturazione comprendono: ph estremi solventi (acetone, alcol) soluti (urea, detergenti) riduzione dei legami S-S, S S, interferenza sulla carica netta (repulsione, e rottura dei legami ad H) interazioni idrofobiche
30 Perdita della forma nativa per riduzione dei ponti disolfuro
31 Un ulteriore livello è la struttura IV struttura IV, che si riferisce alle relazioni spaziali tra più polipeptidi o alle sub-unità interne di una proteina
32 Motivi proteici Motivo βαβ Ripiegamento a forcina Motivo αα Motivi a barile barile α-β
33 Motivo a dito di zinco
34 PROTEINE GLOBULARI Sono proteine di forma sferoidale generalmente solubili in acqua e caratterizzate da una struttura terziaria e talvolta da una struttura quaternaria. Sono biologicamente attive (es. enzimi ed immunoglobuline) e costituiscono la più gran parte delle proteine cellulari. La tradizionale classificazione delle proteine globulari è basata sulle caratteristiche chimico-fisiche.
35 Protamine. Sono proteine basiche, presenti nello sperma di alcune specie di pesci Istoni. Sono proteine basiche di basso PM ( ) associate con il DNA nei nuclei cellulari. Prolamine e gluteline. Sono proteine vegetali ricche di prolina e di acido glutammico fra esse: la zeina del mais la gliadina del frumento l'ordina dell'orzo
36 Albumine. Sono proteine acidiche (ph - 5) con PM fra e , ben solubili in acqua e coagulabili al calore. Fra le albumine animali si ricordino quella del siero ematico e quelle dell'uovo e del latte. Globuline. Sono in realtà delle glicoproteine, hanno PM intorno ai , sono solubili in acqua. Le globuline più note sono quelle del sangue
37 PROTEINE FIBROSE Come tipici esempi di proteine fibrose vengono qui considerate le due principali proteine del tessuto connettivo il collagene e l' elastina. Collagene ed elastina coesistono in proporzioni diverse nelle strutture connettivali: nei tendini, ad esempio, prevale largamente il collagene, per contro i legamenti sono ricchi di elastina. Le fibre di collagene sono particolarmente resistenti alla tensione e quelle di elastina sono invece dotate di una certa elasticità, la prevalenza delle une o delle altre riflette il tipo di funzione meccanica della particolare struttura connettivale.
38 Collagene Il collagene, la più abbondante proteina dell' organismo (il 30% circa, di tutte le proteine) costituisce l'intelaiatura extracellulare di tutti gli esseri pluricellulari. E presente in percentuale varia in tutti i tessuti animali ed in misura dominante nei tessuti di sostegno (tendini, legamenti, fasce, cartilagine, ossa e denti). Il collagene viene sintetizzato dai fibroblasti del tessuto connettivo, dagli osteoblasti dell'osso, dai condroblasti della cartilagine e dagli odontoblasti dei denti. L'unità fondamentale del collagene è il tropocollagene, struttura a tripla elica allungata.
39 Elastina La Elastina, di spiccate proprietà elastiche, è la proteina fibrosa predominante nei legamenti e nelle pareti vasali arteriose, alle quali impartisce le note caratteristiche di elasticità.
40
41 Proteine plasmatiche Tra i componenti solubili del plasma ematico le proteine sono le sostanze più rappresentate. La loro concentrazione va da mg/l, circa il 4% di tutte le proteine corporee. Nel plasma esistono quasi 100 proteine diverse che possono essere distinte in 5 gruppi in base al loro comportamento in elettroforesi: albumine α -1 globuline α -2 globuline β - globuline γ - globuline
42 la proteina più rappresentata è l albumina che dàd un contributo essenziale al mantenimento della pressione osmotica del sangue; agisce inoltre come proteina trasportatrice per sostanze lipofiliche (acidi grassi liberi, bilirubina, alcuni ormoni steroidei e vitamine) le globuline partecipano al trasporto dei lipidi, ioni metallici, vitamine, sono una componente importante del sistema di coagulazione e forniscono gli anticorpi del sistema immunitario
43 L elettroforesi permette la separazione delle proteine plasmatiche, la loro caratterizzazione e quantificazione
44 la maggior parte delle proteine plasmatiche viene sintetizzata nel fegato (fanno eccezione le immunoglobuline prodotte dai linfociti T) sono tutte glicoproteine, ad eccezione dell albumina
45 Tipo albumine: α-1 1 globuline esempio Transtirenina, Albumina Antitripsina Antichimotripsina HDL Transcortina Mr KDa α-2 2 globuline β globuline γ globuline Antitrombina III Colinesterasi Proteina legante Vit D LDL Transferrina IgG, IgA, IgM, IgD, IgE , 162, 900, 172, 196
46
47
48 Elevati valori delle immunoglobuline Si riscontrano nel sangue dei pazienti affetti da infezioni croniche, o da epatopatie, o da altre forme morbose croniche, quali l artrite l reumatoide. Ogni infezione induce l aumento l di una determinata immunoglobulina, questo può fornire una utile indicazione per la diagnosi.
49 Una particolare intensa produzione di immunoglobuline, o delle loro catene leggere o pesanti separate, si ha nel mieloma multiplo o plasmacitoma, una neoplasia plasmacellulare del midollo osseo che porta alla progressiva distruzione delle ossa. La concomitante disfunzione del midollo osseo è responsabile dello stato anemico che si ha in questa malattia e della insufficiente produzione di anticorpi normali che rende i pazienti particolarmente sensibili alle infezioni.
50 Le sostanze che evocano la risposta immune sono gli antigeni e gli anticorpi sono le immunoglobuline che ne vengono evocate e che vi si legano. Un anticorpo si lega ad un sito sulla superficie di un antigene denominato epitope o determinante antigenico. Gli epitopi possono essere, segmenti di una catena polipeptidica, oppure sequenze glucidiche. Gli antigeni formano con gli anticorpi corrispondenti, dei complessi non covalenti antigene-anticorpo, più facilmente eliminabili degli antigeni stessi da parte dei fagociti
51 Schema semplificato di una immunoglobulina (IgG), costituita da due catene pesanti connesse da ponti di solfuro e da due catene leggere. Le porzioni tratteggiate delle catene, che hanno una composizione di amino acidi variabili, costituiscono il sito di legame con l antigene.
52 Organizzazione strutturale delle IgM e delle IgA. Si noti la frequenza di ponti disolfuro intercatena e la presenza sia nelle IgM sia nelle IgA della catena di interconnessione J.
53
54
55
56
57
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Regione cerniera monomero regione cerniera
 Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
Amminoacidi e Proteine
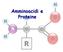 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
PROTEINA GREGGIA (P.G.)
 PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
PROTEINA GREGGIA (P.G.) Il contenuto proteico di un alimento è valutato dal suo tenore in azoto, determinato con il metodo Kjeldahl modificato. Il metodo Kjeldahl valuta la maggior parte dell azoto presente
AMMINO ACIDI. L equilibrio è regolato dal ph
 AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 9
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Rappresentazione dei Dati Biologici
 Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Funzioni delle proteine del sangue:
 PROTEINE DEL SANGUE Funzioni delle proteine del sangue: 1. Funzioni nutrizionali 2. Regolazione dell equilibrio acido base 3. Ripartizione dell acqua nei vari distretti 4. Funzione di trasporto 5. Coagulazione
PROTEINE DEL SANGUE Funzioni delle proteine del sangue: 1. Funzioni nutrizionali 2. Regolazione dell equilibrio acido base 3. Ripartizione dell acqua nei vari distretti 4. Funzione di trasporto 5. Coagulazione
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Capitolo 17. Risposte alle domande interne al capitolo. 17.1 (p. 501) a. glicina. b. prolina. c. treonina. d. aspartato
 apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
Struttura delle proteine
 Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Università di Roma Tor Vergata - Corso di Laurea in Scienze Biologiche - Immunologia Molecolare - dott. Claudio PIOLI - a.a.
 Anticorpi generalità Riconoscimento antigene Anticorpi Molecole MHC Recettore per l Ag dei linfociti T (TCR) Anticorpi riconoscono diversi tipi di strutture antigeniche macromolecole proteine, lipidi,
Anticorpi generalità Riconoscimento antigene Anticorpi Molecole MHC Recettore per l Ag dei linfociti T (TCR) Anticorpi riconoscono diversi tipi di strutture antigeniche macromolecole proteine, lipidi,
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Lezione 2. Sommario. Bioinformatica. Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine. Mauro Ceccanti e Alberto Paoluzzi
 Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi e proteine Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
3.3. UMAMI NEGLI ALIMENTI
 3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
che è caratteristico degli alcoli (es CH 3 -CH 2 -OH etanolo) gruppo carbonilico che si trova in composti detti chetoni;
 LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 7
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI)
 BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI) Sono i composti chimici dei viventi. Sono formate da Carbonio (C), Idrogeno (H), Ossigeno (O), Azoto (N), Fosforo (P) e Zolfo (S).
BIOMOLECOLE (IN ALIMENTAZIONE SONO CLASSIFICATE TRA I MACRONUTRIENTI) Sono i composti chimici dei viventi. Sono formate da Carbonio (C), Idrogeno (H), Ossigeno (O), Azoto (N), Fosforo (P) e Zolfo (S).
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Tipi di immunità acquisita. www.uniroma2.it/didattica/immunotlb
 Tipi di immunità acquisita Caratteristiche dell immunità acquisita Espansione clonale Fasi della risposta immunitaria acquisita Specificità, memoria, risoluzione delle risposte immunitarie acquisite Immunità
Tipi di immunità acquisita Caratteristiche dell immunità acquisita Espansione clonale Fasi della risposta immunitaria acquisita Specificità, memoria, risoluzione delle risposte immunitarie acquisite Immunità
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Traduzione dell informazione genetica (1)
 Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE)
 a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
a cura di : Gaia,Giulia, Lorenzo e Simone 2^ B ( LA MIGLIORE) I grassi nella piramide alimentare Forniscono molta ENERGIA!!! Danno gusto al cibo Trasportano alcune vitamine o LIPIDI Però se se ne mangiano
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
i principi alimentari
 i principi alimentari CARBOIDRATI glucidi PROTEINE protidi GRASSI lipidi VITAMINE SALI MINERALI ACQUA 1 carboidrati glucidi o zuccheri sono composti di carbonio, idrogeno e ossigeno Lo zucchero più semplice
i principi alimentari CARBOIDRATI glucidi PROTEINE protidi GRASSI lipidi VITAMINE SALI MINERALI ACQUA 1 carboidrati glucidi o zuccheri sono composti di carbonio, idrogeno e ossigeno Lo zucchero più semplice
Peptidi, proteine ed e nzim i i 1
 Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
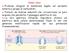 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
DOMINI E MODULI 02/04/2014. Domini modulari delle proteine 2
 Domini modulari delle proteine 1 Proteine della matrice DOMINI E MODULI La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette domini,
Domini modulari delle proteine 1 Proteine della matrice DOMINI E MODULI La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette domini,
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma
 Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Seminario. Domini modulari delle proteine 1
 Seminario Proteine della matrice DOMINI E MODULI Domini modulari delle proteine 1 La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette
Seminario Proteine della matrice DOMINI E MODULI Domini modulari delle proteine 1 La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Strutture molecolari della cellula: Bio-macromolecole. Prof. C. Guarino
 Strutture molecolari della cellula: Bio-macromolecole Prof. C. Guarino INTRO Ogni cellula vivente racchiude una pluralità di molecole diverse L acqua è l elemento dominante, nelle cellule vegetali e nei
Strutture molecolari della cellula: Bio-macromolecole Prof. C. Guarino INTRO Ogni cellula vivente racchiude una pluralità di molecole diverse L acqua è l elemento dominante, nelle cellule vegetali e nei
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI
 GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI AMINOACIDI ESSENZIALI Gli aminoacidi indispensabili, noti anche come aminoacidi essenziali, devono essere forniti al corpo con gli alimenti
GUIDA ORTOMOLECOLARE ALLA INTERPRETAZIONE DEL TEST DEGLI AMINOACIDI AMINOACIDI ESSENZIALI Gli aminoacidi indispensabili, noti anche come aminoacidi essenziali, devono essere forniti al corpo con gli alimenti
LE MOLECOLE INFORMAZIONALI. Lezioni d'autore Treccani
 LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
www.fisiokinesiterapia.biz TRASCRIZIONE
 www.fisiokinesiterapia.biz TRASCRIZIONE TRASCRIZIONE Processo mediante il quale una sequenza di DNA (un gene) viene copiata in una sequenza di RNA Dalla trascrizione derivano gli mrna, che verranno tradotti
www.fisiokinesiterapia.biz TRASCRIZIONE TRASCRIZIONE Processo mediante il quale una sequenza di DNA (un gene) viene copiata in una sequenza di RNA Dalla trascrizione derivano gli mrna, che verranno tradotti
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
strutture di Proteine
 Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
10) Se ad una soluzione aumentiamo la temperatura cosa succede? Dire quale delle seguenti affermazioni è corretta.
 Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Dal DNA all RNA. La trascrizione nei procarioti e negli eucarioti
 Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata lunga catena di ammino acidi struttura spaziale organizzata
 STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
