Unita' necessarie = peso corporeo (kg) x aumento di Fattore IX desiderato (%) x 1.2
|
|
|
- Albina Zanella
- 7 anni fa
- Visualizzazioni
Transcript
1 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE ALPHANINE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Fattore IX della coagulazione (umano) altamente purificato in flaconi, a doppia inattivazione virale. I flaconi sono disponibili con una potenza nominale di UI. Attività' specifica: >150 U/mg proteine. Il processo di produzione di Alphanine comprende due specifici step appositamente studiati per eliminare/rimuovere i virus: 1) trattamento con solvente/detergente 2) nanofiltrazione (ultrafiltrazione spinta) che è stata appositamente studiata per rimuovere i virus (in particolare quelli sprovvisti di involucro lipidico) dai prodotti biologici. 3. FORMA FARMACEUTICA Polvere e solvente per soluzione per infusione. Alphanine viene fornito sotto forma liofilizzata, in flaconi. 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Prevenzione e trattamento di episodi emorragici in soggetti con deficit di Fattore IX da Emofilia B ed in soggetti con deficit acquisito di Fattore IX. 4.2 Posologia e modalità di somministrazione Posologia Il dosaggio e la durata della terapia sostitutiva dipendono dalla gravità del deficit coagulatorio, dalla localizzazione ed estensione dell'emorragia e dalle condizioni cliniche. Una unità di Fattore IX è equivalente alla quantità di Fattore IX contenuta in un millilitro di plasma umano normale. Il calcolo del dosaggio di Fattore IX necessario si basa sulla considerazione empirica che la somministrazione di una 1 I.U. di Fattore IX per chilogrammo di peso corporeo aumenta l attività del Fattore nel plasma dello 0.8%. Pertanto la dose si determina usando la formula seguente: Unita' necessarie = peso corporeo (kg) x aumento di Fattore IX desiderato (%) x 1.2 IMPORTANTE La quantità e la frequenza di somministrazione devono comunque basarsi sulla efficacia clinica nei singoli soggetti. Nei casi di eventi emorragici che seguono, l attività del Fattore IX non deve scendere al di sotto dei livelli indicati (%) per tutto il periodo indicato. 1
2 Eventi emorragici Emorragie minori; emorragie articolari Emorragie maggiori; emorragie muscolari, estrazioni dentarie; traumi moderati al capo operazioni di media gravità; emorragie della cavità orale. Emorragie pericolose per la vita; operazioni maggiori; emorragie gastrointestinali, emorragie intracraniche, intraaddominali o toraciche. Fratture Livelli plasmatici di Durata di mantenimento Fattore IX necessari 30% Almeno un giorno a seconda della gravità dell emorragia 30-50% 3-4 giorni o finché non si è ottenuta adeguata cicatrizzazione 50-75% 7 giorni e continuare la terapia per almeno altri 7 giorni In alcune circostanze possono essere necessarie dosi più elevate di quelle calcolate, specialmente nel caso della dose iniziale. In particolare, in caso di interventi chirurgici maggiori, è indispensabile un monitoraggio preciso della terapia sostitutiva per mezzo di esami dell'andamento dell attività coagulatoria (attività plasmatica del Fattore IX). Per la profilassi a lungo termine delle emorragie, in particolare nei soggetti con Emofilia B grave, vanno somministrate dosi da 10 a 25 I.U. di Fattore IX per chilogrammo di peso ad intervalli di tre - quattro giorni. Per gli emofilici con anticorpi contro il Fattore IX (inibitori) è necessaria una terapia specifica. Si può ottenere una immunotolleranza con l'uso di concentrati di Fattore IX umano Modalità' di somministrazione Dopo aver disciolto il preparato, iniettarlo od infonderlo per via venosa a velocità costante, nell'arco di 5 minuti. 4.3 Controindicazioni - Va usata cautela nei soggetti allergici ai costituenti del preparato. - Alto rischio di trombosi o di coagulazione intravascolare disseminata (vedere al punto 4.4: Avvertenze particolari e speciali precauzioni per l'uso). 4.4 Avvertenze particolari e speciali precauzioni per l'uso Se si verifica una reazione allergica od anafilattica, l iniezione/infusione deve essere immediatamente sospesa. In caso di shock devono essere adottate le terapie specifiche. Sulla base dell'esperienza con prodotti a base di Fattore IX a bassa purezza (Concentrati di complesso Protrombinico) esiste un rischio potenziale di trombosi o di coagulazione intravascolare disseminata quando si usano i concentrati di Fattore IX. 2
3 Ogni paziente deve essere osservato attentamente per evidenziare segni o sintomi di coagulazione intravascolare o di trombosi. A causa del rischio potenziale di complicanze tromboemboliche, va usata cautela nei soggetti con anamnesi di malattie coronariche o di infarto, con malattie epatiche, nei post-operati, nei neonati o nei soggetti a rischio di manifestazioni tromboemboliche o di coagulazione intravascolare disseminata. In ognuno di questi casi va valutato attentamente il rapporto rischio/beneficio. Dopo ripetuti trattamenti con concentrati di Fattore IX, va determinato il livello plasmatico degli inibitori. 4.5 Interazioni con altri medicamenti ed altre forme di interazioni Non sono state segnalate, a tutt'oggi, forme di interazione del concentrato di fattore IX della coagulazione umano con altri prodotti medicinali. 4.6 Gravidanza ed allattamento La sicurezza dei concentrati di Fattore IX in gravidanza non è stata provata in studi clinici controllati. Studi nell'animale non sono sufficienti a valutare la sicurezza d'uso del prodotto in gravidanza, durante lo sviluppo del feto, nel periodo peri e postnatale. Pertanto i concentrati di Fattore IX vanno usati solo in caso di effettiva necessità durante la gravidanza e l'allattamento. 4.7 Effetti sulla guida e sull'uso di macchinari complessi Non sono stati evidenziati effetti negativi di qualunque genere. 4.8 Effetti indesiderati - In rari casi vengono osservate reazioni allergiche od anafilattiche. - In rari casi si verifica un aumento della temperatura corporea. - Si possono sviluppare anticorpi contro il Fattore IX. - Per prodotti ottenuti da plasma o sangue umano, non si può del tutto escludere la possibilità di trasmissione di forme infettive, dovute anche ad elementi patogeni di natura attualmente sconosciuta. Per ridurre il rischio di trasmissione di agenti infettivi, nella preparazione del prodotto viene effettuata un accurata scelta dei donatori e vengono prese misure adatte per rimuovere od inattivare eventuali agenti infettanti, qualora presenti. Queste misure comprendono l'uso del trattamento solvente/detergente ed un processo di nanofiltrazione, capace di rimuovere anche i virus senza involucro lipidico (Epatite A, Parvovirus). - Esiste il rischio potenziale di episodi tromboembolici conseguenti alla somministrazione di concentrati di Fattore IX. 4.9 Sovradosaggio L'uso di dosi elevate di prodotti contenenti Fattore IX (PCC) è stato associato con casi di infarto del miocardio, coagulazione intravascolare disseminata, trombosi venosa ed embolia polmonare. 3
4 Pertanto, in caso di sovradosaggio, la possibilità di sviluppo di complicanze tromboemboliche o di coagulazione intravascolare disseminata aumenta nei pazienti a rischio per queste complicazioni. 5 PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Il Fattore IX è una glicoproteina a catena singola di circa Dalton, vitamina K-dipendente, sintetizzata nel fegato. Il Fattore IX viene attivato a fattore IXa nella via intrinseca della coagulazione e, in quella estrinseca, dal complesso fattore VII/fattore tissutale. Il Fattore IX attivato, in combinazione col fattore VIII attivato, attiva a sua volta il fattore X; ciò consente la conversione della protrombina in trombina, la quale converte il fibrinogeno in fibrina, con formazione del coagulo. L attività del Fattore IX è molto ridotta nei pazienti con Emofilia B. Pertanto, in questi pazienti è necessaria una terapia sostitutiva. 5.2 Proprietà farmacocinetiche L'infusione di concentrati di Fattore IX umano in soggetti con Emofilia B consente un aumento del 30-60% dell attività del fattore stesso nel plasma. L'emivita plasmatica del Fattore IX varia tra 16 e 30 ore con una media di 24 ore. 5.3 Dati preclinici di sicurezza Il Fattore IX dei concentrati è un costituente normale del plasma e si comporta come il Fattore IX endogeno. I test di tossicità per dose singola non hanno significato (per sovraccarico ai dosaggi più alti). I test di tossicità per dosi ripetute negli animali non sono proponibili per le interferenze dovute allo sviluppo di anticorpi nei confronti di proteine eterologhe. Dal momento che l'esperienza clinica non evidenzia possibilità di azione tumorigena o mutagena, studi sperimentali in specie eterologhe non sono considerati necessari. 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Destrosio: 0,01 0,2 mg/unità Fattore IX Eparina: 0,01 2,0 UI/50 unità Fattore IX 6.2 Incompatibilità ALPHANINE non deve essere mescolato con altri prodotti medicinali. Si raccomanda che ALPHANINE venga ricostituito solo con il solvente fornito. 6.3 Periodo di validità 24 mesi a 2-8 C al riparo dalla luce. Non congelare. Il prodotto deve essere usato immediatamente dopo la ricostituzione. 4
5 6.4 Precauzioni particolari per la conservazione Vedere punto Natura e contenuto del contenitore Il flacone è di vetro neutro di Tipo I ed è chiuso con un tappo grigio di gomma butilica, un sigillo di alluminio zigrinato ed una copertura di plastica "Flip- Off". Ogni flacone di AlphaNine contenente polvere liofilizzata viene fornito insieme ad una siringa preriempita di vetro di tipo I contente 10 ml di acqua p.p.i. (solvente). Ogni confezione di AlphaNine è accompagnata dai dispositivi necessari per la sua ricostituzione e somministrazione (un adattatore per flacone, un microfiltro e un set per infusione). 6.6 ISTRUZIONI PER L'USO Non usare dopo la data di scadenza riportata sull etichetta. Il prodotto restante non deve mai essere usato in un secondo tempo, né conservato in frigorifero. Per preparare la soluzione: 1. Scaldare il flacone e la siringa, non superando i 30 C. 2. Inserire lo stantuffo nella siringa contenente il solvente. 3. Estrarre il filtro dal suo involucro. Rimuovere il tappo dal connettore della siringa e collegarla al filtro. 4. Estrarre l adattatore per flacone dal suo involucro e collegarlo al filtro sulla siringa. 5. Rimuovere la protezione in plastica dal flacone e pulire il tappo con alcool. 6. Perforare il tappo del flacone con l ago dell adattatore. 7. Trasferire tutto il solvente dalla siringa al flacone. 8. Ruotare il flacone senza agitare, fino a che tutto il prodotto non si è disciolto. Trattandosi di una soluzione per uso parenterale, non usare il prodotto se non si è disciolto completamente o se sono visibili delle particelle. 9. Separare velocemente la siringa col filtro dal flacone con l adattatore, in modo da perdere il vuoto. Procedere immediatamente ai punti 10 e Col flacone in alto, aspirare la soluzione all interno della siringa. 11. Preparare il sito d iniezione, sconnettere la siringa e iniettare il prodotto usando il set con ago a farfalla fornito, oppure un ago sterile. Iniettare lentamente in vena ad una velocità non superiore a 10 ml/minuto. Dopo avere effettuato la ricostituzione con la siringa fornita, il prodotto va usato immediatamente. Non riutilizzare il set di somministrazione. Tutto il prodotto che non viene usato o il materiale di scarto deve essere gettato secondo le vigenti norme in materia. La soluzione deve risultare chiara o leggermente opalescente. Non usare soluzioni torbide o che presentino depositi. 5
6 Prima della somministrazione, i prodotti ricostituiti devono essere ispezionati visivamente per la presenza di particelle e lo scolorimento. 7. TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO GRIFOLS ITALIA S.p.A. Via Torino, Vicopisano Pisa - ITALIA 8. NUMERO DELL AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO ALPHANINE 500 UI AIC N ALPHANINE 1000 UI AIC N ALPHANINE 1500 UI AIC N DATA DI PRIMA AUTORIZZAZIONE/RINNOVO DELL'AUTORIZZAZIONE: Rinnovo: Giugno DATA DI (PARZIALE) REVISIONE DEL TESTO: 08/2014 6
7 7
Deficit acquisito di antitrombina, per la profilassi e terapia nei casi di coagulazione intravascolare disseminata (DIC).
 1. DENOMINAZIONE DEL MEDICINALE Anbinex 500 U.I. Polvere e solvente per soluzione per infusione Anbinex 1000 U.I. Polvere e solvente per soluzione per infusione Antitrombina umana 2. COMPOSIZIONE QUALITATIVA
1. DENOMINAZIONE DEL MEDICINALE Anbinex 500 U.I. Polvere e solvente per soluzione per infusione Anbinex 1000 U.I. Polvere e solvente per soluzione per infusione Antitrombina umana 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FANHDI 250 U.I. polvere e solvente per soluzione per infusione FANHDI 500 U.I. polvere e solvente per soluzione per infusione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FANHDI 250 U.I. polvere e solvente per soluzione per infusione FANHDI 500 U.I. polvere e solvente per soluzione per infusione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Fattore VIII umano della coagulazione del sangue complessato con fattore von Willebrand.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALPHANATE 250 Polvere e solvente per soluzione per infusione ALPHANATE 500 Polvere e solvente per soluzione per infusione ALPHANATE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALPHANATE 250 Polvere e solvente per soluzione per infusione ALPHANATE 500 Polvere e solvente per soluzione per infusione ALPHANATE
01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare
 1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
Confidex. Stop rapido all emorragia.
 Confidex. Stop rapido all emorragia. Complesso protrombinico completo e bilanciato. Confidex Riassunto delle caratteristiche del prodotto INR iniziale 2,0-3,9 4,0-6,0 > 6,0 Dose approssimativa in ml/kg
Confidex. Stop rapido all emorragia. Complesso protrombinico completo e bilanciato. Confidex Riassunto delle caratteristiche del prodotto INR iniziale 2,0-3,9 4,0-6,0 > 6,0 Dose approssimativa in ml/kg
Fattore IX ad alta efficienza 1,2,3
 Fattore IX ad alta efficienza 1,2,3 PURIFICATO CON ANTICORPO MONOCLONALE Fattore IX della coagulazione umano Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE Mononine 500, 100
Fattore IX ad alta efficienza 1,2,3 PURIFICATO CON ANTICORPO MONOCLONALE Fattore IX della coagulazione umano Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE Mononine 500, 100
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE REKORD B12 polvere e solvente per sospensione orale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il tappo contiene: Principi attivi:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
R IASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. Denominazione del medicinale BIOCHETASI granulato effervescente. BIOCHETASI compresse effervescenti. 2. Composizione qualitativa e quantitativa Granulato
Foglio illustrativo: informazioni per l'utilizzatore PROPLEX 600 UI
 Foglio illustrativo: informazioni per l'utilizzatore PROPLEX 600 UI Polvere e solvente per soluzione iniettabile Principio attivo: complesso protrombinico umano Legga attentamente questo foglio prima di
Foglio illustrativo: informazioni per l'utilizzatore PROPLEX 600 UI Polvere e solvente per soluzione iniettabile Principio attivo: complesso protrombinico umano Legga attentamente questo foglio prima di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE neohepatect 50 UI/ml; soluzione per infusione 2.COMPOSIZIONE QUALITATIVA E QUANTITATIVA Immunoglobulina umana anti epatite B
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE neohepatect 50 UI/ml; soluzione per infusione 2.COMPOSIZIONE QUALITATIVA E QUANTITATIVA Immunoglobulina umana anti epatite B
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE DITANRIX Adulti Sospensione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una dose da 0,5 ml
BOVILIS IBR marker live liofilizzato e solvente per sospensione per bovini
 FOGLIETTO ILLUSTRATIVO BOVILIS IBR marker live liofilizzato e solvente per sospensione per bovini 1. NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO E DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO BOVILIS IBR marker live liofilizzato e solvente per sospensione per bovini 1. NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE ALL IMMISSIONE IN COMMERCIO E DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. WILFACTIN 100 UI/ml polvere e solvente per soluzione iniettabile Fattore von Willebrand umano
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE WILFACTIN 100 UI/ml polvere e solvente per soluzione iniettabile Fattore von Willebrand umano Legga attentamente questo foglio prima di iniziare a usare
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE WILFACTIN 100 UI/ml polvere e solvente per soluzione iniettabile Fattore von Willebrand umano Legga attentamente questo foglio prima di iniziare a usare
Informazioni da apporre sull etichetta {Tubo in polipropilene} 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA IN TERMINI DI PRINCIPIO ATTIVO
 Etichettatura: Informazioni da apporre sull etichetta {Tubo in polipropilene} 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA IN TERMINI DI PRINCIPIO ATTIVO Ciascuna compressa
Etichettatura: Informazioni da apporre sull etichetta {Tubo in polipropilene} 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA IN TERMINI DI PRINCIPIO ATTIVO Ciascuna compressa
Principio attivo: Immunoglobulina umana anti-d (Rh) 1500 U.I. (300 microgrammi) (Percentuale di immunoglobulina umana 95% Ig)
 1. DENOMINAZIONE DEL MEDICINALE IGAMAD 1500 U.I./2 ml Soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: Immunoglobulina umana anti-d (Rh) 1500 U.I.
1. DENOMINAZIONE DEL MEDICINALE IGAMAD 1500 U.I./2 ml Soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: Immunoglobulina umana anti-d (Rh) 1500 U.I.
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TRIATOP 1% shampoo 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un grammo di shampoo contiene: Principio attivo Ketoconazolo 10
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. denominazione della specialità medicinale Confidex 500 Polvere e solvente per soluzione iniettabile. Confidex 1000 Polvere e solvente per soluzione iniettabile.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. denominazione della specialità medicinale Confidex 500 Polvere e solvente per soluzione iniettabile. Confidex 1000 Polvere e solvente per soluzione iniettabile.
Il contenuto di proteina umana è di 50 g/l, di cui almeno il 97% è costituito da IgG.
 1. DENOMINAZIONE DEL MEDICINALE Niuliva 250 U.I./ml soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Immunoglobulina umana antiepatite B. La distribuzione percentuale delle sottoclassi
1. DENOMINAZIONE DEL MEDICINALE Niuliva 250 U.I./ml soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Immunoglobulina umana antiepatite B. La distribuzione percentuale delle sottoclassi
Come interpretare le alterazioni più frequenti del laboratorio: La Coagulazione
 Come interpretare le alterazioni più frequenti del laboratorio: La Coagulazione Gualtiero Palareti U.O. di Angiologia e Malattie della Coagulazione Policlinico S. Orsola-Malpighi Bologna Metodologie utilizzate
Come interpretare le alterazioni più frequenti del laboratorio: La Coagulazione Gualtiero Palareti U.O. di Angiologia e Malattie della Coagulazione Policlinico S. Orsola-Malpighi Bologna Metodologie utilizzate
INDICAZIONI TERAPEUTICHE
 FOGLIO ILLUSTRATIVO Potassio cloruro S.A.L.F. 2 meq/ml concentrato per soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Soluzioni elettrolitiche. INDICAZIONI TERAPEUTICHE Trattamento di deficienze
FOGLIO ILLUSTRATIVO Potassio cloruro S.A.L.F. 2 meq/ml concentrato per soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Soluzioni elettrolitiche. INDICAZIONI TERAPEUTICHE Trattamento di deficienze
L EMOFILIA. Che cos è
 L EMOFILIA Che cos è L emofilia è una malattia rara di origine genetica che colpisce soprattutto i maschi. Se in un individuo sano la fuoriuscita di sangue dai vasi sanguigni si arresta rapidamente, chi
L EMOFILIA Che cos è L emofilia è una malattia rara di origine genetica che colpisce soprattutto i maschi. Se in un individuo sano la fuoriuscita di sangue dai vasi sanguigni si arresta rapidamente, chi
Patologie del sistema emolinfopoietico Molto rari: Linfoadenopatia 1 Disturbi del metabolismo e della nutrizione Comuni: perdita di appetito 2 Disturb
 di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
di effetti indesiderati correlabili a precedenti immunizzazioni. La presenza di infezioni lievi non costituisce controindicazione. L'infezione da virus HIV non è considerata una controindicazione. A scopo
Foglio illustrativo: informazioni per il paziente. ISORAM 4%, soluzione per infusione. Soluzione di aminoacidi
 Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
Vivaglobin, soluzione di 160 mg/ml per iniezione (uso sottocutaneo) 1 ml contiene: immunoglobulina umana normale (sottocutanea)
 1. DENOMINAZIONE DEL MEDICINALE Vivaglobin, soluzione di 160 mg/ml per iniezione (uso sottocutaneo) 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml contiene: immunoglobulina umana normale (sottocutanea)
1. DENOMINAZIONE DEL MEDICINALE Vivaglobin, soluzione di 160 mg/ml per iniezione (uso sottocutaneo) 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 ml contiene: immunoglobulina umana normale (sottocutanea)
ALBUTEIN 50 g/l, soluzione per infusione ALBUTEIN 200 g/l, soluzione per infusione ALBUTEIN 250 g/l, soluzione per infusione
 1. DENOMINAZIONE DEL MEDICINALE ALBUTEIN 50 g/l, soluzione per infusione ALBUTEIN 200 g/l, soluzione per infusione ALBUTEIN 250 g/l, soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio
1. DENOMINAZIONE DEL MEDICINALE ALBUTEIN 50 g/l, soluzione per infusione ALBUTEIN 200 g/l, soluzione per infusione ALBUTEIN 250 g/l, soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3
 DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
Popolazione pediatrica Non c è esperienza sull uso di Prolastin nei bambini e negli adolescenti al di sotto dei 18 anni di età.
 1. DENOMINAZIONE DEL MEDICINALE Prolastin 1000 mg, polvere e solvente per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 flacone di polvere contiene: 1000 mg di inibitore dell alfa
1. DENOMINAZIONE DEL MEDICINALE Prolastin 1000 mg, polvere e solvente per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 flacone di polvere contiene: 1000 mg di inibitore dell alfa
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. UMAN SERUM 5% Soluzione per infusione Proteine plasmatiche umane
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE UMAN SERUM 5% Soluzione per infusione Proteine plasmatiche umane Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE UMAN SERUM 5% Soluzione per infusione Proteine plasmatiche umane Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE NovoSeven 1,2 mg (60 KUI) - polvere e solvente per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE NovoSeven 1,2 mg (60 KUI) - polvere e solvente per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
APIVAR. Riassunto delle caratteristiche del prodotto
 APIVAR Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO APIVAR 500 mg strisce per alveare per api. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una striscia per alveare
APIVAR Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO APIVAR 500 mg strisce per alveare per api. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una striscia per alveare
ALBUMINA GRIFOLS 5 g/100 ml è una soluzione di proteine plasmatiche umane, costituite per almeno il 95% da albumina umana.
 1. DENOMINAZIONE DEL MEDICINALE ALBUMINA GRIFOLS 5 g/100 ml, soluzione per infusione ALBUMINA GRIFOLS 20 g/100 ml, soluzione per infusione ALBUMINA GRIFOLS 25 g/100 ml, soluzione per infusione 2. COMPOSIZIONE
1. DENOMINAZIONE DEL MEDICINALE ALBUMINA GRIFOLS 5 g/100 ml, soluzione per infusione ALBUMINA GRIFOLS 20 g/100 ml, soluzione per infusione ALBUMINA GRIFOLS 25 g/100 ml, soluzione per infusione 2. COMPOSIZIONE
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Elenco dei sinonimi e delle voci correlate...2 Modulistica in uso...3 Norme generali per il prelievo...3
 Pag 1/8 20/09/2010 SOMMARIO Elenco dei sinonimi e delle voci correlate...2 Modulistica in uso...3 Norme per il prelievo...3 FIRMA DI APPROVAZIONE: 20.09.2010 Prof. Gualtiero Palareti Pag 2/8 20/09/2010
Pag 1/8 20/09/2010 SOMMARIO Elenco dei sinonimi e delle voci correlate...2 Modulistica in uso...3 Norme per il prelievo...3 FIRMA DI APPROVAZIONE: 20.09.2010 Prof. Gualtiero Palareti Pag 2/8 20/09/2010
2. P RIMA DI U TILIZZARE ASQUAM
 Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
Il trattamento della trombosi venosa profonda
 Il trattamento della trombosi venosa profonda Fiumicino, 19 dicembre 2015 www.cos.it/mediter Trombosi Venosa Profonda (DVT) [NOACs Anticoagulant therapy for venous thromboembolism] Glossario DVT (Deep
Il trattamento della trombosi venosa profonda Fiumicino, 19 dicembre 2015 www.cos.it/mediter Trombosi Venosa Profonda (DVT) [NOACs Anticoagulant therapy for venous thromboembolism] Glossario DVT (Deep
FOGLIETTO ILLUSTRATIVO. Baytril flavour 25 mg/ml sospensione orale per gatti
 FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE NovoSeven 1 mg (50 KUI) polvere e solvente per soluzione iniettabile NovoSeven 2 mg (100 KUI) polvere e solvente
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE NovoSeven 1 mg (50 KUI) polvere e solvente per soluzione iniettabile NovoSeven 2 mg (100 KUI) polvere e solvente
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione
 Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Purevax FeLV sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da 1 ml contiene:
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Purevax FeLV sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da 1 ml contiene:
Coagulazione del sangue
 Coagulazione del sangue Caratteristiche principali dei sistemi intrinseco ed estrinseco di attivazione del fattore X Meccanismi di attivazione della trombina e ruolo della vitamina K Attivazione della
Coagulazione del sangue Caratteristiche principali dei sistemi intrinseco ed estrinseco di attivazione del fattore X Meccanismi di attivazione della trombina e ruolo della vitamina K Attivazione della
Corretta tecnica di conservazione e somministrazione insulinica
 Corretta tecnica di conservazione e somministrazione insulinica La terapia insulinica la terapia insulinica è il principale trattamento del diabetedi tipo I,mentre puo essere usata nel diabete di tipo
Corretta tecnica di conservazione e somministrazione insulinica La terapia insulinica la terapia insulinica è il principale trattamento del diabetedi tipo I,mentre puo essere usata nel diabete di tipo
Il componente antimorbillo, antiparotite e antirosolia liofilizzato è una polvere che varia dal colore bianco al rosa chiaro
 PRIORIX Polvere e solvente per soluzione iniettabile COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da 0,5 ml di vaccino ricostituito contiene: virus del morbillo vivo attenuato, ceppo Schwarz* non
PRIORIX Polvere e solvente per soluzione iniettabile COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da 0,5 ml di vaccino ricostituito contiene: virus del morbillo vivo attenuato, ceppo Schwarz* non
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
batrevac sospensione iniettabile vaccino influenzale
 batrevac sospensione iniettabile vaccino influenzale RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Batrevac sospensione iniettabile (vaccino influenzale inattivato preparato
batrevac sospensione iniettabile vaccino influenzale RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Batrevac sospensione iniettabile (vaccino influenzale inattivato preparato
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE IMMUNOHBs 180 UI/ml Soluzione iniettabile per uso intramuscolare IMMUNOHBs 334 UI/ml Soluzione iniettabile per uso intramuscolare Immunoglobulina umana
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE IMMUNOHBs 180 UI/ml Soluzione iniettabile per uso intramuscolare IMMUNOHBs 334 UI/ml Soluzione iniettabile per uso intramuscolare Immunoglobulina umana
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Hiberix Polvere e solvente per soluzione iniettabile per uso intramuscolare Vaccino Haemophilus influenzae di tipo b coniugato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Hiberix Polvere e solvente per soluzione iniettabile per uso intramuscolare Vaccino Haemophilus influenzae di tipo b coniugato
Riassunto delle Caratteristiche del Prodotto
 Riassunto delle Caratteristiche del Prodotto 1. DENOMINAZIONE DEL MEDICINALE Omega 3 Mylan Generics Capsule molli da 1000 mg. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000
Riassunto delle Caratteristiche del Prodotto 1. DENOMINAZIONE DEL MEDICINALE Omega 3 Mylan Generics Capsule molli da 1000 mg. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE CODEX 5 miliardi capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Codex 5 miliardi capsule rigide Ogni capsula contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE CODEX 5 miliardi capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Codex 5 miliardi capsule rigide Ogni capsula contiene:
Linee guida sulla gestione di terapie preoperatorie antiaggreganti ed anticoagulanti
 Linee guida sulla gestione di terapie preoperatorie antiaggreganti ed anticoagulanti Marco Moia Centro Emofilia e Trombosi A. Bianchi Bonomi Fondazione IRCCS Ca Granda Ospedale Maggiore Policlinico di
Linee guida sulla gestione di terapie preoperatorie antiaggreganti ed anticoagulanti Marco Moia Centro Emofilia e Trombosi A. Bianchi Bonomi Fondazione IRCCS Ca Granda Ospedale Maggiore Policlinico di
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE CEPROTIN 500 UI Polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Proteina
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE CEPROTIN 500 UI Polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Proteina
Foglio illustrativo: informazioni per l utilizzatore. NEOMERCUROCROMO soluzione cutanea. Eosina/ Cloroxilenolo/ Propilenglicole
 Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
Foglio illustrativo: informazioni per l utilizzatore NEOMERCUROCROMO soluzione cutanea Eosina/ Cloroxilenolo/ Propilenglicole Legga attentamente questo foglio prima di usare questo medicinale perchè contiene
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Nobivac Myxo-RHD liofilizzato e solvente per sospensione iniettabile per conigli 2. COMPOSIZIONE QUALITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Nobivac Myxo-RHD liofilizzato e solvente per sospensione iniettabile per conigli 2. COMPOSIZIONE QUALITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 4 1. DENOMINAZIONE DEL MEDICINALE BeneFIX 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA BeneFIX, Fattore IX della coagulazione, ricombinante, è preparato
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 4 1. DENOMINAZIONE DEL MEDICINALE BeneFIX 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA BeneFIX, Fattore IX della coagulazione, ricombinante, è preparato
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OMEGA 3 DOC Generici 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula molle contiene 1000 mg di
RoActemra. tocilizumab. Che cos è RoActemra? Per che cosa si usa RoActemra? Riassunto destinato al pubblico
 EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Classificazione clinica dell emofilia A e B
 Classificazione clinica dell emofilia A e B Gravità Grave Moderata Lieve Livello di FVIII/ IX < 1 % 1-5 % > 5 % < 40 % Caratteristiche cliniche Emorragie spontanee dalla prima infanzia; frequenti emartri
Classificazione clinica dell emofilia A e B Gravità Grave Moderata Lieve Livello di FVIII/ IX < 1 % 1-5 % > 5 % < 40 % Caratteristiche cliniche Emorragie spontanee dalla prima infanzia; frequenti emartri
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Nonafact 100 UI polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Nonafact 100 UI polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Contiene il virus vivo attenuato ceppo Oka/Merck Contiene il virus vivo attenuato ceppo Oka Tra +2 e +8 Tra +2 e +8
 Varivax Varilrix Ditta Sanofi Pasteur MSD GlaxoSmithKline Ceppo virus varicella Temperatura di conservazione Immunogenicità Inizio della risposta immunitaria Durata della risposta immunitaria Efficacia
Varivax Varilrix Ditta Sanofi Pasteur MSD GlaxoSmithKline Ceppo virus varicella Temperatura di conservazione Immunogenicità Inizio della risposta immunitaria Durata della risposta immunitaria Efficacia
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE TILADE 10 mg/2 ml soluzione da nebulizzare 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA TILADE 10 mg/2 ml soluzione da nebulizzare
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE CLODRONATO ABC 100 mg/3,3 ml soluzione iniettabile CLODRONATO ABC 300 mg/10 ml soluzione per infusione endovenosa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE CLODRONATO ABC 100 mg/3,3 ml soluzione iniettabile CLODRONATO ABC 300 mg/10 ml soluzione per infusione endovenosa
DIF-TET-ALL -ADULTI sospensione iniettabile in siringa pre-riempita J07AM51 senza conservanti RIASSUNTO DELLE CARATTERISTICHE
 1 DIF-TET-ALL -ADULTI sospensione iniettabile in siringa pre-riempita J07AM51 senza conservanti RIASSUNTO DELLE CARATTERISTICHE Voce n. 7 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: DIF-TET-ALL -ADULTI
1 DIF-TET-ALL -ADULTI sospensione iniettabile in siringa pre-riempita J07AM51 senza conservanti RIASSUNTO DELLE CARATTERISTICHE Voce n. 7 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: DIF-TET-ALL -ADULTI
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Gripovac 3 sospensione iniettabile per suini 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Gripovac 3 sospensione iniettabile per suini 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose da
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE BeneFIX 250 UI, polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE BeneFIX 250 UI, polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
Concetti generali PRELIEVO DI SANGUE PER EMOCOLTURA. In condizioni fisiologiche il sangue è STERILE
 Concetti generali In condizioni fisiologiche il sangue è STERILE Batteriemia: presenza di batteri nel sangue Fungemia: presenza di funghi nel sangue PRELIEVO DI SANGUE PER EMOCOLTURA L emocoltura è definita
Concetti generali In condizioni fisiologiche il sangue è STERILE Batteriemia: presenza di batteri nel sangue Fungemia: presenza di funghi nel sangue PRELIEVO DI SANGUE PER EMOCOLTURA L emocoltura è definita
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE INFANRIX Bambini Sospensione iniettabile per uso intramuscolare Vaccino difterico, tetanico, pertossico acellulare (DTPa). 2.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE INFANRIX Bambini Sospensione iniettabile per uso intramuscolare Vaccino difterico, tetanico, pertossico acellulare (DTPa). 2.
AMUKINE MED 0,05% SPRAY CUTANEO, SOLUZIONE Sodio ipoclorito
 PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi e transitori facilmente
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Equilis Te sospensione iniettabile per cavalli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Equilis Te sospensione iniettabile per cavalli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni dose
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE OLEVIA 1000 mg capsule molli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una capsula molle contiene 1000 mg di Acidi omega-3
Richiesta di parere per l inserimento in PTR di:complesso protrombinico umano (Fattori IX, II, VII e X di coagulazione in associazione)
 Richiesta di parere per l inserimento in PTR di:complesso protrombinico umano (Fattori IX, II, VII e X di coagulazione in associazione) 1. Farmaco proposto Farmaco: Confidex o Pronativ Principio attivo:
Richiesta di parere per l inserimento in PTR di:complesso protrombinico umano (Fattori IX, II, VII e X di coagulazione in associazione) 1. Farmaco proposto Farmaco: Confidex o Pronativ Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Influvac S sospensione iniettabile (vaccino influenzale inattivato preparato con l antigene di superficie). 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Influvac S sospensione iniettabile (vaccino influenzale inattivato preparato con l antigene di superficie). 2. COMPOSIZIONE
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore POTASSIO CLORURO MONICO 2 meq/ml concentrato per soluzione per infusione 3 meq/ml concentrato per soluzione per infusione Potassio cloruro Medicinale
Foglio illustrativo: informazioni per l utilizzatore POTASSIO CLORURO MONICO 2 meq/ml concentrato per soluzione per infusione 3 meq/ml concentrato per soluzione per infusione Potassio cloruro Medicinale
COS'È TICALMA E A COSA SERVE
 TESTO UNICO RIPORTATO SUL CONFEZIONAMENTO PRIMARIO TICALMA 400 mg Tisana 20 bustine VALERIANA Radice Prima dell uso leggere con attenzione tutte le informazioni riportate sulla confezione Questo medicinale
TESTO UNICO RIPORTATO SUL CONFEZIONAMENTO PRIMARIO TICALMA 400 mg Tisana 20 bustine VALERIANA Radice Prima dell uso leggere con attenzione tutte le informazioni riportate sulla confezione Questo medicinale
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE SCABIANIL 5% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 g di Scabianil 5% crema, contengono: 5 g di Permetrina (isomeri
A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO
 A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO (Tutte le confezioni registrate in Italia presentano un unico template contenente tutte le informazioni previste dal foglio illustrativo ed etichetta)
A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO (Tutte le confezioni registrate in Italia presentano un unico template contenente tutte le informazioni previste dal foglio illustrativo ed etichetta)
Monitoraggio della terapia eparinica in corso di Angioplastica Coronarica Transluminale Percutanea: dati preliminari
 Monitoraggio della terapia eparinica in corso di Angioplastica Coronarica Transluminale Percutanea: dati preliminari Petronelli Mariella U.O. Patologia Clinica I Azienda Ospedaliero Universitaria Policlinico
Monitoraggio della terapia eparinica in corso di Angioplastica Coronarica Transluminale Percutanea: dati preliminari Petronelli Mariella U.O. Patologia Clinica I Azienda Ospedaliero Universitaria Policlinico
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Boostrix sospensione iniettabile Vaccino difterico, tetanico e pertossico acellulare (adsorbito). 2. COMPOSIZIONE QUALITATIVA
1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Boostrix sospensione iniettabile Vaccino difterico, tetanico e pertossico acellulare (adsorbito). 2. COMPOSIZIONE QUALITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Virus dell influenza* (inattivato con β-propiolattone, split) dei seguenti ceppi:
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE AFLURIA Sospensione iniettabile, in siringa preriempita. Vaccino influenzale (virus split (frammentato), inattivato) 2 COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE AFLURIA Sospensione iniettabile, in siringa preriempita. Vaccino influenzale (virus split (frammentato), inattivato) 2 COMPOSIZIONE
EMOSTASI. Insieme di meccanismi fisiologici che l organismo mette in atto per evitare perdite di sangue.
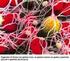 EMOSTASI EMOSTASI Insieme di meccanismi fisiologici che l organismo mette in atto per evitare perdite di sangue. Difetti dell emostasi portano all EMORRAGIA; l incapacità a mantenere il sangue fluido alla
EMOSTASI EMOSTASI Insieme di meccanismi fisiologici che l organismo mette in atto per evitare perdite di sangue. Difetti dell emostasi portano all EMORRAGIA; l incapacità a mantenere il sangue fluido alla
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE INFANRIX Bambini Sospensione iniettabile per uso intramuscolare Vaccino difterico, tetanico, pertossico acellulare (DTPa). 2.
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE INFANRIX Bambini Sospensione iniettabile per uso intramuscolare Vaccino difterico, tetanico, pertossico acellulare (DTPa). 2.
Compressa. La compressa è di forma rotonda, di colore giallo chiaro.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1-DENOMINAZIONE DEL MEDICINALE BALFOLIC 400 microgrammi compresse 2-COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni compressa contiene: Principio attivo : Acido
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PREPIDIL 1 mg/3 g GEL VAGINALE PREPIDIL 2 mg/3 g GEL VAGINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PREPIDIL 1 mg/3 g gel
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PREPIDIL 1 mg/3 g GEL VAGINALE PREPIDIL 2 mg/3 g GEL VAGINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PREPIDIL 1 mg/3 g gel
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/11
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/11 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO HALOCUR 0,5 mg/ml soluzione orale per vitelli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/11 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO HALOCUR 0,5 mg/ml soluzione orale per vitelli 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio
Foglio illustrativo: informazioni per il paziente. Omega 3 Mylan Generics 1000 mg Capsule molli Medicinale Equivalente
 Principio attivo: esteri etilici 90 dell acido omega-3 Foglio illustrativo: informazioni per il paziente Omega 3 Mylan Generics 1000 mg Capsule molli Medicinale Equivalente Legga attentamente questo foglio
Principio attivo: esteri etilici 90 dell acido omega-3 Foglio illustrativo: informazioni per il paziente Omega 3 Mylan Generics 1000 mg Capsule molli Medicinale Equivalente Legga attentamente questo foglio
Il significato degli esami di coagulazione. Walter Ageno
 Il significato degli esami di coagulazione Walter Ageno Principali caratteristiche dei nuovi anticoagulanti Via orale di somministrazione Ampia finestra terapeutica Farmacocinetica e farmacodinamica prevedibili
Il significato degli esami di coagulazione Walter Ageno Principali caratteristiche dei nuovi anticoagulanti Via orale di somministrazione Ampia finestra terapeutica Farmacocinetica e farmacodinamica prevedibili
URISTIKFIT LEV1 REF KCQURST1
 URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
URISTIKFIT LEV1 REF KCQURST1 Per Uso Diagnostico In Vitro USO PREVISTO Il controllo URISTIKFIT è destinato all uso nel laboratorio clinico come materiale di controllo nelle procedure qualitative e semiquantitative
RIASSUNTO CARATTERISTICHE PRODOTTO
 RIASSUNTO CARATTERISTICHE PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 3. FORMA FARMACEUTICA 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche 4.2 Posologia e
RIASSUNTO CARATTERISTICHE PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 3. FORMA FARMACEUTICA 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche 4.2 Posologia e
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Epoprostenolo PH&T 0.5 mg, Polvere e Solvente per soluzione per infusione Epoprostenolo PH&T 1.5 mg, Polvere e Solvente per soluzione per infusione
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Epoprostenolo PH&T 0.5 mg, Polvere e Solvente per soluzione per infusione Epoprostenolo PH&T 1.5 mg, Polvere e Solvente per soluzione per infusione
