Smistamento sistematico H. Staudinger
|
|
|
- Maria Pizzi
- 7 anni fa
- Просмотров:
Транскрипт
1 Smistamento sistematico H. Staudinger Consente mediante procedimenti sistematici lo smistamento in gruppi di una miscela incognita sulla base delle diverse caratteristiche chimico-fisiche dei componenti. Smistamento sistematico H. Staudinger Miscela Riscaldamento su bagno d olio a 140 C Residuo (PV) Frazione volatile (MV) H 2 Soluzione (MV2) Sostanze idrofile a basso PM: acidi, ammine aldeidi, chetoni, alcooli, ecc Residuo (MV1) Sostanze lipofile a basso PM: idrocarburi alogenuri alchilici 1
2 Smistamento sistematico H. Staudinger Frazione volatile La frazione volatile (M.V.) di un miscuglio è la frazione che distilla riscaldando la miscela con bagno d olio esterno a 140 C. Si pone la mix in un palloncino da distillare e si riscalda lentamente, portando la temperatura del bagno d olio fino a 140 C. Se la frazione volatile è presente, cosa da escludersi se la mix è solida, riscaldando si svolgeranno i vapori ed il termometro salirà. La frazione volatile si esamina a parte del residuo non volatile che è rimasto nel palloncino. La separazione della frazione volatile è completa allorché il termometro inizierà a scendere, indicando così assenza di vapori. Conviene fare una prova preliminare per accertarsi della presenza della frazione volatile, distillando una piccola porzione della miscela. In caso positivo si esegue la distillazione su una parte della miscela. gni componente passato nella frazione volatile è sicuramente solubile in etere, in quanto bassobollente e privo quindi di legami ionici, operiamo un primo smistamento con H 2. Smistamento sistematico H. Staudinger Frazione volatile: solubilità in H 2 Nella fase acquosa si scioglieranno i termini contenenti gruppi idrofili (aldeidi, chetoni, acidi, ammine, alcooli a basso P.M.). Mentre il residuo insolubile è costituito da sostanze organiche quali idrocarburi ed alogenuri alchilici (quelli aromatici, altobollenti non passano nella frazione volatile). Alcune sostanze che reagiscono con l acqua sono le anidridi e i cloruri degli acidi con p.e. < 140 2
3 Smistamento sistematico H. Staudinger Residuo (PV) Residuo (PV3 + PV4) H 2 Et 2 Soluzione (PV1 + PV2) H 2 (estrazione) Residuo Soluzione Sol. Acquosa Sol. Eterea evaporazione evaporazione IV gruppo (PV4) III gruppo (PV3) II gruppo (PV2) I gruppo (PV1) amido, cellulosa ed altri polimeri sali organici, ac.solfonici, idrati di C, ac.policarbossilici e idrossipolicarbossilici polifenoli, poliamine, ossiacidi, ac.bicarbossilici Idrocarburi superiori, derivati alogenati, sostanze a carattere neutro, acidi carbossilici, ammine, fenoli, alcoli Smistamento sistematico H. Staudinger Residuo non volatile: trattamento in Et 2 Il residuo della distillazione della frazione volatile viene trattato con etere, dibattendo nello stesso palloncino di distillazione od in una beuta; la soluzione eterea si allontana da un eventuale residuo insolubile preferibilmente per decantazione, evitando per quanto possibile una filtrazione, assai difficile per l elevata volatilità del solvente. Si ripete il trattamento nelle stesse proporzioni. Alla fine dei trattamenti si otterranno 4 gruppi. Residuo non volatile: estrazione con H 2 Il residuo della soluzione eterea viene trattata con acqua dando luogo alla separazione delle sostanze in due gruppi: gruppo IV o PV4 (sostanze insolubili in etere e H 2 ). Tra esse vi sono composti organici ad elevato PM (amido, cellulosa e altri polimeri) gruppo III o PV3 (sostanze insolubili in etere e solubili in H 2 ). Tra esse vi sono sostanze con tipico comportamento minerale quali i sali di acidi e basi organiche, gli acidi solfonici, gli idrati di carbonio e acidi policarbossilici e idrossipolicarbossilici. 3
4 Smistamento sistematico H. Staudinger Residuo non volatile: soluzione acquosa La soluzione eterea, posta in un imbuto separatore, viene dibattuta con H 2 fino a totale estrazione il che apprezza evaporando sotto vuoto piccole porzioni della soluzione acquosa. Si riuniscono le soluzioni acquose e per evaporazione del solvente sotto vuoto si ottiene il II gruppo o PV2 (sostanze solubili in etere e H 2 ). In questo gruppo si trovano sostanze quali: polifenoli, poliamine, ossiacidi ed acidi bicarbossilici. Residuo non volatile: soluzione eterea Dopo il dibattimento nell imbuto separatore la soluzione eterea conterrà le sostanze del gruppo I o PV1 (solubili in etere e poco solubili in acqua) che verranno smistate sulla base dell acidità, basicità o neutralità delle singole sostanze. A tale gruppo appartiene la maggior parte delle sostanze di interesse chimicofarmaceutico:idrocarburi superiori e derivati alogenati, tutte le sostanze a carattere neutro, le sostanze debolmente polari a PM medio come acidi carbossilici, ammine, fenoli alcoli. I gruppo (PV1) Idrocarburi superiori, derivati alogenati, sostanze a carattere neutro, acidi carbossilici, ammine, fenoli, alcoli neutra Acidi forti (sol. bicarbonato) Acidi media forza (sol. carbonato) Eteri, esteri, fenoli, alcoli Aldeidi, chetoni. TUTTI ad ALT P.M, 4
5 I gruppo (PV1) Smistamento del I gruppo: soluzione HCl Una piccola frazione della soluzione eterea viene evaporata alla pompa per accertarsi della presenza del I gruppo. La soluzione etera viene dibattuta in imbuto separatore con HCl 2N, ripetendo il trattamento fino a totale estrazione, controllando se l estratto acido fornisce ancora per alcalinizzazione un precipitato o un semplice intorbidamento. Nella soluzione acida passano i cloridrati delle ammine, che vengono poi messe in libertà mediante alcalinizzazione con una base forte e quindi separate per filtrazione o per estrazione con etere. I gruppo (PV1) Smistamento del I gruppo: soluzione eterea Viene trattata con NaHC 3 e la successiva acidificazione con HCl dell estratto basico fornisce gli acidi forti. Viene quindi estratta con Na 2 C 3 2N in modo da fornire i composti acidi di media forza. Viene infine trattata con NaH 2N in modo da estrarre gli acidi deboli (fenoli, enoli, nitroderivati alifatici, tioli) che si riottengono per acidificazione. La soluzione eterea, estratta in precedenza con acidi e basi, contiene ora la frazione eterea neutra che, previa evaporazione, fornisce la frazione neutra successivamente smistata nei singoli componenti. 5
6 Eteri, esteri, fenoli, alcoli Aldeidi, chetoni. TUTTI ad ALT P.M, Eteri, esteri, fenoli, alcoli Alcuni chetoni TUTTI ad ALT P.M, Eteri, esteri, alcoli, fenoli, Alcuni chetoni TUTTI ad ALT P.M, Trattamento col reattivo di Girard T oppure con NH 2 H Eteri, esteri, alcoli, fenoli, TUTTI ad ALT P.M, Alcoli, Eteri, fenoli, TUTTI ad ALT P.M, Vengono dall idrolisi degli esteri!! Eteri, fenoli, TUTTI ad ALT P.M, Idrocarburi superiori, derivati alogenati, Fenoli, eteri atomatici TUTTI ad ALT P.M, TUTTI ad ALT P.M, + Fenoli provenienti dalla reaz con HI Vengono dagli eteri aromatici + HI Idrocarburi superiori e derivati alogenati, TUTTI ad ALT P.M, Aromatici e non fase eterea (idrocarburi alifatici ed alogenuri) Vengono dagli aromatici!! fase acquosa (sali sodici di acidi solfonici) 6
7 La soluzione eterea viene trattata con HCl gassoso che in etere forma sali insolubili con ammine debolissime (es.trifenilammina): il precipitato, costituito dal cloridrato, si separa per filtrazione. La fase eterea trattata con NaHS 3 forma i prodotti bisolfitici di addizione di Bertagnini con aldeidi (molto reattive) e metil-chetoni a basso P.M.: R C R' + S H Na Bertagnini R' R C S H Na Questi prodotti sono insolubili in etere ed in genere insolubili in H 2 : si raccolgono quindi come pp., che, trattato con acidi od alcali diluiti, fornisce il nuovo composto carbonilico libero. Se il prodotto di addizione è solubile in etere lo si estrae con la fase acquosa, che per successiva idrolisi con acidi o basi diluite, fornisce di nuovo l aldeide ed il chetone. R H CHH + H 2 NaHS 3 + R CH H 2 + RCH S 3 Na H La soluzione eterea risultante si tratta, dopo evaporazione sotto vuoto, con anidride ftalica che con gli alcooli forma gli ftalati acidi, i quali, come monoesteri di un acido bicarbossilico, sono estraibili con Na 2 C 3. 7
8 Dopo il trattamento con anidride ftalica a caldo, si aggiunge etere e si dibatte con Na 2 C 3 2N; nella fase acquosa alcalina si raccoglie lo ftalato acido che si ottiene come precipitato per acidificazione. Per idrolisi a caldo del pp. Si ottiene di nuovo libero l alcool, che si separa per distillazione dell acido ftalico solido: C C + RH CH CR H 2 CH CH + RH Dallo strato etereo risultante si estraggono i chetoni che non hanno reagito con il bisolfito. Questo si può fare con due metodi: 1. Reazione con NH 2 H per dare le chetossime, estraibili con NaH, da cui si ottiene il chetone per idrolisi acida. In queste condizioni reagiscono anche gli esteri che forniscono gli acidi idrossammici, per cui si preferisce il secondo metodo (vedi avanti). R C R' + NH 2 H H 2 + R C NH R' R CR' + NH 2 H R'H + R C NHH 8
9 Reazione con il reattivo di Girard T, sale ammonico della idrazide della glicolla trimetilata dell azoto. CH 3 R CH 3 R H 3 C N CH 2 CH 3 C NH NH 2 Cl + C R' - H 2 H 3 C N CH 2 CH 3 C Cl NH N C R' Il sale ammonico è insolubile in etere, mentre in H 2 precipita o passa in soluzione; nel primo caso si separa per filtrazione e per idrolisi acida anche a freddo si ottiene il chetone libero, nel secondo estrae con la fase acquosa il derivato e per successiva idrolisi si libera il composto carbonilico. La fase eterea contiene varie sostanze organiche: idrocarburi, eteri, esteri ed alogeno derivati. Gli esteri si separano saponificando a caldo con NaH la fase evaporata. Dopo la saponificazione si aggiunge etere; nella fase eterea passano gli idrocarburi, eteri, alogenuri arilici e gli alcooli ad alto P.M., che sono insolubili in H 2, derivanti dalla saponificazione degli esteri. Nella soluzione alcalina acquosa si hanno i sali sodici degli acidi e gli alcooli a basso P.M. originati dall idrolisi. La fase eterea viene evaporata e poi trattata con anidride ftalica per separare gli alcoli ad alto P.M.; si aggiungono poi il Na 2 C 3 e l etere che porta con sé gli eteri, gli idrocarburi e gli alogenuri. 9
10 La soluzione eterea viene evaporata e poi trattata con HCl conc.; si ha passaggio degli eteri alchilici in soluzione nella fase acida come sali di ossonio, riottenibili poi mediante alcalinizzazione. Il residuo insolubile viene idrolizzato con HI azeotropico, in questo caso gli eteri fenolici vengono scissi per dare fenoli ed alogenuri alchilici. R + HI RI + H Si distilla la soluzione e nel distillato passano gli ioduri alchilici volatili; il residuo contiene idrocarburi, alogenuri aromatici e fenoli. Il residuo ottenuto viene trattato con NaH ed etere: nella fase acquosa alcalina passano i fenoli che successivamente si liberano per acidificazione, mentre gli idrocarburi e gli alogenuri si sciolgono in etere. Si evapora questo e si tratta il residuo con H 2 S 4 : in queste condizioni gli idrocarburi aromatici danno gli acidi solfonici corrispondenti. Si aggiunge soda ed etere: nella fase acquosa basica passano gli acidi solfonici, mentre l etere scioglie gli alogenuri arilici e gli idrocarburi alifatici. 10
Smistamento sistema+co H. Staudinger
 Smistamento sistema+co H. Staudinger onsente mediante procedimen+ sistema+ci lo smistamento in gruppi di una miscela incognita sulla base delle diverse cara8eris+che chimico-fisiche dei componen+ Frazione
Smistamento sistema+co H. Staudinger onsente mediante procedimen+ sistema+ci lo smistamento in gruppi di una miscela incognita sulla base delle diverse cara8eris+che chimico-fisiche dei componen+ Frazione
Fasi di identificazione di una sostanza
 Fasi di identificazione di una sostanza Serie di operazioni attraverso le quali è possibile ottenere i dati sul comportamento chimico e fisico del composto, che poi devono essere confrontati con quelli
Fasi di identificazione di una sostanza Serie di operazioni attraverso le quali è possibile ottenere i dati sul comportamento chimico e fisico del composto, che poi devono essere confrontati con quelli
Esteri degli acidi carbossilici
 Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Esteri degli acidi carbossilici Sono sostanze neutre facilmente idrolizzabili in ambiente acido e basico. Stato fisico Il punto di fusione degli esteri è inferiore a quello degli acidi aventi uguale P.M.
Identificazione degli alcoli
 Identificazione degli alcoli R-OH Stato fisico Gli alcoli sono sostanze neutre caratterizzate dalla presenza di un gruppo ossidrilico legato ad un atomo di carbonio alifatico. I primi termini degli alcoli
Identificazione degli alcoli R-OH Stato fisico Gli alcoli sono sostanze neutre caratterizzate dalla presenza di un gruppo ossidrilico legato ad un atomo di carbonio alifatico. I primi termini degli alcoli
ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA
 ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA L'obiettivo dell esperienza è quello di separare una miscela costituita da un composto organico con caratteristiche
ESTRAZIONE DI UN COMPOSTO ACIDO, UNO BASICO E UNO NEUTRO DA UNA FASE INIZIALE ORGANICA L'obiettivo dell esperienza è quello di separare una miscela costituita da un composto organico con caratteristiche
Estrazione. Il processo di estrazione con solventi è impiegato per l isolamento di
 Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
ESTRAZIONE CON SOLVENTE
 ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
ESTRAZIONE CON SOLVENTE TECNICA DI SEPARAZIONE BASATA SUL TRASFERIMENTO SELETTIVO DI UNO O PIÙ COMPONENTI DI UNA MISCELA SOLIDA, LIQUIDA O GASSOSA DA UN SOLVENTE AD UN ALTRO SOLVENTE IMMISCIBILE CON IL
Capitolo 8 Acidi Carbossilici e Derivati
 Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Chimica rganica Scienze della Terra, dell Ambiente e del Territorio Capitolo 8 Acidi Carbossilici e Derivati rganic Chemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic Chemistry, 3 rd Edition
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE
 2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
ANALISI E SEPARAZIONE DI SOSTANZE ORGANICHE TRAMITE LA SOLUBILITÀ. Prof. Antonio Lavecchia
 ANALISI E SEPARAZIONE DI SOSTANZE ORGANICHE TRAMITE LA SOLUBILITÀ Prof. Antonio Lavecchia Solubilità in Acqua Solubilità in Acqua B: + H-OH B + -H + OH - base R-COOH + H 2 O R-COO - + H 3 O + acido Solubilità
ANALISI E SEPARAZIONE DI SOSTANZE ORGANICHE TRAMITE LA SOLUBILITÀ Prof. Antonio Lavecchia Solubilità in Acqua Solubilità in Acqua B: + H-OH B + -H + OH - base R-COOH + H 2 O R-COO - + H 3 O + acido Solubilità
Analisi strutturale Identificazione dei gruppi funzionali
 Identificazione dei gruppi funzionali Riconoscimento di specifici raggruppamenti chimici (gruppi funzionali) presenti nella sostanza in esame. Reazioni chimiche che in determinate condizioni siano specifiche
Identificazione dei gruppi funzionali Riconoscimento di specifici raggruppamenti chimici (gruppi funzionali) presenti nella sostanza in esame. Reazioni chimiche che in determinate condizioni siano specifiche
ESTRAZIONE SOLVENTI. tecnica di separazione e purificazione
 ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
ESTRAZIONE. Prof. Antonio Lavecchia
 ESTRZIONE Prof. ntonio Lavecchia Teoria Estrazione legge di ripartizione o legge di distribuzione di Nernst fase fase Et 2 O H 2 O + soluto Teoria Estrazione Da un punto di vista termodinamico, si avrà:
ESTRZIONE Prof. ntonio Lavecchia Teoria Estrazione legge di ripartizione o legge di distribuzione di Nernst fase fase Et 2 O H 2 O + soluto Teoria Estrazione Da un punto di vista termodinamico, si avrà:
Per estrazione si intende nell accezione più semplice il trasferimento di un soluto da una fase ad un altra
 Per estrazione si intende nell accezione più semplice il trasferimento di un soluto da una fase ad un altra MATRICE LIQUIDA Estrazione liquido liquido (LLE) estrazione in discontinuo (imbuto separatore)
Per estrazione si intende nell accezione più semplice il trasferimento di un soluto da una fase ad un altra MATRICE LIQUIDA Estrazione liquido liquido (LLE) estrazione in discontinuo (imbuto separatore)
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
Analisi dei Medicinali II
 Università degli Studi Magna Græcia cia di Catanzaro Facoltà di Farmacia Corso di Analisi dei Medicinali II A.A. 2007/2008 Francesco rtuso Esame sistematico di una sostanza organica Isolamento della sostanza
Università degli Studi Magna Græcia cia di Catanzaro Facoltà di Farmacia Corso di Analisi dei Medicinali II A.A. 2007/2008 Francesco rtuso Esame sistematico di una sostanza organica Isolamento della sostanza
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
REGISTRO DELLE LEZIONI 2005/2006. Tipologia. Addì Tipologia. Addì Tipologia
 Presentazione del corso. Modalità di svolgimento della prova di esame. Introduzione all'analisi organica qualitativa. Analisi organica qualitativa: comportamento alla calcinazione. Saggio di Laissagne
Presentazione del corso. Modalità di svolgimento della prova di esame. Introduzione all'analisi organica qualitativa. Analisi organica qualitativa: comportamento alla calcinazione. Saggio di Laissagne
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
SAGGI SPECIFICI ACIDI CARBOSSILICI
 SAGGI SPECIFICI ACIDI CARBOSSILICI Acido Acetilsalicilico: - Per riscaldamento a secco con Ca(OH) 2 sviluppa acetone i cui vapori, a contatto con una cartina imbevuta di o-nitrobenzaldeide, la colorano
SAGGI SPECIFICI ACIDI CARBOSSILICI Acido Acetilsalicilico: - Per riscaldamento a secco con Ca(OH) 2 sviluppa acetone i cui vapori, a contatto con una cartina imbevuta di o-nitrobenzaldeide, la colorano
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Sostanza pura. Il termine sostanza indica il tipo di materia di cui è fatto un corpo.
 Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI
 I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico. estere dietilico dell acido adipico (pe 245 C)
 NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Reattività degli acidi carbossilici e loro derivati. La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica
 Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Reattività degli acidi carbossilici e loro derivati La reazione caratteristica di questi composti è la Sostituzione Nucleofila Acilica δ - δ + Nu - Y Il carbonio carbonilico è elettrofilo, in grado di
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Ammine R N + H. ammina terziaria ammina secondaria ammina primaria sale di ammonio quaternario
 AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
SOSTANZE DA IDENTIFICARE ORGANO-METALLICHE ORGANICHE ORGANICHE AZOTATE ORGANICHE NON AZOTATE ORGANICHE AZOTATE NON REAGISCONO CON I REATTIVI
 Il riconoscimento dei gruppi funzionali presenti in un composto organico incognito è utilissimo per la determinazione della struttura del campione in esame. Il riconoscimento viene effettuato attraverso
Il riconoscimento dei gruppi funzionali presenti in un composto organico incognito è utilissimo per la determinazione della struttura del campione in esame. Il riconoscimento viene effettuato attraverso
Leggere attentamente il file sulla sicurezza prima di accedere al laboratorio
 Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Analizziamo i casi più frequenti. Acido forte Base forte Acido debole Base debole Idrolisi Tampone
 Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Materiale occorrente. Introduzione. Procedura. Estrazione della caffeina dalla polvere di caffè. Caffè macinato. Diclorometano, CH2Cl2
 Estrazione della caffeina dalla polvere di caffè Materiale occorrente Caffè macinato Diclorometano, CH2Cl2 Carbonato di calcio, CaCO3 Acqua Introduzione In questa esperienza viene proposta l estrazione
Estrazione della caffeina dalla polvere di caffè Materiale occorrente Caffè macinato Diclorometano, CH2Cl2 Carbonato di calcio, CaCO3 Acqua Introduzione In questa esperienza viene proposta l estrazione
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione
![ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione ESERCIZI ESERCIZI. 3) Una soluzione acquosa è sicuramente acida se: O + ] > 10-7 M O + ] > [OH - ] O + ] < [OH - ] d. [OH - ] < 10-7 M Soluzione](/thumbs/57/40353116.jpg) ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
ESERCIZI 1) Il prodotto ionico dell acqua (K w ) vale 10-14 : a. a qualunque temperatura b. solo per una soluzione acida c. solo per una soluzione basica d. solo a T = 25 C 2) Per l acqua pura risulta
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
RICERCA DELLA FUNZIONE CARBOSSILICA
 RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE
 1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2014/2015 1 Prima di iniziare ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2014/2015 1 Prima di iniziare ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
 Carboidrati I carboidrati (poliidrossialdeidi e poliidrossi chetoni) non hanno proprietà uniformemente riconosciute. Sono solidi bianchi o liquidi sciropposi, con sapore dolce, hanno carattere neutro e
Carboidrati I carboidrati (poliidrossialdeidi e poliidrossi chetoni) non hanno proprietà uniformemente riconosciute. Sono solidi bianchi o liquidi sciropposi, con sapore dolce, hanno carattere neutro e
Saggi preliminari. Esame organolettico Combustione Saggi di solubilità Comportamento chimico
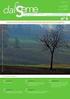 Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Acidi e Basi. Capitolo 15
 Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico
 NP 4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico CEt + FeCl 3 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Classificazione Tipo di
NP 4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico CEt + FeCl 3 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Classificazione Tipo di
Sintesi dell acetanilide
 Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
EQUILIBRI IN SOLUZIONE ACQUOSA
 EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
ALCOLI E FENOLI ALCOL FENOLO. Scaricato da Sunhope.it
 Indice Alcoli e fenoli: gruppo funzionale Alcoli: nomenclatura e classificazione Fenoli: nomenclatura Alcoli: principali reazioni Fenoli Eteri Epossidi Tioli Tioeteri ALLI E FENLI Alcoli e fenoli sono
Indice Alcoli e fenoli: gruppo funzionale Alcoli: nomenclatura e classificazione Fenoli: nomenclatura Alcoli: principali reazioni Fenoli Eteri Epossidi Tioli Tioeteri ALLI E FENLI Alcoli e fenoli sono
2008 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico
 28 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico H 3 C H acido 4-toluensolfonico + H C cicloesano 3 H CH 3 + CH 3 H 2 C 3 H
28 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico H 3 C H acido 4-toluensolfonico + H C cicloesano 3 H CH 3 + CH 3 H 2 C 3 H
Ammine. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Ammine Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
3016 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico
 6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
CHIMICA ORGANICA I - laboratorio AA 2009/10
 CHIMICA RGANICA I - laboratorio AA 2009/10 Esperienza 4 SEPARAZINE DI UN ALDEIDE DA UN SEMPLICE MISCELA UTILIZZATA NELLA MANIFATTURA DI PRFUMI Nell ampia varietà di molecole organiche utilizzate dall industria
CHIMICA RGANICA I - laboratorio AA 2009/10 Esperienza 4 SEPARAZINE DI UN ALDEIDE DA UN SEMPLICE MISCELA UTILIZZATA NELLA MANIFATTURA DI PRFUMI Nell ampia varietà di molecole organiche utilizzate dall industria
5007 Reazione dell anidride ftalica con la resorcina per formare fluoresceina
 57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
Relazione giorno 4 Febbraio 2011
 Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III
 LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
Isolamento della caffeina dalle foglie di tè
 SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
CHIMICA ORGANICA. Gli esteri
 1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
1 E8-ESTERI CHIMICA RGANICA ESTERI Formula generale R C R' Desinenza -ato Gli esteri I composti organici di questa classe presentano una struttura che deriva da quella degli acidi carbossilici in cui,
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE
 SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 5 Maggio 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
Esercitazione 6. Chimica biologica del Fe. Il Ferro ) 2 (SO 4 6H 2. Fe(NH 4
 Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
I METODI O TECNICHE DI SEPARAZIONE
 I METODI O TECNICHE DI SEPARAZIONE La chimica è l arte di separare, pesare e distinguere: sono tre esercizi utili anche a chi si accinge a descrivere fatti o a dare corpo alla propria fantasia... PRIMO
I METODI O TECNICHE DI SEPARAZIONE La chimica è l arte di separare, pesare e distinguere: sono tre esercizi utili anche a chi si accinge a descrivere fatti o a dare corpo alla propria fantasia... PRIMO
4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo
 4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico
 NP 4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me
NP 4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me
PIANO DELLE UDA Terzo Anno
 ITIS ENRICO MEDI PIANO DI STUDIO DELLA DISCIPLINA Chimica organica (indirizzo biotecnologie ambientali) PIANO DELLE UDA Terzo Anno UDA COMPETENZE UDA ABILITÀ UDA CONOSCENZE UDA UDA N. 1 Rappresentare una
ITIS ENRICO MEDI PIANO DI STUDIO DELLA DISCIPLINA Chimica organica (indirizzo biotecnologie ambientali) PIANO DELLE UDA Terzo Anno UDA COMPETENZE UDA ABILITÀ UDA CONOSCENZE UDA UDA N. 1 Rappresentare una
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
ALCOLI, ETERI, TIOLI. Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3
 ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide
 1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
