A N IL IL NUCLEO ATOMICO. Un nucleo atomico è caratterizzato da:
|
|
|
- Antonio Micheli
- 9 anni fa
- Просмотров:
Транскрипт
1 Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni presenti nel nucleo atomico. Se indichiamo con N il numero di neutroni, possiamo scrivere: A=N+Z. Elettroni (-) Protoni (+) Neutroni (neutri) A X Z N Interazione forte interazione coulombiana (elettrostatica) ISOBARI ISOTOPI ISOTONI Nuclidi con eguale numero di massa A Nuclidi con eguale numero atomico Z Nuclidi con eguale numero di neutroni N
2 TAVOLA DEI DEI NUCLIDI Numero di protoni Z Numero di neutroni N
3 TAVOLA DEI DEI NUCLIDI
4 TAVOLA DEI DEI NUCLIDI Con il termine nuclide si indicano tutti gli isotopi conosciuti di elementi chimici Stabili: 279 Instabili: ~ 5000 Numero di protoni Z Numero di neutroni N Con il termine radionuclide si indicano tutti gli isotopi instabili che decadono emettendo energia sotto forma di radiazioni (particelle e/o radiazioni e.m.)
5 LA LA LEGGE DEL DEL DECADIMENTO RADIOATTIVO L istante esatto in cui un radionuclide decadrà non si può prevedere esattamente. Si può tuttavia notare che il numero di decadimenti che avvengono in una sostanza radiaottiva rispetta una legge statistica ben precisa. Consideriamo una sostanza radioattiva contenente, ad un generico istante t, un numero N di nuclei molto grande. Il numero di nuclei N che ci si aspetta che decadono in un intervallo t è proporzionale all intervallo di tempo e al numero N di nuclei presenti: N N t Il segno meno indica il fatto che il numero di atomi diminuisce nel tempo èdetta costante di decadimento, ha le dimensioni di un inverso del tempo (s -1 ) e rappresenta una probabilità di decadimento per unità di tempo, tanto maggiore è il suo valore, tanto più alta è la probabilità di decadimento. ESEMPIO: Il valore della costante di decadimento dipende in modo critico dal 60 Co 238 U probabilità di 1/240 milioni di disintegrarsi in un secondo s -1 probabilità di 1/( ) s -1 radionuclide considerato: probabilità di circa 1/ s Rn Quanto maggiore è, tanto più elevata è la frequenza dei decadimenti
6 LA LA LEGGE DEL DEL DECADIMENTO RADIOATTIVO dn Risolvendo l equazione differenziale si ottiene la legge del N dt decadimento radioattivo: 1.5 N N N0.5 0 /2 0.4 N 0 /e 0.3 N /4 0.1 N N T 1/ T 1/ e t dove si è indicato con N 0 il numero di nuclei di cui è costituito il campione radioattivo al tempo t=0: t 1 vita media T ln tempo di dimezzamento tempo che deve trascorrere affinché il numero di nuclei si riduca della metà Anche il valore del tempo di dimezzamento (e vita media) dipende ovviamente dal radionuclide considerato. Esempio: a parità di elemento chimico: 219 Th: T 1/2 =10-6 secondi 232 Th: T 1/2 = anni
7 LA LA LEGGE DEL DEL DECADIMENTO RADIOATTIVO (dimostrazione) dn N dt Separo le variabili dn N dt Integro ambo i membri ln N t C C è una costante. Dalla definizione di logaritmo N N N 0 tc e Indicando con N 0 il numero di nuclei di cui è costituito il campione al tempo t=0 si ha: e 0C e C Quindi: tc C t e e e N0 e t N N 0 e t
8 LA LA LEGGE DEL DEL DECADIMENTO RADIOATTIVO Una grandezza che esprime la velocità di decadimento di una data sostanza radioattiva è l attività: N t Essa esprime il numero di decadimenti in una unità di tempo. Unità di misura nel S.I. Becquerel (Bq) 1 Bq equivale ad 1 disintegrazione al secondo A N L unità di misura originaria dell attività, ormai in disuso è il Curie (Ci) 1 Ci = Bq La legge di decadimento si può quindi esprimere anche in termini di attività: A A 0 e t dove si è indicato con A 0 l attività del campione al tempo t=0: 1.5 A A A /2 0.4 A 0 /e 0.3 A 0 / T 1/ T 1/ t4.0
9 IL TEMPO DI DIMEZZAMENTO IL TEMPO DI DIMEZZAMENTO Trascorsi n tempi di dimezzamento, l attività iniziale si è ridotta a: n 2 1
10 Nota la massa m (grammi) di una sorgente radioattiva con costante di decadimento, la sua attività è pari a: A CALCOLO DELL ATTIVITA DI DI UNA UNA SOSTANZA RADIOATTIVA ESEMPIO: N m A N A A è il numero di massa e N A il numero di Avogadro Calcolare l attività di 1g di 226 Ra sapendo che il tempo di dimezzamento è pari a 1600 anni. Determinare inoltre il valore dell attività dopo 3200 anni e dopo 2000 anni. T anni A N ln 2 m T A 1/ 2 10 N A s A N Essendo il tempo di dimezzamento pari a 1600 anni, dopo 3200 anni (ossia dopo 2 tempi di ln 2 dimezzamento) l attività si sarà ridotta di un fattore 4: 2T1/ 2 A / 2 0 A(2T1 / 2) A0 e L attività dopo 2000 anni la si ricava dalla legge di decadimento: ln anni anni A( 2000 anni) Bq e Bq Bq T 10 Bq Bq
11 ESEMPI: Calcolare l attività di 40 K in una banana, sapendo che essa contiene 525 mg di potassio. (T 1/2 del 40 K = anni, percentuale isotopica 40 K : 0.01%) 9 T anni A N ln 2 m T A 1/ 2 N A 16 s m è la massa (in grammi) del solo 40 K. E pari allo 0.01% della massa totale di K m A Bq g Nel corpo umano di un adulto vi sono circa 160 grammi di potassio, contenuti essenzialmente nelle ossa. E quindi una sorgente naturale di 40 K la cui attività è: g 23 A Bq s 40 7 g
12 ESEMPIO: Un rivelatore di radiazione sta misurando un'attività di 2000 Bq. Sapendo che il campione radioattivo è costituito da isotopi di 131 I il cui tempo di dimezzamento è di 8 giorni, si chiede quale era la sua attività 40 giorni fa. Si chiede inoltre quanto tempo occorre aspettare affinché l'attività si riduca a 100 Bq. ln 2 40 t t 8 A A 0 e A A e A e Bq In effetti 40 giorni corrispondono a 5 tempi di dimezzamento e si ritrova che: A( 5T1/ 2) A Bq Bq ln A t 1 ln A e t 0 1/ 2 t t ln 0 0 A0 A ln 2 A A T1 / 2 A t ln ln 35giorni ln 2 A ln A T A
13 TIPI TIPI DI DI DECADIMENTO RADIOATTIVO --ALFA ALFA Decadimento alfa: il nucleo instabile emette una particella alfa (), che è composta da due protoni e due neutroni, quindi una particella carica positivamente. Tale trasformazione può quindi essere rappresentata come: A Z X A Z 4 2 Y dove X e Y sono i simboli rispettivamente dell'elemento chimico padre e figlio. Il decadimento alfa interessa principalmente i nuclei pesanti (A>200) e deficitarii in neutroni
14 TIPI TIPI DI DI DECADIMENTO RADIOATTIVO --BETA BETA Decadimento beta: è un processo in cui si ha la trasformazione di un neutrone del nucleo in un protone, o viceversa la trasformazione di un protone in un neutrone. Nel primo caso si ha il decadimento beta meno ( - ) con emissione di un elettrone e di una particella di massa infinitesima (minore di un decimillesimo della massa dell'elettrone) e senza carica detta antineutrino. Nel secondo caso si ha il decadimento beta più ( + ) con emissione di un positrone e di un neutrino. Il positrone è una particella con caratteristiche identiche all'elettrone, ma carica positiva. I decadimenti - e + seguono rispettivamente gli schemi: A Z X A Z 1 Y e A Z X A Z 1 Y e decadimento β - : avviene per quei nuclei in cui vi è un eccesso di neutroni decadimento β + : avviene per quei nuclei in cui vi è un eccesso di protoni
15 TIPI TIPI DI DI DECADIMENTO RADIOATTIVO --GAMMA Emissione gamma: Un nucleo formatosi in seguito ad un decadimento radioattivo può ritrovarsi nel suo stato fondamentale oppure trovarsi in uno dei suoi stati eccitati. Come avviene per l atomo, anche il nucleo si porterà nella configurazione più stabile emettendo radiazione elettromagnetica corrispondente al salto energetico dei livelli interessati. A questa radiazione elettromagnetica viene dato il nome di raggi gamma. 60 Co 2626 kev 2506 kev 2159 kev 1333 kev Per l emissione gamma, sia la massa atomica A che il numero atomico Z rimangono invariati Struttura fine 0 kev 60 Ni
16 POTERE PENETRANTE DELLE RADIAZIONI Irraggiamento: - Esterno - Interno
17 ORIGINE DELLA RADIOATTIVITA Radioattività naturale Raggi cosmici (primari e secondari) Radionuclidi primordiali (isolati) Famiglie radioattive naturali Radioattività artificiale Origine e impieghi
18 LA LA RADIOATTIVITA NATURALE: I I RAGGI COSMICI La radiazione cosmica fu scoperta all inizio del XX secolo. V.F. Hess nel 1912 con un rivelatore di particelle cariche montato su un aerostato mostrò che la radiazione aumentava con l altitudine invece di diminuire. Tale radiazione era esterna alla terra; un flusso di particelle raggiunge le regioni più esterne dell atmosfera e interagisce con essa. A questa radiazione venne dato il nome di radiazione cosmica (o raggi cosmici), distinguendo tra raggi cosmici primari e raggi cosmici secondari; questi ultimi vengono creati dalla l interazione dei raggi cosmici primari con l atmosfera.
19 LA LA RADIOATTIVITA NATURALE: I I RAGGI COSMICI raggi cosmici primari protoni (~ 90%) nuclei di elio (~ 10%) nuclei pesanti (tracce) inoltre elettroni relativistici raggi X e gamma neutrini (solari, da SN) raggi cosmici secondari mesoni π e k muoni elettroni e positroni neutroni e protoni secondari radiazione elettromagnetica neutrini atmosferici
20 I I RADIONUCLIDI DI DI ORIGINE COSMOGENICA I raggi cosmici, interagendo con gli elementi costituenti l atmosfera terrestre, generano degli isotopi radioattivi. Datazioni n 7N 6C 1 1 p Il tempo di dimezzamento di questi radionuclidi è molto inferiore all età della Terra. La loro presenza è possibile solo grazie al fatto che essi sono continuamente prodotti dai raggi cosmici.
21 DATAZIONE CON CON C 14 6 C 14 5 N neutrino Determinazione del rapporto tra 14 C e 12 C nel campione Misure radiometriche (beta counter) Misure isotopiche (AMS)
22 DATAZIONE ESEMPIO: DATAZIONE CON CON C CON CON C Una misura chimica su un osso ha quantificato la presenza di 300 g di carbonio. Una misura dell attività del 14 C ha fornito un valore di 10 Bq. Determinare approssimativamente l epoca di appartenenza del campione. I 300 g di carbonio sono quasi tutto 12 C g di 12 C contengo 6.02x10 23 atomi, quindi 300 g contengono un numero di atomi di 12 C pari a: 23 Il numero di atomi di 14 C presenti quando l animale era in vita era: 12 N N C L attività originale corrispondente : ln 2 ln 2 13 A0 N0 N Bq T s 1/ 2 C 13 atomi atomi g g N C 25 atomi Questa è l attività fintanto che l animale era in vita. Dall istante del decesso cessa l assunzione di carbonio e quindi l attività di 14 C diminuisce secondo la legge di decadimento: A A 0 e t Da cui si ricava il tempo: 1 A0 T1/ 2 A ln ln A ln 2 A t 0
23 DATAZIONE ESEMPIO: DATAZIONE CON CON C CON CON C Sostituendo i valori dell attività al tempo t (ossia quella misurata) e dell attività iniziale (quella dell animale in vita), e ricordando il tempo di dimezzamento del 14 C si ottiene: 1 A0 T 2 A ln 1/ ln A ln 2 A t 0 1 A t ln ln A ln 2 10 anni Ci sarebbe ovviamente da considerare anche l analisi delle incertezze, stimare cioè l errore associato al risultato ottenuto!
24 I I RADIONUCLIDI PRIMORDIALI (ISOLATI) Esistono in natura una serie di radionuclidi di origine terrestre: sono radioisotopi con tempo di dimezzamento confrontabile con l età dell Universo. Il più importante è il 40 K che si trova pressoché ovunque (terreno, materiali edili, cibo, corpo umano).
25 ORIGINE DELLA RADIOATTIVITA LE LE SERIE SERIE RADIOATTIVE Tre radionuclidi con tempo di dimezzamento confrontabile con quello della terra decadono originando dei nuclei instabili che decadono a loro volta, creando, in questo modo, delle catene radioattive. catena dell 238 U Serie dell 238 U abbondanza isotopica = % T 1/2 = anni Serie del 232 Th abbondanza isotopica = 100 % T 1/2 = anni Serie dell 235 U abbondanza isotopica = 0.72 % T 1/2 = anni
26 LA LA RADIOATTIVITA ARTIFICIALE Esistono una serie di radioisotopi che sono, o sono stati, prodotti artificialmente dall uomo. Alcuni di questi sono stati rilasciati nell ambiente a seguito di incidenti nucleari (Chernobyl 1986, Mayak , Fukushima 2011) e test di armamenti nucleari condotti negli anni Alcuni di questi radioisotopi sono tuttora rivelabili in atmosfera o nel terreno (in particolare il 137 Cs, prodotto di fissione con tempo di dimezzamento di 30 anni). Ogni giorno vengono prodotti artificialmente radionuclidi essenziali per condurre esami diagnostici e terapie in medicina nucleare Molteplici sono anche gli usi di sorgenti di radiazioni artificiali utilizzati nell industria (produzione di energia elettrica) e nella ricerca
27 IMPIEGHI MEDICI DEI DEI RADIOISOTOPI Radioisotopi vengono legati chimicamente a molecole ed introdotti nell organismo in genere per via endovena, o orale. Queste molecole si distribuiscono all interno del corpo e vengono captate selettivamente da organi e tessuti. Radioisotopi sono utilizzati sia in diagnostica che in terapia Radio-traccianti gamma emettitori vengono utilizzati per la diagnosi di malattie (in primis tumori). La radiazione gamma emessa dal radioisotopo all interno del corpo riesce a fuoriuscire ed essere opportunamente rivelata ( 18 F, 99m Tc) E possibile la localizzazione del tracciante (e quindi della malattia) e seguirne l evoluzione temporale, valutando così la funzionalità dei tessuti interessati Radio-farmaci beta (o alfa) emettitori vengono utilizzati per la terapia di alcuni tumori. Tali particelle restano localizzate e rilasciano la loro energia in modo confinato ai tessuti tumorali ( 131 I-tiroide) Si sfrutta il danno biologico provocato dalle radiazioni sulle cellule tumorali per ucciderle o inibirne la moltiplicazione
28 IMPIEGHI MEDICI DEI DEI RADIOISOTOPI: SPECT SPECT e e PET PET Positron Emission Tomography 18 F (T 1/2 : 110 m) 99m Tc (T 1/2 : 6 h) Single-Photon Emission Computed Tomography
29 INTERAZIONE RADIAZIONE-MATERIA E CESSIONE DI DI ENERGIA Le radiazioni interagiscono con la materia cedendo la loro energia. Le modalità di interazione sono diverse a seconda del tipo di radiazione e dall energia posseduta. In particolare: Raggi X e gamma (IONIZZANTI): Effetto fotoelettrico Effetto Compton Produzione di coppia Particelle cariche pesanti (protoni, alfa, ioni): - perdita di energia per collisione con elettroni atomici Particelle cariche leggere (elettroni): - perdita di energia per collisione con elettroni atomici - perdita di energia per irraggiamento
30 Effetto Effetto fotoelettrico Processo di ionizzazione di un atomo da parte di radiazione e.m. Il fotone scompare assorbito dall atomo e viene emesso un elettrone la cui energia cinetica è data dalla differenza tra l energia del fotone incidente e l energia di legame dell elettrone: T e hf W E un processo a soglia: il fotone deve possedere un energia almeno pari all energia di legame dell elettrone. Non spiegabile dalla fisica classica (luce come un onda) ma facilmente spiegabile considerando la natura corpuscolare della radiazione e.m. e la proporzionalità tra frequenza ed energia.
31 Effetto Effetto Compton Scattering con un elettrone atomico supposto libero (energia di legame<<energia del fotone) Il fotone sopravvive ma degradato in energia. L energia del fotone in uscita dipende dall angolo di scattering. ' (1 cos) c In altri termini la lunghezza d onda del fotone scatterato è maggiore della lunghezza d onda del fotone incidente La relazione sopra si ricava trattando lo scattering Compton come un urto tra fotone ed elettrone ed imponendo le condizioni di conservazione dell energia e della quantità di moto.
32 Produzione di di coppie coppie Processo di interazione del fotone con il campo elettrico del nucleo. Il fotone scompare e si crea una coppia elettrone - positrone (conversione energia/materia). E un processo a soglia: il fotone deve possedere un energia almeno pari a due volte la massa dell elettrone (1.022 MeV). La vita del positrone è in genere breve: si ha annichilazione con un elettrone atomico a cui segue l emissione di due fotoni da 511 kev in direzioni opposte.
33 Attenuazione dei raggi X I fenomeni di interazione dei fotoni (raggi X) con la materia comportano l attenuazione del fascio: l intensità del fascio decresce esponenzialmente secondo la relazione I ( x) I 0 e x Il coefficiente èdetto coefficiente di attenuazione lineare e dipende dall energia dei fotoni e dal materiale attraversato
34 Attenuazione dei raggi X: esempio Consideriamo due tessuti disposti in successione, aventi coefficiente di attenuazione lineare dei raggi X rispettivamente di 1 =0.5 cm -1 e 2 =0.2 cm -1. Per raggiungere un terzo tessuto il fascio di raggi X deve superare 3 cm del primo tessuto e 5 cm del secondo. Quale percentuale di raggi X arriva al terzo tessuto? I 1 I 0 e 0.53 I 0 I 2 I 1 e 0.25 I 1 I 2 I 2 I 0 e 0.53 e 0.25 I I 0 8.2%
35 Percorso delle particelle cariche pesanti Le particelle cariche pesanti non vengono deviate dagli urti con gli elettroni atomici dell assorbitore. L intensità di un fascio di particelle (numero di particelle rivelate) resta quindi pressoché invariata fino alla fine del loro percorso (range). Il range dipende dal tipo di particella, dalla sua energia e dal materiale attraversato I continui urti con gli elettroni atomici dell assorbitore provocano invece una progressiva perdita di energia delle particelle cariche (rallentamento continuo)
36 Confronto tra diverse radiazioni Rilascio di dose (energia per unità di massa, vd. poi) per varie radiazioni in funzione della profondità in acqua. I protoni hanno la proprietà di rilasciare la maggior parte della loro energia quando si trovano a fine percorso e posseggono una energia molto bassa (picco di Bragg) Esempio: applicazione degli adroni (protoni, ioni pesanti) in radioterapia
37 LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita il rapporto tra l energia assorbita dal mezzo E e la sua massa m: D E m L unità di misura della dose nel S.I. è il Gray 1Gy 1J 1kg Dal punto di vista radioprotezionistico è importante notare che, anche a parità di dose assorbita, radiazioni diverse producono danno biologici diversi. Inoltre gli organi e tessuti hanno una radiosensibilità diversa. Si introducono quindi altre grandezze come la dose equivalente e la dose efficace, ricavate a partire dalla dose assorbita e introducendo opportuni fattori peso (di radiazione e tissutali) L unità di misura della dose equivalente ed efficace nel S.I. è il Sievert 1J 1Sv 1kg
38 DOSE DOSE ASSORBITA, DOSE DOSE EQUIVALENTE E DOSE DOSE EFFICACE D de dm La dose assorbita è definita per un volume infinitesimo di massa dm. 1J 1Gy La sua unità di misura è il Gray. 1kg H T wr DT, R Effetti deterministici E w T H T T Effetti stocastici R La dose equivalente è definita per un singolo organo o tessuto, e tiene conto di tutti i tipi di radiazione che incidono su di esso. Visto che radiazioni diverse hanno un diverso effetto biologico, si introducono dei fattori peso di radiazione w R. La sua unità di misura è il Sievert. 1Sv 1J 1kg La dose efficace è definita per l intero corpo umano, e tiene conto, oltre che di tutti i tipi di radiazione, anche dei principali organi radiosensibili. Visto che organi diversi hanno una diversa risposta alla dose, si introducono dei fattori peso tissutali w T. La sua unità di misura è il Sievert.
39 FATTORI PESO PESO TISSUTALI E DI DI RADIAZIONE
40 DOSE DOSE ASSORBITA, DOSE DOSE EQUIVALENTE E DOSE DOSE EFFICACE: ESEMPI A seguito dell irraggiamento con un fascio di fotoni vengono rilasciati 3 J in 0.5 kg di tessuto biologico. Calcolare la dose equivalente. Calcolare inoltre la dose equivalente nel caso l energia venga rilasciata da un fascio di protoni Per i fotoni: Dose assorbita: Dose equivalente: de 3J D 6Gy dm 0.5kg H T w R R D T, 16Gy R 6Sv Per i protoni: Dose assorbita: de 3J D 6Gy dm 0.5kg Dose equivalente: H T w R R D T, 26Gy R 12Sv
41 DOSE DOSE ASSORBITA, DOSE DOSE EQUIVALENTE E DOSE DOSE EFFICACE: ESEMPI Si consideri una dose equivalente a singoli organi: 3 msv alle gonadi, 2 msv al colon, 1 msv allo stomaco Calcolare la dose efficace E T w T H T msv
42 DOSE DOSE DOSE DOSE ASSORBITA, ASSORBITA, DOSE DOSE esempi esempi EQUIVALENTE E DOSE DOSE EFFICACE: ESEMPI Tessuti viventi esposti ad una dose di 200 Gy sono completamente distrutti. Valutare l aumento di temperatura dei tessuti causata da questa dose assorbita se non vi è alcuna dispersione di calore. Si assuma il calore specifico dei tessuti uguale a quello dell acqua (c=4180 J kg -1 K -1 ) Il calore Q necessario per variare di T la temperatura di una massa m è: Q c mt 1 T Q E D 200 J kg 0. K c m c m c 4180J kg K L effetto termico della dose da radiazione è quindi molto modesto e non è questa l origine del danno biologico.
43 DOSE DOSE DA DA RADIOATTIVITA NATURALE 2.4 msv/a (Intervallo msv/a) Radiazione cosmica: 0.39 msv/a ( ) Radiazione terrestre: 0.48 msv/a ( ) Esposizione per inalazione: 1.26 msv/a (0.2-10) 222 Rn: 1.15 msv/a 220 Rn: 0.10 msv/a Esposizione per ingestione: 0.29 msv/a ( ) % Population < > 10.0 Dose range (msv/a) DOSE DOSE DA DA RADIOATTIVITA ARTIFICIALE Circa 0.4 msv/a Esami medici diagnostici: 0.4 msv/a Test nucleari in atmosfera: msv/a Incidente di Chernobyl: msv/a Produzione di energia nucleare: msv/a Livello di assistenza sanitaria I: 1.2 msv/a II: 0.14 msv/a III: 0.02 msv/a IV: < 0.02 msv/a United Nation Scientific Committee on the Effects of Atomic Radiations, Rapporto 2000
44 EFFETTI BIOLOGICI DELLE RADIAZIONI Il danno cellulare è dovuto ai processi di ionizzazione ed eccitazione. Il danno può essere: diretto: interazione della radiazione con le strutture del DNA e rottura dei legami molecolari (dominante per particelle alfa, neutroni, ioni) indiretto: ionizzazione delle molecole d acqua e produzione di radicali liberi molto reattivi che attaccano chimicamente la cellula (dominante per raggi X e gamma)
45 EFFETTI BIOLOGICI DELLE RADIAZIONI Tipo di danno e durata Processi Fisico s Fisico-chimico 10-6 s Chimico secondi Biologico da minuti a decine di anni Assorbimento dell energia Interazione con le molecole, formazione dei radicali liberi Interazione dei radicali liberi con molecole, cellule e DNA Morte cellulare, mutazioni
46 EFFETTI BIOLOGICI DELLE RADIAZIONI Il danno più grave alla cellula è a carico del materiale genetico (DNA) Alterazioni del DNA possono causare: Morte istantanea della cellula con conseguente detrimento dell organo di appartenenza. Morte riproduttiva, la cellula non è più in grado di riprodursi. Apoptosi, cioè morte programmata della cellula Induzione di processo neoplastico.
47 EFFETTI BIOLOGICI DELLE RADIAZIONI Effetti deterministici Effetti biologici somatici che possono essere posti direttamente in relazione con la dose ricevuta (causa-effetto) - sono effetti a soglia, (al di sotto non si manifesta il danno) -la gravità aumenta all aumetare della dose - brevi periodi di latenza (minuti, ore, giorni) Effetti stocastici Effetti biologici probabilistici la cui frequenza nella popolazione è legata alla dose totale ricevuta dall intera popolazione - non esiste una soglia - sono di tipo probabilistico (non su tutti gli individui hanno lo stesso effetto) -la frequenza della loro comparsa aumenta con la dose - hanno lunghi periodi di latenza (mesi, anni) Esempi: eritema cutaneo, cataratta Esempio: induzione di tumori
L unità di misura della dose nel S.I. è il Gray
 LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
Radioattività e dosimetria
 Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
Radioattività artificiale Origine e impieghi
 ORIGIE DELL RDIOTTIVIT Radioattività naturale Raggi cosmici (primari e secondari) Radionuclidi primordiali (isolati) Famiglie radioattive naturali Radioattività artificiale Origine e impieghi L L RDIOTTIVIT
ORIGIE DELL RDIOTTIVIT Radioattività naturale Raggi cosmici (primari e secondari) Radionuclidi primordiali (isolati) Famiglie radioattive naturali Radioattività artificiale Origine e impieghi L L RDIOTTIVIT
Radioattività e dosimetria
 Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
Radioattività e dosimetria Un nucleo atomico è caratterizzato da: IL IL NUCLEO ATOMICO numero atomico (Z) che indica il numero di protoni numero di massa (A) che rappresenta il numero totale di nucleoni
Cenni di fisica moderna
 Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
DECADIMENTO RADIOATTIVO
 DECADIMENTO RADIOATTIVO Emissione di una o più particelle da parte di un nucleo. Tutti i decadimenti (tranne il decad. γ) cambiano Z e/o N del nucleo. Radionuclidi = Nuclidi radioattivi presenti in natura:
DECADIMENTO RADIOATTIVO Emissione di una o più particelle da parte di un nucleo. Tutti i decadimenti (tranne il decad. γ) cambiano Z e/o N del nucleo. Radionuclidi = Nuclidi radioattivi presenti in natura:
Fisica delle Apparecchiature per Radioterapia, lez. III RADIOTERAPIA M. Ruspa 1
 RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
TECNICHE RADIOCHIMICHE
 TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
TECNICHE RADIOCHIMICHE L ATOMO - Un atomo e costituito da un nucleo carico positivamente, circondato da una nuvola di elettroni carichi negativamente. - I nuclei atomici sono costituiti da due particelle:
Decadimento a. E tipico dei radioisotopi con Z > 82 (Pb), nei quali il rapporto tra il numero dei neutroni e quello dei protoni è troppo basso.
 Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
La Radioattività. da:ispra istituto superiore per la ricerca e protezione ambientale
 La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
La radioattività può avere un origine sia artificiale che naturale.
 http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
Lezione 24 Radiazioni Ionizzanti
 Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
Generalità Lezione 24 Radiazioni Ionizzanti Con il termine radiazione si descrivono fenomeni molto diversi fra loro: Emissione di luce da una lampada Emissione di calore da una fiamma Particelle elementari
DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA D =!E AREA CONTROLLATA. energia assorbita nell'unità di massa
 DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA AREA CONTROLLATA D =!E!m energia assorbita nell'unità di massa 2 UNITA' DI MISURA dose assorbita D =!E!m dimensioni [D] =
DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA AREA CONTROLLATA D =!E!m energia assorbita nell'unità di massa 2 UNITA' DI MISURA dose assorbita D =!E!m dimensioni [D] =
Interazione radiazione materia Dott.ssa Alessandra Bernardini
 Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].
![Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].](/thumbs/62/47096832.jpg) Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Uomo, ambiente e radiazioni
 Uomo, ambiente e radiazioni Natura delle radiazioni 76 Le radiazioni di cui si tratta parlando di tecnologia nucleare sono le radiazioni ionizzanti Natura delle radiazioni Cosa sono le radiazioni ionizzanti?
Uomo, ambiente e radiazioni Natura delle radiazioni 76 Le radiazioni di cui si tratta parlando di tecnologia nucleare sono le radiazioni ionizzanti Natura delle radiazioni Cosa sono le radiazioni ionizzanti?
Misura del coefficiente di assorbimento di vari materiali in funzione dell'energia del fascio dei fotoni incidenti
 materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna [email protected] Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna [email protected] Si definiscono radiazioni ionizzanti tutte le
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z. H deuterio (6000 volte abbondante)
 Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Esercizi su Chimica Nucleare e Nucleogenesi
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
La datazione mediante radioisotopi
 : Le trasformazioni nucleari: La datazione mediante radioisotopi Lezioni d'autore VIDEO Premessa (I) I processi radioattivi sono reazioni che dipendono dalla struttura nucleare degli atomi. Il rapporto
: Le trasformazioni nucleari: La datazione mediante radioisotopi Lezioni d'autore VIDEO Premessa (I) I processi radioattivi sono reazioni che dipendono dalla struttura nucleare degli atomi. Il rapporto
SPECT (Gamma Camera)
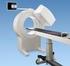 SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
SPECT-PET Nella tomografia a raggi-x si usa la misura del coefficiente di attenuazione del tessuti per dedurre informazioni diagnostiche sul paziente. La tomografia ad emissione d altra parte utilizza
RADIAZIONI IONIZZANTI
 RADIAZIONI IONIZZANTI PREMESSA Le radiazioni ionizzanti sono quelle radiazioni dotate di sufficiente energia da poter ionizzare gli atomi (o le molecole) con i quali vengono a contatto. La caratteristica
RADIAZIONI IONIZZANTI PREMESSA Le radiazioni ionizzanti sono quelle radiazioni dotate di sufficiente energia da poter ionizzare gli atomi (o le molecole) con i quali vengono a contatto. La caratteristica
Il Nucleo. Dimensioni del nucleo dell'ordine di 10. m Il raggio nucleare R = R 0 -15
 Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
La chimica nucleare. A cura della prof. ssa. Barone Antonina
 La chimica nucleare A cura della prof. ssa Barone Antonina La radioattività Nella seconda metà dell 800, Henry Becquerel, Pierre e Marie Curie, scoprirono che alcuni elementi( uranio, torio, radio) emettevano
La chimica nucleare A cura della prof. ssa Barone Antonina La radioattività Nella seconda metà dell 800, Henry Becquerel, Pierre e Marie Curie, scoprirono che alcuni elementi( uranio, torio, radio) emettevano
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
Radioattivita (radiazioni ionizzanti) e salute. 1a parte
 Radioattivita (radiazioni ionizzanti) e salute Cristiana Peroni Dipartimento di Fisica Sperimentale dell Universita di Torine e Istituto Nazionale di Fisica Nucleare 1a parte 4/11/2005 C.Peroni 1 Che cosa
Radioattivita (radiazioni ionizzanti) e salute Cristiana Peroni Dipartimento di Fisica Sperimentale dell Universita di Torine e Istituto Nazionale di Fisica Nucleare 1a parte 4/11/2005 C.Peroni 1 Che cosa
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI
 ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
ORBITALI E CARATTERISTICHE CHIMICHE DEGLI ELEMENTI Nelle reazioni chimiche gli atomi reagenti non cambiano mai la loro natura ( nucleo ) ma la loro configurazione elettronica. Nello specifico ad interagire
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].
![Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].](/thumbs/62/47096834.jpg) Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA
 INDICE Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA Capitolo 1 Le radiazioni ionizzanti 19 1.1 Introduzione 19 1.2 Il fondo naturale di radiazione 21 1.2.1 La radiazione
INDICE Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA Capitolo 1 Le radiazioni ionizzanti 19 1.1 Introduzione 19 1.2 Il fondo naturale di radiazione 21 1.2.1 La radiazione
SPETTROMETRIA GAMMA SPETTROMETRIA GAMMA
 La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
La spettrometria gamma è un metodo di analisi che consente la determinazione qualitativa e quantitativa dei radionuclidi gamma-emettitori presenti in un campione di interesse. Il successo di questo metodo
INTERAZIONE DELLA RADIAZIONE CON CON LA LA MATERIA. Dal punto di vista dell interazione con la materia le radiazioni IONIZZANTI si classificano in:
 INTERAZIONE DELLA RADIAZIONE CON CON LA LA MATERIA Dal punto di vista dell interazione con la materia le radiazioni IONIZZANTI si classificano in: DIRETTAMENTE IONIZZANTI INDIRETTAMENTE IONIZZANTI Le radiazioni
INTERAZIONE DELLA RADIAZIONE CON CON LA LA MATERIA Dal punto di vista dell interazione con la materia le radiazioni IONIZZANTI si classificano in: DIRETTAMENTE IONIZZANTI INDIRETTAMENTE IONIZZANTI Le radiazioni
MISURA DELLA MASSA DELL ELETTRONE
 MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
MISURA DELLA MASSA DELL ELETTRONE di Arianna Carbone, Giorgia Fortuna, Nicolò Spagnolo Liceo Scientifico Farnesina Roma Interazioni tra elettroni e fotoni Per misurare la massa dell elettrone abbiamo sfruttato
Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti.
 1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
ELEMENTI di CHIMICA NUCLEARE. La FISSIONE NUCLEARE
 ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
Radiazioni ionizzanti
 Radiazioni ionizzanti Qualunque radiazione in grado di provocare fenomeni di ionizzazione. Radiazione: trasferimento di energia attraverso lo spazio. Ionizzazione: fenomeno per il quale, da un atomo stabile
Radiazioni ionizzanti Qualunque radiazione in grado di provocare fenomeni di ionizzazione. Radiazione: trasferimento di energia attraverso lo spazio. Ionizzazione: fenomeno per il quale, da un atomo stabile
Radiazioni ionizzanti
 Radiazioni ionizzanti Radiazioni ionizzanti interagiscono con la materia determinando fenomeni di ionizzazione sia direttamente (elettroni, protoni, particelle alfa) che indirettamente (neutroni) cedendo
Radiazioni ionizzanti Radiazioni ionizzanti interagiscono con la materia determinando fenomeni di ionizzazione sia direttamente (elettroni, protoni, particelle alfa) che indirettamente (neutroni) cedendo
Atomi. Negli atomi, il numero di protoni é uguale al numero di elettroni, così che l'atomo é elettricamente neutro.
 Atomi Combinations of 26 letters make up every word in the English language. Similarly, all material things in the world are composed of different combinations of about 100 different elements. La materia
Atomi Combinations of 26 letters make up every word in the English language. Similarly, all material things in the world are composed of different combinations of about 100 different elements. La materia
Un po' di fisica nucleare: La radioattività
 Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
CAPITOLO 20 LA CHIMICA NUCLEARE
 CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
LA FISICA DELLE RADIAZIONI IONIZZANTI
 LA FISICA DELLE RADIAZIONI IONIZZANTI MINISTERO DELL INTERNO Dipartimento dei Vigili del Fuoco, del Soccorso Pubblico e della Difesa Civile Ispettorato Nazionale del Corpo Militare della Croce Rossa Italiana
LA FISICA DELLE RADIAZIONI IONIZZANTI MINISTERO DELL INTERNO Dipartimento dei Vigili del Fuoco, del Soccorso Pubblico e della Difesa Civile Ispettorato Nazionale del Corpo Militare della Croce Rossa Italiana
LE RADIAZIONI IONIZZANTI
 LE RADIAZIONI IONIZZANTI Generalità Le radiazioni ionizzanti sono, per definizione, onde elettromagnetiche e particelle capaci di causare, direttamente o indirettamente, la ionizzazione degli atomi e delle
LE RADIAZIONI IONIZZANTI Generalità Le radiazioni ionizzanti sono, per definizione, onde elettromagnetiche e particelle capaci di causare, direttamente o indirettamente, la ionizzazione degli atomi e delle
TAVOLA DEI DEI NUCLIDI. Numero di protoni Z. Numero di neutroni N.
 TVOL DEI DEI UCLIDI umro di protoni Z www.nndc.bnl.gov umro di nutroni TVOL DEI DEI UCLIDI www.nndc.bnl.gov TVOL DEI DEI UCLIDI Con il trmin nuclid si indicano tutti gli isotopi conosciuti di lmnti chimici
TVOL DEI DEI UCLIDI umro di protoni Z www.nndc.bnl.gov umro di nutroni TVOL DEI DEI UCLIDI www.nndc.bnl.gov TVOL DEI DEI UCLIDI Con il trmin nuclid si indicano tutti gli isotopi conosciuti di lmnti chimici
INTERAZIONE RADIAZIONE MATERIA
 INTERAZIONE RADIAZIONE MATERIA Grandezze pertinenti e relative unità di misura (S.I. o pratiche) E fotone = energia di un fotone X N = numero di fotoni X Ex = N E fotone = energia trasportata da N fotoni
INTERAZIONE RADIAZIONE MATERIA Grandezze pertinenti e relative unità di misura (S.I. o pratiche) E fotone = energia di un fotone X N = numero di fotoni X Ex = N E fotone = energia trasportata da N fotoni
RADIAZIONI IONIZZANTI
 Liceo Scientifico Statale R.L. Satriani di Petilia Policastro (KR) Progetto Nazionale SeT progetto nazionale per l educazione scientifica e tecnologica - Annualità 2004 Monitoriamo l ambiente del Parco
Liceo Scientifico Statale R.L. Satriani di Petilia Policastro (KR) Progetto Nazionale SeT progetto nazionale per l educazione scientifica e tecnologica - Annualità 2004 Monitoriamo l ambiente del Parco
Chimica Nucleare. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
Esempi di esercizi per la preparazione al secondo compito di esonero
 Esempi di esercizi per la preparazione al secondo compito di esonero 1. La forza esercitata fra due cariche di segno opposto è repulsiva od attrattiva? 2. Quanto vale la forza, in modulo, esercitata fra
Esempi di esercizi per la preparazione al secondo compito di esonero 1. La forza esercitata fra due cariche di segno opposto è repulsiva od attrattiva? 2. Quanto vale la forza, in modulo, esercitata fra
Grandezze e unità di misura Dott.ssa Alessandra Bernardini
 Grandezze e unità di misura Dott.ssa Alessandra Bernardini 1 Grandezze radiometriche e coefficienti del mezzo La radiazione ionizzante che attraversa la materia perde la sua energia in processi di eccitazione
Grandezze e unità di misura Dott.ssa Alessandra Bernardini 1 Grandezze radiometriche e coefficienti del mezzo La radiazione ionizzante che attraversa la materia perde la sua energia in processi di eccitazione
Fisica atomica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
3. LA STRUTTURA DELLA MATERIA
 3. LA STRUTTURA DELLA MATERIA La struttura dell'atomo L'atomo è la più piccola parte della materia che conserva le proprietà chimiche di un elemento; è composto da un nucleo centrale, circondato da elettroni
3. LA STRUTTURA DELLA MATERIA La struttura dell'atomo L'atomo è la più piccola parte della materia che conserva le proprietà chimiche di un elemento; è composto da un nucleo centrale, circondato da elettroni
Atomo: modello microscopico
 Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Camera a Ioni. Misure di Radon. Sistema Theremino Rev.1. Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1
 Camera a Ioni Misure di Radon Sistema Theremino Rev.1 Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1 Sommario Misure con Camera a Ioni... 3 Teoria... 3 Apparecchiature... 3 Radon in abitazione -
Camera a Ioni Misure di Radon Sistema Theremino Rev.1 Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1 Sommario Misure con Camera a Ioni... 3 Teoria... 3 Apparecchiature... 3 Radon in abitazione -
LE RADIAZIONI RADIAZIONI CORPUSCOLATE RADIAZIONI ELETTROMAGNETICHE RADIAZIONI TRASPORTO DI ENERGIA ATTRAVERSO IL VUOTOE/O UN MEZZO QUALSIASI
 LE RADIAZIONI RADIAZIONI TRASPORTO DI ENERGIA ATTRAVERSO IL VUOTOE/O UN MEZZO QUALSIASI L ENERGIA PUO SPOSTARSI SIA ASSOCIATA A MATERIA SIA INDIPENDENTE DA QUESTA ENERGIA CINETICA RADIAZIONI CORPUSCOLATE
LE RADIAZIONI RADIAZIONI TRASPORTO DI ENERGIA ATTRAVERSO IL VUOTOE/O UN MEZZO QUALSIASI L ENERGIA PUO SPOSTARSI SIA ASSOCIATA A MATERIA SIA INDIPENDENTE DA QUESTA ENERGIA CINETICA RADIAZIONI CORPUSCOLATE
Radioattività e acque potabili
 Radioattività e acque potabili Silvia Arrigoni Centro Regionale di Radioprotezione (CRR) ARPA Lombardia 1 OBIETTIVO: INQUADRARE IL PROBLEMA Consideriamo le acque destinate al consumo umano vogliamo controllare
Radioattività e acque potabili Silvia Arrigoni Centro Regionale di Radioprotezione (CRR) ARPA Lombardia 1 OBIETTIVO: INQUADRARE IL PROBLEMA Consideriamo le acque destinate al consumo umano vogliamo controllare
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
LA DIFESA CIVILE NELL AMBITO DELLE EMERGENZE NUCLEARI
 LA DIFESA CIVILE NELL AMBITO DELLE EMERGENZE NUCLEARI PACE E DISARMO Sacro Convento di S. Francesco ASSISI, 7 Novembre 2014 Dott. Ing. Mauro Bergamini Dirigente Superiore Ministero dell Interno Capo Staff
LA DIFESA CIVILE NELL AMBITO DELLE EMERGENZE NUCLEARI PACE E DISARMO Sacro Convento di S. Francesco ASSISI, 7 Novembre 2014 Dott. Ing. Mauro Bergamini Dirigente Superiore Ministero dell Interno Capo Staff
RADIAZIONI ELETTROMAGNETICHE IN MEDICINA
 Laurea in LOGOPEDIA corso integrato FISICA - disciplina FISICA MEDICA RADIAZIONI ELETTROMAGNETICHE IN MEDICINA PETTRO ELETTROMAGNETICO ADIAZIONI TERMICHE: MICROONDE E INFRAROSSI ADIAZIONI IONIZZANTI: ULTRAVIOLETTI,
Laurea in LOGOPEDIA corso integrato FISICA - disciplina FISICA MEDICA RADIAZIONI ELETTROMAGNETICHE IN MEDICINA PETTRO ELETTROMAGNETICO ADIAZIONI TERMICHE: MICROONDE E INFRAROSSI ADIAZIONI IONIZZANTI: ULTRAVIOLETTI,
Preparazione di radiofarmaci PET e per terapia radionuclidica: aree critiche per l operatore
 Preparazione di radiofarmaci PET e per terapia radionuclidica: aree critiche per l operatore Marco Chianelli, MD, PhD Unità Operativa di Endocrinologia Ospedale Regina Apostolorum, Albano Roma II WORKSHOP
Preparazione di radiofarmaci PET e per terapia radionuclidica: aree critiche per l operatore Marco Chianelli, MD, PhD Unità Operativa di Endocrinologia Ospedale Regina Apostolorum, Albano Roma II WORKSHOP
Laboratorio di Chimica Generale ed Inorganica. Lezione 3. Atomi ed elementi Unità di massa atomica Mole
 Laboratorio di Chimica Generale ed Inorganica Lezione 3 Atomi ed elementi Unità di massa atomica Mole Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale
Laboratorio di Chimica Generale ed Inorganica Lezione 3 Atomi ed elementi Unità di massa atomica Mole Dott.ssa Lorenza Marvelli Dipartimento di Scienze Chimiche e Farmaceutiche Laboratorio di Chimica Generale
RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI
 RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI Elena Caldognetto Osservatorio Agenti Fisici ARPAV Verona LA RADIOATTIVITÀ NELLE ACQUE POTABILI DEL VENETO
RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI Elena Caldognetto Osservatorio Agenti Fisici ARPAV Verona LA RADIOATTIVITÀ NELLE ACQUE POTABILI DEL VENETO
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
CAPACITA DI PENETRAZIONE DELLA RADIAZIONE PERCORSO MASSIMO (RANGE) PER PARTICELLE CARICHE E SPESSORE EMIVALENTE PER FOTONI E NEUTRONI
 CAPACITA DI PENETRAZIONE DELLA RADIAZIONE NELLA MATERIA: PERCORSO MASSIMO (RANGE) PER PARTICELLE CARICHE E SPESSORE EMIVALENTE PER FOTONI E NEUTRONI Polvani pp 50-57 Particelle cariche Tessuti molli considerati
CAPACITA DI PENETRAZIONE DELLA RADIAZIONE NELLA MATERIA: PERCORSO MASSIMO (RANGE) PER PARTICELLE CARICHE E SPESSORE EMIVALENTE PER FOTONI E NEUTRONI Polvani pp 50-57 Particelle cariche Tessuti molli considerati
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
UNIVERSITÁ DEGLI STUDI DI PADOVA
 Fisica Sanitaria Interazione di raggi X con la materia (diffusione, effetto compton, fotoelettrico, produzione di coppie, fotodisintegrazione). Spessore emivalente, decivalente. Interazione delle particelle
Fisica Sanitaria Interazione di raggi X con la materia (diffusione, effetto compton, fotoelettrico, produzione di coppie, fotodisintegrazione). Spessore emivalente, decivalente. Interazione delle particelle
Esercizi. 1. Fotoni, elettroni. 2. Struttura della materia. 3. Nuclei, radioattività. 4. Produzione e consumo di energia E-X - 0
 Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
DATAZIONI PER PER LUMINESCENZA
 Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
Stima della dose annua: La dose annua è dovuta alle particelle alfa, beta, ai raggi gamma e ai raggi cosmici. Mentre il contributo delle particelle alfa è interamente dovuto ai radionuclidi delle serie
Effetti biologici delle radiazioni
 Trieste 20 Maggio 2011, Caffè San Marco Effetti biologici delle radiazioni Mara Severgnini Esperto in fisica medica e Esperto Qualificato Azienda Ospedaliero-Universitaria Ospedali Riuniti di Trieste Radiazioni
Trieste 20 Maggio 2011, Caffè San Marco Effetti biologici delle radiazioni Mara Severgnini Esperto in fisica medica e Esperto Qualificato Azienda Ospedaliero-Universitaria Ospedali Riuniti di Trieste Radiazioni
INTERAZIONE RADIAZIONE-MATERIA (Effetti biologici ed elementi di radioprotezione)
 INTERAZIONE RADIAZIONE-MATERIA (Effetti biologici ed elementi di radioprotezione) Elementi di interazione radiazione-materia - Radiazioni ionizzanti - Interazione di particelle cariche - Interazione di
INTERAZIONE RADIAZIONE-MATERIA (Effetti biologici ed elementi di radioprotezione) Elementi di interazione radiazione-materia - Radiazioni ionizzanti - Interazione di particelle cariche - Interazione di
VALUTAZIONE DEL RISCHIO DI ESPOSIZIONE A RADIAZIONI IONIZZANTI
 VALUTAZIONE DEL RISCHIO DI ESPOSIZIONE A RADIAZIONI IONIZZANTI Esperto qualificato 3 grado n 506 [email protected] Aggiornamento del 16/05/2016 GENERALITÀ SULLE RADIAZIONI IONIZZANTI Sono
VALUTAZIONE DEL RISCHIO DI ESPOSIZIONE A RADIAZIONI IONIZZANTI Esperto qualificato 3 grado n 506 [email protected] Aggiornamento del 16/05/2016 GENERALITÀ SULLE RADIAZIONI IONIZZANTI Sono
Successioni ESEMPI: Matematica con Elementi di Statistica a.a. 2014/15
 Successioni Vi sono fenomeni naturali e situazioni concrete che presentano sviluppi significativi in tempi discreti. Vale a dire è naturale che i controlli per quei dati fenomeni o per quelle date situazioni
Successioni Vi sono fenomeni naturali e situazioni concrete che presentano sviluppi significativi in tempi discreti. Vale a dire è naturale che i controlli per quei dati fenomeni o per quelle date situazioni
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
Radiazione elettromagnetica
 Radiazione elettromagnetica Si tratta di un fenomeno ondulatorio dato dalla propagazione in fase del campo elettrico e del campo magnetico, oscillanti in piani tra loro ortogonali e ortogonali alla direzione
Radiazione elettromagnetica Si tratta di un fenomeno ondulatorio dato dalla propagazione in fase del campo elettrico e del campo magnetico, oscillanti in piani tra loro ortogonali e ortogonali alla direzione
Fisica delle Radiazioni Ionizzanti. Dott. Mirco Amici Esperto Qualificato U.O.C Medicina Legale e Gestione del Rischio
 Fisica delle Radiazioni Ionizzanti Dott. Mirco Amici Esperto Qualificato U.O.C Medicina Legale e Gestione del Rischio 1 Fisica delle Radiazioni Ionizzanti Cosa sono le radiazioni ionizzanti Tipi di radiazioni
Fisica delle Radiazioni Ionizzanti Dott. Mirco Amici Esperto Qualificato U.O.C Medicina Legale e Gestione del Rischio 1 Fisica delle Radiazioni Ionizzanti Cosa sono le radiazioni ionizzanti Tipi di radiazioni
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
