Azacitidina Indicazioni terapeutiche
|
|
|
- Marcellina Molteni
- 5 anni fa
- Visualizzazioni
Transcript
1 Azacitidina Meccanismo d azione Analogo della citidina. Viene incorporata nel materiale genetico delle cellule (RNA e DNA). Agisce: modificando il modo in cui la cellula attiva e disattiva i geni interferendo con la produzione di nuovo RNA e DNA. Si pensa che tali interventi correggano i problemi di maturazione e crescita dei nuovi globuli sanguigni nel midollo osseo che causano le sindromi mielodisplastiche e che uccidono le cellule cancerose nei casi di leucemia SCHEDA TECNICA: Azacitidina Indicazioni terapeutiche Vidaza è indicato per il trattamento di pazienti adulti non eleggibili al trapianto di cellule staminali emopoietiche con: sindromi mielodisplastiche (SMD) a rischio intermedio-2 e alto secondo l International Prognostic Scoring System (IPSS) leucemia mielomonocitica cronica (LMMC) con il 10-29% di blasti midollari senza disordine mieloproliferativo leucemia mieloide acuta (LMA) con 20-30% di blasti e displasia multilineare
2 Azacitidina Appropriatezza prescrittiva Monitoraggio AIFA (Determinazione 18/10/2010) Indicazioni sottoposte a monitoraggio: Stesse indicazioni della Scheda Tecnica Condizioni negoziate: è previsto un rimborso, pari all 11% del prezzo delle confezioni di farmaco utilizzate fino al terzo ciclo di trattamento. E condizione necessaria, però, che siano state comunicate tutte le schede richiesta/dispensazione e rivalutazione relative al trattamento e che i trattamenti per i quali si intende chiedere il rimborso siano stati dichiarati conclusi tramite la scheda Fine trattamento. Gruppo Regionale Farmaci Oncologici (GReFO)
3 Azacitidina Caratteristiche chimico-farmaceutiche Azacitidina (VIDAZA 100 mg) da SCHEDA TECNICA Polvere da ricostituire con 4 ml acqua p.p.i. Somministrazione s.c. Stabilità chimico-fisica dopo ricostituzione: 22 h T. 2-8 C se la ricostituzione avviene con acqua p.p.i. refrigerata 8 h T 2-8 C con acqua p.p.i. Precauzioni: per dosi superiori a 100 mg (4 ml), dividere equamente la dose in 2 siringhe Schemi di trattamento e modalità di somministrazione Posologia e modo di somministrazione da SCHEDA TECNICA: - Dose iniziale di 75 mg/m 2, via sottocutanea, ogni giorno per 7 giorni, cui deve seguire una pausa di 21 giorni (ciclo di trattamento di 28 gg) indipendentemente dai valori basali dell emocromo Somministrazione in DH/AMB. - Dose iniziale di 75 mg/m 2, via sottocutanea, ogni giorno per 5 giorni + 2 giorni (7 gg totali ) Somministrazione OFF LABEL (sperimentale) - Dose iniziale di 50 mg/m 2, via sottocutanea, ogni giorno per 5 giorni + 5 giorni (10 gg totali ) I pz devono essere trattati per 6 cicli Reazioni avverse più comuni: ematologiche, eventi gastointestinali e reazioni in corrispondenza della sede di somministrazione.
4 2 siringhe per evitare effetti indesiderati Schemi di trattamento Totale di 93 mg = 3,72 ml
5 Informazioni per il TLB Medico responsabile della prescrizione Medico responsabile della somministrazione Firma dell infermiere responsabile della somministrazione Farmacista responsabile della conferma della terapia
6 Valutazione Costo residui produzione 337 / fiala 75 mg/mq Per pz media corporatura : 1,82 mq 136 mg/pz/die = ml 5,4 = 2 fl con scarto di 2,6 ml (219 ) 219 /die x 7 gg terapia = 1533 /pz/ciclo 21 pz nel 2011 Dati RER Azacitidina: spesa e consumi
7 Arsenico triossido Meccanismo d azione Impedisce la riproduzione di DNA necessario per la crescita delle cellule leucemiche Arsenico triossido Indicazione terapeutica SCHEDA TECNICA: L arsenico triossido è indicato per l induzione della remissione e come terapia di consolidamento in pazienti affetti da: üleucemia promielocitica acuta (LPA) recidivata o refrattaria, rara forma di leucemia causata da una traslocazione genetica (scambio di geni tra due cromosomi)
8 Arsenico triossido Caratteristiche chimico-farmaceutiche Arsenico triossido (TRISENOX 10 mg) Soluzione limpida incolore Somministrazione e.v. Stabilità chimico-fisica: 24 h a C e per 48 h a T. 2-8 C Arsenico triossido Allestimento Deve essere diluito con ml di NaCl 0,9% o di Glucosio 5% immediatamente dopo averlo aspirato dalla fiala. Il residuo di preparazione deve essere scartato. La soluzione diluita deve essere limpida ed incolore
9 Modalità di somministrazione Posologia e modo di somministrazione: -Dose iniziale di 0,15 mg/kg, via endovenosa, per la durata di due ore, prolungata ad un massimo di 4 ore se si osservano reazioni vasomotorie Deve essere somministrato 5 giorni la settimana, seguita da un intervallo di 2 giorni e ripetuta per 5 settimane Deve essere somministrato tutti i giorni, fino alla remissione del midollo osseo. Se la remissione del midollo osseo non si verifica entro il 50 giorno, la somministrazione deve essere interrotta Reazioni avverse più comuni: neutropenia, trombocitopenia, iperglicemia, parestesia, dispenea, prolungamento del tratto QT e blocco atrioventricolare completo. Costo del trattamento 426 / fiala 0,15 mg/kg Per pz peso medio: 80 Kg 12 mg/dì 2 f/dì per 5 giorni (10 fiale) per 5 settimane = 50 fiale = solo paziente nel 2011 trattato per 27 giorni La stabilità della preparazione consente di accorpare l allestimento delle terapie di 2 giorni. Quindi: per 5 giorni 8 fl/die per 5 settimane = 40 fiale = Recupero di 10 fiale per 5 gg con Risparmio/terapia di 4260
10 Nelarabina Meccanismo d azione: Fa parte del gruppo degli antimetaboliti, capace di uccidere le cellule in divisione attiva. E convertita in un analogo della guanina, una delle sostanze che formano il DNA; sostituendosi ad essa porta all inibizione della sintesi del DNA e alla morte cellulare per apoptosi. Nelarabina Farmacocinetica La Nelarabina viene convertita rapidamente ad ara- G (l analogo della guanina) ed eliminata dal plasma con un emivita di 30 minuti L emivita dell Ara-G è di 3 ore Nelarabina e Ara-G si distribuiscono in tutto il corpo senza legarsi in maniera significativa alle proteine plasmatiche.
11 Nelarabina Metabolismo e Eliminazione Principale metabolismo: NELARABINA Ara-G Demetilazione (AdenosinDeAminasi) Idrolisi Guanina Xantina Demetilazione Acido urico Eliminazione: Solo parzialmente per via renale: L escrezione urinaria media Per la Nelarabina è tra il 5-10% della dose somministrata Per l Ara G è tra il 20-30% della dose somministrata SCHEDA TECNICA: Nelarabina Indicazioni terapeutiche La Nelarabina è indicata per il trattamento di pazienti affetti da: Leucemia linfoblastica acuta a cellule T (T-ALL) Linfoma linfoblastico a cellule T (T-LBL) che non hanno risposto o hanno avuto recidive dopo trattamento con almeno due regimi di chemioterapia.
12 Nelarabina Appropriatezza prescrittiva Monitoraggio AIFA (Determinazione 19/05/2008) Indicazioni sottoposte a monitoraggio: Stesse indicazioni della Scheda Tecnica Nelarabina Caratteristiche chimico-farmaceutiche Nelarabina (ATRIANCE 250 mg) Soluzione limpida incolore Somministrazione e.v. Stabilità chimico-fisica dopo l apertura del flaconcino: 8 h, fino a 30 C
13 Modalità di somministrazione Posologia e modo di somministrazione: -Dose iniziale di 1500 mg/m 2, via endovenosa, per la durata di due ore, nei giorni 1, 3 e 5 e ripetuta ogni 21 giorni Reazioni avverse più comuni: infezioni, neutropenia, anemia, parestesia, edema. Tossicità più comuni: -neurotossicità dose limitante; -tossicità ematologica (è consigliato un monitoraggio ematocrito regolare) E somministrata senza diluizione
14 Costo del trattamento 352 / fiala 1500 mg/mq Per pz media corporatura : 1,82 mq 2700 mg/die 11 fiale a giorni alterni per 3 gg 11 fiale per 3 giorni = 33 fiale = solo paziente nel 2011 che ha fatto 2 cicli
Leucemie acute e sindromi mielodisplastiche
 Leucemie acute e sindromi mielodisplastiche Gli strumenti di governo clinico e la vigilanza da parte della Farmacia 23/02/2012 Paola Fiacchi Strumenti di governo Individuare per ogni molecola ad alto costo
Leucemie acute e sindromi mielodisplastiche Gli strumenti di governo clinico e la vigilanza da parte della Farmacia 23/02/2012 Paola Fiacchi Strumenti di governo Individuare per ogni molecola ad alto costo
Allegato B al Decreto n. 48 del 17 maggio 2016 pag. 1/6
 giunta regionale Allegato B al Decreto n. 48 del 17 maggio 2016 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI SOGGETTI A REGISTRO AIFA E DEI RELATIVI CENTRI AUTORIZZATI ALLA PRESCRIZIONE NOME FARMACO PRINCIPIO
giunta regionale Allegato B al Decreto n. 48 del 17 maggio 2016 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI SOGGETTI A REGISTRO AIFA E DEI RELATIVI CENTRI AUTORIZZATI ALLA PRESCRIZIONE NOME FARMACO PRINCIPIO
Allegato B al Decreto n. 65 del 7 giugno 2017 pag. 1/6
 giunta regionale Allegato B al Decreto n. 65 del 7 giugno 2017 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Indicazione Per il trattamento di pazienti adulti
giunta regionale Allegato B al Decreto n. 65 del 7 giugno 2017 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Indicazione Per il trattamento di pazienti adulti
Allegato A al Decreto n. 107 del 8 agosto 2017 pag. 1/6
 giunta regionale Allegato A al Decreto n. 107 del 8 agosto 2017 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Atriance (Nelarabina) Arzerra (Ofatumumab) Arzerra
giunta regionale Allegato A al Decreto n. 107 del 8 agosto 2017 pag. 1/6 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Atriance (Nelarabina) Arzerra (Ofatumumab) Arzerra
Allegato A al Decreto n. 14 del 2 FEB pag. 1/7
 giunta regionale Allegato A al Decreto n. 14 del 2 FEB. 2018 pag. 1/7 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Atriance (Nelarabina) Arzerra (Ofatumumab) Arzerra
giunta regionale Allegato A al Decreto n. 14 del 2 FEB. 2018 pag. 1/7 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Adcetris (Brentuximab vedotin) Atriance (Nelarabina) Arzerra (Ofatumumab) Arzerra
Allegato A al Decreto n. 82 del 9 luglio 2018 pag. 1/8
 giunta regionale Allegato A al Decreto n. 82 del 9 luglio 2018 pag. 1/8 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Indicazione Centri autorizzati (con decreti Direttore Generale Area Sanità e Sociale)
giunta regionale Allegato A al Decreto n. 82 del 9 luglio 2018 pag. 1/8 ELENCO FARMACI ONCO-EMATOLOGICI* PRINCIPIO ATTIVO Indicazione Centri autorizzati (con decreti Direttore Generale Area Sanità e Sociale)
Allegato A al Decreto n. 48 del 17 maggio 2016 pag. 1/3
 giunta regionale Allegato A al Decreto n. 48 del 17 maggio 2016 pag. 1/3 INDIVIDUAZIONE DELLA RETE DEI CENTRI PRESCRITTORI DI FARMACI ONCOEMATOLOGICI SOGGETTI A REGISTRO AIFA L area oncoematologica rappresenta
giunta regionale Allegato A al Decreto n. 48 del 17 maggio 2016 pag. 1/3 INDIVIDUAZIONE DELLA RETE DEI CENTRI PRESCRITTORI DI FARMACI ONCOEMATOLOGICI SOGGETTI A REGISTRO AIFA L area oncoematologica rappresenta
I DOCUMENTI DI HEALTH INDUSTRY REGIONE VENETO. Decreto n 48 del 17 maggio 2016
 I DOCUMENTI DI HEALTH INDUSTRY REGIONE VENETO Decreto n 48 del 17 maggio 2016 Attivazione ed individuazione della rete dei Centri Regionali autorizzati alla prescrizione di farmaci soggetti a Registro
I DOCUMENTI DI HEALTH INDUSTRY REGIONE VENETO Decreto n 48 del 17 maggio 2016 Attivazione ed individuazione della rete dei Centri Regionali autorizzati alla prescrizione di farmaci soggetti a Registro
31/10/2014. La centralizzazione al S. Orsola-Malpighi di Bologna. Esigenza di Informatizzazione
 La centralizzazione al S. Orsola-Malpighi di Bologna 4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna, 02 ottobre
La centralizzazione al S. Orsola-Malpighi di Bologna 4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna, 02 ottobre
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO
 EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
SINTESI DEL PROTOCOLLO
 SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
I costi aggiuntivi del confezionamento non ottimale dei farmaci oncologici
 LE DIVERSE FACCE DELL'APPROPRIATEZZA PRESCRITTIVA ISS Roma, 14 luglio 2016 I costi aggiuntivi del confezionamento non ottimale dei farmaci oncologici Annalisa Campomori UO Farmacia ospedaliera di Trento
LE DIVERSE FACCE DELL'APPROPRIATEZZA PRESCRITTIVA ISS Roma, 14 luglio 2016 I costi aggiuntivi del confezionamento non ottimale dei farmaci oncologici Annalisa Campomori UO Farmacia ospedaliera di Trento
La Rete Regionale delle Farmacie Oncologiche: stato dell arte e work in progress
 La Rete Regionale delle Farmacie Oncologiche: stato dell arte e work in progress Daniela Carati Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali III corso regionale Bologna 22
La Rete Regionale delle Farmacie Oncologiche: stato dell arte e work in progress Daniela Carati Servizio Politica del Farmaco Direzione Generale Sanità e Politiche Sociali III corso regionale Bologna 22
DETERMINAZIONE 24 novembre Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009).
 DETERMINAZIONE 24 novembre 2009. Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009). Regime di rimborsabilità e prezzo di vendita della specialità
DETERMINAZIONE 24 novembre 2009. Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009). Regime di rimborsabilità e prezzo di vendita della specialità
Allegato A al Decreto n. 65 del 7 giugno 2017 pag. 1/3
 giunta regionale Allegato A al Decreto n. 65 del 7 giugno 2017 pag. 1/3 INDIVIDUAZIONE DELLA RETE DEI CENTRI PRESCRITTORI DI FARMACI ONCOEMATOLOGICI L area oncoematologica rappresenta uno dei settori nei
giunta regionale Allegato A al Decreto n. 65 del 7 giugno 2017 pag. 1/3 INDIVIDUAZIONE DELLA RETE DEI CENTRI PRESCRITTORI DI FARMACI ONCOEMATOLOGICI L area oncoematologica rappresenta uno dei settori nei
Sindromi Mieloproliferative
 Sindromi Mieloproliferative Sindr. Mieloproliferative croniche Sindr. Mieloprolifer. Sub-acute o Mielodisplasie Sindr. Mieloproliferative Acute o Leucemie Acute Mieloidi SINDROME MIELODISPLASTICA Patologia
Sindromi Mieloproliferative Sindr. Mieloproliferative croniche Sindr. Mieloprolifer. Sub-acute o Mielodisplasie Sindr. Mieloproliferative Acute o Leucemie Acute Mieloidi SINDROME MIELODISPLASTICA Patologia
Mieloma Multiplo. Trattamento del Mieloma Multiplo SCHEDA 12/28/2016 TERAPIA DI PRIMA LINEA IN PAZIENTI CANDIDABILE A TRAPIANTO AUTOLOGO
 TERAPIA DI PRIMA LINEA IN PAZIENTI CANDIDABILE A TRAPIANTO AUTOLOGO 1 di 6 INDUZIONE STANDARD : VTD 4/6 cicli (In label, 648, monitorato AIFA per Talidomide schema Rosinol) Velcade 1.3 mg/mq SC gg 1, 4,
TERAPIA DI PRIMA LINEA IN PAZIENTI CANDIDABILE A TRAPIANTO AUTOLOGO 1 di 6 INDUZIONE STANDARD : VTD 4/6 cicli (In label, 648, monitorato AIFA per Talidomide schema Rosinol) Velcade 1.3 mg/mq SC gg 1, 4,
INTEGRAZIONE MEDICO-INFERMIERE NELLA GESTIONE DELLA TERAPIA AMBULATORIALE o di DAY HOSPITAL IL RUOLO INFERMIERISTICO NELLA GESTIONE DELLE TOSSICITA'
 1 INTEGRAZIONE MEDICO-INFERMIERE NELLA GESTIONE DELLA TERAPIA AMBULATORIALE o di DAY HOSPITAL IL RUOLO INFERMIERISTICO NELLA GESTIONE DELLE TOSSICITA' Montanaro Vincenza, Boetto Daniela, Ponticelli Elena
1 INTEGRAZIONE MEDICO-INFERMIERE NELLA GESTIONE DELLA TERAPIA AMBULATORIALE o di DAY HOSPITAL IL RUOLO INFERMIERISTICO NELLA GESTIONE DELLE TOSSICITA' Montanaro Vincenza, Boetto Daniela, Ponticelli Elena
Le leucemie acute mieloidi La diagnosi
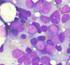 LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Il flacone contiene: Principio attivo:
REGIONE EMILIA-ROMAGNA Atti amministrativi
 REGIONE EMILIA-ROMAGNA Atti amministrativi GIUNTA REGIONALE Atto del Dirigente a firma unica: DETERMINAZIONE n 3314 del 15/03/2012 Proposta: DPG/2012/3962 del 14/03/2012 Struttura proponente: Oggetto:
REGIONE EMILIA-ROMAGNA Atti amministrativi GIUNTA REGIONALE Atto del Dirigente a firma unica: DETERMINAZIONE n 3314 del 15/03/2012 Proposta: DPG/2012/3962 del 14/03/2012 Struttura proponente: Oggetto:
Nel caso del mieoloma multiplo, un tumore che colpisce un tipo di globuli bianchi detti cellule plasmatiche, Revlimid è usato:
 EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Abseamed (epoetina alfa)
 EMA/552931/2018 EMEA/H/C/000727 Sintesi di Abseamed e perché è autorizzato nell Unione europea (UE) Cos è Abseamed e per cosa si usa? Abseamed è un medicinale usato nei seguenti casi: per trattare l anemia
EMA/552931/2018 EMEA/H/C/000727 Sintesi di Abseamed e perché è autorizzato nell Unione europea (UE) Cos è Abseamed e per cosa si usa? Abseamed è un medicinale usato nei seguenti casi: per trattare l anemia
RIASSUNTO DEL PROTOCOLLO DI SPERIMENTAZIONE CLINICA per la richiesta di parere al Comitato Etico dell Istituto Scientifico H.
 pag 1 di 6 Valutazione della tossicità e dell efficacia del treosulfano in combinazione con citarabina e fludarabina come condizionamento pre-autotrapianto di cellule staminali ematopoietiche, nei pazienti
pag 1 di 6 Valutazione della tossicità e dell efficacia del treosulfano in combinazione con citarabina e fludarabina come condizionamento pre-autotrapianto di cellule staminali ematopoietiche, nei pazienti
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI
 STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
REAZIONI AVVERSE EMATOLOGICHE
 REAZIONI AVVERSE EMATOLOGICHE DISTRIBUZIONE DELLE ADR PER SYSTEM ORGAN CLASSES (SOCs) NEL 2016 OsservatOriO NaziONale sull impiego dei medicinali L uso dei Farmaci in Italia - Rapporto Nazionale 2016
REAZIONI AVVERSE EMATOLOGICHE DISTRIBUZIONE DELLE ADR PER SYSTEM ORGAN CLASSES (SOCs) NEL 2016 OsservatOriO NaziONale sull impiego dei medicinali L uso dei Farmaci in Italia - Rapporto Nazionale 2016
Leucemia Mieloide Acuta (LMA)
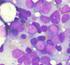 Leucemia Mieloide Acuta (LMA) Il termine di leucemia mieloide acuta (LMA) identifica un gruppo eterogeneo di neoplasie ematologiche con caratteristiche biologiche e cliniche peculiari tali da comportare
Leucemia Mieloide Acuta (LMA) Il termine di leucemia mieloide acuta (LMA) identifica un gruppo eterogeneo di neoplasie ematologiche con caratteristiche biologiche e cliniche peculiari tali da comportare
U.O. Emato-oncologia Pediatrica, I.R.C.S.S Burlo Garofolo, Trieste Dr. Marco RABUSIN
 TITOLO Studio prospettico IRCSS Burlo Garofolo di Trieste S V I L U P P O D I S T R AT E G I E FA R M A C O L O G I C H E P E R L A PERSONALIZZAZIONE DEL TRATTAMENTO DELLA LEUCEMIA LINFOBLASTICA ACUTA
TITOLO Studio prospettico IRCSS Burlo Garofolo di Trieste S V I L U P P O D I S T R AT E G I E FA R M A C O L O G I C H E P E R L A PERSONALIZZAZIONE DEL TRATTAMENTO DELLA LEUCEMIA LINFOBLASTICA ACUTA
Trapianto. Stefano Guidi TMO. AOU Careggi. Firenze. Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche
 Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Aprile 2016 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Trapianto
Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Aprile 2016 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Trapianto
PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO. REVISIONE SCHEDA DI TRATTAMENTO Introduzione nuovi farmaci anno 2017
 PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO REVISIONE SCHEDA DI TRATTAMENTO Introduzione nuovi farmaci anno 2017 A cura del Gruppo di Studio sul Mieloma Multiplo: Coordinatori:
PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO REVISIONE SCHEDA DI TRATTAMENTO Introduzione nuovi farmaci anno 2017 A cura del Gruppo di Studio sul Mieloma Multiplo: Coordinatori:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE CLODRONATO ABC 100 mg/3,3 ml soluzione iniettabile CLODRONATO ABC 300 mg/10 ml soluzione per infusione endovenosa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE CLODRONATO ABC 100 mg/3,3 ml soluzione iniettabile CLODRONATO ABC 300 mg/10 ml soluzione per infusione endovenosa
REPORT HTA REGIONALE. Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO
 REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
DETERMINAZIONE DEL DIRIGENTE SEZIONE PRO GRAMMAZIONE ASSISTENZA TERRITORIALE E PRE VENZIONE 11 novembre 2015, n. 399
 49873 DETERMINAZIONE DEL DIRIGENTE SEZIONE PRO GRAMMAZIONE ASSISTENZA TERRITORIALE E PRE VENZIONE 11 novembre 2015, n. 399 Ricognizione centri regionali autorizzati alla utilizzazione e prescrizione delle
49873 DETERMINAZIONE DEL DIRIGENTE SEZIONE PRO GRAMMAZIONE ASSISTENZA TERRITORIALE E PRE VENZIONE 11 novembre 2015, n. 399 Ricognizione centri regionali autorizzati alla utilizzazione e prescrizione delle
PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO REVISIONE SCHEDA DI TRATTAMENTO
 PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO REVISIONE SCHEDA DI TRATTAMENTO A cura del Gruppo di Studio sul Mieloma Multiplo: Coordinatori: Mario Boccadoro, Sara Bringhen, Marinella
PERCORSO DIAGNOSTICO-TERAPEUTICO PER IL PAZIENTE CON MIELOMA MULTIPLO REVISIONE SCHEDA DI TRATTAMENTO A cura del Gruppo di Studio sul Mieloma Multiplo: Coordinatori: Mario Boccadoro, Sara Bringhen, Marinella
Registri AIFA: strumento di gestione Dott.ssa Stefania Esposito U.O.C. Farmacia A.O.U. Mater Domini-Catanzaro
 IL VALORE DELL'INNOVAZIONE: DALLA VALUTAZIONE ALLA GESTIONE DELLE CRITICITA' Catanzaro, 20 giugno 2017 Registri AIFA: strumento di gestione Dott.ssa Stefania Esposito U.O.C. Farmacia A.O.U. Mater Domini-Catanzaro
IL VALORE DELL'INNOVAZIONE: DALLA VALUTAZIONE ALLA GESTIONE DELLE CRITICITA' Catanzaro, 20 giugno 2017 Registri AIFA: strumento di gestione Dott.ssa Stefania Esposito U.O.C. Farmacia A.O.U. Mater Domini-Catanzaro
CA DEL COLON RETTO E CASI CLINICI. Gli strumenti di governo clinico e la vigilanza da parte della farmacia ottobre 2010 Bologna
 2 corso regionale per farmacisti, tecnici e infermieri dell area oncologica. Schemi terapeutici in oncologia : prescrizione, allestimento e somministrazione CA DEL COLON RETTO E CASI CLINICI Gli strumenti
2 corso regionale per farmacisti, tecnici e infermieri dell area oncologica. Schemi terapeutici in oncologia : prescrizione, allestimento e somministrazione CA DEL COLON RETTO E CASI CLINICI Gli strumenti
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE EPARGRISEOVIT adulti soluzione iniettabile EPARGRISEOVIT bambini soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE EPARGRISEOVIT adulti soluzione iniettabile EPARGRISEOVIT bambini soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
INTRODUZIONE E CONTESTO CLINICO DI UTILIZZO APPROPRIATO
 INTRODUZIONE E CONTESTO CLINICO DI UTILIZZO APPROPRIATO Gli effetti anticoagulanti di Pradaxa sono importanti e salvavita per alcuni pazienti, ma ci sono situazioni in cui e necessario inattivare rapidamente
INTRODUZIONE E CONTESTO CLINICO DI UTILIZZO APPROPRIATO Gli effetti anticoagulanti di Pradaxa sono importanti e salvavita per alcuni pazienti, ma ci sono situazioni in cui e necessario inattivare rapidamente
Dose: 2-5 mg/kg a bolo in 20/30 minuti; successivamente 0,7-1 mg/kg in infusione continua
 CASO 1 Un bambino di 3 anni (14 kg) giunge in Pronto Soccorso, accompagnato dai genitori per difficoltà respiratoria. In Triage vengono rilevati i seguenti parametri vitali: Spo2 in aria ambiente 89%,
CASO 1 Un bambino di 3 anni (14 kg) giunge in Pronto Soccorso, accompagnato dai genitori per difficoltà respiratoria. In Triage vengono rilevati i seguenti parametri vitali: Spo2 in aria ambiente 89%,
Sviluppo di un modulo informatico ad hoc per la gestione dei farmaci in pediatria
 4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELLᾼAREA ONCOLOGICA SCHEMI TERAPEUTICI IN ONCO -EMATOLOGIA PEDIATRICA: PRESCRIZIONE, ALLESTIMENTO E SOMMINISTRAZIONE 02 ottobre 204 Sviluppo di un
4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELLᾼAREA ONCOLOGICA SCHEMI TERAPEUTICI IN ONCO -EMATOLOGIA PEDIATRICA: PRESCRIZIONE, ALLESTIMENTO E SOMMINISTRAZIONE 02 ottobre 204 Sviluppo di un
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Fasturtec 1,5 mg/ml polvere e solvente per concentrato per soluzione per infusione.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fasturtec 1,5 mg/ml polvere e solvente per concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Fasturtec 1,5 mg/ml polvere e solvente per concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
Lenalidomide nelle SMD. Do# Roberto Latagliata Ematologia Policlinico Umberto I
 Lenalidomide nelle SMD Do# Roberto Latagliata Ematologia Policlinico Umberto I Neoplasie di origine mieloide: uno scenario in evoluzione Firenze 23 24 novembre 2016 LENALIDOMIDE: FORMULA CHIMICA Talidomide
Lenalidomide nelle SMD Do# Roberto Latagliata Ematologia Policlinico Umberto I Neoplasie di origine mieloide: uno scenario in evoluzione Firenze 23 24 novembre 2016 LENALIDOMIDE: FORMULA CHIMICA Talidomide
Possibilità terapeutiche attuali nelle sindromi mielodisplastiche
 Possibilità terapeutiche attuali nelle sindromi mielodisplastiche Luca Malcovati, Professore Associato di Ematologia, Dipartimento di Ematologia e Oncologia, Fondazione IRCCS Policlinico San Matteo & Dipartimento
Possibilità terapeutiche attuali nelle sindromi mielodisplastiche Luca Malcovati, Professore Associato di Ematologia, Dipartimento di Ematologia e Oncologia, Fondazione IRCCS Policlinico San Matteo & Dipartimento
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino di polvere contiene:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE GLUTATIONE GERMED 600 mg/4 ml polvere e solvente 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino di polvere contiene:
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 6 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 6 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Per informazioni pratiche sull uso di Revlimid i pazienti devono leggere il foglio illustrativo oppure consultare il medico o il farmacista.
 EMA/113870/2017 EMEA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui l Agenzia ha valutato
EMA/113870/2017 EMEA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui l Agenzia ha valutato
Caso clinico. Benedetta Puccini AOU Careggi Ematologia
 Caso clinico Benedetta Puccini AOU Careggi Ematologia Introduzione Uomo di 63 anni, 1 fratello di 55 anni A.Fisiologica:, non ha figli, non fuma. Da dicembre 2012 comparsa di dolore addominale e febbre
Caso clinico Benedetta Puccini AOU Careggi Ematologia Introduzione Uomo di 63 anni, 1 fratello di 55 anni A.Fisiologica:, non ha figli, non fuma. Da dicembre 2012 comparsa di dolore addominale e febbre
Corso di Tecniche diagnostiche in ematologia
 Corso di Tecniche diagnostiche in ematologia Struttura e funzione del sistema emopoietico Inquadramento fisiopatologico Tecniche di studio, cliniche e sperimentali Trapianto di cellule staminali Principali
Corso di Tecniche diagnostiche in ematologia Struttura e funzione del sistema emopoietico Inquadramento fisiopatologico Tecniche di studio, cliniche e sperimentali Trapianto di cellule staminali Principali
LEUCEMIE DEFINIZIONE PROLIFERAZIONE CLONALE E INCONTROLLATA DI CELLULE EMOPOIETICHE IMMATURE
 LEUCEMIE DEFINIZIONE PROLIFERAZIONE CLONALE E INCONTROLLATA DI CELLULE EMOPOIETICHE IMMATURE LEUCEMIE CLASSIFICAZIONE MIELOIDE Acuta Cronica LINFOIDE Acuta Cronica LEUCEMIE MIELOIDI ACUTE DEFINIZIONE GRUPPO
LEUCEMIE DEFINIZIONE PROLIFERAZIONE CLONALE E INCONTROLLATA DI CELLULE EMOPOIETICHE IMMATURE LEUCEMIE CLASSIFICAZIONE MIELOIDE Acuta Cronica LINFOIDE Acuta Cronica LEUCEMIE MIELOIDI ACUTE DEFINIZIONE GRUPPO
Legnano, 28 Novembre Gruppo infermieristico U.O. Malattie Infettive A.O. Legnano
 Legnano, 28 Novembre 2013 Gruppo infermieristico U.O. Malattie Infettive A.O. Legnano IL RUOLO DELL INFERMIERE NELLA CORRETTA GESTIONE DELLA TERAPIA ANTIBIOTICA L infermiere garantisce la corretta applicazione
Legnano, 28 Novembre 2013 Gruppo infermieristico U.O. Malattie Infettive A.O. Legnano IL RUOLO DELL INFERMIERE NELLA CORRETTA GESTIONE DELLA TERAPIA ANTIBIOTICA L infermiere garantisce la corretta applicazione
4.2 Indicazioni per l utilizzazione specificando le specie di destinazione
 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Melovem 5 mg/ml soluzione iniettabile per bovini e suini 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml contiene: Principio attivo: Meloxicam 5 mg Eccipiente(i):
1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Melovem 5 mg/ml soluzione iniettabile per bovini e suini 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni ml contiene: Principio attivo: Meloxicam 5 mg Eccipiente(i):
Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase
 Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase ELAPRASE (idursulfasi) Terapia enzimatica sostitutiva per il trattamento a lungo termine dei pazienti
Linee guida per il dosaggio e l infusione Informazioni sulla preparazione e somministrazione di Elaprase ELAPRASE (idursulfasi) Terapia enzimatica sostitutiva per il trattamento a lungo termine dei pazienti
LA LEUCEMIA MIELOIDE CRONICA
 LA LEUCEMIA MIELOIDE CRONICA Opuscolo informativo Anno 2014 1 Leucemia Mieloide Cronica (LMC) La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica che colpisce le cellule staminali emopoietica,
LA LEUCEMIA MIELOIDE CRONICA Opuscolo informativo Anno 2014 1 Leucemia Mieloide Cronica (LMC) La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica che colpisce le cellule staminali emopoietica,
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR DASATINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE06 (SPRYCEL ) Presentata da COMMISSIONE PRONTUARIO TERAPEUTICO PROVINCIA SASSARI In data gennaio 2008 Per le seguenti motivazioni (sintesi): Dasatinib è un inibitore
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE06 (SPRYCEL ) Presentata da COMMISSIONE PRONTUARIO TERAPEUTICO PROVINCIA SASSARI In data gennaio 2008 Per le seguenti motivazioni (sintesi): Dasatinib è un inibitore
IL VALORE DELL'INNOVAZIONE: DALLA VALUTAZIONE ALLA GESTIONE DELLE CRITICITA' Catanzaro, 20 giugno 2017
 IL VALORE DELL'INNOVAZIONE: DALLA VALUTAZIONE ALLA GESTIONE DELLE CRITICITA' Catanzaro, 20 giugno 2017 Gestione delle terapie personalizzate in una Unità Farmaci Antiblastici Carmela Oriolo Gestione del
IL VALORE DELL'INNOVAZIONE: DALLA VALUTAZIONE ALLA GESTIONE DELLE CRITICITA' Catanzaro, 20 giugno 2017 Gestione delle terapie personalizzate in una Unità Farmaci Antiblastici Carmela Oriolo Gestione del
LEUCEMIE MIELOIDI CRONICHE
 LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
APPROPRIATEZZA PRESCRITTIVA IN OSPEDALE REV. 1 Pag. 1 / 5 SOLUZIONI CONCENTRATE DI POTASSIO
 OSPEDALE REV. 1 Pag. 1 / 5 Stato delle Modifiche Rev. Data Causale 0 14/05/2011 Prima emissione 1) PREMESSA: - Il Ministero della Salute ha emanato una raccomandazione sul corretto utilizzo delle soluzioni
OSPEDALE REV. 1 Pag. 1 / 5 Stato delle Modifiche Rev. Data Causale 0 14/05/2011 Prima emissione 1) PREMESSA: - Il Ministero della Salute ha emanato una raccomandazione sul corretto utilizzo delle soluzioni
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vidaza 25 mg/ml polvere per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vidaza 25 mg/ml polvere per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
Terapia malattie infiammatorie croniche intestinali. IBD: rettocolite ulcerosa e morbo di Crohn
 Terapia malattie infiammatorie croniche intestinali IBD: rettocolite ulcerosa e morbo di Crohn Prevalenza EU e USA 1-2 per 1000 Sintomi: diarrea, dolore addominale, anemia, perdita di peso. Crohn: patologia
Terapia malattie infiammatorie croniche intestinali IBD: rettocolite ulcerosa e morbo di Crohn Prevalenza EU e USA 1-2 per 1000 Sintomi: diarrea, dolore addominale, anemia, perdita di peso. Crohn: patologia
Assemblaggio e controllo informatico della terapia
 Assemblaggio e controllo informatico della terapia DISTRIBUZIONE DISTRIBUZIONE Somministrazione Sequenza di controllo in somministrazione Identificazione infermiere Identificazione paziente Identificazione
Assemblaggio e controllo informatico della terapia DISTRIBUZIONE DISTRIBUZIONE Somministrazione Sequenza di controllo in somministrazione Identificazione infermiere Identificazione paziente Identificazione
SINOSSI. EudraCT number Versione del protocollo Version Octobre 2013
 SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
IL PROCESSO DELLA LOGISTICA FARMACEUTICA, PROSPETTIVE E SFIDE PER IL FARMACISTA SSN TORINO, MARZO 2014
 IL PROCESSO DELLA LOGISTICA FARMACEUTICA, PROSPETTIVE E SFIDE PER IL FARMACISTA SSN TORINO, 13-14 MARZO 2014 3 farmacisti 14 infermieri 1 caposala 1os PROSPETTIVE E SFIDE PER IL FARMACISTA SSN QUALCHE
IL PROCESSO DELLA LOGISTICA FARMACEUTICA, PROSPETTIVE E SFIDE PER IL FARMACISTA SSN TORINO, 13-14 MARZO 2014 3 farmacisti 14 infermieri 1 caposala 1os PROSPETTIVE E SFIDE PER IL FARMACISTA SSN QUALCHE
Utilizzo dei markers ematologici nella pratica della registrazione
 XVIII Corso di aggiornamento per operatori dei Registri Tumori Monopoli, 3-5 ottobre 2018 Utilizzo dei markers ematologici nella pratica della registrazione Francesca Roncaglia Registro Tumori Reggio Emilia
XVIII Corso di aggiornamento per operatori dei Registri Tumori Monopoli, 3-5 ottobre 2018 Utilizzo dei markers ematologici nella pratica della registrazione Francesca Roncaglia Registro Tumori Reggio Emilia
120518_V11.0_Vidaza_EU_PI_IT ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vidaza 25 mg/ml polvere per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Vidaza 25 mg/ml polvere per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni flaconcino
AGENZIA ITALIANA DEL FARMACO
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 14 novembre 2011 Inserimento del medicinale «Atgam» (siero antilinfocitario di cavallo) nell'elenco dei medicinali erogabili a totale carico del Servizio sanitario
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 14 novembre 2011 Inserimento del medicinale «Atgam» (siero antilinfocitario di cavallo) nell'elenco dei medicinali erogabili a totale carico del Servizio sanitario
PERCORSO DIAGNOSTICO TERAPEUTICO PER LE SINDROMI MIELODISPLASTICHE
 PERCORSO DIAGNOSTICO TERAPEUTICO PER LE SINDROMI MIELODISPLASTICHE PDT 033.1 Protocollo Rev 1 del 13/07/2010 1/10 1. BACKGROUND E RAZIONALE Le interessano prevalentemente persone anziane e presentano una
PERCORSO DIAGNOSTICO TERAPEUTICO PER LE SINDROMI MIELODISPLASTICHE PDT 033.1 Protocollo Rev 1 del 13/07/2010 1/10 1. BACKGROUND E RAZIONALE Le interessano prevalentemente persone anziane e presentano una
APPROFONDIMENTI SUI MODELLI ORGANIZZATIVI GESTIONALI. IL PUNTO DI VISTA DEL FARMACISTA.
 APPROFONDIMENTI SUI MODELLI ORGANIZZATIVI GESTIONALI. IL PUNTO DI VISTA DEL FARMACISTA. Sabrina Beltramini U.O.S GESTIONE DEL FARMACO E INNOVAZIONE TECNOLOGICA U.O. FARMACIA IRCCS Azienda Ospedaliera Universitaria
APPROFONDIMENTI SUI MODELLI ORGANIZZATIVI GESTIONALI. IL PUNTO DI VISTA DEL FARMACISTA. Sabrina Beltramini U.O.S GESTIONE DEL FARMACO E INNOVAZIONE TECNOLOGICA U.O. FARMACIA IRCCS Azienda Ospedaliera Universitaria
VEDOLIZUMAB PIONIERE DI UNA NUOVA CLASSE
 Le Malattie infiammatorie croniche intestinali (MICI) Tra appropriatezza e sostenibilità VEDOLIZUMAB PIONIERE DI UNA NUOVA CLASSE Dr.ssa Mariangela Mercaldo UOC Controllo Interno di Gestione ASL Caserta
Le Malattie infiammatorie croniche intestinali (MICI) Tra appropriatezza e sostenibilità VEDOLIZUMAB PIONIERE DI UNA NUOVA CLASSE Dr.ssa Mariangela Mercaldo UOC Controllo Interno di Gestione ASL Caserta
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE TRISENOX 1 mg/ml, concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di TRISENOX
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE TRISENOX 1 mg/ml, concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di TRISENOX
IRON DEFICENCY. Luciano Arcari - ROMA. Roma, 23 settembre 2017
 IRON DEFICENCY L importanza della correzione del deficit di ferro: esperienza nella gestione ambulatoriale del paziente con insufficienza cardiaca cronica Roma, 23 settembre 2017 Luciano Arcari - ROMA
IRON DEFICENCY L importanza della correzione del deficit di ferro: esperienza nella gestione ambulatoriale del paziente con insufficienza cardiaca cronica Roma, 23 settembre 2017 Luciano Arcari - ROMA
SCHEDA FARMACO. Principio attivo (nome commerciale) Ponatinib. (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Ponatinib SCHEDA FARMACO (Iclusig) 30 cpr da 45 mg 60cpr da 15 mg Posologia: La dose
LE SINDROMI MIELODISPLASTICHE. Sono disordini acquisiti clonali delle cellule staminali emopoietiche
 LE SINDROMI MIELODISPLASTICHE Sono disordini acquisiti clonali delle cellule staminali emopoietiche EMOPOIESI INEFFICACE (midollo ipercellulare) ANEMIA e/o NEUTROPENIA e/o PIASTRINOPENIA EVOLUZIONE IN
LE SINDROMI MIELODISPLASTICHE Sono disordini acquisiti clonali delle cellule staminali emopoietiche EMOPOIESI INEFFICACE (midollo ipercellulare) ANEMIA e/o NEUTROPENIA e/o PIASTRINOPENIA EVOLUZIONE IN
Cardiotossicità da farmaci antiemetici
 PROGETTO SPECIALE CARDIO-ONCOLOGIA 2013-2015 AIOM ANMCO AICO ICOS Cardiotossicità da farmaci antiemetici Sandro Barni, Fausto Petrelli, Mary Cabiddu L'intervallo QT esprime il tempo necessario al miocardio
PROGETTO SPECIALE CARDIO-ONCOLOGIA 2013-2015 AIOM ANMCO AICO ICOS Cardiotossicità da farmaci antiemetici Sandro Barni, Fausto Petrelli, Mary Cabiddu L'intervallo QT esprime il tempo necessario al miocardio
LEUCEMIE SONO TUMORI MALIGNI DEL SISTEMA EMOLINFOPOIETICO. ORIGINANO DA CELLULE STAMINALI
 LEUCEMIE SONO TUMORI MALIGNI DEL SISTEMA EMOLINFOPOIETICO. ORIGINANO DA CELLULE STAMINALI. SONO DETERMINATE DA ALMENO UNA (SPESSO PIU DI UNA) ALTERAZIONE GENICA CHE GENERA UN CLONE DI CELLULE LEUCEMICHE.
LEUCEMIE SONO TUMORI MALIGNI DEL SISTEMA EMOLINFOPOIETICO. ORIGINANO DA CELLULE STAMINALI. SONO DETERMINATE DA ALMENO UNA (SPESSO PIU DI UNA) ALTERAZIONE GENICA CHE GENERA UN CLONE DI CELLULE LEUCEMICHE.
«CORSO SIFO UNDER 40. AGGIORNAMENTO PROFESSIONALE PER IL FARMACISTA»
 «CORSO SIFO UNDER 40. AGGIORNAMENTO PROFESSIONALE PER IL FARMACISTA» IN MEMORIA DI STEFANO FEDERICI Milano, 7 giugno 18 ottobre 2017 I registri di Monitoraggio AIFA Innovazione e registri di monitoraggio
«CORSO SIFO UNDER 40. AGGIORNAMENTO PROFESSIONALE PER IL FARMACISTA» IN MEMORIA DI STEFANO FEDERICI Milano, 7 giugno 18 ottobre 2017 I registri di Monitoraggio AIFA Innovazione e registri di monitoraggio
Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito. Dott. Mattia Luciano
 Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito Dott. Mattia Luciano CALCOLO PER I DOSAGGI FARMACOLOGICI I calcoli per la somministrazione possono riguardare: Ricostituzione
Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito Dott. Mattia Luciano CALCOLO PER I DOSAGGI FARMACOLOGICI I calcoli per la somministrazione possono riguardare: Ricostituzione
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione
 Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Gestione infermieristica dei nuovi farmaci biologici nelle pazienti con carcinoma mammario: modalità di somministrazione Beniamino Micheloni U.O.C. Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar
Alla U. O.C. FARMACIA OSPEDALIERA
 Richiesta motivata per singolo paziente per farmaci inseriti in PTO con limitazioni d uso ( da allegare alla modulistica ordinaria ) sesso M F età... FARMACO :... ( Denominazione / Forma farmaceutica /
Richiesta motivata per singolo paziente per farmaci inseriti in PTO con limitazioni d uso ( da allegare alla modulistica ordinaria ) sesso M F età... FARMACO :... ( Denominazione / Forma farmaceutica /
PROCEDURA PER L'USO CORRETTO DEI FARMACI AD ALTO RISCHIO NELL'ASSISTENZA OSPEDALIERA
 PROCEDURA PER L'USO CORRETTO DEI FARMACI AD ALTO RISCHIO NELL'ASSISTENZA OSPEDALIERA UCO di Chirurgia Generale di Trieste direttore: prof. N. de Manzini "Progetto finanziato nell'ambito del Programma per
PROCEDURA PER L'USO CORRETTO DEI FARMACI AD ALTO RISCHIO NELL'ASSISTENZA OSPEDALIERA UCO di Chirurgia Generale di Trieste direttore: prof. N. de Manzini "Progetto finanziato nell'ambito del Programma per
La Farmacogenetica studia:
 La Farmacogenetica studia: a) Gli effetti dei farmaci sull espressione genica b) La sintesi di farmaci da parte di organismi geneticamente modificati c) Nessuna delle risposte è esatta d) La terapia genica
La Farmacogenetica studia: a) Gli effetti dei farmaci sull espressione genica b) La sintesi di farmaci da parte di organismi geneticamente modificati c) Nessuna delle risposte è esatta d) La terapia genica
1. SINOSSI DEL PROTOCOLLO
 Versione finale 1.0, 23LUGLIO2014 1. SINOSSI DEL PROTOCOLLO Titolo dello studio Codice dello Sponsor Pseudonimo/Acronimo Primo studio nell uomo con MEN1112, un anticorpo monoclonale mirato al CD157 nella
Versione finale 1.0, 23LUGLIO2014 1. SINOSSI DEL PROTOCOLLO Titolo dello studio Codice dello Sponsor Pseudonimo/Acronimo Primo studio nell uomo con MEN1112, un anticorpo monoclonale mirato al CD157 nella
IL DIRETTORE GENERALE. VISTI gli articoli 8 e 9 del decreto legislativo 30 luglio 1999, n. 300;
 DETERMINAZIONE 6 agosto 2010. Regime di rimborsabilità e prezzo di vendita del medicinale «Nplate» (romiplostim) - autorizzata con procedura centralizzata europea dalla Commissione Europea. (Determinazione/C
DETERMINAZIONE 6 agosto 2010. Regime di rimborsabilità e prezzo di vendita del medicinale «Nplate» (romiplostim) - autorizzata con procedura centralizzata europea dalla Commissione Europea. (Determinazione/C
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE TRISENOX 1 mg/ml, concentrato per soluzione per infusione endovenosa 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE TRISENOX 1 mg/ml, concentrato per soluzione per infusione endovenosa 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
FARMACOCINETICA 1. Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA
 FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
Prof AM Vannucchi AA2009 10
 LEUCEMIE ACUTE 1 DEFINIZIONE Leucemia Acuta Sangue bianco decorso rapido, aggressivo Malattia clonale a carico dei progenitori emopoietici caratterizzata da alterate differenziazione e proliferazione con
LEUCEMIE ACUTE 1 DEFINIZIONE Leucemia Acuta Sangue bianco decorso rapido, aggressivo Malattia clonale a carico dei progenitori emopoietici caratterizzata da alterate differenziazione e proliferazione con
Programma evento Focus su leucemie acute c/o Villa Maria Hotel - C.da Pretaro - Francavilla al Mare (CH) 20 aprile 2018
 Programma evento Focus su leucemie acute c/o Villa Maria Hotel - C.da Pretaro - Francavilla al Mare (CH) 20 aprile 2018 Ore: 08:30 Apertura della segreteria e registrazione dei partecipanti Ore 09:15 Presentazione
Programma evento Focus su leucemie acute c/o Villa Maria Hotel - C.da Pretaro - Francavilla al Mare (CH) 20 aprile 2018 Ore: 08:30 Apertura della segreteria e registrazione dei partecipanti Ore 09:15 Presentazione
DEFINIZIONE DI LEUCEMIE
 LEUCEMIE DEFINIZIONE DI LEUCEMIE ü Proliferazione clonale e incontrollata di cellule emopoietiche immature ü Sono caratterizzate da sostituzione diffusa del midollo osseo da parte di cellule neoplastiche.
LEUCEMIE DEFINIZIONE DI LEUCEMIE ü Proliferazione clonale e incontrollata di cellule emopoietiche immature ü Sono caratterizzate da sostituzione diffusa del midollo osseo da parte di cellule neoplastiche.
Allegato III. Modifiche ai paragrafi pertinenti delle Informazioni sul Prodotto
 Allegato III Modifiche ai paragrafi pertinenti delle Informazioni sul Prodotto Nota: Le presenti modifiche ai paragrafi pertinenti delle informazioni sul prodotto sono l esito della procedura di referral.
Allegato III Modifiche ai paragrafi pertinenti delle Informazioni sul Prodotto Nota: Le presenti modifiche ai paragrafi pertinenti delle informazioni sul prodotto sono l esito della procedura di referral.
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
Scelta della terapia di 1 linea
 Scelta della terapia di 1 linea Uomo di 45 anni anamnesi patologica muta Giugno 2009: dolore emicostato a dx FANS (scarsa risposta) Luglio 2009: dolore emicostato sin rx mostra frattura costale emocromo
Scelta della terapia di 1 linea Uomo di 45 anni anamnesi patologica muta Giugno 2009: dolore emicostato a dx FANS (scarsa risposta) Luglio 2009: dolore emicostato sin rx mostra frattura costale emocromo
F O R M A T O E U R O P E O
 F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome Indirizzo Via Vivanti, 3-25133 Brescia Telefono 030-3384874; 348-5500412 Fax 030 3996021 E-mail russo@med.unibs.it
F O R M A T O E U R O P E O P E R I L C U R R I C U L U M V I T A E INFORMAZIONI PERSONALI Nome Indirizzo Via Vivanti, 3-25133 Brescia Telefono 030-3384874; 348-5500412 Fax 030 3996021 E-mail russo@med.unibs.it
Presentazione dei dati
 Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
INTERAZIONI FARMACOLOGICHE
 INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
