ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
|
|
|
- Maria Marconi
- 5 anni fa
- Visualizzazioni
Transcript
1 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1
2 1. DENOMINAZIONE DEL MEDICINALE Luveris 75 UI, polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene 75 UI di lutropina alfa (ormone luteinizzante umano ricombinante LH). Lutropina alfa è prodotta da cellule ovariche di Criceto Cinese (CHO) modificate geneticamente. Per gli eccipienti, vedere FORMA FARMACEUTICA Polvere e solvente per soluzione iniettabile. Aspetto della polvere: pastiglia di liofilizzato bianco Aspetto del solvente: soluzione limpida incolore 4. INFORMAZIONI CLINICHE 4.1 Indicazioni terapeutiche Luveris, in associazione con una preparazione a base di ormone follicolo stimolante (FSH), è raccomandato per la stimolazione dello sviluppo follicolare in donne con grave insufficienza di LH ed FSH. Negli studi clinici tali pazienti venivano identificate in base a livelli sierici di LH endogeno <1,2 UI/l. 4.2 Posologia e modo di somministrazione Il trattamento con Luveris deve essere iniziato sotto la supervisione di un medico esperto nel trattamento dell infertilità. L auto-somministrazione di Luveris deve essere eseguita solo da pazienti ben motivate, adeguatamente istruite e che possano consultarsi con un esperto. In donne con insufficienza di LH ed FSH, l obiettivo della terapia con Luveris in associazione con FSH è lo sviluppo di un singolo follicolo di Graff maturo dal quale verrà liberato l ovocita dopo la somministrazione di gonadotropina corionica umana (hcg). Luveris deve essere somministrato con iniezioni giornaliere simultaneamente ad FSH. Poichè queste pazienti sono amenorroiche e hanno una ridotta secrezione endogena di estrogeni, il trattamento può iniziare in qualsiasi momento. Ad oggi l esperienza clinica con Luveris in questa indicazione è stata acquisita con l uso concomitante di follitropina alfa. Luveris si somministra per via sottocutanea. La polvere deve essere ricostituita, immediatamente prima dell uso, con il solvente fornito. Il trattamento deve essere adattato in base alla risposta individuale della paziente che va valutata (i) attraverso il monitoraggio ecografico delle dimensioni del follicolo e (ii) mediante il dosaggio degli estrogeni. Lo schema posologico raccomandato comincia con 75 UI di lutropina alfa (cioè 1 flaconcino di Luveris) al giorno e UI di FSH. Se si ritiene opportuno un aumento della dose di FSH, l adattamento del dosaggio dovrà essere effettuato preferibilmente con incrementi di 37,5 UI-75 UI ad intervalli di 7-14 giorni. La durata della stimolazione di un ciclo può essere estesa fino a 5 settimane. Una volta ottenuta la risposta ottimale, ore dopo l ultima iniezione di Luveris ed FSH, è necessario somministrare da a UI di hcg in dose unica. Si raccomanda alla paziente di avere rapporti sessuali a scopi procreativi il giorno della somministrazione dell hcg e il giorno successivo. In alternativa, può essere eseguita una inseminazione intrauterina (IUI). 2
3 Al fine di evitare una insufficienza precoce del corpo luteo dopo l ovulazione, dovuta alla carenza di sostanze ad attività luteotropa (LH/hCG), deve essere valutata l opportunità di un supporto della fase luteale. In caso di risposta eccessiva, il trattamento deve essere interrotto e l hcg non deve essere somministrato. Nel ciclo successivo il trattamento deve essere ripreso con dosaggi di FSH più bassi rispetto al ciclo precedente. 4.3 Controindicazioni Luveris è controindicato in pazienti con: ipersensibilità alle gonadotropine o ad uno degli eccipienti; carcinoma dell ovaio, dell utero o della mammella; tumori dell ipotalamo e dell ipofisi attivi, non trattati; ingrossamento ovarico o cisti non dovute a sindrome dell ovaio policistico; emorragie ginecologiche ad eziologia sconosciuta; 4.4 Avvertenze speciali e opportune precauzioni d'impiego Prima di iniziare il trattamento deve essere adeguatamente studiata l infertilità di coppia e devono essere valutate le eventuali controindicazioni per la gravidanza. Questa specialità medicinale non deve essere utilizzata se non può essere ottenuta una risposta efficace come nel caso di insufficienza ovarica, malformazioni degli organi sessuali incompatibili con la gravidanza o fibromi uterini incompatibili con la gravidanza. Inoltre le pazienti devono essere esaminate per verificare l eventuale presenza di ipotiroidismo, insufficienza corticosurrenale, iperprolattinemia, tumori ipotalamici o ipofisari ed essere opportunamente trattate per tali patologie. Le pazienti sottoposte alla stimolazione dello sviluppo follicolare presentano un rischio maggiore di iperstimolazione in considerazione di una possibile risposta estrogenica eccessiva e dello sviluppo follicolare multiplo. La sindrome da iperstimolazione ovarica (OHSS) può divenire un evento clinico serio caratterizzato da grandi cisti ovariche che possono facilmente rompersi. In rari casi, un eccessiva risposta ovarica può dar luogo ad una significativa iperstimolazione se si somministra hcg per indurre l ovulazione. È pertanto consigliabile in questi casi non somministrare l hcg e consigliare la paziente di astenersi da rapporti sessuali o di usare metodi barriera di contraccezione per almeno 4 giorni. Si raccomanda un attento monitoraggio della risposta ovarica tramite ecografia, prima e durante la terapia di stimolazione, specialmente nelle pazienti affette da ovaio policistico. Nelle pazienti sottoposte ad induzione dell ovulazione, l incidenza di gravidanze multiple e nascite gemellari è aumentata rispetto ai concepimenti naturali. Si raccomanda l esecuzione di ecografie ed il dosaggio dei livelli sierici di estradiolo al fine di ridurre i rischi di OHSS o di gravidanze multiple. In pazienti anovulatorie il rischio di OHSS è aumentato in presenza di livelli di estradiolo maggiori di 900 pg/ml (3300 pmol/l) e in presenza di più di tre follicoli di diametro uguale o superiore a 14 mm. L osservanza dei dosaggi raccomandati di Luveris ed FSH e dello schema posologico ed un attento monitoraggio della terapia minimizzano l incidenza dell iperstimolazione ovarica e delle gravidanze multiple. In studi clinici, la specialità medicinale ha dimostrato di aumentare la sensibilità ovarica alla follitropina alfa. Se si ritiene opportuno un aumento della dose di FSH, l adattamento del dosaggio dovrà essere effettuato preferibilmente con incrementi di 37,5-75 UI ad intervalli di 7-14 giorni. 3
4 Nel corso di studi clinici, non sono stati descritti casi di ipersensibilità alla lutropina alfa. Non è stata eseguita una comparazione diretta tra Luveris/FSH e gonadotropina umana menopausale (hmg). Un confronto eseguito su dati storici indica che il tasso di ovulazione ottenuto con Luveris/FSH sia simile a quello ottenibile con hmg. 4.5 Interazioni con altri medicinali ed altre forme d interazione Luveris non deve essere somministrato con altre specialità medicinali nella stessa siringa, ad eccezione della follitropina alfa per la quale sono stati effettuati degli studi che dimostrano che la somministrazione congiunta dei due farmaci non altera significativamente l attività, la stabilità, le proprietà farmacocinetiche e farmacodinamiche dei principi attivi. 4.6 Gravidanza ed allattamento Luveris non deve essere somministrato durante la gravidanza o l allattamento. 4.7 Effetti sulla capacità di guidare veicoli e sull uso di macchinari Luveris non influisce sulla capacità di guidare veicoli o di usare macchinari. 4.8 Effetti indesiderati a) Descrizione generale Lutropina alfa viene utilizzata per la stimolazione dello sviluppo follicolare in associazione a follitropina alfa. In questo contesto è difficile attibuire gli effetti indesiderati all una o all altra sostanza utilizzata. Esiste una considerevole esperienza post-marketing sulla tollerabilità di specialità medicinali contenenti ormone luteinizzante umano (hlh) di origine urinaria. Si ritiene che il profilo di sicurezza di Luveris sia molto simile a quello degli hlh di origine urinaria, ad eccezione delle reazioni di ipersensibilità e delle reazioni locali al sito di iniezione. In uno studio clinico sono state riportate reazioni locali al sito di iniezione (ematoma, dolore, arrossamento, prurito o gonfiore) di grado lieve o moderato, rispettivamente nella percentuale del 7,4% e dello 0,9% delle iniezioni. Non sono state riportate reazioni locali di grado severo. Ad oggi, non sono state riportate reazioni allergiche a livello sistemico a seguito della somministrazione di Luveris. La sindrome da ipertimolazione ovarica è stata osservata in una percentuale inferiore al 6% delle pazienti trattate con Luveris. Non è stato riportato alcun caso di sindrome da iperstimolazione ovarica di grado severo (paragrafo 4.4 Avvertenze speciali e opportune precauzioni d impiego). In rare circostanze, alla terapia con gonadotropina umana della menopausa, sono stati associati tromboembolismo, torsione degli annessi (una complicazione dell ingrossamento ovarico) ed emoperitoneo. Sebbene questi eventi avversi non furono osservati, esiste la possibilità che essi si verifichino anche con il Luveris. Si possono verificare anche gravidanze ectopiche, soprattutto in donne con una precedente storia di disordini alle tube. b) Effetti indesiderati È stata utilizzata la seguente convenzione per la definizione della frequenza (eventi/n pazienti): molto raro: <1/10000, raro: >1/10000, <1/1000, non comune: >1/1000, <1/100, comune: > 1/100, <1/10, molto comune: > 1/10 4
5 Da analisi effettuate con il criterio del best evidence assessment, a seguito della somministrazione di Luveris, sono stati osservati i seguenti effetti indesiderati. Comuni Disordini al sito di applicazione: reazioni al sito di iniezione Disordini generali: cefalea, sonnolenza Disordini al sistema gastro-intestinale: nausea, dolore addominale, dolore pelvico Disordini riproduttivi: sindrome da iperstimolazione ovarica, ciste ovarica, dolore mammario Gli effetti indesiderati riportati coincidono con quanto descritto con altre specialità medicinali contenenti hlh, ad eccezione per le reazioni locali al sito di iniezione ove l incidenza era significativamente inferiore con il trattamento con Luveris. 4.9 Sovradosaggio Gli effetti di un sovradosaggio con lutropina alfa non sono noti, tuttavia potrebbe verificarsi una sindrome da iperstimolazione ovarica così come descritto nel capitolo Avvertenze speciali e opportune precauzioni di impiego. La somministrazione di dosi singole fino a UI di lutropina alfa in volontarie sane non ha causato eventi avversi di grado severo ed è stata ben tollerata. 5. PROPRIETÀ FARMACOLOGICHE 5.1 Proprietà farmacodinamiche Categoria farmacoterapeutica: gonadotropine. Codice ATC: G03G La lutropina alfa è un ormone umano luteinizzante ricombinante, una glicoproteina composta dalle subunità = e > unite da legami non covalenti. L ormone luteinizzante si lega, sulle cellule ovariche della teca (e della granulosa) e sulle cellule testicolari di Leydig, ad un recettore che condivide con l ormone gonadotropina corionica umana (hcg). Questo recettore transmembranario LH/CG fa parte della superfamiglia dei recettori G proteici-accoppiati; nello specifico, questo recettore ha un grande dominio extracellulare. In vitro l affinità di legame dell hlh ricombinante ai recettori LH/CG su cellule tumorali di Leydig (MA-10) è intermedia tra quella dell hcg e quella dell hlh ipofisario, ma entro lo stesso ordine di magnitudo. Nelle ovaie, durante la fase follicolare, l LH stimola le cellule della teca alla secrezione degli androgeni, che verranno usati come substrati dall enzima aromatasi della cellula della granulosa per produrre estradiolo, supportando lo sviluppo follicolare indotto dall FSH. A metà ciclo, alti livelli di LH provocano la formazione del corpo luteo e l ovulazione. Dopo l ovulazione, l LH stimola la produzione di progesterone nel corpo luteo incrementando la conversione del colesterolo in pregnenolone. Nella stimolazione dello sviluppo follicolare nelle donne anovulatorie con deficit di LH ed FSH, l effetto primario dovuto alla somministrazione di lutropina alfa è un incremento della secrezione di estradiolo da parte dei follicoli, la cui crescita è stimolata dall FSH. Negli studi clinici le pazienti venivano identificate in base a livelli sierici di LH endogeno < 1,2 UI/l dosati da un laboratorio centrale. Tuttavia è opportuno tenere conto della variabilità della misurazione dell LH eseguita da differenti laboratori. Il tasso di ovulazione ottenuto in questi studi è stato il 70-75% per ciclo. Il trattamento combinato di r- hlh e r-hfsh non è stato direttamente confrontato con quello a base di hmg. 5
6 5.2 Proprietà farmacocinetiche La farmacocinetica della lutropina alfa è stata studiata in donne volontarie sottoposte a desensibilizzazione ipofisaria con dosaggi da 75 UI fino a UI. Il profilo di farmacocinetica della lutropina alfa, è simile a quello dell hlh di origine urinaria. Dopo somministrazione endovenosa, la lutropina alfa viene rapidamente distribuita con un emivita iniziale di circa un ora ed eliminata dall organismo con un emivita terminale di circa ore. Allo stadio stazionario il volume di distribuzione è di circa l. La lutropina alfa mostra una farmacocinetica lineare, come valutato con l AUC, che è direttamente proporzionale alla dose somministrata. La clearance totale è di circa 2 l/h, e meno del 5% della dose viene escreta nelle urine. Il tempo medio di permanenza è di circa 5 ore. Dopo somministrazione sottocutanea, la biodisponibilità assoluta è di circa il 60%; l emivita terminale è leggermente prolungata. La farmacocinetica della lutropina alfa dopo somministrazione singola e ripetuta di Luveris è confrontabile ed il tasso di accumulo della lutropina alfa è minimo. Non esiste interazione farmacocinetica con la follitropina alfa se somministrata simultaneamente. 5.3 Dati preclinici di sicurezza Sono stati condotti studi tossicologici approfonditi con lutropina alfa su una varietà di modelli animali. Questi hanno previsto il trattamento giornaliero di ratti e scimmie con lutropina alfa per una durata di tre mesi ed hanno portato ad acquisizioni ben note sugli effetti farmacologici e morfologici correlati all LH. Nessuna tossicità è stata osservata in entrambe le specie. Come atteso in base alla natura di proteina eterologa dell ormone, lutropina alfa ha evocato, dopo qualche tempo, negli animali da esperimento, una risposta anticorpale che ha ridotto i livelli di LH misurabili nel siero senza però prevenire completamente la sua azione biologica. Non sono stati osservati segni di tossicità riconducibili allo sviluppo di anticorpi contro la lutropina alfa. La somministrazione ripetuta di lutropina alfa a ratte e coniglie gravide, alle dosi di 10 UI/kg/die ed oltre, ha causato alterazioni delle funzioni riproduttive con riassorbimento del feto e riduzione dell acquisto di peso corporeo da parte delle gestanti. Comunque, non è stato osservato alcun effetto teratogenico correlato al farmaco in entrambi i modelli animali. Altri studi hanno dimostrato che la lutropina alfa non è mutagenica. Dopo somministrazione endovenosa nei ratti di lutropina alfa marcata con radioattivo, la captazione tissutale ha seguito in parallelo il profilo di radioattività plasmatica con unicamente una forte affinità per le ovaie di animali gravide. La penetrazione fetale della radioattività era bassa. Nei ratti in allattamento, la radioattvità nel latte era uguale o superiore a quella plasmatica. A causa della sua natura di proteina eterologa, la lutropina alfa ha prodotto una moderata reazione allergica nelle cavie dopo somministrazione per via endovenosa. Per la stessa ragione è stata osservata una moderata sensibilizzazione nelle cavie dopo applicazione intradermica. 6. INFORMAZIONI FARMACEUTICHE 6.1 Elenco degli eccipienti Saccarosio Disodio fosfato biidrato Sodio diidrogeno fosfato monoidrato Polisorbato 20 Acido fosforico concentrato Sodio idrossido Metionina Azoto 6
7 Solvente: Acqua per preparazioni iniettabili. 6.2 Incompatibilità Il medicinale non deve essere miscelato con altri prodotti ad eccezione di quelli menzionati nella sezione Periodo di validità 24 mesi. 6.4 Speciali precauzioni per la conservazione Conservare a temperatura non superiore ai 25 C. Conservare nella confezione originale. 6.5 Natura e contenuto della confezione La polvere è confezionata in flaconcini da 3 ml in vetro neutro incolore (tipo I). I flaconcini sono sigillati con tappi in bromobutile protetti da ghiera e capsule pre-tagliate in alluminio. Il solvente è confezionato in flaconcini da 2 o da 3 ml di vetro neutro incolore (tipo I) con tappo in gomma rivestito in Teflon o in fiale da 2 ml in vetro neutro incolore (tipo I) Il prodotto è disponibile in confezioni da 1, 3 e 10 flaconcini con il numero corrispondente di flaconcini o di fiale di solvente. È possibile che non tutte le confezioni siano commercializzate. 6.6 Istruzioni per l'impiego e la manipolazione e per lo smaltimento Per uso singolo, da usare immediatamente dopo l apertura e la ricostituzione. La polvere deve essere ricostituita con il solvente prima dell uso operando una leggera roteazione. La soluzione ricostituita non deve essere somministrata se contiene particelle o non è limpida. Luveris può essere ricostituito insieme alla follitropina alfa e somministrato congiuntamente in una sola iniezione. In questo caso Luveris deve essere ricostituito per primo e poi utilizzato per ricostituire la polvere di follitropina alfa. Per evitare l iniezione di grossi volumi, un flaconcino di Luveris può essere ricostituito insieme ad una o due fiale/flaconcini di follitropina alfa da 37,5 UI, 75 UI o 150 UI, in 1 ml di solvente. Il prodotto non utilizzato ed i rifiuti derivati da tale medicinale devono essere smaltiti in conformità ai requisiti di legge locali. 7. TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO SERONO EUROPE LIMITED, 56 Marsh Wall, Londra E14 9TP Regno Unito 8. NUMERO(I) DELL AUTORIZZAZIONE (DELLE AUTORIZZAZIONI) ALL IMMISSIONE IN COMMERCIO EU/1/00/155/001 EU/1/00/155/002 EU/1/00/155/003 EU/1/00/155/004 7
8 EU/1/00/155/005 EU/1/00/155/ DATA DELLA PRIMA AUTORIZZAZIONE/ RINNOVO DELL AUTORIZZAZIONE 29 Novembre DATA DI REVISIONE DEL TESTO 8
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PYRALVEX 0,5% + 0,1% Soluzione gengivale 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 10 ml contengono : Principi attivi - Estratto
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE YOVIS 250 mg Capsule rigide YOVIS 1 g Granulato per sospensione orale YOVIS 250 mg Granulato per sospensione orale
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE GONAL-f 75 UI (5,5 microgrammi) polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE GONAL-f 75 UI (5,5 microgrammi) polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Ovitrelle 250 microgrammi/0,5 ml, soluzione iniettabile in siringa preriempita. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Ovitrelle 250 microgrammi/0,5 ml, soluzione iniettabile in siringa preriempita. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
2. P RIMA DI U TILIZZARE ASQUAM
 Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
Legga attentamente questo foglio prima di usare questo medicinale perchè contiene importanti informazioni per lei. Usi questo medicinale sempre come esattamente descritto in questo foglio o come il medico
Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare
 Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare Gli unici test a domicilio per la pianificazione familiare Test di ovulazione Test precoce di gravidanza Test di gravidanza
Gravidanza o no? Patient Diagnostics Test Rapidi della Progettazione Familiare Gli unici test a domicilio per la pianificazione familiare Test di ovulazione Test precoce di gravidanza Test di gravidanza
CEFODIE Cefonicid. Categoria farmacoterapeutica Antibiotico iniettabile.
 Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto
 MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto 01.0 DENOMINAZIONE DEL MEDICINALE MYCOSTATIN 100.000 UI/ML 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di sospensione orale contiene:
MYCOSTATIN RCP - Riassunto delle caratteristiche del prodotto 01.0 DENOMINAZIONE DEL MEDICINALE MYCOSTATIN 100.000 UI/ML 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un ml di sospensione orale contiene:
IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare
 1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
1. DENOMINAZIONE DEL MEDICINALE IGANTIBE 600 U.I. / 3 ml soluzione iniettabile per uso intramuscolare IGANTIBE 1000 U.I. / 5 ml soluzione iniettabile per uso intramuscolare 2. COMPOSIZIONE QUALITATIVA
SPERMATOGONI A(scuri) poia1(chiari) SPERMATOCITA PRIMARIO (max 64 da 1 cell) SPERMATOCITI SECONDARI SPERMATIDI SPERMATOZOI MATURI.
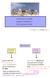 Riproduzione asessuata o agama sessuata o gamica genera individui, questi costituiscono un clone dalla ricombinazione dei genotipi parentali emerge la producono una generazione di figli con un genoma risultante
Riproduzione asessuata o agama sessuata o gamica genera individui, questi costituiscono un clone dalla ricombinazione dei genotipi parentali emerge la producono una generazione di figli con un genoma risultante
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 4 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE Puregon 50 U.I. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Puregon è costituito da una polvere liofilizzata
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 4 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE Puregon 50 U.I. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Puregon è costituito da una polvere liofilizzata
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 3 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. NOME DELLA SPECIALITA' MEDICINALE GONAL-F 75 2. COMPOSIZIONE QUALI-QUANTITATIVA GONAL-F contiene
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 3 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. NOME DELLA SPECIALITA' MEDICINALE GONAL-F 75 2. COMPOSIZIONE QUALI-QUANTITATIVA GONAL-F contiene
I MAMMIFERI Sottoclasse dei Prototeri o Monotremi Sottoclasse dei Metateri o Marsupiali Sottoclasse degli Euteri o Placentati
 I MAMMIFERI Sottoclasse dei Prototeri o Monotremi: le uova si sviluppano al di fuori del corpo materno o all interno ma senza nutrimento fornito dalla madre; Sottoclasse dei Metateri o Marsupiali: embrioni
I MAMMIFERI Sottoclasse dei Prototeri o Monotremi: le uova si sviluppano al di fuori del corpo materno o all interno ma senza nutrimento fornito dalla madre; Sottoclasse dei Metateri o Marsupiali: embrioni
le basi biologiche della riproduzione, il ciclo mestruale, le irregolarità mestrual i
 le basi biologiche della riproduzione, il ciclo mestruale, le irregolarità mestrual i Fisiologia della funzione ovarica Nucleo arcuato dell ipotalamo: produzione di GnRH (gonadotropin - releasing-hormon)
le basi biologiche della riproduzione, il ciclo mestruale, le irregolarità mestrual i Fisiologia della funzione ovarica Nucleo arcuato dell ipotalamo: produzione di GnRH (gonadotropin - releasing-hormon)
Foglio illustrativo: informazioni per il paziente. ISORAM 4%, soluzione per infusione. Soluzione di aminoacidi
 Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
Foglio illustrativo: informazioni per il paziente ISORAM 4%, soluzione per infusione Soluzione di aminoacidi Legga attentamente questo foglio prima che le venga somministrato questo medicinale perché contiene
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Pergoveris 150 UI/75 UI polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Pergoveris 150 UI/75 UI polvere e solvente per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Fertavid 50 UI/0,5 ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene 50
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Fertavid 50 UI/0,5 ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino contiene 50
Foglio illustrativo: informazioni per il paziente. MAALOX 400 mg + 400 mg compresse masticabili. Magnesio idrossido + Alluminio ossido, idrato
 Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente MAALOX 400 mg + 400 mg compresse masticabili Magnesio idrossido + Alluminio ossido, idrato Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per il paziente. Lyseen 4 mg compresse Lyseen 2 mg/ml soluzione iniettabile pridinolo mesilato
 Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
Foglio illustrativo: informazioni per il paziente pridinolo mesilato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. - Conservi questo
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 RINAZINA 100 mg/100 ml SPRAY NASALE, SOLUZIONE nafazolina Foglio illustrativo PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE
RINAZINA 100 mg/100 ml SPRAY NASALE, SOLUZIONE nafazolina Foglio illustrativo PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE
FARMACOCINETICA 1. Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA
 FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
IDI FARMACEUTICI srl - Via dei Castelli Romani 83/85-00040 POMEZIA (Roma).
 ALOXIDIL 2% soluzione cutanea (Minoxidil) COMPOSIZIONE QUALI - QUANTITATIVA. L'ALOXIDIL è una soluzione contenente minoxidil, alla concentrazione del 2% (pari a 20 mg/ml) ed eccipienti costituiti da glicole
ALOXIDIL 2% soluzione cutanea (Minoxidil) COMPOSIZIONE QUALI - QUANTITATIVA. L'ALOXIDIL è una soluzione contenente minoxidil, alla concentrazione del 2% (pari a 20 mg/ml) ed eccipienti costituiti da glicole
Azioni neuroendocrine Apparato riproduttivo Sistema nervoso centrale
 1 I progestinici sono composti con attività simile a quella del progesterone e includono il progesterone e agenti simili come il medrossiprogesterone acetato (pregnani), agenti simili al 19-nortestosterone
1 I progestinici sono composti con attività simile a quella del progesterone e includono il progesterone e agenti simili come il medrossiprogesterone acetato (pregnani), agenti simili al 19-nortestosterone
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinaleperché
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE ANASTROZOLO DOC Generici 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di prendere questo medicinaleperché
PERCORSO GONADI 2 INQUADRAMENTO DELL INFERTILITA DI COPPIA OPZIONI TERAPEUTICHE VINCENZO TOSCANO
 PERCORSO GONADI 2 INQUADRAMENTO DELL INFERTILITA DI COPPIA OPZIONI TERAPEUTICHE VINCENZO TOSCANO DIPARTIMENTO DI MEDICINA CLINICA E MOLECOLARE SAPIENZA UNIVERSITA DI ROMA AZIENDA OPEDALIERA SANT ANDREA
PERCORSO GONADI 2 INQUADRAMENTO DELL INFERTILITA DI COPPIA OPZIONI TERAPEUTICHE VINCENZO TOSCANO DIPARTIMENTO DI MEDICINA CLINICA E MOLECOLARE SAPIENZA UNIVERSITA DI ROMA AZIENDA OPEDALIERA SANT ANDREA
Foglio illustrativo: informazioni per l utilizzatore. Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato
 Foglio illustrativo: informazioni per l utilizzatore Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
Foglio illustrativo: informazioni per l utilizzatore Iridina Due 0,5 mg/ml collirio, soluzione Nafazolina cloridrato Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti
L apparato riproduttore femminile
 L apparato riproduttore femminile 2 Ovaie 2 tube di Falloppio Utero Vagina Forma ovale GONADI femminili (OVAIE) All interno dell addome Producono gli ormoni femminili: gli estrogeni e il progesterone permettono
L apparato riproduttore femminile 2 Ovaie 2 tube di Falloppio Utero Vagina Forma ovale GONADI femminili (OVAIE) All interno dell addome Producono gli ormoni femminili: gli estrogeni e il progesterone permettono
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Fattore VIII umano della coagulazione del sangue complessato con fattore von Willebrand.
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALPHANATE 250 Polvere e solvente per soluzione per infusione ALPHANATE 500 Polvere e solvente per soluzione per infusione ALPHANATE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE ALPHANATE 250 Polvere e solvente per soluzione per infusione ALPHANATE 500 Polvere e solvente per soluzione per infusione ALPHANATE
CONSENSO INFORMATO PER LE TECNICHE DI PROCREAZIONE MEDICO- ASSISTITA. La sottoscritta. documento. e il sottoscritto. documento
 CONSENSO INFORMATO PER LE TECNICHE DI PROCREAZIONE MEDICO- ASSISTITA La sottoscritta e il sottoscritto acconsentono liberamente di sottoporsi al trattamento di procreazione medico-assistita FIVET (Fertilizzazione
CONSENSO INFORMATO PER LE TECNICHE DI PROCREAZIONE MEDICO- ASSISTITA La sottoscritta e il sottoscritto acconsentono liberamente di sottoporsi al trattamento di procreazione medico-assistita FIVET (Fertilizzazione
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
Foglio illustrativo: informazioni per l utilizzatore HAEMATE P 500 UI/10 ml polvere e solvente per soluzione per iniezione o infusione HAEMATE P 1000 UI/15 ml polvere e solvente per soluzione per iniezione
L Inseminazione Intrauterina
 L Inseminazione Intrauterina Informazioni per la coppia UNITÀ OPERATIVA PROCREAZIONE MEDICALMENTE ASSISTITA FONDAZIONE IRCCS IRCCS CA' GRANDA OSPEDALE MAGGIORE POLICLINICO PAD. REGINA ELENA VIA M. FANTI,
L Inseminazione Intrauterina Informazioni per la coppia UNITÀ OPERATIVA PROCREAZIONE MEDICALMENTE ASSISTITA FONDAZIONE IRCCS IRCCS CA' GRANDA OSPEDALE MAGGIORE POLICLINICO PAD. REGINA ELENA VIA M. FANTI,
PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO
 (Foglio illustrativo) PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi
(Foglio illustrativo) PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che può essere usato per curare disturbi lievi
Foglio illustrativo: informazioni per l utilizzatore. BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato
 Foglio illustrativo: informazioni per l utilizzatore BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato Medicinale equivalente Legga attentamente questo foglio prima di usare questo
Foglio illustrativo: informazioni per l utilizzatore BREXAGENBETA 0,1% + 0,1% crema Gentamicina solfato e betametasone valerato Medicinale equivalente Legga attentamente questo foglio prima di usare questo
NEO BOROCILLINA GOLA DOLORE
 FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
FOGLIO ILLUSTRATIVO PRIMA DELL USO LEGGERE CON ATTENZIONE TUTTE LE INFORMAZIONI CONTENUTE NEL FOGLIO ILLUSTRATIVO Questo è un medicinale di AUTOMEDICAZIONE che potete usare per curare disturbi lievi e
L INSEMINAZIONE INTRAUTERINA
 L INSEMINAZIONE INTRAUTERINA Informazioni per la coppia A cura del dott. G. Ragni Unità Operativa - Centro Sterilità Responsabile: dott.ssa C. Scarduelli FONDAZIONE OSPEDALE MAGGIORE POLICLINICO MANGIAGALLI
L INSEMINAZIONE INTRAUTERINA Informazioni per la coppia A cura del dott. G. Ragni Unità Operativa - Centro Sterilità Responsabile: dott.ssa C. Scarduelli FONDAZIONE OSPEDALE MAGGIORE POLICLINICO MANGIAGALLI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC)
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC) 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: Rabipur 2,5 UI/ml, polvere e solvente per soluzioni iniettabili Vaccino rabico per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO Rabipur (Vaccino rabico PCEC) 1. DENOMINAZIONE DELLA SPECIALITÀ MEDICINALE: Rabipur 2,5 UI/ml, polvere e solvente per soluzioni iniettabili Vaccino rabico per
CENTRO DI PROCREAZIONE MEDICALMENTE ASSISTITA
 U.O.C. OSTETRICIA E GINECOLOGIA PRESIDIO OSPEDALIERO SANTA MARIA DEI BATTUTI CONEGLIANO (TV) CENTRO DI PROCREAZIONE MEDICALMENTE ASSISTITA Carta dei Servizi LA STRUTTURA Il Centro di Procreazione Medicalmente
U.O.C. OSTETRICIA E GINECOLOGIA PRESIDIO OSPEDALIERO SANTA MARIA DEI BATTUTI CONEGLIANO (TV) CENTRO DI PROCREAZIONE MEDICALMENTE ASSISTITA Carta dei Servizi LA STRUTTURA Il Centro di Procreazione Medicalmente
Foglio illustrativo: Informazioni per l utilizzatore. Finasteride Ranbaxy 5 mg compresse rivestite con film. Medicinale equivalente
 Foglio illustrativo: Informazioni per l utilizzatore Finasteride Ranbaxy 5 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio illustrativo prima di usare questo medicinale
Foglio illustrativo: Informazioni per l utilizzatore Finasteride Ranbaxy 5 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio illustrativo prima di usare questo medicinale
RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ruconest 2100 U polvere per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
RUCONEST (Conestat alfa) RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Ruconest 2100 U polvere per soluzione iniettabile. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Un flaconcino
FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. CAREFINAST 1 mg compresse rivestite con film Finasteride
 FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE CAREFINAST 1 mg compresse rivestite con film Finasteride Legga attentamente questo foglio prima di usare questo medicinale poiché contiene informazioni
FOGLIETTO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE CAREFINAST 1 mg compresse rivestite con film Finasteride Legga attentamente questo foglio prima di usare questo medicinale poiché contiene informazioni
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica
 Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan.
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan. Legga attentamente questo foglio prima di usare questo medicinale. - Conservi questo
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Busilvex 6 mg/ml concentrato per soluzione per infusione busulfan. Legga attentamente questo foglio prima di usare questo medicinale. - Conservi questo
IGIENE INTIMA AL MASCHILE
 IGIENE INTIMA AL MASCHILE La parola igiene deriva dal greco e significa protezione e miglioramento della salute ; quindi il lavarsi fa parte integrante del modo in cui è corretto vivere, ma è anche vero
IGIENE INTIMA AL MASCHILE La parola igiene deriva dal greco e significa protezione e miglioramento della salute ; quindi il lavarsi fa parte integrante del modo in cui è corretto vivere, ma è anche vero
irsutismo femminile ipertricosi femminile Oggi una bellezza femminile senza peli problemi di salute
 La peluriia femmiiniile iin eccesso Un sserriio prrobllema perr lla ffemmiiniilliittà delllla donna Il modello di un corpo senza peli e con la pelle vellutata Peluria in eccesso : il sentirsi poco femminile
La peluriia femmiiniile iin eccesso Un sserriio prrobllema perr lla ffemmiiniilliittà delllla donna Il modello di un corpo senza peli e con la pelle vellutata Peluria in eccesso : il sentirsi poco femminile
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FANHDI 250 U.I. polvere e solvente per soluzione per infusione FANHDI 500 U.I. polvere e solvente per soluzione per infusione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE FANHDI 250 U.I. polvere e solvente per soluzione per infusione FANHDI 500 U.I. polvere e solvente per soluzione per infusione
Duplicazione cellulare
 Duplicazione cellulare La morte è necessaria? William R. Clark Sesso e origini della morte, McGraw-Hill, 1998 Riproduzione negli organismi pluricellulari Partenogenesi Riproduzione sessuale Riproduzione
Duplicazione cellulare La morte è necessaria? William R. Clark Sesso e origini della morte, McGraw-Hill, 1998 Riproduzione negli organismi pluricellulari Partenogenesi Riproduzione sessuale Riproduzione
Riassunto delle Caratteristiche del Prodotto INDICE. 01.0 DENOMINAZIONE DEL MEDICINALE Inizio Pagina.
 1 di 5 07/11/2012 14:56 A B C D E F G H I J K L M N O P Q R S T U V W X Y Riassunto delle Caratteristiche del Prodotto INDICE 01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
1 di 5 07/11/2012 14:56 A B C D E F G H I J K L M N O P Q R S T U V W X Y Riassunto delle Caratteristiche del Prodotto INDICE 01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ARTROSI ED ACIDO IALURONICO. A cura di Dr Marco Collarile. Medico Chirurgo Specialista in Ortopedia e Traumatologia
 ARTROSI ED ACIDO IALURONICO A cura di Dr Marco Collarile Medico Chirurgo Specialista in Ortopedia e Traumatologia 1. INTRODUZIONE L osteartrosi e di gran lunga l artropatia più diffusa nella popolazione
ARTROSI ED ACIDO IALURONICO A cura di Dr Marco Collarile Medico Chirurgo Specialista in Ortopedia e Traumatologia 1. INTRODUZIONE L osteartrosi e di gran lunga l artropatia più diffusa nella popolazione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO INCURIN 1 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: estriolo 1 mg/compressa
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO INCURIN 1 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: estriolo 1 mg/compressa
La Riproduzione e l Apparato Riproduttivo Umano. Tratto e parzialmente rielaborato da amedeorollo.altervista.org
 La Riproduzione e l Apparato Riproduttivo Umano Tratto e parzialmente rielaborato da amedeorollo.altervista.org La Riproduzione Perché gli esseri viventi si riproducono? La riproduzione (o procreazione)
La Riproduzione e l Apparato Riproduttivo Umano Tratto e parzialmente rielaborato da amedeorollo.altervista.org La Riproduzione Perché gli esseri viventi si riproducono? La riproduzione (o procreazione)
1. DENOMINAZIONE DEL MEDICINALE. CALCITONINA SANDOZ 50 UI/ml Soluzione Iniettabile e per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 Riassunto delle Caratteristiche del Prodotto --------------------------------------------------------------------------------------------------------------- Formattato: Sinistro: 1,59 cm, Destro 1,59 cm
Riassunto delle Caratteristiche del Prodotto --------------------------------------------------------------------------------------------------------------- Formattato: Sinistro: 1,59 cm, Destro 1,59 cm
Gli ormoni sessuali e il differenziamento cerebrale. In che modo?
 Gli ormoni sessuali e il differenziamento cerebrale L esposizione agli androgeni porta allo sviluppo di differenze nelle strutture cerebrali, oltre che degli organi sessuali interni ed esterni, che porterà
Gli ormoni sessuali e il differenziamento cerebrale L esposizione agli androgeni porta allo sviluppo di differenze nelle strutture cerebrali, oltre che degli organi sessuali interni ed esterni, che porterà
VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005
 VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005 2005 VANTAGGI DELLA VIA ORALE! Le forme farmaceutiche orali sono facili e convenienti da usare
VIA ORALE MODULO DI TECNICHE E FORME FARMACEUTICHE CORSO DI LAUREA IN BIOTECNOLOGIE ANNO ACCADEMICO 2004-2005 2005 VANTAGGI DELLA VIA ORALE! Le forme farmaceutiche orali sono facili e convenienti da usare
PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL
 PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: NOVEMBRE 2001 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 ELEMENTI IDENTIFICATIVI
PIERREL FARMACEUTICI S.P.A. SCHEDA DI SICUREZZA: ALFA PIERREL ISTRUZIONE OPERATIVA SICUREZZA DATA DI EMISSIONE: NOVEMBRE 2001 1. ELEMENTI IDENTIFICATIVI DEL PREPARATO E DELLA SOCIETÀ 1.1 ELEMENTI IDENTIFICATIVI
TRIAZOLAM PENSA 0,125 mg compresse 0,25 mg compresse MEDICINALE EQUIVALENTE
 Foglio illustrativo TRIAZOLAM PENSA 0,125 mg compresse 0,25 mg compresse MEDICINALE EQUIVALENTE CATEGORIA FARMACOTERAPEUTICA Neurologici. Ipnotici non barbiturici. Derivati benzodiazepinici. INDICAZIONI
Foglio illustrativo TRIAZOLAM PENSA 0,125 mg compresse 0,25 mg compresse MEDICINALE EQUIVALENTE CATEGORIA FARMACOTERAPEUTICA Neurologici. Ipnotici non barbiturici. Derivati benzodiazepinici. INDICAZIONI
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO THYMOVAR; 15 g strisce per alveare per api mellifere. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una striscia per
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO THYMOVAR; 15 g strisce per alveare per api mellifere. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA una striscia per
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Orgalutran 0,25 mg/0,5 ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna siringa preriempita
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Orgalutran 0,25 mg/0,5 ml soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ciascuna siringa preriempita
FOGLIO ILLUSTRATIVO GAVISCON
 FOGLIO ILLUSTRATIVO GAVISCON 500 mg/10 ml + 267 mg/10 ml sospensione orale GAVISCON 500 mg/10 ml + 267 mg/10 ml sospensione orale aroma menta Sodio alginato + sodio bicarbonato Legga attentamente questo
FOGLIO ILLUSTRATIVO GAVISCON 500 mg/10 ml + 267 mg/10 ml sospensione orale GAVISCON 500 mg/10 ml + 267 mg/10 ml sospensione orale aroma menta Sodio alginato + sodio bicarbonato Legga attentamente questo
ENDOCRINOLOGIA E NUTRIZIONE UMANA LEZIONE 9 GHIANDOLE SESSUALI (SECONDA PARTE)
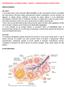 ENDOCRINOLOGIA E NUTRIZIONE UMANA LEZIONE 9 GHIANDOLE SESSUALI (SECONDA PARTE) ORMONI FEMMINILI Altri effetti Gli estrogeni hanno inoltre importanti effetti metabolici: ad alte concentrazioni riducono
ENDOCRINOLOGIA E NUTRIZIONE UMANA LEZIONE 9 GHIANDOLE SESSUALI (SECONDA PARTE) ORMONI FEMMINILI Altri effetti Gli estrogeni hanno inoltre importanti effetti metabolici: ad alte concentrazioni riducono
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Nobivac Myxo-RHD liofilizzato e solvente per sospensione iniettabile per conigli. 2. COMPOSIZIONE QUALITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Nobivac Myxo-RHD liofilizzato e solvente per sospensione iniettabile per conigli. 2. COMPOSIZIONE QUALITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE LYRICA 25 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 25 mg di pregabalin.
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE LYRICA 25 mg capsule rigide 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni capsula rigida contiene 25 mg di pregabalin.
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Norlevo 750 microgrammi compresse Levonorgestrel
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Norlevo 750 microgrammi compresse Levonorgestrel Legga attentamente questo foglio prima di usare questo medicinale Questo medicinale non è soggetto
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Norlevo 750 microgrammi compresse Levonorgestrel Legga attentamente questo foglio prima di usare questo medicinale Questo medicinale non è soggetto
Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale
 Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale Gozzo Endemico - Prevalenza superiore al 5% in una popolazione di bambini - di età compresa tra i 6 e i 12 anni Gozzo Sporadico
Patologia Nodulare Tiroidea: Diagnostica clinica laboratoristica e strumentale Gozzo Endemico - Prevalenza superiore al 5% in una popolazione di bambini - di età compresa tra i 6 e i 12 anni Gozzo Sporadico
APPARATO GENITALE INSIEME DI ORGANI DEPUTATI ALLA : FORMAZIONE DEI GAMETI FECONDAZIONE SVILUPPO DELL EMBRIONE E DEL FETO
 APPARATO GENITALE INSIEME DI ORGANI DEPUTATI ALLA : FORMAZIONE DEI GAMETI FECONDAZIONE SVILUPPO DELL EMBRIONE E DEL FETO APPARATO RIPRODUTTORE MASCHILE GONADI VIE SPERMATICHE convogliano i gameti all uretra
APPARATO GENITALE INSIEME DI ORGANI DEPUTATI ALLA : FORMAZIONE DEI GAMETI FECONDAZIONE SVILUPPO DELL EMBRIONE E DEL FETO APPARATO RIPRODUTTORE MASCHILE GONADI VIE SPERMATICHE convogliano i gameti all uretra
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/18
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/18 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Oncept IL-2 liofilizzato e solvente per sospensione iniettabile per gatti 2. COMPOSIZIONE QUALITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1/18 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Oncept IL-2 liofilizzato e solvente per sospensione iniettabile per gatti 2. COMPOSIZIONE QUALITATIVA
Nota Informativa Importante. Guida alla Terapia per i Paziente. Guida alla Contraccezione. Modulo d'informazione e Consenso Informato
 AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
Dopo ricostituzione, un flaconcino contiene 5 mg di somatropina* (corrispondenti a 15 UI) per ml.
 1. DENOMINAZIONE DEL MEDICINALE Omnitrope 5 mg/ml in polvere e solvente per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Dopo ricostituzione, un flaconcino contiene 5 mg di somatropina*
1. DENOMINAZIONE DEL MEDICINALE Omnitrope 5 mg/ml in polvere e solvente per soluzione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Dopo ricostituzione, un flaconcino contiene 5 mg di somatropina*
FOGLIETTO ILLUSTRATIVO FUSIDIUM 1%
 FOGLIETTO ILLUSTRATIVO FUSIDIUM 1% FUSIDIUM 1 % Gocce oftalmiche Acido Fusidico CATEGORIA FARMACOTERAPEUTICA Antinfettivo oculare. INDICAZIONI Fusidium è indicato in infezioni batteriche oculari causate
FOGLIETTO ILLUSTRATIVO FUSIDIUM 1% FUSIDIUM 1 % Gocce oftalmiche Acido Fusidico CATEGORIA FARMACOTERAPEUTICA Antinfettivo oculare. INDICAZIONI Fusidium è indicato in infezioni batteriche oculari causate
Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE
 Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE PNEUMOVAX, soluzione iniettabile in flaconcino Vaccino pneumococcico polisaccaridico 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Riassunto delle Caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE PNEUMOVAX, soluzione iniettabile in flaconcino Vaccino pneumococcico polisaccaridico 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Riassunto delle caratteristiche del prodotto
 Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE INFLEXAL V Sospensione iniettabile Vaccino influenzale (antigene di superficie, inattivato, virosomale) Stagione 2007/2008 2.
Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE INFLEXAL V Sospensione iniettabile Vaccino influenzale (antigene di superficie, inattivato, virosomale) Stagione 2007/2008 2.
Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3
 giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
giunta regionale Allegato A al Decreto n. 15 del 01 marzo 2016 pag. 1/3 SOMMINISTRAZIONE PER INFUSIONE A DOMICILIO DI FARMACI AD ALTO COSTO PER PERSONE AFFETTE DA MALATTIA RARA (Documento approvato nella
FISIOPATOLOGIA E NEUROREGOLAZIONE DELL ASSE IPOTALAMO IPOFISI GONADI
 FISIOPATOLOGIA E NEUROREGOLAZIONE DELL ASSE IPOTALAMO IPOFISI GONADI Richiami anatomofisiologici Funzionamento dell asse in corso di esercizio fisico Funzionamento dell asse in condizioni critiche Conseguenze
FISIOPATOLOGIA E NEUROREGOLAZIONE DELL ASSE IPOTALAMO IPOFISI GONADI Richiami anatomofisiologici Funzionamento dell asse in corso di esercizio fisico Funzionamento dell asse in condizioni critiche Conseguenze
Azoospermia Assenza di spermatozoi nel liquido seminale Criptozoospermia Assenza di spermatozoi nell eiaculato ma presenza di qualche spermatozoo nel
 Diagnosi Azoospermia Assenza di spermatozoi nel liquido seminale Criptozoospermia Assenza di spermatozoi nell eiaculato ma presenza di qualche spermatozoo nel centrifugato Oligozoospermia severa Grave
Diagnosi Azoospermia Assenza di spermatozoi nel liquido seminale Criptozoospermia Assenza di spermatozoi nell eiaculato ma presenza di qualche spermatozoo nel centrifugato Oligozoospermia severa Grave
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Purevax RC liofilizzato e solvente per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO Purevax RC liofilizzato e solvente per sospensione iniettabile 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Ogni siringa pre-riempita (0,5 ml) contiene 22 microgrammi (6 MUI*) di interferone beta-1a**.
 1. DENOMINAZIONE DEL MEDICINALE Rebif 22 microgrammi soluzione iniettabile in siringa pre-riempita 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni siringa pre-riempita (0,5 ml) contiene 22 microgrammi
1. DENOMINAZIONE DEL MEDICINALE Rebif 22 microgrammi soluzione iniettabile in siringa pre-riempita 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni siringa pre-riempita (0,5 ml) contiene 22 microgrammi
Riassunto delle caratteristiche del prodotto
 Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE INFLEXAL V Sospensione iniettabile Vaccino influenzale (antigene di superficie, inattivato, virosomale) Stagione 2011/2012 2.
Riassunto delle caratteristiche del prodotto 1. DENOMINAZIONE DEL MEDICINALE INFLEXAL V Sospensione iniettabile Vaccino influenzale (antigene di superficie, inattivato, virosomale) Stagione 2011/2012 2.
Folder_farmaci1.qxd 20-09-2006 18:00 Pagina 1 APPROFONDISCI LA TUA CONOSCENZA SUI FARMACI.
 Folder_farmaci1.qxd 20-09-2006 18:00 Pagina 1 APPROFONDISCI LA TUA CONOSCENZA SUI FARMACI. 1 Folder_farmaci1.qxd 20-09-2006 18:00 Pagina 2 COS'È UN FARMACO? E una sostanza chimica, naturale o sintetica,
Folder_farmaci1.qxd 20-09-2006 18:00 Pagina 1 APPROFONDISCI LA TUA CONOSCENZA SUI FARMACI. 1 Folder_farmaci1.qxd 20-09-2006 18:00 Pagina 2 COS'È UN FARMACO? E una sostanza chimica, naturale o sintetica,
Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi
 Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi Legga attentamente questo foglio prima di prendere questo medicinale perchè
Foglio illustrativo: informazioni per l utilizzatore ELEVIT compresse rivestite con film 12 vitamine 7 minerali e oligoelementi Legga attentamente questo foglio prima di prendere questo medicinale perchè
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
Foglio illustrativo: informazioni per l utilizzatore. FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica
 Foglio illustrativo: informazioni per l utilizzatore FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica Legga attentamente questo foglio prima di usare questo medicinale
Foglio illustrativo: informazioni per l utilizzatore FLUORESCEINA SODICA MONICO 1 g/5 ml (20%) soluzione iniettabile Fluoresceina sodica Legga attentamente questo foglio prima di usare questo medicinale
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PROSTATIL 2 mg compresse PROSTATIL 5 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PROSTATIL 2 mg compresse Ogni compressa
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE PROSTATIL 2 mg compresse PROSTATIL 5 mg compresse 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA PROSTATIL 2 mg compresse Ogni compressa
Foglio illustrativo: informazioni per il paziente. Cormeto 250 mg capsule Metirapone
 FOGLIO ILLUSTRATIVO Foglio illustrativo: informazioni per il paziente Cormeto 250 mg capsule Metirapone Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
FOGLIO ILLUSTRATIVO Foglio illustrativo: informazioni per il paziente Cormeto 250 mg capsule Metirapone Legga attentamente questo foglio prima di prendere questo medicinale perché contiene importanti informazioni
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Ogni bustina contiene: Principio attivo: sucralfato (pari ad alluminio 190 mg/g) 2000 mg
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE SUCRALFIN 2 g Granulato per Sospensione Orale 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni bustina contiene: Principio attivo:
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE SUCRALFIN 2 g Granulato per Sospensione Orale 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni bustina contiene: Principio attivo:
- Trattamento dell ipercalcemia indotta da tumori con o senza metastasi.
 1. DENOMINAZIONE DEL MEDICINALE Iasibon 2 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una fiala da 2 ml di concentrato per soluzione per infusione contiene 2 mg
1. DENOMINAZIONE DEL MEDICINALE Iasibon 2 mg concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Una fiala da 2 ml di concentrato per soluzione per infusione contiene 2 mg
L'APPARATO RIPRODUTTORE
 L'APPARATO RIPRODUTTORE L'apparato riproduttore è l'insieme di organi e di strutture che permettono la riproduzione sessuale negli organismi animali. APPARATO RIPRODUTTORE MASCHILE Organi: Testicoli Sistema
L'APPARATO RIPRODUTTORE L'apparato riproduttore è l'insieme di organi e di strutture che permettono la riproduzione sessuale negli organismi animali. APPARATO RIPRODUTTORE MASCHILE Organi: Testicoli Sistema
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Finasteride Teva Generics 1 mg compresse rivestite con film. Medicinale equivalente
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Finasteride Teva Generics 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale.
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Finasteride Teva Generics 1 mg compresse rivestite con film Medicinale equivalente Legga attentamente questo foglio prima di usare questo medicinale.
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO STRONGHOLD 15 mg soluzione per spot-on STRONGHOLD 30 mg soluzione per spot-on STRONGHOLD 45 mg soluzione
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE VETERINARIO STRONGHOLD 15 mg soluzione per spot-on STRONGHOLD 30 mg soluzione per spot-on STRONGHOLD 45 mg soluzione
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE. Oraqix 25/25 mg/g Gel Periodontale lidocaina e prilocaina
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE Oraqix 25/25 mg/g Gel Periodontale lidocaina e prilocaina Legga attentamente questo foglio prima di usare questo medicinale. Conservi questo foglio.
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L'UTILIZZATORE Oraqix 25/25 mg/g Gel Periodontale lidocaina e prilocaina Legga attentamente questo foglio prima di usare questo medicinale. Conservi questo foglio.
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L Agenzia Italiana del Farmaco (AIFA) IMPORTANTI INFORMAZIONI DI SICUREZZA BUFLOMEDIL
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L Agenzia Italiana del Farmaco (AIFA) Febbraio 2010 IMPORTANTI INFORMAZIONI DI SICUREZZA BUFLOMEDIL Nuove informazioni di sicurezza relative ai medicinali contenenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L Agenzia Italiana del Farmaco (AIFA) Febbraio 2010 IMPORTANTI INFORMAZIONI DI SICUREZZA BUFLOMEDIL Nuove informazioni di sicurezza relative ai medicinali contenenti
GAZYVARO. Farmaco di nuova registrazione
 AllegatoallaDeterminaAIFANumero1012/2014del24/09/2014/ Inserimento,inaccordoall articolo12,comma5dellalegge189/2012,inappositasezione(denominataclasse C(nn))dedicataaifarmacinonancoravalutatiaifinidellarimborsabilitànellemoredellapresentazioneda
AllegatoallaDeterminaAIFANumero1012/2014del24/09/2014/ Inserimento,inaccordoall articolo12,comma5dellalegge189/2012,inappositasezione(denominataclasse C(nn))dedicataaifarmacinonancoravalutatiaifinidellarimborsabilitànellemoredellapresentazioneda
IL RUOLO DEL LABORATORIO NELLA DIAGNOSTICA DELL AMENORREA SECONDARIA
 IL RUOLO DEL LABORATORIO NELLA DIAGNOSTICA DELL AMENORREA SECONDARIA S. Bernardi e B. Fabris S.C. Medicina Clinica, DAI di Medicina Interna; AOUTS-Ospedali Riuniti di Trieste L amenorrea secondaria, definita
IL RUOLO DEL LABORATORIO NELLA DIAGNOSTICA DELL AMENORREA SECONDARIA S. Bernardi e B. Fabris S.C. Medicina Clinica, DAI di Medicina Interna; AOUTS-Ospedali Riuniti di Trieste L amenorrea secondaria, definita
1 dose di vaccino (0.5 ml) contiene almeno 24 UI di virus dell'epatite A inattivato (ceppo RG-SB), coltivato su cellule diploidi umane (MRC-5).
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Epaxal sospensione iniettabile in una siringa preriempita. Vaccino dell'epatite A (inattivato, virosomale). 2. COMPOSIZIONE
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Epaxal sospensione iniettabile in una siringa preriempita. Vaccino dell'epatite A (inattivato, virosomale). 2. COMPOSIZIONE
DAL PICK UP TRANSFER. Lab. Biologia della Riproduzione - Potenza
 DAL PICK UP ALL EMBRYO TRANSFER Lab. Biologia della Riproduzione - Potenza Fisiologia del gamete maschile Lo spermatozoo è costituito da tre parti principali: a) La testa: sede del patrimonio genetico;
DAL PICK UP ALL EMBRYO TRANSFER Lab. Biologia della Riproduzione - Potenza Fisiologia del gamete maschile Lo spermatozoo è costituito da tre parti principali: a) La testa: sede del patrimonio genetico;
Ruolo della tromboprofilassi in donne con aborto ricorrente: outcome delle successive gravidanze e terapie a confronto
 Università degli Studi di Roma La Sapienza I FACOLTÀ DI MEDICINA E CHIRURGIA DIPARTIMENTO DI GINECOLOGIA E OSTETRICIA Ruolo della tromboprofilassi in donne con aborto ricorrente: outcome delle successive
Università degli Studi di Roma La Sapienza I FACOLTÀ DI MEDICINA E CHIRURGIA DIPARTIMENTO DI GINECOLOGIA E OSTETRICIA Ruolo della tromboprofilassi in donne con aborto ricorrente: outcome delle successive
N:B. I puntali applicatori/miscelatori sono monouso.
 1. CARATTERISTICHE GENERALI Il gel sbiancante BY X tra 38% è utilizzato per sbiancare denti con discromie. Il gel viene applicato direttamente sui denti. Secondo la direttiva Medical Devices 93/42/CEE
1. CARATTERISTICHE GENERALI Il gel sbiancante BY X tra 38% è utilizzato per sbiancare denti con discromie. Il gel viene applicato direttamente sui denti. Secondo la direttiva Medical Devices 93/42/CEE
Confronto tra l ormone follicolostimolante (FSH) di origine estrattiva umana e quello ricombinante nella procreazione medicalmente assistita
 Confronto tra l ormone follicolostimolante (FSH) di origine estrattiva umana e quello ricombinante nella procreazione medicalmente assistita Position Paper A cura di Achille P. Caputi, Francesco Rossi,
Confronto tra l ormone follicolostimolante (FSH) di origine estrattiva umana e quello ricombinante nella procreazione medicalmente assistita Position Paper A cura di Achille P. Caputi, Francesco Rossi,
SCHEDA TECNICA IMMUNOGLOBULINE ANTI RH(D)
 IMMUNORHO 01.0 DENOMINAZIONE DEL MEDICINALE IMMUNORHO 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: Immunoglobulina umana anti-d (Rho). 1 ml di soluzione iniettabile, ottenuta dalla ricostituzione
IMMUNORHO 01.0 DENOMINAZIONE DEL MEDICINALE IMMUNORHO 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA Principio attivo: Immunoglobulina umana anti-d (Rho). 1 ml di soluzione iniettabile, ottenuta dalla ricostituzione
La terapia con GH ricombinante
 LA SINDROME DI CUSHING IN CONDIZIONI PECULIARI SESSIONE 1. IL CUSHING IN ETA PEDIATRICA La terapia con GH ricombinante Antonio Stigliano Dipartimento di Medicina Clinica e Molecolare Facoltà di Medicina
LA SINDROME DI CUSHING IN CONDIZIONI PECULIARI SESSIONE 1. IL CUSHING IN ETA PEDIATRICA La terapia con GH ricombinante Antonio Stigliano Dipartimento di Medicina Clinica e Molecolare Facoltà di Medicina
Asse ipotalamo-ipofisi-testicolo
 Asse ipotalamo-ipofisi-testicolo Ipotalamo GnRH Ipofisi FSH, LH Testicolo LH cellule di Leydig Testosterone FSH cellule di Sertoli Inibina, MIF Androgeni Testosterone DHEA, Androstenedione Testicolo Cellule
Asse ipotalamo-ipofisi-testicolo Ipotalamo GnRH Ipofisi FSH, LH Testicolo LH cellule di Leydig Testosterone FSH cellule di Sertoli Inibina, MIF Androgeni Testosterone DHEA, Androstenedione Testicolo Cellule
