Liasi senza gruppo prostetico
|
|
|
- Giorgia Gatto
- 7 anni fa
- Visualizzazioni
Transcript
1 Liasi senza gruppo prostetico ALDLASI o ALDLLIASI Enzimi chiave della glicolisi : scinde il glicide originario in due molecole di altri secondari, per essere riconosciuto il substrato deve essere un chetoso marcato in 1 con P e con la L conformazione del 3. Il chetoso riconosciuto con maggiore efficienza è il Fruttoso- 1-P, l aldolasi ha nel sito attivo un gruppo terminale di lisina ed un nucleo di istidina che fa da centro di protonazione. 2 P Fruttoso 1 fosfato + -is 2 -Lys Enzima 1 - attacco nucleofilo dell 2 sul = del chetoso Prof. G. Gilardi - Biological hemistry 2 P + -is + 2 -Lys Enzima 2 formazione del legame di base di Schiff 1
2 Meccanismo 3 protonazione dell con spostamento del doppio legame tra la parte 2-3 a spese del legame 3-4, il 4 resta in forma cationica e con - del mezzo è neutralizzata e diventa gliceraldeide in forma idrata (P) se fossimo partiti da F-1,6-dP o solo gliceraldeide da F-1-P 2 P - + -is -Lys Enzima + Prof. G. Gilardi - Biological hemistry 2
3 Meccanismo 4 l uscita del primo prodotto di reazione modifica il sito attivo ripristino del legame di base di Schiff nella forma originaria e semplice protonazione del carbanione P is + 2 -Lys P Enzima 2 P - + -is 2 -Lys 5 deprotonazione dell azoto e idrolisi del legame di base di Sciff si forma l altro prodotto di reazione. DISSIAETFSFAT : scissione di un monosaccaride in 2 altre unità monocarboniose Enzima Prof. G. Gilardi - Biological hemistry 3
4 Aldolasi Mn dei funghi Stesso discorso vale per le aldolasi nei funghi in cui la destabilizzazione si realizza con legame dativo Mn e poi il legame diviene covalente ; spostamento dell insaturazione tra 2 e 3 a spese del legame 3 4, anche in questo caso si ha GAP idrata per neutralizzazione degli - del mezzo. + -is 2 P + -is Mn Enzima 2 Prof. G. Gilardi - Biological hemistry + P - Mn Enzima gliceraldeide 4
5 Aldolasi Mn dei funghi Il ripristino del legame dativo porta al carbanione sul 3 neutralizzazione per protonazione e liberazione di DISSIAETEFSFAT 2 - P + -is Mn Enzima 2 P + 2 Prof. G. Gilardi - Biological hemistry 5
6 ISMERASI: cl. 5 5 LASSE: ISMERASI A B danno la intertrasformazione di 2 isomeri Sottoclasse: tipo di reazione isomerasica catalizzata Sottosottoclasse:tipi di substrato Prof. G. Gilardi - Biological hemistry 6
7 5. ISMERASI: coenzimi Alcune isomerasi sono proteine coniugate con coenzimi di derivazione vitaminica, dei quali sfruttano le proprietà catalitiche che spesso sono ascrivibili ad una differente classe enzimatica (es. effetto ossidoreduttasico o liasico) Altri enzimi hanno centri catalitici metallici oppure R amino acidi nel sito attivo. el dettaglio vedremo le caratteristiche di reazione di isomerasi che contengono come coenzima: PALP (derivato dalla VITAMIA B6 ): isomerasi specifiche che agiscono sugli aminoacidi DESSSIADESIA BALAMIDE EZIMA (derivato dalla VITAMIA B12): isomerasi delle vie di salvezza metabolica AD + o ADP + (derivati dalla VITAMIA PP): isomerasi di monosaccaridi veicolati da nucleotidi difosfati (es. UDFG: uridindifosfoglucoso) Prof. G. Gilardi - Biological hemistry 7
8 Isomerasi PALP specifiche che agiscono sugli aminoacidi oenzima piridossalfosfato ollegano l aminoacido (attacco 2 su ) legame di base di Schiff formazione del doppio legame transizione verso la struttura chinoide del coenzima con trasporto dei doppi legami il metallo si coordina solo con l dell amino acido. P 2 2 Me 2 R P 2 Base di Schiff Me R 2 -enzima 2 -enzima P 2 Me R + 2 -enzima Prof. G. Gilardi - Biological hemistry 8
9 Isomerasi PALP specifiche che agiscono sugli aminoacidi L altro legame del metallo è R del sito attivo. Il ritorno delle coordinazioni iniziali ha come effetto ribaltamento della stereoisomeria del alfa. In questo modo l amino acido subisce isomerizzazione dalla forma L D reversibilmente. In vivo questa isomerizzazione si ha aa L aa D. Questi enzimi sono situati dulle cosidette vie di salvezza metabolica che servono ad eliminare componenti che potrebbero risultare dannosi per gli intermedi o per i prodotti che formano. La reazione si completa con l idrolisi del legame con liberazione dell aa trasformato. - R P 2 Me 2 -enzima aa L aa D Prof. G. Gilardi - Biological hemistry 9
10 DESSSIADESIA BALAMIDE EZIMA (derivato dalla VITAMIA B12): isomerasi delle vie di salvezza metabolica 2 2 o P Prof. G. Gilardi - Biological hemistry 10
11 DESSSIADESIA BALAMIDE EZIMA (derivato dalla VITAMIA B12): isomerasi delle vie di salvezza metabolica o o. -. Prof. G. Gilardi - Biological hemistry 11
12 Isomerasi B12 che agiscono sulla isomerizzazione dei glicoli X X X + - X Prof. G. Gilardi - Biological hemistry 12
13 Isomerasi B12 che agiscono sulla isomerizzazione dei glicoli Avvenuta la trasposizione : la posizione destabilizzata riceve nuovamente l e l elettrone. Si è ottenuta la forma idrata di un aldeide. Il meccanismo: è cambiato il n di ossidazione dei gruppi interessati () il gruppo alcolico 2 ha il con n di ossidazione = 0.il gruppo alcolico 1 ha n ossid. = a +1. Al termine della reazione l atomo di del gruppo alcolico 2 metilenico 0-2. quello che era gruppo 1 aldeide. Il meccanismo oltre che oxred è anche liasico (aldeide in forma idrata :è come se fosse stata sottratta una molecola d 2 che rappresenta solo la struttura che idrata). Questo E è presente in cellule procariote che riescono a utilizzare i glicoli come fonte di carbonio. Di attualità x la depurazione attraverso ceppi batterici selezionati. I ceppi batterici che esprimono queste isomerasi sono in grado di trasformare glicoli aldeidi poi ossidate a acidi,legati al oa e poi metabolizzati regolarmente secondo i cicli metabolici classici. Prof. G. Gilardi - Biological hemistry 13
14 Isomerasi B12: metil-malonil oa Queste isomerasi sono poi presenti in tutte le cellule quando sono riferite a un substrato particolare il METIL-MALIL-oA. Questo substrato si ottiene in una delle vie di salvezza metabolica. Si esprime nelle vie di salvezza elle cellule eucariote vie di salvezza metabolica intramitocondriale :impedire la formazione di ac. Malonico. I oe B12 isomerasici, quando il substrato è stato riconosciuto dalla apoproteina intervengono togliendo + 1 e- sempre dalla posizione adiacente alla 1 Si forma il carbocatione in α. Il meccanismo del trasferimento riguarda il α destabilizzato e non il 1* ma l atomo di più prossimo in grado di cedere cioè il 3 in sostituzione. Il idrogenato cede l alla struttura carbocationica recupera un sostituente che in questo caso è il 1 bloccato sul oa nuovo α :ex-3 in ramificazione dove è stato trasferito il 1. La catena viene linearizzata:trasposizione di legami. La reazione si completa con la cessione di - al carbocatione sulla catena ormai linearizzata. Dal metilmalonil oa si succinil oa che è un intermedio del ciclo di krebs. Prof. G. Gilardi - Biological hemistry 14
15 Isomerasi B12: metil-malonil oa 3 S oa 3 + S oa S oa S oa 2 Metil malonil oa Succinil oa Prof. G. Gilardi - Biological hemistry 15
16 AD + o ADP + (derivati dalla VITAMIA PP): isomerasi di monosaccaridi veicolati da nucleotidi difosfati (es. uridindifosfoglucoso) i sono altre isomerasi che usano AD o ADP con effetto chiaramente ossidoreduttasico. Queste sono implicate nella trasformazione di molti saccaridi. I monosaccaridi con queste trasformazioni non esistono in forma libera ma veicolati su nucleotidi difosfato. (es. UDFG: uridindifosfoglucoso) 1)ossidazione dell unità monocarboniosa sulla posizione 4 del glucoso che si trasforma in gruppo chetonico. A questo punto: alcune isomerasi possono associare il oe come facevano le ossidoreduttasi classiche e unirsi poi a un altra molecola di oe. Altre danno solo un cambiamento di conformazione e la reazione si ripete in senso simmetrico ma viene a formarsi un isomero (L conf del 4). Altre isomerasi funzionano per trasferimento interno: hanno nel sito attivo il R che puo essere trasferito e poi un Me di transizione con funzione destabilizzante. Prof. G. Gilardi - Biological hemistry 16
17 AD + o ADP + (derivati dalla VITAMIA PP): isomerasi di monosaccaridi veicolati da nucleotidi difosfati L enzima che opera per trasf interno con il suo metallo riconosce l del legame fosfomonoestere presente nel sito attivo prima legame dativo poi covalente si forma il catione fosforico. Il substrato è orientato nel sito attivo dell enzima in modo da avere il gruppo 6 prossimo al sito di fosforilazione,per cui il catione da facilmente attacca elettrofilo nel gruppo alcolicoprimario e si ottiene il glucosio 1,6dP che è intermedio metabolico e può essere liberato. Il gr6 è prossimo al sito di fosforilazione attacco elettrofilo del P+ sull del 6. ambiamento di conformazione che porta a un rovesciamento della parte del substrato nel sito attivo adesso è il terminale 1 a essere orientato Me il Mn riconosce l atomo di del legame fosfoglucosidico e destabilizza col passaggiop del legame dativo a covalente il legame fosfatoossigeno con la formazione del catione fosforico. Il catione fosforico a questo puntodata la prossimità può dare attacco elettrofilo nel gruppo alcolico primario della serina (nel sito attivo). Quindi la serin ritorna nella forma fosforilata. Abbiamo avuto la defosforilazione dell altra posizione del substrato. Il ritorno a legame dativo consente la protonaz del gruppo gluc e scissione da Me. A questo punto il substrato può uscire dal sito attivo dell enzime. Quello che era entyrato come Glu 1 P esce come G6P (o viceversa) a seconda delle necessità metaboliche. Sono dette anche MUTASI rappesentano punti di discriminazione metabolica abbasr tanza importanti. Sono importanti perchè G1P e G6P hanno funzioni diverse. Prof. G. Gilardi - Biological hemistry 17
18 Isomerasi senza oenzima i sono ancora le isomerasi che funzionano senza Me o oe ma solo sfruttando gli effetti di protonazione e deprotonazione. Questi effetti permettono di realizzare l equilibrio fra ALDSI e ETSI importante per mediare gli effetti metabolici. Protonazione del carbonilico promuovendo : la stabilizzazione di doppio legame tra 1 e 2 con il 2 che dissocia un + poi si ha riassestamento a una forma a pot <. Prof. G. Gilardi - Biological hemistry 18
19 LIGASI: cl. 6 Ultima classe di enzimi : catalizzano solo reazioni di formazione di legame, sono irreversibili, questi legami possono essere come per le liasi: ---, S- -P--, nella reazione stechiometrica complessiva partecipa X = composto ad alta energia (ATP o altri). Il legame tra le 2 componenti molecolari si forma sempre a spese di ATP, normalmente abbiamo una mole di ATP per mole di legame, tutte le ligasi visto che usano composti ad alta energia hanno sempre un metallo di transizione nel sito attivo (essenziale). Prof. G. Gilardi - Biological hemistry 19
20 6. LIGASI: coenzimi Tutte le ligasi sono proteine coniugate in quanto contengono un metallo di transizione nel sito attivo (quasi sempre Mn), necessario per destabilizzare il composto ad alta energia Esistono anche -- ligasi che contengono il metallo e un coenzima di derivazione vitaminica: LIGASI A BITIA (VITAMIA ) Prof. G. Gilardi - Biological hemistry 20
21 Schema di reazione Reazioni in due tappe, la prima reazione è reversibile : riguarda la formazione di un intermedio ad alta energia che è un anidride. 1 da acido libero anidride mista 2 l acile è trasferito in una struttra anidridica su ADP liberando P 3 AMP che trasporta l acile la prima metà della reazione è sempre in equilibrio, per realizzarla il metallo riconosce un dei legami anidride dell ATP promuove la formazione del catione fosforico che darà attacco elettrofilo sull del gruppo acido. Seconda metà della reazione : irreversibile, il metallo destabilizza il nuovo legame di anidride formatosi e allora trasforma la struttura carbossilica in struttra cationica in grado di dare attacco elettrofilo sull accettore. Prof. G. Gilardi - Biological hemistry 21
22 -S ligasi -S ligasi : la ligasi accetta il oa che non trasporta acili, il metallo destabilizza i legami di anidride carbossile catione che danno attacco elettrofilo sull S del oa. Prof. G. Gilardi - Biological hemistry 22
23 - ligasi Altro esempio di ligasi : saccaridi amino monosaccaridi. Lo stesso metallo dopo questa trasf. ei rapporti substrato enzima riconosce l in 2 che fa parte del substrato e lega il P nuova destabilizzazione e allontanamento formazione del catione in 2. osubstrato di questa ligasi è la glutammina, ha sul terminale, legato al gamma il gruppo semiamidico : può cedere questo R amminico sulla posizione 2 aminazione. Il gruppo 2 dà attacco nucleofilo sul catione che si è originato dalla rottura dell del P Galattoso galattosamina a questo punto su questo substrato possono intervenire transferasi. Prof. G. Gilardi - Biological hemistry 23
24 --- ligasi Esempio di - ligasi: importante per la sintesi proteica : ligasi che fissano ciascuno amino acido sul proprio RA di trasferimento 1 reazione : destabilizzazione del primo legame dianidride formazione di Ppi formazione catione fosforico sul P del AMP che dà attacco elettrofilo sull del carbossile aminoacil adenilato, questi si formano facilmente perchè il sito attivo dell aenzia può discriminare tra aa la prima metà della reazione su aa molto simili può portare a sovrapposizione fino al 30%. La correzione avviene con la seconda reazione, questa ha come cosubstrato quell t-ra che sul 3 terminale ha la sequenza A, si ha riconoscimento specifico, l errore è di 1\3000 o 1\8000 per trasferimento di aa simili. Il metallo destabilizza l del legame anidridico formazione del catione sul carbossile dell aa questo darà attacco sul 2 o sul 3 irreversibili. Si elimina AMP. Prof. G. Gilardi - Biological hemistry 24
25 PLIULETIDE LIGASI Polinucleotidi a vario grado di polimerizzazione. Realizzano la saldatura 3, 5 per esempio trasformando la molecola da lineare a circolare o unire 2 segmenti per dare un segmento di ampiezza >. Sono usate nei laboratori dove si utilizzano tecniche di biologia molecolare per saldare frammenti. In vivo il ruolo di completare le catene più lunghe e intervengono nella riparazione del DA. i può essere la riorganizzazione di alcuni tratti, per es. con si ritagliano frammenti non corretti ligasi legano il frammento corretto. Le ligasi sono dei Me-Enzimi. perano sui frammnti con 3 libero e 5 fosforilato bisogna che agiscano prima E di classe 2 (IASI), che sono specifiche per riconoscere i 5 e fosforilarli. Le ligasi riconoscono e ospitano il terminale fosfomonestereo in 5. Solo adesso parte la reazione ligasica vera e propria. osubstrato è rappresentato sempre da ATP. Il Mn riconosce l del primo legame lo destabilizza formazione del fosfato cationico liberando pirofosfato. In mancanza di ATP può fornire AMP+ ad esempio il AD. Prof. G. Gilardi - Biological hemistry 25
26 PLIULETIDE LIGASI Il fosfato da attacco elettrofilo sul fosfato in 5 si ha cosi la prima parte della reazione quella reversibile che marca il terminale 5 con una struttura pirofosforica In conseguenza di questi cambiamenti muta la conformazione del sito attivo che solo a questo punto può accogliere il terminale 3 libero. Il Mn in conseguenza di cambiamenti della conformazione del sito si trova ad essere molto vicino al legamedianidride. Formaz leg dativo e poi covalente che interrompe il legame P- e da catione P+. Questo da attacco elettrofilo sull del terminale 3 libero promuovendo l unione dei 2 terminali. Quando cambiano i rapporti con il Mn viene rilasciato AMP. Reazione in 2 tempi: 1 - passaggio fosfomonoestere terminale a struttura di anidride pirofosforica (reversibile). 2 -irreversibile destabilizza della struttura, formazione del catione fosforico e attacco nella struttura 3. Prof. G. Gilardi - Biological hemistry 26
27 LIGASI A BITIA (VITAMIA ) La biotina contiene una struttura eterocliclica fatta da 2 nuclei condensati. La posizione 2 sulla parte tiazolidinica lega una catena -valerianica; questa serve per unire l Enz. Unione: leg carbonilico con un residuo di Lys e il complesso Lys-Biotina viene indicato come BIITIA. el sito attivo dell enzima la struttura eterociclica della biotina è prossima a un residuo imidazolico di istidina. I 2 eterocicli sono vicini, ci sono Me cofattori interposti l interazione fa si che l 1 sia in forma di AZTUR nel sito attivo dell Enz. Mn Lys-E - Lys-E S 3 S 3 Prof. G. Gilardi - Biological hemistry 27
28 LIGASI A BITIA La parte reversibile della reazione ligasica è preceduta da una reazione con un enzima ausiliario. arbonicoanidrasi ha come Me lo Zn e determina l addizione di 2 sulla 2 acido carbonico in quantità >> a quelle che si avrebbe per l eq spontaneo tra i due reagenti. -substrato per la reazione è l ac carbonico che ha accesso al sito attivo dell Enz. Grazie all Mn il fosforile+ da attacco elettrofilo sull dell acido carbonico carbossilfosfato. Questo carbossilfosfato ha: il porta una δ+ nel sito ativo dell Enz.:s truttura che può subire attacco dello ione azoturo forma leg covalente a spese degli e-di legame - del legame anidridico. Liberazione di ac.ortofosforico. Il carbossile si trasf.sull 1. Prof. G. Gilardi - Biological hemistry 28
29 LIGASI A BITIA A ATP ADP + P - - arbossil fosfato Lys-E S P - Prof. G. Gilardi - Biological hemistry 29
30 LIGASI A BITIA Questa è la parte reversibile della reazione (si può ottenere la retrocessione degli equilibri). Questi cambiamenti a livello del sito attivo fanno abbassare la Kd delle ligasi per il oa : queste ligasi possono interagire col oa che accettano non nella forma libera ma in quello con l acile. Questo è un 1 gruppo di - ligasi biotina-dipendenti e dipendenti dal oa. Il oa si lega vicino al sito catalitico (in un sito specifico) e il S che porta l acile è abbastanza prossima come orientamento Mn che alla struttura carbossibiotina. egli Acil oa la struttura è di impedimento alla libera risonanza: il = non può risuonare sulla posizione -S ma solo sull altra posizione.sul α viene a concentrarsi una negativa. Questa struttura carbanionica viene a trovarsi allineata su 1 legame orientato del Mn e prossimo al legame che il Mn da col carbonile legato col = legame. Il Mn destab.il legame - carbossile in forma cationica che da attività nucleofila sul α. Abbiamo la carbossilazione del substrato. Prof. G. Gilardi - Biological hemistry 30
31 1 gruppo di - ligasi biotina-dipendenti Lys-E + - Lys-E S 3 Mn S 3 X---S-oA X---S-oA Prof. G. Gilardi - Biological hemistry 31
32 Sintesi del Metil-malonil oa Lys-E + - Lys-E S 3 Mn S S-oA Propionil oa 3 ---S-oA Metil malonil oa Prof. G. Gilardi - Biological hemistry 32
33 Meccanismo biotina l E ritorna nella sua struttura inziale pronto per un nuovo ciclo di reazioni. Per le cellule procariote non ci sono problemi. Per le cellule eucariote c è il problema della compartimentazione : il Malonil-oA è tossico nel compartimento intramitocondriale. Questa ligasi è però nel comp extram. E la molecola che permette la sintesi di acili a lunga catena e cioè di materiale lipidico. Prof. G. Gilardi - Biological hemistry 33
34 -- ligasi Esiste un gruppo di - ligasi che usano come osubstrato per la seconda reazione acil oa e distribuita intramitocondrialmente rappresenta una via di salvezza metabolica. Le ligasi a biotina e l isomerasi B12 dip operano insieme per succinil oa. Prof. G. Gilardi - Biological hemistry 34
35 2 gruppo di - ligasi biotina-dipendenti ltre a questa prima categoria - ligasica è aciloa dipendenti. Esiste un secondo gruppo che non ha sito interagente con oa ma accetta nel sito attivo degli α-chetoacidi. Lys-E S 3 3 Mn-E Mn-E Mn-E Prof. G. Gilardi - Biological hemistry 35
36 Piruvato carbossilasi il trasf avverrà sulla posiz β. La simmetria dei legami del Mn fa si che da 1 substrato e dall altra col oe. L interazione col substrato riguarda un legame dativo Me-. β può accettare il carbossile. Questo carbanione ha un valore di elettronegatività << del α carbanionico. L altro legame del Mn non riguarda solo più 1 legame orientato una coppia di legami dativi orientati del carbossile e sostituente in posiz 2. Abbiamo prima delle interazioni che promuovono il trasferimento deel Mn dall atomo all atomo di di con un aumento di circa un fattore 2 della δ+ sul. A questo punto si realizza la vera e propria destabilizzazione del legame carbossile formaz del carbossilecatione il suo attacco sul carbanione. Il carbossile è trasferito sull ac.piruvico si ha ac.ossalacetico. Questo è l E chiave della gluconeogenesi (piruvatocarbossilasi)la strutt 4 dell ac ossalacetico è importante è l unità base di entrata delciclo gluconeogenico. In tutti i casi il n do ox del cambia in riduz.; il carbossile è cosi inserito stabilmente nella molecola del substrato per dera i prodotti finali. Prof. G. Gilardi - Biological hemistry 36
37 2 gruppo di - ligasi biotina-dipendenti: schema del meccanismo - δ + Lys-E S 3 Acido piruvico Acido ossalacetico Prof. G. Gilardi - Biological hemistry 37
38 Lesione biochimica da carenza di VIT alterazioni del metabolismo dei lipidi e dei glicidi. La reazione piruvato carbossilasica parziale blocco di2 vie metaboliche. Questo a livello macroscopico da particolare danno ai tessuti nervosi,muscolari ed epiteliali. Prof. G. Gilardi - Biological hemistry 38
39 Vitamina F Gli acidi LILEI, LILEI e ARAIDI, con l acido LUPADI (sei doppi legami) sono definiti acidi poliinsaturi. Fanno parte del cosidetto MPLESS VITAMII F che serve a proteggere le membrane biologiche dall effettto ossidativo dell ossigeno Infatti sono ATSSIDATI VITAMIII: la loro porzione poliinsatura si ossida più facilmente dei lipidi di membrana e perciò fungono da cattura radicali Prof. G. Gilardi - Biological hemistry 39
40 Vitamina F AID LILEI 9,12 AID LILEI 9,12, 15 L acido linoleico è un acido grasso insaturo che è essenziale nei mammiferi, che non sono in grado di sintetizzare doppi legami oltre la posizione 9. Pertanto l acido linoleico e l acido linolenico sono essenziali nella dieta dei mammiferi poichè hanno doppi legami in posizione 9, 12 e 9, 12 e 15 rispettivamente. L acido linoleico è un importante precursore dell acido arachidonico, che a sua volta è un precursore degli eicosanoidi, una classe che comprende le prostaglandine e i leucotrieni Prof. G. Gilardi - Biological hemistry 40
41 Vitamina F AID ARAIDI (AID cis-5,8,11,14-eisatetraei) L AID ARAIDI è un acido grasso poliinsaturo che è un importante precursore degli EISAIDI, che comprendono le PRSTAGLADIE, I LEUTRIEI e i TRMBSSAI. Prof. G. Gilardi - Biological hemistry 41
42 Vitamina D 1,25 Dihydroxycholecalciferol - 1,25()D3 The most abundant form of vitamin D is D3, called cholcalciferol. Vitamin D is not technically a vitamin, because it is not required in the diet. It arises from uv-photolysis of 7-dehydrocholesterol, an intermediate in cholesterol biosynthesis (see here). Vitamin D regulates calcium and phosphorus metabolism, particularly the synthesis of the inorganic matrix of bone, which consists largely of calcium phosphate. D3 undergoes two successive hydroxylations catalyzed by mixed-function oxidases. The first occurs at carbon 25 in liver. When calcium levels are low, hydroxylation occurs at carbon 1, yielding the active form, 1,25()D3, which stimulates osteoblasts to take up calcium. In the intestine, 1,25()D3 stimulates transcription of a protein that stimulates calcium absorption into the bloodstream. When calcium levels are adequate, hydroxylation occurs instead at carbon 24, yielding the inactive 24,25()D3 form. Prof. G. Gilardi - Biological hemistry 42
43 Vitamina D Vitamina D3 Vitamina D2 Prof. G. Gilardi - Biological hemistry 43
Vitamina C O O O O + 2H
 Vitamina + 2 La vitamina è la forma dienolica del γ-lattone dell acido gulonico. In vivo le reazioni sono spostate verso destra e la vitamina è un riducente. E coenzima di ossigenasi: Vit 2 + 2 vit + 2
Vitamina + 2 La vitamina è la forma dienolica del γ-lattone dell acido gulonico. In vivo le reazioni sono spostate verso destra e la vitamina è un riducente. E coenzima di ossigenasi: Vit 2 + 2 vit + 2
La via glicolitica. Caratteristiche generali Le reazioni della via glicolitica. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche La via glicolitica Caratteristiche generali Le reazioni della via glicolitica Francesca
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche La via glicolitica Caratteristiche generali Le reazioni della via glicolitica Francesca
Cap.16 GLICOLISI. Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP H 2 O 2 NAD + 2 NADH + 2H +
 Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
CLASSIFICAZIONE ENZIMI
 CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
Transferasi che hanno come coenzima FOSFOPANTOTEINA E COENZIMA A (derivati dalla VITAMINA B3 )
 Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
Transferasi che hanno come coenzima FSFPANTTEINA E ENZIMA A (derivati dalla VITAMINA B3 ) Altre transferasi hanno come oe: Vitamina B3 (sintetizzata in vegetali e molti procarioti anche ospiti dell intestino
Transferasi che hanno come coenzima PIRIDOSSAL FOSFATO o PALP (derivato dalla VITAMINA B6 )
 Transferasi che hanno come coenzima PIRIDSSAL FSFAT o PALP (derivato dalla VITAMIA B ) Altre transferasi hanno come oe: Vitamina B 2 2 1 2 Prof. G. Gilardi - Biological hemistry 1 Transferasi che hanno
Transferasi che hanno come coenzima PIRIDSSAL FSFAT o PALP (derivato dalla VITAMIA B ) Altre transferasi hanno come oe: Vitamina B 2 2 1 2 Prof. G. Gilardi - Biological hemistry 1 Transferasi che hanno
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato
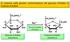 2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
2 a reazione della glicolisi: isomerizzazione del glucosio 6-fosfato in fruttosio 6-fosfato Glucosio 6-fosfato isomerasi Glucosio 6-fosfato anomero α Fruttosio 6-fosfato anomero α Glucosio 6-fosfato Fruttosio
Seminario. Ciclo di Krebs 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A
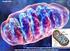 Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Esempi di quiz di biochimica. 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio
 Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Classe 4: liasi. Prof. G. Gilardi - Biological Chemistry
 lasse 4: liasi 1) AH2+B A+BH2 ossidoreduttasi (trasf. Di H+e-) 2) A+B AB+ tranferasi (trasf. Di gruppi) 3) AB+H2 A+B idrolasi (legami:scissione rev idrolitica) LIAI(enzimi di 4 classe) 4) AB A+B La reazione
lasse 4: liasi 1) AH2+B A+BH2 ossidoreduttasi (trasf. Di H+e-) 2) A+B AB+ tranferasi (trasf. Di gruppi) 3) AB+H2 A+B idrolasi (legami:scissione rev idrolitica) LIAI(enzimi di 4 classe) 4) AB A+B La reazione
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Prima di essere ossidati. gli ACIDI GRASSI devono essere attivati. (cioè legati al CoA) e poi entrare nel mitocondrio
 Prima di essere ossidati gli ACIDI GRASSI devono essere attivati (cioè legati al CoA) e poi entrare nel mitocondrio L enzima acil CoA sintetasi (= acido grasso tiokinasi) sta sulla membrana mitocondriale
Prima di essere ossidati gli ACIDI GRASSI devono essere attivati (cioè legati al CoA) e poi entrare nel mitocondrio L enzima acil CoA sintetasi (= acido grasso tiokinasi) sta sulla membrana mitocondriale
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
Respirazione cellulare: processi molecolari medianti i quali le cellule consumano O 2 e producono CO 2
 AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
PIRIDOSSALE-FOSFATO (PLP)
 PIRIDOSSALE-FOSFATO (PLP) Deriva dalla famiglia delle Vitamine B 6 (piridossale, piridossina) Il PLP è il gruppo prostetico di enzimi che catalizzano transamminazione, decarbossilazione, racemizzazione
PIRIDOSSALE-FOSFATO (PLP) Deriva dalla famiglia delle Vitamine B 6 (piridossale, piridossina) Il PLP è il gruppo prostetico di enzimi che catalizzano transamminazione, decarbossilazione, racemizzazione
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Degradazione degli acidi grassi
 Degradazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500 nm. Mobilizzazione dei triacilgliceroli
Degradazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500 nm. Mobilizzazione dei triacilgliceroli
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
METABOLISMO OSSIDATIVO
 METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
Coenzimi. Ioni essenziali. Molti coenzimi hanno come precursori le vitamine.
 COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Introduzione allo studio del metabolismo Parte I
 Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Cap.21 ANABOLISMO DEI LIPIDI
 Cap.21 ANABOLISMO DEI LIPIDI Sintesi di Acidi Grassi I grassi depositati come riserva nel nostro organismo non provengono soltanto dai grassi alimentari normalmente i grassi alimentari rappresentano una
Cap.21 ANABOLISMO DEI LIPIDI Sintesi di Acidi Grassi I grassi depositati come riserva nel nostro organismo non provengono soltanto dai grassi alimentari normalmente i grassi alimentari rappresentano una
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE
 BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
(2 x) (2 x) (2 x) Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi. Gliceraldeide 3-fosfato deidrogenasi
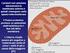 Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
Il NADH prodotto in questa reazione DEVE essere ri-ossidato affinché la glicolisi non si fermi (2 x) (2 x) Gliceraldeide 3-fosfato Fosfato inorganico Gliceraldeide 3-fosfato deidrogenasi Reazione di ossidoriduzione:
GLICOLISI ADP ATP. Condizioni aerobiche. Condizioni anaerobiche ATP
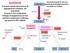 GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
GLICOLISI È la parte iniziale del processo di degradazione ossidativa dei carboidrati. Durante la loro ossidazione l energia immagazzinata nel loro scheletro carbonioso è utilizzata per produrre ATP e
La quantità di glu presente nei liquidi extracellulari è di circa 20g, 80kcal.
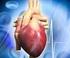 I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
I principali nutrienti metabolici sono il glucosio e gli acidi grassi. In circostanze normali il glucosio è l unico nutriente che possa essere utilizzato dal cervello. E anche utilizzato preferenzialmente
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Cap.21 CATABOLISMO DEI LIPIDI
 Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Carboidrati! Oligosaccaridi Polisaccaridi. B) Carboidrati complessi
 Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
GLUCONEOGENESI fegato, corteccia renale
 GLUCONEOGENESI fegato, corteccia renale Glucosio 6 fosfato Energia Fosfoenolpiruvato Ciclo dell acido citrico Piruvato Glicerolo Lattato Amminoacidi glucogenici Triacilgliceroli Esochinasi (Glucochinasi)
GLUCONEOGENESI fegato, corteccia renale Glucosio 6 fosfato Energia Fosfoenolpiruvato Ciclo dell acido citrico Piruvato Glicerolo Lattato Amminoacidi glucogenici Triacilgliceroli Esochinasi (Glucochinasi)
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
Mobilizzazione dei trigliceridi di riserva IDROLIZZATI DA LIPASI IN GLICEROLO E ACIDI GRASSI
 METABOLISMO DEGLI ACIDI GRASSI Lipidi introdotti con gli alimenti Mobilizzazione dei trigliceridi di riserva IDROLIZZATI DA LIPASI IN GLICEROLO E ACIDI GRASSI Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER,
METABOLISMO DEGLI ACIDI GRASSI Lipidi introdotti con gli alimenti Mobilizzazione dei trigliceridi di riserva IDROLIZZATI DA LIPASI IN GLICEROLO E ACIDI GRASSI Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER,
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH
 Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
6 H 2. con G=-686 kcal/mole di H 12 O 6 O + 6 CO O 2. glucosio La respirazione avviene in tre stadi principali; ognuno di questi
 La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
glicogeno Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVATO glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVATO glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Cofattori e vitamine
 Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Esercitazione Esempi di domande del 1 test
 Esercitazione Esempi di domande del 1 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Esercitazione Esempi di domande del 1 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Ossidazione del glucosio
 Ossidazione del glucosio Vie metaboliche all uso del glucosio Glicolisi e Fermentazioni 1 Reazione di ossidazione C 6 H 12 O 6 + 6 O 2 => 6 CO 2 + 6 H 2 O + 686 Kcal/mole Il glucosio reagisce direttamente
Ossidazione del glucosio Vie metaboliche all uso del glucosio Glicolisi e Fermentazioni 1 Reazione di ossidazione C 6 H 12 O 6 + 6 O 2 => 6 CO 2 + 6 H 2 O + 686 Kcal/mole Il glucosio reagisce direttamente
Respirazione cellullare
 Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Il metabolismo ATP. concetti di base e disegno generale
 Il metabolismo ATP concetti di base e disegno generale Eg e funzioni cellulari Le cellule necessitano di un costante apporto di Eg per svolgere diverse funzioni: lavoro meccanico lavoro elettrico trasporto
Il metabolismo ATP concetti di base e disegno generale Eg e funzioni cellulari Le cellule necessitano di un costante apporto di Eg per svolgere diverse funzioni: lavoro meccanico lavoro elettrico trasporto
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una:
 1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI.
 IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI. reazioni enzimatiche organizzate in vie discrete H recettore procedono attraverso diversi
IL METABOLISMO Somma delle reazioni che convertono sostanze nutrienti in fonti di ENERGIA o PRODOTTI COMPLESSI. reazioni enzimatiche organizzate in vie discrete H recettore procedono attraverso diversi
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Esercitazione Esempi di domande del 2 test
 Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Il laboratorio di Biochimica si svolgerà nei seguenti giorni;
 Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
Principali vie di utilizzo del Glucosio
 Principali vie di utilizzo del Glucosio GLICOGENO (Polimero di riserva) Polimero lineare e ramificato di glucosio che si accumula nel fegato e nel muscolo. Nella catena lineare le molecole di glucosio
Principali vie di utilizzo del Glucosio GLICOGENO (Polimero di riserva) Polimero lineare e ramificato di glucosio che si accumula nel fegato e nel muscolo. Nella catena lineare le molecole di glucosio
IL METABOLISMO ENERGETICO
 IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
AGISCONO NEL SISTEMA NAVETTA 2 ISOFORME DELL ENZIMA: UNA FORMA MITOCONDRIALE ( MEMBRANA MIT. INTERNA) FAD-dipendente
 METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
3) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
BIOCHIMICA. Prof. Stefania Hanau
 BIOCHIMICA Prof. Stefania Hanau Il metabolismo ATP concetti di base e disegno generale Come fanno le cellule ad estrarre Energia dall ambiente che le circonda? Le cellule necessitano di un costante flusso
BIOCHIMICA Prof. Stefania Hanau Il metabolismo ATP concetti di base e disegno generale Come fanno le cellule ad estrarre Energia dall ambiente che le circonda? Le cellule necessitano di un costante flusso
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Una panoramica del ciclo dell acido ciclico
 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Enzimi: catalizzatori biologici
 Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Reazione prossima all equilibrio Molto rapida. Trioso-fosfato isomerasi
 5 a reazione Delle 2 molecole prodotte dalla scissione del fruttosio 1,6-bisfosfato solo la gliceraldeide 3-P è il substrato della successiva reazione della glicolisi, perciò il diidrossiacetonefosfato
5 a reazione Delle 2 molecole prodotte dalla scissione del fruttosio 1,6-bisfosfato solo la gliceraldeide 3-P è il substrato della successiva reazione della glicolisi, perciò il diidrossiacetonefosfato
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
metano alcool metilico formaldeide acido formico CO 2
 -4-2 0 +2 +4 metano alcool metilico formaldeide acido formico CO 2 + ridotto + ossidato + ossidato Glicolisi 2 Glucosio Piruvato Glicolisi Glucosio + 2NAD + 2 piruvato + 2NADH + 2H + ΔG = -146 kj/mol 2ADP
-4-2 0 +2 +4 metano alcool metilico formaldeide acido formico CO 2 + ridotto + ossidato + ossidato Glicolisi 2 Glucosio Piruvato Glicolisi Glucosio + 2NAD + 2 piruvato + 2NADH + 2H + ΔG = -146 kj/mol 2ADP
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia
 I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
Appunti di biologia LA GLICOLISI. Giancarlo Dessì Licenza Creative Commons BY-NC-SA
 Appunti di biologia LA GLILISI Giancarlo Dessì http://www.giand.it Licenza reative ommons BY-N-SA BY: Attribuzione - N: Non commerciale - SA: ondividi allo stesso modo GLILISI o VIA METABLIA DI EMBDEN-MEYERF-PARNAS
Appunti di biologia LA GLILISI Giancarlo Dessì http://www.giand.it Licenza reative ommons BY-N-SA BY: Attribuzione - N: Non commerciale - SA: ondividi allo stesso modo GLILISI o VIA METABLIA DI EMBDEN-MEYERF-PARNAS
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
G i l i A ut u otro r fi G i l i E t E ero r tro r fi I F ototro r fi I C he h mo m tro r fi i us u a s no C e h moete t ro r tr t o r fi
 Organismi differenti utilizzano differenti modalità per ottenere carbonio ed energia: carbonio: Gli Autotrofi usano CO 2 Gli Eterotrofi usano carbonio organico energia: I Fototrofi usano la luce I Chemotrofi
Organismi differenti utilizzano differenti modalità per ottenere carbonio ed energia: carbonio: Gli Autotrofi usano CO 2 Gli Eterotrofi usano carbonio organico energia: I Fototrofi usano la luce I Chemotrofi
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono:
 Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
Le tre funzioni termodinamiche che descrivono le variazioni di energia che avvengono in una reazione sono: G= energia libera di Gibbs H= entalpia S= entropia ΔG = ΔH TΔS ΔH < 0 ΔS > 0 Condizione tipica
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Stampa Preventivo. A.S Pagina 1 di 8
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Catabolismo dei carboidrati Glicolisi
 Catabolismo dei carboidrati Glicolisi Principali vie di utilizzo del Glucosio L estrazione dell energia dai composti organici può essere divisa in tre stadi Metabolismo del glucosio C 6 H 12 O 6 + 6O 2
Catabolismo dei carboidrati Glicolisi Principali vie di utilizzo del Glucosio L estrazione dell energia dai composti organici può essere divisa in tre stadi Metabolismo del glucosio C 6 H 12 O 6 + 6O 2
catalizzatori biologici RUOLO DEGLI ENZIMI: 16/03/15
 I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
Acido maleico anidride maleica acido ftalico andidride ftalica
 Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Le anidridi si ottengono per disidratazione da due molecole di acido (la reazione è particolarmente facile per ottenere anidridi cicliche) Acido maleico anidride maleica acido ftalico andidride ftalica
Mitocondri. -sono visibili al MO (Ø 0,5 µ e lunghezza da 1 a 6 µ) -assenti nei batteri e presenti in tutte le cellule eucariotiche
 Mitocondri sono organelli deputati alla produzione dell energia, capaci di ossidare i prodotti dell assorbimento intestinale degradandoli e di convertire l energia liberata in ATP processo chiamato respirazione
Mitocondri sono organelli deputati alla produzione dell energia, capaci di ossidare i prodotti dell assorbimento intestinale degradandoli e di convertire l energia liberata in ATP processo chiamato respirazione
