Temperatura e Calore.
|
|
|
- Cristiano Giordano
- 5 anni fa
- Visualizzazioni
Transcript
1 emeratura e Calore
2 emeratura e Calore Stati di Aggregazione emeratura Scale ermometriche Dilatazione ermica Leggi dei gas: La rima legge di Gay-Lussac ( costante) La seconda legge di Gay-Lussac ( costante) La legge di Boyle ( costante) Equazione di Stato dei Gas Perfetti Il Calore L Equilibrio ermico La Proagazione del Calore I Passaggi di Stato
3 Gli Stati di Aggregazione La materia si trova essenzialmente in 3 stati di aggregazione: Solido: Forma e olume rorio Condensati Liquido: Forma del reciiente e olume rorio Fluidi Gassoso o Aeriforme: Forma e olume del reciiente Allo stato solido le articelle costituenti la materia (atomi, molecole o ioni) si disongono in modo ordinato e comatto, con limitate ossibilità di muoversi le une risetto alle altre. SOLIDO Allo stato liquido le articelle costituenti la materia si disongono in modo disordinato e ossono scorrere le une sulle altre, con medie ossibilità di muoversi le une risetto alle altre. LIQUIDO Allo stato gassoso le articelle costituenti la materia si disongono in modo estremamente disordinato, con elevata ossibilità di muoversi le une risetto alle altre. GASSOSO
4 emeratura Le articelle che comongono ogni sostanza, qualunque sia lo stato di aggregazione in cui si trova, sono in continuo movimento. ale fenomeno si chiama agitazione termica. La temeratura è un indice del grado di agitazione termica: quanto maggiore è l agitazione termica, tanto maggiore è la temeratura di una sostanza. E una delle 7 grandezze fisiche fondamentali. Storicamente il concetto di temeratura nasce come tentativo di quantificare le nozioni comuni di "caldo" e "freddo". Gli strumenti er misurare la temeratura sono i termometri, basati sul fenomeno della dilatazione termica. Esistono diverse scale termometriche, le iù usate sono la Kelvin e la Celsius.
5 Scale ermometriche Celsius, Kelvin Le scale termometriche iù diffuse sono la scala kelvin (usata nel S.I.) e la scala Celsius (usata nella vita comune). Le due scale differiscono essenzialmente nel valore assegnato allo zero, cioè al unto iniziale, della scala: La scala Celsius è tarata in base a unti fissi: la temeratura del ghiaccio che fonde, cui attribuiamo il valore C, e la temeratura dell acqua che bolle, cui attribuiamo il valore C. L intervallo così individuato viene diviso in arti di cui ognuna vale quindi C. La scala Kelvin è tarata in base allo zero assoluto, che è la temeratura teorica iù bassa cui uò arrivare la materia, il cui valore in gradi Celsius è -73,5 C. Il valore di un grado Kelvin è identico a quello Celsius, cioè K = C. CELSIUS Acqua Bollente K C Ghiaccio Fondente Zero Assoluto KELIN 73,5 NOA: Nella scala Kelvin non ossono esserci valori di temeratura negativi in quanto ha come zero la temeratura iù bassa che ossa mai esistere.
6 Dilatazione ermica La dilatazione termica è il fenomeno fisico er cui in un coro (liquido, gassoso o solido) si verifica un aumento di volume all'aumentare della temeratura. Qualitativamente questo fenomeno si uò giustificare nel seguente modo: qualsiasi aumento di temeratura di un coro è accomagnato da un aumento dell agitazione termica delle sue molecole. Ciò determina un incremento della distanza tra le molecole, er cui il risultato finale si traduce in un aumento del volume. Nel caso di una diminuzione della temeratura la situazione risulta erfettamente simmetrica a quella aena descritta ed il risultato finale consiste in una diminuzione del volume del coro. La dilatazione termica dei materiali crea seri inconvenienti in molte alicazioni tecnologiche. Nella rogettazione di macchinari, edifici, onti occorre lasciare adeguati sazi liberi tra i diversi comonenti, affinché i materiali (sorattutto i metalli) ossano dilatarsi, senza deformare la struttura. Un classico esemio sono i binari ferroviari. Ma la dilatazione termica non è necessariamente un fenomeno negativo, infatti ad esemio è alla base del funzionamento dei termometri!
7 Dilatazione ermica Solidi: Dilatazione Lineare e olumica Ogni solido ha semre 3 dimensioni, ma uò accadere che una delle dimensioni sia reonderante risetto alle altre (si ensi ad es. ad un filo), in tal caso anche la dilatazione avviene revalentemente in quella dimensione e si arla quindi di dilatazione lineare, la cui formula è: L L L LF L ariazione di lunghezza F ariazione di temeratura con L Lunghezza Iniziale Coefficiente di dilatazione lineare Quando il solido si svilua in modo omogeneo nelle 3 dimensioni la dilatazione avviene in tutte le direzioni, si arla quindi di dilatazione volumica, la cui formula è: k F ariazione di volume F ariazione di temeratura con olume Iniziale k Coefficiente di dilatazione volumica (k 3)
8 Dilatazione ermica Liquidi e Gas La dilatazione termica agisce anche nei liquidi e nei gas, seguendo la stessa legge della dilatazione volumica dei solidi: k L unica differenza è che il coefficiente di dilatazione termica k è, er il liquidi e ancor iù er i gas, maggiore di quello dei solidi. Da ciò deriva che, a arità di variazione di temeratura, i liquidi si dilatano iù dei solidi ed i gas iù dei liquidi. Qualitativamente ciò si uò giustificare considerando che nei liquidi, e ancor iù nei gas, le articelle che li comongono sono fra loro legate iù debolmente risetto a quelle dei solidi, quindi ossono allontanarsi maggiormente fra loro.
9 Leggi dei Gas Nel caso dei gas la dilatazione diende non solo dalle variazioni di temeratura ma anche dalle variazioni di ressione. Per oter valutare il comortamento del gas dobbiamo inserirlo in un reciiente chiuso che ci ermetta di agire e di controllare gli andamenti delle grandezze fisiche PRESSIONE, OLUME e EMPERAURA. Le trasformazioni iù interessanti che uò subire un gas sono quelle che si ottengono tenendo costante una delle tre grandezze,, e facendo variare le altre due: COSANE ARIANO RASFORMAZIONE, ISÒBARA, ISOCÒRA, ISOÈRMA
10 Leggi dei Gas La rima legge di Gay-Lussac ( costante) È evidenza serimentale che, a ressione costante, un gas riscaldato si dilata (aumenta di volume) e raffreddato si contrae (diminuisce di volume). Ciò vale er ressioni non troo elevate e er temerature non troo rossime a quella di liquefazione del gas, ovvero quando il gas si comorta come un gas ideale. ( α t) o olume a C o dove t emeratura in C α Coefficiente di dilatazione volumica Δ - ( α t ) - ( α t ) α t - t α Δt Δ α Δt NASA's Glenn Research Center Prima Legge di Gay-Lussac (legge di Charles): In una trasformazione isobara ( costante) la variazione di volume è direttamente roorzionale alla variazione di temeratura t.
11 Leggi dei Gas La rima legge di Gay-Lussac ( costante) Il coefficiente di dilatazione volumica a è uguale er tutti i gas ed è costante: 3 o a 3,66 C o 73,5 C Pertanto, fissato il volume iniziale, la relazione tra e (in gradi Celsius) è lineare. Se esrimiamo la temeratura in kelvin la I legge di Gay-Lussac uò essere esressa in modo ancora iù semlice e il raorto tra e (in kelvin) risulta costante. Pertanto e (in kelvin) sono tra loro direttamente roorzionali ed il grafico è una retta assante er l origine. ( α t) costante, Direttamente Proorzionali (K)
12 Leggi dei Gas La seconda legge di Gay-Lussac ( costante) È evidenza serimentale che, a volume costante, se riscaldiamo un gas la ressione aumenta e raffreddandolo diminuisce. Ciò vale er ressioni non troo elevate e er temerature non troo rossime a quella di liquefazione del gas, ovvero quando il gas si comorta come un gas ideale. ( α t) o Pressione a C o dove t emeratura in C α Coefficiente di dilatazione volumica Δ - ( α t ) - ( α t ) α t - t α Δt Δ α Δt Seconda Legge di Gay-Lussac: In una trasformazione isocora ( costante) la variazione di ressione è direttamente roorzionale alla variazione di temeratura t.
13 Leggi dei Gas La seconda legge di Gay-Lussac ( costante) Il coefficiente di dilatazione volumica a è, come nel caso recedente, uguale er tutti i gas ed è costante. Pertanto, fissata la ressione iniziale, la relazione tra e (in gradi Celsius) è lineare. ( α t) Se esrimiamo la temeratura in kelvin la II legge di Gay-Lussac uò essere esressa in modo ancora iù semlice e il raorto tra e (in kelvin) risulta costante. Pertanto e (in kelvin) sono tra loro direttamente roorzionali ed il grafico è una retta assante er l origine. emeratura in K dove Pressione iniziale emeratura iniziale in K (K)
14 Leggi dei Gas La legge di Boyle ( costante) È evidenza serimentale che, a temeratura costante, se riduciamo il volume di un gas la sua ressione aumenta e se lo aumentiamo la ressione diminuisce. Legge di Boyle: In una trasformazione isoterma ( costante) la ressione e il volume del gas sono inversamente roorzionali, cioè variano mantenendo costante il loro rodotto. Pressione iniziale costante dove olume iniziale NASA's Glenn Research Center
15 Equazione di Stato dei Gas Perfetti Si definisce Gas Ideale o Gas Perfetto un gas che risetta le due leggi di Gay-Lussac e la legge di Boyle-Mariotte in tutte le condizioni di temeratura, densità e ressione. Per i gas ideali si ha: Equazione di Stato dei Gas Perfetti R n K mol J 8,3 dove R n Numero di moli di gas (Costante Universale dei Gas) L equazione di stato dei gas erfetti racchiude le tre leggi dei gas: cost costante cost costante cost costante R n ISOERME R n R n ISOCORE R n R n ISOBARE
16 Equazione di Stato dei Gas Perfetti I gas reali vengono descritti dalla legge dei gas erfetti con buona arossimazione solo quando la ressione è sufficientemente bassa e la temeratura sufficientemente alta. In caso contrario è valida la legge dei gas reali (Legge di an der Waals). Dall equazione di stato segue la legge di Avogadro: n R Cioè: volumi uguali di gas diversi, in condizioni di temeratura e ressione uguali, contengono lo stesso numero di articelle.
17 Il Calore / È eserienza comune che er far aumentare la temeratura di una sostanza, ad esemio dell acqua, è necessario scaldarla. Ciò equivale a fornire al coro una certa quantità di energia, detta calore: Il calore è una forma di energia la cui rorietà rinciale è quella di assare da un coro iù caldo ad un altro coro meno caldo. L unità di misura nel S.I. è il joule (J). Che il calore sia una forma di energia ormai è noto, ma rima si credeva fosse un fluido invisibile e imonderabile, che Lavoisier ( ) chiamò CALORICO, in grado di assare da un coro ad un altro modificandone la temeratura. Questo flusso calorico era misurato in calorie (cal) o chilocalorie ( kcal = cal), dove la kcal è la quantità di calore necessaria er far aumentare di C, da 4,5 C a 5,5 C, la temeratura di un grammo di acqua distillata osta a livello del mare (ressione atm = 35 Pa). Solo nel XIX secolo Joule (88 889) dimostrò che calore e lavoro meccanico otevano convertirsi direttamente l'uno nell'altro, mantenendo erò costante il loro valore comlessivo: in altre arole asserì che il calore è una forma di energia.
18 Il Calore / Per dimostrare l equivalenza tra calore e lavoro realizzò un eserienza nota come mulinello di Joule. In un thermos (un reciiente termicamente isolato, le cui areti imediscono al calore di entrare e uscire) è inserito un mulinello a alette, azionato dalla caduta di due esi, che agita l acqua. Se i esi fossero in caduta libera, la loro energia cinetica finale sarebbe uguale al lavoro W comiuto dalla forza-eso. Invece, al termine della caduta, l energia cinetica K dei due esi è minore di W, a causa dell attrito tra l acqua e le alette, che ostacola la rotazione del mulinello. La differenza tra W e K è il lavoro comiuto dalle alette sull acqua (oosto a quello dell acqua sulle alette). Questo lavoro scalda l acqua contenuta nel thermos, cioè accresce l energia cinetica delle sue molecole. Joule verificò che er innalzare di C la temeratura dell acqua occorrono 486 J di lavoro er ogni kilogrammo di massa o, in modo equivalente, ne occorrono 4,86 J er ogni grammo. Quindi, er come è definita la caloria, tra la caloria e il joule vale la relazione cal = 4,86 J.
19 Caacità ermica e Calore Secifico / L assorbimento della stessa quantità di energia non rovoca lo stesso aumento di temeratura in tutti i cori. Il raorto fra il calore che un coro acquista e la variazione di temeratura si definisce caacità termica del coro, in formule: C Q L unità di misura nel S.I. è J/K o J/ C. con C Caacità ermica Q Quantità di Calore ariazione di emeratura È abbastanza evidente che quanto maggiore è la massa che viene riscaldata tanto maggiore è il calore necessario er farne aumentare la temeratura, la costante di roorzionalità tra caacità e massa si chiama calore secifico: Il calore secifico di una sostanza è il raorto fra la caacità termica e la massa, in formule: c C m Q m L unità di misura nel S.I. è J/(K kg) o J/( C kg). con c Calore Secifico C Caacità ermica m Massa
20 Ciò orta a quella che viene definita come: / Legge Fondamentale della ermologia m c Q ariazione di emeratura Δ Massa m Calore Secifico c Quantità di Calore Q con Caacità ermica e Calore Secifico Se mettiamo a contatto due cori con temerature, calori secifici e masse diverse, che scambiano calore fra loro ma non con l ambiente, si orteranno ad una temeratura di equilibrio che, in base alla legge fondamentale, è data da: m c m c m c m c m c m c Q Q E E E
21 L Equilibrio ermico La legge fondamentale della termologia regola quindi i rocessi di scambio di calore che ortano all equilibrio termico, che consiste nel fatto che quando due cori a diversa temeratura sono messi a contatto si genera un flusso di calore, dal coro iù caldo verso quello iù freddo, che dura sino a quando i due cori non arrivano alla stessa temeratura intermedia tra le due temerature iniziali. A B Q C C A > B Q : Flusso di Calore A > C > B utti i cori tendono all equilibrio termico, cioè a ortarsi alla stessa temeratura attraverso un flusso, ciò uò accadere in quanto il calore si roaga, cioè assa dal coro iù caldo al coro iù freddo. Le sostanze che conducono bene il calore si dicono conduttori termici (ad es. i metalli), mentre le sostanze che non lo conducono bene si dicono isolanti termici (ad es. il legno).
22 La Proagazione del Calore I meccanismi di roagazione del calore sono: Conduzione: E la trasmissione di calore da un coro ad un altro senza sostamento delle sue molecole. Un caso tiico è il riscaldamento di un asta metallica mediante una fiamma alicata alle sue estremità. L energia termica si trasmette er contatto da molecola a molecola dall estremità a iù alta temeratura verso quella fredda. La conduzione è tiica dei solidi. Convezione: E la trasmissione di calore che avviene nei fluidi (liquidi e gas) con sostamento delle molecole. Se un coro caldo (ad esemio un radiatore) riscalda l aria, questa diventa semre iù leggera e sale verso l alto; tale movimento richiama altra aria verso il coro caldo e così via. La sinta naturale di salita dell aria, origina un movimento lento della stessa (convezione), riscaldando il locale in modo uniforme e confortevole. Irraggiamento: E la trasmissione di calore senza contatto diretto dei cori. In questo caso si trasmette il calore mediante onde o radiazioni. Un esemio è il calore che erceiamo da una lamadina accesa quando avviciniamo la mano. Questo è il modo in cui il Sole riscalda la erra.
23 I Passaggi di Stato Al variare di temeratura e ressione la materia uò transitare da uno stato di aggregazione ad un altro, effettuando un PASSAGGIO DI SAO: Passaggi di stato che avvengono con cessione di calore da arte del coro. Passaggi di stato che avvengono con assorbimento di calore da arte del coro. Durante i assaggi di stato la temeratura dei cori è costante, ad esemio se in un bicchiere abbiamo acqua e ghiaccio la temeratura è C sino a quando tutto il ghiaccio non è diventato acqua. Il calore assorbito (o ceduto) dal coro durante il assaggio di stato si chiama Calore Latente ed è utilizzato dal coro solo ed esclusivamente er effettuare il assaggio di stato stesso, quindi non roduce un aumento (o diminuzione) della temeratura del coro. Nota: E ossibile ottenere i assaggi di stato anche senza somministrare o assorbire calore ma agendo invece sulla ressione; ad esemio in laboratorio ossiamo far bollire l acqua anche a temeratura ambiente semlicemente diminuendo la ressione atmosferica.
24 I Passaggi di Stato Al livello microscoico, durante la fusione, l energia assorbita sotto forma di calore serve a vincere le forze che nello stato solido tengono legato ogni singolo atomo alla sua osizione. Sezzando i legami gli atomi diventano liberi di scorrere: così il solido erde la roria forma e rende quella del reciiente. In modo analogo, l energia assorbita durante la vaorizzazione viene sesa contro le forze attrattive intermolecolari e serve a rendere le molecole del tutto libere di allontanarsi l una dall altra.
25 Bibliografia & Sitografia htts://it.wikiedia.org/wiki/prima_legge_di_gay-lussac htts://it.wikiedia.org/wiki/seconda_legge_di_gay-lussac htts://it.wikiedia.org/wiki/legge_di_boyle-mariotte htts://it.wikiedia.org/wiki/gas_ideale htts://
26 htts://commons.wikimedia.org/wiki/file:%c%blegge_gay_lussac.jg#/media/file: %C%Blegge_Gay_Lussac.jg htts://commons.wikimedia.org/wiki/file:charles_and_gay- Lussac%7s_Law_animated.gif#/media/File:Charles_and_Gay- Lussac%7s_Law_animated.gif htts://commons.wikimedia.org/wiki/file:%c%blegge_gay_lussac.jg#/media/file: %C%Blegge_Gay_Lussac.jg htts://commons.wikimedia.org/w/index.h?curid= htts://commons.wikimedia.org/wiki/file:legge_di_boyle_dati_originali.jg#/media/file :Legge_di_Boyle_dati_originali.jg htts://argomentidifisica.files.wordress.com///joulemulin.jg htts://4.b.blogsot.com/-oysxfjrss/wkfxtc8moi/aaaaaaaakm/mdiclupenaiqrvon7jjc6mftmsxrwclcb/s6 /materia-fisica.gif
Peso atomico (meglio massa atomica)
 Nome file d:\scuola\corsi\corso fisica\termodinamica\leggi dei gas.doc Creato il 26/3/2 7.5 Dimensione file: 4864 byte Andrea Zucchini Elaborato il 22//22 alle ore 5.52, salvato il 22//2 7.52 stamato il
Nome file d:\scuola\corsi\corso fisica\termodinamica\leggi dei gas.doc Creato il 26/3/2 7.5 Dimensione file: 4864 byte Andrea Zucchini Elaborato il 22//22 alle ore 5.52, salvato il 22//2 7.52 stamato il
La misura della temperatura
 Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Il termoscopio. Il termoscopio è uno strumento che serve per decidere, in modo oggettivo, se un corpo è più caldo o più freddo di un altro.
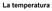 La temperatura Il termoscopio Il termoscopio è uno strumento che serve per decidere, in modo oggettivo, se un corpo è più caldo o più freddo di un altro. In quale vaschetta c è l acqua più calda? temperatura
La temperatura Il termoscopio Il termoscopio è uno strumento che serve per decidere, in modo oggettivo, se un corpo è più caldo o più freddo di un altro. In quale vaschetta c è l acqua più calda? temperatura
Calore e Temperatura
 PROGETTO POTENZIAMENTO DEL LABORATORIO DI FISICA LEZIONI ATTIVE Calore e Temperatura PREREQUISITO Ripetiamo il concetto di ENERGIA DEFINIZIONE TIPOLOGIE TRASFORMAZIONE DISPONIBILITA E CONSUMO FORZE DISSIPATIVE
PROGETTO POTENZIAMENTO DEL LABORATORIO DI FISICA LEZIONI ATTIVE Calore e Temperatura PREREQUISITO Ripetiamo il concetto di ENERGIA DEFINIZIONE TIPOLOGIE TRASFORMAZIONE DISPONIBILITA E CONSUMO FORZE DISSIPATIVE
UNIVERSITÀ DEGLI STUDI DI TERAMO
 UNIVERSITÀ DEGLI STUDI DI TERAMO FACOLTÀ DI MEDICINA VETERINARIA CORSO DI LAUREA IN TUTELA E BENESSERE ANIMALE Corso di FISICA MEDICA A.A. 2015 /2016 Docente: Chiucchi Riccardo mail:rchiucchi@unite.it
UNIVERSITÀ DEGLI STUDI DI TERAMO FACOLTÀ DI MEDICINA VETERINARIA CORSO DI LAUREA IN TUTELA E BENESSERE ANIMALE Corso di FISICA MEDICA A.A. 2015 /2016 Docente: Chiucchi Riccardo mail:rchiucchi@unite.it
T = t o (1.1) Nella scala kelvin il ghiaccio fonde a 273 K e l acqua bolle a 373 K. Un grado kelvin è uguale a un grado celsius
 Termologia. La temperatura è la grandezza fisica che misura lo stato termico di un sistema fisico (un corpo). 2. Scale termometriche. - Scala Celsius ( o C). Proposta nel 742. 0 o C è la temperatura di
Termologia. La temperatura è la grandezza fisica che misura lo stato termico di un sistema fisico (un corpo). 2. Scale termometriche. - Scala Celsius ( o C). Proposta nel 742. 0 o C è la temperatura di
i tre stati di aggregazione
 Temperatura e Calore -temperatura -calore e calore specifico -lavoro in termodinamica -trasformazioni termodinamiche -trasformazioni di stato -energia interna 1 i tre stati di aggregazione solido Ordine
Temperatura e Calore -temperatura -calore e calore specifico -lavoro in termodinamica -trasformazioni termodinamiche -trasformazioni di stato -energia interna 1 i tre stati di aggregazione solido Ordine
Temperatura e Calore
 Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 2. La carta d identità delle sostanze SEGUI LA MAPPA descrivere atomica 1 descrivere
Termodinamica (1) Temperatura e calore Lezione 12, 13/11/2018, JW
 Termodinamica (1) Temperatura e calore Lezione 12, 13/11/2018, JW 15.1-15.6 1 1. Calore Definizione di calore Il calore è l energia trasferita tra oggetti a causa della loro differenza di temperatura.
Termodinamica (1) Temperatura e calore Lezione 12, 13/11/2018, JW 15.1-15.6 1 1. Calore Definizione di calore Il calore è l energia trasferita tra oggetti a causa della loro differenza di temperatura.
Unità 1. La temperatura
 Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
La temperatura. La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso
 1 La temperatura La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso Qualunque sia lo stato di aggregazione, le particelle (molecole o atomi) di cui è fatta
1 La temperatura La materia può trovarsi in tre stati diversi di aggregazione diversi: solido, liquido e gassoso Qualunque sia lo stato di aggregazione, le particelle (molecole o atomi) di cui è fatta
ma come si puo misurare una grandezza fisica della quale si postula l esistenza, ma di cui non si conosce nulla? chiaramente misurarla direttamente
 Princiio zero della termodinamica gli stati di equilibrio termico godono della articolare rorieta che i sistemi all equilibrio termico tra loro condividono una stessa grandezza fisica, detta temeratura
Princiio zero della termodinamica gli stati di equilibrio termico godono della articolare rorieta che i sistemi all equilibrio termico tra loro condividono una stessa grandezza fisica, detta temeratura
Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più
 I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
10. LA MISURA DELLA TEMPERATURA
 1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
Termoscopio di Galileo Sfrutta la dilatazione termica dell aria contenuta al suo interno.
 Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
UNITÀ 1 La temperatura. Test
 Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Calore e Temperatura
 PROGETTO POTENZIAMENTO DEL LABORATORIO DI FISICA LEZIONI ATTIVE Calore e Temperatura PREREQUISITO Ripetiamo il concetto di ENERGIA DEFINIZIONE TIPOLOGIE TRASFORMAZIONE DISPONIBILITA E CONSUMO FORZE DISSIPATIVE
PROGETTO POTENZIAMENTO DEL LABORATORIO DI FISICA LEZIONI ATTIVE Calore e Temperatura PREREQUISITO Ripetiamo il concetto di ENERGIA DEFINIZIONE TIPOLOGIE TRASFORMAZIONE DISPONIBILITA E CONSUMO FORZE DISSIPATIVE
PDF Compressor Pro. Temperatura e calore. Prof Giovanni Ianne
 Temperatura e calore Prof Giovanni Ianne LA TEMPERATURA La temperatura è la grandezza fisica che si misura con il termometro. La temperatura nel Sistema Internazionale si misura in gradi Kelvin (simbolo
Temperatura e calore Prof Giovanni Ianne LA TEMPERATURA La temperatura è la grandezza fisica che si misura con il termometro. La temperatura nel Sistema Internazionale si misura in gradi Kelvin (simbolo
Fisica per scienze ed ingegneria
 Serway, Jewett Fisica per scienze ed ingegneria Capitolo 19 Temperatura e principio zero della termodinamica I nostri sensi non sono affidabili per definire lo stato termico dei corpi. Ocorre un metodo
Serway, Jewett Fisica per scienze ed ingegneria Capitolo 19 Temperatura e principio zero della termodinamica I nostri sensi non sono affidabili per definire lo stato termico dei corpi. Ocorre un metodo
SISTEMA TERMODINAMICO STATO TERMODINAMICO
 SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
La temperatura e il calore
 La temperatura e il calore Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti nel nostro laboratorio Questo simbolo significa che l esperimento si può realizzare
La temperatura e il calore Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti nel nostro laboratorio Questo simbolo significa che l esperimento si può realizzare
Capitolo 13. La temperatura
 Capitolo 13 La temperatura Il termoscopio Il termoscopio è uno strumento che serve per decidere, in modo oggettivo, se un corpo è più caldo o più freddo di un altro. In quale vaschetta c è l acqua più
Capitolo 13 La temperatura Il termoscopio Il termoscopio è uno strumento che serve per decidere, in modo oggettivo, se un corpo è più caldo o più freddo di un altro. In quale vaschetta c è l acqua più
Università degli Studi di Milano. Facoltà di Scienze Matematiche Fisiche e Naturali
 Università degli Studi di Milano Facoltà di Scienze Matematiche Fisiche e Naturali Corsi di Laurea in: Informatica ed Informatica per le Telecomunicazioni Anno accademico 2010/11, Laurea Triennale, Edizione
Università degli Studi di Milano Facoltà di Scienze Matematiche Fisiche e Naturali Corsi di Laurea in: Informatica ed Informatica per le Telecomunicazioni Anno accademico 2010/11, Laurea Triennale, Edizione
Fisica Generale A estensione principio di conservazione dell energia energia termica teoria cinetica dei gas 14. I Principio della Termodinamica
 Fisica Generale A 4. I Princiio della ermodinamica htt://camus.cib.unibo.it/2434/ December 3, 2 Primo Princiio e Moti Molecolari Il rimo rinciio della termodinamica è l estensione del rinciio di conservazione
Fisica Generale A 4. I Princiio della ermodinamica htt://camus.cib.unibo.it/2434/ December 3, 2 Primo Princiio e Moti Molecolari Il rimo rinciio della termodinamica è l estensione del rinciio di conservazione
SISTEMA TERMODINAMICO STATO TERMODINAMICO
 SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
SISTEMA TERMODINAMICO Sistema macroscopico (gas, liquido, solido) chimicamente definito, composto da un grande numero di atomi o molecole. In una mole di sostanza: N 6,02 10 23 Isolato: non scambia né
Termodinamica. Grandezze termodinamiche: funzioni di stato Macro e micro meccanica statistica Principi della termodinamica
 Termodinamica Studia cosa succede macroscopicamente a un sistema sottoposto a trasformazioni energetiche Sistema: parte di spazio o quantità di materia Aperto/chiuso Isolato Omogeneo Grandezze termodinamiche:
Termodinamica Studia cosa succede macroscopicamente a un sistema sottoposto a trasformazioni energetiche Sistema: parte di spazio o quantità di materia Aperto/chiuso Isolato Omogeneo Grandezze termodinamiche:
Temperatura. Temperatura
 TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
Dal modellino dei Gas perfetti alla Tecnologia del vuoto
 Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare i sistemi da vuoto, arte tutto da P= Nk () (*) P ressione del gas, olume
Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare i sistemi da vuoto, arte tutto da P= Nk () (*) P ressione del gas, olume
Termoscopio di Galileo Sfrutta la dilatazione termica dell aria contenuta al suo interno.
 Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
Danno informazioni sullo stato termico di un corpo (ma non ne misurano la temperatura): a contatto con esso, assumono la sua stessa temperatura (si dice che raggiungono l equilibrio termico). Termoscopio
La temperatura questa sconosciuta!
 La temperatura questa sconosciuta! Sondaggio Metti «mi piace» alla definizione che ritieni più giusta Energia Calore Misura del caldo/freddo Stato della materia ermometria e calorimetria Principio zero
La temperatura questa sconosciuta! Sondaggio Metti «mi piace» alla definizione che ritieni più giusta Energia Calore Misura del caldo/freddo Stato della materia ermometria e calorimetria Principio zero
TERMODINAMICA. Il sistema è il corpo o l insieme dei corpi sotto esame.
 TERMODINAMICA SISTEMI TERMODINAMICI Il sistema è il corpo o l insieme dei corpi sotto esame. L ambiente esterno è l insieme di tutti i corpi che possono interagire con il sistema. Tipi di sistemi termodinamici
TERMODINAMICA SISTEMI TERMODINAMICI Il sistema è il corpo o l insieme dei corpi sotto esame. L ambiente esterno è l insieme di tutti i corpi che possono interagire con il sistema. Tipi di sistemi termodinamici
TERMOLOGIA & TERMODINAMICA I
 TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
CLASSI SECONDE Formulario (con esercizi) LEGGI DEI GAS
 CLASSI SECONDE Formulario con esercizi) LEGGI DEI GAS Germano D Abramo Versione 1.1 10/03/2016 N.B. Si invita a trovare errori e/o imrecisioni o a richiedere una stesura del testo iù semlice.) Trasformzioni
CLASSI SECONDE Formulario con esercizi) LEGGI DEI GAS Germano D Abramo Versione 1.1 10/03/2016 N.B. Si invita a trovare errori e/o imrecisioni o a richiedere una stesura del testo iù semlice.) Trasformzioni
Dal modellino dei Gas perfetti alla Tecnologia del vuoto
 Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto dalla relazione: P= Nk (*) P ressione
Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto dalla relazione: P= Nk (*) P ressione
Dal modellino dei Gas perfetti alla Tecnologia del vuoto
 Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto da P Nk () (*) P ressione del gas olume
Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto da P Nk () (*) P ressione del gas olume
La temperatura e il calore. Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3
 La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
IL CALORE. Il calore. Esperimento di Joule. Il calore
 l calore l calore Q è energia che sta transitando da un sistema all altro, e compare ogni volta che c è un dislivello di temperatura. L CALORE l corpo più caldo cede parte della sua energia interna al
l calore l calore Q è energia che sta transitando da un sistema all altro, e compare ogni volta che c è un dislivello di temperatura. L CALORE l corpo più caldo cede parte della sua energia interna al
Effetti della T sui materiali e l ambiente. Dilatazione termica. = coefficiente di dilatazione termica lineare Dilatazione superficiale: A =l o 2
 Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
La temperatura: La pressione: Il volume:
 I gas Un gas è formato da un gran numero di molecole che si muovono in modo disordinato, urtandosi tra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti le molecole esercitano
I gas Un gas è formato da un gran numero di molecole che si muovono in modo disordinato, urtandosi tra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti le molecole esercitano
Fisica Applicata, Area Infermieristica, M. Ruspa REGIMI DI MOTO DI UN FLUIDO REALE
 REGIMI DI MOTO DI UN FLUIDO REALE MOTO LAMINARE O TURBOLENTO? Dipende dalla velocita di scorrimento del fluido! VELOCITA CRITICA La velocita critica per un fluido di viscosita η e di densita d che scorre
REGIMI DI MOTO DI UN FLUIDO REALE MOTO LAMINARE O TURBOLENTO? Dipende dalla velocita di scorrimento del fluido! VELOCITA CRITICA La velocita critica per un fluido di viscosita η e di densita d che scorre
Leggi dei gas Equazione di stato dei gas perfetti
 Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Le leggi dei gas Quale descrizione fisico-matematica si può usare per i diversi stati di aggregazione della materia? Essa è tanto più semplice (equazioni) quanto meno interagenti sono fra loro le particelle
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore.
 Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore. Cambiamenti di stati di aggregazione Gli stati di aggregazione della materia sono: solido, liquido gassoso (e
Lezione 14 Termologia Cambiamenti di stato. Dilatazioni termiche. Trasmissione del calore. Cambiamenti di stati di aggregazione Gli stati di aggregazione della materia sono: solido, liquido gassoso (e
Sia dato un corpo su cui agisce una forza. Supponiamo che inizialmente il corpo sia fermo, dalla relazione
 Lavoro ed energia Sia dato un coro su cui agisce una forza. Suoniamo che inizialmente il coro sia fermo, dalla relazione F = ma doo un certo intervallo di temo in cui la forza agisce sull oggetto, il coro
Lavoro ed energia Sia dato un coro su cui agisce una forza. Suoniamo che inizialmente il coro sia fermo, dalla relazione F = ma doo un certo intervallo di temo in cui la forza agisce sull oggetto, il coro
La misura della temperatura
 LA TEMPERATURA La misura della temperatura Caldo e freddo: semplici esperimenti Toccando un corpo possiamo avvertire una sensazione soggettiva della sua temperatura Per avere una misura precisa e oggettiva
LA TEMPERATURA La misura della temperatura Caldo e freddo: semplici esperimenti Toccando un corpo possiamo avvertire una sensazione soggettiva della sua temperatura Per avere una misura precisa e oggettiva
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA. Lezione 3 TRASFORMAZIONI DEL SISTEMA
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. CHIMICA FISICA Lezione 3 Anno Accademico 00-0 Docente: Dimitrios Fessas RASFORMAZIONI DEL SISEMA i. RASFORMAZIONI
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. CHIMICA FISICA Lezione 3 Anno Accademico 00-0 Docente: Dimitrios Fessas RASFORMAZIONI DEL SISEMA i. RASFORMAZIONI
Calorimetria. Principio zero Trasformazioni termodinamiche Lavoro termodinamico
 Calorimetria Principio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una particella è definito quando per ogni istante siano note, la posizione (x,
Calorimetria Principio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una particella è definito quando per ogni istante siano note, la posizione (x,
CALORE E TEMPERATURA
 CALORE E TEMPERATURA Indice Obiettivi L agitazione termica La dilatazione termica La misura della temperatura Lo stato fisico della materia Flussi di calore ed equilibrio termico La propagazione del calore
CALORE E TEMPERATURA Indice Obiettivi L agitazione termica La dilatazione termica La misura della temperatura Lo stato fisico della materia Flussi di calore ed equilibrio termico La propagazione del calore
Dotto Formazione a tutto tondo Rapid Training 2018 Corso di Fisica Argomento 9 Temperatura e Calore
 1 Dotto Formazione a tutto tondo Rapid Training 2018 Corso di Fisica Argomento 9 Temperatura e Calore 2 La temperatura La temperatura di una sostanza è una grandezza fisica scalare che da una misura dello
1 Dotto Formazione a tutto tondo Rapid Training 2018 Corso di Fisica Argomento 9 Temperatura e Calore 2 La temperatura La temperatura di una sostanza è una grandezza fisica scalare che da una misura dello
Lezione 10 Termodinamica
 rgomenti della lezione: relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot Lezione 0 ermodinamica secondo riiio della termodinamica Gas ideali Un gas
rgomenti della lezione: relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot Lezione 0 ermodinamica secondo riiio della termodinamica Gas ideali Un gas
TEMPERATURA E CALORE. Termometri, dilatazione termica, calore specifico. FISICA - Prof. Massimiliano Bacchi
 TEMPERATURA E CALORE Termometri, dilatazione termica, calore specifico 1 Termoscopio Un oggetto può ad alcuni sembrare caldo, ad altri freddo, oppure due oggetti nella stessa stanza sembrano essere uno
TEMPERATURA E CALORE Termometri, dilatazione termica, calore specifico 1 Termoscopio Un oggetto può ad alcuni sembrare caldo, ad altri freddo, oppure due oggetti nella stessa stanza sembrano essere uno
Termologia. Paolo Bagnaia - CTF Esercizi di termologia e termodinamica 1
 ermologia Paolo Bagnaia - CF - 3 - Esercizi di termologia e termodinamica 1 Esercizio Un cubetto di ghiaccio di 150 g alla temeratura di 0 C è gettato in unreciiente, i che contiene 300 g di acqua alla
ermologia Paolo Bagnaia - CF - 3 - Esercizi di termologia e termodinamica 1 Esercizio Un cubetto di ghiaccio di 150 g alla temeratura di 0 C è gettato in unreciiente, i che contiene 300 g di acqua alla
SCALA TERMOMETRICA CELSIUS
 TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
GAS TERMODINAMICA CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE
 CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE GAS TERMODINAMICA GAS PERFETTI E GAS REALI TRASFORMAZIONI TERMODINAMICHE TRASMISSIONE DEL CALORE A. A. 2015-2016 Fabrizio
CLASSE DELLE LAUREE TRIENNALI DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE GAS TERMODINAMICA GAS PERFETTI E GAS REALI TRASFORMAZIONI TERMODINAMICHE TRASMISSIONE DEL CALORE A. A. 2015-2016 Fabrizio
Lezione 10 Termodinamica
 rgomenti della lezione: Lezione 0 ermodinamica relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot secondo riiio della termodinamica cenni sull entroia
rgomenti della lezione: Lezione 0 ermodinamica relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot secondo riiio della termodinamica cenni sull entroia
Dilatazione termica. Effetti della T sui materiali e l ambiente. l=α l o t. A = 2 α A o t. α = coefficiente di dilatazione termica lineare
 Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
GAS IDEALI E REALI. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche:
 GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
Calore specifico. Il calore che deve essere fornito per aumentare di un grado centigrado un chilogrammo della sostanza è il calore specifico:
 Calore specifico L aumento (diminuzione) di temperatura in una sostanza è proporzionale all energia fornita (sottratta) alla sostanza sotto forma di calore: Il calore che deve essere fornito per aumentare
Calore specifico L aumento (diminuzione) di temperatura in una sostanza è proporzionale all energia fornita (sottratta) alla sostanza sotto forma di calore: Il calore che deve essere fornito per aumentare
Temperatura e calore. Principi della termodinamica Temperatura Calore Gas ideali
 Temperatura e calore Principi della termodinamica Temperatura Calore Gas ideali Termodinamica Termodinamica branca della fisica che descrive le trasformazioni subite da un sistema in seguito a processi
Temperatura e calore Principi della termodinamica Temperatura Calore Gas ideali Termodinamica Termodinamica branca della fisica che descrive le trasformazioni subite da un sistema in seguito a processi
Stati della materia. Esempio. Fusione e solidificazione. Esempio. Stati di aggregazione della materia
 Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE
 1 LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE L energia si presenta in diverse forme e una delle più importanti è il calore. I fenomeni naturali sono quasi sempre accompagnati da sviluppo o assorbimento
1 LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE L energia si presenta in diverse forme e una delle più importanti è il calore. I fenomeni naturali sono quasi sempre accompagnati da sviluppo o assorbimento
Lo stato gassoso. L atmosfera terrestre è il sistema gassoso in cui siamo immersi
 Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Lo stato gassoso L atmosfera terrestre è il sistema gassoso in cui siamo immersi I gas sono comprimibili (ampi spazi vuoti tra le particelle?) I gas si espandono facilmente riempiendo rapidamente lo spazio
Programma svolto a.s. 2015/2016. Materia: fisica
 Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
Fisica per Medicina. Lezione 9 - Termodinamica. Dr. Cristiano Fontana
 Fisica per Medicina Lezione 9 - Termodinamica Dr. Cristiano Fontana Dipartimento di Fisica ed Astronomia Galileo Galilei Università degli Studi di Padova 17 novembre 2016 Grandezze in gioco Trasporto di
Fisica per Medicina Lezione 9 - Termodinamica Dr. Cristiano Fontana Dipartimento di Fisica ed Astronomia Galileo Galilei Università degli Studi di Padova 17 novembre 2016 Grandezze in gioco Trasporto di
Lez 14 16/11/2016. Lezioni in didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617
 Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
Termometro e temperatura
 La tempertura ed il calore Pagina 1 di 11 Termometro e temperatura La temperatura è la grandezza fisica che rende oggettiva la sensazione di caldo e freddo che si prova toccando i corpi, cioè la temperatura
La tempertura ed il calore Pagina 1 di 11 Termometro e temperatura La temperatura è la grandezza fisica che rende oggettiva la sensazione di caldo e freddo che si prova toccando i corpi, cioè la temperatura
Le forze e la loro misura
 Modulo B Le Forze Unità 1 Pagina 1 di 6 Le forze e la loro misura Per forza intendiamo una qualsiasi causa esterna che modifica lo stato di quiete o di moto se alicata ad un coro libero di muoversi, o
Modulo B Le Forze Unità 1 Pagina 1 di 6 Le forze e la loro misura Per forza intendiamo una qualsiasi causa esterna che modifica lo stato di quiete o di moto se alicata ad un coro libero di muoversi, o
L equilibrio dei gas
 L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
L equilibrio dei gas Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura 1 L equilibrio dei gas Un gas esercita una pressione sul recipiente che
La Pressione (1) La Pressione è una grandezza scalare ed in un fluido rappresenta una proprietà meccanica dello stesso.
 La Pressione (1) Trasformazioni termodamiche del Gas Ideale - 1 ds La Pressione è una grandezza scalare ed un fluido raresenta una rorietà meccanica dello stesso. d n F df ds = 1 = mg h (1) = ds ds n π
La Pressione (1) Trasformazioni termodamiche del Gas Ideale - 1 ds La Pressione è una grandezza scalare ed un fluido raresenta una rorietà meccanica dello stesso. d n F df ds = 1 = mg h (1) = ds ds n π
Introduzione alla Chimica. Paolo Mazza
 Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
Introduzione alla Chimica Paolo Mazza 2 aprile 2013 Indice 1 Introduzione 2 2 Le teorie della materia 4 2.1 Teoria atomica.................................... 4 2.2 Teoria cinetica.....................................
TERMOLOGIA TERMOMETRIA E CALORIMETRIA
 1 TERMOLOGIA La termologia è il settore della fisica che si interessa dei fenomeni termici, ovvero studia quei fenomeni in cui hanno una grande importanza la temperatura e il calore. Questa branca della
1 TERMOLOGIA La termologia è il settore della fisica che si interessa dei fenomeni termici, ovvero studia quei fenomeni in cui hanno una grande importanza la temperatura e il calore. Questa branca della
Temperatura Calore Trasformazioni termodinamiche
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione i del calore Termoregolazione del corpo umano pag.1
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione i del calore Termoregolazione del corpo umano pag.1
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Stati della materia. Una sostanza pura è una sostanza la cui composizione chimica non varia. Ossigeno. Acqua. Aria
 1. Una sostanza pura non deve necessariamente essere composta da un unico elemento chimico. 2. Anche una miscela di più sostanze può essere considerata una sostanza pura purchè abbia una composizione chimica
1. Una sostanza pura non deve necessariamente essere composta da un unico elemento chimico. 2. Anche una miscela di più sostanze può essere considerata una sostanza pura purchè abbia una composizione chimica
Calorimetria. Principio zero Trasformazioni termodinamiche Lavoro termodinamico
 Calorimetria Princiio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una articella è definito quando siano note, in un certo istante, la osizione
Calorimetria Princiio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una articella è definito quando siano note, in un certo istante, la osizione
Centrali termiche: per la conduzione ci vuole la patente Obbligo del patentino di abilitazione di 2 grado per
 Centrali termiche: per la conduzione ci vuole la patente Obbligo del patentino di abilitazione di 2 grado per la conduzione degli impianti termici sopra i 232 kw Ing. Diego Danieli Libero Professionista
Centrali termiche: per la conduzione ci vuole la patente Obbligo del patentino di abilitazione di 2 grado per la conduzione degli impianti termici sopra i 232 kw Ing. Diego Danieli Libero Professionista
2 Una sbarra ha l 0: se la sua varia di t, la diviene l = l 0 (1 + λ t), dove λ è una costante, detta coefficiente di, che dipende dal materiale.
 I concetti fondamentali 1 Nel Sistema Internazionale l unità di misura per la temperatura è il In questa scala, detta scala assoluta, la variazione di 1 è identica a quella di 1 Però la temperatura del
I concetti fondamentali 1 Nel Sistema Internazionale l unità di misura per la temperatura è il In questa scala, detta scala assoluta, la variazione di 1 è identica a quella di 1 Però la temperatura del
Lo stato si un gas è caratterizzato da determinanti valori di temperatura, volume e pressione, che rappresentano variabili di stato termodinamico
 Fisica (plus) dei Puffi prof. Angelo Vitiello T 1 Termodinamica La temperatura è una grandezza fisica scalare che si misura con il termometro. Rende oggettiva la sensazione corporea di freddo e di caldo.
Fisica (plus) dei Puffi prof. Angelo Vitiello T 1 Termodinamica La temperatura è una grandezza fisica scalare che si misura con il termometro. Rende oggettiva la sensazione corporea di freddo e di caldo.
GAS IDEALI (o gas perfetti )
 GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
Termodinamica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Termodinamica Studia sistemi estesi caratterizzati da pressione, volume e temperatura Si basa sulla definizione della temperatura e su tre principi Il primo principio riguarda la conservazione dell energia
Termodinamica Studia sistemi estesi caratterizzati da pressione, volume e temperatura Si basa sulla definizione della temperatura e su tre principi Il primo principio riguarda la conservazione dell energia
Fisica Main Training Lorenzo Manganaro
 Fisica Main Training 2016-2017 Lorenzo Manganaro 1. Temperatura e dilatazione termica 2. Calorimetria 3. Scambio di calore 30 25 20 Veterinaria Ottica e Optometria Odontoiatria Medicina 15 10 5 0 Vettori
Fisica Main Training 2016-2017 Lorenzo Manganaro 1. Temperatura e dilatazione termica 2. Calorimetria 3. Scambio di calore 30 25 20 Veterinaria Ottica e Optometria Odontoiatria Medicina 15 10 5 0 Vettori
LA MATERIA ED I SUOI STATI
 LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Unità didattica 5. Quinta unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 5 Termodinamica (1 a parte) Capacità termica. 2 Calore specifico 3 Scale termometriche.. 4 Le leggi di dilatazione termica... 5 Tipi di termometri: Termometri a liquido,... 6 Termometri
Unità didattica 5 Termodinamica (1 a parte) Capacità termica. 2 Calore specifico 3 Scale termometriche.. 4 Le leggi di dilatazione termica... 5 Tipi di termometri: Termometri a liquido,... 6 Termometri
LEGGE DI STOKES. Fisica Applicata, Area Infermieristica, M. Ruspa
 LEGGE DI STOKES La forza di attrito viscoso che agisce su un corpo sfrerico di raggio r che si muove con velocita v non elevata in un fluido di viscosita η in quite si puo calcolare come: SEDIMENTAZIONE
LEGGE DI STOKES La forza di attrito viscoso che agisce su un corpo sfrerico di raggio r che si muove con velocita v non elevata in un fluido di viscosita η in quite si puo calcolare come: SEDIMENTAZIONE
Riassunto. Familiarizzare con i concetti fisici
 Riassunto Grandezze vettoriali e scalari Le grandezze del moto Le cause del moto: Leggi di newton! Moto in iù dimensioni Lavoro Energia e sua conservazione Quantità di moto e sua conservazione amiliarizzare
Riassunto Grandezze vettoriali e scalari Le grandezze del moto Le cause del moto: Leggi di newton! Moto in iù dimensioni Lavoro Energia e sua conservazione Quantità di moto e sua conservazione amiliarizzare
LCE Umberto I - Fisica Compito S 1
 LCE Umberto I - Fisica Compito S 1 Cognome Nome Data Classe Scegliere le risposte corrette e poi scriverle nella riga in fondo al foglio 1 Quale è la definizione corretta di unità di massa atomica? A]
LCE Umberto I - Fisica Compito S 1 Cognome Nome Data Classe Scegliere le risposte corrette e poi scriverle nella riga in fondo al foglio 1 Quale è la definizione corretta di unità di massa atomica? A]
Termodinamica: introduzione
 Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Richiami di Calorimetria Introduzione al Corso Prof. Ing. Giulio Vannucci
 CORSO DI FISICA TECNICA Richiami di Calorimetria Introduzione al Corso Prof. Ing. Giulio Vannucci Calorimetria Calore Il calore è una forma di energia che si trasferisce tra due corpi, o tra due parti
CORSO DI FISICA TECNICA Richiami di Calorimetria Introduzione al Corso Prof. Ing. Giulio Vannucci Calorimetria Calore Il calore è una forma di energia che si trasferisce tra due corpi, o tra due parti
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
LINEE GENERALI DEL PROGRAMMA DI FISICA DELLE CLASSI 3^AOEN E 3^BOEL DELL ANNO SCOLASTICO 2010/ QUADRIMESTRE
 Pagina 1 di 5 LINEE GENERALI DEL PROGRAMMA DI FISICA DELLE CLASSI 3^AOEN E 3^BOEL DELL ANNO SCOLASTICO 2010/2011 1 QUADRIMESTRE Studio delle grandezze termiche Studio dell azione termica sui corpi Studio
Pagina 1 di 5 LINEE GENERALI DEL PROGRAMMA DI FISICA DELLE CLASSI 3^AOEN E 3^BOEL DELL ANNO SCOLASTICO 2010/2011 1 QUADRIMESTRE Studio delle grandezze termiche Studio dell azione termica sui corpi Studio
Termodinamica: introduzione
 Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
Termodinamica: introduzione La Termodinamica studia i fenomeni che avvengono nei sistemi in seguito a scambi di calore (energia termica) ed energia meccanica, a livello macroscopico. Qualche concetto rilevante
Lezione 10. Cenni di Termodinamica. Temperatura e calore Definizione e misura della temperatura Calore Principi della Termodinamica
 Lezione 10 Cenni di Termodinamica Temperatura e calore Definizione e misura della temperatura Calore Principi della Termodinamica Trasporto del calore Fisica Generale per Architettura - G. Cantatore 1
Lezione 10 Cenni di Termodinamica Temperatura e calore Definizione e misura della temperatura Calore Principi della Termodinamica Trasporto del calore Fisica Generale per Architettura - G. Cantatore 1
Fisica dell Atmosfera e del Clima
 Università degli studi di rento Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile, Ambientale e Meccanica Fisica dell Atmosfera e del
Università degli studi di rento Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile, Ambientale e Meccanica Fisica dell Atmosfera e del
Temperatura, calore e prima legge termodinamica
 Temperatura, calore e prima legge termodinamica Principio di conservazione Energia ΔE tot = ΔE i = ΔT tot = ΔT j = L +Q +... Energia Termica - Calore Temperatura Conservazione energia Forme di energia
Temperatura, calore e prima legge termodinamica Principio di conservazione Energia ΔE tot = ΔE i = ΔT tot = ΔT j = L +Q +... Energia Termica - Calore Temperatura Conservazione energia Forme di energia
