SINOSSI DEL PROTOCOLLO
|
|
|
- Valentino Toscano
- 10 anni fa
- Просмотров:
Транскрипт
1 SINOSSI DEL PROTOCOLLO Codice e titolo del protocollo EGF114299: Studio di fase III per confrontare la sicurezza e l'efficacia di lapatinib più trastuzumab più un inibitore dell'aromatasi (IA) rispetto a trastuzumab più un IA rispetto a lapatinib più un IA come terapia di prima linea in pazienti in postmenopausa affette da carcinoma mammario metastatico (CMM) positive a recettori ormonali e per l'her2, che hanno ricevuto trastuzumab e una terapia endocrina in regime neoadiuvante e/o adiuvante. Fase di sviluppo III Data effettiva: 19-MAGGIO-2010 Razionale Quella alla mammella è la forma di cancro più comune e la seconda principale causa di morte per cancro (dopo il cancro al polmone) nelle donne [ACS, 2010]. Secondo le stime, nel 2008 in Europa vi sono stati nuovi casi e circa decessi per cancro alla mammella [Ferlay, 2010]. Negli Stati Uniti nel 2009 sono stati registrati nuovi casi di cancro mammario invasivo e oltre decessi [ACS, 2010] per cancro al seno. Nonostante i miglioramenti significativi nella diagnosi precoce, tutte le pazienti affette da CMM e fino al 40% di quelle che ricevono una terapia endocrina adiuvante subiscono una progressione della malattia che le porta alla morte, a dimostrazione del fatto che vi è una reale esigenza medica di terapie migliorate [Ring, 2003]. I dati dello studio condotto su lapatinib più letrozolo (EGF30008) [snda /S007, 2009] e dello studio su trastuzumab e anastrozolo nel carcinoma mammario ER-positivo e HER2-positivo (TaNDEM) [EMEA, 2007] hanno dimostrato che, per le pazienti affette da CMM, i cui tumori sono positivi per il recettore del fattore di crescita epidermico umano 2 (HER2) e per il recettore dell'ormone (HR+), la combinazione della terapia endocrina e di quella mirata per l'her2 costituisce una strategia migliore della sola terapia endocrina. Al momento non è noto quale sia la terapia migliore per le pazienti il cui cancro mammario si ripresenta dopo la terapia adiuvante con farmaci che bloccano l'her2. L'attuale protocollo, EGF114299, è disegnato per dimostrare un beneficio a livello di sopravvivenza globale (OS) ottenuto con lapatinib nelle pazienti HR+/HER2-positive precedentemente esposte a trastuzumab in regime neoadiuvante e/o adiuvante. Fornirà inoltre ulteriori dati per comprendere il ruolo della duplice soppressione dell'her2 in questa popolazione di pazienti. Questo studio arruolerà donne in post-menopausa con patologia ricorrente dopo terapia neoadiuvante e/o adiuvante, compresa terapia con trastuzumab ed endocrina, avviata come requisito successivo all'immissione in commercio con le autorità di regolamentazione. Obiettivo/i Obiettivo primario: Dimostrare la superiorità della combinazione di lapatinib/trastuzumab/inibitore dell'aromatasi (IA) rispetto alla combinazione di trastuzumab/ia per la sopravvivenza globale (OS) Pagina 1 di 9
2 Obiettivi secondari: Confrontare la sopravvivenza globale con trastuzumab/ia rispetto a lapatinib/ia e trastuzumab/lapatinib/ia rispetto a lapatinib/ia. Confrontare la sopravvivenza libera da progressione (PFS) con lapatinib/trastuzumab/ia rispetto a trastuzumab/ia e lapatinib/ia rispetto a trastuzumab/ia. Confrontare il tasso di risposta globale (risposta completa o parziale), il tempo alla risposta e la durata della risposta con lapatinib/trastuzumab/ia rispetto a trastuzumab/ia e lapatinib/ia rispetto a trastuzumab/ia.3 Confrontare il beneficio clinico (risposta completa, risposta parziale o malattia stabile per almeno 6 mesi) con lapatinib/trastuzumab/ia rispetto a trastuzumab/ia e lapatinib/ia rispetto a trastuzumab/ia. Valutare la sicurezza e la tollerabilità di tutti e tre i gruppi di trattamento (lapatinib/trastuzumab/ia, trastuzumab/ia o lapatinib/ia). Confrontare lapatinib/trastuzumab/ia rispetto a trastuzumab/ia e lapatinib/ia rispetto a trastuzumab/ia relativamente al cambiamento dello stato di qualità della vita (QoL) rispetto alla baseline. Obiettivi esplorativi: Ricerca traslazionale. Identificare i biomarcatori derivati dal tumore (DNA, RNA e proteine) associati al risultato clinico. Valutare i biomarcatori noti per predire la sensibilità o la resistenza a lapatinib e trastuzumab (ad es. p95her2, mutazioni PIK3CA, aberrazioni PTEN e altri marcatori associati con queste vie) e stabilire la relazione con il risultato clinico. Esaminare il DNA libero circolante (cfdna) prima e dopo il trattamento per stabilire se esistano delle correlazioni tra le mutazioni (ad es. PI3KCA) nel cfdna e quella nel tessuto tumorale da cui proviene. Ricerca farmacogenetica. Esaminare la relazione tra varianti genetiche nel DNA ospite e la sicurezza e tollerabilità di lapatinib e/o farmaci di confronto. Esaminare la relazione tra varianti genetiche nel DNA ospite e l'efficacia del trattamento con lapatinib e/o farmaci di confronto. Endpoint di efficacia Endpoint primario L'endpoint di efficacia primario di questo studio è la sopravvivenza globale valutata per la combinazione di lapatinib/trastuzumab/ia (Gruppo di trattamento A) rispetto alla combinazione di trastuzumab/ia (Gruppo di trattamento B). Per sopravvivenza globale si intende il periodo dalla randomizzazione al decesso per qualsiasi causa. Endpoint secondari Gli endpoint di efficacia secondari di questo studio sono: Sopravvivenza globale (OS) nel Gruppo di trattamento B (trastuzumab/ia) rispetto al Gruppo di trattamento C (lapatinib/ia) e nel Gruppo di trattamento A (trastuzumab/lapatinib/ia) rispetto al Gruppo di trattamento C (lapatinib/ia), definita come il periodo dalla randomizzazione al decesso per qualsiasi causa. Sopravvivenza libera da progressione (PFS) nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) e nel Gruppo di trattamento C (lapatinib/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia), definita come il periodo (in settimane) tra la data di Pagina 2 di 9
3 randomizzazione e la prima data di progressione della malattia o la data del decesso per qualsiasi causa, come stabilito dallo sperimentatore. Tasso di risposta globale (risposta completa o parziale), definito come la percentuale di soggetti che raggiungono una CR o una PR in base ai criteri RECIST 1.1 nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) e nel Gruppo di trattamento C (lapatinib/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) come stabilito dallo sperimentatore. Tempo alla risposta, definito come il periodo dalla randomizzazione alla prima evidenza documentata di PR o CR (qualunque sia lo stato registrato per primo) in base ai criteri RECIST 1.1 nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) e nel Gruppo di trattamento C (lapatinib/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) come stabilito dallo sperimentatore. Durata della risposta, definita, per i soggetti che ottengono una CR o una PR, come il periodo tra la prima evidenza documentata di PR o CR e il primo segno documentato di progressione della malattia o il decesso causato dal cancro mammario, se precedente, in base ai criteri RECIST 1.1 nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) e nel Gruppo di trattamento C (lapatinib/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) come stabilito dallo sperimentatore. Beneficio clinico nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia) e nel Gruppo di trattamento C (lapatinib/ia) rispetto al Gruppo di trattamento B (trastuzumab/ia), definito come percentuale di soggetti con evidenza di CR, PR o SD per almeno 6 mesi in base ai criteri RECIST 1.1 come stabilito dallo sperimentatore. Endpoint di sicurezza L'endpoint di sicurezza di questo studio è la valutazione della sicurezza e tollerabilità di tutti i tre gruppi di trattamento (lapatinib più trastuzumab più un IA, trastuzumab più un IA o lapatinib più un IA). Disegno dello studio Si tratta di uno studio in aperto a tre bracci. 525 soggetti in totale affetti da cancro mammario metastatico positivi all'her2 e al recettore dell'estrogeno (ER+) e/o positivi al recettore del progesterone (PgR+), già sottoposti a terapia con trastuzumab e terapia endocrina in un regime neoadiuvante e/o adiuvante e mai sottoposti a precedente trattamento per patologia metastatica, saranno sottoposti a screening per valutarne l'idoneità. I soggetti saranno randomizzati in uno dei tre bracci di trattamento, come segue: 1. Gruppo di trattamento A: lapatinib 1000 mg da assumere oralmente una volta al giorno più trastuzumab (dose di carico di 8 mg/kg) seguito da dose di mantenimento di 6mg/kg per via endovenosa ogni 3 settimane più un IA (letrozolo, anastrozolo o exemestane) a scelta dello sperimentatore da assumere oralmente una volta al giornoidential UM2010/00099/ Gruppo di trattamento B: trastuzumab (dose di carico di 8 mg/kg) seguito da dose di mantenimento di 6 mg/kg per via endovenosa ogni 3 settimane più un IA (letrozolo, anastrozolo o exemestane) a scelta dello sperimentatore da assumere per via orale una volta al giorno. Pagina 3 di 9
4 3. Gruppo di trattamento C: lapatinib 1500 mg da assumere oralmente una volta al giorno più un IA (letrozolo, anastrozolo o exemestane) a scelta dello sperimentatore da assumere oralmente una volta al giorno. I soggetti saranno stratificati sulla base della scelta dello sperimentatore per l'ia in studio (steroideo/non steroideo), il tempo dalla somministrazione di trastuzumab neoadiuvante e/o adiuvante (< 6 mesi/ 6 mesi) e le sedi della malattia (malattia dei tessuti molli/delle viscere vs. malattia solo ossea). L'endpoint di efficacia primario di questo studio è la sopravvivenza globale valutata per la combinazione lapatinib/trastuzumab/ia (Gruppo di trattamento A) rispetto alla combinazione di trastuzumab/ia (Gruppo di trattamento B). I soggetti proseguiranno con il trattamento dello studio fino alla progressione della malattia, al decesso o al manifestarsi di tossicità intollerabili. Dopo l'interruzione del trattamento dello studio, tutti i soggetti saranno seguiti per attestarne la sopravvivenza e la terapia anti-tumorale dopo lo studio, comprese radioterapia e chirurgia, ogni 12 settimane fino al decesso. Criteri di selezione dei soggetti Numero di soggetti Saranno randomizzati in totale 525 soggetti: 175 nel Gruppo di trattamento A, 175 nel Gruppo di trattamento B e 175 nel Gruppo di trattamento C. Fare riferimento alla Sezione del Protocollo per le assunzioni sulle dimensioni del campione. Criteri di inclusione Fare riferimento alle informazioni di prescrizione autorizzate per lapatinib [foglietto informativo TYKERB, 2010], trastuzumab [foglietto informativo HERCEPTIN, 2009], letrozolo [foglietto informativo FEMARA, 2010], anastrozolo [foglietto informativo ARIMIDEX, 2009] ed exemestane [foglietto informativo AROMASIN, 2008] per informazioni specifiche su avvertenze, precauzioni, controindicazioni, eventi avversi e altre informazioni pertinenti sui trattamenti dello studio che potrebbero influire sull'idoneità del soggetto. Non sono ammesse deviazioni dai criteri di inclusione, in quanto potenzialmente in grado di pregiudicare l'integrità scientifica dello studio, l'accettabilità a livello normativo o la sicurezza dei soggetti. Pertanto, è fondamentale l aderenza ai criteri specificati nel protocollo. I soggetti idonei per l'arruolamento nello studio devono soddisfare tutti i criteri seguenti: 1. Firma del consenso informato scritto. 2. Soggetti di sesso femminile in post-menopausa di età 18 anni. Post-menopausa definita da uno dei criteri seguenti: Età > 60 anni Età 45 anni con amenorrea > 12 mesi con utero intatto Precedente ooforectomia bilaterale o sterilizzazione mediante radiazioni con amenorrea da almeno 6 mesi Livelli di FSH e di estradiolo nel range previsto per la post-menopausa (in base ai range del laboratorio locale). Per i soggetti precedentemente trattati con un analogo del GnRH/LHRH, deve essere stata somministrata l'ultima iniezione >4 mesi prima della randomizzazione e il ciclo mestruale non deve più essere comparso Pagina 4 di 9
5 3. Cancro mammario invasivo di stadio IV confermato istologicamente. I soggetti possono presentare una malattia misurabile o non misurabile in base ai criteri di valutazione della risposta nei tumori solidi (RECIST 1.1) [Eisenhauer, 2009] 4. Tumori di tipo ER+ e/o PgR+ confermato dal laboratorio locale. 5. Documentazione di sovraespressione di HER2 o amplificazione genica, nel componente invasivo del tumore primario o della sede della patologia metastatica, definita come: 3+ tramite esame immunoistochimico (IHC) e/o Amplificazione genica HER2/neu tramite analisi di ibridazione in situ a fluorescenza, cromogenica o con argento [FISH, CISH o SISH; >6 copie di gene HER2/neu per nucleo o un rapporto di prova FISH, CISH o SISH (copie gene HER2 a segnali del cromosoma 17) 2,0] 6. il soggetto deve aver precedentemente assunto trastuzumab neoadiuvante e/o adiuvante. 7. il soggetto deve aver precedentemente ricevuto terapia endocrina neoadiuvante e/o adiuvante. 8. i soggetti deveno aver un aspettativa di vita > 6 mesi secondo la valutazione dello sperimentatore responsabile del trattamento. 9. Presenza di frazione di eiezione ventricolare sinistra (LVEF) alla baseline 50% misurata tramite ecocardiografia (ECHO) o angioscintigrafia miocardica (MUGA). 10. Stato di performance ECOG pari a 0-1 (Sezione 12.2 del Protocollo, Appendice2). 11. Tutte le tossicità legate a trattamenti precedenti devono essere CTCAE (versione 4.0) grado 1 [NCI, 2009] al momento della randomizzazione. 12. Completamento delle valutazioni di screening. 13. Funzionalità degli organi alla baseline adeguata, definita tramite (fare riferimento alla Tabella 1): Tabella 1 Valori di laboratorio alla baseline 1 Sistema Ematologico ANC Emoglobina Piastrine Epatico Albumina Bilirubina nel siero AST e ALT Renale Creatinina nel siero Clearance della creatinina calcolata 2 Valori di laboratorio 1,5 x 10 9 /l 9 g/dl (dopo trasfusione, se necessario) 100 x 10 9 /l 2,5 g/dl 1,5 x ULN o 2,5 x ULN con sindrome di Gilbert 3 x ULN 1,5 mg/dl o 132,6 mol/l OPPURE 40 ml/min 1. Per attestare l'idoneità del soggetto occorre impiegare i valori di laboratorio allo screening. Se necessario i valori di laboratorio possono essere nuovamente verificati, per confermare l'idoneità 2. Calcolata tramite il metodo di Cockcroft-Gault (fare riferimento alla Sezione 12.3 per maggiori dettagli). Pagina 5 di 9
6 Abbreviazioni: ANC, conta assoluta di neutrofili; ULN, limite superiore della norma; AST, aspartato aminotransferasi; ALT, alanina aminotransferasi. Soggetti francesi: in Francia un soggetto sarà idoneo all'inclusione nello studio solo se affiliato a o beneficiario di una categoria di previdenza sociale. Criteri di esclusione Non sono ammesse deviazioni dai criteri di esclusione, in quanto potenzialmente in grado di pregiudicare l'integrità scientifica dello studio, l'accettabilità a livello normativo o la sicurezza dei soggetti. Pertanto, è fondamentale l aderenza ai criteri specificati nel protocollo. Non devono essere arruolati nello studio i soggetti che soddisfano uno qualsiasi dei criteri seguenti: 1. Storia di un'altra neoplasia maligna. Eccezione: i soggetti che sono liberi dalla malattia da 5 anni o i soggetti con una storia di tumore cutaneo non-melanomatoso completamente asportato o di carcinoma in situ trattato con successo sono idonei. 2. Malattia viscerale sintomatica estesa, con coinvolgimento epatico e diffusione linfangitica polmonare del tumore, o con malattia considerata dallo sperimentatore in rapida progressione o potenzialmente mortale(soggetti destinati alla chemioterapia). 3. Precedente trattamento con chemioterapia, terapia ormonale, immunoterapia, terapia biologica o terapia anti-her2 per patologia avanzata o metastatica. 4. Patologia cardiaca o condizione medica grave, comprese, in via non limitativa: Aritmia incontrollata Angina incontrollata o sintomatica Storia di insufficienza cardiaca congestizia (CHF) Infarto miocardico documentato <6 mesi dall'ingresso nello studio 5. Storia nota o evidenza clinica di metastasi al sistema nervoso centrale (CNS) o carcinomatosi leptomeningea. 6. Patologia epatica o biliare attualmente attiva (fatta eccezione per soggetti con sindrome di Gilbert, colelitiasi asintomatica, metastasi al fegato o patologia epatica cronica stabile secondo la valutazione dello sperimentatore). 7. Patologia o condizione concomitante che potrebbe interferire con la partecipazione allo studio oppure qualsiasi disturbo medico grave in grado di interferire con la sicurezza del soggetto (ad esempio infezione attiva o incontrollata oppure qualsiasi condizione psichiatrica tale da impedire la comprensione o il rilascio del consenso informato). 8. Anomalia gastrointestinale clinicamente significativa, in grado di alterare l'assorbimento, come la sindrome da malassorbimento oppure resezione di ampia portata di stomaco o intestino. 9. Reazione nota di ipersensibilità immediata o ritardata o idiosincrasia a farmaci chimicamente correlati a un qualsiasi agente dello studio o ai relativi eccipienti e che, secondo lo sperimentatore o il responsabile medico di GSK, è controindicata per la partecipazione. 10. Assunzione di un qualsiasi farmaco vietato, come indicato nella Sezione 6.2 del Protocollo. 11. Assunzione di un farmaco sperimentale nei 30 giorni o nelle 5 emivite, Pagina 6 di 9
7 a seconda della condizione che si protrae più a lungo, precedenti la prima dose del trattamento dello studio. Valutazioni dello studio Le valutazioni delle lesioni definite tramite i criteri di valutazione della risposta nei tumori solidi 1.1(RECIST 1.1) saranno effettuate ogni 12 settimane e alla conclusione dello studio. Sicurezza e tollerabilità saranno valutate ogni 3 settimane per i primi 6 mesi (24 settimane), quindi ogni 6 settimane, tramite risultati di esami fisici di routine, segni vitali, analisi cliniche di laboratorio, monitoraggio e osservazioni di tipo clinico e report degli eventi avversi. Inoltre ogni 12 settimane sarà eseguito un monitoraggio cardiaco tramite ecocardiografia (ECHO) o scintigrafia miocardica (MUGA) ed elettrocardiogramma (ECG). Analisi dei dati e considerazioni statistiche Ipotesi L'obiettivo primario di questo studio è valutare e confrontare la OS in soggetti trattati con lapatinib/trastuzumab/ia (Gruppo di trattamento A) rispetto a quelli trattati con trastuzumab/ia (Gruppo di trattamento B). Lo studio è disegnato per fornire prove a supporto dell'ipotesi nulla H0: λ 1 o per rifiutarla a favore dell'ipotesi alternativa HA: λ < 1, dove λ è il rapporto di rischio tra il Gruppo di trattamento A e il Gruppo di trattamento B. In particolare, lo studio avrà il potere di rilevare un miglioramento del 42% nel rischio di morte (tasso di rischio di 0,70) in tutti i soggetti che ricevono lapatinib/trastuzumab/ia (mediana di 28,5 mesi) rispetto ai soggetti che ricevono trastuzumab/ia (mediana di 20 mesi). L'ipotesi sarà testata usando un test unilaterale per la superiorità con α=0,025. Assunzioni sulle dimensioni del campione Il calcolo delle dimensioni del campione è stato effettuato usando il software East, versione 5.1. Affinché il test abbia una potenza dell'80%, l'analisi per la OS sarà effettuata quando si saranno verificati eventi a sufficienza nel Gruppo di trattamento A (lapatinib/trastuzumab/ia) e nel Gruppo di trattamento B (trastuzumab/ia). Per mostrare un miglioramento del 42% (rapporto di rischio di 0,70) nella OS, il numero necessario di eventi totali per ottenere una potenza dell'80% di rifiuto dell'ipotesi nulla, se l'ipotesi alternativa è vera, è 249. Le assunzioni seguenti sono state fatte sulla stima delle dimensioni del campione necessarie: Distribuzioni della sopravvivenza esponenziali. Periodo di OS mediano di 20 e 28,5 mesi nei bracci trastuzumab/ia e lapatinib/trastuzumab/ia, rispettivamente, cioè un tasso di rischio pari a 0,701. Uno schema di randomizzazione 1:1 Un rischio monolaterale complessivo del 2,5% di erronea dichiarazione di superiorità di lapatinib/trastuzumab/ia in assenza di effettiva differenza di base (errore generale di tipo I). Tasso di incremento medio di 7 soggetti al mese. Nei 2 bracci sarà necessario un massimo di 249 soggetti con un evento (decesso): Gruppo di trattamento A e Gruppo di trattamento B. Per ottenere questo si prevede di dover arruolare un totale di 350 soggetti. Poiché questo studio comprende 3 bracci di trattamento, la durata massima prevista è di circa 6 anni. L'endpoint primario è il confronto dei due bracci di trattamento Pagina 7 di 9
8 lapatinib/trastuzumab/ia rispetto a trastuzumab/ia. Un terzo braccio di trattamento, lapatinib/ia, sarà inoltre arruolato per i confronti relativi all'endpoint secondario. La dimensione totale del campione è di circa 525 soggetti randomizzati con un rapporto1:1:1 per i 3 bracci (175 soggetti/braccio). La randomizzazione sarà stratificata per: 1. IA scelto dallo sperimentatore: steroideo / non-steroideo 2. Tempo trascorso dalla somministrazione di trastuzumab neoadiuvante e/o adiuvante: <6 mesi / 6 mesi 3. Sede/i della malattia alla baseline: tessuto molle o viscere / solo ossa Tutti i soggetti randomizzati saranno inclusi nelle analisi per testare le ipotesi di interesse, indipendentemente dalla lunghezza del follow-up o dal fatto che il trattamento sperimentale sia stato somministrato o meno (ossia i soggetti non saranno sostituiti). Fare riferimento alla Sezione del Protocollo per dettagli sulla gestione dei dati mancanti. Molti esponenti degli organi normativi esprimono dei dubbi sull'uso di un'analisi ad interim degli endpoint di efficacia, soprattutto nel caso in cui i dati sulla OS siano necessari per l'approvazione da parte delle autorità normative o per eventuali rimborsi. Pertanto, per studi nei quali i dati sulla OS sono essenziali, non è consigliata un'analisi ad interim (soprattutto per un endpoint alternativo, come la PFS) a causa delle implicazioni per la validità dei dati sulla OS dopo la divulgazione dei risultati di un'analisi ad interim positiva. Considerazioni sull'analisi dei dati Popolazioni dell'analisi La popolazione Intent-to-Treat (ITT) comprenderà tutti i soggetti randomizzati, indipendentemente dal fatto che il trattamento sia stato somministrato o meno. Questa popolazione sarà basata sul trattamento per il quale il soggetto è stato randomizzato e rappresenterà la popolazione primaria per l'analisi dei dati sull'efficacia. Qualsiasi soggetto che riceverà un numero di randomizzazione per il trattamento sarà considerato randomizzato. La popolazione Per-Protocol (PP) comprenderà tutti i soggetti randomizzati che riceveranno almeno una dose del trattamento dello studio e che rispetteranno rigorosamente il protocollo. Deviazioni di notevole entità dal protocollo, che escluderebbero i soggetti dalla popolazione PP, saranno definite e documentate nel Piano di reporting e analisi (RAP) prima del rilascio del database. La popolazione PP sarà usata per fornire un'analisi supportiva dei soli endpoint sulla OS. La popolazione PP non sarà analizzata se comprenderà oltre il 95% della popolazione ITT. La popolazione di sicurezza (SAFETY) comprenderà tutti i soggetti randomizzati che riceveranno almeno una dose del trattamento dello studio e sarà basata sul trattamento effettivo ricevuto, qualora differisca da quello per il quale il soggetto era stato randomizzato. Questa popolazione sarà impiegata per l'analisi dei dati sulla sicurezza clinica. Gli HER2+ (HER2+ ER+/PgR+) e ER+ e/o PgR+ confermati centralmente comprenderanno tutti i soggetti randomizzati con conferma centrale di HER2+ e ER+/PgR+. Questa popolazione sarà basata sul trattamento per il quale il soggetto era stato randomizzato, indipendentemente dal fatto che il trattamento sia stato somministrato o meno. Questa popolazione sarà impiegata per fornire analisi supportive agli endpoint di efficacia. Gli HER2+ ER+/PgR+ non saranno analizzati se questa popolazione comprenderà oltre il 95% della popolazione ITT. Set di dati di analisi Pagina 8 di 9
9 Il set di dati primari per la valutazione dell'efficacia sarà la popolazione ITT, nell'accezione di cui alla sezione del Protocollo. Gli endpoint basati sulle lesioni saranno a sola discrezione dello sperimentatore. Per questo studio non saranno effettuate valutazioni indipendenti dei dati sulle lesioni. Il set di dati primari per la valutazione della sicurezza sarà la popolazione SAFETY, nell'accezione di cui alla sezione del Protocollo. I dettagli completi sulle analisi di sensibilità saranno riportati nel RAP. Pagina 9 di 9
SINOSSI DELLO STUDIO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO
 SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
Espressione di geni specifici per un determinato tumore
 Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
16th World Conference on Lung Cancer (WCLC): highlights
 16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
SINOSSI. Studio di Fase II: Obiettivo primario Determinare l attività antitumorale della combinazione in termini di tempo alla progressione
 SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SEBASTIANO FILETTI. Dipartimento di Medicina Interna e Specialità Mediche. Università di Roma Sapienza, Roma
 SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
Specialità: Herceptin (Roche spa) Forma farmaceutica:
 TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
TRASTUZUMAB per l'indicazione: in associazione ad un inibitore dell aromatasi nel trattamento di pazienti in postmenopausa affetti da carcinoma mammario metastatico positivo per i recettori ormonali, non
Neoplasie della mammella - 2
 Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Sinossi di studio clinico Codice: GECP06/01 Pag. 1 di 5
 Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
Trials clinici. Disegni di studio
 Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Potenza dello studio e dimensione campionaria. Laurea in Medicina e Chirurgia - Statistica medica 1
 Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
Potenza dello studio e dimensione campionaria Laurea in Medicina e Chirurgia - Statistica medica 1 Introduzione Nella pianificazione di uno studio clinico randomizzato è fondamentale determinare in modo
Documento PTR n.212 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE
 SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE Studio prospettico, non interventistico, di coorte, sul rischio di tromboembolismo venoso (TEV) in pazienti sottoposti a un nuovo trattamento chemioterapico per
SINOSSI PROTOCOLLO STUDIO OSSERVAZIONALE Studio prospettico, non interventistico, di coorte, sul rischio di tromboembolismo venoso (TEV) in pazienti sottoposti a un nuovo trattamento chemioterapico per
Domande relative alla specializzazione in: Oncologia medica
 Domande relative alla specializzazione in: Oncologia medica Domanda #1 (codice domanda: n.541) : Cosa caratterizza il grado T2 del colangiocarcinoma? A: Interessamento del connettivo periduttale B: Coinvolgimento
Domande relative alla specializzazione in: Oncologia medica Domanda #1 (codice domanda: n.541) : Cosa caratterizza il grado T2 del colangiocarcinoma? A: Interessamento del connettivo periduttale B: Coinvolgimento
Le malattie cardiovascolari (MCV) sono la principale causa di morte nelle donne, responsabili del 54% dei decessi femminili in Europa
 Red Alert for Women s Heart Compendio DONNE E RICERCA CARDIOVASCOLARE Le malattie cardiovascolari (MCV) sono la principale causa di morte nelle donne, responsabili del 54% dei decessi femminili in Europa
Red Alert for Women s Heart Compendio DONNE E RICERCA CARDIOVASCOLARE Le malattie cardiovascolari (MCV) sono la principale causa di morte nelle donne, responsabili del 54% dei decessi femminili in Europa
La terapia medica primaria e adiuvante e il follow-up: le principali novità. a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati (Ferrara)
 Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
E.Molfese, P.Matteucci, A.Iurato, M. Fiore, L.E. Trodella, L. Poggesi, R.M. D Angelillo, E. Iannacone, L.Trodella!
 Il trattamento stereotassico delle lesioni surrenaliche in pazienti oligometastatici affetti da NSCLC: una promettente arma per il controllo locale di malattia?! E.Molfese, P.Matteucci, A.Iurato, M. Fiore,
Il trattamento stereotassico delle lesioni surrenaliche in pazienti oligometastatici affetti da NSCLC: una promettente arma per il controllo locale di malattia?! E.Molfese, P.Matteucci, A.Iurato, M. Fiore,
APPROCCIO RADIOTERAPICO
 Unità operativa di Radioterapia Azienda Ospedaliera di Parma APPROCCIO RADIOTERAPICO Dott.ssa Dell Anna Cristina TUMORI PRIMITIVI DELLA PARETE TORACICA Sono tumori eterogenei che possono prendere origine
Unità operativa di Radioterapia Azienda Ospedaliera di Parma APPROCCIO RADIOTERAPICO Dott.ssa Dell Anna Cristina TUMORI PRIMITIVI DELLA PARETE TORACICA Sono tumori eterogenei che possono prendere origine
 Indicatori di qualità nei carcinomi genitali femminili: ovaio e utero Serata di presentazione progetto Zonta Club Locarno 13.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in
Indicatori di qualità nei carcinomi genitali femminili: ovaio e utero Serata di presentazione progetto Zonta Club Locarno 13.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in
Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA. T. Mandarino (MMG ASL RMA )
 Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA T. Mandarino (MMG ASL RMA ) La Malattia di Alzheimer La malattia di Alzheimer è la forma più frequente
Il RUOLO DEL MEDICO DI MEDICINA GENERALE NELLA IDENTIFICAZIONE DELLE PERSONE CON SOSPETTA DEMENZA T. Mandarino (MMG ASL RMA ) La Malattia di Alzheimer La malattia di Alzheimer è la forma più frequente
Diagnosi precoce delle neoplasie del collo dell utero
 Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
POLITERAPIE NEL PAZIENTE ANZIANO. Dipartimento Farmaceutico Azienda USL di Reggio Emilia
 POLITERAPIE NEL PAZIENTE ANZIANO Dipartimento Farmaceutico Azienda USL di Reggio Emilia PAZIENTI ANZIANI Maggiori utilizzatori di farmaci per la presenza di polipatologie spesso croniche Ridotte funzionalità
POLITERAPIE NEL PAZIENTE ANZIANO Dipartimento Farmaceutico Azienda USL di Reggio Emilia PAZIENTI ANZIANI Maggiori utilizzatori di farmaci per la presenza di polipatologie spesso croniche Ridotte funzionalità
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO Titolo Numero di protocollo Studio multicentrico, in aperto, randomizzato e adattivo di palifosfamide-tris, un nuovo DNA crosslinker, in combinazione con chemioterapia con carboplatino
SINOSSI DEL PROTOCOLLO Titolo Numero di protocollo Studio multicentrico, in aperto, randomizzato e adattivo di palifosfamide-tris, un nuovo DNA crosslinker, in combinazione con chemioterapia con carboplatino
STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab. Sinossi del protocollo
 1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO
 STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO FAX: 0916552413 SITO WEB: www.gstu.it E-MAIL: [email protected] CRITERI
STUDIO OSSERVAZIONALE SULLA TERAPIA DELLA PATOLOGIA MAMMARIA INDOTTA DALLA MONOTERAPIA CON ANTIANDROGENO PURO PER ADENOCARCINOMA PROSTATICO FAX: 0916552413 SITO WEB: www.gstu.it E-MAIL: [email protected] CRITERI
VERIFICA DELLE IPOTESI
 VERIFICA DELLE IPOTESI Nella verifica delle ipotesi è necessario fissare alcune fasi prima di iniziare ad analizzare i dati. a) Si deve stabilire quale deve essere l'ipotesi nulla (H0) e quale l'ipotesi
VERIFICA DELLE IPOTESI Nella verifica delle ipotesi è necessario fissare alcune fasi prima di iniziare ad analizzare i dati. a) Si deve stabilire quale deve essere l'ipotesi nulla (H0) e quale l'ipotesi
la storia di HER2 Citogenetica e biologia molecolare dei tumori mammari: implicazioni cliniche HER2: Human Epidermal Receptor
 Citogenetica e biologia molecolare dei tumori mammari: implicazioni cliniche la storia di HER2 V. Martin 28 giugno 2011 HER2: Human Epidermal Receptor HER2 e carcinoma mammario alias c-erb, ERBB2, HER-
Citogenetica e biologia molecolare dei tumori mammari: implicazioni cliniche la storia di HER2 V. Martin 28 giugno 2011 HER2: Human Epidermal Receptor HER2 e carcinoma mammario alias c-erb, ERBB2, HER-
Allegato I. Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato I Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio Conclusioni scientifiche Vista la relazione di valutazione del comitato di valutazione
Allegato I Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio Conclusioni scientifiche Vista la relazione di valutazione del comitato di valutazione
CARTA INTESTATA DEL CENTRO CLINICO
 CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
Discarica di Ginestreto e possibili effetti sullo stato di salute dei residenti
 Discarica di Ginestreto e possibili effetti sullo stato di salute dei residenti Negli ultimi anni i cittadini residenti nel territorio vicino all area della discarica di Ginestreto del comune di Sogliano,
Discarica di Ginestreto e possibili effetti sullo stato di salute dei residenti Negli ultimi anni i cittadini residenti nel territorio vicino all area della discarica di Ginestreto del comune di Sogliano,
La valutazione del rischio chimico
 La valutazione del rischio chimico Introduzione Per sua stessa definizione, l agente chimico è una sostanza o un preparato di natura chimica. L agente chimico può presentarsi sotto forma di gas, vapore,
La valutazione del rischio chimico Introduzione Per sua stessa definizione, l agente chimico è una sostanza o un preparato di natura chimica. L agente chimico può presentarsi sotto forma di gas, vapore,
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO
 LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
Nella provincia di Latina sono diagnosticati in media ogni anno 98 casi ogni 100.000 uomini e 27 ogni 100.000 donne.
 TUMORE DEL POLMONE Nel periodo 27-211 sono stati registrati complessivamente in provincia di Latina 172 nuovi casi di tumore del polmone. E risultato al 1 posto in termini di frequenza fra le neoplasie
TUMORE DEL POLMONE Nel periodo 27-211 sono stati registrati complessivamente in provincia di Latina 172 nuovi casi di tumore del polmone. E risultato al 1 posto in termini di frequenza fra le neoplasie
Studio di ricerca clinica sul dolore da endometriosi. Il dolore che Lei sente è reale... anche se gli altri non possono vederlo.
 Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Studio di ricerca clinica sul dolore da endometriosi Il dolore che Lei sente è reale... anche se gli altri non possono vederlo. A822523 Lo studio SOLSTICE verrà condotto in circa 200 centri di ricerca
Raccolta prospettica di dati di rilevanza prognostica in pazienti con Leucemia Linfatica Cronica a cellule B.
 O-CLL1 CHRONIC LYMPHOCYTIC LEUKEMIA PROGNOSTIC FACTOR PROJECT Raccolta prospettica di dati di rilevanza prognostica in pazienti con Leucemia Linfatica Cronica a cellule B. O-CLL1-PROTOCOL Sinossi O-CLL1-sinossi,
O-CLL1 CHRONIC LYMPHOCYTIC LEUKEMIA PROGNOSTIC FACTOR PROJECT Raccolta prospettica di dati di rilevanza prognostica in pazienti con Leucemia Linfatica Cronica a cellule B. O-CLL1-PROTOCOL Sinossi O-CLL1-sinossi,
METASTASI UVEALI: ESPERIENZA DEGLI ULTIMI 10 ANNI
 METASTASI UVEALI: ESPERIENZA DEGLI ULTIMI 10 ANNI C.Mosci; F.Nasciuti Centro Specialistico di Oncologia Oculare Ente Ospedaliero Ospedali Galliera - Genova [email protected] XXVI RIUNIONE S.O.N.O.
METASTASI UVEALI: ESPERIENZA DEGLI ULTIMI 10 ANNI C.Mosci; F.Nasciuti Centro Specialistico di Oncologia Oculare Ente Ospedaliero Ospedali Galliera - Genova [email protected] XXVI RIUNIONE S.O.N.O.
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere
 Sperimentazione Clinica: ruolo e responsabilità dell Infermiere Fasi dello studio Disegni di ricerca sperimentale Barbara Gorini, Investigator Site Development Lead, Development Operations- Pfizer ITALIA
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere Fasi dello studio Disegni di ricerca sperimentale Barbara Gorini, Investigator Site Development Lead, Development Operations- Pfizer ITALIA
Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio
 Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio Conclusioni scientifiche Tenendo conto della valutazione del Comitato per
Allegato 1 Conclusioni scientifiche e motivazioni per la variazione dei termini dell autorizzazione all immissione in commercio Conclusioni scientifiche Tenendo conto della valutazione del Comitato per
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa TUMORE DEL SENO: FUNZIONA LA TERAPIA "ACCELERATA" "IL 94% DEI PAZIENTI GUARISCE CON I TEMPI DI CURA PIU' BREVI" Intermedia s.r.l. per la comunicazione integrata Via Malta,
Rassegna Stampa Comunicato stampa TUMORE DEL SENO: FUNZIONA LA TERAPIA "ACCELERATA" "IL 94% DEI PAZIENTI GUARISCE CON I TEMPI DI CURA PIU' BREVI" Intermedia s.r.l. per la comunicazione integrata Via Malta,
Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2015
 I numeri del cancro in Italia 2015 Ministero della Salute - Roma 24 Settembre 2015 Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2015 Carmine Pinto Presidente Nazionale AIOM I quesiti per
I numeri del cancro in Italia 2015 Ministero della Salute - Roma 24 Settembre 2015 Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2015 Carmine Pinto Presidente Nazionale AIOM I quesiti per
ONCOVIEW 2012. Istruzioni per la compilazione delle schede pazienti
 ONCOVIEW 2012 Istruzioni per la compilazione delle schede pazienti ONCOVIEW - COME SI COLLABORA Lo studio ONCOVIEW ha l obiettivo di fornire un quadro esaustivo ed approfondito delle terapie farmacologiche
ONCOVIEW 2012 Istruzioni per la compilazione delle schede pazienti ONCOVIEW - COME SI COLLABORA Lo studio ONCOVIEW ha l obiettivo di fornire un quadro esaustivo ed approfondito delle terapie farmacologiche
Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico
 Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico C. Cocco 1, B. Caruso 1, E. Fiorio 2 1 Laboratorio Analisi (sede di BT) 2 Oncologia (sede di BT), AOUI,
Il ruolo di CA15-3 nel monitoraggio della terapia nel carcinoma mammario metastatico: un caso clinico C. Cocco 1, B. Caruso 1, E. Fiorio 2 1 Laboratorio Analisi (sede di BT) 2 Oncologia (sede di BT), AOUI,
SINOSSI DEL PROTOCCOLO
 Protocollo GO27821, versione 2 SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II, RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA
Protocollo GO27821, versione 2 SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II, RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
coin lesion polmonare
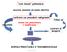 coin lesion polmonare accurata anamnesi ed esame obiettivo impossibile confronto con precedenti radiogrammi lesione non preesistente o modificatasi TC Follow-up caratteri di benignità lesione sospetta
coin lesion polmonare accurata anamnesi ed esame obiettivo impossibile confronto con precedenti radiogrammi lesione non preesistente o modificatasi TC Follow-up caratteri di benignità lesione sospetta
ABRAXANE (nab-paclitaxel) - Carcinoma pancreas esocrino
 Campo obbligatorio ai fini dell'eleggibilità Campo obbligatorio ABRAXAN (nab-paclitaxel) - Carcinoma pancreas esocrino Abraxane in associazione con gemcitabina è indicato per il trattamento di prima linea
Campo obbligatorio ai fini dell'eleggibilità Campo obbligatorio ABRAXAN (nab-paclitaxel) - Carcinoma pancreas esocrino Abraxane in associazione con gemcitabina è indicato per il trattamento di prima linea
Informazioni per potenziali partecipanti. Possiamo sciogliere l'amiloidosi AL?
 Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
Scritto da Giovanni Creton Domenica 27 Febbraio 2011 17:32 - Ultimo aggiornamento Domenica 27 Marzo 2011 19:43
 E evidente che lo screening per un tumore può diagnosticare la malattia molto precocemente, ma nel caso del tumore alla prostata il ricorso al test del PSA può creare dati incerti e rischi sanitari in
E evidente che lo screening per un tumore può diagnosticare la malattia molto precocemente, ma nel caso del tumore alla prostata il ricorso al test del PSA può creare dati incerti e rischi sanitari in
PIANO TERAPEUTICO AIFA PER PRESCRIZIONE DI CLOPIDOGREL
 20-3-2009 GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale - n. 66 ALLEGATO 1 PIANO TERAPEUTICO AIFA PER PRESCRIZIONE DI CLOPIDOGREL Centro prescrittore Nome cognome del clinico prescrittore
20-3-2009 GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale - n. 66 ALLEGATO 1 PIANO TERAPEUTICO AIFA PER PRESCRIZIONE DI CLOPIDOGREL Centro prescrittore Nome cognome del clinico prescrittore
L uso della Lofexidina nei contesti clinici italiani: lo studio DETOX
 L uso della Lofexidina nei contesti clinici italiani: lo studio DETOX dott. Marco Riglietta direttore Dipartimento delle Dipendenze Roma -5 ottobre 03 FEDERSERD V congresso nazionale Il protocollo Obiettivo(i)
L uso della Lofexidina nei contesti clinici italiani: lo studio DETOX dott. Marco Riglietta direttore Dipartimento delle Dipendenze Roma -5 ottobre 03 FEDERSERD V congresso nazionale Il protocollo Obiettivo(i)
Screening dei soggetti a rischio e diagnostica molecolare
 Screening dei soggetti a rischio e diagnostica molecolare Daniela Furlan U.O. Anatomia Patologica Varese, 3 luglio 2012 Il carcinoma pancreatico Patogenesi Suscettibilità genetica Implicazioni diagnostiche
Screening dei soggetti a rischio e diagnostica molecolare Daniela Furlan U.O. Anatomia Patologica Varese, 3 luglio 2012 Il carcinoma pancreatico Patogenesi Suscettibilità genetica Implicazioni diagnostiche
GESTIONE DEL RISCHIO NEI DISPOSITIVI MEDICI: DALLA CLASSIFICAZIONE ALLA COMMERCIALIZZAZIONE
 1 GESTIONE DEL RISCHIO NEI DISPOSITIVI MEDICI: DALLA CLASSIFICAZIONE ALLA COMMERCIALIZZAZIONE Ing. Enrico Perfler Eudax s.r.l. Milano, 23 Gennaio 2014 Indice 2 Il concetto di rischio nei dispositivi medici
1 GESTIONE DEL RISCHIO NEI DISPOSITIVI MEDICI: DALLA CLASSIFICAZIONE ALLA COMMERCIALIZZAZIONE Ing. Enrico Perfler Eudax s.r.l. Milano, 23 Gennaio 2014 Indice 2 Il concetto di rischio nei dispositivi medici
7 domande sui tumori. Convivere con la malattia
 1. 7 domande sui tumori 2. Convivere con la malattia Dott. Andrea Angelo Martoni Direttore Unità Operativa di Oncologia Medica Policlinico S.Orsola-Malpighi Bologna 1. Cosa sono i tumori? i tumori Malattia
1. 7 domande sui tumori 2. Convivere con la malattia Dott. Andrea Angelo Martoni Direttore Unità Operativa di Oncologia Medica Policlinico S.Orsola-Malpighi Bologna 1. Cosa sono i tumori? i tumori Malattia
Il ragionamento diagnostico TEST DIAGNOSTICO. Dott.ssa Marta Di Nicola. L accertamento della condizione patologica viene eseguito TEST DIAGNOSTICO
 Il ragionamento diagnostico http://www.biostatistica biostatistica.unich unich.itit 2 L accertamento della condizione patologica viene eseguito All'inizio del decorso clinico, per una prima diagnosi In
Il ragionamento diagnostico http://www.biostatistica biostatistica.unich unich.itit 2 L accertamento della condizione patologica viene eseguito All'inizio del decorso clinico, per una prima diagnosi In
Statistica. Lezione 6
 Università degli Studi del Piemonte Orientale Corso di Laurea in Infermieristica Corso integrato in Scienze della Prevenzione e dei Servizi sanitari Statistica Lezione 6 a.a 011-01 Dott.ssa Daniela Ferrante
Università degli Studi del Piemonte Orientale Corso di Laurea in Infermieristica Corso integrato in Scienze della Prevenzione e dei Servizi sanitari Statistica Lezione 6 a.a 011-01 Dott.ssa Daniela Ferrante
Il rischio cancerogeno e mutageno
 Il rischio cancerogeno e mutageno Le sostanze cancerogene Un cancerogeno è un agente capace di provocare l insorgenza del cancro o di aumentarne la frequenza in una popolazione esposta. Il cancro è caratterizzato
Il rischio cancerogeno e mutageno Le sostanze cancerogene Un cancerogeno è un agente capace di provocare l insorgenza del cancro o di aumentarne la frequenza in una popolazione esposta. Il cancro è caratterizzato
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO TITOLO DELLO STUDIO: CODICE DEL PROTOCOLLO: SPONSOR: FASE DELLO STUDIO: CENTRI PARTECIPANTI ALLO STUDIO: PERIODO DI STUDIO PIANIFICATO (PRIMO ARRUOLAMENTO ULTIMO PAZIENTE USCITO
SINOSSI DEL PROTOCOLLO TITOLO DELLO STUDIO: CODICE DEL PROTOCOLLO: SPONSOR: FASE DELLO STUDIO: CENTRI PARTECIPANTI ALLO STUDIO: PERIODO DI STUDIO PIANIFICATO (PRIMO ARRUOLAMENTO ULTIMO PAZIENTE USCITO
Indicatori sulla terapia di oncologia medica
 Indicatori sulla terapia di oncologia medica Michela Donadio Oncologia Medica Senologica Azienda Ospedaliera Città della Salute e della Scienza di Torino Torino, 2 dicembre 20 Terapie mediche neoad/adiuvanti:
Indicatori sulla terapia di oncologia medica Michela Donadio Oncologia Medica Senologica Azienda Ospedaliera Città della Salute e della Scienza di Torino Torino, 2 dicembre 20 Terapie mediche neoad/adiuvanti:
TAILOR AIFA TArceva Italian Lung Optimization trial
 H TAILR AIFA TArceva Italian Lung ptimization trial ttimizzazione dell erlotinib per il trattamento di pazienti con tumore del polmone avanzato non a piccole cellule: uno studio italiano randomizzato SISSI
H TAILR AIFA TArceva Italian Lung ptimization trial ttimizzazione dell erlotinib per il trattamento di pazienti con tumore del polmone avanzato non a piccole cellule: uno studio italiano randomizzato SISSI
ANNO MASCHI FEMMINE TOTALE TOTALE 1974 2513 4487
 MORTALITÀ Tra i residenti della ULSS n. 1 nel corso del triennio 2010-2012 si sono verificati 4487 decessi (1974 nei maschi e 2513 nelle femmine, media per anno 1496), in leggero aumento rispetto al dato
MORTALITÀ Tra i residenti della ULSS n. 1 nel corso del triennio 2010-2012 si sono verificati 4487 decessi (1974 nei maschi e 2513 nelle femmine, media per anno 1496), in leggero aumento rispetto al dato
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza
 Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
FINASTERIDE ZENTIVA 5 MG COMPRESSE RIVESTITE CON FILM. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA FINASTERIDE ZENTIVA 5 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA FINASTERIDE ZENTIVA 5 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
Il sale è un elemento fondamentale per l alimentazione umana ed è costituito da cloruro di sodio (NaCl). Una sua eccessiva introduzione però può
 Sale e salute Il sale è un elemento fondamentale per l alimentazione umana ed è costituito da cloruro di sodio (NaCl). Una sua eccessiva introduzione però può causare gravi problemi alla salute. La quantità
Sale e salute Il sale è un elemento fondamentale per l alimentazione umana ed è costituito da cloruro di sodio (NaCl). Una sua eccessiva introduzione però può causare gravi problemi alla salute. La quantità
Premessa. Tratto da American Heart Journal 2004; 147: 705-712
 Effetti del cambiamento di terapia con statine sul raggiungimento delle concentrazioni lipidiche ottimali: lo studio Measuring Effective Reductions in Cholesterol Using Rosuvastatin Therapy (MERCURY I)
Effetti del cambiamento di terapia con statine sul raggiungimento delle concentrazioni lipidiche ottimali: lo studio Measuring Effective Reductions in Cholesterol Using Rosuvastatin Therapy (MERCURY I)
004-IRCC-10IIS-12 Versione del Protocollo Finale 1.0 27 aprile 2012. Trastuzumab. Pertuzumab Formulazione orale. Roche
 1 SINOSSI Titolo del protocollo: Numero del protocollo: Studio in aperto, di fase II, della combinazione trastuzumab e lapatinib o pertuzumab e trastuzumab in pazienti con carcinoma del colon retto metastatico
1 SINOSSI Titolo del protocollo: Numero del protocollo: Studio in aperto, di fase II, della combinazione trastuzumab e lapatinib o pertuzumab e trastuzumab in pazienti con carcinoma del colon retto metastatico
Ricerca farmacologica priclinica e clinica
 Ricerca farmacologica priclinica e clinica SPERIMENTAZIONE PRECLINICA DURATA MEDIA?? ANNI Consente di isolare, dalle migliaia di sostanze sottoposte al primo screening di base farmacologico e biochimico,
Ricerca farmacologica priclinica e clinica SPERIMENTAZIONE PRECLINICA DURATA MEDIA?? ANNI Consente di isolare, dalle migliaia di sostanze sottoposte al primo screening di base farmacologico e biochimico,
STUDI SU MATERIALE GENETICO
 Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
PSA SCREENING NEL TUMORE DELLA PROSTATA
 PSA SCREENING NEL TUMORE DELLA PROSTATA Prof. Giuseppe Martorana Clinica Urologica Alma Mater Studiorum Università di Bologna Convegno medico UniSalute Appropriatezza ed efficacia degli screening Bologna,
PSA SCREENING NEL TUMORE DELLA PROSTATA Prof. Giuseppe Martorana Clinica Urologica Alma Mater Studiorum Università di Bologna Convegno medico UniSalute Appropriatezza ed efficacia degli screening Bologna,
IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici genovesi
 Università degli Studi di Genova Facoltà di Medicina e Chirurgia IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici
Università degli Studi di Genova Facoltà di Medicina e Chirurgia IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici
Allegato II Conclusioni scientifiche e motivi della modifica di riassunto delle caratteristiche del prodotto
 Allegato II Conclusioni scientifiche e motivi della modifica di riassunto delle caratteristiche del prodotto, etichettatura e foglio illustrativo presentati dall Agenzia europea per i medicinali 6 Conclusioni
Allegato II Conclusioni scientifiche e motivi della modifica di riassunto delle caratteristiche del prodotto, etichettatura e foglio illustrativo presentati dall Agenzia europea per i medicinali 6 Conclusioni
Il programma si compone di due ricerche internazionali sulle valutazioni legate all assistenza degli individui affetti da tali patologie.
 Keeping Care Complete Sintesi dei risultati internazionali Keeping Care Complete ha l obiettivo di esaminare e creare consapevolezza circa le questioni emotive e sociali associate al trattamento e all
Keeping Care Complete Sintesi dei risultati internazionali Keeping Care Complete ha l obiettivo di esaminare e creare consapevolezza circa le questioni emotive e sociali associate al trattamento e all
Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia
 EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
Risultati del triage e del follow-up post-trattamento con HPV-DNA test
 Lo screening per la prevenzione dei tumori della cervice uterina in Emilia Romagna Risultati del triage e del follow-up post-trattamento con HPV-DNA test Bologna, 29 marzo 2011 HPV TEST NEL TRIAGE DI ASC-US
Lo screening per la prevenzione dei tumori della cervice uterina in Emilia Romagna Risultati del triage e del follow-up post-trattamento con HPV-DNA test Bologna, 29 marzo 2011 HPV TEST NEL TRIAGE DI ASC-US
PROGETTAZIONE E ORGANIZZAZIONE DI UN PROGRAMMA DI SCREENING. Relatore: Brunella Spadafora
 PROGETTAZIONE E ORGANIZZAZIONE DI UN PROGRAMMA DI SCREENING Relatore: Brunella Spadafora Epidemiologia e prevenzione dei tumori maligni I tumori nel loro insieme, costituiscono la seconda causa di morte,
PROGETTAZIONE E ORGANIZZAZIONE DI UN PROGRAMMA DI SCREENING Relatore: Brunella Spadafora Epidemiologia e prevenzione dei tumori maligni I tumori nel loro insieme, costituiscono la seconda causa di morte,
LE NEOPLASIE DIFFERENZIATE DELLA TIROIDE Paolo Fracchia SOC ORL ASL AL Casale Monferrato
 LE NEOPLASIE DIFFERENZIATE DELLA TIROIDE Paolo Fracchia SOC ORL ASL AL Casale Monferrato 19 marzo-2 aprile 2011 INTRODUZIONE Il carcinoma papillare ed il carcinoma follicolare della tiroide, definiti carcinomi
LE NEOPLASIE DIFFERENZIATE DELLA TIROIDE Paolo Fracchia SOC ORL ASL AL Casale Monferrato 19 marzo-2 aprile 2011 INTRODUZIONE Il carcinoma papillare ed il carcinoma follicolare della tiroide, definiti carcinomi
ANALISI CRITICA DELLA DOCUMENTAZIONE TECNICA RELATIVA ALLA CENTRALE TERMOELETTRICA DI QUILIANO E VADO LIGURE
 6.1 Salute umana Dall analisi della documentazione di progetto sottoposta ad autorizzazione emerge come la tematica della Salute Umana sia stata affrontata in modo inadeguato, ovvero con estrema superficialità
6.1 Salute umana Dall analisi della documentazione di progetto sottoposta ad autorizzazione emerge come la tematica della Salute Umana sia stata affrontata in modo inadeguato, ovvero con estrema superficialità
Conoscere per Vincere Il Rotary per la prevenzione Sanitaria. Giuseppe Failla R.C.Ct & Giovanni Urso R.C. Ct Nord
 Conoscere per Vincere Il Rotary per la prevenzione Sanitaria Giuseppe Failla R.C.Ct & Giovanni Urso R.C. Ct Nord Qualche numero Sul territorio nazionale: Incidenza CRC: 52.000 nuovi casi diagnosticati
Conoscere per Vincere Il Rotary per la prevenzione Sanitaria Giuseppe Failla R.C.Ct & Giovanni Urso R.C. Ct Nord Qualche numero Sul territorio nazionale: Incidenza CRC: 52.000 nuovi casi diagnosticati
DIFETTI VISIVI NEI BAMBINI AFFETTI DALLA SINDROME DOWN
 DIFETTI VISIVI NEI BAMBINI AFFETTI DALLA SINDROME DOWN DADDY FADEL OPTOMETRISTA Nel 1866 John Langdon Down ha descritto per la prima volta la sindrome che porta il suo nome. Nel 1959 Lejeune et al. hanno
DIFETTI VISIVI NEI BAMBINI AFFETTI DALLA SINDROME DOWN DADDY FADEL OPTOMETRISTA Nel 1866 John Langdon Down ha descritto per la prima volta la sindrome che porta il suo nome. Nel 1959 Lejeune et al. hanno
Tabella iniziale con i dati. Malattia Malati Non malati Totale Test Positivo 183 Negativo 280 Totale 199 512. Calcolo i valori mancanti per differenza
 ESERCIZIO DI STATISTICA D.U. / simulazione di esame Esercizio 1: Per una malattia particolarmente grave viene sperimentato l utilizzo di una nuova tecnica radiologica allo scopo di identificare correttamente
ESERCIZIO DI STATISTICA D.U. / simulazione di esame Esercizio 1: Per una malattia particolarmente grave viene sperimentato l utilizzo di una nuova tecnica radiologica allo scopo di identificare correttamente
LA ASL DELLA PROVINCIA DI VARESE PER LA DIAGNOSI PRECOCE DEL TUMORE DEL COLON RETTO AGGIORNAMENTO AL 30 APRILE 2008
 LA ASL DELLA PROVINCIA DI VARESE PER LA DIAGNOSI PRECOCE DEL TUMORE DEL COLON RETTO AGGIORNAMENTO AL 30 APRILE 2008 Dal luglio 2006 è iniziato il programma di screening del cancro del colon retto organizzato
LA ASL DELLA PROVINCIA DI VARESE PER LA DIAGNOSI PRECOCE DEL TUMORE DEL COLON RETTO AGGIORNAMENTO AL 30 APRILE 2008 Dal luglio 2006 è iniziato il programma di screening del cancro del colon retto organizzato
STATISTICA IX lezione
 Anno Accademico 013-014 STATISTICA IX lezione 1 Il problema della verifica di un ipotesi statistica In termini generali, si studia la distribuzione T(X) di un opportuna grandezza X legata ai parametri
Anno Accademico 013-014 STATISTICA IX lezione 1 Il problema della verifica di un ipotesi statistica In termini generali, si studia la distribuzione T(X) di un opportuna grandezza X legata ai parametri
CAPITOLO 8 LA VERIFICA D IPOTESI. I FONDAMENTI
 VERO FALSO CAPITOLO 8 LA VERIFICA D IPOTESI. I FONDAMENTI 1. V F Un ipotesi statistica è un assunzione sulle caratteristiche di una o più variabili in una o più popolazioni 2. V F L ipotesi nulla unita
VERO FALSO CAPITOLO 8 LA VERIFICA D IPOTESI. I FONDAMENTI 1. V F Un ipotesi statistica è un assunzione sulle caratteristiche di una o più variabili in una o più popolazioni 2. V F L ipotesi nulla unita
Atrial Fibrillation Study - Italy Study conducted by Opinion Health
 Atrial Fibrillation Study - Italy Study conducted by Opinion Health Obiettivi Valutare il livello di awareness della FA e dei sintomi Comprendere l impatto della FA e del trattamento sulla qualità di vita
Atrial Fibrillation Study - Italy Study conducted by Opinion Health Obiettivi Valutare il livello di awareness della FA e dei sintomi Comprendere l impatto della FA e del trattamento sulla qualità di vita
Quando il dolore è ancora un problema. XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013
 Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Lo sviluppo del cancro è un processo complesso che coinvolge parecchi cambiamenti nella stessa cellula staminale. Poiché tutte le cellule staminali
 Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
Concetto di potenza statistica
 Calcolo della numerosità campionaria Prof. Giuseppe Verlato Sezione di Epidemiologia e Statistica Medica, Università di Verona Concetto di potenza statistica 1 Accetto H 0 Rifiuto H 0 Ipotesi Nulla (H
Calcolo della numerosità campionaria Prof. Giuseppe Verlato Sezione di Epidemiologia e Statistica Medica, Università di Verona Concetto di potenza statistica 1 Accetto H 0 Rifiuto H 0 Ipotesi Nulla (H
Statistiche campionarie
 Statistiche campionarie Sul campione si possono calcolare le statistiche campionarie (come media campionaria, mediana campionaria, varianza campionaria,.) Le statistiche campionarie sono stimatori delle
Statistiche campionarie Sul campione si possono calcolare le statistiche campionarie (come media campionaria, mediana campionaria, varianza campionaria,.) Le statistiche campionarie sono stimatori delle
Educazione alla Salute Alimentazione e Movimento nella Scuola Primaria: Misurare il cambiamento
 Protocollo n. 26/DDA/2012 Oggetto: progettualità per la valutazione, formazione, educazione alimentare e motoria Educazione alla Salute Alimentazione e Movimento nella Scuola Primaria: Misurare il cambiamento
Protocollo n. 26/DDA/2012 Oggetto: progettualità per la valutazione, formazione, educazione alimentare e motoria Educazione alla Salute Alimentazione e Movimento nella Scuola Primaria: Misurare il cambiamento
VALUTAZIONE EPIDEMIOLOGICA DELLO STATO DI SALUTE DELLA POPOLAZIONE RESIDENTE NEI COMUNI DI CIVITAVECCHIA, ALLUMIERE, TARQUINIA, TOLFA E SANTA
 VALUTAZIONE EPIDEMIOLOGICA DELLO STATO DI SALUTE DELLA POPOLAZIONE RESIDENTE NEI COMUNI DI CIVITAVECCHIA, ALLUMIERE, TARQUINIA, TOLFA E SANTA MARINELLA Febbraio, 2012 Dipartimento di Epidemiologia del
VALUTAZIONE EPIDEMIOLOGICA DELLO STATO DI SALUTE DELLA POPOLAZIONE RESIDENTE NEI COMUNI DI CIVITAVECCHIA, ALLUMIERE, TARQUINIA, TOLFA E SANTA MARINELLA Febbraio, 2012 Dipartimento di Epidemiologia del
 Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
Agenzia Italiana del Farmaco Bando di assegnazione di finanziamento per la Ricerca indipendente sui farmaci Area 2 - Studi comparativi fra farmaci e strategie farmacologiche Art. 48, commi 5 lett. g) e
Tumore del collo dell utero e screening citologico in Veneto
 Regione del Veneto Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Corso regionale sulla rosolia congenita e nuove strategie di prevenzione Villafranca, 5 ottobre 2007 Tumore
Regione del Veneto Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Corso regionale sulla rosolia congenita e nuove strategie di prevenzione Villafranca, 5 ottobre 2007 Tumore
Università del Piemonte Orientale. Corsi di Laurea Triennale. Corso di Statistica e Biometria. Elementi di Epidemiologia
 Università del Piemonte Orientale Corsi di Laurea Triennale Corso di Statistica e Biometria Elementi di Epidemiologia Corsi di Laurea Triennale Corso di Statistica e Biometria: Elementi di epidemiologia
Università del Piemonte Orientale Corsi di Laurea Triennale Corso di Statistica e Biometria Elementi di Epidemiologia Corsi di Laurea Triennale Corso di Statistica e Biometria: Elementi di epidemiologia
Scritto da RyderItalia Mercoledì 12 Maggio 2010 11:19 - Ultimo aggiornamento Mercoledì 03 Novembre 2010 15:57
 LA TERAPIA METRONOMICA Per oltre mezzo secolo, la terapia sistemica per i tumori è stata caratterizzata dalla somministrazione dei farmaci chemioterapici. La maggior parte di questi farmaci ha lo scopo
LA TERAPIA METRONOMICA Per oltre mezzo secolo, la terapia sistemica per i tumori è stata caratterizzata dalla somministrazione dei farmaci chemioterapici. La maggior parte di questi farmaci ha lo scopo
Igiene. Dott. Pamela Di Giovanni. Definizione
 Igiene Dott. Pamela Di Giovanni Definizione Disciplina medica che ha come obiettivo la tutela e la promozione della salute umana, intendendo per salute umana un completo stato di benessere psichico, fisico
Igiene Dott. Pamela Di Giovanni Definizione Disciplina medica che ha come obiettivo la tutela e la promozione della salute umana, intendendo per salute umana un completo stato di benessere psichico, fisico
Finanziamento di Progetti di Ricerca in Oncologia. Bando interno per l anno 2013
 < Finanziamento di Progetti di Ricerca in Oncologia Bando interno per l anno 2013 La Direzione Scientifica emana per l anno 2013 un bando interno per finanziare mediante il budget della Ricerca Corrente
< Finanziamento di Progetti di Ricerca in Oncologia Bando interno per l anno 2013 La Direzione Scientifica emana per l anno 2013 un bando interno per finanziare mediante il budget della Ricerca Corrente
Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons
 Allegato 1 Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons 1. Premessa La rilevazione della customer satisfaction è utilizzata da molte amministrazioni per misurare
Allegato 1 Linee guida per la rilevazione sistematica della customer satisfaction tramite emoticons 1. Premessa La rilevazione della customer satisfaction è utilizzata da molte amministrazioni per misurare
DIFFERENZA DI GENERE E MEDICINA
 DIFFERENZA DI GENERE E MEDICINA L ONU, l Europa e l OMS raccomandano che il determinante genere sia tenuto presente nella programmazione delle politiche sanitarie. L ONU ha inserito la medicina di genere
DIFFERENZA DI GENERE E MEDICINA L ONU, l Europa e l OMS raccomandano che il determinante genere sia tenuto presente nella programmazione delle politiche sanitarie. L ONU ha inserito la medicina di genere
I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese
 I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese Daniela Furlan U.O. Anatomia Patologica, Ospedale di Circolo e Fondazione Macchi, Varese Il
I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese Daniela Furlan U.O. Anatomia Patologica, Ospedale di Circolo e Fondazione Macchi, Varese Il
ESERCITAZIONE. CdL Fisioterapia e Podologia. 25 novembre 2015
 ESERCITAZIONE CdL Fisioterapia e Podologia 25 novembre 2015 Epidemiologia Domanda 1 Le neoplasie gastriche sono: a. diminuite in tutta Europa b. diminuite fino agli anni 80, poi stabili c. aumentate in
ESERCITAZIONE CdL Fisioterapia e Podologia 25 novembre 2015 Epidemiologia Domanda 1 Le neoplasie gastriche sono: a. diminuite in tutta Europa b. diminuite fino agli anni 80, poi stabili c. aumentate in
Le interazioni farmacologiche come causa di reazioni avverse da farmaci
 Le interazioni farmacologiche come causa di reazioni avverse da farmaci Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza
Le interazioni farmacologiche come causa di reazioni avverse da farmaci Corso per farmacisti operanti nei punti di erogazione diretta delle Aziende Sanitarie della Regione Emilia-Romagna AUSL Piacenza
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? 2. Come nasce la sperimentazione clinica e che tipi di studi esistono?
 STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
