e il futuro Anna Maria Marata Roma 25 giugno 2015
|
|
|
- Ada Rizzo
- 7 anni fa
- Visualizzazioni
Transcript
1 Biosimilari: i il i il presente e il futuro Anna Maria Marata Roma 25 giugno 2015
2 Biosimilari: sviluppo di LG/aspetti regolatori nel mondo
3 Biosimilari in uso in Italia dal PASSATO PRESENTE FUTURO Biosimilari di EPO alfa Binocrit Sandoz 28 agosto 2007 Retacrit Hospira 18 dicembre 2007 Biosimilari di genotropin Omnitrope Sandoz 12 April 2006 Biosimilari di filgrastim Nivestim Hospira 8 giugno 2010 Tevagrastim 15 Settembre 2008 Zarzio Sandoz 6 febbraio 2009
4 Uso di biosimilari in Italia DDD % Fonte: Ministero della Salute tracciabilità del farmaco
5 Uso di biosimilari in Italia DDD % Fattori di crescita terapia di supporto per tempi limitati unica indicazione! 3 biosimilari disponibili 1 aveva solo studi di P.K. (Zarzio ) Utilizzo 2014: Zarzio 70% Variabilità region. (91 % - 3%) Fonte: Ministero della Salute tracciabilità del farmaco
6 Uso di biosimilari in Italia DDD % GH terapia di fondo uso continuato unica indicazione i uso prevalente pediatrico 1 biosimilare disponibile ha studi di efficacia Utilizzo 2014 stabile/lieve Variabilità reg. (23 % - 0%) Fonte: Ministero della Salute tracciabilità del farmaco
7 Uso di biosimilari in Italia DDD % Epoetine terapia di supporto uso continuato/limitato indicazioni multiple Timore di PRCA!! 2 biosimilarii il i disponibiliibili estrapolazione delle indicazioni Utilizzo lieve (+7%) Variabilità reg. (62 % - 4%) Fonte: Ministero della Salute tracciabilità del farmaco
8 Epoetine Studi sulla sicurezza Filgrastim
9 Biosimilari: correlazione fra consumi e prezzi 2013 vs nno mento/an g di trattam lari: % gg Biosimil Riduzione % dei prezzi rispetto al 2006
10 PASSATO FUTURO PRESENTE
11 I dubbi ricorrenti I biosimilari sono veramente sovrapponibili agli originator? sovrapponibilità È utile/necessario un RCT specifico per ogni indicazione terapeutica approvata? trasferimento delle indicazioni A chi prescriverli? Ai pazienti inaive o anche ai pretrattati? shift Ci sono differenze nella scelta del farmaco fra un uso limitato nel tempo o un uso continuativo, oppure fra un trattamento di supporto e una vera e propria terapia?
12 due mondi paralleli Farmaco biologico/biotecnologico ben conosciuto dal produttore Modifiche al processo di produzione esercizio dicomparabilità eventuali richieste di studi ad hoc di non inferiorità i ità prodotto accettabile prodotto permesso di continuare la produzione scadenza del brevetto di un biologico/biotecnologicio meno conosciuto dal nuovo produttore nuovo processo di produzione esercizio di comparabilità Ev. richieste di modifiche studi ad hoc di equivalenza Permesso di commercializzazione del biosimilare
13 Herceptin : variazioni autorizzate da EMA dall agosto 2000 ad oggi 24 pagine ema europa eu/docs/en GB/document library/epar Assessment Report
14 Herceptin : alcune delle variazioni autorizzate t da EMA dall agosto 2000 ad oggi tutte Modifiche maggiorinel processodi produzione del principio attivo Le modifiche minori sono almeno una ventina!! Estensione di sede di produzione Trasferimento della produzione da Genentech (USA) a Roche (D) Cambio della via di somministrazione Le nuove indicazioni/estensioni i i/ i idi indicaz.
15 Il caso del cambio della via di somministrazione di un originator: il trastuzumab (Herceptin ) moduli Trastuzumab e.v. Trastuzumab s.c Principali risultati dell esercizio esercizio di comparabilità Alcuni quesiti: 3 Modulo 3: processo di produzione robusto qualità Modulo fareste 4 : aspetti lo shift non clinici alla adeguati formulazione s.c. in Modulo 4una paziente 5: già in trattamento e.v.? Un RCT (HannaH) di non Prove inferiorità mutuate nel setting neoadiuvante vs. efficacia- è accettabile trastuzumab e.v estrapolazione mutuare dall originator le setting indicazioni metastatico al sicurezza preclinica Dose/kg (8 > 6 mg/kg ogni 3 sett.) dose fissa (600 mg ogni 3 setting metastatico dalla formulazione ev? sett.), accettando differenze di concentrazione e di tossicità come non rilevanti 5 nella promozione Prove del mutuate prodotto t s.c. il Analisi come per la nuova sostanza (l enzima rhuph20 ) per gli efficaciasicurezza dall originator aspetti percorso non clinici registrativo e clinici viene presentato? clinica Esercizio di comparabilità
16 I dubbi ricorrenti gli studi registrativi del biosimilare di infliximab: 1 studio di farmacocinetica: RCT in doppio cieco vs Remicade su 250 pz. con spondilite anchilosante 2 studi di efficacia: un piccolo RCT pilota per facilitare il trial vero e proprio un RCT in doppio cieco vs Remicade su 606 pz. con artrite reumatoide
17 I due mondi a confronto la qualità degli studi registrativi certolizumab 2 RCT in doppio cieco vs placebo. 1 su 982 pz (3 gruppi) con AR attiva e risposta inadeguata a MTX di 52 sett. (dalla 16 era possibile abbandonare il gruppo a cui siera stati randomizzati quindi si perdeva il cieco) (farmaco da ricostituire) 1 su 619 pz (3 gruppi) con AR e risposta inadeguata a MTX di 24 sett. ( farmaco pronto all uso) Esiti primari: 1. % d pz. con risposta (ACR 20 a sett.24) entrambi gli studi 2. progressione RX alla 52 sett. rispetto al baseline (solo il 1 ) infliximab biosimilare 1 RCT in doppio cieco di equivalenza vs Remicade (margine di eq.: + 15%) su 606 pz. (2 gruppi) con AR attiva e risposta inadeguata a MTX (viene aperto cieco a 30 sett. poi fino a 54 in cieco solo per paz. e valutatori). Esito primario: % di pz con risposta (ACR20 a sett.30)
18 I dubbi ricorrenti Il problema del trasferimento di indicazioni senza studi ad hoc Ad esempio i dubbi del gastroenterologo o del dermatologo che vedono trasferire i risultati degli studi su artrite reumatoide e (spondilite anchilosante) rispettivamente a M. di Crohn, rettocolite ulcerosa e psoriasi.
19 EMA estende le indicazioni sulla base dei risultati idell esercizio i di comparabilità: Caratteristiche fisico chimiche Test su: Caratteristiche chimico fisiche: Attività biologica (13 pagine) Struttura, purezza, contenuto proteico, glicosilazione. Dati di FK (pz.con SA) Dati di efficacia (pz. con AR) Differenze considerate trascurabili, Dati di sicurezza (tutti gli studi) eccetto per le differenze nei livelli di glicani afucosilati che sono state valutate nella parte di attività biologica. Test su: Attività ità biologica i (neutralizzazione i di TNFae attivazione i della risposta immune) 33 studi in vitro di farmacodinamica I diversi livelli di fucosilazione (assenza o bassi livelli di fucosio) fra i due prodotti non inficiano l affinità di legame per recettore del TNFa. Differenze trascurabili nel binding verso i recettori TNFa su Natural Killer e neutrofili derivanti da pz con morbo di Crohn e donatori sani. Attivazione risposta immune confrontabile in cell da pz. con morbo di Crohn (in particolare nel saggio ADCC nel circolo ematico).
20 EMA estende le indicazioni sulla base dei risultati tidell esercizio i di comparabilità: - Caratteristiche fisico-chimiche - Attività biologica Dati di Farmacocinetica - Dati di efficacia i (pz. con AR) - Dati di sicurezza (tutti gli studi) Based on the robust comparisons of the physicochemical and in vitro and ex vivo biological analyses, Inflectra wasconsidered biosimilar to the reference product Remicade. These data, in combination with clinical data demonstrating pharmacokinetic, and therapeutic equivalence in rheumatology conditions, allow L obiettivo non è dimostrare efficacia e sicurezza del nuovo farmaco, ma che i 2 farmaci sono simili for extrapolation to all other indications of Remicade La ditta produrrà un RCT (in doppio cieco) nei pz con morbo di Crohn
21 L esercizio di comparabilità per la glargine biosimilare Glargine Glargine originator biosimilare moduli Alcune motivazioni per lo switch: Principali risultati dell esercizio di comparabilità (65 pag.) 3 qualità Modulo molecola 3: l processodi semplice produzione, con indicazione soddisfacente i unica Modulo 4 : nessuna obiezione per gli aspetti non clinici è Modulo 4 una proteina non glicosilata 5: studi clinici Prove mutuate efficaciasicurezza equivalenza PK e PD dimostrata è stata 5 RCT oggetto di fase 1 di di PK innovazione e PD ( su dall originator volontari sani incrementale e diabetici tipo 1): preclinica 2 RCT switch di fase 3 di inconsapevoli supporto ( 1 su diabetici (brevetti tipo I, 1 su evergreen) diabetici tipo II ): forti evidenze a supporto della comparability fra i 2 farmaci 5 Prove mutuate gli studi di fase 3 forniscono dati sullo switch da originator a biosimilare efficacia- dall originator insulina sicurezza nessuna in terapia differenza a quella su immunogenicità in studio i i e rischio di ipoglicemia i clinica Gli studi di fase III sono stati condotti effettuando switch dalla La prima insulina estrattiva è stata prodotta dalla Lilly nel 1923 così come il primo biosimilare! (molecola l ben conosciuta dal produttore!) Esercizio di comparabilità
22 Una riflessione sui 2 mondi paralleli: I farmaci di marca spesso sono registrati con studi di NON inferiorità o vs P Nella pratica clinica si accettano come novità farmaci che hanno dimostrato di essere non migliori o difficilmente collocabili rispetto allo standard di cura, mediamente più costosi Si esaltano le uguaglianze I biosimilari sono registrati con un esercizio di comparabilità per qualità, efficacia e sicurezza che deve dimostrare l equivalenza rispetto all originator Nll Nella pratica clinica i non si accetta come simile unprodotto che può essere anche un po meglio dell originator pur costando di meno Si esaltano le differenze
23 Alcune considerazioni finali sui «primi biosimilari» I criteri usati da EMA per definire la biosimilarità L esperienza clinica maturata per i primi biosimilari dal 2006 ad oggi L assenza di segnalazioni di una maggior frequenza di eventi avversi L assenza di eventi avversi specifici per i biosimilari L assenza Lassenza di dati su problematiche di attivazione immunologica Dovrebbero indurre a considerare la possibilità di passare dall originator al biosimilare anche nei pazienti già in trattamento
24 .E per i biosimilari in arrivo? come colmare lo svantaggio rispetto agli originator? Condividere id - Iniziare per tempo un opera di informazione/sensibilizzazione dei clinici - Presentare/discutere i risultati dell esercizio di comparabilità - Rispondere alle obiezioni - Condividere e implementare raccomandazioni sull uso dei biosimilari Costringere (!) La differenza fra condividere e costringere sta nel rispetto della capacità del clinico di scegliere.
25 Cosa abbiamo condiviso con i Clinici
Relatore: Dott.ssa Elisabetta Pasi - Servizio Assistenza Territoriale, Direzione Generale Sanità e Politiche Sociali- Regione Emilia-Romagna
 Le decisioni pratiche tra normative, linee guida e raccomandazioni, il position paper di AIFA, l intercambiabilità e la sostituibilità di originator e biosimilari Relatore: Dott.ssa Elisabetta Pasi - Servizio
Le decisioni pratiche tra normative, linee guida e raccomandazioni, il position paper di AIFA, l intercambiabilità e la sostituibilità di originator e biosimilari Relatore: Dott.ssa Elisabetta Pasi - Servizio
I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico
 DOCUMENTO DI INDIRIZZO della CRF n. 1 I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico Le implicazioni per la pratica clinica in termini di sovrapponibilità, sostituibilità
DOCUMENTO DI INDIRIZZO della CRF n. 1 I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico Le implicazioni per la pratica clinica in termini di sovrapponibilità, sostituibilità
ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Milano, 25 Marzo
Futuro della Reumatologia in Veneto Garantire innovazione generando risparmio
 Futuro della Reumatologia in Veneto Garantire innovazione generando risparmio Margherita Andretta Padova, 7 giugno Andamento della spesa farmaceutica in Veneto Spesa totale 2017: 1,5 mld Calo del prezzo
Futuro della Reumatologia in Veneto Garantire innovazione generando risparmio Margherita Andretta Padova, 7 giugno Andamento della spesa farmaceutica in Veneto Spesa totale 2017: 1,5 mld Calo del prezzo
I biosimilari fra presente e futuro
 ANALISI DELLA PRESCRIZIONE FARMACEUTICA IN ITALIA presentazione del Rapporto Nazionale OsMed 2010 7 luglio 2011 aula Pocchiari I biosimilari fra presente e futuro Anna Maria Marata Lucia Magnano Che cos
ANALISI DELLA PRESCRIZIONE FARMACEUTICA IN ITALIA presentazione del Rapporto Nazionale OsMed 2010 7 luglio 2011 aula Pocchiari I biosimilari fra presente e futuro Anna Maria Marata Lucia Magnano Che cos
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA 1 2 Il Ruolo
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA 1 2 Il Ruolo
ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA
 Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Il Ruolo del
Evento formativo sulla promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici ALESSANDRO NOBILI LUCA PASINA EVIDENZE CLINICHE DI BIOSIMILARITA Il Ruolo del
Franco Silvestris UNIVERSITÀ DEGLI STUDI DI BARI
 UNIVERSITÀ DEGLI STUDI DI BARI Dipartimento di Scienze Biomediche e Oncologia Umana Sezione di Medicina Interna e Oncologia Clinica U.O.C. Oncologia Medica Universitaria Direttore: Franco Silvestris Franco
UNIVERSITÀ DEGLI STUDI DI BARI Dipartimento di Scienze Biomediche e Oncologia Umana Sezione di Medicina Interna e Oncologia Clinica U.O.C. Oncologia Medica Universitaria Direttore: Franco Silvestris Franco
Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica
 Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Siamo partiti da questo La Repubblica 24
Armando A. Genazzani Università del Piemonte Orientale genazzani@pharm.unipmn.it 347.9829981 Centro Ricerca Interdipartimentale Farmacogenetica Farmacogenomica Siamo partiti da questo La Repubblica 24
SCHEDA FARMACO BIOSIMILARE
 SCHEDA FARMACO BIOSIMILARE (a cura del Coordinamento HTA) Farmaco biosimilare Nome commerciale (ditta, data di approvazione EMA) Farmaco biologico di riferimento (ditta) CT-P10 (RITUXIMAB) Truxima Ditta:
SCHEDA FARMACO BIOSIMILARE (a cura del Coordinamento HTA) Farmaco biosimilare Nome commerciale (ditta, data di approvazione EMA) Farmaco biologico di riferimento (ditta) CT-P10 (RITUXIMAB) Truxima Ditta:
Biosimilari in Reumatologia
 Biosimilari in Reumatologia Carlomaurizio Montecucco Unità di Reumatologia Università di Pavia IRCCS Policlinico S. Matteo Agenti biologici approvati per l artrite reumatoide Biosimilare 2015 Infliximab
Biosimilari in Reumatologia Carlomaurizio Montecucco Unità di Reumatologia Università di Pavia IRCCS Policlinico S. Matteo Agenti biologici approvati per l artrite reumatoide Biosimilare 2015 Infliximab
ONCOEMATOLOGIA TRA SOSTENIBILITÀ E ADERENZA Azienda Provinciale per i Servizi Sanitari della Provincia Autonoma di Trento AOU PADOVA 22 MARZO 2019
 ONCOEMATOLOGIA TRA SOSTENIBILITÀ E ADERENZA Azienda Provinciale per i Servizi Sanitari della Provincia Autonoma di Trento AOU PADOVA 22 MARZO 2019 Giovanni M. Guarrera Direttore Servizio Ospedaliero Provinciale
ONCOEMATOLOGIA TRA SOSTENIBILITÀ E ADERENZA Azienda Provinciale per i Servizi Sanitari della Provincia Autonoma di Trento AOU PADOVA 22 MARZO 2019 Giovanni M. Guarrera Direttore Servizio Ospedaliero Provinciale
Commissione Regionale Farmaco MEDICINALI BIOSIMILARI DEL FILGRASTIM
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento PTR n. 117 relativo a: MEDICINALI BIOSIMILARI DEL FILGRASTIM Ottobre 2010 Premessa...3 Confronto delle indicazioni terapeutiche
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento PTR n. 117 relativo a: MEDICINALI BIOSIMILARI DEL FILGRASTIM Ottobre 2010 Premessa...3 Confronto delle indicazioni terapeutiche
L'USO DEL FARMACO BIOLOGICO NELLA REGIONE: ACCESSIBILITÀ, COSTI, PROSPETTIVE. Carla Sorrentino, statistico sanitario
 1 L'USO DEL FARMACO BIOLOGICO NELLA REGIONE: ACCESSIBILITÀ, COSTI, PROSPETTIVE Carla Sorrentino, statistico sanitario 2 Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia:
1 L'USO DEL FARMACO BIOLOGICO NELLA REGIONE: ACCESSIBILITÀ, COSTI, PROSPETTIVE Carla Sorrentino, statistico sanitario 2 Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia:
CIPOMO Torino 3 ottobre Sostenibilità ed innovazione in oncologia: il modello del cancro della mammella HER2+
 CIPOMO Torino 3 ottobre 2014 Sostenibilità ed innovazione in oncologia: il modello del cancro della mammella HER2+ Importanza della sostenibilità: collaborazione tra oncologo e farmacista per garantire
CIPOMO Torino 3 ottobre 2014 Sostenibilità ed innovazione in oncologia: il modello del cancro della mammella HER2+ Importanza della sostenibilità: collaborazione tra oncologo e farmacista per garantire
Commissione Regionale Farmaco MEDICINALI BIOSIMILARI DELL ERITROPOIETINA
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento PTR n.119 relativo a: MEDICINALI BIOSIMILARI DELL ERITROPOIETINA Novembre 2010 Premessa...3 Confronto delle indicazioni terapeutiche
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento PTR n.119 relativo a: MEDICINALI BIOSIMILARI DELL ERITROPOIETINA Novembre 2010 Premessa...3 Confronto delle indicazioni terapeutiche
Documento PTR n. 119 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Sostenibilità dell innovazione e HTA delle terapie innovative
 Sostenibilità dell innovazione e HTA delle terapie innovative Marco Marchetti Responsabile dell'unità di Valutazione delle Tecnologie Policlinico Gemelli Università Cattolica del Sacro Cuore Roma, 14 Aprile
Sostenibilità dell innovazione e HTA delle terapie innovative Marco Marchetti Responsabile dell'unità di Valutazione delle Tecnologie Policlinico Gemelli Università Cattolica del Sacro Cuore Roma, 14 Aprile
Regione del Veneto Coordinamento Regionale Unico sul Farmaco - CRUF
 giunta regionale Allegato A al Decreto n. 90 del 25 luglio 2017 pag. 1/18 Regione del Veneto Coordinamento Regionale Unico sul Farmaco - CRUF Documento regionale di approfondimento sui Medicinali Biosimilari
giunta regionale Allegato A al Decreto n. 90 del 25 luglio 2017 pag. 1/18 Regione del Veneto Coordinamento Regionale Unico sul Farmaco - CRUF Documento regionale di approfondimento sui Medicinali Biosimilari
Milano, 13 gennaio 2017
 Milano, 13 gennaio 2017 L esperienza della ASST di Brescia U.O. Farmacia Spedali Civili di Brescia Daria Bettoni Responsabile del Settore Farmaci e Farmacovigilanza Progetto Spedali Civili, criticità e
Milano, 13 gennaio 2017 L esperienza della ASST di Brescia U.O. Farmacia Spedali Civili di Brescia Daria Bettoni Responsabile del Settore Farmaci e Farmacovigilanza Progetto Spedali Civili, criticità e
SCHEDA FARMACO BIOSIMILARE
 SCHEDA FARMACO BIOSIMILARE (a cura del Coordinamento HTA) Farmaco biosimilare LY2963016 (INSULINA GLARGINE) Nome commerciale (ditta, data di approvazione EMA) Farmaco biologico di riferimento (ditta) Abasaglar
SCHEDA FARMACO BIOSIMILARE (a cura del Coordinamento HTA) Farmaco biosimilare LY2963016 (INSULINA GLARGINE) Nome commerciale (ditta, data di approvazione EMA) Farmaco biologico di riferimento (ditta) Abasaglar
AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI*
 1/5 Abatacept, Adalimumab, Anakinra, Certolizumab Pegol, Etanercept, Golimumab, Infliximab, Tocilizumab, Rituximab ARTRITE REUMATOIDE: i farmaci devono essere prescritti solamente dai centri specializzati
1/5 Abatacept, Adalimumab, Anakinra, Certolizumab Pegol, Etanercept, Golimumab, Infliximab, Tocilizumab, Rituximab ARTRITE REUMATOIDE: i farmaci devono essere prescritti solamente dai centri specializzati
Azienda Ospedaliera San Carlo Borromeo - U.O.C. Farmacia Clinica Prontuario alla dimissione aggiornamento luglio 14 Pagina 1 di 5
 Farmaci Biosimilari Azienda Ospedaliera San Carlo Borromeo - U.O.C. Farmacia Clinica Prontuario alla dimissione aggiornamento luglio 14 Pagina 1 di 5 EPOETINE B03XA01 EPOETINA ALFA a) Anemia associata
Farmaci Biosimilari Azienda Ospedaliera San Carlo Borromeo - U.O.C. Farmacia Clinica Prontuario alla dimissione aggiornamento luglio 14 Pagina 1 di 5 EPOETINE B03XA01 EPOETINA ALFA a) Anemia associata
Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN
 Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN Dr. Eugenio Ciacco Servizio Aziendale del Farmaco ASL1 Avezzano Sulmona L Aquila PARTIAMO DALL i presupposti dell Abruzzo
Innovazione e Sosteniblità dei farmaci biologici: quale ruolo per il farmacista SSN Dr. Eugenio Ciacco Servizio Aziendale del Farmaco ASL1 Avezzano Sulmona L Aquila PARTIAMO DALL i presupposti dell Abruzzo
Governance del farmaco e modelli di health technology assessment in ematologia: esperienze regionali
 Bolzano 26-27 ottobre 2017 Governance del farmaco e modelli di health technology assessment in ematologia: esperienze regionali Ospedale Centrale di Bolzano 26 ottobre 2017 Annalisa Campomori SC Farmacia
Bolzano 26-27 ottobre 2017 Governance del farmaco e modelli di health technology assessment in ematologia: esperienze regionali Ospedale Centrale di Bolzano 26 ottobre 2017 Annalisa Campomori SC Farmacia
I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO
 I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO INTRODUZIONE I farmaci I farmaci generici Bioequivalenza I farmaci generici equivalenti I farmaci biologici Biosimilarità
I BIOSIMILARI TRA PROFILI BREVETTUALI E REGOLATORI 30 OTTOBRE 2015 PARMA MARINA MAURO INTRODUZIONE I farmaci I farmaci generici Bioequivalenza I farmaci generici equivalenti I farmaci biologici Biosimilarità
GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE
 XXXI CONGRESSO NAZIONALE SIFO CAGLIARI 6-8 OTTOBRE 2010 GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE DOTT.ssa ENRICA MARIA PROLI DOTT.ssa ELENA JACOBONI COSA SONO I FARMACI
XXXI CONGRESSO NAZIONALE SIFO CAGLIARI 6-8 OTTOBRE 2010 GENERICI E BIOSIMILARI A CONFRONTO: PROBLEMATICHE FARMACOLOGICHE E REGOLATORIE DOTT.ssa ENRICA MARIA PROLI DOTT.ssa ELENA JACOBONI COSA SONO I FARMACI
UN INQUADRAMENTO. Armando Genazzani
 I BIOSIMILARI: UN INQUADRAMENTO Armando Genazzani Il processo produttivo di un farmaco biologico è complesso Differenze in diverse parti del processo Gene umano Vettore DNA Trasferimento in cellula ospite
I BIOSIMILARI: UN INQUADRAMENTO Armando Genazzani Il processo produttivo di un farmaco biologico è complesso Differenze in diverse parti del processo Gene umano Vettore DNA Trasferimento in cellula ospite
La penetrazione dei biosimilari nell ASL di Bergamo in Regione Lombardia
 PROGETTO FARMAGOOD Corso sui biosimilari Bergamo 22 aprile 2015 La penetrazione dei biosimilari nell ASL di Bergamo in Regione Lombardia Dr.ssa Rossana Piccinelli S.S. Farmacoeconomia Servizio Farmaceutico
PROGETTO FARMAGOOD Corso sui biosimilari Bergamo 22 aprile 2015 La penetrazione dei biosimilari nell ASL di Bergamo in Regione Lombardia Dr.ssa Rossana Piccinelli S.S. Farmacoeconomia Servizio Farmaceutico
Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema. Dott.ssa Maria Susanna Rivetti
 Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema Dott.ssa Maria Susanna Rivetti 1 D.L.vo 219/2006 e s.m.i. Definizione Medicinali biologici Medicinali il cui principio attivo
Utilizzo dei farmaci biologici in Regione Liguria: sostenibilità del sistema Dott.ssa Maria Susanna Rivetti 1 D.L.vo 219/2006 e s.m.i. Definizione Medicinali biologici Medicinali il cui principio attivo
I biosimilari tra presente e futuro. L impatto nella pratica clinica. dei biosimilari in: Nefrologia. G. Brunori. Trento
 I biosimilari tra presente e futuro L impatto nella pratica clinica dei biosimilari in: Nefrologia G. Brunori Trento Corso di formazione manageriale per dirigenti sanitari 2 marzo 2010 Valutazione della
I biosimilari tra presente e futuro L impatto nella pratica clinica dei biosimilari in: Nefrologia G. Brunori Trento Corso di formazione manageriale per dirigenti sanitari 2 marzo 2010 Valutazione della
FLIXABI Biogen H-RRL Reumatologo, dermatologo, endovena REMSIMA Mundipharma gastroenterologo, internista INFLECTRA Pfizer-Hospira
 SPECIALITA MEDICINALI IN COMMERCIO L04AA IMMUNOSOPPRESSIVI AD AZIONE SELETTIVA Ditta Produttrice Formulazione FASCIA SPECIALISTI L04AA24 ABATACEPT ORENCIA Bristol Myers Squibb sottocute H-RRL Reumatologo,
SPECIALITA MEDICINALI IN COMMERCIO L04AA IMMUNOSOPPRESSIVI AD AZIONE SELETTIVA Ditta Produttrice Formulazione FASCIA SPECIALISTI L04AA24 ABATACEPT ORENCIA Bristol Myers Squibb sottocute H-RRL Reumatologo,
I dati dell'uso in Italia
 I FARMACI BIOSIMILARI: USO, SICUREZZA, SOSTENIBILITÀ Istituto Superiore di Sanità Roma, 25 Giugno 2015 I dati dell'uso in Italia Giuseppe Traversa Centro di epidemiologia, sorveglianza e promozione della
I FARMACI BIOSIMILARI: USO, SICUREZZA, SOSTENIBILITÀ Istituto Superiore di Sanità Roma, 25 Giugno 2015 I dati dell'uso in Italia Giuseppe Traversa Centro di epidemiologia, sorveglianza e promozione della
Azioni di Appropriatezza Prescrittiva. Esperienza dell Azienda USL Toscana Centro nel 2018
 Azioni di Appropriatezza Prescrittiva Esperienza dell Azienda USL Toscana Centro nel 2018 Governance Farmaceutica Con l arrivo di nuove e promettenti terapie, con un marcato invecchiamento della popolazione
Azioni di Appropriatezza Prescrittiva Esperienza dell Azienda USL Toscana Centro nel 2018 Governance Farmaceutica Con l arrivo di nuove e promettenti terapie, con un marcato invecchiamento della popolazione
FARMACI BIOSIMILARI IN ONCOLOGIA
 FARMACI BIOSIMILARI IN ONCOLOGIA Opuscolo per cittadini e pazienti Ottobre 2018 Associazione Italiana di Oncologia Medica Associazione Italiana di Oncologia Medica In questo opuscolo troverà informazioni,
FARMACI BIOSIMILARI IN ONCOLOGIA Opuscolo per cittadini e pazienti Ottobre 2018 Associazione Italiana di Oncologia Medica Associazione Italiana di Oncologia Medica In questo opuscolo troverà informazioni,
Le potenzialità degli studi registrativi e post marketing
 Dr.ssa Silvia Adami Area Sanità e Sociale Settore Farmaceutico-Protesica -Dispositivi medici Rio Novo Dorsoduro, 3493 30123 -Venezia 1 Studio Clinico - Classificazioni per fasi degli studi clinici La classificazione
Dr.ssa Silvia Adami Area Sanità e Sociale Settore Farmaceutico-Protesica -Dispositivi medici Rio Novo Dorsoduro, 3493 30123 -Venezia 1 Studio Clinico - Classificazioni per fasi degli studi clinici La classificazione
Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore)
 1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
DELIBERAZIONE N. 20/5 DEL
 Oggetto: Direttive alle Aziende Sanitarie per l espletamento delle gare per l approvvigionamento di farmaci ed emoderivati relativamente ai farmaci biosimilari. L Assessore dell Igiene e Sanità e dell
Oggetto: Direttive alle Aziende Sanitarie per l espletamento delle gare per l approvvigionamento di farmaci ed emoderivati relativamente ai farmaci biosimilari. L Assessore dell Igiene e Sanità e dell
Allegato A al Decreto n. 331 del pag. 1/17
 giunta regionale Allegato A al Decreto n. 331 del 30.12.2015 pag. 1/17 MEDICINALI BIOSIMILARI (Documento approvato nella seduta del 15 ottobre 2015 della Commissione Tecnica Regionale Farmaci, ex DGR n.
giunta regionale Allegato A al Decreto n. 331 del 30.12.2015 pag. 1/17 MEDICINALI BIOSIMILARI (Documento approvato nella seduta del 15 ottobre 2015 della Commissione Tecnica Regionale Farmaci, ex DGR n.
Biosimilare: Normativa di riferimento
 214 A cura di Laura Ricci Area Legislazione SIFO sifo.legislazione@gmail.com Biosimilare: Normativa di riferimento DEFINIZIONE La definizione di farmaco biologico e biosimilare, più volte ripresa e precisata,
214 A cura di Laura Ricci Area Legislazione SIFO sifo.legislazione@gmail.com Biosimilare: Normativa di riferimento DEFINIZIONE La definizione di farmaco biologico e biosimilare, più volte ripresa e precisata,
FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI
 FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI nelle Malattie Infiammatorie Croniche Intestinali Dr.ssa Valentina CASINI ASST Bergamo EST Bolognini Seriate (BG) FARMACO BIOLOGICO FARMACO BIOSIMILARE DI COSA
FARMACI BIOLOGICI vs FARMACI BIOEQUIVALENTI nelle Malattie Infiammatorie Croniche Intestinali Dr.ssa Valentina CASINI ASST Bergamo EST Bolognini Seriate (BG) FARMACO BIOLOGICO FARMACO BIOSIMILARE DI COSA
 SCHEDA PER LA PRESCRIZIONE DI ENBREL nella PSORIASI Farmaco H REGIONE LAZIO Paziente (Nome /Cognome) Codice Fiscale Data di Nascita sesso M F Regione di residenza dell assistito Azienda USL Domicilio:
SCHEDA PER LA PRESCRIZIONE DI ENBREL nella PSORIASI Farmaco H REGIONE LAZIO Paziente (Nome /Cognome) Codice Fiscale Data di Nascita sesso M F Regione di residenza dell assistito Azienda USL Domicilio:
Innovatività e appropriatezza : criteri di valutazione dei farmaci
 Innovatività e appropriatezza : criteri di valutazione dei farmaci Massimo Medaglia Dipartimento Farmaceutico Ospedale L. Sacco Azienda Ospedaliera Polo Universitario Milano L innovazione nella terapia
Innovatività e appropriatezza : criteri di valutazione dei farmaci Massimo Medaglia Dipartimento Farmaceutico Ospedale L. Sacco Azienda Ospedaliera Polo Universitario Milano L innovazione nella terapia
Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi
 Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi Giambattista Bonanno Sezione di Farmacologia e Tossicologia Dipartimento di Farmacia Scuola di Scienze Mediche e Farmaceutiche
Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi Giambattista Bonanno Sezione di Farmacologia e Tossicologia Dipartimento di Farmacia Scuola di Scienze Mediche e Farmaceutiche
Uso di farmaci biosimilari Ylenia Ingrasciotta
 Uso di farmaci biosimilari Ylenia Ingrasciotta A.O.U. Policlinico «G. Martino», Messina Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia: tecnologia per la manipolazione
Uso di farmaci biosimilari Ylenia Ingrasciotta A.O.U. Policlinico «G. Martino», Messina Farmaci biologici Biologici: prodotti o derivati da organismi viventi Biotecnologia: tecnologia per la manipolazione
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici
 Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
La commercializzazione dei biosimilari ha modificato il pattern prescrittivo dei fattori di crescita granulocitari?
 La commercializzazione dei biosimilari ha modificato il pattern prescrittivo dei fattori di crescita granulocitari? Ilaria Marcianò Dip. Scienze Biomediche, Odontoiatriche e delle Immagini Morfologiche
La commercializzazione dei biosimilari ha modificato il pattern prescrittivo dei fattori di crescita granulocitari? Ilaria Marcianò Dip. Scienze Biomediche, Odontoiatriche e delle Immagini Morfologiche
ATTIVITA DI IMPLEMENTAZIONE LOCALE DELLE RACCOMANDAZIONI DI INDIRIZZO REGIONALI: ALCUNI ESEMPI
 ATTIVITA DI IMPLEMENTAZIONE LOCALE DELLE RACCOMANDAZIONI DI INDIRIZZO REGIONALI: ALCUNI ESEMPI FARMACIA AZIENDA OSPEDALIERA PADOVA Dott.ssa Elisabetta di Lenardo Padova 24 novembre 2016 CONTESTO GENERALE
ATTIVITA DI IMPLEMENTAZIONE LOCALE DELLE RACCOMANDAZIONI DI INDIRIZZO REGIONALI: ALCUNI ESEMPI FARMACIA AZIENDA OSPEDALIERA PADOVA Dott.ssa Elisabetta di Lenardo Padova 24 novembre 2016 CONTESTO GENERALE
Diabete e biosimilari dell insulina: evidenze cliniche
 Diabete e biosimilari dell insulina: evidenze cliniche Francesco Rossi I progressi in farmacologia: le biotecnologie 1 La crescita dell industria biotech in Italia Anche in Italia, l industria biotecnologica
Diabete e biosimilari dell insulina: evidenze cliniche Francesco Rossi I progressi in farmacologia: le biotecnologie 1 La crescita dell industria biotech in Italia Anche in Italia, l industria biotecnologica
GOLIMUMAB (Indicazione: Spondilite Anchilosante) ( )
 GOLIMUMAB (Indicazione: Spondilite Anchilosante) (05-04-2011) Specialità: Simponi (Centocor) Forma farmaceutica: 1 PEN 50mg, 0,5ml - Prezzo: euro 1723.33 1 SIR 50mg, 0,5ml - Prezzo: euro 1723.33 ATC: L04AB06
GOLIMUMAB (Indicazione: Spondilite Anchilosante) (05-04-2011) Specialità: Simponi (Centocor) Forma farmaceutica: 1 PEN 50mg, 0,5ml - Prezzo: euro 1723.33 1 SIR 50mg, 0,5ml - Prezzo: euro 1723.33 ATC: L04AB06
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: USTEKINUMAB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: USTEKINUMAB Giugno 2010 Assessorato Politiche per la salute Commissione Regionale del Farmaco Ustekinumab Indicazioni
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: USTEKINUMAB Giugno 2010 Assessorato Politiche per la salute Commissione Regionale del Farmaco Ustekinumab Indicazioni
Oncologia: i fattori della crescita
 Convegno Nazionale I FARMACI BIOSIMILARI: USO, SICUREZZA, SOSTENIBILITÀ Roma, ISS 25 giugno 2015 Oncologia: i fattori della crescita Annalisa Campomori, Direttore SC Farmacia Ospedaliera Struttura Ospedaliera
Convegno Nazionale I FARMACI BIOSIMILARI: USO, SICUREZZA, SOSTENIBILITÀ Roma, ISS 25 giugno 2015 Oncologia: i fattori della crescita Annalisa Campomori, Direttore SC Farmacia Ospedaliera Struttura Ospedaliera
Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva
 Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva Pierluigi Navarra Istituto di Farmacologia Facoltà di Medicina e Chirurgia Università Cattolica - Roma Analisi
Bioequivalenti e biosimilari: aspetti regolatori e loro impatto sull appropriatezza prescrittiva Pierluigi Navarra Istituto di Farmacologia Facoltà di Medicina e Chirurgia Università Cattolica - Roma Analisi
Revisione della posizione sui farmaci biosimilari da parte della Società. Italiana di Farmacologia: working paper 2016
 Revisione della posizione sui farmaci biosimilari da parte della Società Italiana di Farmacologia: working paper 2016 a cura di Giorgio Cantelli Forti (Presidente, Società Italiana di Farmacologia) e Francesco
Revisione della posizione sui farmaci biosimilari da parte della Società Italiana di Farmacologia: working paper 2016 a cura di Giorgio Cantelli Forti (Presidente, Società Italiana di Farmacologia) e Francesco
Corso Regionale Gastrocare 2016 Ferrara 23 settembre 2016 Imbarcadero Castello Estense Drssa Renata D Incà Gastroenterologia Azienda Ospedaliera di
 Corso Regionale Gastrocare 2016 Ferrara 23 settembre 2016 Imbarcadero Castello Estense Drssa Renata D Incà Gastroenterologia Azienda Ospedaliera di Padova Il percorso della terapia nelle IBD Dal miglioramento
Corso Regionale Gastrocare 2016 Ferrara 23 settembre 2016 Imbarcadero Castello Estense Drssa Renata D Incà Gastroenterologia Azienda Ospedaliera di Padova Il percorso della terapia nelle IBD Dal miglioramento
Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO)
 Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO) SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi
Position Paper sui farmaci biosimilari della Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie (SIFO) SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
SCHEDA REGIONALE PER LA PRESCRIZIONE ORENCIA 250 MG Farmaco HOSP2
 ORENCIA 250 MG Nome Cognome Codice Fiscale dell Assistito Data di nascita / / Sesso M F Indirizzo trattamento di pazienti adulti affetti da artrite reumatoide grave in fase attiva in associazione con il
ORENCIA 250 MG Nome Cognome Codice Fiscale dell Assistito Data di nascita / / Sesso M F Indirizzo trattamento di pazienti adulti affetti da artrite reumatoide grave in fase attiva in associazione con il
Strategie per l inserimento in Prontuario dei farmaci respiratori in Emilia Romagna
 Strategie per l inserimento in Prontuario dei farmaci respiratori in Emilia Romagna Anna Maria Marata Servizio Assistenza Territoriale Area Farmaco e Dispositivi Medici Il sistema regolatorio: premessa
Strategie per l inserimento in Prontuario dei farmaci respiratori in Emilia Romagna Anna Maria Marata Servizio Assistenza Territoriale Area Farmaco e Dispositivi Medici Il sistema regolatorio: premessa
Le sfide dell innovazione terapeutica in ematologia: tra sostenibilità e appropriatezza in Trentino Alto Adige
 Bolzano 26-27 ottobre 2017 Le sfide dell innovazione terapeutica in ematologia: tra sostenibilità e appropriatezza in Trentino Alto Adige Ospedale Centrale di Bolzano 26 ottobre 2017 Annalisa Campomori
Bolzano 26-27 ottobre 2017 Le sfide dell innovazione terapeutica in ematologia: tra sostenibilità e appropriatezza in Trentino Alto Adige Ospedale Centrale di Bolzano 26 ottobre 2017 Annalisa Campomori
(ab)uso dei farmaci in Italia: situazione nazionale e regionale Antonio Addis
 (ab)uso dei farmaci in Italia: situazione nazionale e regionale Antonio Addis Agenda Perché parliamo sempre di farmaci Uso dei farmaci in Italia Esercizio di confronto e sulla variabilità Strumenti per
(ab)uso dei farmaci in Italia: situazione nazionale e regionale Antonio Addis Agenda Perché parliamo sempre di farmaci Uso dei farmaci in Italia Esercizio di confronto e sulla variabilità Strumenti per
Farmaci Biosimilari. Aspetti scientifici e regolatori
 Farmaci Biosimilari Aspetti scientifici e regolatori 19/12/2014 0 Riassunto I farmaci biologici rappresentano una risorsa terapeutica importante per trattare malattie gravi e debilitanti, ma sono gravati
Farmaci Biosimilari Aspetti scientifici e regolatori 19/12/2014 0 Riassunto I farmaci biologici rappresentano una risorsa terapeutica importante per trattare malattie gravi e debilitanti, ma sono gravati
REPORT HTA REGIONALE. Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO
 REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
REPORT HTA REGIONALE Decisioni CTR Data riunione: 16/11/2011 Decisione: INSERITO fd Commenti: si tratta di un nuovo biosimilare di filgrastim, la cui efficacia è stata dimostrata da uno studio randomizzato
LINEE GUIDA PER L USO DEI FARMACI BIOSIMILARI
 Regione Molise DIREZIONE GENERALE V Politiche per la Tutela della Salute e Assistenza Socio-Sanitaria Servizio Programmazione e Assistenza Farmaceutica LINEE GUIDA PER L USO DEI FARMACI BIOSIMILARI I farmaci
Regione Molise DIREZIONE GENERALE V Politiche per la Tutela della Salute e Assistenza Socio-Sanitaria Servizio Programmazione e Assistenza Farmaceutica LINEE GUIDA PER L USO DEI FARMACI BIOSIMILARI I farmaci
Insulina glargine biosimilare
 Scheda di valutazione del farmaco Insulina glargine biosimilare A cura della Commissione Regionale del Farmaco della Regione Emilia-Romagna Doc PTR n. 278 Recepito con determina n. 8419 del 26/05/2016
Scheda di valutazione del farmaco Insulina glargine biosimilare A cura della Commissione Regionale del Farmaco della Regione Emilia-Romagna Doc PTR n. 278 Recepito con determina n. 8419 del 26/05/2016
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Linee guida AIFA e SIF per l uso dei Biosimilari
 Linee guida AIFA e SIF per l uso dei Biosimilari Prof. Giovambattista De Sarro Dipartimento di Scienze della Salute Università degli Studi Magna Graecia di Catanzaro Dichiarazione di trasparenza/interessi*
Linee guida AIFA e SIF per l uso dei Biosimilari Prof. Giovambattista De Sarro Dipartimento di Scienze della Salute Università degli Studi Magna Graecia di Catanzaro Dichiarazione di trasparenza/interessi*
Farmaci Biotecnologici e Biosimilari:
 Farmaci Biotecnologici e Biosimilari: Innovazione e sostenibilità del sistema pubblico Luca Pani Direttore Generale Outline Il processo regolatorio del biosimilare Le iniziative europee Gli aspetti economici
Farmaci Biotecnologici e Biosimilari: Innovazione e sostenibilità del sistema pubblico Luca Pani Direttore Generale Outline Il processo regolatorio del biosimilare Le iniziative europee Gli aspetti economici
La prescrizione dei biosimilari: il punto di vista dell oncologo
 La prescrizione dei biosimilari: il punto di vista dell oncologo Prof. Giuseppe Nastasi Direttore U.O.C Oncologia Medica A.O. Bolognini - Seriate (BG) Cosa si aspetta il paziente? Sicurezza ed efficacia
La prescrizione dei biosimilari: il punto di vista dell oncologo Prof. Giuseppe Nastasi Direttore U.O.C Oncologia Medica A.O. Bolognini - Seriate (BG) Cosa si aspetta il paziente? Sicurezza ed efficacia
Position Paper SIFO sui farmaci biosimilari
 Position Paper SIFO sui farmaci biosimilari SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie Position Paper SIFO sui farmaci biosimilari e d i z i o n
Position Paper SIFO sui farmaci biosimilari SIFO Società Italiana di Farmacia Ospedaliera e dei Servizi Farmaceutici delle Aziende Sanitarie Position Paper SIFO sui farmaci biosimilari e d i z i o n
MEDICINALI BIOEQUIVALENTI E BIOSIMILARI. Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara
 MEDICINALI BIOEQUIVALENTI E BIOSIMILARI Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara FARMACO GENERICO e EQUIVALENTE Con la Legge 28/12/1995 art. 130 comma 3, il
MEDICINALI BIOEQUIVALENTI E BIOSIMILARI Dipartimento Farmaceutico Interaziendale Azienda Ospedaliero Universitaria di Ferrara FARMACO GENERICO e EQUIVALENTE Con la Legge 28/12/1995 art. 130 comma 3, il
I biosimilari dell insulina
 I biosimilari dell insulina Seconda Università degli Studi di Napoli Dipartimento di Medicina Sperimentale - Sezione di Farmacologia L. Donatelli Genova, 15 maggio 2015 Francesco Rossi Dichiarazione conflitto
I biosimilari dell insulina Seconda Università degli Studi di Napoli Dipartimento di Medicina Sperimentale - Sezione di Farmacologia L. Donatelli Genova, 15 maggio 2015 Francesco Rossi Dichiarazione conflitto
FARMACI BIOSIMILARI: OPPORTUNITÀ TERAPEUTICA E DI RISPARMIO? CLINICI E PAZIENTI SI CONFRONTANO
 FARMACI BIOSIMILARI: OPPORTUNITÀ TERAPEUTICA E DI RISPARMIO? CLINICI E PAZIENTI SI CONFRONTANO Tutelare le esigenze del paziente e il diritto ad avvalersi delle migliori terapie disponibili e al tempo
FARMACI BIOSIMILARI: OPPORTUNITÀ TERAPEUTICA E DI RISPARMIO? CLINICI E PAZIENTI SI CONFRONTANO Tutelare le esigenze del paziente e il diritto ad avvalersi delle migliori terapie disponibili e al tempo
Recenti novità sull impiego pediatrico di paracetamolo all insegna dell appropriatezza
 Recenti novità sull impiego pediatrico di paracetamolo all insegna dell appropriatezza Fonte: de Martino, M, Chiarugi A. Recent advances in pediatric use of oral paracetamol in fever and pain management.
Recenti novità sull impiego pediatrico di paracetamolo all insegna dell appropriatezza Fonte: de Martino, M, Chiarugi A. Recent advances in pediatric use of oral paracetamol in fever and pain management.
Strategie di implementazione dell informazione indipendente nell interfaccia ospedale territorio: opportunità e limiti di un modello complesso
 Strategie di implementazione dell informazione indipendente nell interfaccia ospedale territorio: opportunità e limiti di un modello complesso Anna Maria Marata Nicola Magrini Roma 11 gennaio 2011 Aumento
Strategie di implementazione dell informazione indipendente nell interfaccia ospedale territorio: opportunità e limiti di un modello complesso Anna Maria Marata Nicola Magrini Roma 11 gennaio 2011 Aumento
CLASSICHE GENETICA BIOTECNOLOGIE MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA
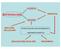 CLASSICHE BIOTECNOLOGIE GENETICA MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA BIOLOGIA MOLECOLARE BIOCHIMICA CREAZIONE A FINI MEDICI DI MICRO-ORGANISMI GENETICAMENTE MODIFICATI
CLASSICHE BIOTECNOLOGIE GENETICA MODERNE BIOLOGIA CELLULARE TECNOLOGIA DEL DNA RICOMBINANTE INGEGNERIA GENETICA BIOLOGIA MOLECOLARE BIOCHIMICA CREAZIONE A FINI MEDICI DI MICRO-ORGANISMI GENETICAMENTE MODIFICATI
EFFICACIA E SOSTENIBILITA DELLA TERAPIA INSULINICA CON BIOSIMILARI
 EFFICACIA E OTENIBILITA DELLA TERAPIA INULINICA CON BIOIMILARI C. Baggiore OC Diabetologia e Malatt. Metab. Che cos è un biosimilare? Il termine biosimilare rappresenta per lo più una designazione normativa
EFFICACIA E OTENIBILITA DELLA TERAPIA INULINICA CON BIOIMILARI C. Baggiore OC Diabetologia e Malatt. Metab. Che cos è un biosimilare? Il termine biosimilare rappresenta per lo più una designazione normativa
SOSTENIBILITA ed ACCESSO ALLE CURE. Maurizio Pastorello Dip.to Farmaceutico ASP Palermo
 SOSTENIBILITA ed ACCESSO ALLE CURE Maurizio Pastorello Dip.to Farmaceutico ASP Palermo Sin dal 2012, tra gli scopi primari del Dipartimento Farmaceutico c è stata la promozione dell utilizzo del biosimilare
SOSTENIBILITA ed ACCESSO ALLE CURE Maurizio Pastorello Dip.to Farmaceutico ASP Palermo Sin dal 2012, tra gli scopi primari del Dipartimento Farmaceutico c è stata la promozione dell utilizzo del biosimilare
SCHEDA DI PRESCRIZIONE DELLA TERAPIA
 ALLEGATO A-1 SCHEDA DI PRESCRIZIONE DELLA TERAPIA PRESCRIZIONE FARMACI BIOLOGICI REGIONE CALABRIA Artrite Reumatoide, Artrite Psoriasica, Spondiloartriti Cognome: Nome:. Codice Fiscale Sesso: M F Luogo
ALLEGATO A-1 SCHEDA DI PRESCRIZIONE DELLA TERAPIA PRESCRIZIONE FARMACI BIOLOGICI REGIONE CALABRIA Artrite Reumatoide, Artrite Psoriasica, Spondiloartriti Cognome: Nome:. Codice Fiscale Sesso: M F Luogo
epoetine Anita Conforti Istituto Superiore di Sanità, 25 giugno 2015 Dipartimento di Sanità Pubblica e Medicina di Comunità Università di Verona
 Nefrologia: profilo di sicurezza delle epoetine Anita Conforti Dipartimento di Sanità Pubblica e Medicina di Comunità Università di Verona Istituto Superiore di Sanità, 25 giugno 2015 Ruolo dell eritropoietina
Nefrologia: profilo di sicurezza delle epoetine Anita Conforti Dipartimento di Sanità Pubblica e Medicina di Comunità Università di Verona Istituto Superiore di Sanità, 25 giugno 2015 Ruolo dell eritropoietina
 www.fisiokinesiterapia.biz LA TERAPIA DELL ARTRITE REUMATOIDE Concetti introduttivi e nuove terapie farmacologiche MODELLO EVOLUTIVO AR A- Popolazione generale + Fattori di rischio B- Poliartrite infiammatoria
www.fisiokinesiterapia.biz LA TERAPIA DELL ARTRITE REUMATOIDE Concetti introduttivi e nuove terapie farmacologiche MODELLO EVOLUTIVO AR A- Popolazione generale + Fattori di rischio B- Poliartrite infiammatoria
I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico
 DOCUMENTO DI INDIRIZZO della CRF n. 1 I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico Le implicazioni per la pratica clinica in termini di sovrapponibilità, sostituibilità
DOCUMENTO DI INDIRIZZO della CRF n. 1 I farmaci biosimilari ovvero quando scade il brevetto di un farmaco biotecnologico Le implicazioni per la pratica clinica in termini di sovrapponibilità, sostituibilità
MONOGRAFIA SINTESI. IBRANCE (palbociclib) Carcinoma Mammario. A cura della Commissione Terapeutica Oncologica
 MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali e nazionali. Francesca Mattioli
 FARMACO DI MARCA O EQUIVALENTE? Qualità, efficacia e responsabilità nell'attività prescrittiva Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali
FARMACO DI MARCA O EQUIVALENTE? Qualità, efficacia e responsabilità nell'attività prescrittiva Caratteristiche delle preparazioni farmaceutiche degli equivalenti: aspetti farmacologici e legislativi internazionali
Eritropoietina e biosimilari: il punto di vista dell ematologo
 Eritropoietina e biosimilari: il punto di vista dell ematologo Roberto Latagliata Università Sapienza Dipartimento di Ematologia Azienda Policlinico Umberto I Roma Ematologia LE ERITROPOIETINE: UNA NUMEROSA
Eritropoietina e biosimilari: il punto di vista dell ematologo Roberto Latagliata Università Sapienza Dipartimento di Ematologia Azienda Policlinico Umberto I Roma Ematologia LE ERITROPOIETINE: UNA NUMEROSA
WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO
 WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE
WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE SOSTENIBILE DEI FARMACI ONCOLOGICI INNOVATIVI AD ALTO COSTO WORKSHOP IL GOVERNO DELL INNOVAZIONE FARMACEUTICA: MODELLI DI GESTIONE
BIOSIMILARI: PRIMI DATI OSSERVAZIONALI PRESSO LA DIALISI DEL POLICLINICO DI MONZA
 POLICLINICO DI MONZA BIOSIMILARI: PRIMI DATI OSSERVAZIONALI PRESSO LA DIALISI DEL POLICLINICO DI MONZA ERITROPOIETINA IL GENE UMANO E' STATO CLONATO NEL 1985: rhuepo è stata utlilizzata con successo nel
POLICLINICO DI MONZA BIOSIMILARI: PRIMI DATI OSSERVAZIONALI PRESSO LA DIALISI DEL POLICLINICO DI MONZA ERITROPOIETINA IL GENE UMANO E' STATO CLONATO NEL 1985: rhuepo è stata utlilizzata con successo nel
Impatto dello switching da infliximab originator a infliximabbiosilimare. la dimensione clinica
 12 Dicembre 2018 Villa La Quiete Firenze Impatto dello switching da infliximab originator a infliximabbiosilimare in reumatologia: la dimensione clinica Irma Convertino, PhD student University of Pisa
12 Dicembre 2018 Villa La Quiete Firenze Impatto dello switching da infliximab originator a infliximabbiosilimare in reumatologia: la dimensione clinica Irma Convertino, PhD student University of Pisa
FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF
 FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF Nell ambito della Terza edizione del progetto Il sistema regolatorio in Italia tra certezze
FOCUS ON IL SISTEMA REGOLATORIO IN ITALIA TRA CERTEZZE E CONTRADDIZIONI Prof. Giorgio Cantelli Forti, Presidente SIF Nell ambito della Terza edizione del progetto Il sistema regolatorio in Italia tra certezze
Parte D. Farmaci equivalenti classe A-SSN e biosimilari
 Parte D Farmaci equivalenti classe A-SSN e biosimilari Con il simbolo ^ si intende la prescrizione territoriale effettuata dai MMG e PLS rimborsata alle farmacie pubbliche e private dal SSN esclusa la
Parte D Farmaci equivalenti classe A-SSN e biosimilari Con il simbolo ^ si intende la prescrizione territoriale effettuata dai MMG e PLS rimborsata alle farmacie pubbliche e private dal SSN esclusa la
PRESCRIZIONE FARMACI BIOLOGICI REGIONE del VENETO Artrite Reumatoide, Artrite Psoriasica, Spondiloartriti. Cognome:..Nome:.. Codice Fiscale Sesso: M F
 Servizio Sanitario Nazionale - Regione Veneto AZIENDA ULSS N. 6 VICENZA Viale F. Rodolfi n. 37 36100 VICENZA COD. REGIONE 050 COD. U.L.SS. 006 COD.FISC. E P.IVA 02441500242 PRESCRIZIONE FARMACI BIOLOGICI
Servizio Sanitario Nazionale - Regione Veneto AZIENDA ULSS N. 6 VICENZA Viale F. Rodolfi n. 37 36100 VICENZA COD. REGIONE 050 COD. U.L.SS. 006 COD.FISC. E P.IVA 02441500242 PRESCRIZIONE FARMACI BIOLOGICI
 giunta regionale Allegato A al Decreto n. 329 del 22.12.2015 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
giunta regionale Allegato A al Decreto n. 329 del 22.12.2015 pag. 1/5 ELENCO DEI CENTRI AUTORIZZATI ALLA PRESCRIZIONE DI FARMACI BIOLOGICI PER IL PAZIENTE ADULTO E PEDIATRICO AREA REUMATOLOGICA, DERMATOLOGICA
Innovazione sostenibile in dermatologia e in reumatologia
 Innovazione sostenibile in dermatologia e in reumatologia Enrica Menditto CIRFF - Dipartimento di Farmacia Università degli Studi di Napoli Federico II Napoli, 26 maggio 2017 La sostenibilità del sistema
Innovazione sostenibile in dermatologia e in reumatologia Enrica Menditto CIRFF - Dipartimento di Farmacia Università degli Studi di Napoli Federico II Napoli, 26 maggio 2017 La sostenibilità del sistema
BIOSIMILARI LUCI E OMBRE
 BIOSIMILARI LUCI E OMBRE L avvento dei farmaci biotecnologici risale agli anni Ottanta del secolo scorso, con l immissione in commercio della prima insulina ricombinante. Attualmente sono disponibili numerosi
BIOSIMILARI LUCI E OMBRE L avvento dei farmaci biotecnologici risale agli anni Ottanta del secolo scorso, con l immissione in commercio della prima insulina ricombinante. Attualmente sono disponibili numerosi
Medicinali biosimilari nell UE Guida informativa per gli operatori sanitari
 Medicinali biosimilari nell UE Guida informativa per gli operatori sanitari Elaborata congiuntamente dall Agenzia europea per i medicinali e dalla Commissione europea Indice Prefazione 2 Sommario 3 Medicinali
Medicinali biosimilari nell UE Guida informativa per gli operatori sanitari Elaborata congiuntamente dall Agenzia europea per i medicinali e dalla Commissione europea Indice Prefazione 2 Sommario 3 Medicinali
Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche Napoli 26 Maggio 2017, Hotel Holiday Inn
 Federico II University of Naples Founded in 1224 Divisione di Farmacologia Scuola di Medicina Università di Napoli Federico II Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche
Federico II University of Naples Founded in 1224 Divisione di Farmacologia Scuola di Medicina Università di Napoli Federico II Sostenibilità e L.E.A.: il Caso delle Malattie Autoimmuni Non Oncologiche
Le nuove prospettive cliniche
 VI Meeting Progetto Multicentrico Piemontese di standardizzazione dei percorsi diagnostici di coliti IBD e NON IBD alla prima diagnosi Le nuove prospettive cliniche Dott. Marco Astegiano AO Città della
VI Meeting Progetto Multicentrico Piemontese di standardizzazione dei percorsi diagnostici di coliti IBD e NON IBD alla prima diagnosi Le nuove prospettive cliniche Dott. Marco Astegiano AO Città della
