FRONTESPIZIO. Azacitidina (orale)
|
|
|
- Modesto Lolli
- 8 anni fa
- Просмотров:
Транскрипт
1 FRONTESPIZIO STUDIO DI FASE 3, MULTICENTRICO, RANDOMIZZATO, IN DOPPIA CECITÀ, CHE SI PROPONE DI CONFRONTARE L EFFICACIA E LA SICUREZZA DELL AZACITIDINA ORALE SOMMINISTRATA INSIEME ALLA MIGLIOR TERAPIA DI SUPPORTO CON IL PLACEBO SOMMINISTRATO INSIEME ALLA MIGLIORE TERAPIA DI SUPPORTO A SOGGETTI CON ANEMIA TRASFUSIONE-DIPENDENTE E TROMBOCITOPENIA CAUSATE DA SINDROMI MIELODISPLASTICHE A PIÙ BASSO RISCHIO SECONDO L IPSS FARMACO SPERIMENTALE: NUMERO DI PROTOCOLLO: DATA FINALE: DATA FINALE EMENDAMENTO N. 1.0: DATA FINALE EMENDAMENTO N. 2.0: NUMERO EudraCT: Azacitidina orale AZA-MDS maggio aprile 2014 NUMERO IND: NOME/INDIRIZZO DELLO SPONSOR: 8 ottobre Morris Avenue Summit, NJ RISERVATO Il presente protocollo Le viene fornito in quanto Sperimentatore, potenziale Sperimentatore o consulente per una valutazione da parte Sua, del Suo staff e del Comitato Etico di revisione. Le informazioni contenute nel presente documento sono da considerarsi riservate e, tranne se necessario per ottenere il consenso informato, non possono essere divulgate a terzi, a meno che ciò non sia richiesto dalla legge o da altri regolamenti. Le persone a cui verranno rivelate tali informazioni devono essere informate del fatto che si tratta di informazioni riservate, non divulgabili a terzi. Riservato ed esclusivo 1 Sinossi AZA-MDS-003 Italia - Versione italiana 3.0 datata 11 novembre 15 basata sull emendamento 2.0 alla Sinossi AZA-MDS-003 Finale 08 ottobre 2015
2 MEDICAL MONITOR/CONTATTI DI RIFERIMENTO PER LE EMERGENZE Contatti di riferimento: Nome: Barry Skikne, MD, FACP; FCP (SA) Titolo: Direttore esecutivo, Ricerca clinica e Sviluppo Indirizzo: 9225 Indian Creek Parkway, Suite Overland Park, KS Telefono: [email protected] Nota: in caso di emergenza rivolgersi al call-center generale, disponibile 24 ore su 24, solo nel caso in cui non sia possibile contattare il Responsabile Scientifico della ricerca clinica o il Medical Monitor o un incaricato per le chiamate di emergenza Call-center generale da contattare in caso di emergenza, disponibile 24 ore su 24: Riservato ed esclusivo 2
3 1. SINOSSI Nome dello sponsor/dell azienda: Nome del farmaco sperimentale: Azacitidina orale Numero di protocollo: AZA-MDS-003 Titolo del protocollo: Studio di fase 3, multicentrico, randomizzato, in doppia cecità, che si propone di confrontare l efficacia e la sicurezza dell azacitidina orale somministrata insieme alla miglior terapia di supporto con il placebo somministrato insieme alla migliore terapia di supporto a soggetti con anemia trasfusione-dipendente e trombocitopenia causate da sindromi mielodisplastiche a più basso rischio secondo l IPSS. Indicazione: Trattamento delle sindromi mielodisplastiche (SMD) a più basso rischio secondo il sistema di punteggio prognostico internazionale (IPSS) con anemia dipendente da trasfusioni di globuli rossi (GR) e trombocitopenia. Durata dello studio: La durata prevista per lo studio è di 60 mesi, che comprende un periodo di arruolamento di 26 mesi, seguito da 34 mesi di trattamento e/o osservazione del soggetto. Lo studio si concluderà al raggiungimento del numero totale di eventi (n=250 decessi) necessario per un'analisi completa della sopravvivenza globale, atteso presumibilmente circa 60 mesi dopo la randomizzazione del primo soggetto nello studio. Lo Sponsor potrebbe terminare la sperimentazione una volta analizzati tutti gli endpoint e obiettivi principali dello studio, e in presenza della disponibilità di un protocollo di roll-over in cui eventuali soggetti rimanenti nello studio possono essere inseriti (in seguito all apertura del cieco) e continuare a ricevere il trattamento con azacitidina orale. Tale protocollo sarebbe redatto per un composto che non sarebbe ancora disponibile in commercio. Obiettivi: Primario: Secondario: Fase di sviluppo: 3 Valutare l'indipendenza da trasfusioni di globuli rossi nei 2 bracci di trattamento (azacitidina orale associata alla migliore terapia di supporto rispetto a placebo associato alla migliore terapia di supporto) in soggetti con anemia dipendente da trasfusioni di globuli rossi e trombocitopenia (numero di piastrine 75 x 109/l) a causa della SMD a più basso rischio secondo l IPSS. Valutare in entrambi i bracci di trattamento - la sopravvivenza globale (OS); Riservato ed esclusivo 3
4 Esplorativi: - la risposta ematologica con miglioramento della conta piastrinica (HI-P); - la durata dell'indipendenza da trasfusioni di globuli rossi e il tempo trascorso fino al raggiungimento dell'indipendenza da trasfusioni di globuli rossi; - la progressione a Leucemia Mieloide Acuta (LAM) e il tempo trascorso prima della comparsa di tale progressione; - la risposta ematologica con miglioramento eritroide (HI-E); - l'indipendenza dalle trasfusioni di piastrine, la durata dell'indipendenza dalle trasfusioni di piastrine e il tempo trascorso prima del raggiungimento dell'indipendenza dalle trasfusioni di piastrine; - la risposta ematologica; - eventi di sanguinamento clinicamente significativi; - la sicurezza; - la qualità della vita relativa allo stato di salute (HRQoL); e - l'utilizzo di risorse mediche. Determinare la concentrazione di azacitidina nel plasma e valutare le relazioni esposizione-risposta con gli endpoint di efficacia e sicurezza. Valutare alla visita basale i marker molecolari e cellulari nel midollo osseo che potrebbero fornire un'ulteriore classificazione prognostica di sottotipi di SMD e avere un potenziale impatto sull'efficacia di azacitidina. Valutare alla visita basale e durante la terapia sia i marker molecolari e cellulari nei campioni di midollo osseo e/o del sangue periferico, che potrebbero essere in grado di fornire informazioni sul meccanismo di azione di azacitidina, che i marker terapeutici predittivi di risposta o ricaduta della malattia. Endpoint dello studio: Primario Secondari Numero di soggetti nella popolazione globale dello studio che raggiungono un'indipendenza dalle trasfusioni di globuli rossi di durata a 84 giorni (12 settimane) Sopravvivenza globale. HI-P (criteri IWG 2006; Cheson et al., Blood, 2006). Percentuale dei soggetti nella popolazione globale che raggiunge l indipendenza da trasfusioni di globuli rossi per 56 giorni (8 settimane). Durata dell'indipendenza da trasfusioni di globuli rossi 84 giorni (12 settimane). Riservato ed esclusivo 4
5 Durata dell indipendenza da trasfusioni di globuli rossi 56 giorni (8 settimane); Tempo trascorso prima dell'indipendenza da trasfusioni di globuli rossi 84 giorni (12 settimane). Tempo trascorso prima dell'indipendenza da trasfusioni di globuli rossi 56 giorni (8 settimane). Numero di soggetti che manifestano una progressione a LAM e tempo trascorso prima dell insorgenza della progressione a LAM. HI-E (criteri IWG 2006; Cheson et al., Blood, 2006). Numero di soggetti dipendenti dalle trasfusioni di piastrine alla visita basale che raggiungono un'indipendenza dalle trasfusioni di piastrine di durata a 56 giorni (8 settimane). Durata dell'indipendenza da trasfusioni di piastrine. Tempo trascorso prima dell'indipendenza da trasfusioni di piastrine. Risposta ematologica (criteri IWG 2006; Cheson et al., Blood, 2006). Esplorativi Disegno dello studio: Numero di soggetti con eventi di sanguinamento clinicamente significativi. Sicurezza (tipo, frequenza, gravità degli eventi avversi e relazione tra gli eventi avversi e azacitidina orale/placebo; monitoraggio della progressione a LAM e seconde neoplasie primarie). HRQoL con l utilizzo della scala di Valutazione Funzionale dell'anemia dovuta a Terapia anti-cancro (FACT-An) ed dell EuroQoL Group EQ-5D-3L. Valutazione dell'utilizzo di risorse mediche. Analisi correlative per valutare la relazione tra l'esposizione ad azacitidina e la farmacodinamica (ad es. sicurezza, efficacia) e altri endpoint esplorativi (ad es. i biomarcatori). Le analisi dei biomarcatori (caratteristiche molecolari e/o cellulari nel midollo osseo e/o nel sangue periferico) possono includere, ma non essere limitati a, analisi di citogenetica, della metilazione del DNA, delle varianti genetiche (polimorfismi di un singolo nucleotide [SNP] e della sequenza dei geni), dell espressione dell acido ribonucleico messaggero (mrna), dell espressione del micro RNA (mirna), della metilazione dell'rna, analisi di immuno-fenotipizzazione e valutazione delle proteine nel plasma. Si tratta di uno studio di fase 3, multicentrico, randomizzato, in doppio cieco, controllato con placebo, a gruppi paralleli, condotto su soggetti con anemia dipendente da trasfusioni di globuli rossi e trombocitopenia (ad es. numero di piastrine 75 x 10 9 /l) causate di sindromi mieloplastiche a più basso rischio secondo l IPSS. Lo studio prevede tre fasi: screening, Riservato ed esclusivo 5
6 trattamento in doppio cieco e follow-up. La Figura 1 illustra una panoramica schematizzata dello studio. Le procedure e le valutazioni eseguite sui soggetti durante la fase di screening devono essere completate entro 56 giorni dalla randomizzazione (vedere Tabella 1). La revisione indipendente centralizzata dei campioni di aspirato midollare, della biopsia e dei vetrini di sangue periferico, l'analisi centralizzata della citogenetica e i risultati delle analisi ematologiche condotte dal laboratorio centralizzato saranno utilizzati per confermare la SMD e la classificazione WHO, nonché per determinare il rischio secondo l IPSS. La dipendenza da trasfusioni di globuli rossi e la trombocitopenia devono essere confermate anche dai criteri di eleggibilità. È necessario disporre della storia cronologica delle trasfusioni di globuli rossi eseguite nei 84 giorni prima della randomizzazione, nonché, se applicabile, di una cronologia delle trasfusioni di piastrine eseguite nei 56 giorni prima della randomizzazione. I dati sulle trasfusioni dovrebbero comprendere tipo, numero di unità, motivo e data della trasfusione; inoltre è necessario riportare il valore dell'emoglobina (Hgb) o il numero delle piastrine che ha causato la somministrazione della trasfusione. Dopo la conferma dell eleggibilità che deve essere eseguita alla visita di screening, i soggetti saranno randomizzati in un rapporto 1:1 per ricevere 300 mg di azacitidina orale o placebo una volta al giorno (QD) per i primi 21 giorni di ciascun ciclo di trattamento di 28 giorni. La randomizzazione verrà eseguita centralmente, mediante un sistema di risposta vocale interattivo (IVRS), con stratificazione secondo quanto descritto nella sezione dell analisi statistica. La prima dose di farmaco sperimentale (IP, azacitidina orale o placebo) dovrebbe essere somministrata entro 3 giorni dalla randomizzazione. I soggetti che soddisfano tutti i criteri specificati dal protocollo (ad es. i soggetti devono continuare a soddisfare i criteri relativi alla funzione renale ed epatica) continueranno a ricevere cicli aggiuntivi del trattamento in studio. La terapia in studio sarà somministrata per tutto il tempo in cui il soggetto ne trarrà beneficio. Dal momento che la risposta ematologica al trattamento con azacitidina spesso si manifesta tardivamente, è consigliabile che i soggetti ricevano almeno 6 cicli di trattamento con il farmaco sperimentale; tuttavia, i soggetti possono interrompere il trattamento a discrezione dello Sperimentatore prima di raggiungere il numero di cicli minimo consigliato. I motivi per interrompere il trattamento possono comprendere la comparsa di progressione della malattia (Appendice A), comparsa di eventi avversi, il ritiro del consenso, il decesso, la mancata presenza alla visita di follow-up o una violazione del protocollo. Lo stato della malattia dei soggetti sarà valutata alla fine del Ciclo 6 e prima dell'inizio del Ciclo 7. Se i soggetti soddisferanno i seguenti criteri, potranno continuare il trattamento con il Ciclo 7 ed i successivi, e lo stato della malattia sarà valutato di alla fine di ciascun ciclo: indipendenza dalle trasfusioni di globuli rossi o indipendenza dalle trasfusioni di piastrine per quei soggetti che erano dipendenti dalle trasfusioni di piastrine alla visita basale o miglioramento ematologico (HI; Cheson, 2006; Appendice D) o riduzione 50% del fabbisogno medio di trasfusioni di globuli rossi nei 56 giorni Riservato ed esclusivo 6
7 (8 settimane) immediatamente precedente la valutazione dello stato della malattia rispetto al fabbisogno medio di trasfusioni di globuli rossi alla visita basale o qualsiasi altro beneficio clinico, compresa l'assenza di evidenza di progressione della malattia (vedere la Sezione 12 del protocollo per le definizioni di progressione di malattia). Se i soggetti non soddisferanno tali criteri alla fine del Ciclo 6, la terapia in studio sarà interrotta. Prima di interrompere la terapia di un soggetto, lo Sperimentatore dovrebbe contattare il Medical Monitor dello ed inoltrare un adeguata documentazione per una revisione e discussione del caso. Tutti i soggetti che hanno ricevuto almeno una dose di farmaco sperimentale devono sottoporsi alla visita di fine trattamento (vedere Tabella 1) non appena la terapia viene interrotta. Tutti i pazienti per i quali la terapia in studio è stata interrotta per un qualsiasi motivo, devono essere esaminati per valutare la sopravvivenza, le successive terapie somministrate per la SMD la progressione a LAM e secondi tumori primari. Se necessario è possibile somministrare la migliore terapia di supporto in combinazione con il trattamento dello studio. La migliore terapia di supporto può comprendere, ma non essere limitata a, le trasfusioni di globuli rossi (concentrati di globuli rossi o sangue intero), le trasfusioni di piastrine da donatore singolo o gruppo di donatori, gli antibiotici, la terapia antivirale e/o antifungina, il supporto nutritivo - se necessario- e la somministrazione di fattori di crescita che stimolano la produzione di granulocitici nei soggetti con infezioni neutropeniche. In questo studio la migliore terapia di supporto esclude l'utilizzo di ESA e di altri fattori di crescita ematopoietica (l uso di i fattori stimolanti la produzione di granulociti è ammesso solo nei soggetti con infezioni neutropeniche). Durante il trattamento è possibile variare la dose per gestire un'eventuale tossicità. In caso di tossicità duratura, è consentito ridurre la dose al massimo a 200 mg ed è consentito variare, gradualmente, il trattamento previsto, da 21 a 14 giorni e poi da 14 a 7 giorni, sempre al dosaggio di 200 mg. Le valutazioni di efficacia e sicurezza da effettuare durante lo studio sono descritte in dettaglio nella Tabella 1. Dopo la randomizzazione non sono ammessi crossover tra i bracci di trattamento per tutta la durata dello studio. Numero previsto di soggetti: Saranno randomizzati nello studio circa 386 soggetti (circa 193 per ogni braccio di trattamento) che soddisfano tutti i criteri di inclusione e non soddisfano alcun criterio di esclusione. Popolazione dello studio Criteri di inclusione: Per essere arruolati nello studio, i soggetti devono soddisfare i Riservato ed esclusivo 7
8 seguenti criteri: 1. Età a 18 anni 1 al momento della firma del modulo di consenso informato 2. Diagnosi documentata di SMD in base alla classificazione WHO Dipendenza da trasfusioni di globuli rossi, definita come: Fabbisogno medio di trasfusioni pari a 2 unità 2 di globuli rossi nell'arco di 28 giorni confermate per un minimo di 56 giorni prima della randomizzazione (si prega di notare che il periodo che copre la storia trasfusionale si sovrappone alla fase di screening) I livelli di emoglobina al momento della somministrazione della trasfusione di globuli rossi o nei 7 giorni precedenti devono essere 10,0 g/dl affinché la trasfusione sia conteggiata per definire lo stato di dipendenza da trasfusioni di globuli rossi. Le trasfusioni di globuli rossi somministrate con livelli Hgb > 10,0 g/dl e/o le trasfusioni somministrate nel corso di un intervento di chirurgia elettiva non vengono considerate necessarie e non sono comprovanti dello stato di dipendenza da trasfusioni di globuli rossi Nessun periodo di 28 giorni consecutivi senza la somministrazione di trasfusioni di globuli rossi negli 56 giorni immediatamente precedenti la randomizzazione 4. Trombocitopenia definita come valutazione di due conte piastriniche 75 x 10 9 /l eseguite a 21 giorni di distanza. La seconda valutazione di conta piastrinica di deve essere confermata 14 giorni prima della randomizzazione Almeno una conta piastrinica deve essere analizzata a livello centrale nel periodo di screening di 56 giorni con risultati 75 x 10 9 /l; la seconda conta piastrinica può essere analizzata a livello centrale o locale con risultati anch essi 75 x 10 9 /l. Una pregressa anamnesi medica documentata di trombocitopenia può essere usata per dimostrare l idoneità per lo studio se almeno una precedente conta piastrinica 75 x 10 9 /l è stata ottenuta nei 56 giorni successivi alla randomizzazione e a distanza di 21 giorni dalla conta piastrinica analizzata a livello centrale. Se durante il periodo a interim sono state eseguite delle conte piastriniche aggiuntive, anche queste devono avere un valore 75 x 10 9 /l. Se le conte piastriniche nel periodo a interim sono > 75 x 10 9 /l, ciò sarebbe accettabile solo se direttamente associate a una trasfusione di piastrine somministrata nei 7 giorni precedenti la data della conta piastrinica 1 In Giappone, sia il soggetto che il rappresentante legale del soggetto devono firmare il modulo di consenso informato se il soggetto non ha ancora compiuto i 20 anni. 2 In conformità alla prassi medica in Giappone, 1 unità di globuli rossi indicata nel protocollo equivale a 2 unità di globuli rossi in Giappone. Riservato ed esclusivo 8
9 5. Performance Status secondo ECOG di 0, 1 o 2 6. Le donne potenzialmente fertili (FCBP) 3 possono partecipare allo studio se soddisfano le condizioni seguenti: Accettino di usare almeno due metodi contraccettivi efficaci (contraccettivo ormonale orale, iniettabile o impiantabile; legatura delle tube; dispositivo intrauterino; contraccettivo a barriera con spermicida o partner vasectomizzato) per tutta la durata dello studio e per 3 mesi dopo l assunzione dell'ultima dose dell IP; e Abbiano un test di gravidanza sul siero negativo allo screening (Sezione del protocollo); e Abbiano un test di gravidanza sul siero o sulle urine negativo (a discrezione dello Sperimentatore; sensibilità di almeno 25 miu/ml) nelle 72 ore precedenti l'inizio dell IP (il test di gravidanza sul siero allo screening può essere usato come test prima dell'inizio della terapia sperimentale se eseguito entro le 72 ore) (Sezione del protocollo) 7. I soggetti di sesso maschile con partner di sesso femminile potenzialmente fertile devono accettare di usare almeno due metodi contraccettivi approvati dal medico per l'intero corso dello studio ed evitare di concepire un figlio per l'intero corso dello studio e nei 3 mesi successivi l assunzione dell'ultima dose dell IP 8. Comprensione e sottoscrizione volontaria del modulo di consenso informato prima che venga effettuata qualsiasi valutazione/procedura correlata allo studio 9. Capacità di attenersi al programma di visite dello studio e agli altri requisiti del protocollo Criteri di esclusione: La presenza di uno dei seguenti fattori potrà escludere un soggetto dall'arruolamento: 1. SMD a rischio (Appendice B del protocollo) più elevato secondo l IPSS (rischio INT-2 o elevato) 2. SMD secondaria, ad es. SMD causata da danno chimico o dal trattamento con chemioterapia e/o da radiazioni per altre malattie a meno che il soggetto abbia ricevuto l ultima dose da una precedente terapia antineoplastica 24 settimane prima della randomizzazione 3. SMD ipoplastica o altro sottotipo candidate al trattamento con immunoterapia in base al giudizio dello sperimentatore, a meno che il soggetto abbia ricevuto l ultima dose da una precedente chemio ~ o immunoterapia 24 settimane prima della randomizzazione 3 Una donna potenzialmente fertile è una donna sessualmente matura che 1) non è stata sottoposta ad isterectomia (l asportazione chirurgica dell utero) o ad ovariectomia bilaterale (l asportazione chirurgica di entrambe le ovaie) oppure 2) non è in stato di post-menopausa naturale (l amenorrea dovuta a terapia anticancro non esclude la potenziale fertilità) da almeno 24 mesi consecutivi (cioè ha avuto almeno un ciclo mestruale nei 24 mesi precedenti). Riservato ed esclusivo 9
10 4. LMMC, Leucemia Mieloide Cronica Atipica (LMC) e malattia mieloproliferativa non classificabile (MMP) 5. Precedente trattamento con uno dei farmaci seguenti: Azacitidina (una qualsiasi formulazione), decitabina o altro agente ipometilante Lenalidomide a meno che il soggetto abbia ricevuto l ultima dose 8 settimane prima della randomizzazione 6. Precedente trapianto di cellule staminali autologo o allogenico 7. Storia di malattia infiammatoria dell'intestino (ad es. morbo di Crohn, colite ulcerosa), celiachia, precedente gastrectomia o asportazione del tratto intestinale superiore o qualsiasi patologia o difetto gastrointestinale di altro tipo in grado di interferire con l'assorbimento, la distribuzione, il metabolismo o l'eliminazione dell IP e/o predisporre il soggetto a un aumentato rischio di tossicità gastrointestinale 8. Trombocitopenia secondaria ad altre possibili cause, compresa l assunzione di farmaco/i, patologia/e congenita/e, disturbo/i del sistema immunitario (ad es. porpora trombocitopenica idiopatica [PIT]) o disturbo/i microvascolare/i (ad es. coagulazione intravascolare disseminata, sindrome uremico emolitica, porpora trombocitopenica trombotica) 9. Uso di uno qualsiasi dei farmaci seguenti nei 28 giorni precedenti la randomizzazione: Agenti citotossici, agenti chemioterapici, agenti/terapie mirati/e o/sperimentali Agenti stimolanti la formazione di trombi (AST; ad es. Romiplostim, Eltrombopag, Interleukina-11) ESA e altri fattori di crescita ematopoietica (ad es. Interleukina-3) Idrossiurea 10. Eventi avversi significativi da un punto di vista medico da trattamento precedente ancora in corso, a prescindere dall'arco di tempo 11. Uso concomitante di uno dei farmaci seguenti: Agenti ferrochelanti, tranne per soggetti che ricevono un trattamento a dosaggio stabile o decrescente da almeno 8 settimane (56 giorni) prima della randomizzazione Corticosteroidi, tranne per soggetti che, per condizioni mediche diverse dalla SMD, ricevono un trattamento a dosaggio stabile o in diminuzione da 1 settimana prima della randomizzazione 12. Storia precedente di tumori maligni diversi dalla SMD, a meno che il soggetto non presenti tracce di malattia da 3 anni. Sono ammessi i soggetti con storia/condizioni concomitanti seguenti: Carcinoma della pelle a cellule basali o cellule squamose Carcinoma in situ della cervice Riservato ed esclusivo 10
11 Carcinoma mammario in situ Riscontro istologico di cancro alla prostata (T1a o T1b secondo il sistema di classificazione clinica di tumore, nodi, metastasi [TNM]) 13. Malattia cardiaca significativamente attiva nei 6 mesi precedenti, tra cui: Insufficienza cardiaca congestizia di classe IV secondo la New York Heart Association (NYHA) Angina instabile o angina che richiede intervento medico o chirurgico; e/o Infarto del miocardio 14. Infezione fungina, batterica, o virale sistemica non controllata (definita come presenza di segni/sintomi correlati all'infezione e senza miglioramento nonostante una terapia antibiotica o antivirale appropriata e/o altro trattamento) 15. Virus da immunodeficienza umana (HIV) o infezione da epatite C (HCV) note, o evidenza di infezione attiva da virus dell epatite B (HBV) 16. Parametri di coagulazione del sangue anomali (PT > 15 secondi, PTT > 40 secondi e/o INR > 1.5). In seguito alla consultazione con il responsabile medico del monitoraggio, livelli ad un intervallo più elevato del normale possono essere accettabili se il soggetto viene trattato con dose stabile di anticoagulanti per la profilassi trombotica (ovvero con fibrillazione atriale, precedente evento tromboembolico, sostituzione di valvola cardiaca meccanica o presenza di lupus o anticorpi antifosfolipidi). Sarà responsabilità dello sperimentatore prendere la decisione relativa all inclusione di tali pazienti. 17. Una delle seguenti anomalie nei valori di laboratorio: AST/SGOT o ALT/SGPT sieriche 2,5 volte il limite superiore della norma (ULN), a meno che i risultati anomali in questo/i esame/i sulla funzione epatica possano essere attribuiti al sovraccarico di ferro come dimostrato da una saturazione della transferrina sierica >65% e da una ferritina sierica >1000 µg/l. Bilirubina sierica > 1,5 x ULN. Livelli più elevati sono accettabili se attribuibili a distruzione di precursori dei globuli rossi attiva all'interno del midollo osseo (ad es. eritropoiesi inefficiente) o in presenza di nota storia di sindrome di Gilbert. I soggetti sono esclusi in caso di evidenza di anemia emolitica autoimmune che si manifesta con una conta dei reticolociti corretta > 2% con test di Coombs positivo o bilirubina indiretta superiore al 50% Creatinina sierica 2,5 X ULN 18. Anemia nota e clinicamente significativa dovuta a carenza di ferro, di vitamina B 12 o di folato oppure anemia emolitica autoimmune o ereditaria oppure causata da sanguinamento gastrointestinale. La mancanza di ferro viene valutata con l esecuzione di agoaspirato con mezzo di contrasto per ferro, calcolando la saturazione della transferrina (capacità ferro-legante totale [Fe/TIBC] 20%) o la ferritina nel siero 15 ng/ml Riservato ed esclusivo 11
12 19. Ipersensibilità nota o sospetta ad azacitidina o mannitolo 20. Gravidanza o allattamento 21. Qualsiasi condizione medica significativa, anomalia di laboratorio o malattia psichiatrica che potrebbe impedire al soggetto di partecipare allo studio 22. Qualsiasi condizione, compresa la presenza di anomalie di laboratorio, che esporrebbero il soggetto a rischio nel caso in cui partecipasse allo studio 23. Qualsiasi condizione che impedisca di interpretare i dati provenienti dallo studio Riservato ed esclusivo 12
13 Farmaco sperimentale, dosaggio e modalità di somministrazione: fornirà l azacitidina in compresse da 150 e/o 200 mg e le compresse del placebo corrispondente, da assumere per via orale. Ciascuna compressa contiene eccipienti generalmente ritenuti sicuri e usati in farmaci già commercializzati. I dettagli sulle specifiche formulazioni sono descritti nell'investigator s Brochure. Tutte le compresse saranno preparate in confezioni blister. L'assunzione del prodotto sperimentale è prevista per i primi 21 giorni di ciascun ciclo di trattamento di 28 giorni, tranne nel caso in cui sia necessario modificare il piano di somministrazione a causa dell insorgenza di tossicità. Il farmaco antiemetico (non fornito dallo Sponsor) può essere assunto 30 minuti prima della somministrazione del farmaco sperimentale a discrezione dello sperimentatore (Sezione 9.1 del protocollo). Il soggetto ingerirà il farmaco sperimentale con circa 240 ml di acqua a temperatura ambiente. Il prodotto sperimentale può essere assunto a stomaco vuoto o pieno (è possibile fornire come indicazione una colazione leggera o un pasto di circa 600 calorie al massimo). Valutazioni chiave: Efficacia: L'endpoint di efficacia primario è il numero di soggetti nella popolazione globale in studio che raggiungono un'indipendenza dalle trasfusioni di globuli rossi per un periodo a 56 giorni (12 settimane). Il numero di trasfusioni di globuli rossi somministrate negli 84 giorni immediatamente precedenti la data di randomizzazione (compresa) saranno usate per stabilire i requisiti di arruolamento al basale. Le trasfusioni di globuli rossi somministrate durante il periodo di trattamento saranno usate nell'analisi di efficacia. Le trasfusioni di globuli rossi effettuate per interventi di chirurgia elettiva non saranno conteggiate per valutare i requisiti di arruolamento al basale, o durante l'analisi della sicurezza o per determinare lo stato di progressione della malattia. Gli endpoint di efficacia secondari comprendono OS, HI-P, percentuale dei soggetti nella popolazione globale che raggiunge l'indipendenza da trasfusioni di globuli rossi con una durata 56 giorni (8 settimane), durata dell indipendenza da trasfusioni di globuli rossi [ 84 giorni (12 settimane) e 56 giorni (8 settimane)], tempo per raggiungere l' indipendenza da trasfusioni di globuli rossi [ 84 giorni (12 settimane) e 56 giorni (8 settimane)], numero di soggetti che progrediscono a LAM, tempo all insorgenza della progressione a LAM, HI-E (criteri IWG 2006; Cheson et al., Blood, 2006), numero di soggetti dipendenti da trasfusioni di piastrine al basale che raggiungono l'indipendenza per un periodo a 56 giorni (8 settimane), durata dell'indipendenza da trasfusioni di piastrine, tempo trascorso prima del raggiungimento dell'indipendenza dalle trasfusioni di piastrine, risposta ematologica (criteri IWG 2006; Cheson et al., Blood, 2006) e numero di soggetti che manifestano eventi di sanguinamento clinicamente significativi. Il numero di trasfusioni di piastrine somministrate nei 56 giorni immediatamente precedenti la data di randomizzazione (compresa) saranno valutate per stabilire i requisiti di arruolamento al basale. Il numero di trasfusioni di piastrine somministrate durante il periodo di trattamento saranno valutate nell'analisi di efficacia. Le trasfusioni di piastrine somministrate per interventi di chirurgia elettiva non saranno considerate per determinare i requisiti di arruolamento al basale, per eseguire l'analisi dell'efficacia o per stabilire lo stato Riservato ed esclusivo 13
14 di progressione della malattia. Sicurezza: Le valutazioni di sicurezza includono gli eventi avversi, il monitoraggio della progressione a LAM e dell insorgenza del secondo tumore maligno primario, l esame fisico, la misura dei segni vitali e peso corporeo, la valutazione del performance status secondo ECOG, gli esami ematologici e chimici, il livello di ferritina nel siero, le terapie concomitanti, le terapie e le procedure e i test di gravidanza (solo per soggetti FCBP). L elettrocardiogramma, le analisi delle urine e i test della coagulazione saranno ripetuti in base all'indicazione clinica durante la fase di trattamento in doppio cieco. Esplorazione: Saranno effettuate analisi correlative per valutare i rapporti tra esposizione all azacitidina e gli endpoint di farmacodinamica, compresi la sicurezza, l efficacia e i biomarcatori esplorativi. Saranno eseguite analisi di farmacocinetica /farmacodinamica della popolazione,a seconda dei casi. In questo studio saranno raccolti dati sparsi relativi alla concentrazione/tempo che saranno inoltre inseriti in un database più ampio per consentire lo sviluppo e la convalida di un modello farmacocinetico della popolazione esposta all azacitidina e contribuire all'identificazione di covariate che potrebbero influenzare la risposta farmacocinetica/farmacodinamica all azacitidina e gli endpoint di efficacia e sicurezza. Le valutazioni dei biomarcatori comprenderanno l analisi della sequenza di DNA dei geni che impattano sulla prognosi di SMD (ad es. TP53, EZH2, ETV6, RUNX1 e ASXL1), l analisi della metilazione del DNA e dell immunofenotipizzazione. Ulteriori analisi possono comprendere la citogenetica ad alta risoluzione (cariotipo A SNP), la metilazione dell'rna, ulteriori analisi di varianti genetiche (polimorfismi di un singolo nucleotide [SNP] e della sequenza di geni), l espressione dell'acido ribonucleico messaggero (mrna), l espressione del micro RNA (mirna) e l analisi delle proteine nel plasma. Campioni di cellule della mucosa boccale, di midollo osseo e di sangue saranno raccolti obbligatoriamente ai soggetti allo screening per eseguire le analisi dei biomarcatori molecolari e/o cellulari per una valutazione basale. Le valutazioni dei biomarcatori saranno eseguite su soggetti del braccio di controllo e di quello di trattamento, per ottenere una distinzione tra la natura prognostica e/o predittiva del/i marcatore/i. Nei soggetti che forniscono il consenso opzionale per l analisi dei campioni di midollo osseo e del sangue durante la fase di trattamento, saranno valutate le variazioni nei biomarcatori rispetto al basale. Questi dati saranno usati per identificare i potenziali meccanismi dell'attività di azacitidina e per analizzare i marcatori che predicono una risposta o una ricaduta di malattia durante la terapia con azacitidina orale. Analisi statistica: Panoramica statistica: Questo studio di fase 3, multicentrico, randomizzato, in doppio cieco, controllato con placebo, a gruppi paralleli confronta l'efficacia e la sicurezza dell azacitidina orale associata alla migliore terapia di supporto rispetto a placebo associato alla migliore terapia di supporto in soggetti con anemia dipendente da trasfusioni di globuli rossi e trombocitopenia (cioè numero di piastrine 75 x 109/l) causate da SMD a basso rischio Riservato ed esclusivo 14
15 o rischio Int-1. Dimensioni del campione: La base per la determinazione di potenza e dimensione del campione sarà un test dell'equivalenza delle curve di sopravvivenza globale tra i gruppi di trattamento con l azacitidina e il placebo con un'analisi log-rank stratificata. Ipotizzando una sopravvivenza globale media di 18 mesi nel gruppo trattato con placebo (Garcia-Manero et al, Leukemia 2008), che comprende un adeguamento per possibili cross-over esterni al protocollo dei soggetti trattati con placebo verso il trattamento attivo durante il periodo di osservazione, e una sopravvivenza globale media di 25,7 mesi (miglioramento del 43%) nel gruppo trattato con azacitidina, 386 soggetti (193 in ciascun gruppo) avranno all'incirca una potenza dell'80% di rilevare un rapporto di rischio costante di 0,70 utilizzando un'analisi log-rank bilaterale con livello della significatività globale di 0,05. Si ipotizza che la distribuzione della sopravvivenza globale sia esponenziale con tasso (di rischio) di insuccesso costante e che l arruolamento sia sempre uniforme con una percentuale di interruzione globale dell'1% in entrambi i gruppi di trattamento. Si otterranno informazioni complete affinché l analisi di log-rank abbia l 80% di potenza quando circa 250 soggetti saranno deceduti in entrambi i gruppi di trattamento. Dati demografici, disposizione e dosaggio L età, l altezza, il peso del soggetto e altre caratteristiche raccolte al basale saranno riassunti per mezzo di statistiche descrittive, mentre la fascia di età, il sesso, la razza e altre variabili saranno rappresentate con tabulazioni di frequenza per gruppo di trattamento. I dati sulla storia medica (codificati tramite la terminologia MedDRA) saranno riassunti usando le tabulazioni di frequenza per gruppo di trattamento, per classificazione organosistemica e per termine preferito. La disposizione del soggetto (assegnazione alla popolazione di analisi, randomizzazione, interruzione, unitamente alla ragione primaria dell interruzione) sarà riassunta con frequenza e percentuale per entrambe le fasi di trattamento e di follow up. Verrà fornita una sintesi dei soggetti arruolati per centro. Le deviazioni dal protocollo saranno riassunte utilizzando tabulazioni di frequenza. Analisi d'efficacia: Le analisi d'efficacia saranno effettuate sulla popolazione Intent-to-Treat (ITT), che comprende tutti i soggetti randomizzati, indipendentemente dal fatto che il trattamento sia stato loro somministrato o meno. I soggetti saranno analizzati come randomizzati. Saranno inoltre effettuate analisi d'efficacia di supporto usando la popolazione ITT modificata (mitt), che comprende tutti i soggetti per i quali è stata effettuata almeno una valutazione d'efficacia post-dosaggio, che soddisfano tutti i criteri di inclusione/esclusione, che non hanno presentato violazioni di protocollo maggiori durante lo studio e che hanno ricevuto almeno un ciclo di trattamento. Per effettuare la verifica dell'ipotesi su molteplici endpoint, controllando il tasso complessivo di errore di tipo I, sarà impiegato un approccio sequenziale in cui l'ordine degli endpoint da testare è pre-specificato. L'endpoint di efficacia primario sarà un test bilaterale con un livello di significatività di 0,05. Se viene dimostrata la superiorità Riservato ed esclusivo 15
16 dell azacitidina per l'endpoint di efficacia primario, l'endpoint di efficacia secondario, cioè la sopravvivenza globale, sarà testato in modo bilaterale con un livello di significatività di 0,05. L'endpoint primario del raggiungimento dell'indipendenza dalle trasfusioni di globuli rossi viene definito come assenza di trasfusioni di globuli rossi per un periodo di 84 giorni consecutivi nel corso del trattamento, ad es. nei Giorni 1-84, nei Giorni 2-85, nei Giorni 3-86, ecc. I soggetti che hanno interrotto il trattamento in doppio cieco per assenza di efficacia terapeutica saranno considerati come casi di mancata risposta. L'analisi di efficacia primaria sarà condotta sulla popolazione ITT e confronterà i tassi di indipendenza da trasfusioni di globuli rossi nei due gruppi di trattamento. Per questo confronto sarà impiegato un test chi-quadrato di Cochran-Mantel-Haenszel (CMH), stratificato in base al fabbisogno medio di trasfusioni di globuli rossi al basale ( 4 unità versus > 4 unità RBC nell'arco di 28 giorni), allo stato delle trasfusioni di piastrine al basale (dipendente o indipendente), al paese di arruolamento (ad es. Giappone versus Resto del mondo) e al Performance Status secondo l ECOG (da 0 a 1 versus 2), ad un livello alfa bilaterale di 0,05. L'omogeneità dell'effetto del trattamento tra gli strati sarà valutata utilizzando un test esatto per rapporto tra odds. Il rapporto tra odds comune e il corrispondente intervallo di confidenza del 95% saranno stimati a condizione che non vi sia alcuna prova di eterogeneità dell'effetto del trattamento tra gli strati. I principali endpoint secondari di sopravvivenza globale (OS) e il tempo prima del decesso per una qualsiasi causa, saranno calcolati usando la data di randomizzazione e la data del decesso o la data dell'ultimo follow-up per i soggetti che sono stati censurati (persi). Il tempo trascorso prima del decesso per una qualsiasi causa, è definito come il tempo che intercorre tra la randomizzazione e il decesso per qualsivoglia motivo. Tutti i soggetti saranno esaminati fino all'interruzione del trattamento, al decesso o alla conclusione dello studio. L'interruzione del trattamento può essere dovuta al ritiro del consenso per un ulteriore raccolta di dati o alla mancata presenza alle visite di follow-up. Per i soggetti che interrompono il trattamento o sono in vita al termine dello studio la sopravvivenza globale sarà censurata al momento dell'ultimo contatto, se opportuno. La sopravvivenza globale sarà testata con un livello di significatività generale di 0,05 (bilaterale). Per salvaguardare il livello alfa totale di 0,05 per l'analisi della sopravvivenza globale verrà impiegata una soglia sequenziale di gruppo di O Brien-Fleming. Le curve di sopravvivenza globale saranno valutate con il metodo Kaplan-Meier ed esaminate con un'analisi log-rank stratificata. Per stimare il corrispondente rapporto di rischio e gli intervalli di confidenza del 95% sarà utilizzato un modello di rischio proporzionale di Cox stratificato. L'endpoint secondario di risposta del numero di piastrine (HI-P) viene definito in base ai criteri IWG 2006 modificati. Le percentuali HI-P saranno confrontate tra i due gruppi di trattamento usando gli stessi metodi dell'endpoint primario. Per stimare le curve delle variabili secondarie relative al tempo aggiuntivo intercorso prima dell'evento si farà ricorso al metodo Kaplan-Meier. Tutte le altre variabili di efficacia secondarie saranno analizzate in modo descrittivo. Per descrivere le variabili secondarie di tipo categorico verranno usati conteggi e percentuali. Riservato ed esclusivo 16
17 Analisi di sicurezza: Tutte le analisi di sicurezza verrano effettuate sulla popolazione di sicurezza, che comprende tutti i soggetti randomizzati che hanno ricevuto almeno una dose del farmaco sperimentale. I soggetti saranno analizzati in base al trattamento effettivamente ricevuto. Gli eventi avversi verranno codificati mediante la terminologia medica per le attività regolatorie MedDRA (Medical Dictionary for Regulatory Activities). L'elenco degli eventi avversi comprenderà la classificazione letterale e il termine preferito MedDRA. Gli eventi avversi correlabili al trattamento (TEAE) saranno riassunti per grado di gravità, classificazione organo-sistemica e per termine preferito. I TEAE che determinano il decesso o l interruzione del trattamento, gli eventi classificati come CTCAE (versione 4.0) di grado 3 o 4, gli eventi avversi correlati al farmaco sperimentale e gli eventi avversi gravi (SAE) saranno riepilogati separatamente. Verrà generato anche l'elenco di tutti i decessi e di tutti i SAE, a prescindere dal momento in cui si sono verificati. La progressione a LAM e/o l insorgenza di un secondo tumore primario saranno documentati come SAE (che sarà considerato un evento medico importante anche se non si possono applicare altri criteri di gravità) per l'intera permanenza di un soggetto nello studio (dalla firma del modulo di consenso informato fino all'interruzione dello studio). I risultati delle analisi cliniche di laboratorio saranno riepilogati in modo descrittivo in base al gruppo di trattamento, evidenziando la variazione rispetto al basale. Saranno identificati i valori di laboratorio che esulano dai range di normalità. Saranno elencate e riepilogate le anomalie di laboratorio ematologiche e non ematologiche clinicamente significative e conformi ai criteri di grado 3 o grado 4 secondo CTCAE. A ogni visita per ciascun soggetto sarà eseguito un esame fisico e saranno misurati i segni vitali. Per ogni gruppo di trattamento saranno riassunti i dati statistici descrittivi dei segni vitali, in termini di valori rilevati e variazioni rispetto al basale. Analisi esplorativa: Saranno effettuate analisi correlative per valutare il rapporto tra l'esposizione e la farmacodinamica (sicurezza, efficacia) e altri endpoint esplorativi (biomarcatore). Saranno eseguite analisi appropriate di farmacocinetica/farmacodinamica della popolazione. I dati di farmacocinetica raccolti in questo studio saranno inoltre inseriti in un database più ampio per consentire l'ulteriore sviluppo e convalida del modello farmacocinetico della popolazione esposta all azacitidina e contribuire all'identificazione di covariate che potrebbero influenzare il comportamento farmacocinetico/farmacodinamico e l'attività clinica di azacitidina. Campioni di agoaspirato (o biopsia) del midollo osseo e campioni del sangue periferico saranno raccolti prima e dopo la fase di trattamento per l'analisi molecolare e/o cellulare. Le valutazioni, tra cui (ma non limitatamente a) la citogenetica, la metilazione del DNA/RNA, SNP, la sequenza di geni, l espressione del mrna, l espressione del mirna e l immunofenotipizzazione della presenza, di proporzioni e dello stato di attivazione delle popolazioni di cellule immunitarie potranno essere effettuate utilizzando il campione di midollo osseo prelevato al basale e i campioni di sangue periferico. I risultati ottenuti dalle caratterizzazioni molecolari e/o cellulari saranno valutati unitamente ai parametri del Riservato ed esclusivo 17
18 beneficio clinico, per stabilire se è possibile identificare biomarcatori predittivi di risposta o mancata risposta all'azacitidina orale. Le analisi saranno eseguite su soggetti di entrambi i gruppi di trattamento, per ottenere anche una distinzione tra la natura prognostica e/o predittiva del/i marcatore/i. Saranno inoltre analizzati i marcatori nei campioni di midollo osseo raccolti durante la fase di trattamento per fornire informazioni sul meccanismo di azione del farmaco sperimentale e i marcatori associati alla risposta o alla mancata risposta ad azacitidina orale. Non saranno effettuate analisi statistiche formali dei dati sui biomarcatori. Potranno essere analizzate, se appropriato, le possibili relazioni tra le variabili di farmacodinamica, sicurezza ed efficacia. Analisi ad interim: Un'analisi ad interim dell'endpoint di sopravvivenza globale sarà eseguita quando tutti i 386 soggetti avranno completato 12 mesi di trattamento in doppio cieco o interrotto lo studio prima di raggiungere i 12 mesi di trattamento in doppio cieco (100% delle informazioni per l endpoint primario), a seconda dell'evento che si verifica per primo. A quella data si sarà verificato all'incirca il 75% dei decessi totali previsti. Qualora sia effettuata un'analisi ad interim della sopravvivenza globale, verrà impiegata una soglia sequenziale di gruppo di O Brien-Fleming con funzione d uso alfa di Lan e DeMets per conservare il livello alfa generale a 0,05. Si prevede che i necessari livelli di significatività (bilaterale) siano pari a 0,019 al momento dell'analisi a interim e a 0,031 al momento dell'analisi finale per la sopravvivenza globale, ma i livelli effettivamente usati dipenderanno dal numero effettivo di eventi nell'analisi a interim e in quella finale. Un'analisi dell'endpoint primario sarà effettuata solo dopo che saranno disponibili tutte (100%) le informazioni sull incidenza di indipendenza dalle trasfusioni di globuli rossi (ad es. dopo che tutti i soggetti hanno completato 12 mesi di trattamento in doppio cieco o interrotto lo studio prima di raggiungere i 12 mesi di trattamento in doppio cieco). Se viene dimostrata la superiorità dell azacitidina per l'endpoint di efficacia primario al livello di significatività di 0,05 bilaterale, sarà effettuata anche l'analisi della sopravvivenza globale. L'analisi dell'endpoint della sopravvivenza globale può essere un'analisi ad interim oppure un'analisi finale, a seconda del grado di disponibilità dei dati sulla sopravvivenza (ad es. numero di decessi intercorsi) al momento dell'analisi finale per l'endpoint primario. L'analisi finale per la sopravvivenza globale sarà condotta dopo il verificarsi di 250 decessi. Comitato di monitoraggio dei dati Un Comitato indipendente di monitoraggio dei dati (DMC), multidisciplinare, valuterà prospetticamente la sicurezza nel corso dello studio. Il DMC sarà formato da oncologi/ematologi professionisti con esperienza nel trattamento della SMD e da un esperto in statistica, nessuno dei quali coinvolto nello studio come Sperimentatore. Un esperto in statistica, indipendente,creerà dei report critici sulla sicurezza che il DMC analizzerà periodicamente. Il Presidente del DMC potrà organizzare riunioni formali del DMC, se ci saranno problematiche legate alla sicurezza. Lo Sponsor può inoltre chiedere al DMC una revisione dei dati sulla sicurezza. Le responsabilità, l autorità e le procedure di DMC saranno Riservato ed esclusivo 18
19 registrate nel documento DMC, che sarà approvato e firmato dal DMC prima della prima riunione per la revisione dei dati. Analisi della patologia Un patologo indipendente revisionerà a livello centrale i vetrini di a aspirato midollare, la biopsia del midollo osseo e lo striscio di sangue periferico, nonché i risultati rilasciati dal laboratorio centrale prima della randomizzazione, per confermare la diagnosi della SMD e la classificazione WHO. Se il patologo responsabile della revisione centralizzata e il patologo locale saranno in disaccordo sulla diagnosi di un soggetto, la valutazione finale sarà effettuata da un terzo revisore. In casi di questo tipo la valutazione del terzo revisore sarà utilizzata per le analisi statistiche. L'esperto patologo indipendente responsabile della centralizzata valuterà anche i campioni di agoaspirati, le biopsie (se non è possibile ottenere un agoaspirato adeguato), gli strisci di sangue periferico e i risultati pertinenti del laboratorio centrale durante lo studio. Revisione citogenetica Un citogenetista indipendente i eseguirà le analisi citogenetiche nel corso dello studio. La revisione citogenetica centralizzata indipendente fornirà analisi e reporting standardizzati per tutti i soggetti. I risultati dell analisi citogenetica centralizzata indipendente saranno utilizzati per le analisi statistiche. Riservato ed esclusivo 19
20 Figura 1: Disegno generale dello studio Fase di screening (dal Giorno -56 al Giorno -1) SDM a più basso rischio IPSS Dipendenza da trasfusioni di globuli rossi ( 2 unità 1 di globuli rossi nell'arco di 28 giorni per 56 giorni 2 e nessun periodo di 28 giorni consecutivi senza una trasfusione RBC) Trombocitopenia (ad esempio, 2 conteggi delle piastrine 75 x 10 9 /L che sono distanti l una dall altra 21 giorni, con il secondo conteggio 14 giorni 2 prima della randomizzazione) Randomizzazione 3 e fase di trattamento in doppio cieco Randomizzazione 1:1 per trattamento in cieco (azacitidina orale o placebo) Azacitidina orale 300 mg QD Primi 21 giorni di ogni ciclo da 28 giorni Placebo Primi 21 giorni di ogni ciclo da 28 giorni Valutazione dello stato di malattia alla fine del Ciclo 6 Il soggetto ha manifestato quanto segue? Indipendenza da trasfusioni di globuli rossi Oppure indipendenza da trasfusioni di piastrine per i soggetti dipendenti dalle trasfusioni di piastrine al basale Oppure miglioramento ematologico (Cheson, 2006; Appendice D) Oppure 50% di riduzione del fabbisogno medio di trasfusioni di globuli rossi valutate nei 56 giorni (8 settimane) immediatamente precedente la valutazione dello stato della malattia comparato al fabbisogno medio di trasfusioni di globuli rossi al basale. Oppure ogni beneficio clinico, inclusa la non evidenza di progressione di malattia (vedere la sezione 12 del protocollo per le definizioni di progressione di malattia) SÌ Continuare la terapia prevista dal protocollo fino alla progressione della malattia o all'interruzione del trattamento 4 per un qualsiasi altro motivo, quindi ingresso nella Fase di follow-up NO Interrompere 4 la terapia prevista dal protocollo e entrare nella fase di follow-up Fase di follow-up Follow-up per valutazione della sopravvivenza, successive terapie per SMD, progressione a LAM e secondo tumore maligno primario. 1 In accordo alla prassi medica in Giappone, 1 unità di globuli rossi indicata nel protocollo equivale a 2 unità di globuli rossi in Giappone. Riservato ed esclusivo 20
21 2 Immediatamente prima e in concomitanza della data di randomizzazione (vedere Sezione 7.2 per dettagli). 3 Fattori di stratificazione: fabbisogno medio di trasfusioni di globuli rossi al basale ( 4 unità 1 versus > 4 unità di di globuli rossi nell'arco di 28 giorni), stato trasfusioni di piastrine al basale (dipendente versus indipendente), paese di arruolamento (ad es. Giappone versus Resto del mondo) e stato di performance ECOG (da 0 a 1 versus 2). 4 La decisione di ritirare un soggetto, che non sarà ritardata o rifiutata dallo sponsor, resta di responsabilità del medico curante. Tuttavia, prima di ritirare un soggetto, lo Sperimentatore può contattare il Medical Monitor dello studio e inoltrare l'adeguata documentazione di supporto per la revisione e la discussione del caso. Riservato ed esclusivo 21
22 Tabella degli eventi La tabella 1 fornisce una descrizione dettagliata di tutti gli eventi o le procedure dello studio per ogni ciclo di trattamento di 28 giorni. Tabella 1: Tabella degli eventi Procedura Screening 56 giorni prima della randomizzazione Randomizzazione b Fase di trattamento in doppio cieco a Cicli 1 2 Cicli 3 12 Giorno 1 b Giorni 8, 15, 22 Giorno 1 Ciclo 13 e successivi Giorno 15 Giorno 1 Fine del trattamento c Followup a Consenso Informato Criteri di inclusione ed esclusione Diagnosi di SMD, classificazione WHO e punteggio IPSS Cronologia delle trasfusioni di globuli rossi e di piastrine d e Storia della trombocitopenia f Storia medica e dati demografici Precedente trattamento per SMD (e altro tumore maligno, se applicabile) g Farmaci assunti precedentemente h Esame fisico -- i Segni vitali (pressione sanguigna, battito cardiaco, temperatura, frequenza respiratoria) Misurazione peso corporeo Altezza Performance Status ECOG -- i ECG Locale j Analisi delle urine k Riservato ed esclusivo 22
23 Tabella 1: Tabella degli eventi (continua) Procedura Screening 56 giorni prima della randomizzazione Randomizzazione b Fase di trattamento in doppio cieco a Cicli 1 2 Cicli 3 12 Giorno 1 b Giorni 8, 15, 22 Giorno 1 Ciclo 13 e successivi Giorno 15 Giorno 1 Riservato ed esclusivo 23 Interruzione del trattamento c Coagulazione l Test di Coombs (diretto/indiretto) - Locale m Conta dei reticolociti Locale n Livello di EPO nel siero o o Ferritina nel siero p Saturazione della transferrina nel siero (Fe/TIBC) Ematologia q -- i -- Chimica nel siero r -- i Test di gravidanza (solo FCBP) s Valutazione eventi avversi Monitoraggio della progressione a LAM e secondo tumore maligno primario Followup a Dopo la firma del consenso informato e fino a 28 giorni dopo l assunzione delll'ultima dose di farmaco sperimentale o all'ultima visita dello studio, a seconda dell'evento che si protrae più a lungo. Dopo la firma del consenso informato o fino a decesso, perdita al follow-up, ritiro del consenso all'ulteriore raccolta di dati o conclusione dello studio. Terapie concomitanti, terapia e procedure -- Dalla data della randomizzazione e fino a 28 giorni dopo l'ultima dose di farmaco sperimentale o fino all'ultima visita dello studio, a seconda dell'evento che si protrae più a lungo Agoaspirato e/o biopsia del midollo osseo (biopsia obbligatoria allo screening) Striscio del sangue periferico Test di citogenetica d t -- t Biomarcatore - midollo osseo u t, v -- t, v Biomarcatore - sangue periferico u t, v v, w t, v -- --
24 Tabella 1: Tabella degli eventi (continua) Procedura Screening 56 giorni prima della randomizzazione Randomizzazione b Fase di trattamento in doppio cieco a Cicli 1 2 Cicli 3 12 Giorno 1 b Giorni 8, 15, 22 Giorno 1 Ciclo 13 e successivi Giorno 15 Giorno 1 Interruzione del trattamento c Followup a Biomarcatore - cellule buccali u FACT-An e EQ-5D x Utilizzo di risorse mediche Dopo la firma del consenso informato e fino a 28 giorni dopo l assunzione dell'ultima dose di farmaco sperimentale o all'ultima visita dello studio, a seconda dell'evento che si protrae più a lungo. Randomizzazione Consegna del farmaco sperimentale y Somministrazione del farmaco sperimentale Dal Giorno 1 al Giorno 21 dei cicli di trattamento di 28 giorni z Contabilità del farmaco sperimentale aa Farmacocinetica - sangue periferico u, bb -- u, bb Valutazione trasfusioni cc Dopo la data della randomizzazione e fino a 28 giorni dopo l assunzione dell'ultima dose di farmaco sperimentale o fino all'ultima visita dello studio, a seconda dell'evento che si protrae più a lungo Valutazione degli eventi di sanguinamento dd Risposta/Miglioramento IWG ee t -- t Valutazione dello stato di malattia ff -- ff -- Successive terapie per SMD gg Sopravvivenza al follow-up gg Riservato ed esclusivo 24
25 Legenda: LAM =leucemia mieloide acuta; ECG=elettrocardiogramma; ECOG=Eastern Cooperative Oncology Group (organizzazione di ricerca clinica sul cancro degli Stati Uniti); EPO=eritropoietina; EQ-5D=EuroQol Group EQ-5D-3L; FACT-An=valutazione funzionale dell'anemia dovuta a terapia anticancro; FCBP=donna potenzialmente fertile; ICD=modulo di consenso informato; IPSS=International Prognostic Scoring System (sistema di punteggio prognostico internazionale); IWG = International Working Group (gruppo di lavoro internazionale); SMD =sindromi mielodisplastiche; RBC=globuli rossi; WHO=World Health Organization (Organizzazione Mondiale della Sanità). a. La finestra per le visite dello studio per le valutazioni associate alla visita nella fase di trattamento in doppio cieco è ± 3 giorni per i Cicli 1 e 2; ± 7 giorni per il Ciclo 3 e oltre, tranne se diversamente indicato per una particolare valutazione. Tuttavia, tenere presente che in tutte le circostanze, deve essere osservata una sospensione del farmaco di 7 giorni per i regimi di trattamento di 300 mg e 200 mg per 21 giorni/ciclo di 28 giorni (rispettivamente 14 e 21 giorni, per i regimi di trattamento modificati di 200 mg per 14 giorni/ciclo di 28 giorni e 7 giorni/ciclo di 28 giorni). Le visite dello studio devono valutare anche la fornitura di farmaco sperimentale al soggetto. Il Giorno 1 di ciascun ciclo al soggetto sarà fornito soltanto 1 ciclo di farmaco sperimentale. Il Giorno 1 dei Cicli da 2 in poi può essere ritardato rispetto al Giorno 28 del ciclo precedente per consentire ai soggetti di guarire da eventuali tossicità e soddisfare i criteri per la ripresa del trattamento. Durante il follow-up la finestra per le visite dello studio è ± 7 giorni per visite con cadenza mensile (compresa la visita di followup 28 giorni dopo l'ultima dose, se necessario) o ± 14 giorni per visite con cadenza trimestrale. Un ciclo (un mese) corrisponde a 28 giorni (cioè 4 settimane). b. La prima dose di farmaco sperimentale del Ciclo 1 deve essere somministrata entro 3 giorni dalla randomizzazione e la somministrazione può avvenire lo stesso giorno della randomizzazione. c. Tutti i soggetti che hanno ricevuto almeno una dose di farmaco sperimentale devono eseguire la visita di fine trattamento quando la terapia sarà interrotta. Il motivo dell'interruzione sarà registrato nella CFR e nella cartella clinica per tutti i soggetti randomizzati, a prescindere dalla somministrazione o meno del dosaggio. I motivi per interrompere il trattamento possono includere la progressione della malattia, eventi avversi, ritiro del consenso, decesso, mancata presenza alle visite di follow-up o violazione del protocollo. d. Diagnosi di SMD, classificazione WHO (Appendice A) e classificazione di rischio IPSS (Appendice B) saranno confermate attraverso l analisi patologica e citogenetica centralizzata e dall analisi dei risultati del laboratorio centralizzato pertinente. I campioni di midollo osseo e della biopsia unitamente ai campioni di sangue periferico, devono essere raccolti allo screening così come indicato nella sezione In tutti i momenti successivi, si rende necessaria una biopsia solo se non è possibile ottenere un aspirato adeguato. I campioni di sangue dello screening devono essere raccolti lo stesso giorno in cui viene eseguito l'agoaspirato/biopsia di midollo osseo. Le istruzioni per la preparazione di vetrini di midollo osseo, la raccolta di campioni, l'elaborazione, la conservazione e le procedure di spedizione sono fornite nel Manuale del Laboratorio Centrale dello studio. e. La cronologia delle trasfusioni di globuli rossi deve essere disponibile per gli 56 giorni immediatamente precedenti la data di randomizzazione (inclusa) e la cronologia delle trasfusioni di piastrine deve essere disponibile per i 56 giorni immediatamente precedenti la data di randomizzazione (inclusa). I dati sulla cronologia delle trasfusioni possono essere raccolti durante il periodo di screening di 56 giorni, come indicato in dettaglio nei criteri di inclusione. f. La trombocitopenia al basale deve essere confermata dalla valutazione di due conte piastriniche 75 x 10 9 /l eseguite a 21 giorni di distanza. La seconda conta piastrinica deve essere effettuata 14 giorni prima della randomizzazione. Almeno una conta piastrinica deve essere analizzata a livello centrale nel periodo di screening di 56 giorni con risultati 75 x 10 9 /l; la seconda conta piastrinica può essere analizzata a livello centrale o locale con risultati anch essi 75 x 10 9 /l. Se durante il periodo a interim vengono eseguite delle conte piastriniche aggiuntive, anche queste devono avere un valore 75 x 10 9 /l. Se le conte piastriniche nel periodo a interim sono 75 x 10 9 /l, ciò sarebbe accettabile solo se associate a una trasfusione di piastrine somministrata nei 7 giorni precedenti la data della conta piastrinica (Sezione 6.1.3). g. Il precedente trattamento per la SMD comprende tutti i precedenti trattamenti per la SMD a prescindere da una loro eventuale interruzione, come riportato in dettaglio nella Sezione Riservato ed esclusivo 25
26 h. Tutti i farmaci assunti nelle 8 settimane (56 giorni) precedenti la randomizzazione devono essere registrati nell'apposita scheda di raccolta dati (CRF). i. j. La valutazione non deve essere effettuata se l'esame di screening statovene effettuato entro 7 giorni dall assunzione della prima dose di farmaco sperimentale nella fase di trattamento. L'elettrocardiogramma verrà effettuato localmente allo screening e quando clinicamente indicato. Lo Sperimentatore riesaminerà e valuterà i risultati come normali, anomali - non clinicamente significativi, o anomali - clinicamente significativi e registrerà il/i valore/i anomalo/i nell'apposita CFR. Se l'ecg presenta anomalie, lo Sperimentatore dovrebbe consultare un cardiologo se opportuno. k. Le analisi delle urine vengono effettuate presso il laboratorio centralizzato allo screening e quando clinicamente indicato. l. La coagulazione viene esaminata presso il laboratorio centralizzato allo screening e quando clinicamente indicato. m. Un test di Coombs diretto o indiretto allo screening viene effettuato presso il laboratorio locale. n. La conta dei reticolociti allo screening viene eseguita presso il laboratorio locale. o. Idealmente il livello di EPO nel siero (sezione ) dovrebbe essere misurato allo screening nello stesso giorno in cui è prevista la trasfusione di globuli rossi, e non dovrebbe essere raccolto entro la settimana successiva a una trasfusione di globuli rossi a causa della possibile riduzione del livello di siero correlata al livello di emoglobina ottenuto dopo l ultima trasfusione. Il test del livello di EPO nel siero deve essere effettuato inoltre nel Giorno 1 del Ciclo 6. Tuttavia, se possibile, il campione non deve essere raccolto entro 1 settimana successiva a una trasfusione di globuli rossi a causa della possibile riduzione del livello di siero correlata al livello di emoglobina ottenuto dopo l ultima trasfusione. Quindi, nel caso in cui il Giorno 1 del Ciclo 6 sia programmato entro una settimana da una trasfusione di globuli rossi, il prelievo di EPO potrebbe essere eseguito nel Giorno 1 del ciclo successivo (Sezione 6.7.7). Il test del livello di EPO nel siero viene eseguito presso il laboratorio centrale. p. Il livello di ferritina nel siero deve essere misurato allo screening il Giorno 1 del Ciclo 1, il Giorno 1 di ogni 3 cicli successivi (cioè Giorno 1 dei Cicli 4, 7, 10, 13, ecc.) e alla visita di fine trattamento. Il test del livello di ferritina nel siero viene effettuato dal laboratorio centralizzata. q. La valutazione ematologica comprende una conta ematica completa (Conta ematologia completa, globuli rossi, emoglobina, ematocrito, volume corpuscolare medio [MCV], media corpuscolare di emoglobina [MCH], media corpuscolare media della concentrazione di emoglobina [MCHC], ampiezza di distribuzione dei globuli rossi [RDW], conta globuli bianchi con differenziale, conta assoluta dei neutrofili [ANC] e conta piastrinica. I campioni ematologici saranno raccolti allo Screening e prima della somministrazione del farmaco sperimentale. La frequenza della valutazione ematologica nella fase di trattamento è: settimanale nei Giorni 1, 8, 15 e 22 nei Cicli 1-2, bisettimanale i Giorni 1 e 15 dei Cicli 3-12 e mensile il Giorno 1 dei cicli successivi e alla visita di fine trattamento. Una o tutte le valutazioni di laboratorio possono essere ripetute con maggiore frequenza se clinicamente indicato. Tutti i campioni saranno analizzati dal laboratorio centralizzato. r. I parametri clinici del siero includono sodio, potassio, cloruro, bicarbonato (se disponibile), calcio, magnesio, fosforo, azoto ureico nel sangue (BUN), creatinina, glucosio, albumina, proteine totali, fosfatasi alcalina, bilirubina diretta/indiretta/totale, aspartato aminotransferasi (AST)/transaminasi glutammicoossalacetica (SGOT) o alanino-transaminasi (ALT)/transaminasi glutammico-piruvica (SGPT), lattato deidrogenasi (LDH) e acido urico. Tutti i campioni saranno analizzati dal laboratorio centralizzato. Una o tutte le valutazioni di laboratorio possono essere ripetute con maggiore frequenza se clinicamente indicato. I campioni devono essere raccolti allo screening e prima della somministrazione del farmaco sperimentale. La frequenza della valutazione dei valori chimici nel siero nella fase di trattamento è: settimanale nei Cicli 1-2 e mensile il Giorno 1 dei cicli successivi e alla visita di fine trattamento. Riservato ed esclusivo 26
27 s. Per i soggetti di sesso femminile potenzialmente fertili, (FCBP, fare riferimento alla sezione per la definizione di FCBP) occorre eseguire un test di gravidanza sul siero con supervisione medica (eseguito presso il laboratorio centrale o a livello locale) verificato come negativo allo screening (Sezione ). Durante la fase di trattamento, un test di gravidanza sulle urine o sul siero (a discrezione dello Sperimentatore), con sensibilità di almeno 25mIU/ml, deve essere eseguito nelle 72 ore precedenti al Giorno 1 di ogni ciclo e alla visita di fine trattamento (sezione 6.6.7). Ricordiamo che il test di gravidanza allo screening ha valore di test valido prima dell'inizio della terapia sperimentale nella fase di trattamento se effettuato entro un intervallo di 72 ore. Il soggetto non potrà ricevere il farmaco sperimentale prima che lo Sperimentatore abbia verificato l'esito negativo del test di gravidanza. t. Giorno 1 dei Cicli 3, 6 e 12 e successivamente ogni 6 mesi (cioè Giorno 1 dei Cicli 18, 24, ecc.). Vedere Sezione 6.7.3, Sezione e Sezione del protocollo per i dettagli. u. Raccolta di campioni di biomarcatori obbligatoria. I soggetti devono acconsentire alla raccolta di questi campioni firmando il consenso informato nella sezione relativa alla raccolta obbligatoria di campioni. v. Raccolta di campioni di biomarcatori opzionale. I campioni saranno raccolti ai soggetti che hanno acconsentito alla raccolta di questi campioni firmando il consenso informato, nella sezione relativa alla raccolta opzionale di campioni. w. Biomarcatori - Prelievo di sangue periferico: Giorno 15 (± 7 giorni) dei Cicli 3, 6 e 12 (Sezione ). x. I questionari FACT-An e EQ-5D devono essere compilati prima dell'interazione con il personale dello studio e prima della somministrazione del farmaco sperimentale, all inizio di ogni Ciclo e all'interruzione del trattamento (Sezione 6.8). Se il sangue viene prelevato prima del Giorno 1 di un particolare ciclo o prima della visita di interruzione del trattamento, i questionari saranno comunque completati alla prima visita con il personale del centro in tale specifico ciclo o visita di interruzione del trattamento. y. Il farmaco sperimentale deve essere dispensato solo il Giorno 1 di ciascun ciclo di trattamento dopo che tutte le procedure del Giorno 1 sono state completate e l'intero quantitativo di farmaco sperimentale del ciclo precedente è stato contabilizzato (se applicabile). Il Giorno 1 di ciascun ciclo al soggetto sarà fornito soltanto 1 ciclo di farmaco sperimentale. (Sezione 8.2.1). z. L'assunzione del farmaco sperimentale è prevista dal Giorno 1 al Giorno 21 di ciascun ciclo, tranne in caso di variazione del piano di somministrazione a causa di tossicità. Nei giorni di raccolta di campioni per la farmacocinetica (PK) il prodotto sperimentale sarà somministrato dal personale del centro sperimentale presso l ospedale. I soggetti si autosomministreranno tutte le altre dosi di farmaco sperimentale. Il farmaco antiemetico (non fornito dallo sponsor) può essere somministrato 30 minuti prima del farmaco sperimentale a discrezione dello sperimentatore (Sezione 8.2.2). aa. Solo Giorno 1 del Ciclo 2. bb. Due campioni di sangue (3 ml/campione) per la valutazione farmacocinetica di azacitidina saranno raccolti ad almeno 2 ore di distanza il Giorno 1 dei Cicli 1, 3 e 6 tra 0,5 e 6 ore dopo la somministrazione del farmaco sperimentale. Nel corso dello studio saranno raccolti un massimo di 6 campioni per soggetto. I campioni di sangue devono essere trattati e il plasma deve essere raccolto e conservato secondo quanto descritto nel Manuale del laboratorio centralizzato dello studio. cc. I dati relativi a tipo, numero di unità, motivo e data delle trasfusioni devono essere raccolti dopo la randomizzazione e fino a 28 giorni dopo l'ultima dose di farmaco sperimentale o fino alla visita di fine studio, a seconda dell'evento che si verifica per ultimo. Il valore di emoglobina legato alla trasfusioni di globuli rossi e il valore delle piastrine legato alle relative trasfusioni devono essere a loro volta registrati nella CRF. Le trasfusioni di globuli rossi e/o di piastrine somministrate per interventi di chirurgia elettiva non devono essere considerate per determinare il fabbisogno basale, la valutazione di efficacia e lo stato di progressione della malattia. Riservato ed esclusivo 27
28 dd. La valutazione di tutti gli eventi di sanguinamento deve essere effettuata durante la fase di trattamento a partire dal Giorno 1 del Ciclo 1, come indicato in dettaglio nella Sezione e alla visita di fine trattamento. Le informazioni per ogni evento di sanguinamento devono essere registrate nell adeguata pagina di CRF. ee. La risposta dell'international Working Group/valutazione del miglioramento si esegue il Giorno 1 dei Cicli 3, 6 e 12 e successivamente ogni 6 cicli (cioè Giorno 1 dei Cicli 18, 24, ecc.) e potrebbe essere effettuata in qualsiasi momento prima dell'inizio del ciclo successivo (cioè rispettivamente prima dell'inizio dei Cicli 4, 7, 13 ecc.) (Sezione 6.7.5). ff. Una valutazione dello stato della malattia deve essere effettuata alla fine del Ciclo 6, prima dell'inizio del Ciclo 7. Se i soggetti rispecchiano uno dei seguenti, possono continuare con il Ciclo 7 e oltre e lo stato della malattia sarà valutato alla fine di ciascun ciclo. indipendenza dalle trasfusioni di globuli rossi o indipendenza dalle trasfusioni di piastrine per quei soggetti che sono dipendenti dalle trasfusioni di piastrine al basale o miglioramento ematologico (HI; Cheson et al., Blood, 2006) o riduzione 50% del fabbisogno medio di trasfusioni di globuli rossi nei 56 giorni (8 settimane) immediatamente precedente alla valutazione dello stato della malattia rispetto mediala fabbisogno medio di trasfusioni di globuli rossi al basale o qualsiasi altro beneficio clinico, compresa l'assenza di evidenza di progressione della malattia (vedere Appendice A per le definizioni di malattia in progressione). Successivamente per i soggetti può essere interrotta la terapia in studio per uno qualsiasi dei motivi riportati in dettaglio nella sezione 12. Se i soggetti non soddisfano qualunque dei precedenti criteri alla fine del Ciclo 6, la terapia in studio sarà interrotta. La decisione di ritirare un soggetto, che non sarà ritardata o rifiutata dallo sponsor, resta di responsabilità del medico curante. Tuttavia, prima di ritirare un soggetto, lo Sperimentatore può contattare il Medical Monitor dello studio e inoltrare l'adeguata documentazione per la revisione e discussione del caso. gg. Tutti i soggetti per i quali è stata interrotta la terapia prescritta in studio per un motivo qualsiasi devono essere esaminati per valutare la sopravvivenza e le successive terapie per la SMD. Riservato ed esclusivo 28
29 Appendice A: Definizioni di progressione di malattia per la decisione clinica sull'interruzione del trattamento con il farmaco sperimentale e/o dello studio per i soggetti Categoria Criteri di progressione/ricaduta 4 Progressione nel midollo osseo Per soggetti con: Meno del 5% di blasti al basale: aumento di blasti da > 50% a > 5% 5%-10% blasti al basale: aumento di blasti da 50% a > 10% Nota: Un 2 campione di midollo osseo dovrebbe essere prelevato entro 4 settimane per confermare la progressione di malattia prima di interrompere il trattamento per il soggetto. Progressione in base al fabbisogno di trasfusioni di globuli rossi Ricaduta in base al fabbisogno di trasfusioni di globuli rossi Per soggetti dipendenti dalle trasfusioni di globuli rossi al basale: Chi non raggiunge un'indipendenza dalle trasfusioni di globuli rossi per un periodo a 84 giorni (12 settimane) durante il trattamento sperimentale, un incremento > 50% del fabbisogno medio di trasfusioni di globuli rossi durante un qualsiasi periodo negli 84 giorni (12 settimane) durante il trattamento sperimentale rispetto al fabbisogno medio di trasfusioni di globuli rossi negli 84 giorni (12 settimane) precedenti la randomizzazione. Per soggetti dipendenti da trasfusioni di globuli rossi al basale: Chi raggiunge una indipendenza dalle trasfusioni di globuli rossi per un periodo a 84 giorni (12 settimane) durante il trattamento sperimentale, una ricaduta allo stato di dipendenza da trasfusioni RBC. Per ricaduta si intende il ritorno al fabbisogno basale di trasfusioni di globuli rossi. Per soggetti dipendenti da trasfusioni di piastrine al basale: Progressione in base al fabbisogno di trasfusioni di piastrine Chi non raggiunge l'indipendenza dalle trasfusioni di piastrine per un periodo a 56 giorni (8 settimane) durante il trattamento sperimentale, un aumento > 50% nel fabbisogno di trasfusione di piastrine durante un qualsiasi periodo di 56 giorni (8 settimane) durante il trattamento sperimentale rispetto al periodo di 56 giorni (8 settimane) prima della randomizzazione. Per soggetti non dipendenti dalle trasfusioni di piastrine al basale: Sviluppo della dipendenza dalle trasfusioni di piastrine, cioè 2 trasfusioni di piastrine in un qualsiasi periodo di 56 giorni (8 settimane) durante il trattamento sperimentale. Ricaduta in base al fabbisogno di trasfusioni di piastrine Per soggetti dipendenti da trasfusioni di piastrine al basale: Chi raggiunge una indipendenza dalle trasfusioni di piastrine 56 giorni (8 settimane) durante il trattamento sperimentale, una ricaduta allo stato di dipendenza da trasfusioni di piastrine. Per ricaduta si intende il ritorno al fabbisogno basale di trasfusioni di piastrine. 4 Le trasfusioni di globuli rossi e/o di piastrine somministrate per interventi di chirurgia elettiva non devono essere considerate per determinare lo stato di progressione della malattia o ricaduta. Riservato ed esclusivo 29
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
Possibilità terapeutiche attuali nelle sindromi mielodisplastiche
 Possibilità terapeutiche attuali nelle sindromi mielodisplastiche Luca Malcovati, Professore Associato di Ematologia, Dipartimento di Ematologia e Oncologia, Fondazione IRCCS Policlinico San Matteo & Dipartimento
Possibilità terapeutiche attuali nelle sindromi mielodisplastiche Luca Malcovati, Professore Associato di Ematologia, Dipartimento di Ematologia e Oncologia, Fondazione IRCCS Policlinico San Matteo & Dipartimento
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI
 ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
ALLEGATO CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE DEL FARMACO CHE DEVONO ESSERE IMPLEMENTATE DAGLI STATI MEMBRI CONDIZIONI O RESTRIZIONI RELATIVE ALL UTILIZZO SICURO ED EFFICACE
RICHIESTA DI PARERE SU SPERIMENTAZIONE CLINICA DI DISPOSITIVO MEDICO
 COMITATO ETICO INTERAZIENDALE (istituito con Delibera n. 236 del 10/09/13 e successiva Delibera n. 267 del 25/10/13 ed iscritto al Registro Regionale al n. 2) Sede: Via Venezia n.16, 15121 tel.0131206974-6651
COMITATO ETICO INTERAZIENDALE (istituito con Delibera n. 236 del 10/09/13 e successiva Delibera n. 267 del 25/10/13 ed iscritto al Registro Regionale al n. 2) Sede: Via Venezia n.16, 15121 tel.0131206974-6651
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO
 Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
ZACTIMA è un marchio commerciale del gruppo di società AstraZeneca.
 Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
Sindromi Mieloproliferative
 Sindromi Mieloproliferative Sindr. Mieloproliferative croniche Sindr. Mieloprolifer. Sub-acute o Mielodisplasie Sindr. Mieloproliferative Acute o Leucemie Acute Mieloidi SINDROME MIELODISPLASTICA Patologia
Sindromi Mieloproliferative Sindr. Mieloproliferative croniche Sindr. Mieloprolifer. Sub-acute o Mielodisplasie Sindr. Mieloproliferative Acute o Leucemie Acute Mieloidi SINDROME MIELODISPLASTICA Patologia
COMITATO ETICO Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione clinica
 COMITATO ETICO In data 05-05-2014 il Comitato Etico ha approvato la stesura definitiva del Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione
COMITATO ETICO In data 05-05-2014 il Comitato Etico ha approvato la stesura definitiva del Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione
SINOSSI. EudraCT number Versione del protocollo Version Octobre 2013
 SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
(CRICKET) - EUDRACT Gruppo Oncologico Nord-Ovest (G.O.N.O.)
 APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
II GOIM Prof. Giuseppe Colucci Direttore Dipartimento Oncologia Medica Istituto Tumori G.PaoloII, Bari
 1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
La gestione degli eventi avversi e dei SAE
 Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
Oncology Business Unit - GMO La gestione degli eventi avversi e dei SAE Francesca Bamonte, GMO Study Manager Negrar 21 Ottobre 2016 Definizione di evento avverso (AE) Qualsiasi episodio sfavorevole di
STUDI CLINICI IN CORSO nella MIELOFIBROSI
 Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
Written by Tuesday, 12 August :26 - Last Updated Sunday, 21 November :45
 Anemia Aplastica acquisita Rara malattia ematologia, non oncologica Sua caratteristica è una netta riduzione di globuli bianchi, rossi e piastrine nel sangue (pancitopenia periferica) a volte gravissima
Anemia Aplastica acquisita Rara malattia ematologia, non oncologica Sua caratteristica è una netta riduzione di globuli bianchi, rossi e piastrine nel sangue (pancitopenia periferica) a volte gravissima
Schema dello studio clinico di Fase 2b
 Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
Sommario dei risultati dello studio clinico di Fase 2b di Ataluren presentato in occasione dell American Academy of Neurology Meeting il 16 Aprile 2010 Toronto, 16 Aprile 2010 - Un nuovo farmaco sperimentale
Trapianto. Stefano Guidi TMO. AOU Careggi. Firenze. Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche
 Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Aprile 2016 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Trapianto
Sesta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Aprile 2016 CRIMM Centro di Ricerca e Innovazione per le Malattie Mieloproliferative AOU Careggi Trapianto
SINTESI DEI RISULTATI
 Nell 22 in provincia di Modena sono stati diagnosticati 4138 nuovi casi di tumore, 2335 tra gli uomini e 183 tra le donne. Sempre nello stesso periodo sono deceduti per tumore 1159 uomini e 811 donne.
Nell 22 in provincia di Modena sono stati diagnosticati 4138 nuovi casi di tumore, 2335 tra gli uomini e 183 tra le donne. Sempre nello stesso periodo sono deceduti per tumore 1159 uomini e 811 donne.
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI
 PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
LEUCEMIE MIELOIDI CRONICHE
 LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
LEUCEMIE MIELOIDI CRONICHE La Leucemia Mieloide Cronica (LMC) è una malattia neoplastica relativamente rara (1-2 casi/100.000 abitanti/anno) prevalente nell adulto-anziano. Le cellule leucemiche sono caratterizzate
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs
 Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Approssimativamente 20 sperimentatori (oncologi o pneumologi). Approssimativamente 20 centri in tutto il mondo.
 SINOSSI Nome dello sponsor/azienda: Eisai Inc. Riservato alle Autorità Titolo dello studio: N. di protocollo: Sperimentatori: Centri dello studio: Studio in aperto, multicentrico, randomizzato, di fase
SINOSSI Nome dello sponsor/azienda: Eisai Inc. Riservato alle Autorità Titolo dello studio: N. di protocollo: Sperimentatori: Centri dello studio: Studio in aperto, multicentrico, randomizzato, di fase
Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali
 Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
Allegato II Modifica del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo presentata dall'agenzia Europea per i Medicinali Il Riassunto delle Caratteristiche del Prodotto e il foglio
Sinossi Protocollo Sperimentale GOIM 21002
 1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
Prevalenza microangiopatie trombotiche nel Policlinico Gemelli: un approccio informatico. Gianmarco Lombardi, Giovanni Gambaro UOC Nefrologia
 Prevalenza microangiopatie trombotiche nel Policlinico Gemelli: un approccio informatico Gianmarco Lombardi, Giovanni Gambaro UOC Nefrologia I set di criteri considerati, variamente combinati tra loro,
Prevalenza microangiopatie trombotiche nel Policlinico Gemelli: un approccio informatico Gianmarco Lombardi, Giovanni Gambaro UOC Nefrologia I set di criteri considerati, variamente combinati tra loro,
Terapia Medica Malattie del sangue Anemie
 Inquadramento della anemia Definire: Causa Grado Rapidità di comparsa (acuta e cronica) Parametri fondamentali: Hb Hct (ematocrito) VCM (volume corpuscolare medio) Reticolociti Esame dello striscio periferico
Inquadramento della anemia Definire: Causa Grado Rapidità di comparsa (acuta e cronica) Parametri fondamentali: Hb Hct (ematocrito) VCM (volume corpuscolare medio) Reticolociti Esame dello striscio periferico
U.O. UTIC Chiara Valbusa NUOVO APPROCCIO ALLA GESTIONE DEL PAZIENTE IN TERAPIA ANTICOAGULANTE ORALE: L INFERMIERE NAO
 NUOVO APPROCCIO ALLA GESTIONE DEL PAZIENTE IN TERAPIA ANTICOAGULANTE ORALE: L INFERMIERE NAO La fibrillazione atriale (FA) è l aritmia cardiaca più comune nella popolazione, con una prevalenza del 5,5%,
NUOVO APPROCCIO ALLA GESTIONE DEL PAZIENTE IN TERAPIA ANTICOAGULANTE ORALE: L INFERMIERE NAO La fibrillazione atriale (FA) è l aritmia cardiaca più comune nella popolazione, con una prevalenza del 5,5%,
LETTURA CRITICA DELLA LETTERATURA SCIENTIFICA
 LA STATISTICA NELLA RICERCA Raccolta dei dati Elaborazione Descrizione Una raccolta di dati non corretta, una loro presentazione inadeguata o un analisi statistica non appropriata rendono impossibile la
LA STATISTICA NELLA RICERCA Raccolta dei dati Elaborazione Descrizione Una raccolta di dati non corretta, una loro presentazione inadeguata o un analisi statistica non appropriata rendono impossibile la
SINOSSI. Istituto Clinico Humanitas - Humanitas Cancer Center Dr.ssa Monica Balzarotti. Versione 2.0 / 11 Novembre 2013
 SINOSSI Title Investigator Sponsor Coordinatore dello studio Numero identificativo Versione del protocollo Razionale Fase Popolazione in studio e selezione dei pazienti Ofatumumab-Bendamustina nei linfomi
SINOSSI Title Investigator Sponsor Coordinatore dello studio Numero identificativo Versione del protocollo Razionale Fase Popolazione in studio e selezione dei pazienti Ofatumumab-Bendamustina nei linfomi
STUDY ID: FIL_RENOIR12 EUDRACT NUMBER
 Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
SINOSSI. Titolo. Coordinatori e Promotori dello studio
 SINOSSI Titolo PLERIXAFOR (PLX) IN MODALITA ON DEMAND PER LA RACCOLTA DI CELLULE STAMINALI EMOPOIETICHE AUTOLOGHE IN PAZIENTI AFFETTI DA MIELOMA MULTIPLO DA LINFOMA CHE MOSTRINO POVERA MOBILIZZAZIONE DOPO
SINOSSI Titolo PLERIXAFOR (PLX) IN MODALITA ON DEMAND PER LA RACCOLTA DI CELLULE STAMINALI EMOPOIETICHE AUTOLOGHE IN PAZIENTI AFFETTI DA MIELOMA MULTIPLO DA LINFOMA CHE MOSTRINO POVERA MOBILIZZAZIONE DOPO
INTERRUZIONE VOLONTARIA DI GRAVIDANZA CON METODICA FARMACOLOGICA (RU 486)
 INTERRUZIONE VOLONTARIA DI GRAVIDANZA CON METODICA FARMACOLOGICA (RU 486) Dottor Roberto Gherzi II Divisione ginecologia ostetricia Azienda Ospedaliero Universitaria Maggiore della Carità Novara L interruzione
INTERRUZIONE VOLONTARIA DI GRAVIDANZA CON METODICA FARMACOLOGICA (RU 486) Dottor Roberto Gherzi II Divisione ginecologia ostetricia Azienda Ospedaliero Universitaria Maggiore della Carità Novara L interruzione
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Versione PROTOCOLLO DI STUDIO
 Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Parte I - LINEE GUIDA. (Centro Nazionale Trapianti - 1 marzo 2005) PRINCIPI GENERALI. Razionale
 Parte I - LINEE GUIDA PROTOCOLLO PER L UTILIZZO DI DONATORI POSITIVI PER GLI ANTICORPI DIRETTI CONTRO L ANTIGENE CORE (HBCA-IGG) DEL VIRUS B DELL EPATITE (HBV) NEL TRAPIANTO DI FEGATO (Centro Nazionale
Parte I - LINEE GUIDA PROTOCOLLO PER L UTILIZZO DI DONATORI POSITIVI PER GLI ANTICORPI DIRETTI CONTRO L ANTIGENE CORE (HBCA-IGG) DEL VIRUS B DELL EPATITE (HBV) NEL TRAPIANTO DI FEGATO (Centro Nazionale
Lezione 2 Come leggere l articolo scientifico
 Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR)
 Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO
 EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
EMOPATIE MALIGNE NEL PAZIENTE ANZIANO EMOPATIE MALIGNE NEL PAZIENTE ANZIANO Il progressivo invecchiamento della popolazione aumenta l incidenza delle patologie dell anziano Netto incremento delle emopatie
Allegato IV. Conclusioni scientifiche
 Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
Allegato IV Conclusioni scientifiche 1 Conclusioni scientifiche Il 7 giugno 2017, la Commissione europea (CE) è stata informata di un caso mortale di insufficienza epatica fulminante in un paziente trattato
I medici non devono più prescrivere medicinali contenenti calcitonina in forma di spray nasale per il trattamento dell'osteoporosi.
 20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
SINOSSI DEL PROTOCOLLO ML21868
 TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
U.O. Emato-oncologia Pediatrica, I.R.C.S.S Burlo Garofolo, Trieste Dr. Marco RABUSIN
 TITOLO Studio prospettico IRCSS Burlo Garofolo di Trieste S V I L U P P O D I S T R AT E G I E FA R M A C O L O G I C H E P E R L A PERSONALIZZAZIONE DEL TRATTAMENTO DELLA LEUCEMIA LINFOBLASTICA ACUTA
TITOLO Studio prospettico IRCSS Burlo Garofolo di Trieste S V I L U P P O D I S T R AT E G I E FA R M A C O L O G I C H E P E R L A PERSONALIZZAZIONE DEL TRATTAMENTO DELLA LEUCEMIA LINFOBLASTICA ACUTA
PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO
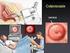 PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA
PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA
Fondazione Italia Fondazione It alia Linf omi Linf ONLUS
 Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
Indicatori di qualità nei carcinomi genitali femminili"
 Indicatori di qualità nei carcinomi genitali femminili" Corso DAS Oncologia 19.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in Selva 24 6600 Locarno Indicatori di qualità Introduzione"
Indicatori di qualità nei carcinomi genitali femminili" Corso DAS Oncologia 19.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in Selva 24 6600 Locarno Indicatori di qualità Introduzione"
Costruzione di un indicatore prognostico di ospedalizzazioni ripetute nella Regione Lazio
 Costruzione di un indicatore prognostico di ospedalizzazioni ripetute nella Regione Lazio A. Lallo, P. Schifano, A. Bargagli, N. Agabiti, P. Michelozzi Dipartimento Epidemiologia del SSR Regione Lazio
Costruzione di un indicatore prognostico di ospedalizzazioni ripetute nella Regione Lazio A. Lallo, P. Schifano, A. Bargagli, N. Agabiti, P. Michelozzi Dipartimento Epidemiologia del SSR Regione Lazio
Epidemiologia e disegni di studio
 Epidemiologia e disegni di studio L epidemiologia valuta le associazioni tra fattori di esposizione ed esiti di salute all interno di predefinite cornici logico-formali Esposizione X Malattia Y Tali cornici
Epidemiologia e disegni di studio L epidemiologia valuta le associazioni tra fattori di esposizione ed esiti di salute all interno di predefinite cornici logico-formali Esposizione X Malattia Y Tali cornici
Responsabile: Prof. Stefano Milani SINTESI DEL PROTOCOLLO DI STUDIO
 Assegno di Ricerca dal titolo: Sperimentazione, studio, sviluppo e collaudo di nuovi metodi di prevenzione avanzata del cancro al colon-retto mediante colonscopia virtuale in modalità di telediagnosi.
Assegno di Ricerca dal titolo: Sperimentazione, studio, sviluppo e collaudo di nuovi metodi di prevenzione avanzata del cancro al colon-retto mediante colonscopia virtuale in modalità di telediagnosi.
Le leucemie acute mieloidi La diagnosi
 LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
LEUCEMIE MIELOIDI Le leucemie acute mieloidi sono una patologia dell adulto più frequente nell anziano con un età media >60 anni; entrambi i sessi sono colpiti, con una lieve predominanza per quello maschile.
Tab. VII - Protocollo per le indagini di laboratorio e strumentali consigliate nella gravidanza fisiologica
 Per gli esami di laboratorio, presentiamo il protocollo della regione Toscana (Tab. VII) per vedere se c'è stato un adeguamento alla gravidanza (Tab. VIII); i segni della emodiluizione dovrebbero essere
Per gli esami di laboratorio, presentiamo il protocollo della regione Toscana (Tab. VII) per vedere se c'è stato un adeguamento alla gravidanza (Tab. VIII); i segni della emodiluizione dovrebbero essere
Anemia Infiammatoria (Sideroacrestica o delle malattie croniche) Luciano Masini. Maria Brini
 Anemia Infiammatoria (Sideroacrestica o delle malattie croniche) Luciano Masini Ematologia ASMN/IRCCS Reggio Emilia Maria Brini Ordine dei Medici Reggio emilia 14/03/2012 Scuola Formazione Medicina Generale
Anemia Infiammatoria (Sideroacrestica o delle malattie croniche) Luciano Masini Ematologia ASMN/IRCCS Reggio Emilia Maria Brini Ordine dei Medici Reggio emilia 14/03/2012 Scuola Formazione Medicina Generale
Evidenze cliniche: punto d incontro fra ricercatore e clinico. 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1
 Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
Un esempio: CE Policlinico Gemelli
 Un esempio: CE Policlinico Gemelli Tipologia degli studi 32% 2% 3% 4% Farmacologici 41% 3% 9% 6% Diagnostici Chirurgici Anestesiologici Osservazionali Studi di laboratorio Dispositivi medici Radioterapia
Un esempio: CE Policlinico Gemelli Tipologia degli studi 32% 2% 3% 4% Farmacologici 41% 3% 9% 6% Diagnostici Chirurgici Anestesiologici Osservazionali Studi di laboratorio Dispositivi medici Radioterapia
Francesco Baudo S.C. Ematologia, A.O. Ospedale Niguarda Ca Granda, Milano
 LA REL e L ITP Francesco Baudo S.C. Ematologia, A.O. Ospedale Niguarda Ca Granda, Milano REL - RETE EMATOLOGICA LOMBARDA La REL, istituita nel 2008, è un modello di collaborazione finalizzato alla realizzazione
LA REL e L ITP Francesco Baudo S.C. Ematologia, A.O. Ospedale Niguarda Ca Granda, Milano REL - RETE EMATOLOGICA LOMBARDA La REL, istituita nel 2008, è un modello di collaborazione finalizzato alla realizzazione
Seconda Parte Specifica per la tipologia di scuola - Statistica sanitaria e Biometria - 22/07/2016
 Domande relative alla specializzazione in: Statistica sanitaria e Biometria Scenario 1: In uno studio prospettivo condotto per valutare la relazione tra l'uso di estrogeni e rischio di cancro alla mammella,
Domande relative alla specializzazione in: Statistica sanitaria e Biometria Scenario 1: In uno studio prospettivo condotto per valutare la relazione tra l'uso di estrogeni e rischio di cancro alla mammella,
Quality Editor. Data. 3M Sistemi Informativi per la Salute
 3M Sistemi Informativi per la Salute Quality Editor Data L utilizzo del Data Quality Editor per la valutazione della qualità delle informazioni della Scheda di Dimissione Ospedaliera (SDO) Utilizzo del
3M Sistemi Informativi per la Salute Quality Editor Data L utilizzo del Data Quality Editor per la valutazione della qualità delle informazioni della Scheda di Dimissione Ospedaliera (SDO) Utilizzo del
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Il significato degli esami di coagulazione. Walter Ageno
 Il significato degli esami di coagulazione Walter Ageno Principali caratteristiche dei nuovi anticoagulanti Via orale di somministrazione Ampia finestra terapeutica Farmacocinetica e farmacodinamica prevedibili
Il significato degli esami di coagulazione Walter Ageno Principali caratteristiche dei nuovi anticoagulanti Via orale di somministrazione Ampia finestra terapeutica Farmacocinetica e farmacodinamica prevedibili
IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA?
 IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA? Dr. Giorgio Bonciarelli Oncologia Medica Azienda ULSS17 Monselice, 8 Marzo 2014 ALCUNI NUMERI IN EUROPA In ITALIA, nel 2013, sono stati stimati
IL NODO (tumorale) AL SENO: QUANDO LA TERAPIA FARMACOLOGICA? Dr. Giorgio Bonciarelli Oncologia Medica Azienda ULSS17 Monselice, 8 Marzo 2014 ALCUNI NUMERI IN EUROPA In ITALIA, nel 2013, sono stati stimati
SINOSSI DEL PROTOCOLLO
 SINOSSI DEL PROTOCOLLO EudraCT: 2015 004856 24 Numero IND: 74,552 Numero di protocollo: Prodotto sperimentale: Principio attivo/inn: Titolo dello studio: AC220-A-U302 Quizartinib (AC220) AC010220 2HCl
SINOSSI DEL PROTOCOLLO EudraCT: 2015 004856 24 Numero IND: 74,552 Numero di protocollo: Prodotto sperimentale: Principio attivo/inn: Titolo dello studio: AC220-A-U302 Quizartinib (AC220) AC010220 2HCl
I trigger relativi alle cure
 Massimo Geraci Direttore MCAU ARNAS Ospedali Civico Di Cristina Benfratelli Palermo Rosario Squatrito Direttore MCAU San Raffaele Giglio Cefalù Sono 14 trigger identificati dalla lettera C Trigger: solo
Massimo Geraci Direttore MCAU ARNAS Ospedali Civico Di Cristina Benfratelli Palermo Rosario Squatrito Direttore MCAU San Raffaele Giglio Cefalù Sono 14 trigger identificati dalla lettera C Trigger: solo
RICERCA SCIENTIFICA. Come compilare il Protocollo di ricerca per Studi Osservazionali. Protocollo. osservazionale ISTRUZIONI GENERALI
 RICERCA SCIENTIFICA 5b Protocollo osservazionale Come compilare il Protocollo di ricerca per Studi Osservazionali Prof. Paolo Chiari Dipartimento di Scienze Mediche echirurgiche Università di Bologna Codice
RICERCA SCIENTIFICA 5b Protocollo osservazionale Come compilare il Protocollo di ricerca per Studi Osservazionali Prof. Paolo Chiari Dipartimento di Scienze Mediche echirurgiche Università di Bologna Codice
Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Novità della Ricerca
 Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Alessandro M Vannucchi Università di Firenze, AOU Careggi Biologia delle malattie Inquadramento prognostico Nuovi
Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Alessandro M Vannucchi Università di Firenze, AOU Careggi Biologia delle malattie Inquadramento prognostico Nuovi
PROFILASSI ANTITROMBOTICA IN CHIRURGIA GENERALE
 CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
Screening oncologico di popolazione: principi e valutazione
 Screening oncologico di popolazione: principi e valutazione Screening oncologico organizzato: definizione Somministrazione attiva e periodica di un test diagnostico di provata efficacia ad una popolazione
Screening oncologico di popolazione: principi e valutazione Screening oncologico organizzato: definizione Somministrazione attiva e periodica di un test diagnostico di provata efficacia ad una popolazione
Trombocitemia essenziale. Paola Guglielmelli (Firenze)
 Trombocitemia essenziale Paola Guglielmelli (Firenze) Incidenza: 1 per 100.000 ab/anno Prevalenza: 10 40 per 100.000 Aumentata conta piastrinica (> 450 x 109/L) Storia naturale della TE Neoplasia mieloproliferativa
Trombocitemia essenziale Paola Guglielmelli (Firenze) Incidenza: 1 per 100.000 ab/anno Prevalenza: 10 40 per 100.000 Aumentata conta piastrinica (> 450 x 109/L) Storia naturale della TE Neoplasia mieloproliferativa
RIVISTA: lnt Journal of lmpotence Research (2006) 18, MJ. Dresser, D. Desai, S. Gidwani, AD. Seftel, NB. Modi O B I E T T I V I
 I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
Studio SENIORS Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza
 Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
INTRODUZIONE. continua. Obiettivi dello Studio. Processo Pazienti in (ABMT)
 Master in Evidence-Based Practice e Metodologia della Ricerca Clinico-assistenziale Relazione tra Nutrizione Parenterale Totale (NPT), Peso Corporeo e rischio di Mucosite del cavo orale correlata a chemioterapia
Master in Evidence-Based Practice e Metodologia della Ricerca Clinico-assistenziale Relazione tra Nutrizione Parenterale Totale (NPT), Peso Corporeo e rischio di Mucosite del cavo orale correlata a chemioterapia
Proposta di un percorso HCV nei pazienti nefropatici. Anastasio Grilli UO Malattie Infettive Universitaria FERRARA 26 maggio 2017
 Anastasio Grilli UO Malattie Infettive Universitaria FERRARA 26 maggio 2017 L infezione da virus dell epatite C (HCV) è una delle principali cause di malattia cronica del fegato nel mondo L impatto clinico
Anastasio Grilli UO Malattie Infettive Universitaria FERRARA 26 maggio 2017 L infezione da virus dell epatite C (HCV) è una delle principali cause di malattia cronica del fegato nel mondo L impatto clinico
Febbre Mediterranea Familiare
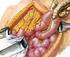 www.printo.it/pediatric-rheumatology/ch_it/intro Febbre Mediterranea Familiare Versione 2016 2. DIAGNOSI E TRATTAMENTO 2.1 Come viene diagnosticata? In genere si segue il seguente approccio: Sospetto clinico:
www.printo.it/pediatric-rheumatology/ch_it/intro Febbre Mediterranea Familiare Versione 2016 2. DIAGNOSI E TRATTAMENTO 2.1 Come viene diagnosticata? In genere si segue il seguente approccio: Sospetto clinico:
LA STRATEGIA TERAPEUTICA ADIUVANTE. Luciano Galletto
 I TUMORI DEL CORPO DELL UTERO: STRATEGIE TERAPEUTICHE IN EVOLUZIONE Torino, 26 Febbraio 2010 LA STRATEGIA TERAPEUTICA ADIUVANTE Luciano Galletto Proporzione dei tumori del corpo dell utero vs proporzione
I TUMORI DEL CORPO DELL UTERO: STRATEGIE TERAPEUTICHE IN EVOLUZIONE Torino, 26 Febbraio 2010 LA STRATEGIA TERAPEUTICA ADIUVANTE Luciano Galletto Proporzione dei tumori del corpo dell utero vs proporzione
MODELLO UNICO DI PRESCRIZIONE SERVIZIO SANITARIO REGIONE CAMPANIA A.S.L.
 REGIONE CAMPANIA - SANI.A.R.P. MODELLO UNICO DI PRESCRIZIONE SERVIZIO SANITARIO REGIONE CAMPANIA A.S.L. Codice a barra N.: CENTRO PRESCRITTORE (DEMINAZIONE):... CODICE STRUTTURA:... IL/LA SOTTOSTRITT0/A
REGIONE CAMPANIA - SANI.A.R.P. MODELLO UNICO DI PRESCRIZIONE SERVIZIO SANITARIO REGIONE CAMPANIA A.S.L. Codice a barra N.: CENTRO PRESCRITTORE (DEMINAZIONE):... CODICE STRUTTURA:... IL/LA SOTTOSTRITT0/A
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti
 Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
Cardiotossicità del trattamento del carcinoma mammario: l uso di sistemi informativi correnti Cuccaro F., Autelitano M., Bertù L., Randi G., Chiaffarino F., Ghilardi S., Leone R., Filipazzi L., Bonini
STUDIO GRUPPO ITALIANO PANCREAS GIP-2
 STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA.
 FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
FOGLIO INFORMATIVO E CONSENSO INFORMATO PER GASTROSCOPIA DIAGNOSTICA E TERAPEUTICA. Gentile Paziente, La gastroscopia è un esame endoscopico che permette la visualizzazione della mucosa dell esofago, dello
DETERMINAZIONE 24 novembre Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009).
 DETERMINAZIONE 24 novembre 2009. Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009). Regime di rimborsabilità e prezzo di vendita della specialità
DETERMINAZIONE 24 novembre 2009. Regime di rimborsabilità e prezzo di vendita del medicinale per uso umano «Zarzio». (Determinazione /C320/2009). Regime di rimborsabilità e prezzo di vendita della specialità
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE. Reggio Emilia 4 giugno 2008
 O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
SCHEDA DI SEGNALAZIONE DI CASO PER ESPOSIZIONE IN OPERATORE SANITARIO
 Le schede per la segnalazione di caso di profilassi post.-esposizione (PPE) ad HIV sono due; una per le esposizioni occupazionali in operatore sanitario, l altra per le esposizioni occupazionali in non
Le schede per la segnalazione di caso di profilassi post.-esposizione (PPE) ad HIV sono due; una per le esposizioni occupazionali in operatore sanitario, l altra per le esposizioni occupazionali in non
Il protocollo di ricerca
 Infermiere di ricerca Il protocollo di ricerca Dr. Monica Turazza Negrar, 17 maggio 2017 Cosa rappresenta: percorso da seguire in qualsiasi forma di sperimentazione pianificata che riguardi prevenzione,
Infermiere di ricerca Il protocollo di ricerca Dr. Monica Turazza Negrar, 17 maggio 2017 Cosa rappresenta: percorso da seguire in qualsiasi forma di sperimentazione pianificata che riguardi prevenzione,
IRON DEFICENCY. Luciano Arcari - ROMA. Roma, 23 settembre 2017
 IRON DEFICENCY L importanza della correzione del deficit di ferro: esperienza nella gestione ambulatoriale del paziente con insufficienza cardiaca cronica Roma, 23 settembre 2017 Luciano Arcari - ROMA
IRON DEFICENCY L importanza della correzione del deficit di ferro: esperienza nella gestione ambulatoriale del paziente con insufficienza cardiaca cronica Roma, 23 settembre 2017 Luciano Arcari - ROMA
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO
 RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
