CALCOLO DELLA STRUTTURA MOLECOLARE: 1. LE SUPERFICI DI ENERGIA POTENZIALE E L APPROSSIMAZIONE DI BORN-OPPENHEIMER
|
|
|
- Aurora Vacca
- 5 anni fa
- Visualizzazioni
Transcript
1 CALCOLO DELLA STRUTTURA MOLECOLARE: 1. LE SUPERFICI DI ENERGIA POTENZIALE E L APPROSSIMAZIONE DI BORN-OPPENHEIMER 1
2 COSA E UNA MOLECOLA Tutti gli atomi a piccola distanza si attraggono (forze di van der Waals); si tratta di forze piccole e non direzionali, che danno luogo ad aggregati senza una struttura ed una composizione definita. (Es.: liquidi). Quando si instaura un LEGAME CHIMICO fra due atomi, ovvero quando entrano in gioco forze grandi e direzionali, si formano le molecole, i.e. aggregati sufficientemente stabili da possedere composizione e struttura definite. 2
3 Le molecole sono composte da ATOMI, o + in generale, da un insieme di particelle cariche, i.e. nuclei (positivi) ed elettroni (negativi). L unica forza fisica importante per i processi chimici è l interazione di Coulomb fra particelle cariche. Due molecole differiscono perché contengono un diverso numero di elettroni e protoni nel nucleo, o perché è diversa la posizione dei nuclei a parità di numero di elettroni (i.e. isomeri). 3
4 CALCOLO DELLA STRUTTURA MOLECOLARE Le forze che determinano la struttura molecolare sono governate dalle leggi della meccanica quantistica. Equazione di Schrödinger: descrive il comportamento di un insieme di particelle: Φ dipende dalla posizione di tutte le particelle e dal tempo, i.e. Φ(r,t). T energia cinetica V energia potenziale 4
5 Per uno stato stazionario nel tempo: Ψ dipende dalla posizione di tutte le particelle, i.e. Ψ(r). 5
6 COSTRUZIONE DI H APPROSSIMAZIONE: Considero SOLO le interazioni elettrostatiche, i.e. trascuro gli effetti relativistici (contrazione degli orbitali s e p; espansione degli orbitali d e f; accoppiamento spin-orbita). Gli effetti relativistici sono dovuti al fatto che all aumentare del numero atomico Z la velocità degli elettroni degli strati più interni aumenta e diventa comparabile con c (velocità della luce). Per problemi di interesse CHIMICO, gli effetti relativistici possono essere trascurati, con buona approssimazione, per gli atomi fino a Z=36 (Kr). Per il V periodo gli errori possono essere accettabili nella maggior parte dei casi; gli effetti più marcati si hanno per i metalli di transizione. 6
7 7
8 HAMILTONIANO MOLECOLARE Per un sistema composto da N nuclei ed M elettroni: M Il sistema è assunto isolato: non ci sono forze esterne. 8
9 Dove: 9
10 Introducendo le unità atomiche: 10
11 11 l espressione di H si semplifica: < < + + = N B A AB B A M M N A A A N A A A M R Z Z r R Z m H ν µ µν µ µ µ µ è più pratico eseguire i calcoli quantomeccanici in unità atomiche.
12 COSTANTI: 12
13 Equazione di Schrödinger per una molecola in uno stato stazionario: L equazione di Schrödinger per le molecole, anche le più piccole, appare molto complicata. La funzione d onda Ψ(r,R), soluzione dell equazione di Schrödinger, è una complicata funzione di tutte le variabili elettroniche e nucleari: r = x 1, y 1, z 1, x 2, y 2, z 2, coordinate di tutti gli elettroni R = X 1, Y 1, Z 1, X 2, Y 2, Z 2, coordinate di tutti i nuclei E èl energia totale del sistema. 13
14 H èl operatore energia totale: T e operatore energia cinetica degli elettroni (opera su r) T n operatore energia cinetica dei nuclei (opera su R) V operatore energia potenziale elettrostatica totale: V ne attrazione nuclei-elettroni (funzione di r e R) V ee repulsione tra gli elettroni (funzione di r) V nn repulsione tra i nuclei (funzione di R) 14
15 Quindi: m protone 1840 m elettrone i nuclei sono almeno 2000 volte + pesanti degli elettroni. Dal punto di vista della meccanica classica il moto dei nuclei è molto + lento del moto degli elettroni. si può assumere che il moto degli elettroni dipenda dalla sola POSIZIONE DEI NUCLEI (e non dal loro moto). Dal punto di vista della meccanica quantistica Born e Oppenheimer dimostrarono che il moto elettronico può, approssimativamente, essere separato dal moto nucleare. 15
16 APPROSSIMAZIONE DI BORN-OPPENHEIMER (BO) O ADIABATICA: consente di separare il moto degli elettroni dal moto dei nuclei Definiamo: H el = T e + V ne + V ee + V nn Hamiltoniano elettronico, i.e. H privato del termine di energia cinetica dei nuclei: H el non comprende operatori differenziali che contengano le coordinate nucleari. Ovvero considero i nuclei fissi ad una distanza R. 16
17 Quindi: H el Ψ el,i (r;r) = E el,i (R) Ψ el,i (r;r) dove le coordinate nucleari R appaiono come PARAMETRI che possiamo fissare a nostra discrezione,ovvero: Ψ el,i (r;r) funzione d onda dello stato elettronico i-esimo E el,i (R) energia dello stato elettronico i-esimo sono funzioni PARAMETRICHE delle coordinate nucleari. ; separa le coordinate dinamiche degli elettroni dalle coordinate parametriche dei nuclei. 17
18 1. La risoluzione dell eq. di Schrödinger elettronica fornisce una pluralità di soluzioni per una data geometria nucleare R; l energia + bassa e la relativa funzione d onda definiscono lo STATO FONDAMENTALE ELETTRONICO i-esimo della molecola a quella geometria; le altre energie e funzioni d onda si riferiscono a STATI ELETTRONICAMENTE ECCITATI i+1 della molecola. 2. Al cambiare della geometria nucleare R, cambieranno sia E el,i che Ψ el,i ; una volta ottenuta E el,i (R), possiamo studiare il suo andamento al variare di R: punti di minimo GEOMETRIE DI EQUILIBRIO. 18
19 In base all approssimazione BO, Ψ tot è fattorizzata: Ψ tot (r,r) = Ψ el (r;r) χ n (R) χ n (R) funzione delle sole coordinate nucleari, perché la Ψ el è a variazione molto lenta vs le coordinate nucleari e le sue derivate vs queste possono essere trascurate ( Ψ el / R j ) 0, con R j =coord. nucl. Posso quindi scrivere due equazioni di Schrödinger separate, una per i nuclei, ed una per gli elettroni: 19
20 tot tot Ψ tot (r,r) = Ψ el (r;r) χ n (R) H Ψ el χ n = (T n + H el ) Ψ el χ n = T n (Ψ el χ n ) + H el (Ψ el χ n ) = Ψ el T n χ n + E el (R) Ψ el χ n = Ψ el [T n + E el (R)] χ n = E tot Ψ el χ n avendo imposto: [T n + E el (R)] χ n (R) = E tot χ n (R) eq. di Schrödinger per i nuclei, che si muovono in un en. pot. E el 20
21 Riassumendo: funzione d onda completa per una molecola in approx. BO: Ψ tot (r,r) = Ψ el (r;r) χ n (R) il moto degli elettroni è disaccoppiato da quello dei nuclei Ho due equazioni indipendenti: per il moto degli elettroni: 1) H el Ψ el (r;r) = E el (R) Ψ el (r;r) la Ψ el soddisfa un eq. di Schrödinger per gli elettroni nel campo dei nuclei FISSI. per il moto dei nuclei: 2) (T n + E el ) χ n (R) = E tot χ n (R) la χ n soddisfa un eq. di Schrödinger per i nuclei con energia potenziale E el. Risolvendo la (1), si ricava E el da introdurre nella (2). 21
22 NB: E el è contemporaneamente: 1. l autovalore per gli elettroni nell eq. (1) = energia dello stato elettronico i-esimo. 2. l operatore energia potenziale nell equazione per i nuclei (2) = potenziale a cui sono soggetti i nuclei, quando gli elettroni sono nello stato i-esimo. E el (R) è detta superficie di Born-Oppenheimer o Superficie di Energia Potenziale (PES, Potential Energy Surface). 22
23 NUMERO DI GRADI DI LIBERTA Per descrivere ciascun nucleo, occorrono 3 coordinate x, y, z. Posizione di una molecola con N atomi 3N coordinate nucleari. Tuttavia per una molecola isolata (assenza di forze esterne) la PES dipende SOLO dalla posizione reciproca dei nuclei (COORDINATE INTERNE): Se considero: 3 gradi di libertà per le traslazioni e 3 per le rotazioni (2 per le molecole lineari) 3N-6 (3N-5 per molecole lineari) coordinate interne la PES è funzione di 3N-6 (3N-5 per molecole lineari) parametri. 23
24 Molecola biatomica N=2 1 sola coordinata interna, i.e. la distanza internucleare R: E el può essere graficata come una curva (E el vs R). Ad es.: H 2 la curva dell energia elettronica per lo stato fondamentale ha un minimo per R = 0.7Ǻ (= R e distanza di equilibrio della molecola H 2 ). D 0 E (repulsione nuclei) Punto di partenza D E en. atomi separati (asintoticamente) Punto di arrivo Minimizzazione uni-dimensionale: l energia dipende solo da una 24 coordinata, la distanza di legame R.
25 La PES è completamente determinata specificando: numero e specie dei nuclei SISTEMA MOLECOLARE numero di elettroni stato elettronico considerato 25
26 Approssimazione di Born-Oppenheimer Valida in generale per lo stato fondamentale. Stati legati Stati non legati Per gli stati eccitati ci sono problemi perché le superfici di potenziale sono vicine e possono incrociarsi: interazioni non adiabatiche. 26
27 Stato fondamentale e stati eccitati stati eccitati Mg 2 stato fondamentale 27
28 I termini trascurati nell approssimazione BO sono piccoli se la funzione d onda elettronica è una funzione che varia lentamente al variare delle coordinate nucleari. Condizioni di applicabilità della approx. BO: i nuclei sono fermi o al max si muovono intorno ad una posizione di equilibrio (no fenomeni di urto,..); la funzione d onda elettronica NON è degenere, o quasi degenere, ( i termini trascurati possono causare una significativa interazione tra superfici BO). Sono quindi esclusi: i casi di accoppiamento vibro-elettronico (effetto Jahn-Teller) i casi in cui la PES si incrocia con la PES di un altro stato elettronico (vedi fluorescenza) 28
29 L approx. BO non è valida quando la PES è troppo vicina o addirittura si incrocia con la PES di un altro stato elettronico (vedi fluorescenza). 29
Molecole. 04/09/13 3-MOL-0.doc 0
 Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
Molecole 04/09/13 3-MOL-0.doc 0 Legame covalente H 2 + Il potenziale cui è soggetto l elettrone ha 2 minimi equivalenti 1) H + si avvicina a H 2) Se la barriera diventa abbastanza sottile la probabilità
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Superfici di Potenziale
 Superfici di Potenziale 10/05/12 BO.DOC 0 I modelli più semplici dei fenomeni chimici descrivono le molecole come un insieme di atomi soggetti ad un potenziale (PES) Un potenziale di questo tipo viene
Superfici di Potenziale 10/05/12 BO.DOC 0 I modelli più semplici dei fenomeni chimici descrivono le molecole come un insieme di atomi soggetti ad un potenziale (PES) Un potenziale di questo tipo viene
Campo elettromagnetico
 Campo elettromagnetico z y Classicamente, è formato da un campo elettrico E e da un campo magnetico B oscillanti B E λ E = E 0 cos 2π(νt x/λ) B = B 0 cos 2π(νt x/λ) νλ = c ν, frequenza x λ, lunghezza d
Campo elettromagnetico z y Classicamente, è formato da un campo elettrico E e da un campo magnetico B oscillanti B E λ E = E 0 cos 2π(νt x/λ) B = B 0 cos 2π(νt x/λ) νλ = c ν, frequenza x λ, lunghezza d
Le molecole ed il legame chimico
 La meccanica quantistica è in grado di determinare esattamente i livelli energetici dell atomo di idrogeno e con tecniche matematiche più complesse è anche in grado di descrivere l atomo di elio trovando
La meccanica quantistica è in grado di determinare esattamente i livelli energetici dell atomo di idrogeno e con tecniche matematiche più complesse è anche in grado di descrivere l atomo di elio trovando
Fondamenti di Meccanica Quantistica (Prof. Tarantelli)
 Fondamenti di Meccanica Quantistica (Prof. Tarantelli) 1 MOTO LINEARE E L OSCILLATORE ARMONICO 2 EQUAZIONE DI SCHRODINGER Equazione di Schrödinger: descrive il comportamento di un insieme di particelle:
Fondamenti di Meccanica Quantistica (Prof. Tarantelli) 1 MOTO LINEARE E L OSCILLATORE ARMONICO 2 EQUAZIONE DI SCHRODINGER Equazione di Schrödinger: descrive il comportamento di un insieme di particelle:
Chimica quantistica. Loriano Storchi.
 Chimica quantistica Loriano Storchi loriano@storchi.org http://www.storchi.org/ FISICA CLASSICA Meccanica Classica La meccanica classica descrive il movimento di oggetti macroscopici come veicoli spaziali,
Chimica quantistica Loriano Storchi loriano@storchi.org http://www.storchi.org/ FISICA CLASSICA Meccanica Classica La meccanica classica descrive il movimento di oggetti macroscopici come veicoli spaziali,
Università degli Studi di Roma La Sapienza. Approssimazione di M. Born & R. Oppenheimer.
 Università degli Studi di Roma La Sapienza Facoltà di Scienze Matematiche, Fisiche, e Naturali. (Appunti di Fisica Nucleare) Approssimazione di M. Born & R. Oppenheimer. F. López (Pancho) pako.lopez@virgilio.it
Università degli Studi di Roma La Sapienza Facoltà di Scienze Matematiche, Fisiche, e Naturali. (Appunti di Fisica Nucleare) Approssimazione di M. Born & R. Oppenheimer. F. López (Pancho) pako.lopez@virgilio.it
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. L atomo di Bohr 3. Il modello atomico
Ottimizzazione della geometria. Ottimizzazione della geometria A.A ! " B. Civalleri Chimica Computazionale a.a
 Ottimizzazione della geometria A.A. 2006-07 07! " B. Civalleri Chimica Computazionale a.a. 2006-07 1 Ottimizzazione della geometria Definizioni (I) Superficie di energia potenziale (PES) La PES descrive
Ottimizzazione della geometria A.A. 2006-07 07! " B. Civalleri Chimica Computazionale a.a. 2006-07 1 Ottimizzazione della geometria Definizioni (I) Superficie di energia potenziale (PES) La PES descrive
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Comune ordine di riempimento degli orbitali di un atomo
 Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
Comune ordine di riempimento degli orbitali di un atomo Le energie relative sono diverse per differenti elementi ma si possono notare le seguenti caratteristiche: (1) La maggior differenza di energia si
Proprietà termiche. Reazione che oppone materiale alla somministrazione di calore. Corpo aumenta dimensioni e aumenta la sua temperatura
 Proprietà termiche Reazione che oppone materiale alla somministrazione di calore Corpo aumenta dimensioni e aumenta la sua temperatura Gradiente di T, l energia viene trasportata dalle regioni più calde
Proprietà termiche Reazione che oppone materiale alla somministrazione di calore Corpo aumenta dimensioni e aumenta la sua temperatura Gradiente di T, l energia viene trasportata dalle regioni più calde
L atomo di idrogeno (1) H T = p2 1 2m 1. + p2 2 2m 2. + V ( r 1 r 2 ) (2) Definiamo le nuove variabili: 1. La massa totale M M = m 1 + m 2 (3)
 L atomo di idrogeno Il problema dell atomo di idrogeno é un problema esattamente risolubili ed i suoi risultati possono essere estesi agli atomi idrogenoidi, in cui solo c é solo un elettrone sottoposto
L atomo di idrogeno Il problema dell atomo di idrogeno é un problema esattamente risolubili ed i suoi risultati possono essere estesi agli atomi idrogenoidi, in cui solo c é solo un elettrone sottoposto
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA. (Plank Einstein)
 L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
L ATOMO SECONDO LA MECCANICA ONDULATORIA IL DUALISMO ONDA-PARTICELLA POSTULATO DI DE BROGLIÈ Se alla luce, che è un fenomeno ondulatorio, sono associate anche le caratteristiche corpuscolari della materia
Le molecole ed il legame chimico
 LA MOLECOLA DI IDROGENO X r A2 e 2 r A1 r 12 r B2 e 1 r B1 È il primo caso di molecola bielettronica da noi incontrato ed è la base per lo studio di ogni altra molecola. A R AB B Z Y Se si applica l approssimazione
LA MOLECOLA DI IDROGENO X r A2 e 2 r A1 r 12 r B2 e 1 r B1 È il primo caso di molecola bielettronica da noi incontrato ed è la base per lo studio di ogni altra molecola. A R AB B Z Y Se si applica l approssimazione
Meccanica quantistica (5)
 Meccanica quantistica (5) 0/7/14 1-MQ-5.doc 0 Oscillatore armonico Se una massa è sottoposta ad una forza di richiamo proporzionale allo spostamento da un posizione di equilibrio F = kx il potenziale (
Meccanica quantistica (5) 0/7/14 1-MQ-5.doc 0 Oscillatore armonico Se una massa è sottoposta ad una forza di richiamo proporzionale allo spostamento da un posizione di equilibrio F = kx il potenziale (
La struttura elettronica degli atomi
 1 In unità atomiche: a 0 me 0,59A unità di lunghezza e H 7, ev a H=Hartree unità di energia L energia dell atomo di idrogeno nello stato fondamentale espresso in unità atomiche è: 4 0 me 1 e 1 E H 13,
1 In unità atomiche: a 0 me 0,59A unità di lunghezza e H 7, ev a H=Hartree unità di energia L energia dell atomo di idrogeno nello stato fondamentale espresso in unità atomiche è: 4 0 me 1 e 1 E H 13,
Proprietà molecolari. Struttura elettronica, vibrazionale, e rotazionale
 Proprietà molecolari Struttura elettronica, vibrazionale, e rotazionale molecole biatomiche eteronucleari: legame ionico attrazione fra gli ioni e E p = + repulsione fra i nuclei e gli elettroni interni
Proprietà molecolari Struttura elettronica, vibrazionale, e rotazionale molecole biatomiche eteronucleari: legame ionico attrazione fra gli ioni e E p = + repulsione fra i nuclei e gli elettroni interni
Lezione 3. Legame Chimico. Teoria degli Orbitali Molecolari
 Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà.
 Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà. Nell atomo l energia associata ad un elettrone (trascurando
Ma se dobbiamo trattare l elettrone come un onda occorre una funzione (che dobbiamo trovare) che ne descriva esaurientemente queste proprietà. Nell atomo l energia associata ad un elettrone (trascurando
ATOMI MONOELETTRONICI
 ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
ATOMI MONOELETTRONICI L equazione di Schrödinger per gli atomi contenenti un solo elettrone (atomo di idrogeno, ioni He +, Li 2+ ) può essere risolta in maniera esatta e le soluzioni ottenute permettono
Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica
 ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
CHIMICA: studio della struttura e delle trasformazioni della materia
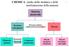 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Gli elettroni della molecola sono quindi descritti da
 IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Calcolo variazionale. Calcolo variazionale.
 antonino.polimeno@unipd.it Indice Perchè, quando e come Il calcolo variazionale: basi Equazioni di Eulero Bolle di sapone Equazioni di Hamilton Equazioni di Hartree-Fock G.M. Ewing, Calculus of Variations
antonino.polimeno@unipd.it Indice Perchè, quando e come Il calcolo variazionale: basi Equazioni di Eulero Bolle di sapone Equazioni di Hamilton Equazioni di Hartree-Fock G.M. Ewing, Calculus of Variations
Eccitazioni nucleari. Capitolo Spettro rotazionale
 Capitolo 1 Eccitazioni nucleari 1.1 Spettro rotazionale Consideriamo un nucleo pari pari, con spin zero, che abbia però una deformazione permanente. Supponiamo inoltre che il nucleo goda di una simmetria
Capitolo 1 Eccitazioni nucleari 1.1 Spettro rotazionale Consideriamo un nucleo pari pari, con spin zero, che abbia però una deformazione permanente. Supponiamo inoltre che il nucleo goda di una simmetria
Eccitazioni nucleari
 1 Spettro rotazionale Lezione 28 Eccitazioni nucleari Consideriamo un nucleo pari pari, con spin zero, che abbia però una deformazione permanente. Supponiamo inoltre che il nucleo goda di una simmetria
1 Spettro rotazionale Lezione 28 Eccitazioni nucleari Consideriamo un nucleo pari pari, con spin zero, che abbia però una deformazione permanente. Supponiamo inoltre che il nucleo goda di una simmetria
ORBITA ORBIT LI ALI MOLECOLARI
 ORBITALI MOLECOLARI Una molecola è dotata di una serie di orbitali detti orbitali molecolari Gli elettroni risiedono negli orbitali molecolari che, in molti casi, sono distribuiti (delocalizzati) su tutta
ORBITALI MOLECOLARI Una molecola è dotata di una serie di orbitali detti orbitali molecolari Gli elettroni risiedono negli orbitali molecolari che, in molti casi, sono distribuiti (delocalizzati) su tutta
Generalità delle onde elettromagnetiche
 Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
Generalità delle onde elettromagnetiche Ampiezza massima: E max (B max ) Lunghezza d onda: (m) E max (B max ) Periodo: (s) Frequenza: = 1 (s-1 ) Numero d onda: = 1 (m-1 ) = v Velocità della luce nel vuoto
ATOMO. Avogadro (1811) Volumi uguali di gas diversi contengono un ugual numero di MOLECOLE (N A =6,022*10 23 )
 ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
Chimica Fisica 2. Vibrazioni di molecole poliatomiche
 Chimica Fisica 2 chimica industriale 2 anno A.A. 2009-0 Vibrazioni di molecole poliatomiche Antonio Toffoletti Spettroscopia vibrazionale Molecole Bi-atomiche Approssimazione armonica E v = (v + ½)ħω ω
Chimica Fisica 2 chimica industriale 2 anno A.A. 2009-0 Vibrazioni di molecole poliatomiche Antonio Toffoletti Spettroscopia vibrazionale Molecole Bi-atomiche Approssimazione armonica E v = (v + ½)ħω ω
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Metodi Pseudopotenziale
 Oltre HF Metodi Pseudopotenziale Il moto degli elettroni interni è poco influenzato dall'intorno molecolare Il calcolo può essere semplificato modificando lo hamiltonano: limitandosi a calcolare solo il
Oltre HF Metodi Pseudopotenziale Il moto degli elettroni interni è poco influenzato dall'intorno molecolare Il calcolo può essere semplificato modificando lo hamiltonano: limitandosi a calcolare solo il
Corso di Chimica Generale CL Biotecnologie
 Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
Corso di Chimica Generale CL Biotecnologie STATI DELLA MATERIA Prof. Manuel Sergi MATERIA ALLO STATO GASSOSO MOLECOLE AD ALTA ENERGIA CINETICA GRANDE DISTANZA TRA LE MOLECOLE LEGAMI INTERMOLECOLARI DEBOLI
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Non c è alcuna possibilità che gli uomini un giorno accedano all energia. Robert Millikan Premio Nobel per la Fisica 1923
 Capitolo 3 Atomi Non c è alcuna possibilità che gli uomini un giorno accedano all energia atomica. Robert Millikan Premio Nobel per la Fisica 1923 3.1 Potenziali a simmetria sferica In problemi a simmetria
Capitolo 3 Atomi Non c è alcuna possibilità che gli uomini un giorno accedano all energia atomica. Robert Millikan Premio Nobel per la Fisica 1923 3.1 Potenziali a simmetria sferica In problemi a simmetria
Struttura Elettronica degli Atomi Meccanica quantistica
 Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Unbowed, Unbent, Unbroken
 Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole.
 4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
delle curve isoterme dell anidride carbonica
 COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
Prof. Mariano Casu (modulo II) (Prof. Navarra) (Prof. Casu)
 Università degli Studi di Cagliari Corso di Laurea triennale in Chimica Chimica fisica II e laboratorio CFU 6 + 6 Docenti Prof. Gabriele Navarra (modulo I) Prof. Mariano Casu (modulo II) SSD CHIM/02 Tel.
Università degli Studi di Cagliari Corso di Laurea triennale in Chimica Chimica fisica II e laboratorio CFU 6 + 6 Docenti Prof. Gabriele Navarra (modulo I) Prof. Mariano Casu (modulo II) SSD CHIM/02 Tel.
LA STRUTTURA DELL ATOMO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 3 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LA STRUTTURA DELL
Struttura del sistema periodico Stato fondamentale degli elementi
 Struttura del sistema periodico Stato fondamentale degli elementi Singolo elettrone: 1)Numero quantico principale n 2)Numero quantico del momento angolare orbitale l = 0, 1,, n-1 3)Numero quantico magnetico
Struttura del sistema periodico Stato fondamentale degli elementi Singolo elettrone: 1)Numero quantico principale n 2)Numero quantico del momento angolare orbitale l = 0, 1,, n-1 3)Numero quantico magnetico
6. DFT. Il metodo del funzionale densità
 6. DFT Il metodo del funzionale densità Un po di storia 1920: modello di Thomas-Fermi 1964: articolo di Hohenberg-Kohn che dimostra l esistenza di una DF esatta 1965: schema di Kohn-Sham 1970/80: prime
6. DFT Il metodo del funzionale densità Un po di storia 1920: modello di Thomas-Fermi 1964: articolo di Hohenberg-Kohn che dimostra l esistenza di una DF esatta 1965: schema di Kohn-Sham 1970/80: prime
FACOLTÀ DI SCIENZE MM.FF.NN. CORSO DI LAUREA IN CHIMICA Chimica Fisica II a.a
 1 FACOLTÀ DI SCIENZE MM.FF.NN. CORSO DI LAUREA IN CHIMICA Chimica Fisica II a.a. 2012-2013 Testo di riferimento: D.A. McQuarrie, J.D.Simon, Chimica Fisica. Un approccio molecolare, Zanichelli Editore,
1 FACOLTÀ DI SCIENZE MM.FF.NN. CORSO DI LAUREA IN CHIMICA Chimica Fisica II a.a. 2012-2013 Testo di riferimento: D.A. McQuarrie, J.D.Simon, Chimica Fisica. Un approccio molecolare, Zanichelli Editore,
Equazione di Schrödinger
 Equazione di Schrödinger dualità onda- particella particella libera come onda piana de Broglie Einstein NB - 1 derivata temporale: Equazione di Schrödinger derivata 2^ spaziale: 2 Equazione di Schrödinger
Equazione di Schrödinger dualità onda- particella particella libera come onda piana de Broglie Einstein NB - 1 derivata temporale: Equazione di Schrödinger derivata 2^ spaziale: 2 Equazione di Schrödinger
Chimica e computer Principi di spettroscopia IR
 Chimica e computer Principi di spettroscopia IR Marco Bortoli, Laura Orian Dipartimento di Scienze chimiche Università degli Studi di Padova Via Marzolo 1 35131 Padova La spettroscopia è lo studio dell
Chimica e computer Principi di spettroscopia IR Marco Bortoli, Laura Orian Dipartimento di Scienze chimiche Università degli Studi di Padova Via Marzolo 1 35131 Padova La spettroscopia è lo studio dell
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Spettroscopia infrarossa
 Spettroscopia infrarossa Utilizzata per studiare i livelli vibrazionali nelle molecole Energie in gioco: 5000-200 cm -1 (corrispondono a 2000-50000 nm), Il coefficiente di estinzione è circa di un ordine
Spettroscopia infrarossa Utilizzata per studiare i livelli vibrazionali nelle molecole Energie in gioco: 5000-200 cm -1 (corrispondono a 2000-50000 nm), Il coefficiente di estinzione è circa di un ordine
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
I legami chimici. Programma: a che punto siamo? Funzioni di stato. Corso di Studi di Fisica Corso di Chimica. Luigi Cerruti
 Corso di Studi di Fisica Corso di Chimica Programma: a che punto siamo? Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica Programma: a che punto siamo? Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 Programma: a che punto siamo? I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 11-12 2010 Programma: a che punto siamo? I legami chimici Un volume di gas, una certa quantità di soluzione, un cristallo
STRUTTURA ATOMICA. Per lo studio della struttura dell atomo ci si avvale della Spettroscopia.
 STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
STRUTTURA ATOMICA Il modello planetario dell atomo secondo Rutherford si appoggia sulla meccanica classica. Il modello non può essere corretto visto che per descrivere il comportamento delle particelle
Modello atomico ad orbitali e numeri quantici
 Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
Modello atomico ad orbitali e numeri quantici Il modello atomico di Bohr permette di scrivere correttamente la configurazione elettronica di un atomo ma ha dei limiti che sono stati superati con l introduzione
Risultati della teoria di Hartree
 Risultati della teoria di Hartree Il potenziale è a simmetria sferica, come nell atomo di idrogeno, quindi: ψ n, l, m = Rn, l ( r) Θ l, m ( θ ) Φ m ( ϕ ) l l l La dipendenza angolare delle autofunzioni
Risultati della teoria di Hartree Il potenziale è a simmetria sferica, come nell atomo di idrogeno, quindi: ψ n, l, m = Rn, l ( r) Θ l, m ( θ ) Φ m ( ϕ ) l l l La dipendenza angolare delle autofunzioni
E. SCHRODINGER ( )
 E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
E. SCHRODINGER (1887-1961) Elettrone = onda le cui caratteristiche possono essere descritte con un equazione simile a quella delle onde stazionarie le cui soluzioni, dette funzioni d onda ψ, rappresentano
Programma della I parte
 Programma della I parte Cenni alla meccanica quantistica: il modello dell atomo Dall atomo ai cristalli: statistica di Fermi-Dirac il modello a bande di energia popolazione delle bande livello di Fermi
Programma della I parte Cenni alla meccanica quantistica: il modello dell atomo Dall atomo ai cristalli: statistica di Fermi-Dirac il modello a bande di energia popolazione delle bande livello di Fermi
LA STRUTTURA DELLE MOLECOLE. Meccanica Quantistica e Orbitali Atomici
 LA STRUTTURA DELLE MOLECOLE Meccanica Quantistica e Orbitali Atomici LE MOLECOLE Le molecole sono i costituenti di tutta la materia e possono essere considerate degli oggetti costruiti con componenti chiamati
LA STRUTTURA DELLE MOLECOLE Meccanica Quantistica e Orbitali Atomici LE MOLECOLE Le molecole sono i costituenti di tutta la materia e possono essere considerate degli oggetti costruiti con componenti chiamati
mvr = n h e 2 r = m v 2 e m r v = La configurazione elettronica r = e 2 m v 2 (1) Quantizzazione del momento angolare (2) 4 πε.
 La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
La configurazione elettronica Modello atomico di Bohr-Sommerfeld (1913) Legge fondamentale della meccanica classica F = m a. F Coulomb = 1 4 πε. q q ' F r centrifuga = m v r ε =8.85*10-1 Fm-1 (costante
MECCANICA QUANTISTICA. Corso di laurea in fisica PROGRAMMA DEL CORSO E PROGRAMMA D ESAME. Anno accademico 2011/2012
 MECCANICA QUANTISTICA Corso di laurea in fisica PROGRAMMA DEL CORSO E PROGRAMMA D ESAME Anno accademico 2011/2012 Argomenti facenti parte del programma d esame. Argomenti facenti parte del programma d
MECCANICA QUANTISTICA Corso di laurea in fisica PROGRAMMA DEL CORSO E PROGRAMMA D ESAME Anno accademico 2011/2012 Argomenti facenti parte del programma d esame. Argomenti facenti parte del programma d
Il legame chimico. Legame metallico
 Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
14 Moto vibrazionale delle molecole. Moto vibrazionale di molecole biatomiche (in assenza di rotazioni)
 14 Moto vibrazionale delle molecole Moto vibrazionale di molecole biatomiche (in assenza di rotazioni) 1 Modello analitico dell energia potenziale: potenziale di Morse ( r r ) V( r ) = D 1 e e e α Equazioni
14 Moto vibrazionale delle molecole Moto vibrazionale di molecole biatomiche (in assenza di rotazioni) 1 Modello analitico dell energia potenziale: potenziale di Morse ( r r ) V( r ) = D 1 e e e α Equazioni
Modelli atomici Modello atomico di Rutheford Per t s d u i diare la t s rutt ttura t a omica Ruth th f or (
 Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Modello atomico di Rutheford Per studiare la struttura tt atomica Rutherford (1871-1937) 1937) nel 1910 bombardòb una lamina d oro con particelle a (cioè atomi di elio) Rutherford suppose che gli atomi
Effetto Stark (1) H 0 nlm > = E n nlm > (4) Ricordiamo che. E n = me4 2 h 2 n 2 = E 1
 Effetto Stark Studiamo l equazione di Schrödinger per l atomo di idrogeno in presenza di un campo elettrico costante e diretto lungo l asse z, E = E k. La hamiltoniana di Schrödinger per l atomo di idrogeno
Effetto Stark Studiamo l equazione di Schrödinger per l atomo di idrogeno in presenza di un campo elettrico costante e diretto lungo l asse z, E = E k. La hamiltoniana di Schrödinger per l atomo di idrogeno
Interazione luce- atomo
 Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Università Primo Levi
 Università Primo Levi Primo Levi 2013 Le forze fondamentali e la fisica dei quanta INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
Università Primo Levi Primo Levi 2013 Le forze fondamentali e la fisica dei quanta INAF Osservatorio Astronomico di Bologna via Ranzani, 1 40127 - Bologna - Italia Tel, 051-2095721 Fax, 051-2095700 http://www.bo.astro.it/~bedogni/primolevi
Metalli come gas di elettroni liberi
 Metalli come gas di elettroni liberi I metalli sono caratterizzati da elevata conducibilità elettrica e termica. La conducibilità elettrica in particolare (o il suo inverso, la resistività) è una delle
Metalli come gas di elettroni liberi I metalli sono caratterizzati da elevata conducibilità elettrica e termica. La conducibilità elettrica in particolare (o il suo inverso, la resistività) è una delle
Lezione 8. Cenni di struttura della materia
 Lezione 8 Cenni di struttura della materia Struttura della materia La meccanica, di cui ci siamo occupati finora, ha studiato il moto di corpi solidi sotto l azione di forze generiche e in particolare
Lezione 8 Cenni di struttura della materia Struttura della materia La meccanica, di cui ci siamo occupati finora, ha studiato il moto di corpi solidi sotto l azione di forze generiche e in particolare
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno:
 La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
La Teoria dell Atomo di Bohr Modello di Bohr dell atomo di idrogeno: Vedi documento Atomo di Bohr.pdf sul materiale didattico per la derivazione di queste equazioni Livelli Energetici dell Atomo di Idrogeno
Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein. Assorbimento
 Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein Emissione Spontanea b Assorbimento b Emissione Stimolata b a a a -Energia del fotone (Emesso/Assorbito) uguale alla
Interazione Radiazione materia (intro) Sistema a due livelli e coefficienti di Einstein Emissione Spontanea b Assorbimento b Emissione Stimolata b a a a -Energia del fotone (Emesso/Assorbito) uguale alla
Già con l atomo di Elio l interazione e-e non poteva essere trattata in termini perturbativi perchè molto grande.
 Atomi a multi elettroni Già con l atomo di Elio l interazione e-e non poteva essere trattata in termini perturbativi perchè molto grande. Nel caso di atomi a multi elettroni questa approssimazione è ancora
Atomi a multi elettroni Già con l atomo di Elio l interazione e-e non poteva essere trattata in termini perturbativi perchè molto grande. Nel caso di atomi a multi elettroni questa approssimazione è ancora
INSIEMI DI FUNZIONI DI BASE (BASIS SETS)
 INSIEMI DI FUNZIONI DI BASE (BASIS SETS Basi: insiemi di funzioni {χ} utilizzati per rappresentare gli orbitali molecolari φ i. converge se le {χ p } costituiscono un "insieme completo. Ci sono infinite
INSIEMI DI FUNZIONI DI BASE (BASIS SETS Basi: insiemi di funzioni {χ} utilizzati per rappresentare gli orbitali molecolari φ i. converge se le {χ p } costituiscono un "insieme completo. Ci sono infinite
Gli argomenti trattati
 LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
1 3 STRUTTURA ATOMICA
 1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
1 3 STRUTTURA ATOMICA COME SI SPIEGA LA STRUTTURA DELL ATOMO? Secondo il modello atomico di Rutherford e sulla base della fisica classica, gli elettroni dovrebbero collassare sul nucleo per effetto delle
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L
 IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
Teoria Atomica Moderna. Chimica generale ed Inorganica: Chimica Generale. sorgenti di emissione di luce. E = hν. νλ = c. E = mc 2
 sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
sorgenti di emissione di luce E = hν νλ = c E = mc 2 FIGURA 9-9 Spettro atomico, o a righe, dell elio Spettri Atomici: emissione, assorbimento FIGURA 9-10 La serie di Balmer per gli atomi di idrogeno
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
Capitolo 8 I LEGAMI CHIMICI Aspetti elettrostatici ed energetici dei legami chimici
 Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
FORZE INTERMOLECOLARI
 FORZE INTERMOLECOLARI Oltre alle forze intramolecolari (legami) esistono nella materia forze intermolecolari (tra molecole diverse), anch esse dovute ad interazioni elettrostatiche. Le forze intermolecolari
FORZE INTERMOLECOLARI Oltre alle forze intramolecolari (legami) esistono nella materia forze intermolecolari (tra molecole diverse), anch esse dovute ad interazioni elettrostatiche. Le forze intermolecolari
= GEOMETRIA MOLECOLARE. (numero di legami) + (angolo di legame) = geometria. V.S.E.P.R.: Valence Shell Electron Pair Repulsion
 GEOMETRIA MOLECOLARE I legami covalenti sono direzionali I metodi sperimentali moderni permettono di conoscere sia la DISTANZA di legame (d) che l ANGOLO di legame (α), quindi una buona teoria del legame
GEOMETRIA MOLECOLARE I legami covalenti sono direzionali I metodi sperimentali moderni permettono di conoscere sia la DISTANZA di legame (d) che l ANGOLO di legame (α), quindi una buona teoria del legame
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 14 Le nuove teorie di legame 3 Sommario 1. I limiti della teoria di Lewis 2. Il legame chimico secondo la meccanica quantistica
Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti).
 4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
4. ORBITALI ATOMICI Energia degli orbitali atomici Nell'atomo l'energia dell'elettrone varia per quantità discrete (quanti). Il diagramma energetico dell'atomo di idrogeno: i livelli (individuati da n)
ORBITALE ATOMICO. Forma
 L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
Elettronica II L equazione di Schrödinger p. 2
 Elettronica II L equazione di Schrödinger Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/ liberali
Elettronica II L equazione di Schrödinger Valentino Liberali Dipartimento di Tecnologie dell Informazione Università di Milano, 26013 Crema e-mail: liberali@dti.unimi.it http://www.dti.unimi.it/ liberali
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR)
 TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
Struttura atomica, configurazione elettronica e periodicità chimica
 Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
Chimica Computazionale
 Chimica Computazionale Ottimizzazione della geometria A.A. 2013-14 Bartolomeo Civalleri Dip. Chimica IFM Via P. Giuria 5 10125 Torino bartolomeo.civalleri@unito.it B. Civalleri Chimica Computazionale a.a.
Chimica Computazionale Ottimizzazione della geometria A.A. 2013-14 Bartolomeo Civalleri Dip. Chimica IFM Via P. Giuria 5 10125 Torino bartolomeo.civalleri@unito.it B. Civalleri Chimica Computazionale a.a.
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
FISICA delle APPARECCHIATURE per RADIOTERAPIA
 Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
Anno Accademico 2012-2013 Corso di Laurea in Tecniche Sanitarie di Radiologia Medica per Immagini e Radioterapia FISICA delle APPARECCHIATURE per RADIOTERAPIA Marta Ruspa 20.01.13 M. Ruspa 1 ONDE ELETTROMAGNETICHE
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR)
 TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta e quantitativa della struttura elettronica delle molecole,
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta e quantitativa della struttura elettronica delle molecole,
2.1.1 Approssimazione di Born e Oppenheimer
 60 CAPITOLO. FISICA MOLECOLARE di massa m, carica e eposizione~r e,è,inunitàatomiche, M r A M r B r e ~r e ~ RA ~r e RB ~ + R ~ A RB ~ (.) Supponiamo fin dall inizio che il centro di massa della molecola
60 CAPITOLO. FISICA MOLECOLARE di massa m, carica e eposizione~r e,è,inunitàatomiche, M r A M r B r e ~r e ~ RA ~r e RB ~ + R ~ A RB ~ (.) Supponiamo fin dall inizio che il centro di massa della molecola
Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O?
 IL LEGAME CHIMICO Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O? Configurazione degli elettroni diversa ed energeticamente più favorevole di quella degli atomi isolati? Ionico (trasferimento di
IL LEGAME CHIMICO Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O? Configurazione degli elettroni diversa ed energeticamente più favorevole di quella degli atomi isolati? Ionico (trasferimento di
