Il trasporto dell ossigeno
|
|
|
- Cristina Ferretti
- 10 anni fa
- Просмотров:
Транскрипт
1 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene ad opera di PIGMETI RESPIRATORI Proteine coniugate con metalli che legano O 2, lo trasportano attraverso i fluidi, lo convogliano nei tessuti dove viene rilasciato ed utilizzato. V 1.9 gsartor Il trasporto dell ossigeno - 2-1
2 I pigmenti respiratori Pigmento Colore Struttura Sito per O 2 Localizzazione Mioglobina (Mb) - Proteina Eme Fe ++ 1O 2 /1Fe ++ Muscolo Emoglobina (Hb) Rosso Proteina Eme Fe ++ 1O 2 /1Fe ++ Globuli rossi Soluzione Clorocruorina (Ch) Verde Proteina Eme Fe ++ 1O 2 /1Fe ++ Soluzione Emeritrina (Hr) Violetto Incolore Proteina Fe ++ 1O 2 /2Fe ++ Soluzione (Globuli rossi) Emocianina (Hc) Blu Incolore Proteina Cu ++ 1O 2 /2Cu ++ Soluzione V 1.9 gsartor Il trasporto dell ossigeno I pigmenti respiratori Pigmento Mioglobina (Mb) Emoglobina (Hb) Clorocruorina (Ch) Emeritrina (Hr) Emocianina (Hc) V 1.9 gsartor Il trasporto dell ossigeno - 4-2
3 Proteine multimeriche I pigmenti respiratori dedicati al trasporto dell ossigeno sono formati da più subunità: Mioglobina, immagazzina O 2, una subunità Emoglobina, trasporta O 2, da 2 a 10 subunità a secondo dell organismo Emocianina, trasporta O 2, da 1 6 subunità a 8 6 subunità a secondo dell organismo La presenza di più subunità rende il legame dell O 2 cooperativo permettendone un trasporto efficiente. V 1.9 gsartor Il trasporto dell ossigeno Aria Perché i pigmenti respiratori Volume occupato da 1 mole di gas: 22.4 L (STP) Contenuto di gas in 1 litro di aria: 1/22.4 = moli = 45 mmoli Solo 21% dei gas dell aria è O 2, quindi 45 21/100 = 9.5 mmoli Acqua o plasma Solubilità di O 2 in acqua (α): 1.4 x 10-6 moli L -1 mmhg -1 (a 37 C) [O 2 ] = α x PO 2 = 1.4 x 10-6 x 150 = moli o 0.21 mmoli Emoglobina (160 g/l, globuli rossi concentrati) PM = 16,000 [Hb ]= 160/16,000 = 10 mm Sangue (50% plasma + 50% globuli rossi) Plasma: [O 2 ] = 0.21 mm Emoglobina: [O 2 ] = 10 mm Sangue: [O 2 ] = ( ) + (10 0.5) = = mmoli (2% + 98%) 98% dell O 2 del sangue è legato a Hb, 2% è disciolto nel plasma. V 1.9 gsartor Il trasporto dell ossigeno - 6-3
4 Cellule specializzate Globuli rossi Prive di nucleo Alto contenuto in Hb Previene l effetto osmotico V 1.9 gsartor Il trasporto dell ossigeno Legame con l ossigeno Dipende da po 2 Alta po 2 PR + O 2 PR-O 2 O SATURATO Bassa po 2 SATURATO V 1.9 gsartor Il trasporto dell ossigeno - 8-4
5 Legame con l ossigeno Dipende da po 2 V 1.9 gsartor Il trasporto dell ossigeno Mioglobina ed Emoglobina Le funzioni biologiche delle due proteine sono diverse: Mioglobina: lega strettamente l O 2 e lo rende disponibile SOLO quando la po 2 èmolto bassa (muscolo, cetacei in immersione). Emoglobina: lega l O 2 quando la po 2 è alta (polmoni, branchie) rilascia l O 2 quando la po 2 è bassa (tessuti, cellule). La struttura delle due proteine è diversa: Mioglobina: monomero con gruppo prostetico (eme) che complessa uno ione Fe 2+. Emoglobina: tetramero (nei mammiferi) fatto di subunità (α 2 β 2 ) ognuna delle quali è simile alla mioglobina e contiene un gruppo prostetico (eme) che complessa uno ione Fe 2+. V 1.9 gsartor Il trasporto dell ossigeno
6 Mioglobina e emoglobina V 1.9 gsartor Il trasporto dell ossigeno Mioglobina Trasporto dell O 2, immagazzinamento nella cellula. Due parti: proteina gruppo prostetico Proteina: 155 aminoacidi, ~ 17 kda. Compatta, globina. 75% α-elica. V 1.9 gsartor Il trasporto dell ossigeno
7 Mioglobina Trasporto dell O 2, immagazzinamento nella cellula. Due parti: proteina gruppo prostetico Proteina: 155 aminoacidi, ~ 17 kda. Compatta, globina. 75% α-elica. V 1.9 gsartor Il trasporto dell ossigeno Gruppo eme Il gruppo eme è composta di porfirina e Fe 2+. La porfirina è un gruppo non polare, ci sono inoltre due gruppi polari di propionato. La porfirina lega O 2, CO. CO è 10,000 volte più affine alla porfirina del O 2. Propionato O O O O CH 3 CH 3 Fe ++ CH 3 CH2 CH 3 CH 2 Fe ++ V 1.9 gsartor Il trasporto dell ossigeno
8 Gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ligando Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. V 1.9 gsartor Il trasporto dell ossigeno Gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ligando Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. V 1.9 gsartor Il trasporto dell ossigeno
9 Gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ligando Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. V 1.9 gsartor Il trasporto dell ossigeno Gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ligando Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. V 1.9 gsartor Il trasporto dell ossigeno
10 Gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ligando Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. V 1.9 gsartor Il trasporto dell ossigeno Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. O O V 1.9 gsartor Il trasporto dell ossigeno
11 Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. V 1.9 gsartor Il trasporto dell ossigeno Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. O C V 1.9 gsartor Il trasporto dell ossigeno
12 Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. V 1.9 gsartor Il trasporto dell ossigeno Interazione eme proteina Il gruppo eme stabilizza il ripiegamento della proteina. Il legame è del tipo interazione idrofobica. I gruppi propionato sono presenti nella superficie. Gruppi carbossilici del propionato V 1.9 gsartor Il trasporto dell ossigeno
13 Mioglobina La proteina circonda completamente il gruppo eme. Funzione della proteina: aumentare la solubilità del gruppo eme. Impedisce l ossidazione del gruppo eme (Fe 2+ Fe 3+ ) La metamioglobina (Fe 3+ ) è inattiva. Diminuisce il legame di CO. V 1.9 gsartor Il trasporto dell ossigeno Ossidazione del Fe ++ Il legame del Fe ++ attraverso la proteina impedisce l ossidazione a Fe +++ a seguito del legame con l ossigeno: 2 eme-fe ++ + ½ 2O 2 + 2H + 2 eme-fe H 2 O O Fe++ 2 Fe ++ + ½ O 2 + 2H + 2 Fe H 2 O Fe ++ O V 1.9 gsartor Il trasporto dell ossigeno
14 Ossidazione del Fe ++ Il legame del Fe ++ attraverso la proteina impedisce l ossidazione a Fe +++ a seguito del legame con l ossigeno: 2 eme-fe ++ + ½ 2O 2 + 2H + 2 eme-fe H 2 O O Fe++ 2 Fe ++ + ½ O 2 + 2H + 2 Fe H 2 O Fe ++ O V 1.9 gsartor Il trasporto dell ossigeno Emoglobina, enzima honoris causa In tutti gli animali superiori il metabolismo è aerobico, Assunzione diretta di O 2 efficace solo in organismi unicellulari, Emoglobina (Hb): trasporta O 2 dai polmoni ai tessuti, Mioglobina (Mb): presente nei tessuti muscolari, funge da deposito di O 2, Se non ci fosse Hb, il cuore dovrebbe pompare sangue ad un flusso >100 maggiore. Ci sono organismi superiori che non hanno emoglobina? V 1.9 gsartor Il trasporto dell ossigeno
15 Pesci antartici Temperatura corporea bassa ( 1.7 C) l acqua salata congela a 1.8 C Solubilità O 2 0.3% Basso metabolismo essun pigmento respiratorio Risparmio di sintesi proteica Bassa viscosità del sangue Facile da pompare Poca spesa energetica V 1.9 gsartor Il trasporto dell ossigeno obel V 1.9 gsartor Il trasporto dell ossigeno
16 Il colore del sangue Il colore della proteina è diverso a seconda del fatto che l ossigeno sia o no legato al Fe ++. V 1.9 gsartor Il trasporto dell ossigeno Il colore del sangue Deossiglobine Ossiglobine Carbossiglobine Metaglobine V 1.9 gsartor Il trasporto dell ossigeno
17 Mioglobina e emoglobina V 1.9 gsartor Il trasporto dell ossigeno Similarità strutturale Emoglobina e mioglobina Le quattro subunità della emoglobina sono strutturalmente simili alla mioglobina, Il legame con l ossigeno avviene sempre attraverso lo ione Fe ++ del gruppo eme V 1.9 gsartor Il trasporto dell ossigeno
18 Emoglobina Proteina tetramerica Dimero di dimeri, (αβ) 2 Le catene α, β sono simili alla Mb. Ogni catena contiene un gruppo eme. Ogni gruppo eme lega un O 2. L interfaccia αβ è diversa dall interfaccia αα e ββ. Legami a ponte salino stabilizzano la struttura deossi. V 1.9 gsartor Il trasporto dell ossigeno Il legame con l ossigeno ella mioglobina Mb + O 2 MbO 2 K D = [Mb] [O 2 ] [MbO 2 ] Si definisce la saturazione frazionale (γo 2 ) la frazione di siti che hanno ossigeno legato: γo 2 = [MbO 2 ] [Mb] + [O 2 ] γo 2 = [O 2 ] K D + [O 2 ] V 1.9 gsartor Il trasporto dell ossigeno
19 Il legame con l ossigeno ell emoglobina O 2 O 2 O 2 O 2 Hb Hb(O 2 ) Hb(O 2 ) 2 Hb(O 2 ) 3 Hb(O 2 ) 4 O 2 O 2 O 2 O 2 K D = [Hb] [O 2 ]n [Hb(O 2 ) n ] Si definisce la saturazione frazionale (γo 2 ) la frazione di siti che hanno ossigeno legato: γo 2 = n[hb(o 2 ) n ] n([hb] + [Hb(O 2 ) n ] γo 2 = [O 2 ] n K D + [O 2 ] n V 1.9 gsartor Il trasporto dell ossigeno Saturazione e po 2 HbO 2 /(Hb+HbO 2 ), % o unità 100% P 0.5 = 3 mmhg Mioglobina Emoglobina P 0.5 = mmhg 50% 0% 0 P Pressione parziale di O 2 o tensione di O 2 o po 2 (mmhg, torr o kpa) V 1.9 gsartor Il trasporto dell ossigeno
20 Cooperatività γo 2 = [O 2 ] n K D + [O 2 ] n n = costante di Hill n = 1 nessuna cooperatività n > 1 cooperatività positiva n < 1 cooperatività negativa Per l emoglobina n 2.5 V 1.9 gsartor Il trasporto dell ossigeno Legame dell ossigeno a Hb: Cooperatività Il legame dell ossigeno alla Hb nello stato deossi avviene con una data affinità (K D ) Le molecole di ossigeno che si legano successivamente hanno un affinità maggiore per il sito di legame. Ciò viene definito come cooperatività positiva. Avviene solo in proteine multimeriche. Il coefficiente di Hill ha un valore vicino al numero delle subunità. Il vantaggio è che l affinità del legame è sensibile a piccole variazioni in concentrazioni del ligando. V 1.9 gsartor Il trasporto dell ossigeno
21 Immagazzinamento e trasporto La mioglobina è un ottimo sistema per immagazzinare O 2 : riesce a caricarsi di ossigeno anche a bassi valori di po 2 per tenerlo strettamente legato P 0.5 (γo 2 = 0.5) a po 2 = 2.8 torr. L emoglobina è un ottimo sistema per trasportare l O 2 : Si carica di O 2 quando po 2 è alta, cede O 2 quando po 2 è basso P 0.5 (γo 2 = 0.5) a po 2 = torr. V 1.9 gsartor Il trasporto dell ossigeno HbO 2 /(Hb+HbO 2 ) Saturazione 100% O 2 ceduto da MbO 2 O 2 ceduto da Hb(O 2 ) n 0% 0 Sangue venoso Sangue arterioso po 2 (mmhg) V 1.9 gsartor Il trasporto dell ossigeno
22 Modello Molecolare ello stato deossi il Fe ++ è fuori dal piano del gruppo eme. Il legame con O 2, sposta il Fe ++. Trascina la His prossimale e l elica. Il movimento altera l interfaccia α/β Å His93 (prossimale) His64 (distale) H T Fe++ H 0.33 Å Piano del gruppo eme H Fe++ O O His64 (distale) H His93 (prossimale) 0.22 Å R Stato deossi = stato T (Tense) Stato ossi = stato R (Relaxed) V 1.9 gsartor Il trasporto dell ossigeno Modello Molecolare L alterazione dell interfaccia α/β provoca la variazione dell affinità nelle subunità adiacenti Å His93 (prossimale) His64 (distale) H Fe++ H 0.33 Å Piano del gruppo eme H Fe++ O O His64 (distale) H His93 (prossimale) 0.22 Å Stato deossi = stato T (Tense) Stato ossi = stato R (Relaxed) T R V 1.9 gsartor Il trasporto dell ossigeno
23 V 1.9 gsartor Il trasporto dell ossigeno α 2 β 1 β 2 α 1 V 1.9 gsartor Il trasporto dell ossigeno
24 α 2 β 1 β 2 α 1 V 1.9 gsartor Il trasporto dell ossigeno Deossiemoglobina V 1.9 gsartor Il trasporto dell ossigeno
25 Ossiemoglobina V 1.9 gsartor Il trasporto dell ossigeno Transizione T R ella transizione fra lo stato T (deossigenata) e lo stato R (ossigenata) la coppia di subunità α 1 β 1 si comporta come un unica subunità. V 1.9 gsartor Il trasporto dell ossigeno
26 Transizione T R α 2 β 1 α 2 β 1 I maggiori riarrangiamenti avvengono all interfaccia tra i due dimeri α 2 /β 1 e α 1 /β 2. V 1.9 gsartor Il trasporto dell ossigeno Transizione T R ella proteina deossigenata esiste un legame idrogeno tra Asp nell elica e His amino terminale. Il piccolo movimento causato dal legame con l ossigeno viene amplificato attraverso una ridistribuzione dei legami idrogeno all interfaccia α 2 /β 1 V 1.9 gsartor Il trasporto dell ossigeno
27 Transizione T R His146 Asp94 His146 Asp94 Il legame dell ossigeno sposta lo ione Fe ++ il quale si trascina l elica e si rompe il legame idrogeno tra Asp94 e His146. V 1.9 gsartor Il trasporto dell ossigeno Transizione T R α 2 stato T α 2 stato R β 1 stato R β 1 stato R Cambia quindi la distribuzione dei legami idrogeno all interfaccia α/β e cambia quindi lo stato della subunità adiacente che passa da T a R con aumento dell affinità per O 2. V 1.9 gsartor Il trasporto dell ossigeno
28 V 1.9 gsartor Il trasporto dell ossigeno Dimeri Zoom In Zoom Out Coop V 1.9 gsartor Il trasporto dell ossigeno
29 Regolazione ph Effetto Bohr Effetto Root CO 2 Formazione di bicarbonato, (anidrasi carbonica) Formazione di carbammati Cl - Scambio Cl - /HCO 3 - Formazione di ponti salini Composti fosforilati 2,3 bifosfoglicerato Inositoli fosfati ATP, GTP V 1.9 gsartor Il trasporto dell ossigeno Effetto Bohr L affinità per l O 2 è sensibile al ph. ph acido; diminuzione dell affinità. Il ponte salino tra Asp94 e His146 si forma solo nello stato T. L eccesso di H + forma il ponte salino e favorisce lo stato deossi. His146 Asp94 1 γo ph = 7.5 ph = 7.2 ph = po 2 V 1.9 gsartor Il trasporto dell ossigeno
30 CO 2 ed effetto Bohr el tessuto La CO 2 è legata alla Hb per formare un carbammato o convertita in bicarbonato dall enzima Anidrasi Carbonica (EC ). Sistema tampone del sangue La Hb lega 2 H + ogni 4 O 2 rilasciati (effetto Bohr). ei polmoni Bassa pco 2 la reazione avviene in senso opposto CO 2 e H + rilasciati da Hb Aumenta l affinità per O 2 CO 2 2CO 2 + H 2 O Anidrasi carbonica EC POLMOI 2H 2 CO 3 2HCO H + 4O 2 SAGUE Hb 4O 2 Hb 2H + TESSUTO 4O 2 2HCO H + Anidrasi carbonica EC H 2 CO 2CO H 2 O Metabolismo V 1.9 gsartor Il trasporto dell ossigeno HbH + O 2 H + + Hb-H-COO - HbO 2 + H + HCO H + HbO 2 Hb-H 2 + O 2 Anidrasi carbonica EC H 2 O + CO 2 CO 2 CO 2 Krebs Ciclo di HbO 2 Hb + O 2 O 2 ADH ADP Hb + Cl - HbCl - H 2 O AD + K + ATP HCO 3 - Cl - Lento a + H 2 O + CO 2 V 1.9 gsartor Il trasporto dell ossigeno
31 Anidrasi carbonica V 1.9 gsartor Il trasporto dell ossigeno Effetto Root ei mammiferi l aumento di acidità provoca l effetto Bohr con una diminuzione di affinità per O 2 attraverso un aumento della K m apparente, ei pesci l aumento di acidità provoca anche l effetto Root con una diminuzione della massima quantità di O 2 che si può legare (varia la V max apparente). L acidosi, metabolica (acido lattico) o respiratoria (CO 2 ) porta ad una riduzione dell affinità dell Hb per O 2, IMPORTATE PER IL RIEMPIMETO DELLA VESCICA ATATORIA. Root RW. The respiratory function of the blood of marine fishes. Biol Bull 61: , V 1.9 gsartor Il trasporto dell ossigeno
32 Effetto Borh ed effetto Root V 1.9 gsartor Il trasporto dell ossigeno Emoglobine di pesci Al contrario dei mammiferi nei pesci c è una grande varietà di emoglobine e nel meccanismo di modulazione del legame con l ossigeno per adattarsi alle differenti condizioni ambientali Convenzionalmente le emoglobine dei pesci si dividono in due categorie elletroforetiche: Emoglobine catodiche con punto isoelettrico alto (pi 8) Emoglobine anodiche con punto isolettrico basso (pi 8) Con differenti proprietà di modulazione del legame con l O 2 V 1.9 gsartor Il trasporto dell ossigeno
33 Emoglobine di pesci L anguilla europea (Anguilla anguilla) viene considerata come specie modello con due distinte emoglobine: Una Hb catodica la cui affinità con l O 2 è debolmente influenzata dal ph (piccolo effetto Bohr) Una Hb anodica che ha una minore affinità per l O 2 e con un grande effetto Bohr e Root. Oltre a nuotare, striscia. V 1.9 gsartor Il trasporto dell ossigeno Effetto Root e galleggiamento Il gas che riempie la vescica natatoria è principalmente O 2 La Hb dei pesci è estremamente sensibile all acidità, l ambiente acido a causa della produzione di acido lattico o CO 2 Il valore della costante di Hill, n γo 2 = [O 2 ] n K D + [O 2 ] n diminuisce fino a valori al disotto dell unità (cooperatività negativa) con rilascio (fino al 80%) dell ossigeno legato all Hb in prossimità della vescica natatoria. V 1.9 gsartor Il trasporto dell ossigeno
34 H 2 O + CO 2 AnCarb H + + HCO 3 - H + + HbO 2 HHb + O 2 Cl - Sangue HCO 3 - Cl - H + H+ H + + HCO 3 - H 2 O + CO 2 AnCarb Endotelio ADP ATP Glucoso a + H + Lattato + H + GlicolisiG6P Piruvato CO 2 Cellule della ghiandola del gas Krebs PPO Lume della vescica natatoria O 2 Adattato da:the Generation of Hyperbaric Oxygen Tensions in Fish. Bernd Pelster. ews Physiol. Sci. (2001), 16, V 1.9 gsartor Il trasporto dell ossigeno Effetto Bohr ed effetto Root L aumento di acidità nei mammiferi provoca l effetto Bohr con una diminuzione di affinità per O 2 (varia la K m apparente), In altri organismi (pesci) l aumento di acidità provoca l effetto Root con una diminuzione della massima quantità di O 2 che si può legare (varia la V max apparente). V 1.9 gsartor Il trasporto dell ossigeno
35 Modulazione ed adattamento In altura Composti fosforilati Il 2,3 bifosfoglicerato (2,3-BPG) è un sottoprodotto della glicolisi. La sua presenza è un segnale di necessità di O 2. Si lega alla forma T nella regione cationica. Una volta legato favorisce la forma deossi, favorisce quindi il rilascio di O 2 al tessuto. V 1.9 gsartor Il trasporto dell ossigeno
36 Altra vista del 2,3-BPG ei mammiferi il 2,3- BPG funziona come una zeppa che favorisce lo stato T dell emoglobina. Forza il rilascio di O 2 nel tessuto. È largamente responsabile dell adattamento all altitudine. V 1.9 gsartor Il trasporto dell ossigeno Altra vista del 2,3-BPG ei mammiferi il 2,3- BPG funziona come una zeppa che favorisce lo stato T dell emoglobina. Forza il rilascio di O 2 nel tessuto. È largamente responsabile dell adattamento all altitudine. V 1.9 gsartor Il trasporto dell ossigeno
37 Composti fosforilati Il 2,3 bifosfoglicerato (2,3-BPG) è un sottoprodotto della glicolisi. La sua presenza è un segnale di necessità di O 2. Si lega alla forma T nella regione cationica. Una volta legato favorisce la forma deossi, favorisce quindi il rilascio di O 2 al tessuto. V 1.9 gsartor Il trasporto dell ossigeno Modulazione In altri organismi (Pesci teleostei, elasmobranchi, rettili ecc.) tale effetto viene provocato da altri composti fosforilati: Inositoli fosfati, ATP, GTP. V 1.9 gsartor Il trasporto dell ossigeno
38 Tutorial Per visualizzare un tutorial su mioglobina ed emoglobina visitare il sito: Utilizzando la versione 4.7 di ETSCAPE completo di plugin CHIME. Entrambi sono scaricabili da: V 1.9 gsartor Il trasporto dell ossigeno Crediti e autorizzazioni all utilizzo Questo materiale è stato assemblato da informazioni raccolte dai seguenti testi di Biochimica: CHAMPE Pamela, HARVEY Richard, FERRIER Denise R. LE BASI DELLA BIOCHIMICA [ISB ] Zanichelli ELSO David L., COX Michael M. I PRICIPI DI BIOCHIMICA DI LEHIGER - Zanichelli GARRETT Reginald H., GRISHAM Charles M. BIOCHIMICA con aspetti molecolari della Biologia cellulare - Zanichelli VOET Donald, VOET Judith G, PRATT Charlotte W FODAMETI DI BIOCHIMICA [ISB ] - Zanichelli E dalla consultazione di svariate risorse in rete, tra le quali: Kegg: Kyoto Encyclopedia of Genes and Genomes Brenda: Protein Data Bank: Rensselaer Polytechnic Institute: Il materiale è stato inoltre rivisto e corretto dalla Prof. Giancarla Orlandini dell Università di Parma alla quale va il mio sentito ringraziamento. Questo ed altro materiale può essere reperito a partire da: oppure da gsartor.org/ Il materiale di questa presentazione è di libero uso per didattica e ricerca e può essere usato senza limitazione, purché venga riconosciuto l autore usando questa frase: Materiale ottenuto dal Prof. Giorgio Sartor Università di Bologna a Ravenna Giorgio Sartor - [email protected] 38
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Struttura delle proteine
 Struttura delle proteine I II III Copyright 2001-2015 by Giorgio Sartor. All rights reserved. Versione 1.0.2 oct 2015 Struttura quaternaria Èil livello di organizzazione per il quale si formano strutture
Struttura delle proteine I II III Copyright 2001-2015 by Giorgio Sartor. All rights reserved. Versione 1.0.2 oct 2015 Struttura quaternaria Èil livello di organizzazione per il quale si formano strutture
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Trasporto dell ossigeno
 Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: [email protected] Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
MOVIMENTO. Motori molecolari. IV Movimento Miosina e actina. Prof. Giorgio Sartor. P04 - Versione 2.0 oct 2013
 Prof. Giorgio Sartor Motori molecolari IV Movimento Miosina e actina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P04 - Versione 2.0 oct 2013 MOVIMENTO Miosina Actina P04 v. 2.0 gsartor
Prof. Giorgio Sartor Motori molecolari IV Movimento Miosina e actina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P04 - Versione 2.0 oct 2013 MOVIMENTO Miosina Actina P04 v. 2.0 gsartor
Fisiologia Renale 3. Equilibrio acido-base: Principi generali e fisico chimica
 Fisiologia Renale 3. Equilibrio acido-base: Principi generali e fisico chimica Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Definizione
Fisiologia Renale 3. Equilibrio acido-base: Principi generali e fisico chimica Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Definizione
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro [email protected]; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro [email protected]; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Funzioni dell apparato respiratorio
 Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Funzioni dell apparato respiratorio -Scambi di O2 e CO2 -Regolazione ph -Protezione da patogeni inalati -Vocalizzazione respirazione Ventilazione Scambi gassosi polmonari Trasporto dei gas respiratori
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
Modulo 4. Una proteina in azione
 Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi
 2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
FISIOLOGIA DELLA RESPIRAZIONE
 FISIOLOGIA DELLA RESPIRAZIONE SCAMBIO E TRASPORTO DEI GAS La composizione dell aria alveolare differisce rispetto all aria ambiente. A livello alveolare si verifica la continua diffusione della del sangue
FISIOLOGIA DELLA RESPIRAZIONE SCAMBIO E TRASPORTO DEI GAS La composizione dell aria alveolare differisce rispetto all aria ambiente. A livello alveolare si verifica la continua diffusione della del sangue
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro [email protected]; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro [email protected]; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
Prof. Giorgio Sartor. Il metabolismo. Metabolismo. È il processo che permette di ricavare energia da legami chimici (sottoforma di
 Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
MACROSTRUTTURA DEL MUSCOLO STRIATO SCHELETRICO
 FUNZIONE DEL MUSCOLO SCHELETRICO Ultrastruttura della cellula muscolare. Miofilamenti. Meccanismo della contrazione. Trasmissione neuromuscolare. Scossa semplice e tetano muscolare. Unità motoria. PROPRIETA
FUNZIONE DEL MUSCOLO SCHELETRICO Ultrastruttura della cellula muscolare. Miofilamenti. Meccanismo della contrazione. Trasmissione neuromuscolare. Scossa semplice e tetano muscolare. Unità motoria. PROPRIETA
unità C2. Le trasformazioni energetiche nelle cellule
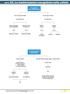 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
EMOGLOBINA (Hb) nei globuli rossi e
 Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Il Sistema Respiratorio. Fisica Medica
 Il Sistema Respiratorio La respirazione Trachea Bronchi Muscoli del diaframma I muscoli che controllano la respirazione fanno variare volume e pressione interna ai polmoni Fase Inspirazione Espirazione
Il Sistema Respiratorio La respirazione Trachea Bronchi Muscoli del diaframma I muscoli che controllano la respirazione fanno variare volume e pressione interna ai polmoni Fase Inspirazione Espirazione
Attivitá e cinetica enzimatica
 Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE
 FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
FISIOPATOLOGIA dell EQUILIBRIO ACIDO-BASE ACIDO = molecola contenente atomi di idrogeno capaci di rilasciare in soluzione ioni idrogeno (H( + ) BASE = ione o molecola che può accettare uno ione idrogeno
gruppo prostetico) Cromoproteine Legare l ossigeno Impedire che ossidi altre sostanze Cedere O 2 in particolari e ben definite condizioni
 Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
Le proteine globulari: mioglobina ed emoglobina Caratteristiche generali Forma: sferoidale Solubilità: acqua Struttura: terziaria e, spesso, quaternaria Classificazione: caratteristiche chimico-fisiche
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma
 Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
Lezione 4 *membrana cellulare *trasporti *specializzazioni del plasmalemma Lezione 3 membrana cellulare Le membrane, sia quelle che delimitano e costituiscono gli organuli cellulari che quelle che rivestono
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Dalla Chimica Generale
 RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
RISNANZA RISNANZA Vi sono molecole le cui proprietà non sono ben spiegate da una singola struttura di Lewis che tenga conto cioé delle proprietà osservate (contenuto energetico, lunghezza dei legami, comportamento
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO
 EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
METABOLISMO E SISTEMI ENERGETICI
 METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
GLICOGENOLISI & GLICOGENOSINTESI
 GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
Istituto di Istruzione Superiore L. da Vinci Civitanova Marche. Anno scolastico 2014-2015. Programma svolto. Docente: Silvana Venditti
 Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Anno scolastico 2014-2015 Programma svolto Docente: Silvana Venditti Disciplina: Scienze Naturali Classe : IV sez. E - Indirizzo Linguistico ARTICOLAZIONE DEI CONTENUTI E DEGLI OBIETTIVI SECONDO UNITA
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Le proteine che legano ossigeno:
 Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
FUNZIONI DEI MITOCONDRI
 FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
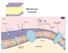 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare.
 Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
MEMBRANE. MEMBRANE equilibri gas-liquido. elio giroletti
 UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - [email protected] - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - [email protected] - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
La pompa Na + /Glucosio: simporto
 MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CARBOSSILAZIONE/OSSIGENAZIONE
 CARBOSSILAZIONE/OSSIGENAZIONE COSA SUCCEDE SE LA TEMPERATURA AUMENTA? LEGGE DI HENRY: a T costante, la quantità di un gas che si scioglie in un dato liquido è proporzionale alla pressione parziale del
CARBOSSILAZIONE/OSSIGENAZIONE COSA SUCCEDE SE LA TEMPERATURA AUMENTA? LEGGE DI HENRY: a T costante, la quantità di un gas che si scioglie in un dato liquido è proporzionale alla pressione parziale del
SENSORI E TRASDUTTORI
 SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
CENNI DI ELETTROCHIMICA
 CENNI DI ELETTROCHIMICA Gli elettrodi a membrana sono elettrodi che permettono la determinazione rapida e selettiva, per potenziometria diretta, di numerosi cationi ed anioni. Il meccanismo di formazione
CENNI DI ELETTROCHIMICA Gli elettrodi a membrana sono elettrodi che permettono la determinazione rapida e selettiva, per potenziometria diretta, di numerosi cationi ed anioni. Il meccanismo di formazione
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
10000 Everest (m 8850) 8000. Monte Bianco (m 4810) 4000. 0 20 40 60 80 100 120 140 160 180 pressione parziale dell O 2 (in mmhg)
 Il ruolo dell ossigeno nel metabolismo Le sostanze nutritive forniscono la loro energia alle cellule attraverso una reazione chimica di ossidazione, analoga alla combustione. Questa reazione, come tutte
Il ruolo dell ossigeno nel metabolismo Le sostanze nutritive forniscono la loro energia alle cellule attraverso una reazione chimica di ossidazione, analoga alla combustione. Questa reazione, come tutte
DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY
 DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY Una reazione acido/base coinvolge un trasferimento di protone: l'acido è il donatore di protone e la base è l'accettore del protone. Questa definizione spiega
DEFINIZIONE ACIDO/BASE SECONDO BRONSTED-LOWRY Una reazione acido/base coinvolge un trasferimento di protone: l'acido è il donatore di protone e la base è l'accettore del protone. Questa definizione spiega
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI
 Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
TEST BIOLOGIA 1 ANNO ABEI Da inviare a [email protected] entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
GIOCHI DELLA CHIMICA
 GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
Regione cerniera monomero regione cerniera
 Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
A livello della loro struttura chimica, come i grassi, anche i carboidrati sono composti ternari, formati cioè da tre molecole:
 I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I GAS GAS IDEALI. PV=nRT. Pressione Volume numero di moli Temperatura Costante dei gas. P V n T R. n, T= cost Legge di Boyle
 I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
