Biochimica Applicata - Monica Stoppini e Vittorio Bellotti - Edises. 19.
|
|
|
- Carlotta Paoletti
- 7 anni fa
- Visualizzazioni
Transcript
1 Testi consigliati Biochimica Applicata - Monica Stoppini e Vittorio Bellotti - Edises. 19. Metodologie Biochimiche - M.C. Bonaccorsi di Patti, R. Contestabile, M.G. Di Salvo - Ambrosiana. 39. Principi di metodologia Biochimica - Carlo De Marco e Chiara Cini - Piccin. Biochimica e Biologia Molecolare. Principi e tecniche - Wilson K, Walker J - Zanichelli. The Protein protocols Handbook - Walker, John M. Biochimica - J. M. Berg, J. L. Tymoczko e L. Stryer. - Zanichelli. Membrane Protein Protocols - Selinsky BS. Metodologie di base per le scienze biomolecolari - Reed R, Holmes D, Weyers J, Jones A. - Zanichelli.
2 Struttura del corso Teoria OBBLIGATORIO Laboratorio ma non la frequenza
3 DISPENSE di BIOCHIMICA APPLICATA L ordine delle dispense può variare, perciò è meglio tenerle separate per argomento.
4 BIOCHIMICA APPLICATA
5 UNITA DI MISURA Prefissi del Sistema Internazionale 10 n Prefisso Simbolo Nome Equivalente decimale yotta Y Quadrilione zetta Z Triliardo exa E Trilione peta P Biliardo tera T Bilione giga G Miliardo mega M Milione kilo o chilo k Mille etto h Cento deca da Dieci deci d Decimo 0, centi c Centesimo 0, milli m Millesimo 0, micro µ Milionesimo 0, nano n Miliardesimo 0, pico p Bilionesimo 0, femto f Biliardesimo 0, atto a Trilionesimo 0, zepto z Triliardesimo 0, yocto y Quadrilionesimo 0,
6 INDAGINE BIOCHIMICA MODERNA Esperimenti Kit commerciali Automatizzazione
7 PRINCIPALI METODOLOGIE BIOCHIMICHE 1. TECNICHE CENTRIFUGATIVE 2. TECNICHE ENZIMATICHE 3. TECNICHE IMMUNOCHIMICHE 4. TECNICHE DI BIOLOGIA MOLECOLARE 5. TECNICHE CROMATOGRAFICHE 6. TECNICHE ELETTROFORETICHE 7. TECNICHE SPETTROSCOPICHE 8. TECNICHE RADIOISOTOPICHE 9. TECNICHE DI SPETTROSCOPIA DI MASSA 10. TECNICHE ELETTROCHIMICHE
8 MICROPIPETTE
9 LE PIPETTE Strumento per dispensare volumi di soluzioni in assenza di una connessione diretta fra i recipienti in uso.
10 «PIPETTARE» Metodo accurato e preciso per trasferire volumi, decisi dall operatore, di liquidi. Pistone mobile
11 AEROSOL: particelle di liquido o solido ( nm) disperse in un gas. PRINCIPIO Contatto diretto Sistema ad aria ideale per soluzioni acquose o poco viscose.
12 PIPETTATA SEMPLICE
13 PIPETTATA A ROVESCIO Per prelievi ripetuti della medesima sostanza.
14 COMPORTAMENTO DI UNO STRUMENTO Preciso, ma non accurato Accurato, ma non preciso Accurato e preciso
15 PROFONDITA DI IMMERSIONE Due problemi opposti: - volume maggiore - aria Taglia della pipetta Immersione Con la giusta profondità l accuratezza incrementa dall 1 al 5%!
16 ANGOLO DI PIPETTATA L accuratezza incrementa dall 1 al 5%!
17 TOLLERANZE Pipette di ditte diverse, hanno caratteristiche differenti. Taglie della pipetta Errore massimo Errore casuale L errore diventa minimo quando si preleva il volume massimo possibile di una pipetta.
18 PUNTALI Generalmente di plastica, economici, intercambiabili. Due parametri: materiale e forma.
19 EIEZIONE DEI PUNTALI Dipende dalla pipetta.
20 PIPETTE MULTICANALE OK
21 I have a dream Channel Multichannel Pipettes
22 TAMPONI Organismi complessi e singole cellule resistono generalmente a grandi variazioni di ph dell ambiente esterno. Al contrario, vi è una forte sensibilità al ph dei processi endocellulari Proprietà finemente regolata (generalmente mantenuto vicino alla neutralità) mediante sistemi tampone.
23 SELEZIONE DEI TAMPONI Utilizzare un tampone con pk a vicina al ph richiesto. Oltre l intervallo di ph = pka 1 la capacità tamponante è scarsa.
24 SELEZIONE DEL TAMPONE SULLA BASE DELLA pka
25 SELEZIONE DEI TAMPONI Assicurarsi che il tampone non causi precipitazioni indesiderate (citrati e fosfati). Per certi enzimi il fosfato di alcuni tamponi è substrato, attivatore o inibitore. Il tris 2-idrossimetil-amminometano cloridrato o TRIS (pka = 8.06 a 20 C, range ph: ) è spesso tossico in sistemi biologici, per la sua solubilità in lipidi.
26 Fluorescenza ESEMPIO DI TAMPONE DANNOSO Più è alta la campana più è efficiente il sistema. Thr gen Pnp+dil.scalari DMSO RFU 6 Pnp DMSO 1/4 DMSO in H2O 1/2 1/8 DMSO // 1/4 4 1/16 DMSO // 1/8 1/32 DMSO // 1/16 1/64 DMSO // 1/32 H2O DMSO pura 1/64 2 Tampone puro Time Tempo (s)
27 RIASSUMENDO Il tampone adatto: 1. pka opportuna. 2. Range di ph sufficiente. 3. Solubilizza le molecole in studio. 4. Non interferisce con la reazione.
28 GOOD S BUFFERS Sono 12 tamponi descritti da Norman Good (1966), basati su molecole zwitterioniche, portate al ph di lavoro con un acido forte o una base forte. - Scelti per aver PK a fra 6 e 8. - Bassa solubilità in solventi non polari. - Chimicamente stabili. - Non attraversano le membrane cellulari. - Non assorbono nell UV-visibile. Buffer pk a at 20 C ΔpK a / C MES ADA PIPES ACES Cholamine chloride BES TES HEPES Acetamidoglycine Tricine Glycinamide Bicine
29 HEPES N-2-Hydroxyethylpiperazine-N -2-ethanesulfonic acid Normalmente neutralizzato con NaOH pk a at 25 C of 7.55 (7.31 at 37 C) a second pk a at ph 3 is not of interest usable buffering range of 6.8 to 8.2 molecular weight HEPES contains tertiary amines, which are reactive under certain conditions. Chemical formula: C 8 H 18 N 2 O 4 S Fototossico: produzione di perossido di idrogeno se esposto a luce solare (riproducibilità a rischio!).
30 DETERGENTI I detergenti sono molecole ANFIPATICHE, ovvero contengono sia gruppi polari (idrofili), sia apolari (idrofobici, lipofili). Alcuni sono naturali, la > parte di sintesi (dal 1836). Proteine transmembrana, se isolate dalle membrane, espongon regioni idrofobiche, causando aggregazione.
31 DETERGENTI Proteine transmembrana, se isolate dalle membrane, espongon regioni idrofobiche, causando aggregazione. I detergenti possono solubilizzare tali proteine avendo affinità per i gruppi idrofobici/idrofilici presenti in esse.
32 CONCENTRAZIONE MICELLARE CRITICA (CMC) Basse Detergente = in H 2 O come molecola isolata. Alte Detergente = forma micelle. Proteine di membrana Concentrazione superiore alla CMC Detergente Concentrazione inferiore alla CMC La CMC è caratteristica di ogni detergente e dipende dalla sua struttura chimica.
33 TIPI DI DETERGENTI NON IONICI: gruppo idrofilo non carico (alchiloamidi, esteri del glucosio e del saccarosio, alchilaminossidi, derivati etossilati). ANIONICI: gruppo idrofilo carico - (alchilsolfati, alcoilsarcoinati, alchilsemisolfuccinati, condensati tra acidi grassi ed aminoacidi). CATIONICI: gruppo idrofilo carico + (sali quaternari di ammonio, sali di piridinio quaternario, sali di isochinolinio quaternario). ANFOTERI: contengono sia un gruppo carico - sia uno carico + (imidazoline e le betaine). Hanno un comportamento diverso a seconda del ph.
34 Triton X-100 DETERGENTI Non ionici: (estrazione DNA) CMC = ~0,2 mm Tween 20 (studi di interazione e funzione) CMC = 0,06 mm Octilglucoside (elettroforesi 2D) C14H28O6 Mr CMC = 14.5 mm
35 DETERGENTI I detergenti ionici, a causa della propria carica, distruggono legami ionici e ponti idrogeno, portando anche alla completa denaturazione una proteina. Anionici: Sodio dodecil solfato (SDS) o sodio laurilsolfato (SLS) C12H25NaO4S Mr g mol 1 CMC = 8.3 mm Usato in prodotti, come dentifricio, shampoo, schiuma da barba e saponi liquidi. La polvere di SDS è molto volatile, irritante per occhi, cute e vie respiratorie. Contatti ripetuti o prolungati posson causar dermatiti. Alla combustione, forma gas tossici.
36 DETERGENTI Cationici: Medio/Alto potere disinfettante, per la capacità di agire sulla membrana esterna dei batteri gram - Cloruro di benzalconio: miscela di cloruri di alchil-benzil-dimetilammonio (largamente presente in colliri e colluttori) Trovano scarsa o nessuna applicazione nei comuni laboratori di biochimica e biologia molecolare.
37 Preparazione di un tampone (1L) pesare H 2 O (~ l 80%) miscelare ph portare a volume
38 FORZA IONICA = 1 cz 2 2 c = concentrazione specie ionica z = carica dello ione L unità di misura di è la molarità. Calcolo della forza ionica di 2 soluzioni: 1) 0.5 M KCl 2) 0.2 M NaCl M Na 2 SO 4
Date importanti. RECUPERI: 17 Marzo (2 ore) - Elettroforesi 2D. 24 Marzo (2 ore) - Purificazioni proteiche.
 Date importanti 9 Marzo Congresso telethon RECUPERI: 17 Marzo (2 ore) - Elettroforesi 2D. 24 Marzo (2 ore) - Purificazioni proteiche. ESCLUSI BIOLOGI LT 30 Marzo (3 ore) - Fast Blot e Ab Fluorescenti.
Date importanti 9 Marzo Congresso telethon RECUPERI: 17 Marzo (2 ore) - Elettroforesi 2D. 24 Marzo (2 ore) - Purificazioni proteiche. ESCLUSI BIOLOGI LT 30 Marzo (3 ore) - Fast Blot e Ab Fluorescenti.
Il metodo scientifico
 Il metodo scientifico Legge Galileo Galilei (1564-1642) Misurare: confrontare una grandezza con l unità di misura di quella grandezza 10 24 yotta Y Quadrilione 10 21 zetta Z Triliardo 10 18 exa E Trilione
Il metodo scientifico Legge Galileo Galilei (1564-1642) Misurare: confrontare una grandezza con l unità di misura di quella grandezza 10 24 yotta Y Quadrilione 10 21 zetta Z Triliardo 10 18 exa E Trilione
Il Sistema Internazionale di unità di misura. Ing. Gianfranco Miele
 Il Sistema Internazionale di unità di misura Ing. Gianfranco Miele g.miele@unicas.it Background Sin dall antichità vi è stata la necessità di definire delle unità campione delle più importanti grandezze
Il Sistema Internazionale di unità di misura Ing. Gianfranco Miele g.miele@unicas.it Background Sin dall antichità vi è stata la necessità di definire delle unità campione delle più importanti grandezze
Appunti di Stechiometria per Chimica GRANDEZZE FISICHE
 Appunti di Stechiometria per Chimica GRANDEZZE FISICHE Una grandezza fisica è una qualunque proprietà della materia che può essere misurata (quantificata). Misurare significa confrontare (rapportare) due
Appunti di Stechiometria per Chimica GRANDEZZE FISICHE Una grandezza fisica è una qualunque proprietà della materia che può essere misurata (quantificata). Misurare significa confrontare (rapportare) due
STRUMENTI ED UNITA' DI MISURA
 STRUMENTI ED UNITA' DI MISURA Si chiama GRANDEZZA qualunque cosa sia suscettibile di essere misurata. Esempi di Grandezza sono la LUNGHEZZA, la MASSA, il TEMPO, l' AREA, il VOLUME. Il PESO, l' INTENSITA'
STRUMENTI ED UNITA' DI MISURA Si chiama GRANDEZZA qualunque cosa sia suscettibile di essere misurata. Esempi di Grandezza sono la LUNGHEZZA, la MASSA, il TEMPO, l' AREA, il VOLUME. Il PESO, l' INTENSITA'
Metodi di studio delle proteine (o altre macromolecole)
 Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Metodi di studio delle proteine (o altre macromolecole) Purificazione Separazione da altri componenti cellulari; determinazione del grado di purezza Studio Determinazione della struttura funzione regolazione
Misurare Grandezze. ( Testo: teoria pag ; esercizi )
 Misurare Grandezze. ( Testo: teoria pag. 53 73; esercizi 131 139) 1) La grandezza. Una grandezza è una quantità che può essere misurata con strumenti di misura. Tutto ciò che non è misurabile non può essere
Misurare Grandezze. ( Testo: teoria pag. 53 73; esercizi 131 139) 1) La grandezza. Una grandezza è una quantità che può essere misurata con strumenti di misura. Tutto ciò che non è misurabile non può essere
c) In quanti modi possono mettersi uno affianco all altro i 21 allievi della vostra classe?
 La notazione scientifica l ordine di grandezza di un numero. 0) Introduzione. Capita frequentemente di dover scrivere grandi o piccoli numeri con un enorme quantità di cifre; vedremo come sia possibile
La notazione scientifica l ordine di grandezza di un numero. 0) Introduzione. Capita frequentemente di dover scrivere grandi o piccoli numeri con un enorme quantità di cifre; vedremo come sia possibile
Soluzioni unità 3, modulo D del libro
 Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
2. La chimica della vita Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA
 Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
L'attività di queste proteine, a sua volta è modulata dalla composizione dei fosfolipidi della membrana
 La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
La funzione di ogni membrana biologica è determinata principalmente dall insieme di proteine integrali incorporate e dalle proteine periferiche collegate alla superficie della membrana L'attività di queste
La Misura Esercizi guida con soluzioni
 La misura Esercizi guida (UbiMath) - 1 La Misura Esercizi guida con soluzioni Grandezze e sistema metrico decimale Scrivi in forma di numerica e come potenza di dieci i seguenti prefissi SI. 1. mega- =
La misura Esercizi guida (UbiMath) - 1 La Misura Esercizi guida con soluzioni Grandezze e sistema metrico decimale Scrivi in forma di numerica e come potenza di dieci i seguenti prefissi SI. 1. mega- =
Alcune informazioni utili
 Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Alcune informazioni utili DATE 12 incontri 10-17-24 ottobre 2016 7-14-21-28 novembre 2016 5-12-19 dicembre 2016 9-16 gennaio 2017 ogni lunedì ORARIO dalle 8.30 alle 10.30 Aula VM1 Dove trovarmi E-mail:
Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto grandi e molto piccoli.
 Elevamento a potenza Potenze del 10, SI e potenze del 2 (UbiMath) - 1 Potenze del 10 e SI Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto
Elevamento a potenza Potenze del 10, SI e potenze del 2 (UbiMath) - 1 Potenze del 10 e SI Particolare importanza assumono le potenze del numero 10, permettendo di semplificare la scrittura di numeri molto
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE
 CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
CORSO DI TIROCINIO FORMATIVO ATTIVO (TFA) CLASSE DI CONCORSO A033 METODOLOGIE DIDATTICHE PER L INSEGNAMENTO DELLA TECNOLOGIA ANNO ACCADEMICO 2014/15 PROF. GIUSEPPE NATALE La misura delle grandezze fisiche
Corso di FISICA. Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci
 Anno accademico 2003/2004 Corso di Laurea in Biologia Cellulare e Molecolare Corso di FISICA Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci LEZIONI martedi ore 9-11
Anno accademico 2003/2004 Corso di Laurea in Biologia Cellulare e Molecolare Corso di FISICA Docente: Prof. M.P. De Pascale Esercitazioni a cura: Prof. L. Narici, Dr.P.Castrucci LEZIONI martedi ore 9-11
FORMULE INVERSE. Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso.
 FORMULE INVERSE FORMULE INVERSE Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso. FORMULE INVERSE Nello studio della fisica si incontrano
FORMULE INVERSE FORMULE INVERSE Nello studio della fisica si incontrano molte formule matematiche e spesso è necessario utilizarle in modo inverso. FORMULE INVERSE Nello studio della fisica si incontrano
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Lipidi. Grassi e Oli Cere Fosfolipidi Eicosanoidi (Prostaglandine, Trombossani, Leucotrieni) Terpeni Steroidi Vitamine solubili nei lipidi
 Lipidi I lipidi sono un gruppo di composti organici, a struttura anche molto diversa, che hanno come comune caratteristica la solubilità in solventi organici (es. etere, cloroformio, acetone e benzene)
Lipidi I lipidi sono un gruppo di composti organici, a struttura anche molto diversa, che hanno come comune caratteristica la solubilità in solventi organici (es. etere, cloroformio, acetone e benzene)
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
GENERALITA SULLA CROMATOGRAFIA
 GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
GENERALITA SULLA CROMATOGRAFIA COSA SONO LE TECNICHE CROMATOGRAFICHE? La cromatografia consiste nello sfruttare la diversa attitudine di ogni molecola o ione nel distribuirsi fra 2 fasi differenti. Una
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
APPUNTI delle lezioni prof. Celino PARTE 1
 APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
APPUNTI delle lezioni prof. Celino PARTE 1 PREREQUISITI MATEMATICI per lo studio della fisica e della chimica... 2 NOTAZIONE SCIENTIFICA... 2 APPROSSIMAZIONE DEI NUMERI DECIMALI... 2 MULTIPLI e SOTTOMULTIPLI...
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Lezione di oggi. Sistema internazionale di unità di misura
 Lezione di oggi Sistema internazionale di unità di misura Processo di misura Risultato di una misurazione = STIMA + INCERTEZZA + U.M. Miglior stima della grandezza che deve essere quantificata Ampiezza
Lezione di oggi Sistema internazionale di unità di misura Processo di misura Risultato di una misurazione = STIMA + INCERTEZZA + U.M. Miglior stima della grandezza che deve essere quantificata Ampiezza
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
TECNOLOGIE BIOMOLECOLARI
 TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
TECNOLOGIE BIOMOLECOLARI Purificazione di DNA da cellule vive Rif. Brown: cap. 3 T. A. Brown, BIOTECNOLOGIE MOLECOLARI, Zanichelli editore S.p.A Copyright 2007 Trattamento dei campioni biologici per l
Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2
 Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2 Esercizio Risposta PAG 40 ES 1 Per permettere un confronto quantitativo tra i dati raccolti da operatori diversi.
Brady Senese Pignocchino Chimica.blu Zanichelli 2013 Soluzione degli esercizi Capitolo 2 Esercizio Risposta PAG 40 ES 1 Per permettere un confronto quantitativo tra i dati raccolti da operatori diversi.
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa
 Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
FISICA. Prof. Enrico Maglione. Dip. Di Fisica, Via Marzolo 8. tel.: web:
 FISICA Prof. Enrico Maglione Dip. Di Fisica, Via Marzolo 8 email: maglione@pd.infn.it tel.: 049-8277189 web: http://www.pd.infn.it/~maglione lucidi http://www.pd.infn.it/~maglione/corso2009 ppt http://www.openoffice.org
FISICA Prof. Enrico Maglione Dip. Di Fisica, Via Marzolo 8 email: maglione@pd.infn.it tel.: 049-8277189 web: http://www.pd.infn.it/~maglione lucidi http://www.pd.infn.it/~maglione/corso2009 ppt http://www.openoffice.org
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
L ACQUA. E il mezzo in cui avvengono le maggiori reazioni. Tutte le molecole biologiche assumono forma e
 L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
GRANDEZZE FISICHE - UNITÀ DI MISURA
 GRANDEZZE FISICHE - UNITÀ DI MISURA DOWNLOAD Il pdf di questa lezione (0227b.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/scamb/ 27/02/2012 2 3 4 UNITÀ DI MISURA Ogni buona unità di misura
GRANDEZZE FISICHE - UNITÀ DI MISURA DOWNLOAD Il pdf di questa lezione (0227b.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/scamb/ 27/02/2012 2 3 4 UNITÀ DI MISURA Ogni buona unità di misura
Funzioni CHIMICA SUPRAMOLECOLARE. Riconoscimento (Sensors Sensori ) Trasporto (Carriers) Trasformazione. Supermolecola. Supermolecule.
 CHIMICA SUPRAMOLECOLARE Sistemi Organizzati Recettore Receptor Substrato Substrate Supermolecola Supermolecule Strumenti Supramolecolari Devices Funzioni Riconoscimento (Sensors Sensori ) Trasformazione
CHIMICA SUPRAMOLECOLARE Sistemi Organizzati Recettore Receptor Substrato Substrate Supermolecola Supermolecule Strumenti Supramolecolari Devices Funzioni Riconoscimento (Sensors Sensori ) Trasformazione
UNITA DI MISURA BASE
 Revisione del 2/9/15 ISTITUTO TECNICO INDUSTRIALE V.E.MARZOTTO Valdagno (VI) Corso di Fisica prof. Nardon UNITA DI MISURA BASE Richiami di teoria Il Sistema Internazionale (S.I.) di unità di misura è composto
Revisione del 2/9/15 ISTITUTO TECNICO INDUSTRIALE V.E.MARZOTTO Valdagno (VI) Corso di Fisica prof. Nardon UNITA DI MISURA BASE Richiami di teoria Il Sistema Internazionale (S.I.) di unità di misura è composto
Genomica e Proteomica
 Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Genomica e Proteomica Genomica: sequenziamento del DNA presente in un organismo e analisi dei geni (bioinformatica) Proteomica: analisi delle proteine di un organismo: Quali proteine in un dato momento
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 5 Maggio 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
OGRAMMA DI CHIMICA 2016
 ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
ISTITUT TO DI ISTRUZIONE SUPERIORE M MARIANO IV D ARBOREA Sede distaccata IPSIA di GHILARZA PRO OGRAMMA DI CHIMICA A.S. 2015-2016 2016 Classe: I sez. A Docenti: Federica Piras, Carmelo Floris PARTE TEORICA
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD
![7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD](/thumbs/59/43238545.jpg) 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
Esercitazioni di Elementi di Chimica. Modulo 3 Trasformazioni della Materia
 Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Parti svolte dal libro di testo Chimica Analitica Quantitativa
 PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2007-2008 E stato seguito il testo: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 mentre
PROGRAMMA DEL CORSO DI CHIMICA ANALITICA 1 CON LABORATORIO a.a. 2007-2008 E stato seguito il testo: Daniel C. Harris, Chimica Analitica Quantitativa, Seconda Edizione Italiana, Ed. Zanichelli, 2005 mentre
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tab 2/1. Grandezze e unità SI fondamentali e supplementari.
 2. UNITA' DI MISURA. R. Mi ha detto che avremmo incontrato spesso la sigla SI. Di che cosa si tratta, esattamente? D. SI è la sigla di Sistema internazionale di unità di misura, in vigore, nei Paesi dell
2. UNITA' DI MISURA. R. Mi ha detto che avremmo incontrato spesso la sigla SI. Di che cosa si tratta, esattamente? D. SI è la sigla di Sistema internazionale di unità di misura, in vigore, nei Paesi dell
Misure e Unità di Misura
 2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
2. La Mole Misure e Unità di Misura L Incertezza delle Misure - come utilizzare le cifre significative nel calcolo Le Quantità Chimiche - la MOLE - la MASSA MOLARE - la misura dei composti La Determinazione
Organizzazione. 6 ore/ settimana: lunedì (15-19) e venerdì (11-13) (+ quando volete - per le esperienze specifiche)
 Laboratorio 1 Livio Fano - Dipartimento di Fisica - V piano 075 585-2751 livio.fano@cern.ch http://www.fisgeo.unipg.it/fano/ ricevimento: contattatemi testi: Introduzione all analisi degli errori - J.
Laboratorio 1 Livio Fano - Dipartimento di Fisica - V piano 075 585-2751 livio.fano@cern.ch http://www.fisgeo.unipg.it/fano/ ricevimento: contattatemi testi: Introduzione all analisi degli errori - J.
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 17 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione
LICEO SCIENTIFICO "FRANCESCO SEVERI" BIOLOGIA
 LICEO SCIENTIFICO "FRANCESCO SEVERI" Programma consuntivo A. S. 2009/2010 Testo utilizzato,volume unico:"invito alla biologia" H.Curtis & N.Sue Barnes Classi 3 A - 3 H - 3 D BIOLOGIA U.D. N 1 COME NACQUE
LICEO SCIENTIFICO "FRANCESCO SEVERI" Programma consuntivo A. S. 2009/2010 Testo utilizzato,volume unico:"invito alla biologia" H.Curtis & N.Sue Barnes Classi 3 A - 3 H - 3 D BIOLOGIA U.D. N 1 COME NACQUE
Tutte le altre grandezze fisiche derivano da queste e sono dette grandezze DERIVATE (es. la superficie e il volume).
 Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
Grandezze fisiche e misure La fisica studia i fenomeni del mondo che ci circonda e ci aiuta a capirli. Tutte le grandezze che caratterizzano un fenomeno e che possono essere misurate sono dette GRANDEZZE
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
SAFE - Scuola di Scienze Agrarie, Forestali, Alimentari ed Ambientali. School of Agriculture, forest, Food and Environmental sciences
 Protocollo SAFE Determinazione dell attività antiossidante Valutazione della resistenza allo stress ossidativo in presenza di perossido d idrogeno Soluzione di perossido d idrogeno 1,6 M. Esporre i campioni
Protocollo SAFE Determinazione dell attività antiossidante Valutazione della resistenza allo stress ossidativo in presenza di perossido d idrogeno Soluzione di perossido d idrogeno 1,6 M. Esporre i campioni
20/03/2014 ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE REQUISITI PER UNA TITOLAZIONE
 ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE In una titolazione l analita reagisce con un reagente addizionato sotto forma di una soluzione di concentrazione nota (soluzione
ANALISI VOLUMETRICA ACIDO-BASE PRECIPITAZIONE COMPLESSOMETRICA OSSIDO-RIDUZIONE In una titolazione l analita reagisce con un reagente addizionato sotto forma di una soluzione di concentrazione nota (soluzione
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
ESERCIZI sulle SOLUZIONI
 ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
ESERCIZI sulle SOLUZIONI 1. Calcola la molarità delle seguenti soluzioni acquose, per le quali è data la massa di soluto disciolta in 200 cm 3 di soluzione: a) 20 g di NaCl; b) 20 g di HCl; c) 20 g di
Corso di Fisica per Scienze e Tecnologie per l Ambiente.
 Corso di Fisica per Scienze e Tecnologie per l Ambiente Fernando Scarlassara tel. 049-87-5911 tel. 049-8068 65 Dipartimento di Fisica (Paolotti) Laboratori Nazionali di Legnaro e-mail: scarlassara@pd.infn.it
Corso di Fisica per Scienze e Tecnologie per l Ambiente Fernando Scarlassara tel. 049-87-5911 tel. 049-8068 65 Dipartimento di Fisica (Paolotti) Laboratori Nazionali di Legnaro e-mail: scarlassara@pd.infn.it
BIOCHIMICA BIOCHIMICA APPLICATA
 BIOCHIMICA BIOCHIMICA APPLICATA Corso di Laurea in Farmacia Prof. Ivano F. Santarelli Introduzione Testi consigliati -I principi di Biochimica di Lehninger. D.L.Nelson, M.M. Cox. Zanichelli -Biochimica
BIOCHIMICA BIOCHIMICA APPLICATA Corso di Laurea in Farmacia Prof. Ivano F. Santarelli Introduzione Testi consigliati -I principi di Biochimica di Lehninger. D.L.Nelson, M.M. Cox. Zanichelli -Biochimica
LA DISINFEZIONE. Università G. d Annunzio - CHIETI - Facoltà di Medicina Dipartimento di Scienze Biomediche Sezione di Microbiologia Clinica
 Università G. d Annunzio - CHIETI - Facoltà di Medicina Dipartimento di Scienze Biomediche Sezione di Microbiologia Clinica Dott. Giovanni Catamo CONCETTI GENERALI CONSISTE NEL TRATTAMENTO DI MATERIALE
Università G. d Annunzio - CHIETI - Facoltà di Medicina Dipartimento di Scienze Biomediche Sezione di Microbiologia Clinica Dott. Giovanni Catamo CONCETTI GENERALI CONSISTE NEL TRATTAMENTO DI MATERIALE
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
LA MISURA DELLE GRANDEZZE FISICHE. Prof Giovanni Ianne
 LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
LA MISURA DELLE GRANDEZZE FISICHE Prof Giovanni Ianne Il metodo scientifico La Fisica studia i fenomeni naturali per: fornire una descrizione accurata di tali fenomeni interpretare le relazioni fra di
NUMERI. Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali
 NUMERI Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali N NUMERI Per contare i soldi del proprio conto in banca! 0,+1, 1,+2, 2,+3, 3,... Numeri interi Z NUMERI Per tagliare le torte! 0,1,-1,1/2,-1/2,2,-2,1/3,-1/3,2/3.-2/3,...
NUMERI Per contare le caramelle. 0, 1, 2,3, 4,.. Numeri naturali N NUMERI Per contare i soldi del proprio conto in banca! 0,+1, 1,+2, 2,+3, 3,... Numeri interi Z NUMERI Per tagliare le torte! 0,1,-1,1/2,-1/2,2,-2,1/3,-1/3,2/3.-2/3,...
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Grandezze Fisiche, Sistema Internazionale e Calcolo Vettoriale
 Grandezze Fisiche, Sistema Internazionale e Calcolo Vettoriale Soluzioni ai Quiz 1 Il Sistema Internazionale di Unità di Misura Le grandezze fisiche di base sono sei, ognuna delle quali ha una unità di
Grandezze Fisiche, Sistema Internazionale e Calcolo Vettoriale Soluzioni ai Quiz 1 Il Sistema Internazionale di Unità di Misura Le grandezze fisiche di base sono sei, ognuna delle quali ha una unità di
Richiami di matematica per lo studio delle discipline scientifiche
 Richiami di matematica per lo studio delle discipline scientifiche La misura in chimica : Misurare significa confrontare una grandezza in rapporto con un altra ad essa omogenea, scelta come campione.i
Richiami di matematica per lo studio delle discipline scientifiche La misura in chimica : Misurare significa confrontare una grandezza in rapporto con un altra ad essa omogenea, scelta come campione.i
Trasporto di membrana
 Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
PROGRAMMA FINALE SVOLTO DI CHIMICA CLASSE 3 A - A.S 2013/14 DOCENTE: MASSIMILIANO QUINZI
 CLASSE 3 A - A.S 2013/14 Chimica e proprietà della materia; Concetto di trasformazione chimica (in particolare decomposizione, e sintesi) e suo impiego per caratterizzare elementi e composti, Sistemi omogenei
CLASSE 3 A - A.S 2013/14 Chimica e proprietà della materia; Concetto di trasformazione chimica (in particolare decomposizione, e sintesi) e suo impiego per caratterizzare elementi e composti, Sistemi omogenei
Estrazione con solventi. Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti
 Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Stabilizzazione tartarica attraverso l'impiego di resina a scambio ionico
 Stabilizzazione tartarica attraverso l'impiego di resina a scambio ionico Angelo Bertacchini Riduzione del ph contestuale alla stabilizzazione tartarica Cos'è lo scambio ionico Lo scambio ionico è un fenomeno
Stabilizzazione tartarica attraverso l'impiego di resina a scambio ionico Angelo Bertacchini Riduzione del ph contestuale alla stabilizzazione tartarica Cos'è lo scambio ionico Lo scambio ionico è un fenomeno
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
FARMACODINAMICA. La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci.
 FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
Il metodo scientifico
 Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
Il metodo scientifico n La Fisica studia i fenomeni naturali per: n fornire una descrizione accurata di tali fenomeni n interpretare le relazioni fra di essi n Il metodo scientifico: n osservazione sperimentale
Le MEMBRANE in biologia
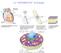 Le MEMBRANE in biologia Le membrana plasmatica Delimitazione delle cellule Genesi del potenziale elettrico trans-membrana Mantenimento delle differenze tra l ambiente intra ed extracellulare Trasferimento
Le MEMBRANE in biologia Le membrana plasmatica Delimitazione delle cellule Genesi del potenziale elettrico trans-membrana Mantenimento delle differenze tra l ambiente intra ed extracellulare Trasferimento
ph e indicatori acido-base
 ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
PROGRAMMA DISCIPLINARE SVOLTO a. s / N.B. il programma è pubblico ad uso degli studenti e delle famiglie.
 Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
Pagina 1 di 5 PROGRAMMA DISCIPLINARE SVOLTO a. s. 2015 / 2016 DOCENTE: Ghezzi Maria Grazia CLASSE: 2^ ID DISCIPLINA: S.I.CHIMICA MACROARGOMENTI che sono stati trattate nel corso del corrente anno scolastico
CHIMICA (Corso Integrato) CHIMICA GENERALE ED INORGANICA Dott. Francesco Musiani (6 crediti -48 ore)
 CHIMICA (Corso Integrato) CHIMICA GENERALE ED INORGANICA Dott. Francesco Musiani (6 crediti -48 ore) Orario (prime tre settimane di Ottobre) Mercoledì 14-16 Giovedì 14-16 Venerdì 14-16 Chimica Generale
CHIMICA (Corso Integrato) CHIMICA GENERALE ED INORGANICA Dott. Francesco Musiani (6 crediti -48 ore) Orario (prime tre settimane di Ottobre) Mercoledì 14-16 Giovedì 14-16 Venerdì 14-16 Chimica Generale
Al Dirigente Scolastico dell I.I.S.. F. Algarotti Venezia PROGRAMMA
 MATERIA: SCIENZE INTEGRATE -SCIENZE DELLA TERRA CLASSE: I E -La Terra come sistema integrato: litosfera, atmosfera, idrosfera, biosfera; esempi di relazioni ed interazioni che tra queste intercorrono -
MATERIA: SCIENZE INTEGRATE -SCIENZE DELLA TERRA CLASSE: I E -La Terra come sistema integrato: litosfera, atmosfera, idrosfera, biosfera; esempi di relazioni ed interazioni che tra queste intercorrono -
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 22 Acidi e basi si scambiano protoni 3 Sommario 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. La forza
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
