Introduzione alla Biochimica
|
|
|
- Alberta Leone
- 5 anni fa
- Visualizzazioni
Transcript
1 Introduzione alla Biochimica
2 Rappresenta più del 70% del peso degli organismi viventi Notevoli Forze di attrazione Bassa tendenza a ionizzarsi
3 I protoni liberi in soluzione non esistono
4 Ione Ossidrile Ione Idronio
5
6 tetraedro regolare Legame H-O-H O è ibridato sp3 Z=8 è una molecola polare
7 Legame idrogeno Interazione elettrostatica tra l atomo di O di una molecola di H 2 O e l atomo di H di una molecola di H 2 O adiacente. Ogni molecola forma legami idrogeno con altre 4 molecole vicine
8 Legame idrogeno nell acqua libera
9 Legame idrogeno nel ghiaccio: Struttura regolare a reticolo
10 Comuni legami idrogeno nei sistemi biologici I legami Idrogeno si formano tra un atomo elettronegativo ( O o N) e un atomo di H legato covalentemente ad un altro atomo elettronegativo Accettore di idrogeno (atomo elettronegativo) Donatore di idrogeno (atomo elettronegativo)
11 Comuni legami idrogeno nei sistemi biologici FORTE
12 Legami idrogeno di importanza biologica I legami Idrogeno si formano tra un atomo elettronegativo ( O o N) e un atomo di H legato covalentemente ad un altro atomo elettronegativo
13 Comuni legami idrogeno nei sistemi biologici: Le BASI AZOTATE NEL DNA CITOSINA Ξ GUANINA TIMINA = ADENINA
14 I soluti polari sono dissolti facilmente dall acqua LEGAME IONICO INTERAZIONE ELETTROSTATICA PONTE SALINO I legami Idrogeno soluto- soluto vengono sostituiti da I legami Idrogeno acqua-soluto
15 I soluti polari sono dissolti facilmente dall acqua
16 I soluti polari sono dissolti facilmente dall acqua Interazioni IONE- DIPOLO Interazioni DIPOLO- DIPOLO
17 Salto Protonico Il trasferimento di protoni tra molecole d acqua unite da legami Idrogeno consente un rapido movimento di un protone anche per lunghe distanze
18 FORZE DI VAN DER WAALS Le variazioni casuali della posizione degli elettroni attorno ad un nucleo possono generare un dipolo elettrico transitorio che a sua volta induce un altro dipolo elettrico transitorio ma opposto, nell atomo vicino 1) molecole non polari: in istanti definiti, il movimento degli elettroni provoca la formazione di dipoli istantanei che cambiano continuamente e polarizzano le molecole vicine. 2) molecole polari: l estremità positiva di una molecola attrae l estremità negativa di un altra dipolo elettrico transitorio
19 Alla forza di Van der Waals si attribuisce l'abilità del geco di camminare su superfici lisce senza l'uso di secrezioni adesive (le estremità delle sue zampe sono ricoperte da milioni di peli che moltiplicano le deboli forze elettromagnetiche di interazione con la superficie)
20 LEGAME IDROFOBICO: forza che tiene unite molecole che non riescono a formare legami con molecole d acqua senza che tra di esse si istauri un tipico legame chimico. Nell acqua ogni molecola è legata ad altre 4 da forti legami H. Per inserire in acqua un composto (incapace di formare legami con le molecole di acqua), dobbiamo rompere questi legami e quindi consumare energia. Se il composto con l'acqua formasse legami (ionici, ione-dipolo, H, dipolari etc) l'energia che ricaveremmo dalla formazione di questi nuovi legami compenserebbe quella spesa per rompere i legami tra le molecole dell'acqua, quindi il processo sarebbe energeticamente favorito e il composto si scioglierebbe in acqua.
21 Immaginiamo ora di mettere in acqua 2 molecole di benzene Ognuna di queste 2 molecole, insinuandosi tra le molecole di acqua, rompe legami acqua-acqua. Immaginiamo che ognuna ne rompa 6. Abbiamo avuto la rottura di 12 legami senza che se ne formino altri, quindi il processo è energeticamente sfavorevole. Ma se le 2 molecole,invece di esser separate si mettono adiacenti, l'una attaccata all'altra, senza molecole di acqua tra di esse il n dei legami acqua-acqua rotti è 6 e non 12. Per evitare di rompere molti legami acqua-acqua, le 2 molecole rimangono attaccate tra loro come se fossero legate, come se vi fosse un legame chimico, che non c'è Le molecole rimangono attaccate non perché formano un legame chimico, ma perché non riescono a formare legami con le molecole del solvente, che le respingono. LEGAME IDROFOBICO: forza che tiene unite molecole che non riescono a formare legami con molecole d acqua.
22 I composti non polari non si solubilizzano in acqua Interazione idrofobica
23 Quando mettiamo in acqua goccioline di olio (fatto da composti chimici che non riescono a formare legami con le molecole di acqua), queste goccioline non si sciolgono in acqua e non restano separate tra loro, ma si riuniscono per formare gocce più grandi, che, avendo una densità minore di quelle dell'acqua, salgono alla superficie e formano uno strato formato da solo olio. Legame idrofobico: enorme importanza in biologia - stabilizza la struttura delle proteine e degli acidi nucleici - mantiene la struttura delle membrane biologiche
24 Molecole ANFIPATICHE Contengono contemporaneamente: REGIONI POLARI o CARICHE IDROFILICHE Interagiscono favorevolmente con l acqua REGIONI NON POLARI IDROFOBICHE Evitano il contatto con l acqua
25 Molecole ANFIPATICHE: Dispersione dei Lipidi in acqua Interazioni IDROFOBICHE
26 Molecole ANFIPATICHE: Interazioni IDROFOBICHE Tengono unite le regioni non polari delle molecole
27 Esempi di biomolecole polari, non polari e anfipatiche
28 Legame idrogeno Interazione ionica Interazione ione-dipolo Interazione dipolo-dipolo Interazioni deboli tra le biomolecole in soluzioni acquose interazioni idrofobiche Interazioni di van der Waals (tra dipoli transitori)
29 Biomolecole Macromolecole, cioè polimeri con peso molecolare elevato che si formano a partire da precursori relativamente semplici POLISACCARIDI: polimeri di zuccheri semplici con funzione di struttura, di riserva o di riconoscimento cellulare. Il GLICOMA di una cellula è costituito da tutto l insieme di glucidi di una cellula. ACIDI NUCLEICI: DNA e RNA sono polimeri dei nucleotidi. il GENOMA è l intera sequenza di DNA di una cellula mentre la genomica è la scienza che si occupa della caratterizzazione dei genomi
30 Biomolecole PROTEINE: macromolecole formate da amminoacidi, l insieme di tutte le proteine di un organismo è detto PROTEOMA e la proteomica è la caratterizzazione della serie completa di proteine presenti in una determinata condizione. LIPIDI: derivati da idrocarburi insolubili con funzione di componenti strutturali delle membrane biologiche, riserve di energia, pigmenti, segnali intracellulari Il LIPIDOMA è l insieme delle molecole che contengono lipidi all interno della cellula
31 lipidi
LEGAMI SECONDARI. Queste forze si hanno sia tra molecole polari che. (note anche con il nome di INTERAZIONI DI NON LEGAME o LEGAMI DEBOLI)
 LEGAMI SECONDARI L esistenza di aggregati della materia allo stato solido e liquido indica che esistano anche altre forze in grado di legare molecole neutre Queste forze si hanno sia tra molecole polari
LEGAMI SECONDARI L esistenza di aggregati della materia allo stato solido e liquido indica che esistano anche altre forze in grado di legare molecole neutre Queste forze si hanno sia tra molecole polari
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
Il Legame Chimico. Prof.ssa Tiziana Bellini
 Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
Il Legame Chimico. Prof.ssa Tiziana Bellini
 Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
Legami secondari e lo stato fisico
 Legami secondari e lo stato fisico Gli stati aggregati (stato solido, liquido) richiedono la presenza di forze intermolecolari tra le molecole che compongono la sostanza. Legame ione dipolo (si forma fra
Legami secondari e lo stato fisico Gli stati aggregati (stato solido, liquido) richiedono la presenza di forze intermolecolari tra le molecole che compongono la sostanza. Legame ione dipolo (si forma fra
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
La massa è la quantità di materia di cui è fatta una qualsiasi cosa
 Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
I Legami intermolecolari
 I Legami intermolecolari Legami tra gli atomi di una molecola riepilogando Ionico D >1,9 Legami forti Covalente D = differenza di elettronegatività tra gli atomi Metallico (dovuto alla dislocazione di
I Legami intermolecolari Legami tra gli atomi di una molecola riepilogando Ionico D >1,9 Legami forti Covalente D = differenza di elettronegatività tra gli atomi Metallico (dovuto alla dislocazione di
Le interazioni reversibili tra le macromolecole sono mediate da 3 specie di legami non covalenti:
 Le interazioni reversibili tra le macromolecole sono mediate da 3 specie di legami non covalenti: 1) Legami elettrostatici 2) Legami idrogeno 3) Forze di van der Waals Le interazioni deboli tra biomolecole
Le interazioni reversibili tra le macromolecole sono mediate da 3 specie di legami non covalenti: 1) Legami elettrostatici 2) Legami idrogeno 3) Forze di van der Waals Le interazioni deboli tra biomolecole
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
IL LEGAME A IDROGENO
 IL LEGAME A IDROGENO Il legame idrogeno è un particolare tipo di interazione fra molecole che si forma ogni volta che un atomo di idrogeno, legato ad un atomo fortemente elettronegativo (cioè capace di
IL LEGAME A IDROGENO Il legame idrogeno è un particolare tipo di interazione fra molecole che si forma ogni volta che un atomo di idrogeno, legato ad un atomo fortemente elettronegativo (cioè capace di
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
GLI ATOMI TENDONO A LEGARSI SPONTANEAMENTE FRA DI LORO, PER FORMARE DELLE MOLECOLE, OGNI QUAL VOLTA QUESTO PROCESSO PERMETTE LORO DI RAGGIUNGERE UNA
 Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
Il Legame Chimico Per raggiungere configurazioni elettroniche stabili gli elementi tendono a reagire fra loro formando legami chimici. Configurazione stabile = situazione di minima energia Il legame chimico
20/10/2015. Importanza dei legami non covalenti in Biologia. Legami covalenti
 Legami covalenti Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di atomi. La formazione del legame covalente si basa
Legami covalenti Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di atomi. La formazione del legame covalente si basa
Introduzione alla biologia della cellula. Lezione 3 Le biomolecole DNA e RNA
 Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
OVERVIEW. Teoria atomica e tavola periodica. Legami e interazioni degli atomi
 OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
FORZE INTERMOLECOLARI o LEGAMI DEBOLI
 FRZE INTERMLECLARI o LEGAMI DEBLI 1 Le forze intermolecolari sono forze attrattive tra entità discrete come atomi o molecole, dette anche legami o interazioni deboli (E
FRZE INTERMLECLARI o LEGAMI DEBLI 1 Le forze intermolecolari sono forze attrattive tra entità discrete come atomi o molecole, dette anche legami o interazioni deboli (E
FORZE INTERMOLECOLARI o LEGAMI DEBOLI
 FRZE INTERMLECLARI o LEGAMI DEBLI 1 Le forze intermolecolari sono forze attrattive tra entità discrete come atomi o molecole, dette anche legami o interazioni deboli (E
FRZE INTERMLECLARI o LEGAMI DEBLI 1 Le forze intermolecolari sono forze attrattive tra entità discrete come atomi o molecole, dette anche legami o interazioni deboli (E
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
L acqua. Ci devono essere delle forze che tengono saldamente insieme le molecole d acqua
 L acqua Comparata a molecole con caratteristiche atomiche simili e di grandezza comparabile, l acqua presenta alcune caratteristiche peculiari Comparando l idruro dell ossigeno con gli idruri degli elementi
L acqua Comparata a molecole con caratteristiche atomiche simili e di grandezza comparabile, l acqua presenta alcune caratteristiche peculiari Comparando l idruro dell ossigeno con gli idruri degli elementi
Le interazioni deboli:
 Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
FORZE INTERMOLECOLARI
 FORZE INTERMOLECOLARI Le forze intermolecolari sono forze di attrazione che si stabiliscono tra le molecole che costituiscono una sostanza Determinano la tendenza delle molecole ad avvicinarsi. Per ogni
FORZE INTERMOLECOLARI Le forze intermolecolari sono forze di attrazione che si stabiliscono tra le molecole che costituiscono una sostanza Determinano la tendenza delle molecole ad avvicinarsi. Per ogni
FORMAZIONE DI LEGAMI. Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato.
 FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame.
 Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
Le macromolecole, a loro volta, derivano dall associazione di piccole molecole che risultano formate da atomi. LA MATERIA E GLI ATOMI
 7. Biologia 7 La biologia (dal greco bìos vita e lògos discorso) è la scienza della vita; essa comprende tutte le discipline che studiano la forma e la struttura (per esempio l anatomia e la citologia),
7. Biologia 7 La biologia (dal greco bìos vita e lògos discorso) è la scienza della vita; essa comprende tutte le discipline che studiano la forma e la struttura (per esempio l anatomia e la citologia),
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Introduzione alla chimica organica. 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole
 Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
 ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
Idrogeno (H) Azoto (N) La materia è costituita da elementi chimici. In natura sono presenti 92 elementi
 Gli organismi sono fatti da MATERIA*. (*qualsiasi cosa che occupa uno spazio e ha una massa) Gli antichi filosofi greci dicevano che la materia deriva da 4 ingredienti di base o ELEMENTI (ARIA, ACQUA,
Gli organismi sono fatti da MATERIA*. (*qualsiasi cosa che occupa uno spazio e ha una massa) Gli antichi filosofi greci dicevano che la materia deriva da 4 ingredienti di base o ELEMENTI (ARIA, ACQUA,
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
Come si costruiscono le molecole in natura ed in laboratorio. Giuseppe Macino
 Come si costruiscono le molecole in natura ed in laboratorio Giuseppe Macino E Dio creo la luce Cosa tiene insieme tutta la materia che forma la terra? Tutto questo e costituito da ELEMENTI Gli elementi
Come si costruiscono le molecole in natura ed in laboratorio Giuseppe Macino E Dio creo la luce Cosa tiene insieme tutta la materia che forma la terra? Tutto questo e costituito da ELEMENTI Gli elementi
12/10/2016. Biologia della Cellula Animale Legami covalenti. Importanza dei legami non covalenti in Biologia. Legami covalenti (1)
 Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise da coppie di atomi. Legami covalenti Importanza dei legami non covalenti in Biologia
Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise da coppie di atomi. Legami covalenti Importanza dei legami non covalenti in Biologia
Acqua: peso molecolare = 18 In un bicchiere circa ml, quindi 10 moli una mole 6x10 23 molecole, quindi in un bicchiere 6x10 24 molecole
 Acqua: peso molecolare = 18 In un bicchiere circa 180-200 ml, quindi 10 moli una mole 6x10 23 molecole, quindi in un bicchiere 6x10 24 molecole Volume degli oceani 1.3 miliardi di km 3 = 1.3 x 10 18 m
Acqua: peso molecolare = 18 In un bicchiere circa 180-200 ml, quindi 10 moli una mole 6x10 23 molecole, quindi in un bicchiere 6x10 24 molecole Volume degli oceani 1.3 miliardi di km 3 = 1.3 x 10 18 m
L ACQUA. E il mezzo in cui avvengono le maggiori reazioni. Tutte le molecole biologiche assumono forma e
 L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Le forze intermolecolari Manifestazione delle forze intermolecolari
 1 Le forze intermolecolari Manifestazione delle forze intermolecolari 2 I gas nobili (He, Ne, Ar...) che NON formano legami chimici dovrebbero restare gassosi a qualsiasi temperatura. Invece a T molto
1 Le forze intermolecolari Manifestazione delle forze intermolecolari 2 I gas nobili (He, Ne, Ar...) che NON formano legami chimici dovrebbero restare gassosi a qualsiasi temperatura. Invece a T molto
FORZE INTERMOLECOLARI
 FORZE INTERMOLECOLARI Oltre alle forze intramolecolari (legami) esistono nella materia forze intermolecolari (tra molecole diverse), anch esse dovute ad interazioni elettrostatiche. Le forze intermolecolari
FORZE INTERMOLECOLARI Oltre alle forze intramolecolari (legami) esistono nella materia forze intermolecolari (tra molecole diverse), anch esse dovute ad interazioni elettrostatiche. Le forze intermolecolari
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
02/12/2014. Tutti gli esseri viventi sono composti da cellule LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI
 Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
PROPRIETA DEI MATERIALI
 PROPRIETA DEI MATERIALI Una proprietà è la risposta di un materiale ad una sollecitazione esterna. Per i materiali solidi le proprietà possono raggrupparsi in sei differenti categorie: 1. Meccaniche 2.
PROPRIETA DEI MATERIALI Una proprietà è la risposta di un materiale ad una sollecitazione esterna. Per i materiali solidi le proprietà possono raggrupparsi in sei differenti categorie: 1. Meccaniche 2.
Importanza dei legami non covalenti in Biologia
 Importanza dei legami non covalenti in Biologia Biotecnologie / Biologia Sperimentale Applicata Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni
Importanza dei legami non covalenti in Biologia Biotecnologie / Biologia Sperimentale Applicata Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Modulo 1. Introduzione alle biomolecole. Ottobre 2017
 Modulo 1 Introduzione alle biomolecole Ottobre 2017 La logica molecolare della vita I sistemi viventi sono composti da molecole (biomolecole) inanimate (Albert Lehninger) Le biomolecole seguono le leggi
Modulo 1 Introduzione alle biomolecole Ottobre 2017 La logica molecolare della vita I sistemi viventi sono composti da molecole (biomolecole) inanimate (Albert Lehninger) Le biomolecole seguono le leggi
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 8 La chimica dell acqua 3 Sommario 1. Come si formano i legami chimici 2. I legami covalenti ionici 3. La molecola dell acqua
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 8 La chimica dell acqua 3 Sommario 1. Come si formano i legami chimici 2. I legami covalenti ionici 3. La molecola dell acqua
Forze intermolecolari
 Forze intermolecolari Le forze intermolecolari sono forze attrattive tra molecole, tra ioni o tra ioni e molecole. In assenza di tali forze tutte le molecole sarebbero gas le molecole possono stabilire
Forze intermolecolari Le forze intermolecolari sono forze attrattive tra molecole, tra ioni o tra ioni e molecole. In assenza di tali forze tutte le molecole sarebbero gas le molecole possono stabilire
L ACQUA. E il mezzo in cui avvengono le maggiori reazioni. Tutte le molecole biologiche assumono forma e
 L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
L ACQUA E il mezzo in cui avvengono le maggiori reazioni biochimiche Tutte le molecole biologiche assumono forma e funzione in base alle proprietà chimiche e fisiche delle molecole di H 2 O che le circondano
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti 2009-2010 Introduzione alla chimica - terminologia e definizioni Elemento sostanza
Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti 2009-2010 Introduzione alla chimica - terminologia e definizioni Elemento sostanza
Interazioni deboli. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Interazioni deboli 1 Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012 Legami deboli o interazioni deboli La forza di un legame chimico viene stabilita in base alla energia del
Interazioni deboli 1 Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012 Legami deboli o interazioni deboli La forza di un legame chimico viene stabilita in base alla energia del
ESERCIZI ESERCIZI. il basso d. aumenta lungo un periodo da sinistra verso
 ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte.
 Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Legame Covalente Polare e MOT. Polarità del legame aumenta con differenza di elettronegatività.
 Legame Covalente Polare e MOT Polarità del legame aumenta con differenza di elettronegatività. Legame Ionico Se differenza di elettronegatività è molto grande si ottiene un legame ionico. Legame Ionico
Legame Covalente Polare e MOT Polarità del legame aumenta con differenza di elettronegatività. Legame Ionico Se differenza di elettronegatività è molto grande si ottiene un legame ionico. Legame Ionico
le SOSTANZE Sostanze elementari (ELEMENTI) COMPOSTI Costituiti da due o più atomi DIVERSI tra loro
 Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
20/12/2013. Importanza dei legami non covalenti in Biologia. Legami covalenti
 Legami covalenti Importanza dei legami non covalenti in Biologia Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di
Legami covalenti Importanza dei legami non covalenti in Biologia Gli atomi che costituiscono le molecole sono tenuti insieme da legami covalenti in cui coppie di elettroni sono condivise tra coppie di
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
L acqua: struttura e proprietà La vita come noi la conosciamo ha luogo in ambiente acquoso*
 L acqua: struttura e proprietà La vita come noi la conosciamo ha luogo in ambiente acquoso* In biochimica l acqua è estremamente importante perché: La struttura e funzione delle molecole biologiche dipende
L acqua: struttura e proprietà La vita come noi la conosciamo ha luogo in ambiente acquoso* In biochimica l acqua è estremamente importante perché: La struttura e funzione delle molecole biologiche dipende
Di cosa è fatta una cellula?
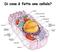 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.
 LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.il modello a mosaico fluido descrive la struttura comune a tutte
LE MEMBRANE Le membrane sono composte da lipidi e proteine in composizioni che variano in base alla specie,al tipo cellulare e all organello.il modello a mosaico fluido descrive la struttura comune a tutte
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole.
 4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
LE MOLECOLE. 5.1 I legami molecolari 5.2 Le forze di Van der Walls 5.3 Il legame idrogeno 5.4 La teoria VSEPR
 LE MOLECOLE 5.1 I legami molecolari 5.2 Le forze di Van der Walls 5.3 Il legame idrogeno 5.4 La teoria VSEPR 5.1 I legami molecolari Si ha un legame chimico quando una forza di natura elettrostatica tiene
LE MOLECOLE 5.1 I legami molecolari 5.2 Le forze di Van der Walls 5.3 Il legame idrogeno 5.4 La teoria VSEPR 5.1 I legami molecolari Si ha un legame chimico quando una forza di natura elettrostatica tiene
Acidi Nucleici: DNA = acido deossiribonucleico
 Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
L acqua. Prof.ssa Tiziana Bellini
 L acqua L acqua: struttura e proprietà La vita come noi la conosciamo ha luogo in ambiente acquoso* In biochimica l acqua è estremamente importante perché: La struttura e funzione delle molecole biologiche
L acqua L acqua: struttura e proprietà La vita come noi la conosciamo ha luogo in ambiente acquoso* In biochimica l acqua è estremamente importante perché: La struttura e funzione delle molecole biologiche
Gli Acidi Nucleici DNA RNA
 Gli Acidi Nucleici DNA RNA Gli Acidi nucleici Gli acidi nucleici sono il: DNA (acido desossiribonucleico) RNA (acido ribonucleico) Essi sono formati dai polimeri (molecole molto grosse) i cui monomeri
Gli Acidi Nucleici DNA RNA Gli Acidi nucleici Gli acidi nucleici sono il: DNA (acido desossiribonucleico) RNA (acido ribonucleico) Essi sono formati dai polimeri (molecole molto grosse) i cui monomeri
L'energia media V di interazione fra uno ione avente carica q e un dipolo permanente ad una distanza r Ä
 Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
Interazioni intermolecolari Interazioni ione-dipolo Interazioni dipolo-dipolo Interazione dipolo permanente-dipolo indotto Interazione dipolo istantaneo-dipolo indotto Forze di Van der Waals Legame idrogeno
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
LIVELLI di ORGANIZZAZIONE BIOLOGICA
 LIVELLI di ORGANIZZAZIONE BIOLOGICA ATOMO 1) Unità fondamentale della MATERIA, cioè di tutto ciò che ha una MASSA e occupa un VOLUME. 2) È presente si anella materia VIVENTE sia in quella NON VIVENTE.
LIVELLI di ORGANIZZAZIONE BIOLOGICA ATOMO 1) Unità fondamentale della MATERIA, cioè di tutto ciò che ha una MASSA e occupa un VOLUME. 2) È presente si anella materia VIVENTE sia in quella NON VIVENTE.
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
CONOSCENZE ABILITA' (capacità) TEMPI. Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari)
 Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari) CONTENUTI RISULTATI DI APPRENDIMENTO (competenze) CONOSCENZE ABILITA' (capacità) TEMPI MODULO 0 Richiamo della
Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari) CONTENUTI RISULTATI DI APPRENDIMENTO (competenze) CONOSCENZE ABILITA' (capacità) TEMPI MODULO 0 Richiamo della
L acqua: struttura e proprietà
 L acqua: struttura e proprietà Proprietà dell acqua Proprietà fisiche dell acqua Proprietà dell acqua allo stato liquido La molecola H 2 O Una molecola simmetrica in continua vibrazione La molecola di
L acqua: struttura e proprietà Proprietà dell acqua Proprietà fisiche dell acqua Proprietà dell acqua allo stato liquido La molecola H 2 O Una molecola simmetrica in continua vibrazione La molecola di
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
ATOMI E MOLECOLE. Psicobiologia Lezione nr. 1. Prof. Lasaponara
 ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno 5. Legami a confronto
 Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Unità n 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia
 Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Capitolo 12 Le forze intermolecolari e gli stati condensati della materia 1. Le forze intermolecolari 2. Molecole polari e apolari 3. Le forze dipolo-dipolo e le forze di London 4. Il legame a idrogeno
Bioingegneria Elettronica I. Potenziali interatomici e interazioni speciali
 Bioingegneria Elettronica I Potenziali interatomici e interazioni speciali Interazioni repulsive Per completare il quadro delle interazioni possibili tra molecole, occorre ricordare che a cortissima distanza,
Bioingegneria Elettronica I Potenziali interatomici e interazioni speciali Interazioni repulsive Per completare il quadro delle interazioni possibili tra molecole, occorre ricordare che a cortissima distanza,
04/10/17 I LEGAMI DEL CARBONIO. Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole
 04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
CENNI SUL TIPO DI FORZE
 CENNI SUL TIPO DI FORZE Forze deboli che influenzano la struttura delle proteine: le interazioni di van der Waals repulsione attrazione Forze attrattive dovute a interazioni istantanee che si generano
CENNI SUL TIPO DI FORZE Forze deboli che influenzano la struttura delle proteine: le interazioni di van der Waals repulsione attrazione Forze attrattive dovute a interazioni istantanee che si generano
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
