Occorrente: mascherina; guanti; spatola, capillari chiusi per pf, coccio di porcellana porosa.
|
|
|
- Stefania Di Giacomo
- 5 anni fa
- Visualizzazioni
Transcript
1 PRIMA ESERCITAZIONE DETERMINAZIONE PUNTO DI FUSIONE CON IL METODO DEL CAPILLARE Occorrente: mascherina; guanti; spatola, capillari chiusi per pf, coccio di porcellana porosa. METODO DEL CAPILLARE CON IL PRERISCALDAMENTO Per punto di fusione con preriscaldamento s intende che la sostanza deve essere messa nel blocco riscaldante circa 5 C prima dell inizio della fusione ed il riscaldamento dovrebbe essere regolato in modo tale che la temperatura salga di circa 1 C al minuto. Segnare l intervallo di temperatura tra l inizio della fusione e la fine di questa. Se la sostanza non fonde, ma si decompone dando sostanze più o meno colorate, si segna l intervallo di questa trasformazione e si dice che il punto di fusione è con decomposizione indicando la temperatura con accanto la dizione dec o d. Attenzione: non farsi ingannare dal fenomeno del rammollimento. Questo fenomeno che si riscontra nel comportamento di alcune sostanze consiste nella trasformazione del cristallo che collassa, rassomigliando ad una spugna strizzata con tutto il liquido intorno. Questo non è il punto di fusione, ma viene definito punto di rammollimento. Preparazione del campione per l esecuzione del punto di fusione Pulire un coccio di porcellana con un pezzo di carta assorbente (non bagnare con acqua). Mettere sul coccio di porcellana pulito 1 punta di spatola di sostanza e polverizzare i cristalli schiacciando con la parte piatta di una spatola. Riempire il capillare chiuso (se necessario aiutandosi con una spatola) fino a far depositare sul fondo una colonnina di circa 2 mm di altezza. Tenendo la parte chiusa verso il basso, far cadere il capillare nel tubo di plastica o di vetro per far assestare tutto il campione verso il fondo del capillare. Determinazione del punto di fusione di una sostanza a p.f. ignoto Se non si ha alcuna idea sul punto di fusione di una sostanza, bisogna preparare 3 capillari carichi ed eseguire le seguenti operazioni. 1 Primo capillare: si inserisce il primo capillare, si riscalda innalzando la temperatura rapidamente (5 C/min); si ottiene una misura indicativa sul punto di fusione della sostanza (quello reale sarà leggermente più basso di quello osservato in questa misura rapida). Immaginiamo di ottenere un valore di Si lascia raffreddare l apparecchio fini ad almeno 20 C al disotto del valore osservato (fino a C). 2 Si riaccende il riscaldamento regolando la velocità di riscaldamento in modo tale che la temperatura salga di 1-3 C/min. 1
2 3 Si inserisce nel blocco il secondo capillare: questa operazione fornirà un dato più affidabile. Immaginiamo di aver ottenuto C. Si fa raffreddare lo strumento di circa 10 C. 4 Si regola la velocità di riscaldamento in modo tale che la temperatura salga di 1 C al minuto. Il terzo capillare: si inserisce nel blocco quando questo ha raggiunto la temperatura di C. 5 Si legge il punto di fusione. Determinazione del punto di fusione di una sostanza a p.f. noto Avendo idea del pf della sostanza si evita la misurazione con riscaldamento rapido. Si preriscalda l apparecchio fino a 10 C al disotto del pf della sostanza; si imposta la velocità di riscaldamento a 1-3 C/min, si inserisce il primo capillare e si determina il pf. Lasciar raffreddare e ripetere l operazione per confermare la misura. ES. Acido benzoico (p.f.= C). Preparare due capillari. Scaldare lo strumento rapidamente fino a C. Mettere il capillare e abbassare la velocità di riscaldamento a 1-3 C al minuto. Determinare il punto di fusione. Ripetere 2
3 SUBLIMAZIONE Sublimazione del cloruro di ammonio: separazione da una miscela cloruro di ammonio/carbone: Da eseguire in gruppi di 2-3 studenti Occorrente: mascherina; occhiali di protezione; guanti; 2 vetrini da orologio puliti, un imbutino pulito il cui gambo viene tappato all estremità con un batuffolino di ovatta o di carta, spatola. Accendere la piastra riscaldante a circa C. Mettere 2-3 spatolate di miscela NH4Cl/carbone in un vetrino da orologio e coprire con l imbutino. Mettere il tutto sulla piastra riscaldante calda (utilizzando le pinze di metallo) e scaldare per ottenere la sublimazione di NH4Cl. Con le pinze di metallo allontanare dalla piastra l apparecchio per la sublimazione e poggiarlo sul cubo/parallelepipedo di legno (attenzione non poggiarlo sul banco, l escursione termica troppo rapida potrebbe rompere il vetrino). Lasciar raffreddare l apparecchio sublimatore; togliere il batuffolo di cotone dal gambo e recuperare in il sublimato grattandolo dalle pareti dell imbutino con la spatola e facendolo scendere nel gambo dell imbuto in un vetrino pulito. Se la quantità di sublimato è sufficiente raccoglierlo in un contenitore. 3
4 CRISTALLIZZAZIONE OPERARE SOTTO CAPPA Cristallizzazione dell acido benzoico da acqua: Occorrente: Mascherina; occhiali di protezione; guanti; beuta da 25 ml; bacchetta di vetro; pinze di legno; imbutino di vetro; carta da filtro; portaprovette e una provetta, 3-4 spatolate abbondanti di ac. benzoico vengono poste in una beuta da 25 ml. Nella beuta deve essere aggiunta una quantità di acqua tale da lasciare abbondante corpo di fondo a freddo ma portata all ebollizione deve essere in grado di sciogliere la sostanza. NOTA: Non riempire mai la beuta più di 1/3 del suo volume. Per ottenere questo si aggiunge una piccola quantità di H 2 O. Ci si reca alla cappa e si riscalda all ebollizione la sospensione agitando continuamente prendendo la beuta con una pinza di legno (non di metallo) o con una cravattina di carta. Se all ebollizione la sostanza non risulta disciolta, si deve aggiungere ancora acqua in piccole quantità, riportare il tutto all ebollizione, finché la dissoluzione è completa. Tutta la fase di riscaldamento della soluzione di acido benzoico si effettua sotto cappa. A dissoluzione completata all ebollizione allontanare la beuta dalla piastra ed attendere il lento raffreddamento. Si osserva la precipitazione di acido benzoico in scaglie iridescenti. Se la sostanza non riprecipita significa che il volume di solvente aggiunto è eccessivo per la quantità di sostanza utilizzata. In questo caso bisogna concentrare la soluzione (per ebollizione) e attendere il raffreddamento. Si prepara il filtro a pieghe, lo si pone nell imbuto e l imbuto a sua volta si pone su una provetta pulita. Si raccoglie in maniera quantitativa tutto il cristallizzato sul filtro a pieghe e il filtrato (acque madri di cristallizzazione) nella provetta. Il cristallizzato si lava con H2O distillata fredda (2 lavaggi da circa 1-2 ml). Si lascia asciugare a T ambiente; quando il cristallizzato è secco si controlla la purezza determinando il pf. Le acque di cristallizzazione si scartano nel recipiente per lo smaltimento delle soluzioni. 4
5 SECONDA ESERCITAZIONE Si lavora in gruppi (un gruppo per banco) Occorrente: occhiali; mascherina; guanti; spatola; 2 beute da 100 ml; imbuto, imbuto separatore; sostegno con anello; provette e portaprovette; beaker da 25 ml; cilindro da 50 ml: SEPARAZIONE DI UNA MISCELA CAFFEINA E BENZOATO DI SODIO Preparazione: sciogliere 0,5 g della miscela caffeina sodio benzoato (4-5 punte di spatola) in 3 ml di NaOH 2N, e diluire con circa 30 ml di acqua. Utilizzando un imbuto, trasferire la soluzione nell imbuto separatore: aggiungere 25 ml di cloruro di metilene, chiudere l imbuto separatore con il tappo ed effettuare l estrazione. Lasciare stratificare i due solventi (CH2Cl2 è più denso e si posiziona in basso). Si toglie il tappo dell imbuto separatore, si pone una beuta da 100 ml sotto il gambo dell imbuto e si apre il rubinetto facendo scendere la soluzione organica. Si chiude il rubinetto dell imbuto quando il menisco di separazione delle due fasi raggiunge il rubinetto. Si esegue una seconda estrazione con altri 25 ml di CH2Cl2 unendo la seconda fase organica (CH2Cl2) a quella della prima estrazione. NB: La tecnica per eseguire le estrazioni verrà illustrata prima di iniziare l esperienza. Le fasi organiche riunite contengono la caffeina. La fase acquosa alcalina contenente il benzoato di sodio viene raccolta in un altra beuta pulita. REAZIONI DI RICONOSCIMENTO CAFFEINA A 5 ml della soluzione di CH2Cl2 aggiungere 2 ml di HCl 2M; dopo agitazione e stratificazione delle due fasi, si aggiungono poche gocce di potassio iodobismutato (Reattivo di Druggendorf) alla fase acquosa: si forma immediatamente un precipitato rosso-arancio. REAZIONI DI RICONOSCIMENTO BENZOATO DI SODIO 1) Una porzione della soluzione acquosa alcalina viene acidificata con HCl 2M: si forma un precipitato bianco di acido benzoico. 2) Ad 1 ml della soluzione acquosa, portata a ph neutro con HCl 2M si aggiunge la soluzione di FeCl3: il precipitato salmone che si forma si scioglie in etere; la soluzione eterea si colora di rosso. LE SOLUZIONI ACQUOSE SI SMALTISCONO NELL APPOSITO CONTENITORE PRESENTE IN LABORATORIO. LE SOLUZIONI DI CHCl2 SI SMALTISCONO NELL APPOSITO CONTENITORE ALLESTITO IN UNA DELLE CAPPE ASPIRANTI. 5
6 ESECUZIONE DI UNA CROMATOGRAFIA SU STRATO SOTTILE IDENTIFICAZIONE CALCIO PANTOTENATO Occorrente: occhiali; guanti; mascherina; tubicini da saggio; cubo di legno; vaschetta cromatografica; lastrine TLC (gel di silice). 3 campioni: a, b, c; 2 soluzioni di riferimento: Ra - calcio pantotenato; Rb acido 3-amminopropionico. Preparare 3 tubicini da saggio segnati rispettivamente a, b, c contenenti ognuno una puntina di spatola di sostanza in esame (a, b o c) e aggiungere in ognuno 0.5 ml di etanolo (10 gocce). Su una lastra cromatografica di gel di silice (5x10cm), con una matita, segnare una linea parallela alla base a circa 1,5 cm dalla base stessa. E bene non calcare per non rovinare lo strato sottile di silice. Si segnano 5 punti equidistanti sulla linea disegnata. Attenzione, i punti esterni non devono essere a meno di 1 cm dal lato della lastrina! Con un capillare si depone la soluzione del campione a, sul secondo una goccia della soluzione b, sul terzo una goccia della soluzione c, sul quarto una goccia della soluzione di riferimento Ra e sul quinto una goccia della soluzione di riferimento Rb. Sotto ogni punto si consiglia di scrivere a matita con cautela a, b, c, Ra e Rb rispettivamente. La lastrina è posta in una camera cromatografica nella quale è presente l eluente (1 cm max!) costituito da una miscela H2O/Etanolo 35:65. Si eluisce con la camera cromatografica ben chiusa evitando movimenti della stessa. Quando il livello dell eluente è arrivato a circa 1 cm dalla sommità della lastrina, quest ultima viene prelevata dalla camera e con una matita si segna il fronte del solvente. Lasciare asciugare la lastra TLC sotto cappa e poi spruzzare con una soluzione di ninidrina (mettere la lastra TLC su un foglio di carta e poi spruzzare); scaldare leggermente la lastra dopo averla spruzzata. Identificare quale dei campioni (a, b o c) è calcio pantotenato, ed identificare in esso l impurezza (acido 3- amminopropionico). 6
7 TERZA ESERCITAZIONE Si lavora in gruppi (un gruppo per banco) Occorrente: 1 spatola grande, occhiali, mascherina, guanti, spatola, 4 beute da 100 ml, imbuto, imbuto separatore, sostegno con anello, provette e portaprovette, beaker (o beuta) da 50 ml, cilindro da 50 ml. TUTTE LE OPERAZIONI DI ESTRAZIONE SI SVOLGONO SOTTO CAPPA ASPIRANTE ESTRAZIONE DEI PRINCIPI ATTIVI (CAFFEINA E PARACETAMOLO DA UNA PREPARAZIONE FARMACEUTICA Versare circa 2 g della miscela solida in un beaker da 50 ml, aggiungere 20 ml di acqua bollente (prelevata sotto cappa), agitare e filtrare con filtro di carta a pieghe allestito su un imbuto di vetro, raccogliendo il filtrato in una beuta da 100 ml. Aggiungere al beaker altri 20 ml di acqua bollente, agitare e filtrare nuovamente con lo stesso filtro, unendo al precedente filtrato. Dopo raffreddamento, il filtrato ottenuto viene acidificato a ph 2 con HCl 2M e versato in un imbuto separatore da 100 ml, si aggiungono 30 ml di CH2Cl2 e si effettua una estrazione. La fase organica viene raccolta in una beuta pulita da 100 ml e la fase acquosa acida viene nuovamente estratta con 30 ml di CH2Cl2, quest ultimo viene riunito alla soluzione di diclorometano della prima estrazione. La fase acquosa acida viene recuperata in una beuta pulita. RICONOSCIMENTO DELLA CAFFEINA Circa 2 ml della soluzione acida dell estrazione vengono addizionati di 3-4 gocce di reattivo di Draggendorf: si forma un precipitato arancio-rosso. RICONOSCIMENTO DEL PARACETAMOLO Circa metà della soluzione di diclorometano viene trasferita in una beuta pulita e, con cautela, portata a secchezza su piastra riscaldante (sotto cappa). Si lascia raffreddare e poi aggiungono 2 ml di acido cloridrico diluito e si scalda all'ebollizione a bagnomaria per 15 min. Si aggiungono 3 ml di acqua e si raffredda accuratamente. Non si forma alcun precipitato. Aggiungere 0,2 ml di sodio nitrito soluzione e dopo 1 o 2 min, aggiungere 1 ml di β-naftolo soluzione: si sviluppa una colorazione arancione o rossa intensa e generalmente si forma un precipitato dello stesso colore. LE SOLUZIONI ACQUOSE SI SMALTISCONO NELL APPOSITO CONTENITORE PRESENTE IN LABORATORIO. LE SOLUZIONI DI CH2Cl2 SI SMALTISCONO NELL APPOSITO CONTENITORE ALLESTITO IN UNA DELLE CAPPE ASPIRANTI. 7
8 QUARTA ESERCITAZIONE CALCINAZIONE OPERARE LA CALCINAZIONE SOTTO CAPPA Occorrente: Mascherina; occhiali di protezione; guanti; capsula o crogiolo di porcellana; spatola. Con questo saggio per via secca si può capire se la sostanza solida è: ORGANICA: ad es. acido benzoico INORGANICA: ad es. ZnO METALLORGANICA (anione organico, catione inorganico): ad es. Calcio pantotenato. Si mettono nel crogiolo 1-2 punte di spatola di sostanza (si consiglia di non eccedere con la quantità). Prendere il crogiolo con le pinze di metallo. Si va alla cappa e si scalda sulla fiamma ossidante del bunsen, prima blandamente (ci può essere la proiezione di materiale dovuto alla perdita di acqua o alla decomposizione della sostanza) poi più vivacemente, fino a completa calcinazione. SOSTANZE ORGANICHE: le sostanze organiche hanno come caratteristica comune quella di CARBONIZZARE. Se il riscaldamento viene continuato, la parte carboniosa viene ulteriormente ossidata e il carbone si trasforma in CO2. Quindi alla fine della calcinazione la sostanza organica deve lasciare il crogiuolo PULITO. Di solito i vapori delle sostanze organiche prendono fuoco più o meno spontaneamente. Alcune sostanze organiche lasciano un residuo vetroso nero omogeneo. Il residuo non deve dare colorazione alla fiamma. METALLORGANICA: prendono fuoco più o meno spontaneamente, e anche dopo minuti di riscaldamento lasciano dei residui inorganici (minerali). Di solito è difficile ottenere una mineralizzazione completa: normalmente i residui lasciati sono simili alla cenere di una sigaretta: il colore grigio finale è dovuto a due componenti: la parte organica nera per i residui carboniosi e il bianco dei sali minerali. E utile saggiare le ceneri con il filo di Pt per osservare la colorazione della fiamma ed acquisire informazioni sui cationi presenti nella sostanza. NB: il calcio glicerofosfato e il calcio fosfato non danno colorazione rossa perchè con il riscaldamento si forma calcio ortofosfato che non da colorazione. INORGANICHE: l unica sostanza inorganica che prende fuoco è il sodio tiosolfato: dà affioramenti gialli di zolfo che si incendiano con esalazioni acri di anidride solforosa. Le altre sostanze della FU, restano inalterate, danno qualche scoppiettio oppure sublimano ma senza prendere fuoco (NH 4 Cl), o fondono rigonfiando (borace, H 3 BO 3 ), oppure cambiano colore diventando gialle (ZnO, TiO 2 ). L ossido di zinco torna bianco dopo raffreddamento. 8
9 SAGGI DI SOLUBILITA E CARATTERISTICHE ACIDO/BASE. Occorrente: mascherina; guanti; occhiali; provette; portaprovette; bacchetta di vetro; cartina indicatrice di ph. Una sostanza è definita solubile in un determinato solvente se 1 g di essa si scioglie in cc ad una temperatura di C. (equivale a circa 30 mg una punta di spatola - in circa 1-2 ml di solvente) Per provare la solubilità mettere in una provetta una punta di spatola di sostanza (eventualmente ridotta prima a polvere fine nel mortaio) e 1 ml (20 gocce) del solvente in esame. Agitare con decisione anche per 2-3 minuti. Se si ha una sola fase omogenea e limpida si ha completa solubilità. I due solventi più usati sono l acqua e l etere etilico. Le prove di solubilità in etere etilico vanno eseguite in cappa aspirante. Per determinare le caratteristiche acido/base di una sostanza si opera come segue: Si saggia la sua solubilità in acqua ed in etere etilico. Se la sostanza è solubile in acqua, va determinato il ph, bagnando nella soluzione ottenuta una bacchetta di vetro e umettando con essa una cartina indicatrice di ph. Si usano cartine universali con ph Se la sostanza è insolubile in acqua e solubile in etere etilico, si saggia la sua solubilità in HCl 2N, NaHCO 3 sat., Na 2 CO 3 sat. e NaOH 2N (in questo ordine!!). Dalle prove di solubilità ricavare il carattere acido/base della sostanza saggiata. NOTA BENE: se la sostanza risulta solubile in NaHCO 3, NON vanno effettuate le prove di solubilità in Na2CO3 e NaOH. Se la sostanza risulta solubile in Na2CO3, NON vanno effettuate le prove di solubilità in NaOH. SAGGIARE LA SOLUBILITA IN H 2 O, etere etilico, NaHCO 3 sat, Na 2 CO 3 sat, NaOH 2N, HCl 2N DI ALCUNE DELLE SEGUENTI SONTANZE, IDENTIFICARNE LE CARATTERISTICHE ACIDO/BASE: Acido benzoico; acido salicilico; Acido tartarico; Benzocaina; Metile-p-idrossibenzoato; Saccarosio; Acido citrico; Acido acetilsalicilico; Mannitolo; Glucosio; Caffeina. LE SOLUZIONI ACQUOSE SI SMALTISCONO NELL APPOSITO CONTENITORE PRESENTE IN LABORATORIO. LE SOLUZIONI ETEREE SI SMALTISCONO NELL APPOSITO CONTENITORE ALLESTITO IN UNA DELLE CAPPE ASPIRANTI. 9
10 QUINTA ESERCITAZIONE RICONOSCIMENTO GRUPPI FUNZIONALI Occorrente: mascherina; occhiali; guanti; spatola; provette; portaprovette; cartina indicatrice di ph. RICONOSCIMENTO DEGLI ESTERI CON SAGGIO DI ANGELI RIMINI Etile acetato Mettere 3-4 gocce di acetato di etile in una provetta. Aggiungere una punta di spatola di idrossilamina cloridrato NH2OH. HCl) solida. Aggiungere una minima quantità di acqua ed alcalinizzare con NaOH 2N fino a ph Riscaldare a bagnomaria fino a completa solubilizzazione. Raffreddare e acidificare con HC1 2N. Aggiungere alcune gocce di soluzione di cloruro ferrico. Si avrà una colorazione violetta dovuta all`idrossammato ferrico. NB: se si aggiunge la soluzione di FeCl3 alla soluzione alcalina si avrà il precipitato di Fe(OH)3 di colore ruggine. Riacidificando si forma l idrossammato ferrico di colore violetto. RICONOSCIMENTO DELLE ALDEIDI CON SAGGIO DI FEHLING Glucosio Mettere una spatolata di glucosio in una provetta. Aggiungere 0.5 ml di una soluzione denominata Fehling A e 0.5 ml di una soluzione denominata Fehling B. Mettere la soluzione a scaldare a bagnomaria. Dopo qualche minuto si ha la precipitazione di Cu2O di colore rosso-mattone. NB: L eventuale colorazione verde è dovuta a reazioni secondarie ed indica saggio negativo. RICONOSCIMENTO DEI CHETONI CON SAGGIO DELLO IODOFORMIO Acetone gocce di acetone sono messe in una provetta. Si aggiungono circa 15 gocce di NaOH 2N e, quindi, goccia a goccia e agitando, una soluzione di I2 al 10% in KI acquoso al 20%, fino a persistenza di un lieve eccesso di iodio (colore rosso-bruno della soluzione). Si scalda la provetta a bagnomaria e si continua l aggiunta della soluzione fino ad ottenere nuovamente una colorazione rosso-bruna persistente per circa 2 minuti. Con l aggiunta di poche gocce di NaOH 2N sotto agitazione si elimina l eccesso di iodio e si lascia raffreddare la soluzione decolorata. Lo iodoformio precipita come solido cristallino giallo. 10
11 RICONOSCIMENTO DEI FENOLI CON CLORURO FERRICO Resorcina Ad una piccola quantità di fenolo o resorcina sciolto in 1 ml di acqua o di etanolo, si aggiungono 1-2 gocce di una soluzione acquosa o alcolica al 3% di FeCl3 e si osserva la variazione di colore. RICONOSCIMENTO DEI CARBOIDRATI CON SAGGIO DI MOLISH Glucosio Mettere una punta di spatola di glucosio nella provetta e sciogliere nella minima quantità di H2O. Aggiungere 2-3 gocce di α-naftolo e LAVORANDO ALLA CAPPA eseguire le seguenti operazioni cercando di NON AGITARE la provetta: tenendo la provetta con la pinza e lontano dagli occhi si fa scivolare qualche goccia di H2SO4 concentrato lungo la parete della provetta. All interfaccia tra H2SO4 e H2O si forma un anello di colore rosso violetto. RICONOSCIMENTO DI AMMINOACIDI CON NINIDRINA Sodio glutammato Mettere una punta di spatola di glutammato di sodio nella provetta. Sciogliere nella minima quantità di H2O. Aggiungere qualche goccia di ninidrina e scaldare a bagnomaria. Il saggio è positivo se compare lentamente una colorazione violetta. NB: la ninidrina macchia la pelle! usare i guanti durante l esecuzione del saggio e il lavaggio della provetta. RICONOSCIMENTO DI ALCALOIDI Caffeina Disciogliere in 5 ml di acqua posti in provetta qualche milligrammo di sostanza in esame, acidificare con HCl 2M e quindi aggiungere 1 ml di potassio iodobismutato. Si forma immediatamente un precipitato arancio o rossoarancio. RICONOSCIMENTO DI AMMINE PRIMARIE AROMATICHE Sulfamerazina In una provetta contenente circa 2 ml di acqua aggiungere una punta di spatola della sostanza da analizzare. Acidificare la soluzione con HCl 2M e aggiungere 0,2 ml di sodio nitrito soluzione. Dopo 1 o 2 min, aggiungere 1 ml di β-naftolo soluzione: si sviluppa una colorazione arancione o rossa intensa e generalmente si forma un precipitato dello stesso colore. 11
12 RICONOSCIMENTO DI BENZOATI Sodio benzoato In una provetta, aggiungere una punta di spatola della sostanza in esame e 1 ml di acqua. Aggiungere 0,5 ml di cloruro ferrico soluzione. Si forma un precipitato giallo-pallido, solubile in etere. RICONOSCIMENTO DI SALICILATI Sodio salicilato Preparare 1 ml di soluzione contente la sostanza in esame e acqua. Aggiungere 0,5 ml di cloruro ferrico soluzione. Si forma una colorazione violetta che persiste dopo aggiunta di 0,1 ml di acido acetico 2M. RICONOSCIMENTO DI TARTRATI Ac. tartarico A) Disciogliere circa 15 mg della sostanza in esame in 5 ml di acqua. Aggiungere 0,05 ml di una soluzione solfato ferroso e 0,05 ml di idrogeno perossido soluzione diluita. Si forma una colorazione gialla che svanisce rapidamente. Quando questa colorazione è svanita aggiungere, goccia a goccia, NaOH 2M. Si sviluppa una colorazione violetta o porpora. 12
Riconoscimento sostanza incognita FU
 1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
Riconoscimento sostanza incognita FU
 Riconoscimento sostanza incognita FU 1. Calcinazione: Carbonizza e non lascia residuo o caramellizza: Sostanza organica Determinazione p.f. Determinazione p.f. 1 determinazione primo capillare 2 determinazione
Riconoscimento sostanza incognita FU 1. Calcinazione: Carbonizza e non lascia residuo o caramellizza: Sostanza organica Determinazione p.f. Determinazione p.f. 1 determinazione primo capillare 2 determinazione
Sostanze organiche: determinazioni qualitative
 Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Sostanze organiche: determinazioni qualitative
 Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
TERZA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 TERZA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Terza Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbossilica Ricerca del Carattere Acido Saggio di Angeli e Rimini
TERZA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Terza Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbossilica Ricerca del Carattere Acido Saggio di Angeli e Rimini
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) H 2 SO 4. Quantità: Acido salicilico 5.0 g (PM = 138.
 ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
SESTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
QUARTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
QUARTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quarta Esperienza di Laboratorio Prove di solubilità Riconoscimento della funzione carbonilica Formazione di 2,4-dinitrofenilidrazoni (reazione
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
SECONDA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 SECONDA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Seconda Esperienza di Laboratorio Riconoscimento del doppio legame Saggio con KMnO 4 (Baeyer) Riconoscimento della struttura aromatica Saggio di
SECONDA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Seconda Esperienza di Laboratorio Riconoscimento del doppio legame Saggio con KMnO 4 (Baeyer) Riconoscimento della struttura aromatica Saggio di
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III
 LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a - 2 a ESERCITAZIONE Ø SAGGIO AL COCCIO Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE METALLORGANICHE Ø SAGGIO ALLA FIAMMA Ø SOLUBILITA
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE
 2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
2 e 3 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2011/2012 Prima di iniziare 1- ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
O CH 3 C COOH OH H + O
 Chimica rganica - Laboratorio A.A. 2012/13 Esperienza Sintesi dell acido acetilsalicilico (aspirina) 2 H CH 3 C CH 3 C H + C CH 3 CH 3 Reazione collaterale: H H H + H + H H Introduzione L aspirina è uno
Chimica rganica - Laboratorio A.A. 2012/13 Esperienza Sintesi dell acido acetilsalicilico (aspirina) 2 H CH 3 C CH 3 C H + C CH 3 CH 3 Reazione collaterale: H H H + H + H H Introduzione L aspirina è uno
Isolamento della caffeina dalle foglie di tè
 SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo)
 4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
TECNICHE DI PURIFICAZIONE. Cristallizzazione
 TECNICHE DI PURIFICAZIONE Cristallizzazione I composti organici solidi ottenuti nel corso delle reazioni non sono quasi mai puri, per cui è necessario adottare delle tecniche di purificazione in grado
TECNICHE DI PURIFICAZIONE Cristallizzazione I composti organici solidi ottenuti nel corso delle reazioni non sono quasi mai puri, per cui è necessario adottare delle tecniche di purificazione in grado
Acido 3,5-dinitrosalicilico Glucosio Acido 3-amino-5-nitrosalicilico Acido gluconico (Incolore-giallo leggero)
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione (Corso di Fisiologia della produzione e della post-raccolta) In banana durante il processo di maturazione
CHIMICA ORGANICA - laboratorio AA 2012/13
 CHIMICA ORGANICA - laboratorio AA 2012/13 Esperienza 1 SEPARAZIIONE ACIIDO--BASE.. CROMATOGRAFIIA ssu STRATO SOTTIILE ((TLC)).. L esperienza si propone di separare tre composti mediante estrazione da solvente
CHIMICA ORGANICA - laboratorio AA 2012/13 Esperienza 1 SEPARAZIIONE ACIIDO--BASE.. CROMATOGRAFIIA ssu STRATO SOTTIILE ((TLC)).. L esperienza si propone di separare tre composti mediante estrazione da solvente
REAZIONI ACIDO-BASE OSSERVARE, DESCRIVERE E DARE UNA SPIEGAZIONE DEI FENOMENI CHIMICI AVVENUTI
 ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
3011 Sintesi dell acido eritro-9,10-diidrossistearico dall acido oleico
 311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
QUINTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 QUINTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quinta Esperienza di Laboratorio Prove di solubilità Riconoscimento dei fenoli Reazione di Reimer-Tiemann Saggio con FeCl 3 Riconoscimento della
QUINTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Quinta Esperienza di Laboratorio Prove di solubilità Riconoscimento dei fenoli Reazione di Reimer-Tiemann Saggio con FeCl 3 Riconoscimento della
Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione
 1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
1 Determinazione di zuccheri riducenti e di amido in banana in relazione alle condizioni di conservazione In banana durante il processo di maturazione avviene la trasformazione di amido in zuccheri riducenti
Chimica Organica II - Laboratorio A.A. 2008/09 2. H 3 O+
 Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
DISPENSE DI LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III
 DISPENSE DI LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a- ESERCITAZIONE (D.P.I.: Occhiali guanti) Ø SAGGIO AL COCCIO (SOTTO CAPPA) Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE
DISPENSE DI LABORATORIO ANALISI CHIMICO FARMACEUTICA E TOSSICOLOGICA III 1 a- ESERCITAZIONE (D.P.I.: Occhiali guanti) Ø SAGGIO AL COCCIO (SOTTO CAPPA) Ø SOLUBILITA SOSTANZE ORGANICHE Ø SOLUBILITA SOSTANZE
SAGGI DI RICONOSCIMENTO DEI FENOLI
 SAGGI DI RICONOSCIMENTO DEI FENOLI pka = 9,89 OH OH OH Cl Cl OH OH Cl Cl Cl SAGGI DI RICONOSCIMENTO ADOPERATI: 1- Saggio con FeCl 3 2- Saggio con Acqua di Bromo 3- Formazione coloranti Azoici 4- Saggio
SAGGI DI RICONOSCIMENTO DEI FENOLI pka = 9,89 OH OH OH Cl Cl OH OH Cl Cl Cl SAGGI DI RICONOSCIMENTO ADOPERATI: 1- Saggio con FeCl 3 2- Saggio con Acqua di Bromo 3- Formazione coloranti Azoici 4- Saggio
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo
 1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5
1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
IV Gruppo: I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. nero. rosa-salmone. NiS
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Prima esperienza di Laboratorio. Alcune reazioni del rame
 Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Identificazione degli alcoli
 Identificazione degli alcoli R-OH Stato fisico Gli alcoli sono sostanze neutre caratterizzate dalla presenza di un gruppo ossidrilico legato ad un atomo di carbonio alifatico. I primi termini degli alcoli
Identificazione degli alcoli R-OH Stato fisico Gli alcoli sono sostanze neutre caratterizzate dalla presenza di un gruppo ossidrilico legato ad un atomo di carbonio alifatico. I primi termini degli alcoli
estrazione e poi una separazione, con una (TLC) di pg pigmenti (clorofille, caroteni ) estratto di foglie di spinaci o di fili d erba.
 Pigmenti da spinaci o foglie verdi In questa esperienza si effettuerà una estrazione e poi una separazione, con una cromatografia di adsorbimento in strato t sottile (TLC) di pg pigmenti (clorofille, caroteni
Pigmenti da spinaci o foglie verdi In questa esperienza si effettuerà una estrazione e poi una separazione, con una cromatografia di adsorbimento in strato t sottile (TLC) di pg pigmenti (clorofille, caroteni
4002 Sintesi del benzile dal benzoino
 4002 Sintesi del benzile dal benzoino H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Classificazione Tipo di reazione e classi di sostanze ssidazione; Alcol, chetone, metallo
4002 Sintesi del benzile dal benzoino H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Classificazione Tipo di reazione e classi di sostanze ssidazione; Alcol, chetone, metallo
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica
 NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
3016 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico
 6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
CRISTALLIZZAZIONE. Scelta del solvente: Affinché la cristallizzazione possa essere efficace, è necessario scegliere il solvente più
 CRISTALLIZZAZIONE La cristallizzazione è stata a lungo utilizzata nella purificazione delle sostanze. Si tratta essenzialmente di una tecnica di separazione solido-liquido molto importante per ricavare
CRISTALLIZZAZIONE La cristallizzazione è stata a lungo utilizzata nella purificazione delle sostanze. Si tratta essenzialmente di una tecnica di separazione solido-liquido molto importante per ricavare
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
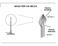 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
RICERCA DELLA FUNZIONE CARBOSSILICA
 RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
RICERCA DELLA FUNZIONE CARBOSSILICA IMPORTANTI ACIDI DI USO COMUNE ALCUNI IMPORTANTI ACIDI ALCUNI IMPORTANTI ACIDI NUMERO DI OSSIDAZIONE Preparazione degli Acidi Carbossilici Riconoscimento
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Alcaloidi: Caffeina. Alcaloidi: Caffeina. Cosimo Mansueto
 Cosimo Mansueto Gli alcaloidi sono una classe di sostanze naturali estremamente importante. Di origine soprattutto vegetale ma anche, in misura minore, animale e da microorganismi, sono caratterizzati
Cosimo Mansueto Gli alcaloidi sono una classe di sostanze naturali estremamente importante. Di origine soprattutto vegetale ma anche, in misura minore, animale e da microorganismi, sono caratterizzati
Sintesi dell acetanilide
 Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
SAGGI DI RICONOSCIMENTO DEI FENOLI
 SAGGI DI RICONOSCIMENTO DEI FENOLI SAGGI DI RICONOSCIMENTO ADOPERATI: 1- Saggio con FeCl 3 2- Saggio con Acqua di Bromo 3- Formazione coloranti Azoici 4- Saggio di Liebermann (Indofenolo) 5- Saggio
SAGGI DI RICONOSCIMENTO DEI FENOLI SAGGI DI RICONOSCIMENTO ADOPERATI: 1- Saggio con FeCl 3 2- Saggio con Acqua di Bromo 3- Formazione coloranti Azoici 4- Saggio di Liebermann (Indofenolo) 5- Saggio
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone)
 1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone) H acido polifosforico (PPA) C 9 H 10 2 (150.2) C 9 H 8 (132.2) Classificazione Tipo di reazione e classi
1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone) H acido polifosforico (PPA) C 9 H 10 2 (150.2) C 9 H 8 (132.2) Classificazione Tipo di reazione e classi
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico
 3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
PROGRAMMAZIONE DI LABORATORIO: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E DI ORGANIZZAZIONE INDUSTRIALE
 PROGRAMMAZIONE DI LABORATORIO: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E DI ORGANIZZAZIONE INDUSTRIALE IV D chimica a.s. 2013/2014 ITIS PASCAL sede Via dei Robilant Docente Gaetana Mirabelli
PROGRAMMAZIONE DI LABORATORIO: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E DI ORGANIZZAZIONE INDUSTRIALE IV D chimica a.s. 2013/2014 ITIS PASCAL sede Via dei Robilant Docente Gaetana Mirabelli
Materiale occorrente. Introduzione. Procedura. Estrazione della caffeina dalla polvere di caffè. Caffè macinato. Diclorometano, CH2Cl2
 Estrazione della caffeina dalla polvere di caffè Materiale occorrente Caffè macinato Diclorometano, CH2Cl2 Carbonato di calcio, CaCO3 Acqua Introduzione In questa esperienza viene proposta l estrazione
Estrazione della caffeina dalla polvere di caffè Materiale occorrente Caffè macinato Diclorometano, CH2Cl2 Carbonato di calcio, CaCO3 Acqua Introduzione In questa esperienza viene proposta l estrazione
Analisi di farmaci inorganici XI esercitazione di laboratorio
 Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
CROMATOGRAFIA. Tecniche di purificazione
 CROMATOGRAFIA Tecniche di purificazione La cromatografia è tra i metodi fisici più impiegati per la separazione e la purificazione dei composti organici. Principio base (valido per tutte le tecniche cromatografiche)
CROMATOGRAFIA Tecniche di purificazione La cromatografia è tra i metodi fisici più impiegati per la separazione e la purificazione dei composti organici. Principio base (valido per tutte le tecniche cromatografiche)
BENZILPENICILLINA BENZATINICA PREPARAZIONE INIETTABILI. Benzilpenicillina Benzatinica polvere sterile per preparazioni iniettabili
 1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
Fe(OH) 3. Mn(OH) 2. bianco. MnO 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Sintesi verde malachite
 Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide
 1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Classificazione Tipo di reazione e classi
1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Classificazione Tipo di reazione e classi
A) Determinazione gravimetrica di manganese(ii) e di zinco(ii)
 UNIVERSITA DEGLI STUDI DI NAPOLI FEDERICO II A.A. 2015/16 Laurea triennale in CHIMICA ANALITICA I E LABORATORIO CHIMICA INDUSTRIALE Determinazione della percentuale di manganese(ii) e Esercitazione n 15
UNIVERSITA DEGLI STUDI DI NAPOLI FEDERICO II A.A. 2015/16 Laurea triennale in CHIMICA ANALITICA I E LABORATORIO CHIMICA INDUSTRIALE Determinazione della percentuale di manganese(ii) e Esercitazione n 15
CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale
 CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale ESERCITAZIONE N 4 bis Stati di ossidazione del manganese Il manganese è un tipico elemento di transizione del blocco d.
CORSO DI LABORATORIO DI CHIMICA Corso di Laurea triennale in Chimica Industriale ESERCITAZIONE N 4 bis Stati di ossidazione del manganese Il manganese è un tipico elemento di transizione del blocco d.
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI:
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
MISURA DEL Δ 0 IN COMPLESSI OTTAEDRICI DI Cr(III)
 MISURA DEL Δ 0 IN COMPLESSI OTTAEDRICI DI Cr(III) Obiettivi delle prossime esperienze: 1. Sintetizzare complessi di Cr(III): nella prima esperienza, tris-etilendiammina Cr(III) [Cr(en) 3 ]Cl 3 e triossolato
MISURA DEL Δ 0 IN COMPLESSI OTTAEDRICI DI Cr(III) Obiettivi delle prossime esperienze: 1. Sintetizzare complessi di Cr(III): nella prima esperienza, tris-etilendiammina Cr(III) [Cr(en) 3 ]Cl 3 e triossolato
CROMATOGRAFIA INTRODUZIONE TEORICA. OBIETTIVO: riuscire a separare i vari componenti dell inchiostro
 CROMATOGRAFIA INTRODUZIONE TEORICA La separazione di miscugli complessi, composti da molti componenti, può avvenire attraverso una tecnica chiamata cromatografia. Le tecniche cromatografiche sono dei metodi
CROMATOGRAFIA INTRODUZIONE TEORICA La separazione di miscugli complessi, composti da molti componenti, può avvenire attraverso una tecnica chiamata cromatografia. Le tecniche cromatografiche sono dei metodi
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
3021 Ossidazione dell antracene ad antrachinone
 ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ESPERIENZA 4. Permanganometria
 ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
ESPERIENZA 4 Permanganometria Il permanganato di potassio è uno dei titolanti più frequentemente usati nell analisi volumetrica per via redox. Può essere usato in soluzione acida, neutra o leggermente
1023 Separazione dell esperidina dalla buccia d arancia
 NP 0 Separazione dell esperidina dalla buccia d arancia buccia d'arancia H H C H H H H H H H CH C 8 H 5 (60.5) Classificazione Tipo di reazione e classi di sostanze Separazione di composti da prodotti
NP 0 Separazione dell esperidina dalla buccia d arancia buccia d'arancia H H C H H H H H H H CH C 8 H 5 (60.5) Classificazione Tipo di reazione e classi di sostanze Separazione di composti da prodotti
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
Riconoscimento dei Glucidi (Glucosio):
 Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
Riconoscimento dei Glucidi (Glucosio): Materiale occorrente: Soluzione di Glucosio Liquido di Feheling A (soluzione di solfato rameico pentaidrato (CuSO 4 5 H 2 O)) Liquido di Feheling B (soluzione di
4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico
 NP 4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico H 3 C (CH 2 ) 8 I Cu + CH 2 CH 3 H 3 C (CH 2 ) 8 + CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198.3)
NP 4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico H 3 C (CH 2 ) 8 I Cu + CH 2 CH 3 H 3 C (CH 2 ) 8 + CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198.3)
Sostanza pura. Il termine sostanza indica il tipo di materia di cui è fatto un corpo.
 Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
Sostanza pura Il termine sostanza indica il tipo di materia di cui è fatto un corpo. Corpi formati da un unico tipo di materia sono costituiti da sostanze pure. Una sostanza pura ha composizione definita
5007 Reazione dell anidride ftalica con la resorcina per formare fluoresceina
 57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE
 ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE Materiale: un pallone da 100 ml, una colonna di frazionamento, una testa di distillazione, un termometro, un refrigerante, un raccordo
ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE Materiale: un pallone da 100 ml, una colonna di frazionamento, una testa di distillazione, un termometro, un refrigerante, un raccordo
SAGGI SPECIFICI ACIDI CARBOSSILICI
 SAGGI SPECIFICI ACIDI CARBOSSILICI Acido Acetilsalicilico: - Per riscaldamento a secco con Ca(OH) 2 sviluppa acetone i cui vapori, a contatto con una cartina imbevuta di o-nitrobenzaldeide, la colorano
SAGGI SPECIFICI ACIDI CARBOSSILICI Acido Acetilsalicilico: - Per riscaldamento a secco con Ca(OH) 2 sviluppa acetone i cui vapori, a contatto con una cartina imbevuta di o-nitrobenzaldeide, la colorano
ESTRAZIONE SOLVENTI. tecnica di separazione e purificazione
 ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
ESTRAZIONE CON SOLVENTI tecnica di separazione e purificazione L estrazione con solventi è una tecnica di separazione e purificazione, frequentemente usata in laboratorio, basata sulla diversa distribuzione
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
Chimica Organica II - Laboratorio A.A. 2012/13
 Chimica rganica II - Laboratorio A.A. 2012/13 Esperienza N. 2 REAZINE DEL (-)(R)-2-TTANL CN IL p-tluen-slfnil CLRUR C 6 H 13 H H Cl S C 6 H 13 S H HCl Materiali: pallone ad un cono da 50 ml (cono 14/23)
Chimica rganica II - Laboratorio A.A. 2012/13 Esperienza N. 2 REAZINE DEL (-)(R)-2-TTANL CN IL p-tluen-slfnil CLRUR C 6 H 13 H H Cl S C 6 H 13 S H HCl Materiali: pallone ad un cono da 50 ml (cono 14/23)
4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico
 4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico H lievito C 8 H 12 3 C 8 H 14 3 (156.2) (158.2) Classificazione Tipo di reazione e classi di sostanze
4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico H lievito C 8 H 12 3 C 8 H 14 3 (156.2) (158.2) Classificazione Tipo di reazione e classi di sostanze
Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni
 Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
Estrazione. Il processo di estrazione con solventi è impiegato per l isolamento di
 Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
Purificazione di sostanze organiche 1. Cristallizzazione 2. Sublimazione 3. Distillazione 4. 5. Cromatografia 1 Il processo di estrazione con solventi è impiegato per l isolamento di sostanze da soluzioni
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Attività laboratoriale di «Trasformazione dei prodotti»
 Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Attività laboratoriale di «Trasformazione dei prodotti» IL PROCESSO DELLA SAPONIFICAZIONE DEI GLICERIDI - IDROLISI BASICA DEI TRIGLICERIDI DELL OLIO D OLIVA TITOLO: «SAPER PREPARARE UN SAPONE» CLASSE:
Analisi Chimica Relazione
 Titolo Pagina 1 di 6 20/01/2006 Analisi Chimica Relazione Determinazione del manganese presente in un acciaio per via colorimetrica Obiettivo Determinare la quantità di manganese presente in un acciaio
Titolo Pagina 1 di 6 20/01/2006 Analisi Chimica Relazione Determinazione del manganese presente in un acciaio per via colorimetrica Obiettivo Determinare la quantità di manganese presente in un acciaio
PRINCIPIO TESTATO: reazioni di sintesi, doppio scambio con precipitazione, eso-endotermiche e di ossido-riduzione.
 TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
