DETERMINAZIONE SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA SPETTROFOTOMETRICA
|
|
|
- Luciana Piazza
- 7 anni fa
- Visualizzazioni
Transcript
1 DETERMINAZIONE SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA SPETTROFOTOMETRICA L obiettivo di questa esperienza è quello di studiare la cinetica della reazione tra una soluzione del noto colorante cristallo violetto (denominato d ora in poi con la sigla CV + ) e NaOH presente in eccesso Man a mano che avviene la reazione, la soluzione, inizialmente di colore blu-viola, si decolora sino a diventare incolore. Tale tipo di reazione può essere facilmente studiato per via spettrofotometrica, facendo misure di assorbanza in funzione del tempo e supponendo valida la legge di Lambert Beer. La seguente figura mostra lo spettro di una soluzione acquosa di CV + in assenza di NaOH. 1
2 La banda responsabile del colore blu-viola è quella intensa avente un massimo a 592 nm. Se eseguiamo delle misure nel tempo, dopo aver mescolato la soluzione di CV + con una soluzione di NaOH, osserveremo che la densità ottica della banda diminuisce lentamente sino a confondersi con la linea di base quando la soluzione è diventata incolore. In altre parole l intensità della banda è direttamente proporzionale alla concentrazione di CV + presente a un dato istante. Applicando la legge di Lambert Beer avremo A t( ) ( t) c t dove A t () è l assorbanza della soluzione alla lunghezza d onda e a un dato istante t, c t è la concentrazione del reagente CV + rimasto al tempo t, è il coefficiente di estinzione molare della banda e t è lo spessore della celletta utilizzata per contenere la soluzione. Utilizzando un ambiente termostatato ed eseguendo le misure a più temperature, possiamo inoltre studiare come la cinetica della reazione dipende dalla temperatura elaborando i dati ottenuti mediante l equazione di Arrhenius. 2
3 DESCRIZIONE DELLO SPETTROFOTOMETRO Lo spettrofotometro utilizzato per misurare l assorbanza è stato realizzato in laboratorio per scopi didattici: esso funziona come un colorimetro in grado di misurare l intensità della luce proveniente da un campione colorato, che viene illuminato con un diodo led. Quest ultimo deve avere un responso spettrale tale da eccitare il campione nella zona dove vi è la banda di assorbimento. Nel caso del cristallo violetto va bene un diodo led di colore verde, che possiede un responso spettrale compreso tra 500 e 600 nm. Come rivelatore viene usato un sensore ottico con elettronica integrata e relativo microprocessore in grado di visualizzare su un display a cristalli liquidi l intensità della luce che arriva sul rivelatore. Il sistema costituito dalla sorgente led, porta campioni e sensore ottico sono alloggiati all interno di un termostato in modo da effettuare delle misure di cinetica a temperatura costante. Quest ultima viene impostata direttamente dal microprocessore. In laboratorio sono disponibili 2 colorimetri diversi di cui uno utilizzante un singolo led verde come sorgente luminosa, denominato PICCOL e un altro un led RGB, denominato ARDUCOL, utilizzante la nota piattaforma ARDUINO in grado di eccitare il campione con 3 sorgenti a diverso responso spettrale. Istruzioni d uso del colorimetro con singolo led (PICCOL) Per impostare la temperatura della camera termostatica e misurare l intensità della luce che esce dal campione illuminato con una sorgente led verde, sono necessarie le seguenti operazioni: 1. Accendere lo strumento. Sul display compariranno le seguenti informazioni: - T ovvero la temperatura attuale della camera termostatica in cui alloggia la sorgente, il porta campioni e il rilevatore - Ts ovvero la temperatura da impostare sul termostato - P% ovvero la potenza in percentuale da inviare all elemento riscaldante (es. una resistenza) per portare il sistema alla temperatura Ts - mv ovvero l intensità del segnale, in mv, in uscita dal sensore ottico. 2. Impostare la temperatura tenendo premuto il tasto A sino a che sul display non compare la scritta Immetti Tset. Digitare la temperatura con la tastiera (es. 28 C) e premere F per terminare. Successivamente tenere premuto il tasto B sino a che non compare la scritta Immetti Power(%). Digitare la potenza (es. 40%) e premere F per terminare. 3
4 Istruzioni d uso del colorimetro con led RGB (ARDUCOL) ARDUCOL è costituito dalle seguenti parti: una sorgente luminosa utilizzante un led RGB a catodo comune in modo da scegliere la banda opportuna per eccitare correttamente il campione un rivelatore ottico costituito dall'integrato TSL230RP-LF che contiene al suo interno un fotodiodo e un convertitore corrente-frequenza programmabile. Tale tipo di sensore è estremamente sensibile e fornisce un segnale con frequenza direttamente proporzionale all'intensità di luce. un sensore di temperatura LM35 utilizzato per controllare la temperatura del portacampioni la scheda "open source" ARDUINO UNO montata all interno di un vecchio conduttimetro AMEL non più funzionante. un portacellette un box di polistirolo con regolatore di temperatura, che permette di eseguire le misure cinetiche mantenendo la temperatura costante. 4
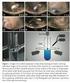
5 La seguente foto il portacampioni. Su quest'ultimo sono stati già montati sia il led RGB che i 2 sensori. Inoltre il led e il rivelatore TSL230RP-LF sono stati allineati otticamente, in modo da avere in uscita il massimo segnale. Per eseguire misure cinetiche a temperatura costante il porta campioni viene inserito all interno di un box di polistirolo funzionante da camera termostatica. La temperatura viene impostata tramite un apparecchio elettronico costruito ad hoc. Per leggere l intensità del segnale in uscita dal rivelatore e conoscere la temperatura della camera, è necessario accendere lo strumento e premere il pulsante di RESET che si trova sul retro. Il microprocessore visualizzerà l intensità luminosa espressa in u.a. direttamente sul display assieme al valore della temperatura. Sotto il display vi sono 3 potenziometri, che permettono di impostare l intensità dei 3 led ROSSO, VERDE e BLU. PARTE SPERIMENTALE 1 parte : VERIFICA LEGGE DI LAMBERT BEER PRODOTTI CHIMICI : Una soluzione 7.5 x 10-5 M di CV ottenuta pesando m 34. 0mg e portando a volume in un matraccio da 1 L 0.9 Acqua distillata 5
6 APPARECCHIATURA: 1 matraccio tarato da 1L 5 matracci tarati da 25 ml 1 pipetta da 10 ml con pompetta 1 colorimetro 1 contagocce 2 cellette di quarzo con tappo Un box di polistirolo funzionante come termostato PROCEDURA : 1. Si prepara una soluzione circa 7.5 x 10-5 M di CV pesando circa 34.0 mg di CV e portando a volume con acqua distillata in un matraccio da 1L. 2. La seguente tabella riporta i volumi V(ml) di soluzione madre da prelevare con la pipetta e da sgocciolare in matracci tarati da 25 ml per preparare delle soluzioni aventi concentrazioni C sol comprese tra 6 x 10-6 M e 3.6 x 10-5 M: Sol. Partenza c=7.5 x 10-5 M C sol (moli/litro) 6.0 x x x x x V(ml) 3. Una volta che il sistema ha raggiunto la temperatura prevista per l esperienza, inserire nel porta campioni una celletta metallica, che interrompendo la luce, permette di misurare il cosiddetto SEGNALE DI BUIO e annotare il valore in mv riportato sul display. 4. Inserire nel portacampioni una cella contenente acqua distillata (oppure riempire per circa 2/3 una celletta con acqua) e annotare il valore in mv relativo al cosiddetto SEGNALE DI RIFERIMENTO. 5. Riempire con la prima soluzione di CV (c=6.0 x 10-6 M) un altra celletta vuota per circa 2/3, utilizzando un contagocce e metterla nel porta campioni al posto della celletta contenente l acqua. 6. Annotare l intensità del segnale in mv. 7. Misurare l intensità delle altre soluzioni riportate nella tabella sopra. 8. Per ogni soluzione ricavare l assorbanza mediante la seguente formula: 6
7 A log 10 I ( I rif camp. I I buio buio ) 2 a PARTE : Determinazione della costante cinetica k del pseudo primo ordine a T costante (25 C), operando in eccesso di NaOH e verifica dell ordine di reazione rispetto a NaOH e determinazione della costante di velocità specifica del 2 ordine k 2. PRODOTTI CHIMICI : Una soluzione 7.5 x 10-5 M di CV ottenuta pesando m 34. 0mg e portando a volume in un matraccio da 1 L 0.9 Acqua distillata Sol. NaOH 0.1 M APPARECCHIATURA: 2 cilindri graduati da 25 ml 1 beuta da 100 ml 2 pipette da 10 ml con pompetta 1 colorimetro 2 cellette di quarzo con tappo Un termostato Le misure vanno eseguite a temperatura costante all interno di un box di polistirolo termostatato. Un cronometro 1. Preparare le seguenti soluzioni utilizzando 2 cilindri da 25 ml con tappo denominati con le lettere A e B. 7
8 CILINDRO A da 25 ml CILINDRO B da 25 ml n. ml CV (7.5 x 10-5 M) ml H 2 O ml ml H 2 O esperienza NaOH(0.1M) OSSERVAZIONE La quantità di colorante utilizzata è stata determinata tenendo conto che dalle misure effettuate precedentemente per verificare la legge di Lambert Beer, si è visto che la concentrazione ottimale del colorante per eseguire delle misure di assorbanza deve essere compresa tra 6 x 10-6 M e 7.5 x 10-5 M. Tale concentrazione è quella effettiva dopo il mescolamento del colorante con NaOH. (Usando nel mescolamento volumi uguali di colorante e di NaOH,la concentrazione risultante sia di CV che di NaOH sarà la metà di quella iniziale. In questa esperienza è stata scelta una concentrazione effettiva pari a 7.5 x 10-6 M. 2. Mettere i 2 cilindri contenenti le soluzioni relative alla prima esperienza a termostatare nella scatola di polistirolo (o nella camera termostatica) assieme a 2 cellette e a una beuta da 100 ml. 3. Impostare la temperatura del termostato a 25 C. (N.B Il termostato contiene al suo interno già lo spettrofotometro!). 4. Misurare l intensità del segnale di BUIO e del segnale di RIFERIMENTO. 5. Dopo una decina di minuti estrarre velocemente dal termostato i due cilindri A e B, poi versare il loro contenuto nella beuta da 100 ml facendo contemporaneamente partire il cronometro. Dopo aver ben mescolato la soluzione contenuta nella beuta, versare alcuni ml nella celletta e misurare l intensità del segnale ad intervalli di circa 30 secondi per circa 15 minuti. 6. Ripetere le misure con le altre soluzioni riportate nella tabella sopra. 3 a PARTE :INFLUENZA DELLA TEMPERATURA SULLA COSTANTE DI VELOCITA PRODOTTI CHIMICI : COME SOPRA APPARECCHIATURA: COME SOPRA 8
9 1. Prelevare con una pipetta da 10 ml 5 ml di soluzione 7.5 x 10-5 M di CV, preparata precedentemente e sgocciolarli all interno di un cilindro graduato da 25 ml. Successivamente mettere il cilindro a termostatare (T=22 C), dopo averlo portato a volume con acqua distillata. 2. Prelevare con un altra pipetta da 5 ml 2 ml di NaOH 0.1M e sgocciolarli all interno di un altro cilindro da 25 ml. Successivamente portare il cilindro a volume e metterlo a termostatare (T=22 C). 3. Mettere una beuta vuota da 100 ml e le cellette a termostatare. 4. Estrarre velocemente dal termostato i 2 cilindri e la beuta, poi versare in quest ultima il contenuto dei 2 cilindri e far partire contemporaneamente il cronometro. Dopo aver ben mescolato la soluzione contenuta nella beuta, versare alcuni ml nella celletta e misurare l intensità del segnale. 5. Ripetere i punti 1-5 operando a temperature diverse (es. 25 C, 28 C, 32 C, 35 C). ELABORAZIONE DEI DATI 1) 1 parte : VERIFICA LEGGE DI LAMBERT BEER Verificare la legge di Lambert Beer con il metodo dei minimi quadrati. 2) Determinazione della costante cinetica k del pseudo primo ordine a T costante (25 C), operando in eccesso di NaOH e verifica dell ordine di reazione rispetto a NaOH e determinazione della costante di velocità specifica del 2 ordine k 2. Supponendo che il meccanismo avvenga in un solo stadio, l equazione cinetica assume la seguente forma Velocità = k[cv + ] m [OH - ] n Essendo OH - presente in eccesso rispetto a CV +, possiamo ritenere costante il termine [OH - ] n e inglobarlo nella costante k. Pertanto se poniamo k = k[oh - ] n, avremo che Velocità = k [CV + ] m Come verificheremo col calcolo, la reazione in questione segue una cinetica del primo ordine, per cui m=1 e quindi Velocità = k [CV + ] 9
10 Indicando con a la concentrazione iniziale di CV + e con x la concentrazione del prodotto al tempo t e ponendo v= -d[cv + ]/dt = d[prodotto]/dt, avremo che l equazione cinetica diventa dx/dt = k (a-x) Integrando opportunamente tale equazione differenziale, avremo a ln k' t a x Indicando con A 0 e con A t le assorbanze della soluzione a 592 nm misurate rispettivamente a tempo 0 e a tempo t e applicando La Legge di Lambert Beer,avremo quanto segue: A t A t a 0 t ( a x) A ln 0 A t k't ovvero ln A t = ln A 0 k t Riportando in un grafico il ln A t (asse y) in funzione di t (asse x), otteniamo un andamento rettilineo, in cui k, ovvero la costante di velocità specifica, corrisponde alla pendenza della retta. Eseguire una regressione lineare con lo strumento REGRESSIONE di EXCEL e riportare il valore di k con un livello di fiducia del 95%. Per quanto riguarda la determinazione dell ordine di reazione rispetto a OH - (ovvero n), basta tenere conto delle seguenti relazioni: k =k[oh - ] n ln k = ln k + n ln[oh - ] Ponendo y=ln k ; x= ln[oh - ] ; a=ln k ; b =n, È possible ricavare n applicando il metodo dei minimi quadrati ai dati ottenuti con la seconda parte dell esperienza. 3 a PARTE: INFLUENZA DELLA TEMPERATURA SULLA COSTANTE DI VELOCITA 10
11 Esiste una equazione fenomenologica, introdotta da Arrhenius, che riporta come varia la velocità di una reazione chimica al variare di T ln k = cost - E attiv. /RT dove k è la costante di velocità specifica della reazione, relativamente a un singolo stadio cinetico, E attiv. è l energia di attivazione e R è la costante dei gas. Se ricaviamo la costante di velocità specifica di una reazione a varie temperature, possiamo ricavare l energia di attivazione dalla pendenza della retta che è uguale a - E attiv. /R ovvero applicando il metodo dei minimi quadrati ai dati ottenuti con la terza parte dell esperienza. BIBLIOGRAFIA 1)G.Corsaro, J.Chem.Educ. 1964,41, )J.C.Turgeon and V.K.LaMer, J. Am. Chem. Soc.1952,74,
STUDIO SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA CONDUTTOMETRICA
 STUDIO SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA CONDUTTOMETRICA Lo scopo di questa esperienza è quello di vedere come sia possibile studiare, da un punto di vista cinetico, l'evolversi
STUDIO SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA CONDUTTOMETRICA Lo scopo di questa esperienza è quello di vedere come sia possibile studiare, da un punto di vista cinetico, l'evolversi
MISURE SPERIMENTALI DI CONDUCIBILITA DI ELETTROLITI FORTI
 MISURE SPERIMENTALI DI CONDUCIBILITA DI ELETTROLITI FORTI APPARECCHIATURA: - Conduttimetro CRISON GLP 31+ - Cella conduttometria - Bagno termostatico - Termometro - Bicchiere da 100 ml - 2 matracci da
MISURE SPERIMENTALI DI CONDUCIBILITA DI ELETTROLITI FORTI APPARECCHIATURA: - Conduttimetro CRISON GLP 31+ - Cella conduttometria - Bagno termostatico - Termometro - Bicchiere da 100 ml - 2 matracci da
DETERMINAZIONE SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA SPETTROFOTOMETRICA
 DETERMINAZIONE SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA SPETTROFOTOMETRICA L obiettivo di questa esperienza è quello di studiare la cinetica della reazione tra una soluzione acida di
DETERMINAZIONE SPERIMENTALE DELLA CINETICA DI UNA REAZIONE CHIMICA PER VIA SPETTROFOTOMETRICA L obiettivo di questa esperienza è quello di studiare la cinetica della reazione tra una soluzione acida di
MA + H + MAH + Materiale: 500 cc di soluzione di NaOH 0.01 M 500 cc di soluzione di HCl 0.01 M fresca Metil-arancio (MA) Etanolo Acqua distillata
 Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
Cambiamenti nell aspetto degli spettri di assorbimento elettronico del metilarancio in funzione del ph a seguito della reazione di protonazione del metilarancio. Scopo dell esperimento è osservare la variazione
DETERMINAZIONE DEL CONTENUTO IN CAFFEINA
 DETERMINAZIONE DEL CONTENUTO IN CAFFEINA (PER VIA SPETTROFOTOMETRICA ATTRAVERSO LA COSTRUZIONE DELLA RETTA DI TARATURA). O CH 3 H 3 C 1 6 N N 7 5 2 8 O N N 3 4 9 CH 3 Caffeina (1,3,7-trimetil-3,7-diidro-1H-purin-2,6-dione)
DETERMINAZIONE DEL CONTENUTO IN CAFFEINA (PER VIA SPETTROFOTOMETRICA ATTRAVERSO LA COSTRUZIONE DELLA RETTA DI TARATURA). O CH 3 H 3 C 1 6 N N 7 5 2 8 O N N 3 4 9 CH 3 Caffeina (1,3,7-trimetil-3,7-diidro-1H-purin-2,6-dione)
La legge. Il colorimetro. L esperienza. Realizzato da. August Beer ( ) Johann Heinrich Lambert ( )
 LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
LA LEGGE DI LAMBERT-BEER BEER Esperienza con il sensore colorimetrico La legge Il colorimetro August Beer (1825-1863) L esperienza Johann Heinrich Lambert (1728-1777) Realizzato da La legge di Lambert
Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo
 UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
UNIVERSITÀ DEGLI STUDI DI PAVIA CORSO DI LAUREA INTERFACOLTÀ IN BIOTECNOLOGIE Determinazione dell azoto totale e ammoniacale in spettrofotometria: modalità di calibrazione e confrontabilità nel tempo Relatore:
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile
 Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A
 1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
Esercitazione 1 PEROSSIDI IN OLIO D OLIVA
 Esercitazione 1 TITOLAZIONE ACIDO ACETICO IN ACETO E PEROSSIDI IN OLIO D OLIVA Acido acetico in aceto 2 L esperienza consiste nel misurare il grado di acidità di un aceto. L'aceto è una soluzione acquosa
Esercitazione 1 TITOLAZIONE ACIDO ACETICO IN ACETO E PEROSSIDI IN OLIO D OLIVA Acido acetico in aceto 2 L esperienza consiste nel misurare il grado di acidità di un aceto. L'aceto è una soluzione acquosa
ESERCITAZIONI CHIMICA-FISICA I a.a. 2012/2013. Metodo differenziale. Problema
 ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
Esperienze di spettrofotometria per la scuola, con arduino
 Esperienze di spettrofotometria per la scuola, con arduino Andrea Canesi (1), Daniele Grosso (2) 1. Ministero della Pubblica Istruzione Liceo Classico e Linguistico C. Colombo, Genova 2. Università di
Esperienze di spettrofotometria per la scuola, con arduino Andrea Canesi (1), Daniele Grosso (2) 1. Ministero della Pubblica Istruzione Liceo Classico e Linguistico C. Colombo, Genova 2. Università di
IN QUESTA PROVA ANDREMO A DETERMINARE L ACIDITA DI UN CAMPIONE DI LATTE MEDIANTE UNA TITOLAZIONE ACIDO-BASE
 IN QUESTA PROVA ANDREMO A DETERMINARE L ACIDITA DI UN CAMPIONE DI LATTE MEDIANTE UNA TITOLAZIONE ACIDO-BASE Prima di passare però al procedimento vero e proprio è necessario fornire alcune definizioni
IN QUESTA PROVA ANDREMO A DETERMINARE L ACIDITA DI UN CAMPIONE DI LATTE MEDIANTE UNA TITOLAZIONE ACIDO-BASE Prima di passare però al procedimento vero e proprio è necessario fornire alcune definizioni
Spettroscopia molecolare: interazioni luce-materia
 Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
FORMULARIO DI CHIMICA
 ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da:
 Analisi chimica strumentale Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da: (31.4) dove s y è la varianza dei valori
Analisi chimica strumentale Intervallo di fiducia del coefficiente angolare e dell intercetta L intervallo di fiducia del coefficiente angolare (b 1 ) è dato da: (31.4) dove s y è la varianza dei valori
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Università degli Studi di Milano Corso di Laurea in Chimica Industriale. Laboratorio di Processi e Impianti Industriali Chimici I
 Milano, marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione della ENSIONE DI VAPOE di un liquido a
Milano, marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione della ENSIONE DI VAPOE di un liquido a
CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA - A.A
 CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA - A.A. 00-0 Turno: Nome Studenti Gruppo: Data SCHEMA RIASSUNTIO DELL'ESPERIENZA DI ELETTROLISI. Preparare la soluzione elettrolitica
CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA - A.A. 00-0 Turno: Nome Studenti Gruppo: Data SCHEMA RIASSUNTIO DELL'ESPERIENZA DI ELETTROLISI. Preparare la soluzione elettrolitica
Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L (include l errata corrige del dicembre 2002)
 Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L 00.00-6 (include l errata corrige del dicembre 2002) Ricerche su Alimenti ( L35LMBG ) Determinazione di Ammine Aromatiche Primarie
Traduzione integrale ( non ufficiale) del metodo L35 LMBG Gennaio 1995 L 00.00-6 (include l errata corrige del dicembre 2002) Ricerche su Alimenti ( L35LMBG ) Determinazione di Ammine Aromatiche Primarie
Spettroscopia UV-visibile
 Spettroscopia UV-visibile Cosa si misura: Trasmittanza ed Assorbanza Molti composti assorbono la radiazione elettromagnetica nelle regioni del visibile (vis) e dell ultravioletto (UV). Nel diagramma sottostante
Spettroscopia UV-visibile Cosa si misura: Trasmittanza ed Assorbanza Molti composti assorbono la radiazione elettromagnetica nelle regioni del visibile (vis) e dell ultravioletto (UV). Nel diagramma sottostante
Estrazione di acido salicilico con acetato di n-butile
 S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Estrazione di acido salicilico con acetato di n-butile L estrazione liquido-liquido
CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA
 CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA Turno: Nome Studenti Gruppo: Data ----------------------------------------------------------------------------------- Al termine dell
CORSO DI LAUREA TRIENNALE IN SCIENZE BIOLOGICHE LABORATORIO DI FISICA Turno: Nome Studenti Gruppo: Data ----------------------------------------------------------------------------------- Al termine dell
DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE
 DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE Comparazione dei risultati ottenuti con il metodo dell additività delle assorbanze e il metodo di analisi per regressione lineare a diverse lunghezze d
DETERMINAZIONE CONTEMPORANEA DI CROMO E MANGANESE Comparazione dei risultati ottenuti con il metodo dell additività delle assorbanze e il metodo di analisi per regressione lineare a diverse lunghezze d
DETERMINAZIONE DEL pk a DI UN INDICATORE DA MISURE SPETTROFOTOMETRICHE
 DETERMINAZIONE DEL pk a DI UN INDICATORE DA MISURE SPETTROFOTOMETRICHE Con il nome di indicatori di ph vengono denominate delle sostanze in grado di assumere diverse colorazioni a seconda della concentrazione
DETERMINAZIONE DEL pk a DI UN INDICATORE DA MISURE SPETTROFOTOMETRICHE Con il nome di indicatori di ph vengono denominate delle sostanze in grado di assumere diverse colorazioni a seconda della concentrazione
Estrazione di pigmenti vegetali da sostanze naturali
 Estrazione di pigmenti vegetali da sostanze naturali Il cavolo rosso deve il suo colore agli antociani o antocianine, che sono una classe di pigmenti idrosolubili appartenente alla famiglia dei flavonoidi.
Estrazione di pigmenti vegetali da sostanze naturali Il cavolo rosso deve il suo colore agli antociani o antocianine, che sono una classe di pigmenti idrosolubili appartenente alla famiglia dei flavonoidi.
ESTRAZIONE CO. Scopo. Strumenti e sostanze. Principi teorici. Metodica. Calcoli. Malboro gold
 ESTRAZIONE CO Scopo Determinare i milligrammi di CO all interno di una sigaretta Strumenti e sostanze STRUMENTI: Becher, buretta, beuta, pipetta, matraccio, cappa, bilancia, bacchetta di vetro, ragno.
ESTRAZIONE CO Scopo Determinare i milligrammi di CO all interno di una sigaretta Strumenti e sostanze STRUMENTI: Becher, buretta, beuta, pipetta, matraccio, cappa, bilancia, bacchetta di vetro, ragno.
XVII ZOLFO. Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE. Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI
 XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
MISURA DELLA VELOCITA DELLA LUCE
 MISURA DELLA VELOCITA DELLA LUCE La misura della velocità della luce (c=3x10 8 m/s) effettuata su distanze dell ordine del metro richiede la misura di intervalli di tempo brevissimi (~3x10-9 s). Il metodo
MISURA DELLA VELOCITA DELLA LUCE La misura della velocità della luce (c=3x10 8 m/s) effettuata su distanze dell ordine del metro richiede la misura di intervalli di tempo brevissimi (~3x10-9 s). Il metodo
Esperienza di Polarimetria
 Esperienza di Polarimetria Docente di riferimento: Prof.ssa Marilena Di Valentin Si ringraziano il Dott. Antonio Barbon, Dott. Alfonso Zoleo e Prof.ssa Elisabetta Collini per avere contribuito al materiale
Esperienza di Polarimetria Docente di riferimento: Prof.ssa Marilena Di Valentin Si ringraziano il Dott. Antonio Barbon, Dott. Alfonso Zoleo e Prof.ssa Elisabetta Collini per avere contribuito al materiale
INTRODUZIONE ALLA SPETTROMETRIA
 INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
INTRODUZIONE ALLA SPETTROMETRIA La misurazione dell assorbimento e dell emissione di radiazione da parte della materia è chiamata spettrometria. Gli strumenti specifici usati nella spettrometria sono chiamati
PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE
 PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE ACIDO L-LATTICO su uova L acido L-lattico reagisce, per via enzimatica, con un derivato fenolico e induce la formazione di
PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA TRATTAMENTO DEL CAMPIONE ACIDO L-LATTICO su uova L acido L-lattico reagisce, per via enzimatica, con un derivato fenolico e induce la formazione di
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
FISICA. Elaborazione dei dati sperimentali. Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica
 FISICA Elaborazione dei dati sperimentali Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica LE GRANDEZZE FISICHE Una grandezza fisica è una quantità che può essere misurata con uno strumento
FISICA Elaborazione dei dati sperimentali Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica LE GRANDEZZE FISICHE Una grandezza fisica è una quantità che può essere misurata con uno strumento
ESERCITAZIONE N 1 DETERMINAZIONE DI ACIDO FOSFORICO NELLA COCA-COLA ] / [H 2 PO 4- ] HPO 4
![ESERCITAZIONE N 1 DETERMINAZIONE DI ACIDO FOSFORICO NELLA COCA-COLA ] / [H 2 PO 4- ] HPO 4 ESERCITAZIONE N 1 DETERMINAZIONE DI ACIDO FOSFORICO NELLA COCA-COLA ] / [H 2 PO 4- ] HPO 4](/thumbs/55/35880910.jpg) ESERCITAZIONE N 1 DETERMINAZIONE DI ACIDO FOSFORICO NELLA COCA-COLA Si titola con NaOH. H 3 PO 4 H + + H 2 PO 4 - K a1 = 1.1 x 10-2 = [H + ] [H 2 PO 4- ] / [H 3 PO 4 ] H 2 PO 4- H + + HPO 4 2- K a2 = 7.5
ESERCITAZIONE N 1 DETERMINAZIONE DI ACIDO FOSFORICO NELLA COCA-COLA Si titola con NaOH. H 3 PO 4 H + + H 2 PO 4 - K a1 = 1.1 x 10-2 = [H + ] [H 2 PO 4- ] / [H 3 PO 4 ] H 2 PO 4- H + + HPO 4 2- K a2 = 7.5
Valorizzazione delle produzioni vitifrutticole valtellinesi mediante metodi innovativi INNOVI
 Valorizzazione delle produzioni vitifrutticole valtellinesi mediante metodi innovativi INNOVI Attività 1 Sistemi portatili per misure rapide e non distruttive di parametri ottici di mirtillo, uva e mela
Valorizzazione delle produzioni vitifrutticole valtellinesi mediante metodi innovativi INNOVI Attività 1 Sistemi portatili per misure rapide e non distruttive di parametri ottici di mirtillo, uva e mela
A fine titolazione la concentrazione iniziale della soluzione da titolare risulta essere stata pari a:
 Titolazione acido-base Nella pratica di laboratorio è frequente la determinazione del ph incognito di una soluzione. Pensiamo ad esempio di voler conoscere il ph di un campione acquoso derivante da uno
Titolazione acido-base Nella pratica di laboratorio è frequente la determinazione del ph incognito di una soluzione. Pensiamo ad esempio di voler conoscere il ph di un campione acquoso derivante da uno
RISOLUZIONE ENO 25/2004
 DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
SPETTROFOTOMETRIA UV/VIS
 SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
DISPLAY A CRISTALLI LIQUIDI J-LCD
 DISPLAY A CRISTALLI LIQUIDI J-LCD 1 INDICE 1. Introduzione...3 2. Aspetto e dimensioni......3 2.1 Materiale e colori......3 2.2 Dimensioni display...3 3. Descrizione funzioni e pulsanti......4 3.1 Breve
DISPLAY A CRISTALLI LIQUIDI J-LCD 1 INDICE 1. Introduzione...3 2. Aspetto e dimensioni......3 2.1 Materiale e colori......3 2.2 Dimensioni display...3 3. Descrizione funzioni e pulsanti......4 3.1 Breve
Esercitazione 1a: Determinazione fotometrica dell antimonio
 Esercitazione 1a: Determinazione fotometrica dell antimonio Principio del metodo L antimonio(iii), presente in soluzione come catione antimonile (SbO + ) complessato dal tartrato (C 4 H 4 O 6 2- ), reagisce
Esercitazione 1a: Determinazione fotometrica dell antimonio Principio del metodo L antimonio(iii), presente in soluzione come catione antimonile (SbO + ) complessato dal tartrato (C 4 H 4 O 6 2- ), reagisce
ISTRUZIONI PROGRAMMAZIONE 14445
 ISTRUZIONI PROGRAMMAZIONE 14445 Per impostare il crontermostato elettronico, dalla videata base del display, premere uno qualsiasi dei quattro tasti frontali. Vengono visualizzate le icone: - Esc (tasto
ISTRUZIONI PROGRAMMAZIONE 14445 Per impostare il crontermostato elettronico, dalla videata base del display, premere uno qualsiasi dei quattro tasti frontali. Vengono visualizzate le icone: - Esc (tasto
 ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
ACIDITA su burro, margarine, panna e grassi semilavorati PRINCIPIO REAGENTI PREPARAZIONE DEL REAGENTE STABILITA PREPARAZIONE DEL CAMPIONE CONDIZIONI DI REAZIONE (Edit) Gli acidi grassi del campione, in
TeeJet 834 MANUALE OPERATIVO E DI PROGRAMMAZIONE - v Pag 1 di 8
 834 MANUALE 834 TeeJet 834 MANUALE OPERATIVO E DI PROGRAMMAZIONE - v1.02 - Pag 1 di 8 Funzione Azione/i Lettura iniziale Lettura successiva Computer: procedura di accensione Accensione Premere il tasto
834 MANUALE 834 TeeJet 834 MANUALE OPERATIVO E DI PROGRAMMAZIONE - v1.02 - Pag 1 di 8 Funzione Azione/i Lettura iniziale Lettura successiva Computer: procedura di accensione Accensione Premere il tasto
ISTITUTO TECNICO AGRARIO Carlo Gallini LABORATORIO DI CHIMICA Procedura Operativa Standard
 ISTITUTO TECNICO AGRARIO Carlo Gallini LABORATORIO DI CHIMICA Procedura Operativa Standard Determinazione del Titolo Alcolometrico Volumico effettivo mediante ebulliometro di Malligand (Metodo rapido)
ISTITUTO TECNICO AGRARIO Carlo Gallini LABORATORIO DI CHIMICA Procedura Operativa Standard Determinazione del Titolo Alcolometrico Volumico effettivo mediante ebulliometro di Malligand (Metodo rapido)
Misure di velocità con la guidovia a cuscino d aria (1)
 Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
Termografia a infrarossi
 Termografia a infrarossi Nella radiometria a microonde si verifica che hν
Termografia a infrarossi Nella radiometria a microonde si verifica che hν
L Oscillatore Armonico
 L Oscillatore Armonico Descrizione del Fenomeno (max 15) righe Una molla esercita su un corpo una forza di intensità F=-kx, dove x è l allungamento o la compressione della molla e k una costante [N/m]
L Oscillatore Armonico Descrizione del Fenomeno (max 15) righe Una molla esercita su un corpo una forza di intensità F=-kx, dove x è l allungamento o la compressione della molla e k una costante [N/m]
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO
 COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO L esercitazione è divisa in due parti. Nella prima parte si costruisce un voltmetro
COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO L esercitazione è divisa in due parti. Nella prima parte si costruisce un voltmetro
Dispense di Analisi Volumetrica
 Dispense di Analisi Volumetrica IIS Gobetti - Marchesini Casale sezione Tecnica Chimica e Materiali Analisi chimica, elaborazione dati e Laboratorio L analisi volumetrica è la procedura o il metodo analitico
Dispense di Analisi Volumetrica IIS Gobetti - Marchesini Casale sezione Tecnica Chimica e Materiali Analisi chimica, elaborazione dati e Laboratorio L analisi volumetrica è la procedura o il metodo analitico
Prodotto realizzato con il contributo della Regione Toscana nell'ambito dell'azione regionale di sistema. Laboratori del Sapere Scientifico
 Prodotto realizzato con il contributo della Regione Toscana nell'ambito dell'azione regionale di sistema Laboratori del Sapere Scientifico Liceo Statale C. Lorenzini Classico, Linguistico, Scientifico,Scienze
Prodotto realizzato con il contributo della Regione Toscana nell'ambito dell'azione regionale di sistema Laboratori del Sapere Scientifico Liceo Statale C. Lorenzini Classico, Linguistico, Scientifico,Scienze
DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE
 DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE La tecnica della calorimetria a scansione differenziale (DSC) permette di effettuare
DETERMINAZIONE DELLA TEMPERATURA ED ENTALPIA DI FUSIONE DELLO STAGNO MEDIANTE CALORIMETRIA A SCANSIONE DIFFERENZIALE La tecnica della calorimetria a scansione differenziale (DSC) permette di effettuare
Analisi Chimica Relazione
 Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
I grafici a torta. Laboratorio con EXCEL. 1 Come si costruisce un grafico a torta
 I grafici a torta 1 Come si costruisce un grafico a torta In un gruppo di 130 persone è stata condotta un indagine per sapere quale è la lingua più parlata, oltre l italiano. Gli intervistati potevano
I grafici a torta 1 Come si costruisce un grafico a torta In un gruppo di 130 persone è stata condotta un indagine per sapere quale è la lingua più parlata, oltre l italiano. Gli intervistati potevano
Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a
 Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a. 2001-2002 Daniela Favaretto* favaret@unive.it Stefania Funari* funari@unive.it *Dipartimento di Matematica Applicata Università
Appunti di Excel per risolvere alcuni problemi di matematica (I parte) a.a. 2001-2002 Daniela Favaretto* favaret@unive.it Stefania Funari* funari@unive.it *Dipartimento di Matematica Applicata Università
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link
 Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Laboratorio Materiali Introduzione Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link Userai un sensore
Progetto lauree scientifiche Scheda 2 Studente:. Scuola e classe: Data:.. Laboratorio Materiali Introduzione Programma DataStudio Sensore di moto PASPORT Interfaccia PASPORT-USB Link Userai un sensore
SIMULAZIONE - 29 APRILE QUESITI
 www.matefilia.it SIMULAZIONE - 29 APRILE 206 - QUESITI Q Determinare il volume del solido generato dalla rotazione attorno alla retta di equazione y= della regione di piano delimitata dalla curva di equazione
www.matefilia.it SIMULAZIONE - 29 APRILE 206 - QUESITI Q Determinare il volume del solido generato dalla rotazione attorno alla retta di equazione y= della regione di piano delimitata dalla curva di equazione
Capitolo Calcoli di equazioni
 Capitolo Calcoli di equazioni Questa calcolatrice grafica può risolvere i seguenti tre tipi di calcoli: Equazioni lineari con due ~ sei incognite Equazioni di ordine elevato (quadratiche, cubiche) Calcoli
Capitolo Calcoli di equazioni Questa calcolatrice grafica può risolvere i seguenti tre tipi di calcoli: Equazioni lineari con due ~ sei incognite Equazioni di ordine elevato (quadratiche, cubiche) Calcoli
MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO
 MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO Scopo dell esperienza è lo studio della propagazione delle onde sonore all interno di un tubo, aperto o chiuso, contenete aria o altri gas. Si verificherà
MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO Scopo dell esperienza è lo studio della propagazione delle onde sonore all interno di un tubo, aperto o chiuso, contenete aria o altri gas. Si verificherà
Sorgenti di luce Colori Riflettanza
 Le Schede Didattiche di Profilocolore IL COLORE Sorgenti di luce Colori Riflettanza Rome, Italy 1/37 La luce: natura e caratteristiche La luce è una radiazione elettromagnetica esattamente come lo sono:
Le Schede Didattiche di Profilocolore IL COLORE Sorgenti di luce Colori Riflettanza Rome, Italy 1/37 La luce: natura e caratteristiche La luce è una radiazione elettromagnetica esattamente come lo sono:
Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta.
 Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta. Reattivi: acido acetico; acetato di sodio; idrossido di ammonio e cloruro di ammonio; acqua distillata.
Materiale occorrente: una bilancia tecnica; due matracci da 250 ml; una pipetta tarata con propipetta. Reattivi: acido acetico; acetato di sodio; idrossido di ammonio e cloruro di ammonio; acqua distillata.
Risoluzione di problemi ingegneristici con Excel
 Risoluzione di problemi ingegneristici con Excel Problemi Ingegneristici Calcolare per via numerica le radici di un equazione Trovare l equazione che lega un set di dati ottenuti empiricamente (fitting
Risoluzione di problemi ingegneristici con Excel Problemi Ingegneristici Calcolare per via numerica le radici di un equazione Trovare l equazione che lega un set di dati ottenuti empiricamente (fitting
Le misure di tempo e frequenza
 Le misure di tempo e frequenza Le misure di tempo e frequenza costituiscono un importante branca delle misure elettriche ed elettroniche ed in generale delle misure di grandezze fisiche. E possibile raggiungere
Le misure di tempo e frequenza Le misure di tempo e frequenza costituiscono un importante branca delle misure elettriche ed elettroniche ed in generale delle misure di grandezze fisiche. E possibile raggiungere
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
OTOSYSTEM ED100 IRRIGATORE CALORICO
 OTOSYSTEM ED100 IRRIGATORE CALORICO SCHEDA TECNICA Rev. 3 L Irrigatore calorico ED100 è un apparecchiatura atta all ausilio della diagnosi delle turbe dell equilibrio. L irrigatore calorico ED100 è uno
OTOSYSTEM ED100 IRRIGATORE CALORICO SCHEDA TECNICA Rev. 3 L Irrigatore calorico ED100 è un apparecchiatura atta all ausilio della diagnosi delle turbe dell equilibrio. L irrigatore calorico ED100 è uno
Natura corpuscolare della luce: misura della costante di Planck utilizzando i diodi LED
 Natura corpuscolare della luce: misura della costante di Planck utilizzando i diodi LED 1. Introduzione e teoria Nell ambito della teoria corpuscolare della luce, la stessa è costituita da particelle (o
Natura corpuscolare della luce: misura della costante di Planck utilizzando i diodi LED 1. Introduzione e teoria Nell ambito della teoria corpuscolare della luce, la stessa è costituita da particelle (o
MANUALE RAPIDO DI INSTALLAZIONE SISTEMI FLEXA 2.0 CON TERMOSTATI TACTO E BLUEFACE INFORMAZIONI IMPORTANTI
 INFORMAZIONI IMPORTANTI YOUTUBE:Video di utilizzo e configurazione dei sistemi all indirizzo www.youtube.com/airzoneitalia SITO AZIENDALE: www.airzoneitalia.it TIPOLOGIE DI TERMOSTATI I termostati dovranno
INFORMAZIONI IMPORTANTI YOUTUBE:Video di utilizzo e configurazione dei sistemi all indirizzo www.youtube.com/airzoneitalia SITO AZIENDALE: www.airzoneitalia.it TIPOLOGIE DI TERMOSTATI I termostati dovranno
GARA NAZIONALE DI ELETTRONICA E TELECOMUNICAZIONI. Progetto di un sistema di riempimento e svuotamento di un contenitore.
 GARA NAZIONALE DI ELETTRONICA E TELECOMUNICAZIONI PROVA SCRITTA 25 NOVEMBRE 2008 Progetto di un sistema di riempimento e svuotamento di un contenitore. Un acquario situato in appartamento è collegato ad
GARA NAZIONALE DI ELETTRONICA E TELECOMUNICAZIONI PROVA SCRITTA 25 NOVEMBRE 2008 Progetto di un sistema di riempimento e svuotamento di un contenitore. Un acquario situato in appartamento è collegato ad
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
INFORMAZIONI TECNICHE
 INFORMAZIONI TECNICHE 003/01/TEC 09 ottobre 01 OGGETTO: BERETTA ECOMIX Egregi Collaboratori, Vi informiamo che a breve verrà commercializzata la caldaia a bassa emissione di Nox, denominata ECOMIX, nelle
INFORMAZIONI TECNICHE 003/01/TEC 09 ottobre 01 OGGETTO: BERETTA ECOMIX Egregi Collaboratori, Vi informiamo che a breve verrà commercializzata la caldaia a bassa emissione di Nox, denominata ECOMIX, nelle
CON L EUROPA INVESTIAMO NEL VOSTRO FUTURO Fondi Strutturali Europei Programmazione FSE PON "Competenze per lo sviluppo" Bando 2373
 CON L EUROPA INVESTIAMO NEL VOSTRO FUTURO Fondi Strutturali Europei Programmazione 2007-2013 FSE PON "Competenze per lo sviluppo" Bando 2373 26/02/2013 Piano integrato 2013 Codice progetto: C-2-FSE-2013-313
CON L EUROPA INVESTIAMO NEL VOSTRO FUTURO Fondi Strutturali Europei Programmazione 2007-2013 FSE PON "Competenze per lo sviluppo" Bando 2373 26/02/2013 Piano integrato 2013 Codice progetto: C-2-FSE-2013-313
MISURE DI VISCOSITA CON IL METODO DI STOKES
 MISURE DI VISCOSITA CON IL METODO DI STOKES INTRODUZIONE La viscosità di un fluido rappresenta l attrito dinamico nel fluido. Nel caso di moto in regime laminare, la forza di attrito è direttamente proporzionale
MISURE DI VISCOSITA CON IL METODO DI STOKES INTRODUZIONE La viscosità di un fluido rappresenta l attrito dinamico nel fluido. Nel caso di moto in regime laminare, la forza di attrito è direttamente proporzionale
Istruzioni di funzionamento. Sensore di livello capacitivo KNM. N. di disegno /00 04/2001
 Istruzioni di funzionamento Sensore di livello capacitivo N. di disegno 70642/00 04/200 KNM Indice Pagina Utilizzo conforme all applicazione ------------------------------------ 2 2 Montaggio ----------------------------------------------------------------
Istruzioni di funzionamento Sensore di livello capacitivo N. di disegno 70642/00 04/200 KNM Indice Pagina Utilizzo conforme all applicazione ------------------------------------ 2 2 Montaggio ----------------------------------------------------------------
ESERCITAZIONI 1 e 2: calcoli
 ESERCITAZIONI 1 e 2: calcoli L uso del foglio elettronico nel laboratorio di ispezione degli alimenti. Funzioni utilizzate negli esercizi e traduzione in inglese americano per l utilizzo su computer con
ESERCITAZIONI 1 e 2: calcoli L uso del foglio elettronico nel laboratorio di ispezione degli alimenti. Funzioni utilizzate negli esercizi e traduzione in inglese americano per l utilizzo su computer con
SCHEDA DI LABORATORIO
 SCHEDA DI LABORATORIO Elettrolisi dell Acqua e Separazione Elettrolitica di un Metallo Premessa Teorica Connessione tra materia e la carica elettrica Metodo per misurare la carica elettrica mediante elettrolisi
SCHEDA DI LABORATORIO Elettrolisi dell Acqua e Separazione Elettrolitica di un Metallo Premessa Teorica Connessione tra materia e la carica elettrica Metodo per misurare la carica elettrica mediante elettrolisi
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO
 DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO OBIETTIVO: determinare i grammi di acido acetico presenti in 1 litro di aceto comune (concentrazione in g/l). Approccio al problema:
DETERMINAZIONE della MASSA di ACIDO ACETICO PRESENTE in un 1 L di ACETO OBIETTIVO: determinare i grammi di acido acetico presenti in 1 litro di aceto comune (concentrazione in g/l). Approccio al problema:
Regolamento della Gara Nazionale di Chimica per gli Istituti Tecnici. Regolamento della prova pratica
 Regolamento della Gara Nazionale di Chimica per gli Istituti Tecnici La Gara è costituita da: una prova scritta multidisciplinare con domande a risposta multipla inerenti i programmi delle materie di indirizzo
Regolamento della Gara Nazionale di Chimica per gli Istituti Tecnici La Gara è costituita da: una prova scritta multidisciplinare con domande a risposta multipla inerenti i programmi delle materie di indirizzo
DETERMINAZIONE DELLA F.E.M. E DELLA RESISTENZA INTERNA DI UNA PILA CON IL METODO POTENZIOMETRICO
 DETERMINAZIONE DELLA F.E.M. E DELLA RESISTENZA INTERNA DI UNA PILA CON IL METODO POTENZIOMETRICO Per determinare la forza elettromotrice E x di una pila è necessario utilizzare un metodo in cui la pila
DETERMINAZIONE DELLA F.E.M. E DELLA RESISTENZA INTERNA DI UNA PILA CON IL METODO POTENZIOMETRICO Per determinare la forza elettromotrice E x di una pila è necessario utilizzare un metodo in cui la pila
Problemi di massimo e minimo
 Problemi di massimo e minimo Supponiamo di avere una funzione continua in Per il teorema di Weierstrass esistono il massimo assoluto M e il minimo assoluto m I problemi di massimo e minimo sono problemi
Problemi di massimo e minimo Supponiamo di avere una funzione continua in Per il teorema di Weierstrass esistono il massimo assoluto M e il minimo assoluto m I problemi di massimo e minimo sono problemi
Misure voltamperometriche su dispositivi ohmici e non ohmici
 Misure voltamperometriche su dispositivi ohmici e non ohmici Laboratorio di Fisica - Liceo Scientifico G.D. Cassini Sanremo 7 ottobre 28 E.Smerieri & L.Faè Progetto Lauree Scientifiche 6-9 Ottobre 28 -
Misure voltamperometriche su dispositivi ohmici e non ohmici Laboratorio di Fisica - Liceo Scientifico G.D. Cassini Sanremo 7 ottobre 28 E.Smerieri & L.Faè Progetto Lauree Scientifiche 6-9 Ottobre 28 -
MISURA DELLA DISTANZA FOCALE DI UNA LENTE CONVERGENTE
 MISURA DELLA DISTANZA FOCALE DI UNA LENTE CONVERGENTE La distanza focale f di una lente convergente sottile è data dalla formula: da cui 1 f = 1 p + 1 q f = pq p + q dove p e q sono, rispettivamente, le
MISURA DELLA DISTANZA FOCALE DI UNA LENTE CONVERGENTE La distanza focale f di una lente convergente sottile è data dalla formula: da cui 1 f = 1 p + 1 q f = pq p + q dove p e q sono, rispettivamente, le
SCHEDA PER LO STUDENTE
 SCHEDA PER LO STUDENTE LA FORZA ELASTICA I Titolo dell esperienza LA FORZA ELASTICA Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti del L.S.S. Labriola (Ostia, Roma) II
SCHEDA PER LO STUDENTE LA FORZA ELASTICA I Titolo dell esperienza LA FORZA ELASTICA Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti del L.S.S. Labriola (Ostia, Roma) II
Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA
 Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA AA 2015-2016 Temperatura Temperatura misura oggettiva della sensazione di caldo e freddo Grandezza intensiva Misura la direzione del trasferimento
Esperimentazioni di Fisica 1 Tracce delle lezioni di TERMOLOGIA AA 2015-2016 Temperatura Temperatura misura oggettiva della sensazione di caldo e freddo Grandezza intensiva Misura la direzione del trasferimento
Il semiconduttore è irradiato con fotoni a λ=620 nm, che vengono assorbiti in un processo a due particelle (elettroni e fotoni).
 Fotogenerazione -1 Si consideri un semiconduttore con banda di valenza (BV) e banda di conduzione (BC) date da E v =-A k 2 E c =E g +B k 2 Con A =10-19 ev m 2, B=5, Eg=1 ev. Il semiconduttore è irradiato
Fotogenerazione -1 Si consideri un semiconduttore con banda di valenza (BV) e banda di conduzione (BC) date da E v =-A k 2 E c =E g +B k 2 Con A =10-19 ev m 2, B=5, Eg=1 ev. Il semiconduttore è irradiato
la vasca si riempie e, per tali valori di k il tempo necessario affinché la vasca si riempia.
 Esercizio In una vasca della capacità di 0 dm 3 e che inizialmente contiene 00 lt. di acqua, una pompa immette k lt. (k > 0) di acqua al minuto. Da un foro sul fondo l acqua esce con portata proporzionale
Esercizio In una vasca della capacità di 0 dm 3 e che inizialmente contiene 00 lt. di acqua, una pompa immette k lt. (k > 0) di acqua al minuto. Da un foro sul fondo l acqua esce con portata proporzionale
Problemi di Fisica per l ammissione alla Scuola Galileiana Problema 1
 Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq) + H 2 O (l)
 2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
2. Titolazione di un acido debole con una base forte : CH 3 COOH (aq) + NaOH (aq) (a cura di Giuliano Moretti) La titolazione è descritta dalla seguente reazione CH 3 COOH (aq) + OH - (aq) CH 3 COO - (aq)
1.0 - La natura della luce
 appunti di chimica 1.0 - La natura della luce Studiando la luce si sono ottenute importanti informazioni sulla struttura degli atomi. Sir Isaac Newton, fisico e matematico inglese, sostenne, nella seconda
appunti di chimica 1.0 - La natura della luce Studiando la luce si sono ottenute importanti informazioni sulla struttura degli atomi. Sir Isaac Newton, fisico e matematico inglese, sostenne, nella seconda
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE
 SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
SCHEDA PER LO STUDENTE DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO TRAMITE IL PRINCIPIO DI ARCHIMEDE I Titolo dell esperienza N 4 DETERMINAZIONE DELLA DENSITÀ DI UN LIQUIDO CON IL PRINCIPIO DI ARCHIMEDE
DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI
 RISOLUZIONE OIV/ENO 404/2010 DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI L ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
RISOLUZIONE OIV/ENO 404/2010 DOSAGGIO DELLA CARBOSSIMETILCELLULOSA (GOMMA DI CELLULOSA, CMC) NEI VINI BIANCHI L ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
TERMODINAMICA DI UNA REAZIONE DI CELLA
 TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
Circuito RC con d.d.p. sinusoidale
 Circuito C con d.d.p. sinusoidale Un circuito C-serie ha la seguente configurazione: G è la resistenza interna del generatore. Misura dello sfasamento della tensione ai capi del condensatore rispetto alla
Circuito C con d.d.p. sinusoidale Un circuito C-serie ha la seguente configurazione: G è la resistenza interna del generatore. Misura dello sfasamento della tensione ai capi del condensatore rispetto alla
GARA NAZIONALE DI CHIMICA XV EDIZIONE Aprile 2016 PRATO PROVA PRATICA
 MECCATRONICA ED ENERGIA ELETTRONICA ED ELETTROTECNICA INFORMATICA E TELECOMUNICAZIONI Viale della Repubblica, 9 59100 PRATO - Tel. 057458981 Fax 0574589830 Cod. Fisc.84004990481 Part. IVA 00337080972 http://www.itistulliobuzzi.it
MECCATRONICA ED ENERGIA ELETTRONICA ED ELETTROTECNICA INFORMATICA E TELECOMUNICAZIONI Viale della Repubblica, 9 59100 PRATO - Tel. 057458981 Fax 0574589830 Cod. Fisc.84004990481 Part. IVA 00337080972 http://www.itistulliobuzzi.it
DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto:
 Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Esperienza n. 3. Analisi di una miscela di NaHCO 3 e Na 2 CO 3
 Esperienza n. 3 Laboratorio di Chimica Analisi di una miscela di NaHCO 3 e Na 2 CO 3 OBBIETTIVI Lo scopo di questa esperienza è quello di risalire alla composizione percentuale di una miscela di carbonato
Esperienza n. 3 Laboratorio di Chimica Analisi di una miscela di NaHCO 3 e Na 2 CO 3 OBBIETTIVI Lo scopo di questa esperienza è quello di risalire alla composizione percentuale di una miscela di carbonato
Spettroscopia nell ultravioletto e nel visibile
 Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
